
Упреки в нарциссомике
17 марта 2012
Упреки в нарциссомике
- 1179
- 2
- 3
Нарцисси́зм — черта характера, заключающаяся в исключительной самовлюблённости. Термин происходит из греческого мифа о Нарциссе, прекрасном молодом человеке, который отверг любовь нимфы Эхо. В наказание за это он был обречён влюбиться в собственное отражение в воде озера, и умер от этой любви.
-
Автор
-
Редакторы
Последнее десятилетие в биологических науках было ознаменовано взрывным развитием геномных технологий и появлением способов собирать почти астрономические объемы данных о молекулярных особенностях организма. Однако ученые до сих пор не могут похвастать тем, что ориентируются в этом океане данных, хотя в нем, несомненно, «растворена» информация о предрасположенности к заболеваниям и другие важные для медицины, здравоохранения и даже криминалистики сведения. Американские исследователи положили начало по-настоящему персональной геномике, идентифицировав на основе анализа огромного количества молекулярной информации начинающийся у своего руководителя сахарный диабет 2-го типа.
Даже самые ярые приверженцы газет, продающихся в пригородных электричках, в курсе того, что мы живем в постгеномную эру (хотя самое меньшее, с чем столкнется в этой электричке произнесший такое непопулярное слово, это вращательный жест пальцем около виска) [1]. В наши дни прочесть полную геномную последовательность человека лишь немногим сложнее, чем во времена Остапа Бендера — подделать советский паспорт, учитывая развитие печатного дела на Западе [2]. Однако нельзя не отметить, что при современном развитии геномного дела на Западе, технология пока намного опережает свои потенциальные применения: прочесть-то геном можно, но вот извлечь из него полезную информацию едва ли кому удавалось, если говорить о такой растиражированной в СМИ пользе, как персонализованная медицина.
Это, конечно, не значит, что среди достижений геномики нет таких, которые были бы понятны самой широкой аудитории: ведь генетический анализ выявил наследственные компоненты не только многих заболеваний, но и таких, казалось бы, отнюдь не механистических вещей, как поведение [4] (в том числе преступное [5]!) или вредные привычки [6].
Однако того, чего общественность ожидает от развития геномных проектов больше всего — а именно, персонализованной медицины (индивидуального прогноза заболеваемости и индивидуального лечения), — пока не видно. И дело не только в том, что секвенирование генома стоит пока отнюдь не копейки, а соответствующие стандарты в здравоохранении отсутствуют. Проблема в том, что ученые не могут «отделить зерна от плевел» и получить ту несложную, в общем-то, информацию, которой все и ждут: болен ли человек и грозит ли ему какое-то заболевание в будущем? Ведь лечить запущенные заболевания сложнее многократно, а, значит, ранний диагноз — это одно из наиболее революционных новшеств в здравоохранении, которые сулит персональная геномика.
Когда «персональная» геномика станет персональной
По-настоящему персональной геномика стать все никак не может. Пока что приходится довольствоваться исследованиями по генетической ассоциации, где на основе анализа генома сотен или тысяч пациентов делаются довольно-таки скромные выводы о том, что такое-то заболевание в 5% случаев сцеплено с частотой такого-то генетического аллеля [7].
Но вот запахло ветром перемен — по крайней мере, западные СМИ заговорили о первой работе, являющейся примером действительно персональной геномики. Консорциум американских молекулярных биологов, анализировавший не только геном, но и большой массив других молекулярных данных одного пациента, позволил выявить у него сахарный диабет 2 типа в очень ранней стадии, что дает ему реальный шанс сохранить здоровье до старости, несмотря на неизлечимость этого заболевания [8].
Остроты истории добавляет то, что пациентом (называемым в статье скромно добровольцем IRB-8629) был руководитель исследования — Майкл Снайдер (Michael Snyder), генетик с медицинского факультета Стэнфорда (Калифорния, США). За то, что группа под руководством Снайдера настолько пристально исследовала самого Снайдера, один остроумный генетик окрестил подход «нарциссомикой», намекая на древнегреческий миф о Нарциссе.
Когда один важнее, чем много
Как уже было сказано, от исследования генетической ассоциации (Genome-wide association study) не так уж много толку, когда речь идет о здоровье конкретного человека. Так что сила работы Снайдера именно в том, что помочь удалось конкретному человеку, вовремя вооружив его информацией о грозящей болезни.
Ученые назвали использованный ими подход iPOP (integrative personal omics profile) — интегративный персональный профиль «-омик» . Он включает в себя определение полной последовательности ДНК, матричных и микро-РНК, а также уровня синтеза белков, различных метаболитов и аутоантител (рис. 1). Этот профиль определяли 20 раз в течение 14-месячного периода, в начале которого научный руководитель работы еще считал себя безукоризненно здоровым. В результате анализа сотен гигабайт собранной информации Снайдеру был преподнесен сюрприз: предрасположенность к несахарному диабету (диабет 2-го типа), хотя никто из его родственников не страдает и не страдал от этой болезни.
Под «-омиками» в англоязычной научной литературе понимают научно-технологические подходы, позволяющие исследовать какой-либо молекулярный аспект целиком, например: геномика, протеомика, транскриптомика, липидомика, метаболомика и т.д.
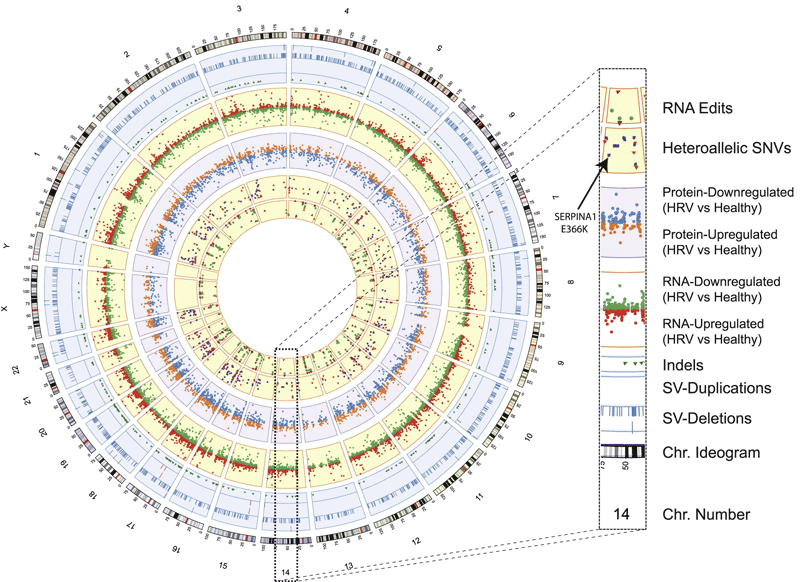
Рисунок 1. Как выглядит «нарциссомика»: часть исследований, проведенных на Снайдере. Наблюдение продолжалось 726 дней, и в течение этого времени Снайдер перенес две вирусные инфекции и у него начался несахарный диабет. Ему отсеквенировали ДНК, неоднократно секвенировали транскриптóм (матричную РНК и микро-РНК), чтобы следить за активностью генов и редактированием молекул РНК, неоднократно профилировали протеóм (определяли, какие белки и в каком количестве содержатся в клетках), определяли концентрации метаболитов и наличие в крови аутоантител. Кроме того, он постоянно проходил «стандартные» медицинские обследования.
На диаграмме показано картирование собранной информации по хромосомам (снизу вверх): идеограмма хромосомы, геномные (на голубом фоне), транскриптомные (на желтом фоне) и протеомные данные (на лиловом фоне). Так удалось установить, активность каких генов существенно меняется в процессе вирусной инфекции. Внутреннее транскриптомное кольцо (также желтое) показывает места редактирования мРНК и гетероаллельные варианты.
И действительно: не успели 400 дней исследования подойти к концу, как концентрация сахара в крови Снайдера начала повышаться, с чем он успешно справился, резко изменив образ жизни, начав соблюдать диету и сбросив вес. Всем бы так.
Конечно, есть и более простые способы диагноза диабета (возраст за 40 и полнота уже являются факторами риска), но здесь важно другое: ученые получили возможность наблюдать на молекулярном уровне самое начало заболевания, и сумели связать его с неизвестным ранее изменением активности генов и активацией биохимических путей.
Другой американский специалист по молекулярной генетике — Джордж Чёрч (George Church), инициатор и участник проекта «100 тысяч геномов», — уверен, что исследования в этом направлении необходимо продолжать: «В медицине есть принцип: „лечить не болезнь, а пациента“. И нам стоит ориентироваться на то же» [9].
Снайдер уверен, что времена, когда в листке с анализами значится 5–10, редко больше, показателей, постепенно отходят в прошлое. Современные технологии могут анализировать намного более широкий спектр данных — в его случае, речь идет условно о трех миллиардах молекулярных «измерений». Предприимчивые ученые уже открыли в Пало-Альто компанию Personalis, которая займется внедрением концепции в жизнь.
Предупрежден — значит вооружен
Страховая компания Снайдера, как только узнала о том, что у него диабет (Cell они прочли, что ли?), немедленно подняла ему взносы. Но тот не в обиде, потому что справедливо считает, что дешево отделался. С тех пор, как эти результаты начали докладываться на конференциях, Снайдеру надавали массу советов, как жить с диабетом припеваючи, так что он еще поработает.
Литература
- Геном человека: как это было и как это будет;
- Перевалило за тысячу: третья фаза геномики человека;
- Код жизни: прочесть не значит понять;
- Слово о генетике поведения;
- В тюрьму за гены;
- Спасибо, дорогой Минздрав, что предупредил!;
- Загадочная генетика «загадочной болезни кожи» — витилиго;
- Rui Chen, George I. Mias, Jennifer Li-Pook-Than, Lihua Jiang, Hugo Y.K. Lam, et. al.. (2012). Personal Omics Profiling Reveals Dynamic Molecular and Medical Phenotypes. Cell. 148, 1293-1307;
- Carina Dennis. (2012). The rise of the 'narciss-ome'. Nature.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




