Дофаминовые болезни
27 февраля 2015
Дофаминовые болезни
- 113592
- 6
- 61
Дофамин не наркотик, он — мотиватор.
сайт meatshop-tattoo.deviantart.com.
-
Автор
-
Редакторы
Мозг человека — хитросплетение множества нервных волокон, по которым идут разнообразные сигналы. Несмотря на свою электрическую природу, сигнал может передаться от одной клетки к другой только при помощи особых веществ — нейромедиаторов. Именно они в месте соприкосновения двух нейронов — синапсе — осуществляют передачу информации. Одним из нейромедиаторов является дофамин; с этим веществом связаны важнейшие биологические процессы в мозге и серьезные заболевания.
Три пути
Дофамин — довольно простая молекула. Бензольное кольцо с двумя гидроксильными группами, короткая цепочка в два атома углерода с аминогруппой на конце — вот строение одного из самых влиятельных веществ в нашем организме. Кроме несложного строения дофамин обладает и коротким путем синтеза (рис. 1). В организме человека к незаменимой аминокислоте фенилаланину присоединяется гидроксильная группа — так получается L-тирозин. При продолжении гидроксилирования он превращается в дигидроксифенилаланин. Когда у последнего отнимают атомы углерода и кислорода из боковой цепочки, т.е. происходит декарбоксилирование, образуется молекула дофамина. Многие слышали, что иногда вместо «дофамин» произносят «допамин». Это связано с различным написанием короткого названия вещества-предшественника дигидроксифенилаланина на английском и русском языках. По-английски оно пишется DOPA (dihydroxyphenylalanine). На русском языке аббревиатура выглядит по-другому: ДОФА (дигидроксифенилаланин). Производные этих молекул будут называться соответственно сокращениям — dopamine в английском языке и дофамин по-русски.
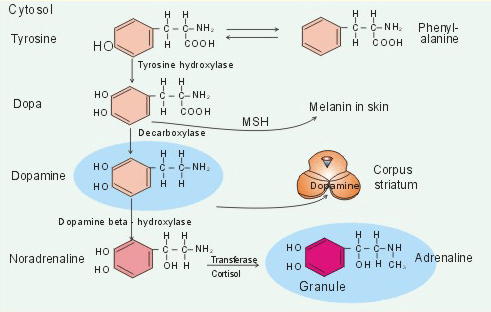
Рисунок 1. Синтез дофамина. На схеме также показаны пути синтеза других нейромедиаторов.
учебник «Новая физиология человека».
Если в нервной системе играет важную роль какое-то вещество, то должны быть и рецепторы к нему — точка приложения вещества. Сейчас насчитывают 5 типов дофаминовых рецепторов. Называются они до скучного предсказуемо: DRD1, DRD2, DRD3, DRD4 и DRD5. Рецепторы DRD1 и DRD5 относятся к одной группе, а остальные типы — к другой. При взаимодействии дофамина с рецепторами первой группы запускается каскад реакций, приводящий к росту внутриклеточной концентрации циклического аденозинмонофосфата (цАМФ), а при реакции с другими типами рецепторов количество цАМФ снижается. То есть взаимодействие дофамина с разными группами рецепторов приводит либо к активации, либо к ингибированию клеточной активности. А это в свою очередь оказывает влияние на поведение человека [1].
Дофаминовые шоссе проложены в мозге по трем основным направлениям (рис. 2). Первая дорога (мезолимбический путь) ведет из вентральной области покрышки (ventral tegmental area, VTA) в лимбическую систему — часть мозга, в которой формируются наши эмоции и желания. Вторая трасса проложена между VTA и лобной корой (мезокортикальный путь): здесь осуществляются когнитивные процессы, а также процессы, связанные с мотивацией и эмоциями. Легко заметить, что мезолимбический и мезокортикальный пути осуществляют схожие функции. Они отвечают за формирование желаний, за мотивацию и эмоциональные реакции у всех людей. Есть еще третий путь — нигростриарный, связывающий черное вещество (substantia nigra) с полосатым телом (striatum). У нигростриарного пути особенная функция: в нервной системе он запускает двигательную активность, снижая напряжение в мышцах.
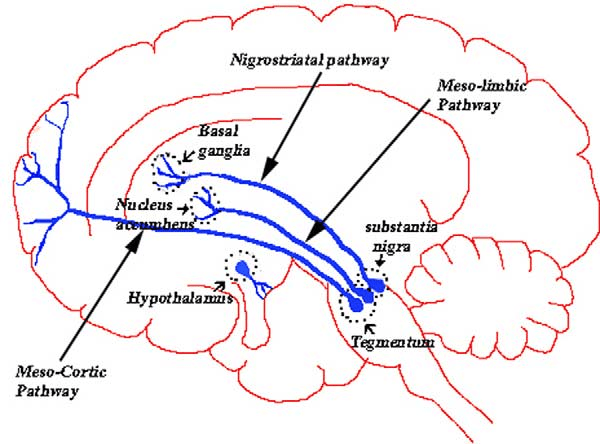
Рисунок 2. Дофаминовые пути. Нигростриарный путь контролирует движения, мезолимбический и мезокортикальный пути вовлечены в высшие психические функции.
сайт www.researchgate.net.
Молекулярный пряник
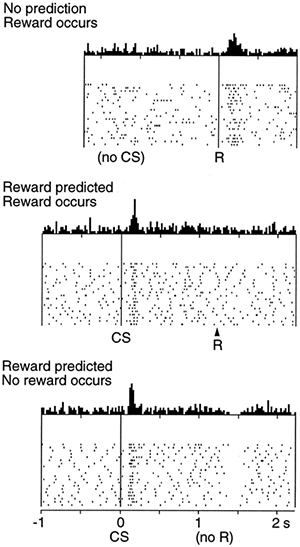
Рисунок 3. Выделение дофамина при получении и неполучении награды. Верхняя часть — действие производится, в ответ на награду вырабатывается дофамин — происходит закрепление связи «действие — награда». Средняя часть — всплеск дофаминовой активности сдвинут к самомý действию, что показывает сформированную связь между действием и ожидаемой наградой. Получение награды уже не вызывает подъема уровня дофамина. Нижняя часть — при неполучении ожидаемой награды после выполненного действия уровень дофамина снижается, уменьшая ценность этого действия в будущем.
Часто можно прочесть, что дофамин является нейромедиатором удовольствия, но это не совсем верно. Дофамин помогает мозгу выбрать правильные стратегии поведения и создает мотивацию для конкретных действий. В этих процессах задействованы мезолимбические и мезокортикальные дофаминовые волокна.
В наглядном изложении участие дофамина в процессе обучения будет выглядеть следующим образом. Человек красит забор и получает за это деньги. Есть действие (красить забор) и награда (деньги), которые мозг увязывает между собой. Первое денежное вознаграждение за покраску забора приводит к выбросу дофамина. В дальнейшем выделение дофамина по времени будет сдвигаться не к получению зарплаты за работу, а к самой работе. Так образуется мотивация, основанная на выгоде, на получаемых положительных эмоциях. Если после действия, к которому была сформирована мотивация, ожидаемая награда не поступила, то количество дофамина в соответствующих структурах головного мозга снижается, уменьшая ценность этого действия. Если Вы красите забор, а Вам за это не платят или платят слишком мало, то в конце концов Вы оставите кисть и краску (рис. 3). Эти простые механизмы управляют всей нашей жизнью — от похвалы в детском саду до голосования против того кандидата, который нас не устраивает. Примечательно, что при получении награды и ее отсутствии задействованы нейроны с разными типами дофаминовых рецепторов (рис. 4а и 4б). В случае получения награды меняется активность нейронов с дофаминовым рецептором 1-го типа, а при ее отсутствии — с дофаминовым рецептором 2-го типа [2].
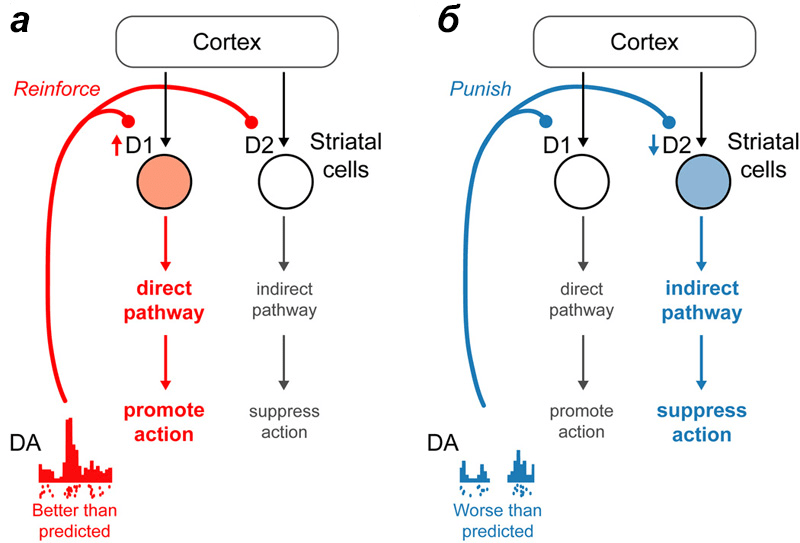
Рисунок 4. Вовлечение разных дофаминовых путей при обучении. При получении награды большей, чем ожидалось, происходит возбуждение нейронов с дофаминовыми рецепторами I типа. При награде менее значимой, чем раньше, снижается активность клеток с дофаминовыми рецепторами II типа.
Кроме этого существуют такие схемы дофаминовых путей, которые реагируют возбуждением на отрицательные стимулы [3]. С учетом этого становится ясно, что дофамин связан не с удовольствием, а с мотивацией и формированием целенаправленного поведения. Дофаминовые волокна проникают в различные отделы мозга — в префронтальную кору, отвечающую за планирование и обучение, в гиппокамп (центр нашей памяти) — и формируют устойчивые функциональные связи между нейронами для осуществления поведенческих программ.
Нарушения в различных дофаминовых путях приводят к различным заболеваниям.
Наблюдательный доктор
В начале XIX века один врач, практикующий на северо-востоке Лондона, опубликовал небольшую работу «Эссе о дрожательном параличе». В эссе он описал заболевание, симптомами которого были дрожь рук в покое и повышенный тонус мышц. Он также подробно изложил характер заболевания, скорость его течения: «Так малы и почти незаметны признаки этой болезни и так чрезвычайно медленно ее развитие, что редко бывает, чтобы пациент мог сформировать какое-то воспоминание о точном сроке ее начала» [4]. Автором этих слов был Джеймс Паркинсон.
Болезнь Паркинсона — это заболевание, при котором поражаются структуры мозга, входящие в состав нигростриарного дофаминового пути. При болезни Паркинсона в нейронах черного вещества накапливается белок α-синуклеин, что приводит к нарушению функционирования клеток и их гибели. Под микроскопом скопления белка видны в виде гранул — так называемых телец Леви (рис. 5).
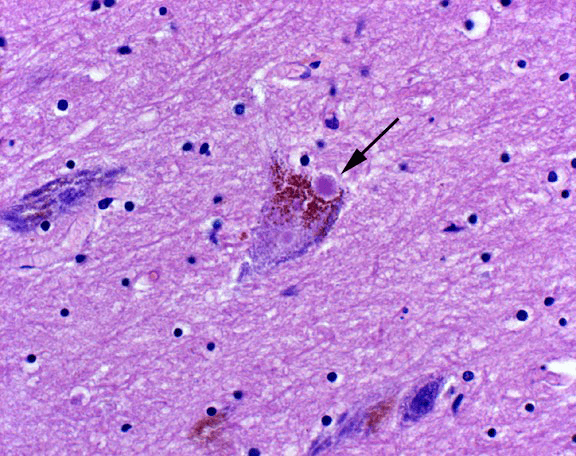
Рисунок 5. Нейрон с тельцем Леви — патологическим скоплением белка α-синуклеина в цитоплазме.
Чтобы понять, что происходит при болезни, для начала надо разобраться с нормой. У здорового человека сигналы из черного вещества по отросткам дофаминовых нейронов поступают в полосатое тело. Туда же, но по глутаматным путям, идут импульсы с моторных центров коры головного мозга. По дофаминовым путям приходят сигналы, влияющие на тонус мышцы и делающие движения плавными. Глутаматные сигналы — это резкие сокращения скелетной мускулатуры. При болезни Паркинсона происходит постепенное отмирание дофаминовых нейронов, постепенно снижается интенсивность импульсов. Это долго происходит незаметно, оставшиеся клетки используют резервы мощности. Рано или поздно мощность сигнала падает критически. Как правило, это происходит при гибели 3/4 нейронов черной субстанции. Появляются признаки болезни — нарастающее повышение мышечного тонуса и дрожание рук. На ранних этапах заболевания у пациента сохраняется способность к целенаправленным действиям, но чем дальше оно прогрессирует, тем сложнее человеку совершать простые бытовые действия, например, держать ложку.
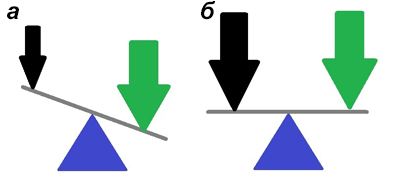
Рисунок 6. Патофизиология нарушений при болезни Паркинсона. а — До лечения: глутаматный сигнал (зеленая стрелка) не меняется при болезни Паркинсона, интенсивность дофаминового воздействия (черная стрелка) падает, возникает функциональное преимущество глутаматной системы. б — После применения лекарств сила дофаминового сигнала возрастает, система приходит к равновесию. Двигательные нарушения уменьшаются.
рисунок автора статьи.
Болезнь Паркинсона проявляется не только специфическими двигательными расстройствами. Кроме черного вещества в патологический процесс вовлекаются другие отделы мозга; это приводит к возникновению так называемых немоторных (non-motor) симптомов болезни Паркинсона. Нарушения сна, сниженное настроение, тревога, набор или снижение веса, проблемы со зрением, замедление мышления и даже деменция — список симптомов внушителен, и часто пациенту мешают жить даже не двигательные нарушения, а именно немоторные проявления болезни.
Одним из главных лекарств от болезни Паркинсона является леводопа — L-изомер диоксифенилаланина (L-DOPA), который проникает в мозг лучше, чем сам дофамин. Однако в мозг проникает относительно небольшая часть леводопы, а оставшееся количество начинает превращаться ферментами периферических тканей в дофамин путем декарбоксилирования. Избыток дофамина может привести к падению давления, обморокам и другим неприятным побочным эффектам. Чтобы избежать этого, в дополнение к леводопе назначают ингибиторы периферической L-DOPA-декарбоксилазы. Существуют противопаркинсонические препараты, где леводопа уже совмещена с ингибитором фермента, и они повышают эффективность лечения (рис. 6).
Дофаминовая гипотеза
Другим заболеванием, которое тесно связано с дофамином, является шизофрения. В ходе обсуждения происхождения, диагностики и лечения этой болезни ломались копья не одного поколения врачей, ученых, психологов, журналистов и прочих причастных. Чтобы не уходить в дебри этого спора, стоит дать краткое описание современного подхода к шизофрении. Во-первых, шизофрения существует, и это болезнь. Во-вторых, у нее есть четкие диагностические критерии, с которыми знаком любой врач-психиатр. Несмотря на разнообразие клинических проявлений, шизофрения хорошо распознается специалистами. Кроме диагностики разработано лечение и доказано, что оно успешно работает. Это в-третьих. Но к лечению мы еще вернемся.
Разнообразные симптомы шизофрении обычно делятся на три группы. Первая включает в себя позитивные симптомы — то, что добавляется к психической деятельности человека: слуховые и зрительные галлюцинации, идеи преследования, воздействия излучением. Вторая группа — это негативные симптомы. Этим термином обозначается утрата пациентом того, что было ему присуще ранее. К негативным симптомам относятся: уменьшение повседневной активности, утрата интересов и снижение эмоциональных проявлений, как внутренних (сила эмоций, их разнообразие), так и внешних (выражение эмоций на лице). Как правило, группа негативных симптомов описывается в специальной литературе термином «эмоционально-волевое снижение». Вне обострения шизофрении именно они определяют состояние и качество жизни человека, больного шизофренией. В третью группу входят когнитивные симптомы — специфические проблемы с обработкой информации.
В начале 50-х годов была выдвинута первая версия дофаминовой гипотезы. Врачи использовали экспериментальные препараты-антипсихотики и впервые получили стойкие улучшения при лекарственном лечении. В ходе исследований выяснилось, что эти препараты снижали воздействие дофамина на нервные клетки. Психиатры стали связывать возникновение шизофрении с избытком дофамина в нервной системе. В течение следующих 40 лет накопились новые данные, и к концу XX века дофаминовая гипотеза была пересмотрена. Позитивные симптомы (бред, галлюцинации) стали связываться с избытком дофамина в мезолимбическом пути, а негативные симптомы — с его недостатком в мезокортикальном. Причем избыток дофамина, приводящий к тому, что называется психозом — «голосá» и паранойя, — вероятно, вызывается повышенным выделением дофамина в подкорковых отделах головного мозга, а не повышенной чувствительностью нейронов к веществу [5].
Знакомые побочные эффекты
Сейчас для лечения шизофрении используются специальные препараты — антипсихотики. Они блокируют дофаминовые рецепторы, снижая избыточное воздействие дофамина на нейрон. Антипсихотики делятся на типичные (галоперидол, аминазин) и атипичные (рисперидон, кветиапин); типичные антипсихотики были синтезированы раньше, чем атипичные. Принципиальное различие между двумя группами препаратов заключается в спектре симптомов, на которые они воздействуют. Мишенью для «старых» лекарств были преимущественно галлюцинации и бред, т.е. позитивные симптомы, а целью нового поколения стали и негативные симптомы шизофрении. Разница в клиническом воздействии может объясняться тем, что атипичные антипсихотики значимо воздействуют и на другие рецепторы нейронов (например, на серотониновые).
Проблема применения препаратов разных поколений связана с тем, что типичные антипсихотики вызывают двигательные побочные эффекты чаще, чем атипичные [6]. Побочные эффекты часто возникают в виде мышечной скованности и дрожания рук, что очень напоминает болезнь Паркинсона. Комплекс этих симптомов так и называется — лекарственный паркинсонизм. Антипсихотик блокирует все рецепторы в мозге без разбора и рано или поздно добирается до нигростриарной системы, снижая воздействие дофаминовых сигналов на двигательные структуры нервной системы. Пациент может жаловаться на мышечную скованность, дрожание рук, и это одни из самых неприятных побочных эффектов, которые часто приводят к отказу от лечения. В самом начале истории применения антипсихотиков врачи считали, что пока у человека не развились двигательные расстройства, доза препарата не может считаться адекватной. К счастью, сейчас выработаны и применяются разумные схемы лечения психических расстройств, и у препаратов из новой группы антипсихотиков меньше выражены двигательные побочные эффекты.
Литература
- Тонкие нити судьбы;
- Ethan S. Bromberg-Martin, Masayuki Matsumoto, Okihide Hikosaka. (2010). Dopamine in Motivational Control: Rewarding, Aversive, and Alerting. Neuron. 68, 815-834;
- Masayuki Matsumoto, Okihide Hikosaka. (2009). Two types of dopamine neuron distinctly convey positive and negative motivational signals. Nature. 459, 837-841;
- Hurwitz B. (2014). Urban observation and sentiment in James Parkinson’s Essay on the Shaking Palsy (1817). Lit Med. Spring, 74–104;
- O. D. Howes, S. Kapur. (2009). The Dopamine Hypothesis of Schizophrenia: Version III--The Final Common Pathway. Schizophrenia Bulletin. 35, 549-562;
- Stefan Leucht, Caroline Corves, Dieter Arbter, Rolf R Engel, Chunbo Li, John M Davis. (2009). Second-generation versus first-generation antipsychotic drugs for schizophrenia: a meta-analysis. The Lancet. 373, 31-41.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚