
Наука из первых рук: как гомеостаз хлора влияет на возникновение эпилепсии
02 декабря 2016
Наука из первых рук: как гомеостаз хлора влияет на возникновение эпилепсии
- 1924
- 5
- 3
рисунок Ольги Пташник
-
Автор
-
Редакторы
Эпилепсия — хроническое неврологическое заболевание, при котором в нервной системе нарушается правильный баланс между возбуждением и торможением. Из-за этого в мозге возникают очаги неконтролируемого возбуждения, что проявляется в виде судорожных приступов. Только что наша международная исследовательская группа опубликовала работу о том, как гомеостаз ионов хлора может повлиять на развитие эпилепсии.
Короткая история звучит примерно так. У пациентов с эпилепсией височной доли мозга было найдено, что в небольшой группе нейронов отсутствует молекула, которая поддерживает гомеостаз ионов хлора (KCC2, potassium chloride cotransporter 2, т.е. хлорно-калиевый котранспортер 2). Эта молекула относится к целому классу сходных молекул, которые называются cation chloride cotransporters.
Эти белки занимаются тем, что поддерживают баланс различных ионов внутри и вне клетки [1]. Котранспортерами их называют потому, что за один раз они переносят сразу несколько ионов, например, KCC2 переносит ионы калия и хлора. Поскольку заряды этих ионов компенсируют друг друга, такой перенос можно проводить без затрат энергии. Энергия, конечно, используется, но та, которая запасена за счет натрий-калиевой помпы. Стоит помнить о том, что баланс именно этих ионов позволяет запускать потенциал действия , чтобы нейроны могли генерировать спайки в принципе.
О путешествиях ионов сквозь мембрану нейронов и мембранных потенциалах подробнее можно прочитать в статьях: «Формирование мембранного потенциала покоя» [2] и «Метроном: как руководить разрядами?» [3]. — Ред.
Зачем же нужен KCC2 в нейроне? Дело в том, что баланс хлора крайне важен для того, чтобы торможение было эффективным. Если хлора в нейроне слишком много, это может привести к тому, что тормозные синапсы могут стать возбуждающими (рис. 1) [4]. Причина в том, что из-за накопления хлора потенциал реверсии для тормозных ГАМК-синапсов начинает расти, и торможение перестает быть столь эффективным. Если таких клеток в сети накапливается слишком много, это может привести к увеличению возбуждения за счет рекуррентных синапических связей. В норме баланс возбужения-торможения регулируется для того, чтобы нейроны могли эффективно обрабатывать информацию и генерировать небольшое количество спайков. Существуют теории о том, что именно редкое срабатывание спайков может помогать сетям мозга оптимально кодировать информацию. Но об этом в другой раз, а пока вернемся к эпилепсии.
О возникновении вихрей возбуждения (но уже в сердечной мышце) и их изучении рассказывает обзор «Лаборатория биофизики возбудимых систем: сердце, его вихри и фотоуправление» [5]. — Ред.
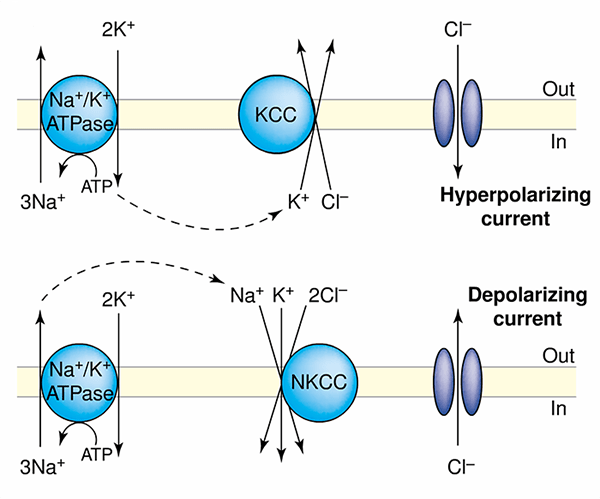
Рисунок 1. Схема работы хлорно-калиевых котранспортеров. Стрелочками показано направление тока ионов. Оба котранспортера, KCC2 и NKCC1, работают за счет поддержание натрий-калиевого гомеостаза с помощью натрий-калиевой АТФазы.
Если визуализировать эпилептический приступ в мозге крысы с помощью ультразвукового имиджинга мозга [6], то он будет выглядеть так:
Видео. Эпилептический приступ в мозге крысы, записанный с помощью ультразвукового имаджинга
Было известно, что у некоторых пациентов, страдающих эпилепсией, нарушен баланс ионов хлора внутри нейронов. Но как именно накопление хлора в сети взаимодействующих клеток может приводить к эпилепсии, было непонятно. Дело в том, что помимо медленного изменения концентрации ионов нейроны обмениваются нервными импульсами, что также меняет концентрацию ионов — как хлора внутри клеток, так и калия снаружи. Чтобы лучше понять механизмы приступа, мы построили подробную модель нейронов сети с динамической концентрацией хлора и других ионов. С ее помощью мы показали, что динамика сети может легко стать эпилептической, если есть около 30% клеток, у которых отсутствует KCC2 котранспортер (рис. 2).
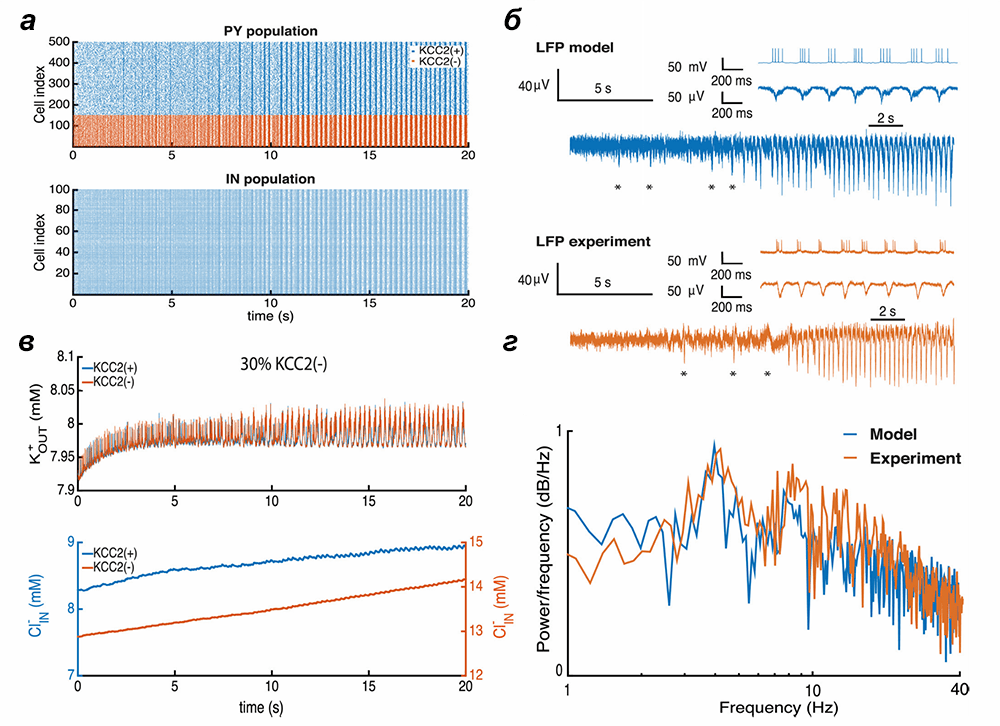
Рисунок 2. КСС2(−)-патология. а — Активность в модели сети возбуждающих (PY) и тормозных (IN) нейронов при переходе к эпилептическому приступу. б — Полевой потенциал (LFP), рассчитанный в модели нейронов (LFP model) и записанный в эпилептогенных срезах мозга (LFP experiment). в — Изменение концентрации внеклеточного калия (K+_OUT) и внутриклеточного хлора (Cl−_IN) при переходе к эпилептическому приступу. г — Спектр полевого потенциала во время приступа в модели и эксперименте.
Более того, наша модель оказалась способна воспроизвести активность, записанную в срезах мозга человека, где была запущена эпилепсия. Людей мы для этого не резали, но использовали данные, полученные после хирургического удаления очага эпилепсии в гиппокампе.
Любопытно, что предсказания, которые мы сделали, косвенно нашли подтверждение в результатах другой научной группы. Независимо от нас было найдено, что у мышей с увеличенной экспрессией KCC2 котранспортера сложнее вызвать эпилепсию, чем у обычных мышей [7]. Что подтверждает нашу идею о том, что отсутствие KCC2 может приводить к приступам.
Более того, с помощью нашей модели мы предсказали, что восстановление KCC2 может прекратить приступ (рис. 3). Для этого необходимо восстановить баланс хлора в пораженных нейронах, что сделает возбуждающие ГАМК-синапсы снова тормозными и в конечном итоге приведет к восстановлению балланса возбуждения и торможения в сети. Правда это или нет — пока неясно, потому что не совсем понятно, с помощью каких веществ можно строго и селективно изменять концентрацию хлора в нейронах. Но будем надеяться, что фармакология и оптогенетика помогут когда-нибудь решить эту проблему.
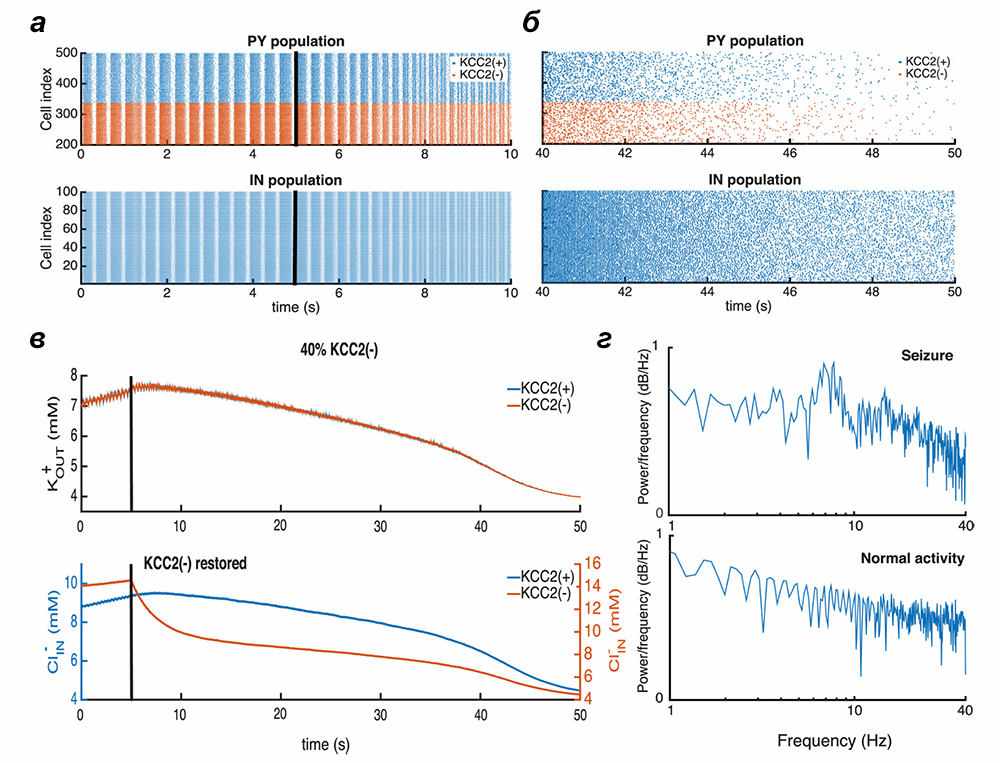
Рисунок 3. Восстановление функции КСС2 предотвращает приступ. а, б — Активность сети нейронов в состоянии эпилепсии до и после восстановления работы KCC2-контранспортера. в — Изменение концентрации ионов калия и хлора после восстановления KCC2. г — Спектр осцилляций полевого потенциала во время приступа и в норме.
P.S. Если интересна техническая сторона модели или просто хотите с ней поиграть, рабочую версию кода в Matlab найдете тут. Оригинальную статью можно посмотреть здесь [1].
Литература
- Buchin A., Chizhov A., Huberfeld G., Miles R., Gutkin B.S. (2016). Reduced efficacy of the KCC2 cotransporter promotes epileptic oscillations in a subiculum network model. J. Neurosci. 36, 11619–11633;
- Формирование мембранного потенциала покоя;
- Метроном: как руководить разрядами?;
- Blaesse P., Airaksinen M.S., Rivera C., Kaila K. (2009). Cation-chloride cotransporters and neuronal function. Neuron. 61, 820–838;
- Лаборатория биофизики возбудимых систем: сердце, его вихри и фотоуправление;
- Macé E., Montaldo G., Cohen I., Baulac M., Fink M., Tanter M. (2011). Functional ultrasound imaging of the brain. Nat. Methods. 8, 662–664;
- Cheung D.L., Goulton C.S., Watanabe M., Nabekura J., Moorhouse A.J. (2016). The effect of upregulated KCC2 expression on chemically induced seizures and diazepam therapy in vivo. Neuroscience 2016.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





