Рулетка для спектроскописта
31 августа 2010
Рулетка для спектроскописта
- 3102
- 6
- 2
Изменение флуоресценции, возникающее при резонансном переносе энергии между парой флуорофоров, позволяет судить о расстоянии, разделяющем эти молекулы в пространстве, — подобно молекулярной рулетке
-
Автор
-
Редакторы
Беспроводным может быть не только интернет или телефон. В мире макромолекул бесконтактный перенос энергии используется в датчиках контакта, молекулярных дальномерах и динамометрах, позволяя изучать детали взаимодействия молекул между собой.
Умный проездной
Как пользоваться бесконтактными картами для оплаты проезда или бесконтактными пропусками на работу — знает каждый горожанин. Проще простого. Поднес к турникету, загорелся зеленый — проходи. Технически подкованные читатели наверняка смогут объяснить и принцип действия таких карт: в турникете есть передатчик, а в билете спряталась маленькая антенна. Как только эта антенна оказывается достаточно близко к передатчику (обычно не более десяти сантиметров), она начинает принимать излучение передатчика. В контуре появляется электрический ток, который питает простенькую электронику билета и позволяет ему (билету) в свою очередь общаться с турникетом — сверять месяц и число оставшихся поездок. То есть, билет сначала получает энергию от турникета, а потом её же испускает. Энергия испущенного билетом излучения по закону сохранения энергии всегда меньше той, что он поглотил: разница ушла на обработку информации, а ещё часть рассеялась в виде тепла. Для нас же более важно то, что взаимодействие происходит только в том случае, если приёмник и передатчик находятся достаточно близко друг к другу. А теперь вопрос: насколько маленькими могут быть передатчик и приёмник?
Очень маленькие передатчики
Да хоть с молекулу размером. Самым главным отличием будут частоты (и, соответственно, расстояния), на которых работает перенос энергии. Более того, перенос энергии между флуорофорами учёные стали использовать задолго (лет за пятьдесят) до того, как появились первые бесконтактные проездные и пропуска. Для того чтобы это работало, нужны две подходящие молекулы. Первая должна быть флуорофором — то есть, уметь испускать свет, — а вторая обязана поглощать излучение, испущенное первой молекулой. Хотя вторая молекула не обязательно должна быть флуорофором, обычно на её роль тоже берут флуорофор, потому что в этом случае появляется возможность дополнительно контролировать опыт по излучению молекулы № 2.
Первая молекула, поглощая квант света (фотон), переходит в возбуждённое состояние. Теперь она способна сама испускать электромагнитное излучение — например, свет. Эта молекула теперь становится передатчиком. (В терминах флуоресцентной спектроскопии — донор излучения.) Если поблизости оказывается молекула № 2 (акцептор), то донор не испускает свет, а безызлучательно передаёт энергию молекуле № 2. Часть энергии при этом теряется (за то время пока первая молекула находилась в возбуждённом состоянии, она заставила перестроиться ближайшие к ней молекулы растворителя, — попросту, немножко их нагрела). Молекула № 2, принимая энергию, тоже переходит в возбуждённое состояние, и теперь она сама способна излучать свет.
Перенос энергии возможен не для любых, а для строго определённых пар доноров и акцепторов. (В конце концов, Ваш пропуск на работу не срабатывает в метро, и наоборот.) Кроме того, перенос энергии произойдёт, только если донор и акцептор окажутся близко друг к другу (обычно не более чем несколько десятков ангстрем). Если сравнение бесконтактных проездных с переносом энергии всё ещё кажется Вам надуманным, то вот интересная особенность. И в работе бесконтактного проездного, и в переносе энергии между флуорофорами расстояние, на котором происходит взаимодействие, значительно меньше длины волны излучения, которое испускает передатчик — турникет или донор.
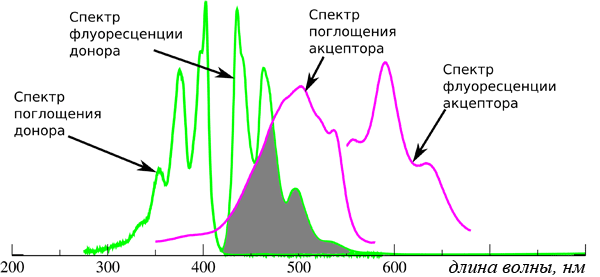
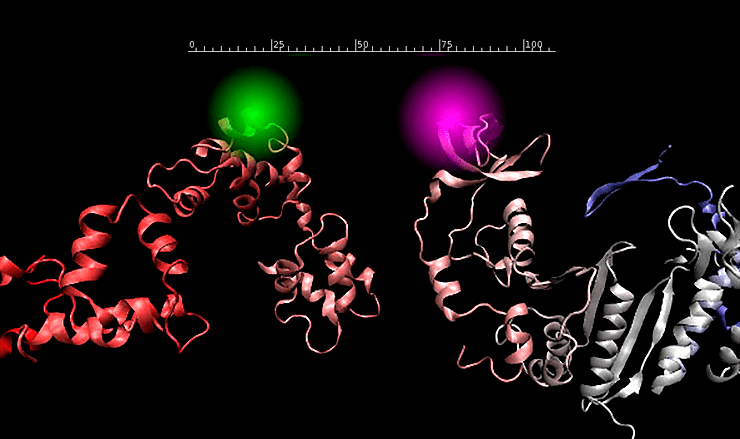
Рисунок 1. Главное требование к паре донор-акцептор — перекрывание спектров (показано серым). Донор должен испускать свет как раз тех длин волн, которые может поглотить акцептор. Перенос энергии, тем не менее, происходит без излучения фотона. Дело в том, что если молекулы с близкими энергетическими уровнями (перекрывание спектров) оказываются не далеко друг от друга, то между этими уровнями возможно возникновение резонанса, и энергия с одной молекулы передается на другую. Поэтому само явление называют FRET (от английского Fluorescence Resonance Energy Transfer — резонансный перенос энергии флуоресценции).
Большая практика
У явления переноса энергии между флуорофорами есть две особенности, которые сделали его незаменимым инструментом исследователя в области молекулярной биологии, биофизики и смежных дисциплин. Первая и важнейшая особенность — это то, что при сближении донора и акцептора перенос энергии происходит неизбежно. Эта достоверная неизбежность позволяет использовать перенос энергии как датчик сближения двух молекул в пространстве. Достаточно пометить (покрасить) эти молекулы флуоресцентными зондами. Такая универсальность позволяет использовать метод для изучения всего диапазона возможных взаимодействий между ДНК, белками и мембранами. Подбирая флуорофоры и модифицируя ими белки или другие биомолекулы, учёный как бы ставит сигнализацию. Появление переноса энергии (наблюдаемого по флуоресцентному сигналу в микроскоп) равносильно её срабатыванию.
Для того чтобы белки обладали флуоресценцией, не обязательно химически присоединять к ним флуорофор. Можно использовать белки, которые обладают собственной флуоресценцией и светятся подобно медузам (см., например, «Флуоресцирующая Нобелевская премия по химии» [1]). Достоинство такого подхода в том, что флуоресцентный белок может синтезировать сама клетка, а значит, воздействие извне будет минимальным.
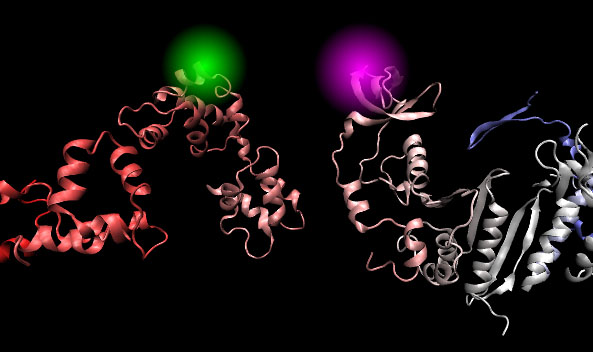
Рисунок 2. Если к одной молекуле белкá прикрепить флуорофор-донор, а к другой — флуорофор-акцептор, то, как только молекулы сблизятся (фермент подойдет к субстрату или антиген к антителу), произойдет перенос энергии с донора на акцептор. Так мы сможем узнать, что молекулы сблизились и находятся друг рядом с другом. Это очень важные сведения: на основании того, что молекулы удерживаются вместе, можно сделать вывод, что они обладают «сродством» друг к другу — например, что данное антитело связывается именно с этим антигеном.
На что ставить такую «флуоресцентную сигнализацию»? — вопрос уникальный для каждой научной задачи. Например, можно пометить флуорофорами фермент и субстрат и потом следить, когда и при каких условиях (pH, концентрация кальция, температура и пр.) происходит ферментативная реакция.
Вторая важная особенность — это то, что эффективность переноса энергии зависит от расстояния между флуорофорами; точнее, она обратно пропорциональна расстоянию в шестой степени (~r−6) . А раз так, то перенос энергии очень удобно использовать для измерения расстояний. Некоторые даже называют этот метод спектроскопической рулеткой. Диапазон измерений составляет несколько десятков ангстрем. То, что нужно для измерения расстояний в мире биомолекул! Например, запросто можно измерить расстояние, на которое сближаются два белка на поверхности мембраны клетки. Да что там расстояние! Можно измерить любую производную от него величину — например, силу сцепления клетки с поверхностью, на которой она лежит.
Теорию резонансного переноса энергии разработал в середине XX века Теодор Фёрстер. Первоначально теория называлась FRET — резонансный перенос энергии флуоресценции. Термин некорректный, поскольку в самом переносе энергии не излучается фотон, а значит и нет флуоресценции. Некоторое время специалисты называли теорию просто RET, без слова «флуоресценция». Но аббревиатура FRET была уже слишком распространена. В память о Фёрстере сегодня FRET расшифровывается как Forster Resonance Energy Transfer — резонансный перенос энергии по Фёрстеру. Интересно, что в русско-язычной литературе путаницы изначально не было. Теория называется ИРПЭ — индуктивно резонансный перенос энергии, что позволяет использовать единую терминологию, как для механизма предложенного Фёрстером, так и для механизма предложенного Декстером, а также для множества более поздних расширений и дополнений.
При должном умении исследователи ухитряются даже проследить с помощью флуоресцентных инструментов за последовательными шагами работы рибосомы — связыванием аминоацил-тРНК с рибосомой, образованием новой пептидной связи, перемещением «новосинтезированной» пептидной цепочки в соседнее положение и диссоциацией «пустой» тРНК! (см. «Рибосома за работой» [2]).
Увидеть невидимое
Теоретический (но при этом труднодостижимый) предел разрешения оптической микроскопии — половина длины волны используемого света (не менее 200 нм в случае излучения видимого диапазона). Это значит, что в оптический микроскоп нельзя различить два объекта, если расстояние между ними меньше этой величины. Такой точности вполне хватает, чтобы изучать морфологию клеток; но вот чтобы наблюдать молекулы внутри живой клетки, нужно разрешение в десятки ангстрем — то есть, в сто раз меньше «барьера». Конечно, можно использовать более коротковолновое излучение (как в случае электронной микроскопии), но оно разрушительно для клеток, и, следовательно, позволяет работать только с фиксированными (мёртвыми) объектами. Явление переноса энергии позволяет частично обойти это препятствие: свечение появляется, если донор и акцептор сблизились в пространстве. В конце концов, всё, что мы хотим увидеть в микроскоп — это взаимное расположение объектов. Или хотя бы насколько близко они друг к другу находятся.
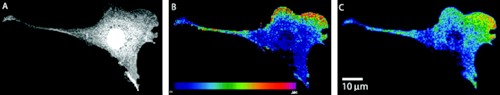
Рисунок 3. Взаимодействие двух белков внутри клетки. Красный цвет означает высокую эффективность переноса энергии, а синий — низкую. То есть, в том месте, где клетка окрашена красным, два белка взаимодействуют друг с другом.
Заключение
Конечно, перенос энергии между флуорофорами — это далеко не аналог радио в мире макромолекул. Но большой мир, в котором мы живем — с интернетом и метрополитеном — подчиняется тем же самым законам, что и мир малый, в котором функционируют (или все-таки живут?) макромолекулы — белки и ДНК, липиды и углеводы. Но аналогии и параллели, даже самые интересные и неожиданные, это ещё не научное знание. А это значит, что ученым ещё предстоит работать и работать. Ну-ка! Кого мы еще не измерили — покажись!
Эта статья написана при поддержке РФФИ (конкурс на написание научно-популярных статей), № проекта: 10-3-11503-с.
Литература
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚