
Коронавирусная инфекция уже привела к заражению около 180 миллионов людей и летальному исходу около 3,9 млн человек, согласно Our World in Data и JHU CSSE COVID-19 Data. SARS-CoV-2 характеризуется длительным инкубационным периодом, высокой контагиозностью и патогенностью, а также отсутствием стандартов лечения. Вакцинация — многообещающее решение формирования быстрого коллективного иммунитета для прекращения пандемии COVID-19.
Компания Genetex разработала белки и антитела к SARS-CoV-2 для создания белковых вакцин и наборов для молекулярной диагностики. Продукция доступна у официального дистрибьютора в России — компании Микротесты б.м.в.
Также компания Genetex проводит вебинар «Открытие новых противовирусных веществ в борьбе с патогенными вирусами человека: история двух новых вирусов — SARS-CoV-2 и вируса Зика» (на английском) 25 августа 2021 г. (ср) 18:30–20:00 (по московскому времени). Необходима регистрация.
В рекордное время был секвенирован геном вируса и определена его структура, что позволило в кратчайшие сроки начать разработку вакцин. На данный момент известно более 150 вакцин, которые классифицируются на 8 биотехнологических платформ. Подавляющее большинство из них — это белковые вакцины [1–3].
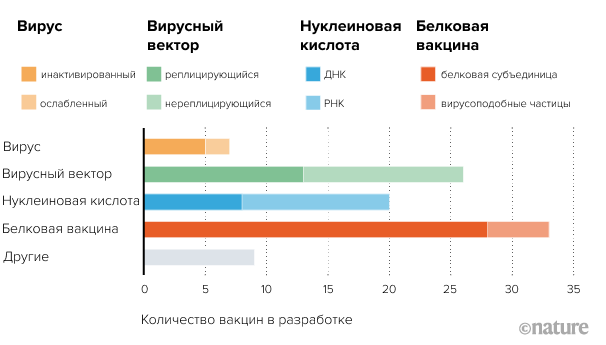
Рисунок 1. Биотехнологические платформы вакцин
Белковые вакцины состоят из белковых субъединиц или вирусоподобных частиц.
- В настоящее время в разработке находятся 28 вакцин, содержащих вирусные белковые субъединицы: шиповидный белок или рецептор-связывающий домен (RBD) шиповидного белка. Данным вакцинам требуются адъюванты (молекулы, усиливающие иммунный ответ), а также неоднократное введение доз вакцин [2].
- Вакцины на основе вирусоподобных частиц представляют собой оболочку вируса с белками, лишенную генетической информации. Такую биотехнологическую платформу используют для 5 разрабатываемых вакцин: они безопасны и дают сильный клеточный иммунный ответ, но сложны в производстве [2].
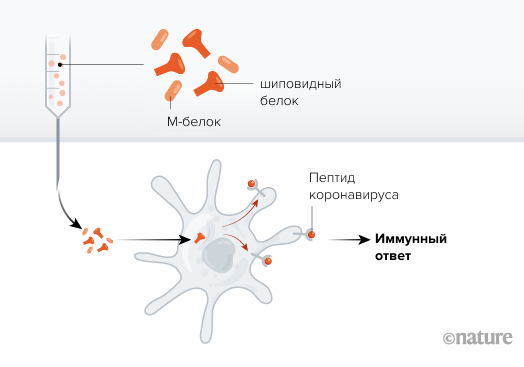
Рисунок 2. Белковая субъединица
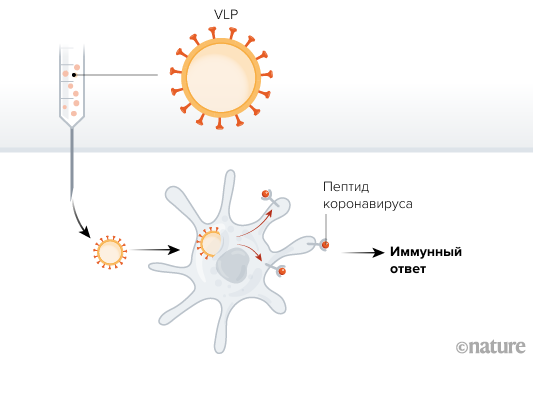
Рисунок 3. Вирусоподобные частицы (VLP, Virus-like particle)
Ситуация осложняется тем, что с конца 2020 года произошла эволюция SARS-CoV-2 благодаря мутациям, которые повлияли на его трансмиссивность и антигенность (появление британского, южноафриканского, бразильского и индийского штаммов). Это так называемый дрейф антигенов, естественный случайный процесс образования и накопления ошибок в ходе репликации вируса. Если дрейф антигенов происходит в регионе RBD, то он способен приводить к снижению нейтрализующей активности антител, образующихся после вакцинации или болезни.
Для того чтобы преодолеть пандемию в короткий период, критически важно иметь возможность адаптировать вакцины и наборы для молекулярной диагностики к новым вариантам SARS-CoV-2 [4–6].
Компания Genetex рада предложить вам антитела и рекомбинатные белки дикого типа шиповидного белка, с одиночными мутациями, а также белки 4 мутантных штаммов коронавируса (таблицы 1–5, рис. 4–5).
| Название продукта | Система экспрессии | Каталожный номер |
|---|---|---|
| Spike (ECD) protein, His tag (active) | HEK293 | GTX135972-pro |
| Spike RBD protein, His tag (active) | HEK293 | GTX136090-pro |
| Spike S1 protein, His tag (active) | HEK293 | GTX135817-pro |
| Spike S2 (ECD) protein, mouse IgG Fc tag | HEK293 | GTX135684-pro |
| Spike (D614G Mutant) protein (ECD), His tag (active) | HEK293 | GTX02575-pro |
| Название продукта | Система экспрессии | Каталожный номер |
|---|---|---|
| Spike (del69-70, del144, N501Y, A570D, D614G, P681H,T716I, S982A, D1118H) (ECD) Protein, His tag (active) | HEK293 | GTX136059-pro |
| Spike RBD (N501Y Mutant) protein, His tag (active) | HEK293 | GTX136014-pro |
| Spike RBD (E484K, N501Y Mutant) protein, His tag (active) | HEK293 | GTX136058-pro |
| Spike S1 (del69-70, del144, N501Y, A570D, D614G, P681H Mutant) protein, His tag | HEK293 | GTX136085-pro |
| Spike S2 (T716I, S982A, D1118H Mutant) (ECD) protein, His tag | HEK293 | GTX136023-pro |
| Название продукта | Система экспрессии | Каталожный номер |
|---|---|---|
| Spike (L18F,..., K417N, E484K, N501Y,...)(ECD) Protein, His tag (active) | HEK293 | GTX136061-pro |
| Spike RBD (K417N, E484K, N501Y Mutant) protein, His tag (active) | HEK293 | GTX136022-pro |
| Spike S1 (L18F, D80A, D215G, R246I, K417N, E484K, N501Y, D614G Mutant) protein, His tag | HEK293 | GTX136095-pro |
| Название продукта | Система экспрессии | Каталожный номер |
|---|---|---|
| Spike (L18F, T20N, P26S, D138Y, R190S, K417T, E484K, N501Y, D614G, H655Y, T1027I, V1176F Mutant) (ECD) protein, His tag | HEK293 | GTX136091-pro |
| Spike RBD (K417T, E484K, N501Y Mutant) protein, His tag (active) | HEK293 | GTX136043-pro |
| Spike S1 (L18F, T20N, P26S, D138Y, R190S, K417T, E484K, N501Y, D614G Mutant) protein, His tag | HEK293 | GTX136094-pro |
| Название продукта | Система экспрессии | Каталожный номер |
|---|---|---|
| SARS-CoV-2 (COVID-19) Spike RBD (L452R, E484Q Mutant) protein, His tag (active) | HEK293 | GTX136299-pro |
| SARS-CoV-2 (COVID-19) Spike RBD (L452R, T478K Mutant) protein, His tag | HEK293 | GTX136332-pro |
| Название продукта | Каталожный номер | Характеристика | Применение |
|---|---|---|---|
| SARS-CoV-2 (COVID-19) Spike RBD antibody [HL1002] | GTX635791 | Кроличьи моноклональные антитела. Иммуноген: полноразмерный рекомбинантный белок RBD SARS-CoV-2 |
ИФА, сэндвич ИФА, функциональный тест, анализ на нейтрализацию/ингибирование |
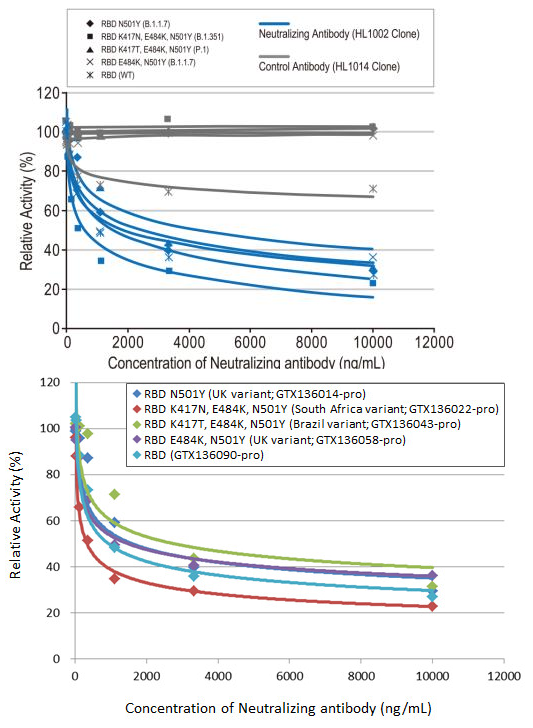
Рисунок 4. Анализы ингибирования взаимодействия RBD дикого типа и новых штаммов коронавируса с рецептором ACE2 с помощью нейтрализующих антител (конкурентный непрямой ИФА). Иммобилизованные RBD шиповидного белка SARS-CoV-2 с активной гистидиновой меткой (дикий тип) и RBD шиповидного белка SARS-CoV-2 с активной гистидиновой меткой новых вариантов коронавируса (адсорбировали в концентрации 2 мкг/мл), связывающихся с растворимым белком ACE2 (ECD) человека, содержащим активную метку Fc-фрагмента мышиного IgG (GTX135683-pro) (1000 нг/мл). Связывание ингибировалось при повышении концентрации нейтрализующего антитела [HL1002] к RBD (13,72-10000 нг/мл). Для выявления белковых комплексов добавляли козьи антимышиные антитела IgG, меченные пероксидазой хрена (HRP) (GTX213111-01) (1:10000).
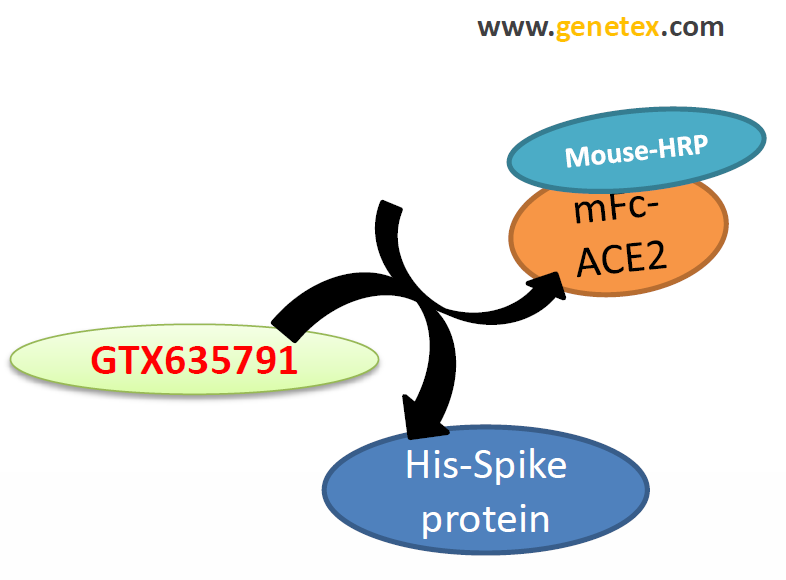
Рисунок 5. Схема анализа ингибирования взаимодействия RBD и ACE2 с помощью нейтрализующих антител HL1002 (GTX635791).
Производимые компанией Genetex антитела обладают разной аффинностью к новым штаммам коронавируса (анализ проведен с помощью непрямого ИФА; табл. 6).
| Эпитопная специфичность антитела | Каталожный номер антитела | Клон | WIV04/2019 (дикий тип) | B.1.1.7 | B.1.351 | P.1 |
|---|---|---|---|---|---|---|
| RBD | GTX635807 | HL1014 | • | • | • | • |
| RBD | GTX635792 | HL1013 | • | • | ○ | ○ |
| RBD | GTX635793 | HL1004 | • | • | ○ | • |
| S1 | GTX635713 | HL13402 | • | • | • | • |
| S1 | GTX635708 | GT263 | ✖ | ✖ | ○ | ✖ |
| S2 | GTX632604 | 1A9 | • | • | • | ○ |
| S2 | GTX635693 | HL237 | ○ | • | • | ✖ |
| • — сильная реакция. Определяется как значение оптической плотности (450нм) >1 при использовании 1 мкг/мл белка. ○ — слабая реакция. Определяется как значение оптической плотности (450нм) >1 при использовании 4 мкг/мл белка. ✖ — никакой реакции. Определяется как значение оптической плотности (450нм) <1 при использовании 4 мкг/мл белка. |
||||||
Литература
- Shin M.D., Shukla S., Chung Y.H. et al. (2020). COVID-19 vaccine development and a potential nanomaterial path forward. Nature Nanotechnology. 15, 646–655
- Callaway E. (2020). The race for coronavirus vaccines: a graphical guide. Nature. 580, 576–577
- «Биомолекула»: «Гонки вакцин 2020»
- Harvey W.T., Carabelli A.M., Jackson B. et al. (2021). SARS-CoV-2 variants, spike mutations and immune escape. Nat Rev Microbiol.. 19, 409–424
- Volkan E. (2021). Structural Considerations for Virus Pathogenesis, Therapeutic Strategies and Vaccine Design in the Novel SARS-CoV-2 Variants Era. Mol Biotechnol. 18, 1–13
- Starr T.N., Greaney A.J., Hilton S.K., Ellis D., Crawford K.H.D., Dingens A.S., Navarro M.J., Bowen J.E., Tortorici M.A., Walls A.C., King N.P., Veesler D., Bloom J.D. (2020). Deep Mutational Scanning of SARS-CoV-2 Receptor Binding Domain Reveals Constraints on Folding and ACE2 Binding. Cell. 182 (5), 1295–1310
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚


