-
В 1953 году, после того как Уотсон и Крик предложили модель двойной спирали ДНК, одной из центральных тайн молекулярной биологии оставался вопрос: как генетическая информация передается от «молекулы жизни» к функциональным компонентам клетки — белкам? Открытие матричной РНК — чрезвычайно важной молекулы-посредника — позволило сделать кардинальный шаг к его разгадке. Как выяснилось, она была своего рода «мессенджером», передавая зашифрованные в ДНК инструкции клеточным механизмам белкового синтеза. Казалось бы, какое простое (!) открытие… Однако кроме этого оказалось, что РНК не просто переносит информацию — это молекула с впечатляющим разнообразием форм и функций. Ее лабильность, ферментативная активность и способность к генной регуляции указывали на исключительное значение в клеточных процессах. В этом обзоре раскрываем удивительную роль РНК в патогенезе заболеваний, представляя хронологию развития РНК-терапии: от первых гипотез до клинического применения. Вы узнаете о ключевых прорывах в этой области, различных платформах на основе РНК, их механизмах действия, преимуществах и недостатках. Особое внимание уделим уже одобренным терапиям, а также перспективным лекарствам, проходящим клинические испытания. Почему мРНК-вакцины, препараты РНК-интерференции и антисенсы стали основными трендами в этой области? Как они купируют патологические процессы? Обо всем этом — в нашей статье.
-
3067Мы продолжаем увлекательное путешествие в мир инструментов для «генных правок». Если в предыдущей статье спецпроекта «Генная и клеточная терапии» мы познакомились с основами модификации генома животных, то теперь перейдем к самой интригующей части истории — изменению человеческой ДНК в медицинских целях. Теоретически уже сейчас можно переписывать «код жизни», превращая ранее неизлечимые недуги в поддающиеся коррекции. Но насколько далеко простираются границы этих возможностей? Что реально достижимо уже сегодня? Наше воображение будоражат соблазнительные картины: мы могли бы изменять врожденный цвет глаз, длину конечностей, уже с пеленок наделять детей исключительными способностями... Однако на практике передовые разработки сосредоточены на закрытии по-настоящему неудовлетворенных потребностей: исправлении ошибок природы, ведущих к тяжелым наследственным заболеваниям. Эта статья станет проводником в удивительный мир генной инженерии; раскроет секреты технологий, подаривших инструменты редактирования генома; подробно расскажет, как они появились и функционируют, какие перспективы открывают в науке и медицине; а также какие трудности стоят на пути ученых, и почему изменения в генах способны перевернуть представления человечества о здоровье и лечении.
-
1255Полгода назад мы рассказывали о новостях биофармы за первую половину 2024 года. В обзоре второй половины пойдет речь о статистике новых лекарств, одобренных FDA, о новых ярких препаратах, новостях клинических исследований и фундаментальной биомедицинской науки. Расскажем о первых в своем роде клеточных терапиях, новых применениях лекарств от ожирения, неожиданной пользе вакцинации от опоясывающего лишая и новом подходе к редактированию генов.
-
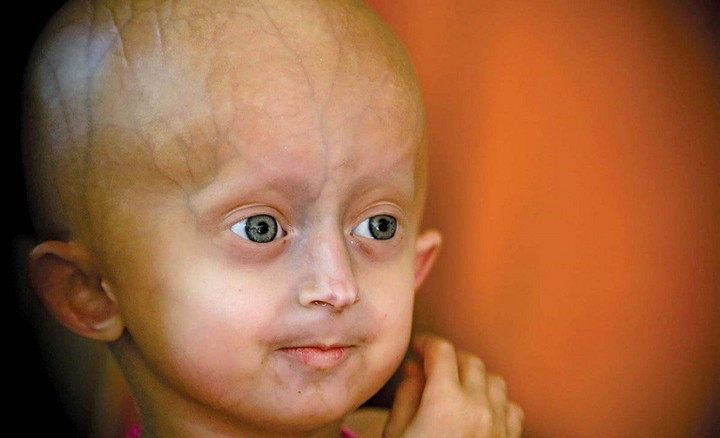
Статья на конкурс «Био/Мол/Текст»: Помните ли вы фантастическую историю Ф. Скотта Фицджеральда про необычного человека по имени Бенджамин Баттон, ставшую впоследствии основой фильма «Загадочная история Бенджамина Баттона»? Это история о человеке, который родился восьмидесятилетним мужчиной и в течение последующих восьмидесяти лет физиологически развивался в обратном порядке. Несмотря на фантастичность, в этой новелле есть момент реалистичности — главный герой рождается пожилым, что очень резонирует с редким генетическим заболеванием, при котором человек стареет преждевременно и молниеносно — детской прогерией (синдромом Хатчинсона-Гилфорда). По сравнению с другими прогероидными синдромами, которые различаются в зависимости от мутировавшего гена, при этом типе прогерии признаки преждевременного старения проявляются наиболее ярко. Для детей с этим синдромом жизнь настолько коротка, что они уже к трем годам приобретают вид 60-летнего человека и умирают, едва достигнув подросткового возраста. Прогерия изучается исследователями не только для того, чтобы найти заветное лекарство для помощи стареющим детям, но и для того, чтобы открыть путь к лечению миллионов взрослых с сердечно-сосудистыми заболеваниями и инсультом, связанными с естественным процессом старения. В этой статье речь пойдет о том, что такое детская прогерия и каков механизм ее развития, а также будут рассмотрены новейшие терапевтические достижения и будущие перспективы. Но обо всем по порядку.
-
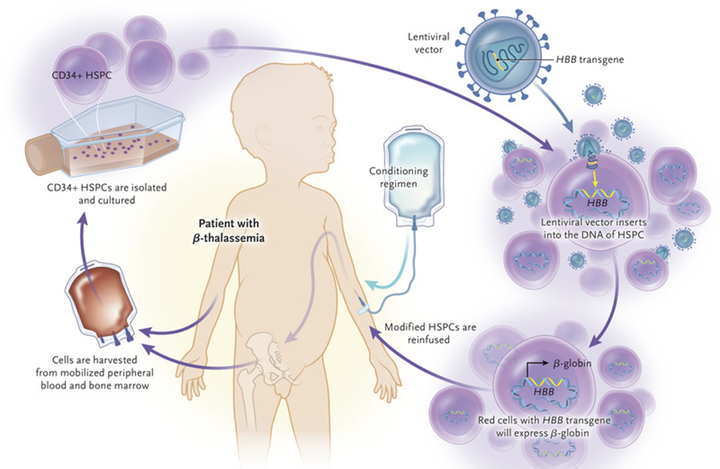
1612Терапия наследуемых моногенных заболеваний — серьезный вызов мировому здравоохранению, ведь далеко не все из них в принципе поддаются лечению. Особая их группа — лизосомные болезни накопления: хотя по отдельности они весьма редки, но в совокупности встречаются довольно часто, причем нередко бывают летальны. Причина этих патологий — снижение уровня одного или нескольких лизосомных ферментов, что приводит к накоплению в организме их субстратов, а это — к полиорганной недостаточности и зачастую к преждевременной смерти. Эти болезни сами по себе не проходят, но достаточно «хороши» для генной терапии: в теории тут достаточно лишь «починить» поломанный ген или же доставить его здоровую копию в нужные клетки и ткани, и — вуаля! — пациент излечится. На практике всё, конечно, не так просто...
-
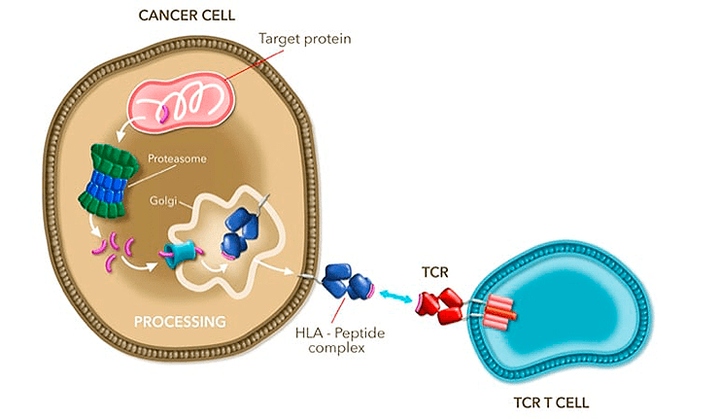
Август 2024-го ознаменовался ускоренным одобрением FDA препарата Tecelra (от Adaptimmune), ставшего на рынке инновацией сразу по трем направлениям. Во-первых, это первая генно-инженерная клеточная терапия, направленная на уничтожение со́лидной опухоли; во-вторых — первое новое лечение по данному показанию (неоперабельная/метастатическая синовиальная саркома) более чем за десятилетие; наконец, в-третьих — это совсем новый тип терапии (ранее исследовавшийся лишь в клинических испытаниях). Очевидно, что американский регулятор подарил этому препарату путевку в жизнь совсем не случайно, но насколько он на самом деле прорывной и эффективный? Разбираемся в нашей статье.
-
Термин «рак» обозначает группу болезней, вызванных аномально перерождающимися клетками, способными также распространяться по организму. Казалось бы: «понял проблему, так реши ее»! Но правда в том, что этиология рака невероятно сложна (притом до конца не изучена), а лечить его до сих пор непросто. В раковый патогенез часто вовлечены самые разные мутации, а потому логично использовать против него генную терапию, уже помогающую от ряда неизлечимых ранее болезней. Однако каждая опухоль индивидуальна (гены в опухолевых клетках могут иметь тысячи различных нарушений), и потому подобрать по-настоящему эффективное лечение получается далеко не всегда. В этой статье спецпроекта о генных и клеточных терапиях мы рассмотрим подводные камни применения генной терапии при раке, обсудим текущее состояние дел и поразмышляем о перспективах.
-
1068Статья на конкурс «Био/Мол/Текст»: Мы знаем, как сделать операцию на разные органы и исправить какие-то недостатки в них. Но как исправить то, что находится в каждой клетке нашего организма — наши гены? Этим и занимается генная терапия стволовых клеток, к которым и относятся гемопоэтические стволовые клетки (ГСК).
-
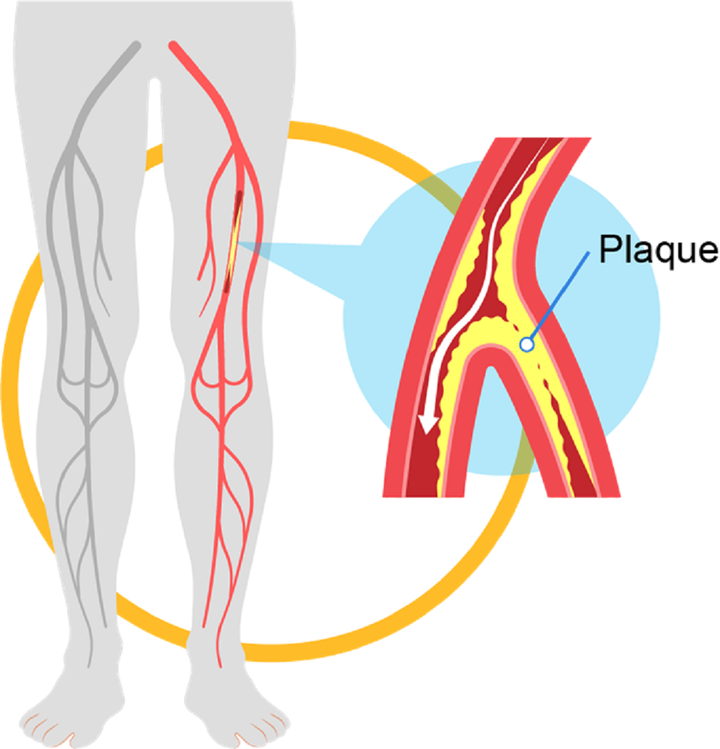
660Статья на конкурс «Био/Мол/Текст»: Сердечно-сосудистые заболевания являются одной из главнейших проблем медицины XXI века. Всем известно об ишемии и ее влиянии на сердечную мышцу, но не только сердце страдает от данной патологии. В нашей работе мы рассмотрим проблему ишемии задних конечностей и новые методы лечения с помощью клеточных и генных технологий. Кроме того, мы подробнее расскажем, что представляют собой процессы ангиогенеза и артериогенеза.
-
2023 год стал рекордным по количеству новых препаратов, одобренных FDA. Помимо одобрений, год ознаменовался множеством новостей в области клинических исследований и открытий в фундаментальной науке. Расскажем о самых ярких одобрениях, новостях клиники и биофармацевтической науки. Знаменитые обзоры биофармацевтического рынка Ильи Ясного, долгое время выходившие на портале «XX2 век», теперь перебрались на «Биомолекулу» — в спецпроект «Современные лекарства»!


- Лента
- Спецпроекты
- ▶Подкаст
-
Конкурс
- О конкурсе «Био/мол/текст»
- «Био/мол/текст»-2025/2026
- «Био/мол/текст»-2024/2025
- «Био/мол/текст»-2023/2024
- «Био/мол/текст»-2022/2023
- «Био/мол/текст»-2021/2022
- «Био/мол/текст»-2020/2021
- «Био/мол/текст»-2019
- «Био/мол/текст»-2018
- «Био/мол/текст»-2017
- «Био/мол/текст»-2016
- «Био/мол/текст»-2015
- «Био/мол/текст»-2014
- «Био/мол/текст»-2013
- «Био/мол/текст»-2012
- «Био/мол/текст»-2011
- Объявления
- Авторы
- Партнеры
- Поддержать
Публикации
—
Темы
—
Авторы
—
Комментарии
—
Поиск не дал результатов
По вашему запросу ничего не найдено
- Медицина
- SARS-CoV-2
- «Биомолекула» — Forbes
- Аллергия
- Антибиотики
- Атеросклероз
- Аутоиммунитет
- Боль
- ВИЧ/СПИД
- Вакцины
- Вирус Зика
- Вирус Эбола
- Генная терапия
- Грипп
- Депрессия
- Дерматология
- Диагностика
- Здравоохранение
- Нейродегенерация
- Никотин
- Онкология
- Персонализированная медицина
- Питание
- Сон
- Стволовые клетки
- Фармакология
- Эпилепсия
- Биология
- «Сухая» биология
- Антропология
- Бионика
- Биофизика
- Вирусология
- Вопросы пола
- ГМО
- Генетика
- Иммунология
- Микробиология
- Нейробиология
- Носимые технологии
- Психогенетика
- Синтетическая биология
- Старение
- Структурная биология
- Цитология
- Эволюционная биология
- Экология
- Эмбриология
- Эпигенетика
- Этология
- Биомолекулы
- GPCR
- АФК
- Амилоиды
- Биомембраны
- Гормоны растений
- ДНК
- Ионные каналы
- МГЭ
- Матрикс
- Нейромедиаторы
- РНК
- Рецепторы
- Хроматин