Когда в уравнении «мама, папа, я = вместе дружная семья» может появиться еще одна переменная?
31 марта 2026
Когда в уравнении «мама, папа, я = вместе дружная семья» может появиться еще одна переменная?
- 205
- 0
- 1
Привет, родня по митохондриям!
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Митохондрии известны всем под названием «энергетических станций клетки», но может ли случиться так, что собственная станция создаст серьезные риски — и дело тут не в экологии. Ученые придумали, как спастись от нависшей угрозы.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Истоки идеи
В сферу интересов современной медицинской генетики прочно вошли митохондриальные болезни. Основная роль в возникновении целой группы этих сложных заболеваний принадлежит мутационным изменениям в ДНК, причем в зависимости от локализации и особенностей изменений, можно разделить митохондриальные болезни на три группы. Патологические процессы могут быть вызваны:
-
мутациями в ядерной ДНК;
-
мутациями в митохондриальной ДНК (мтДНК);
-
нарушениями межгеномных сигнальных эффектов (связаны с мутациями ядерных генов-регуляторов) [1].
По крайней мере в 15–25 % случаев митохондриальные заболевания вызваны мутациями митохондриальной ДНК (мтДНК), которые могут возникать de novo (25 %) или передаваться по материнской линии [2], [3]. Эти заболевания «коварны» тем, что медицина не в силах предложить таким пациентам полноценного лечения — оно представлено симптоматической и поддерживающей терапией. Тем не менее, отсутствие эффективного лечения вовсе не означает, что помочь нельзя — возможно, именно так рассуждали ученые из Университета Ньюкасла. В 2025 году Медицинским журналом Новой Англии были опубликованы исследования, сообщающие о результатах пронуклеарного переноса митохондрий для семей, в которых вероятность передачи патогенной мтДНК от матери к ребенку была высока [4].
Именно митохондрия от донора смогла стать недостающим элементом пазла, чтобы сложить картинку полноценной и счастливой семьи.
Почему нужен донор и чем страшны митохондриальные болезни?
Нуклеотидная последовательность мтДНК человека (и многих других живых организмов) полностью расшифрована: в 37 генах мтДНК человека закодировано 13 структурных компонентов системы окислительного фосфорилирования (ОФ), 22 молекулы транспортных РНК (тРНК) и две рибосомальные РНК (рРНК) (рис. 1). Для синтеза белковых основ комплексов I, III, IV и V электрон-транспортной цепи используются упомянутые 13 генов, а закодированные в оставшихся 24 областях РНК имеют вспомогательное значение в процессах транскрипции и трансляции.
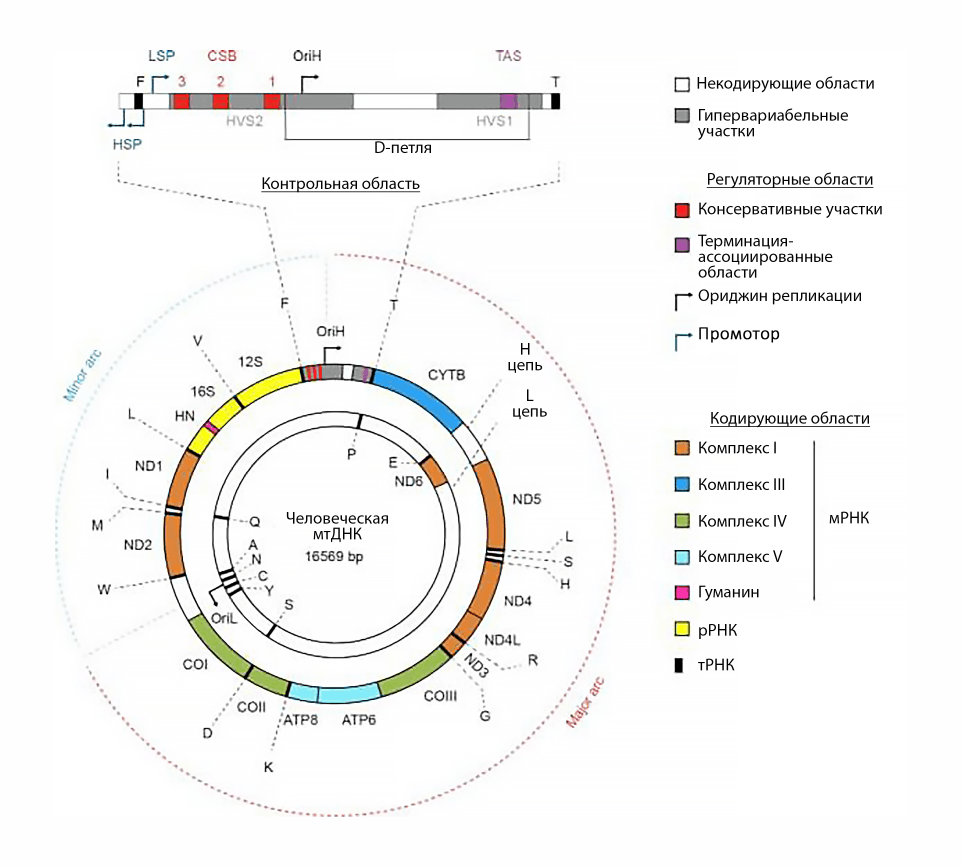
Рисунок 1. Структура мтДНК человека, показаны 37 генов и регуляторные области. Рекомендую обратить внимание на D-петлю — некодирующий регуляторный участок. Далее в тексте будет упомянуто одно из ее назначений!
[7], рисунок адаптирован
Митохондриальная ДНК обладает относительно высокой «поражаемостью»: особенности ее расположения делают мтДНК уязвимой «мишенью» для атаки свободных радикалов кислорода, образующихся по ходу окислительного фосфорилирования. Белки внутренней митохондриальной мембраны (TFAM, TWNK, ADAT3) образуют мультибелковый комплекс, связанный с нуклеоидом — формой организации генома в органелле. Комплекс прикрепляется к D-петле мтДНК, обеспечивая распределение нуклеиновой кислоты по матриксу вблизи внутренней мембраны — по совместительству, места протекания реакций дыхательной цепи [5], [6] (рис. 2).
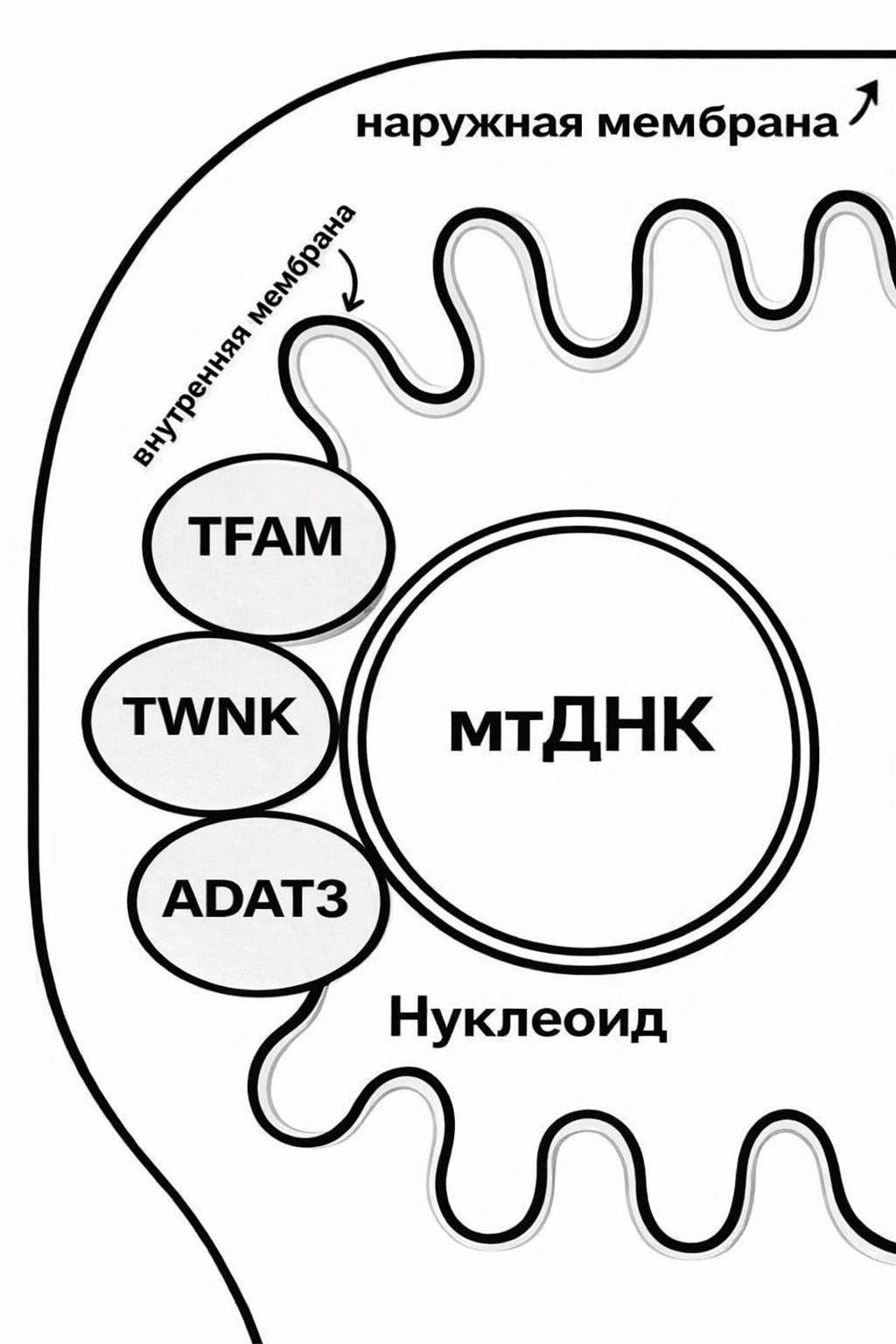
Рисунок 2. Схематичное изображение пространственной организации нуклеоида по отношению к внутренней мембране с помощью мультибелкового комплекса.
[5], в переводе и с изменениями
Пребывание усложняется и отсутствием специальной системы упаковки нуклеиновой кислоты — белков гистонов: выступая в качестве защиты в ядерной ДНК, гистоны способны «принять на себя» удар от супероксид-аниона, что невозможно в случае митохондриальной ДНК — для ее упаковки используются другие белки (прохибитины, ATAD3, TFAM, POLG). Возникшие вследствие окислительного стресса мутации способны сохраняться из-за недостаточно эффективной репарационной системы [7].
Проявления поражений напрямую связаны с экспрессируемыми с мтДНК генами, а значит — с компонентами дыхательной цепи: происходит снижение уровня энергоснабжения тканей и органов.
Наиболее серьезным нарушениям подвержены структуры, зависимые от аэробного катаболизма и требующие больших объемов энергии: клетки мозга, сердца и почек, структуры глаза (мышцы, зрительный нерв), скелетная мускулатура. Симптоматика митохондриальных заболеваний разнообразна: задержки развития, судороги, энцефалопатия, гипотония (миопатия) и нарушения зрения (ретинопатия). Более 80 % всех пациентов с митохондриальными заболеваниями жалуются на симптомы, связанные с мышцами (непереносимость мышечных нагрузок, утомляемость) [8].
Совершенно очевидно, что митохондриальные болезни имеют тяжелое течение с системными поражениями, а эффективные методы лечения на данный момент практически полностью отсутствуют. Риск рождения ребенка с таким диагнозом может обернуться для семьи серьезным испытанием.
Механизмы наследования митохондриальных болезней, связанных с мутациями в митохондриальной ДНК, отличны от менделевских. Вспомним, как возникает новая жизнь: сперматозоид оплодотворяет яйцеклетку. При этом генетический материал, представленный в виде молекулы ДНК, передается от обоих родителей. Но ещё со времен школьной скамьи всем нам известно: клетке нужно совсем не только ядро с генетической информацией, но и полный набор внутриклеточных органелл. Здесь на помощь приходит яйцеклетка: весь необходимый комплект органоидов несет именно она, прямо на своих, казалось бы, «хрупких женских» плечах. С таким разделением обязанностей связан механизм наследования митохондриальных болезней, вызванных мутациями в мтДНК — они наследуются по материнской линии.
Введем немного терминологии и разберемся с гомо- и гетероплазмией. В каждой клетке содержатся сотни, а то и тысячи копий мтДНК — явление многокопийности. Подобное изобилие делает возможным одновременное сосуществование и нормальных, и мутантных копий генетического материала, что называется гетероплазмией . При гомоплазмии , напротив, все мтДНК идентичны. Процент гетероплазмии ((число копий мутантной мтДНК / общее число копий мтДНК) × 100%), наравне с распределением поврежденных мтДНК по организму, определяет тяжесть заболевания и его клинические проявления [9], [10].
При оценке рисков используется еще одно понятие — пороговое значение гетероплазмии . Под ним понимают величину (в процентах) мутантной мтДНК, при которой появляются фенотипические проявления. Для разных типов тканей пороговое значение варьирует в диапазоне от 60% до 90% [11].
Для женщин с высоким уровнем мутантной митохондриальной ДНК существуют огромные риски при планировании беременности. Вероятность рождения малыша с упомянутыми патологиями может быть практически стопроцентной. Однако, если заменить исходные, «опасные» митохондрии теми, что мутаций не несут, получится минимизировать (или вовсе, свести к нулю?) шансы развития заболевания у ребенка.
Дуглас Тернбулл, директор Центра исследования митохондрий, полученный прорыв в репродуктологии комментирует так: «Митохондриальные заболевания могут разрушительно влиять на семьи. Однако в нынешних реалиях у женщин в группе риска возрастает возможность иметь ребенка, растущего без этих ужасных заболеваний.»
Как понять, когда «бить тревогу»? О методах выявления нарушений митохондриального генома
Абсолютным авангардом методов оценки повреждений мтДНК в клетках является секвенирование «нового поколения» (NGS — next generation sequencing). С помощью него выявляются не только крупномасштабные делеции, но и точечные мутации путем сравнения мтДНК исследуемого и референсного генома. Более того, становится возможным точно оценить уровень гетероплазмии — пожалуй, ключевой в нашем разговоре момент. Для упомянутого метода используют образцы из периферической крови, мочи и биоптаты мышечной ткани. На просторах «Биомолекулы» есть работы, посвященные NGS — рекомендую ознакомиться любопытному читателю [12]. Ненадолго погрузимся в рабочее пространство лаборатории (рис. 3).
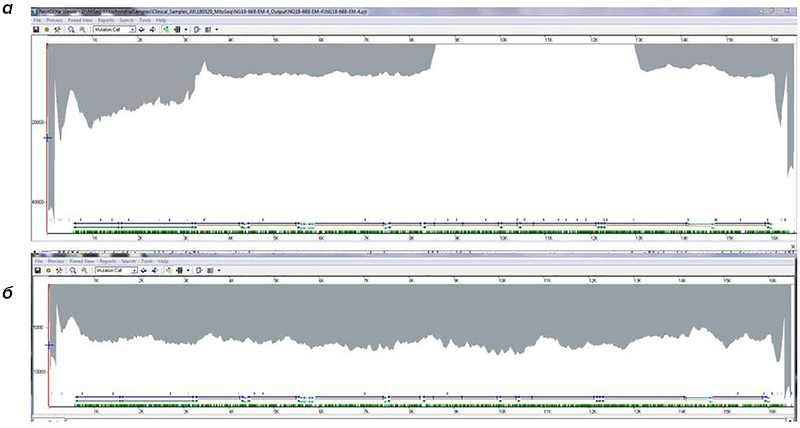
Рисунок 3. Обнаружение крупномасштабной делеции методом NGS у пациента с 96% гетероплазмии. а — панель результатов пациента, б — панель референса. Серое поле отражает глубину покрытия — простыми словами, число независимых прочтений на каждый нуклеотид референсной последовательности (отложены по оси X сверху). Само число прочтений отложено по оси Y, поэтому оценить их количество позволяет высота серых пиков. У пациента видна обширная делеция — участок, где серое поле «проваливается» — заметные различия обусловлены высоким уровнем гетероплазмии (т.е. искомого фрагмента совсем мало!)
Отдельного внимания требует пиросеквенирование — один из методов, относящихся к секвенированию «нового поколения». С его использованием предстоит встретиться далее. В основе лежит последовательный синтез дочерней цепи ДНК на матрице ДНК-фрагментов изучаемого организма (в нашем случае — на матрице мтДНК пациентки). В ходе элонгации происходит высвобождение пирофосфатов, которые запускают последовательные процессы, оканчивающиеся хемилюминесценцией — по-простому, маленькой вспышкой света. Раскрыть таинства последовательности процессов, лежащих в основе метода, предлагаю коллеге [13].
Традиционно, мутации в мтДНК выявляются с помощью Саузерн-блоттинга. Суть метода заключается в связывании ДНК-зонда, содержащего радиоизотоп или флуоресцентную метку, с искомой последовательностью [14]. Результаты в виде полос на фотопластинке (фрагменты и их размеры) служат индикатором, содержится ли в материале только нормальная мтДНК, или имеются и поврежденные участки. Для анализа используются образцы, полученные из мышечной ткани. Однако метод не позволяет точно оценить уровень гетероплазмии или выявить конкретные участки, содержащие нарушения [10] (рис. 4).
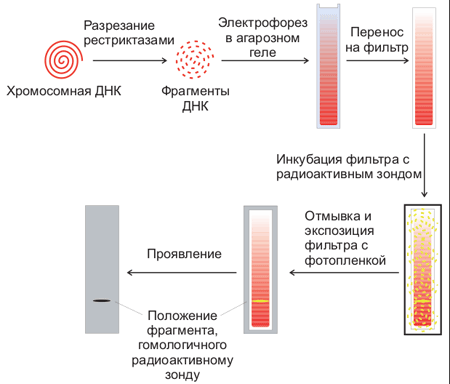
Рисунок 4. Схема проведения Саузерн-блоттинга.
Для визуализации соотношения нормальной митохондриальной ДНК и ДНК, содержащей нарушения, используется реакция флуоресцентной in situ гибридизации (FISH-метод). В анализе используются 2 типа зондов, каждый с различными флуорофорами (например, красный и зеленый). Первый зонд «универсален» и связывается с последовательностями, имеющимися и в нормальной, и в поврежденной мтДНК. Второй же нацелен на участки, утраченные в мутантной копии, но имеющиеся в нуклеиновой кислоте дикого типа — их выясняют с помощью уже упомянутых методов секвенирования «нового поколения» или ПЦР. В результате «универсальный» зонд будет связываться с каждой мтДНК, а второй будет действовать более избирательно — «внимания» удостоится только неповрежденная генетическая информация митохондрии. Полученные результаты позволяют хоть и не точно, но оценить соотношение разных типов мтДНК в клетках [10].
Достижения британцев
16 июля 2025 года свет увидела публикация о прорыве в мире вспомогательных репродуктивных технологий: сообщается о появлении на свет и успешном постнатальном развитии 8 детей, получивших митохондрии от донора [4].
Всего в исследовании приняли участие 71 пациентка с высоким уровнем гетероплазмии или гомоплазмией по мутантной мтДНК. Женщины были разделены на следующие группы: 32 пациентки получили разрешение властей (HFEA — Human Fertilisation and Embryology Authority, Управление по оплодотворению и эмбриологии человека Великобритании) на проведение пронуклеарного переноса; 39 пациенток получали помощь в обретении детей с помощью технологии преимплантационного генетического тестирования (ПГТ).
- Пронуклеарный перенос
- — вспомогательная репродуктивная технология, основанная на объединении цитопласта с мтДНК дикого типа от донора и пронуклеусов от родителей: пациентки с высоким уровнем гетероплазмии (или же гомоплазмией по мутантной мтДНК) и ее партнера.
- Пронуклеусы
- — гаплоидные ядра гамет в зиготе; формируются в процессе оплодотворения из ядра яйцеклетки и ядра сперматозоида.
Необходимость получения первой группой особого разрешения со стороны органов управления обусловлена очень тонким биоэтическим аспектом проблемы: с точки зрения морали, этики и закона, допустимо ли рождение детей с «тремя» родителями? Тем не менее, на проведение пронуклеарного переноса было «дано добро», хоть это и заняло время исследователей — путь к разрешению применения технологии в практике начинался еще в 2015 [15].
Деление на группы обусловлено уровнем мутантной мтДНК. В случае гомоплазмии (12 участниц), при которой появление яйцеклетки с допустимым, т.е. <30% содержанием патогенной мтДНК, невозможно, ПГТ было неэффективным, и единственно возможным вариантом становилось использование пронуклеарного переноса. На пронуклеарный перенос направлялись и женщины с гетероплазмией, в случае отсутствия у них эмбрионов с низким уровнем мутантной ДНК по результатам ПГТ в рамках этого же исследования — таких было 3; еще 10 «обладательниц» высокого уровня гетероплазмии сразу вошли в группу переноса.
Возможно, вы усомнитесь в моих математических способностях, ведь 12 + 3 + 10 явно не дадут в сумме 32, но спешу оправдаться: на момент публикации лишь 25 участниц прошли процедуру полностью (рис. 5).
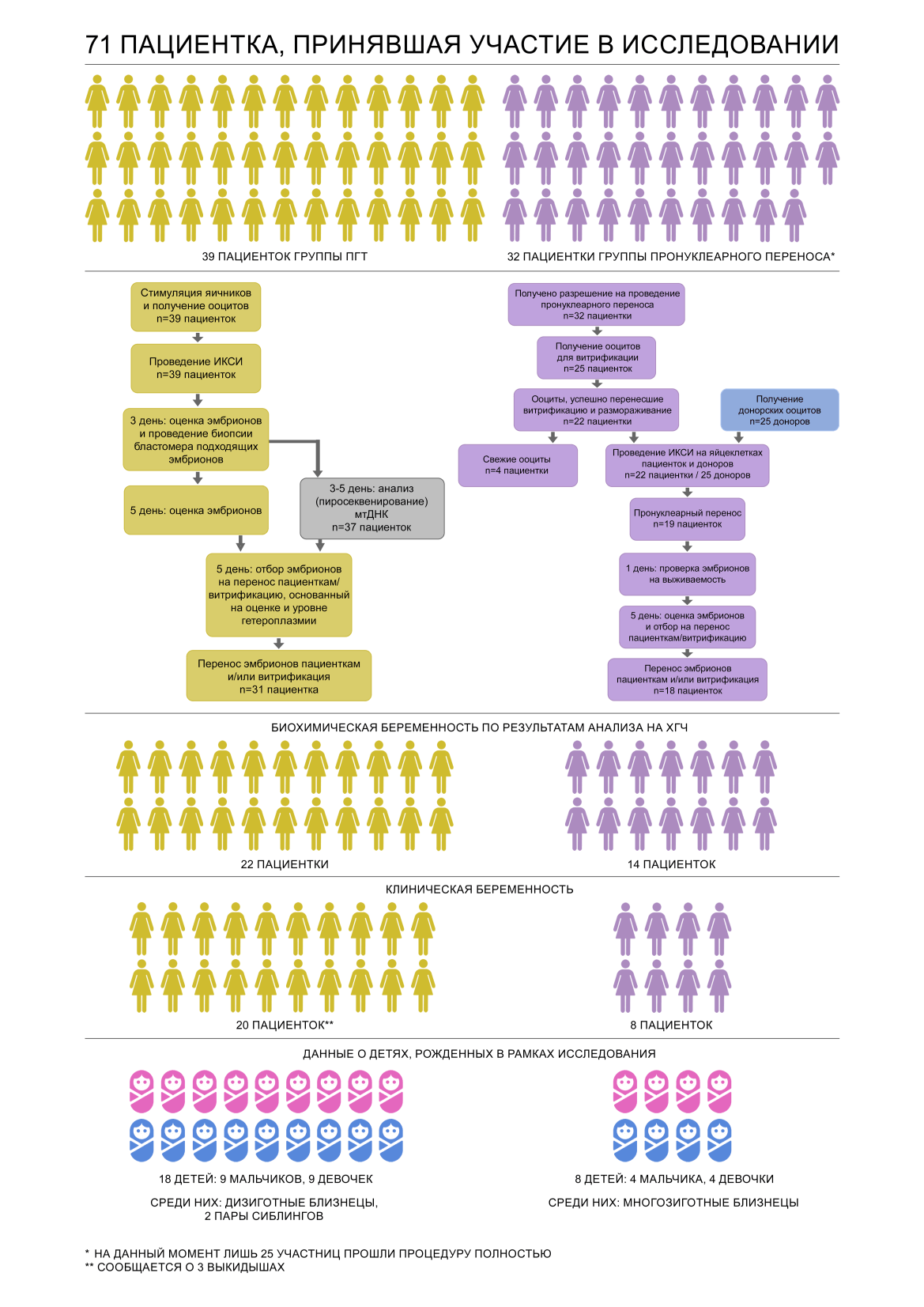
Рисунок 5. Результаты различных этапов исследования Университета Ньюкасла.
авторская схема, с дополнениями из [18]
С 39 участницами, попавшими в группу ПГТ, все, относительно мира репродуктологии, «просто»: производилась гормональная стимуляция яичников по протоколу (выбор протокола зависит от репродуктивного здоровья женщины, предполагаемого и реального овариального ответа [16]) для получения яйцеклеток, которые в дальнейшем оплодотворялись посредством ИКСИ (intracytoplasmic sperm injection — интрацитоплазматическая инъекция сперматозоида). После культивации на 3 день происходил забор одного бластомера для анализа, после чего эмбрионы развивались еще 2–3 дня. Для дальнейшего переноса отбирались те эмбрионы, в которых, по результатам анализа, уровень гетероплазмии оказывался достаточно низким, чтобы говорить о рождении здоровых детей. Все произведенные процедуры прочно вошли в современную стезю вспомогательных репродуктивных технологий и едва ли способны кого-то удивить. Тем не менее, даже «знакомость» этих технологий и частота использования не гарантируют стопроцентные результаты: из 39 пациенток успешно выносить и родить удалось лишь 14. Проследить за изменениями количества пациенток на каждом из последовательных этапов удобно на схеме (рис. 5). От случая к случаю причины неудачи на каком-либо из шагов разнятся. Среди них:
-
на 3 день эмбрионы только 37 пациенток содержали 6 и более бластомеров;
-
эмбрионы 31 пациентки были отобраны для имплантации/витрификации по результатам оценки качества эмбриона и результатам пиросеквенирования;
-
биохимическая беременность по результатам теста на хорионический гонадотропин человека (ХГЧ) наступила в 22 случаях — свидетельствует об успешной имплантации эмбриона
-
клиническая беременность, подтвержденная УЗИ на 7 неделе беременности, была установлена у 20 пациенток. Причины самопроизвольного прерывания беременности, когда положительный тест на ХГЧ был, но дальнейшего развития плода не произошло, не уточняются. В целом, среди причин выделяют генетические аномалии эмбриона, гормональные причины, иммунные и аутоиммунные причины, особенности строения матки, социальный и психоэмоциональный факторы [17].
А вот детей у 14 пациенток получилось 18 — одна из пациенток родила дизиготных близнецов, а еще двое обзавелись парой сиблингов в результате нескольких беременностей. (рис. 5)
Интереснее обстоят дела у группы пронуклеарного переноса. Начальные этапы различий не имели. Гормональную стимуляцию яичников для получения яйцеклеток проводили и пациенткам, и донорам митохондрий. Яйцеклетки последних также проходили дополнительную проверку для определения патогенных последовательностей мтДНК, чтобы не вышло обмена «шила на мыло». Все полученные женские гаметы далее проходили через процедуру ИКСИ, и через 8–13 часов начиналась репродуктивная магия.
Из оплодотворенных донорских яйцеклеток извлекались «ненужные» пронуклеусы — гаплоидные ядра гамет, сформировавшиеся в процессе оплодотворения. Полученная безъядерная структура, называемая цитопластом, сохраняла все функциональные компоненты цитоплазмы, мембрану, и что самое важное, — митохондрии с генетическим материалом дикого типа. Место, ранее занятое пронуклеусами доноров, спешили занять пронуклеусы, полученные от будущих родителей. Они вводились в энуклеированную донорскую зиготу с предварительной обработкой агентом, способствующим слиянию (рис. 6). Результаты манипуляций можно представить в виде уравнения: реконструированная зигота = цитопласт донора с мтДНК дикого типа + пронуклеусы с генетическим материалом от пары, обратившейся за помощью к ученым.
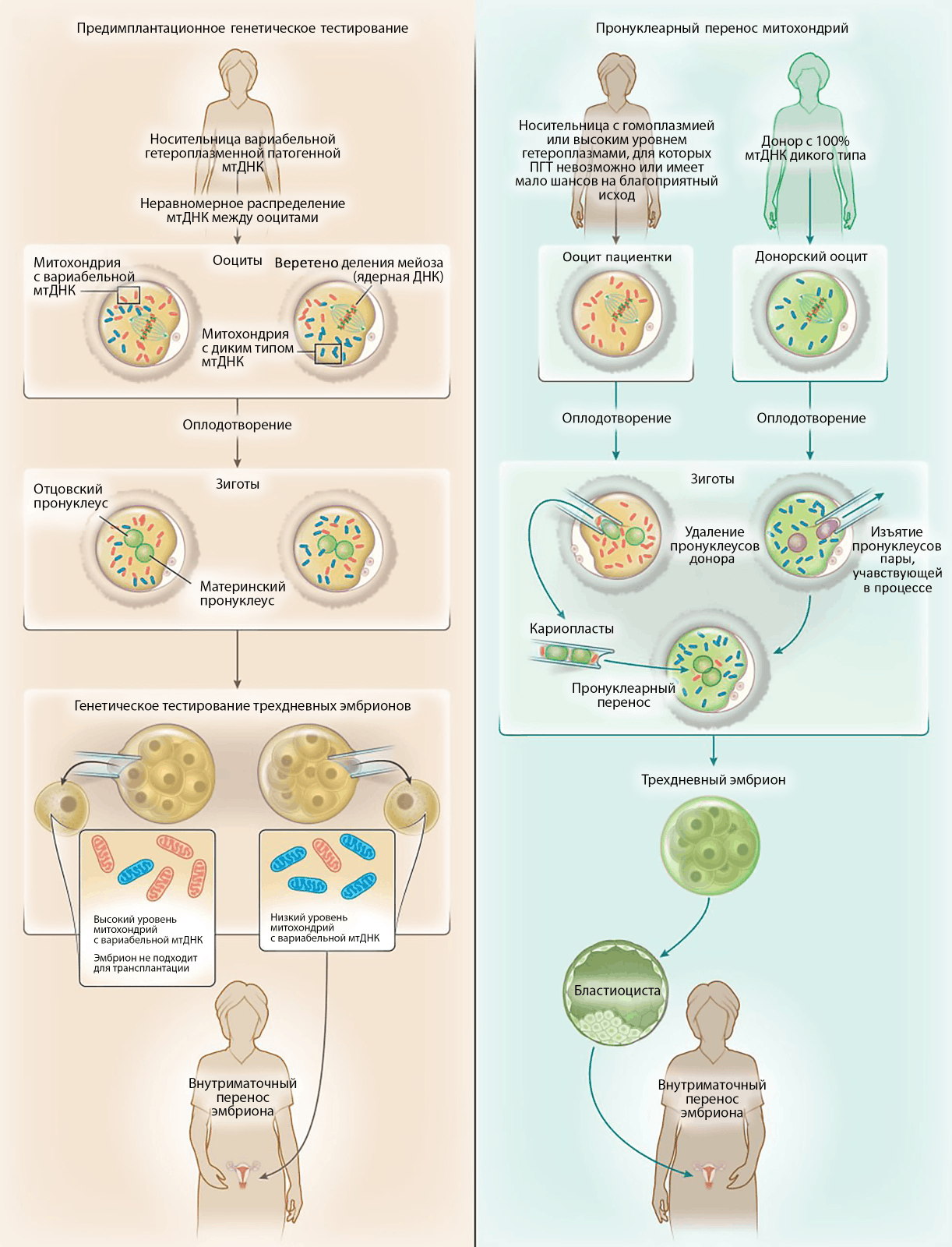
Рисунок 6. Технология пронуклеарного переноса.
Принципиально важным был следующий шаг ученых: оценить все произошедшие изменения в объеме цитоплазмы. Говоря простыми словами, измеряли, сколько цитоплазмы (а значит, и митохондрий в ее составе) «ушло» при изъятии донорских пронуклеусов, и сколько цитоплазмы «пришло» при переносе ядер гамет родителей. Такое внимание обуславливается связью «цитозольных махинаций» с уровнем гетероплазмии — все-таки термин иллюстрирует отношение патогенной мтДНК к нормальной. И без знаний высшей математики ясно: как увеличение числителя, так и уменьшение знаменателя приведут к росту показателя. Поэтому надзор — самый строжайший [18]!
Из полученных эмбрионов уже привычно нам изымалось по одному бластомеру для исследования, а результаты ложились в основу ранжирования и дальнейшего отбора эмбриона для трансплантации. Пристальные наблюдения, совместные надежды исследователей и пар, и на свет появилось 8 малышей, формально имеющие троих родителей. 4 мальчика и 4 девочки родились без признаков митохондриальных болезней, и на момент публикации сообщается о нормальном развитии, соответствующем возрасту (рис. 5).
¡Espere señora!
¡Espere señora!, что в переводе «Сеньора, подождите!» могли бы воскликнуть ученые из другой исследовательской группы, не получив упоминания в этом разговоре. И действительно — испанские коллеги заявляли о результатах митохондриального переноса ещё в 2023 [19].
Публикация сообщает о 6 детях в возрасте 12–24 месяцев, родившихся и развивающихся без признаков мтДНК-ассоциированных патологий. Так почему же новость из Соединенного Королевства вызвала резонанс, если все это уже где-то было?
На самом деле, проведенные исследования имели в основе разные механизмы. И в Британии, и в Испании (а на деле — на базе Института Жизни в Греции, потому как испанские законы митохондриальную донацию запрещают) производился перенос, но на разных этапах жизни материнской гаметы. Команда сеньоров и сеньор сумела транспортировать веретено деления метафазы II. По достижении нужной фазы из ооцита-донора извлекался собственный генетический материал с последующей заменой генетическим материалом от женщины с высоким уровнем гетероплазмии. Только после, в уже реконструированный ооцит, вводился сперматозоид посредством хорошо знакомого ИКСИ (рис. 7). Описанный механизм снимает необходимость, например, последующей обработки агентом для слияния. [19]
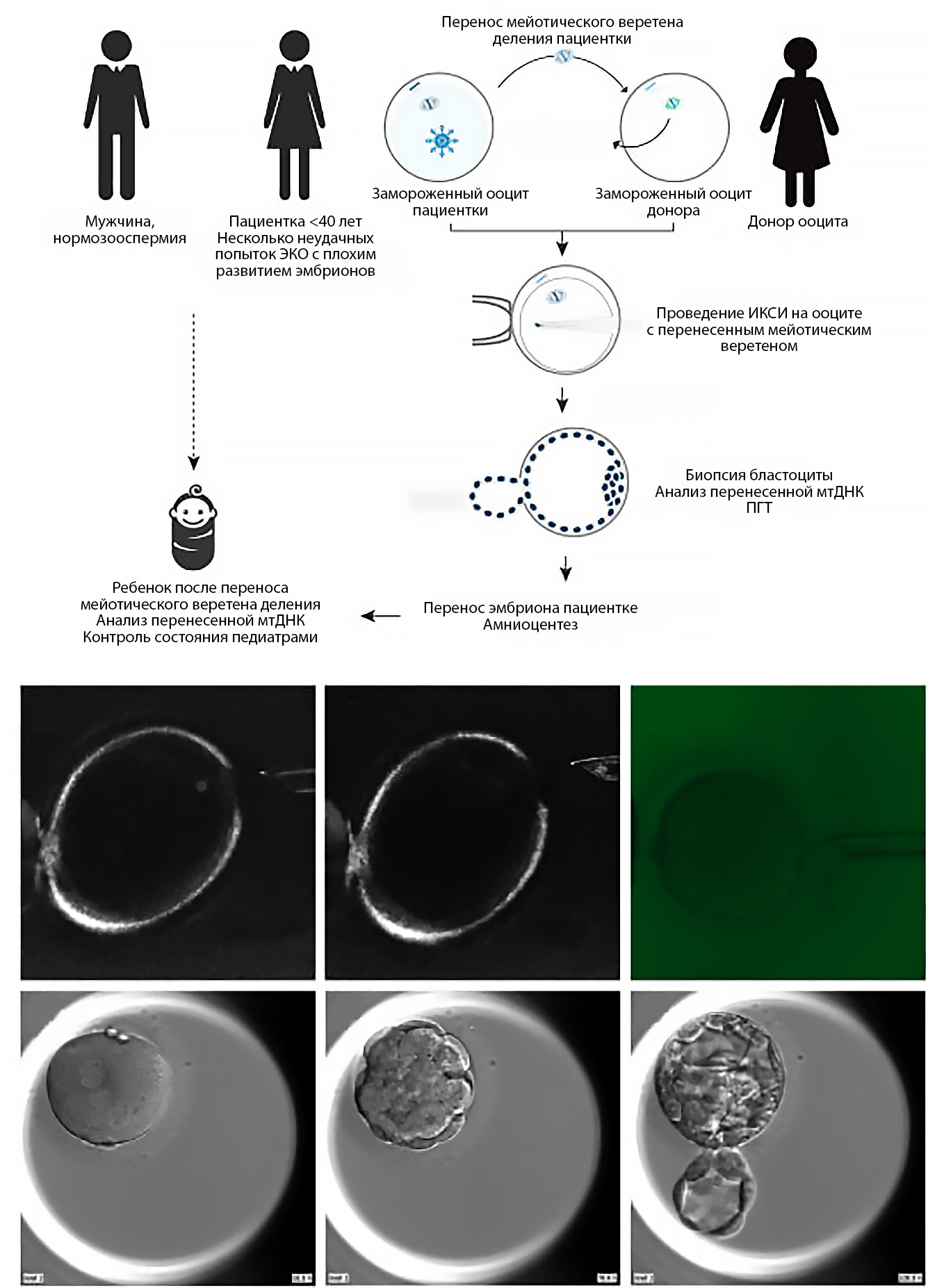
Рисунок 7. Технология переноса мейотического веретена деления.
[19], рисунок адаптирован
Интересно на примере данного исследования вспомнить о значении соотношения цитоплазм «пришедших» и «ушедших». У одного из детей, рожденного в рамках работы испанского коллектива, впоследствии был выявлен достаточно высокий уровень гетероплазмии — он оценивался учеными в диапазоне от 30% до 60%. К счастью, никаких клинических проявлений полученное соотношение не нашло, но случай позволяет посмотреть на события в ретроспективе. Несмотря на низкий процент перенесенной от материнского ооцита цитоплазмы вместе с веретеном деления (заявляется о попадании не более 1% мтДНК мамы), содержание патогенной ДНК митохондрий выросло в десятки раз. Механизм такого «скачка» загадочен, но, наиболее вероятно, связан со способностью «энергетических станций» к самоудвоению. По всей видимости, самоудвоение попавших в донорскую цитоплазму митохондрий из материнского ооцита происходило чаще, чем могло ожидать. К сожалению, порою и столь ювелирные методы не могут давать стопроцентных гарантий.
Погрузимся в хроники
Ошибочно полагать, что за возможность помочь семьям, столкнувшимся с проблемой наследования патогенной мтДНК, боролись лишь 2 страны (если считать Грецию — 3). На самом деле, попытки минимизации рисков передачи митохондриальных болезней предпринимались еще в прошлом столетии: с помощью процедуры переноса в 1997 году на свет родился первый ребенок. Однако, перенос там был несколько иной: переносились не конкретные структуры, а цитоплазма целиком, образуя некий «микс» из донорской и материнской. К 2016 году было рождено по различным данным от 30 до 50 детей с использованием переноса цитоплазмы [20]. Позднее, этот метод был вытеснен более прогрессивными и уже известными нам переносом пронуклеусов и переносом веретена деления на стадии метафазы II.
Есть еще один способ, по которому зарегистрированных случаев рождения на данный момент нет, — использование для переноса генетического материала полярных телец, образующихся по ходу оогенеза (рис. 8). К сегодняшнему дню результаты переноса полярных телец получены в доклинических испытаниях на мышах и макаках [2], [21]. Конкурентное преимущество методу может обеспечить малое содержание митохондрий в направительных тельцах. Тем не менее, без внимания не остались и риски этой технологии: задача полярных телец, образующихся по ходу мейоза, в выведении избыточного генома, что может повлиять на качество уже ядерной генетической информации. Ясно одно — для оценки безопасности и эффективности необходимо продолжение исследовательских работ, в частности — на ооцитах человека.
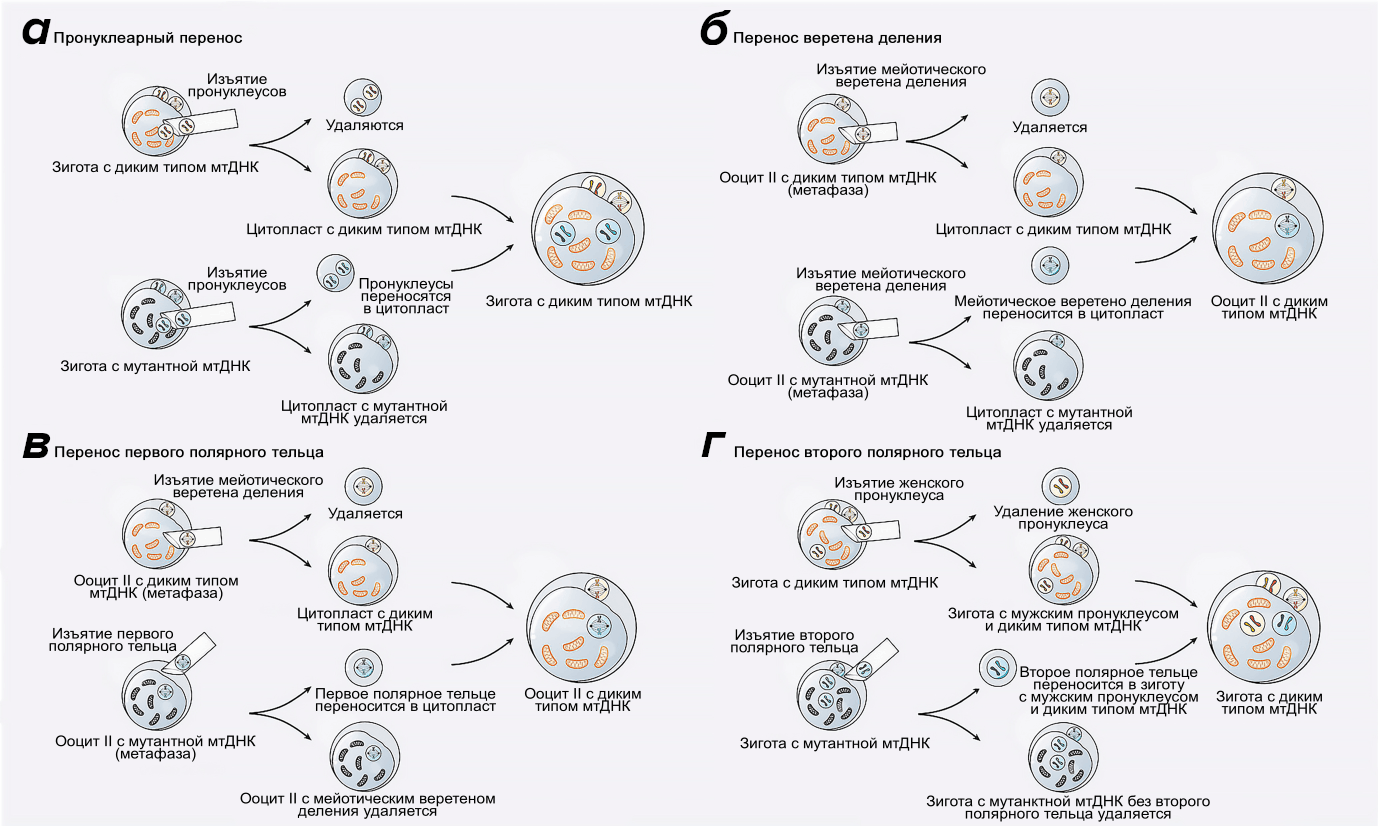
Рисунок 8. Методы митохондриального переноса.
а, б — рассмотрены ранее на отдельных иллюстрациях;
в — перенос первого полярного тельца. Из ооцита II донора извлекается мейотическое веретено деления, заменяемое в дальнейшем первым направительным тельцем от пациента;
г — перенос второго полярного тельца. Из зиготы донора извлекается женский пронуклеус, на его место вносится второе направительное тельце от пациента. Мужской пронуклеус изменений не претерпевает.
[3], рисунок адаптирован
Интересны и правовые стороны вопроса: подавляющее большинство стран не разрешает проведение любых форм митохондриального переноса на своей территории, во всех остальных процедура проводится только по предоставленному разрешению от органов власти. В России на сегодняшний день применение митохондриальной заместительной терапии никак не регламентируется юридически. В связи с этим внедрение и применение описанных технологий в нашей стране пока невозможно [22].
Биоэтический аспект всегда немного философский: с одной стороны, все признаки, которые получит ребенок, определены ядерной ДНК, и закодированную в мтДНК информацию глаз «обывателя» увидеть не способен. Какое дело до белков дыхательной цепи, когда носик — явно мамин, а кудрявая голова точно от такого же кудрявого папы? С другой же стороны, как, например, самому юному человеку от мысли, что где-то у него есть родня по, скажем, комплексу IV? Как бы там ни было, этим вопросом предстоит заняться другим людям, а приближенным к миру медицинских технологий остается лишь оценить открывшиеся перспективы.
Литература
- Ярыгин В.Н. Биология. М.: ГЭОТАР-Медиа, 2023. — 1287 с.;
- Hubert J.M. Smeets, Suzanne C.E.H. Sallevelt, Mary Herbert. (2023). Reproductive options in mitochondrial disease. Handbook of Clinical Neurology. 207–228;
- Haipeng Wen, Hui Deng, Bingyan Li, Junyu Chen, Junye Zhu, et. al. (2025). Mitochondrial diseases: from molecular mechanisms to therapeutic advances. Sig Transduct Target Ther. 10;
- Eight babies born after Mitochondrial donation. (2025). Newcastle University;
- Mohammed Almannai, Azza Salah, Ayman El-Hattab. (2022). Mitochondrial Membranes and Mitochondrial Genome: Interactions and Clinical Syndromes. Membranes. 12, 625;
- Sung Ryul Lee, Jin Han. (2017). Mitochondrial Nucleoid: Shield and Switch of the Mitochondrial Genome. Oxidative Medicine and Cellular Longevity. 2017;
- Gabriele A Fontana, Hailey L Gahlon. (2020). Mechanisms of replication and repair in mitochondrial DNA deletion formation. Nucleic Acids Research. 48, 11244–11258;
- Michelangelo Mancuso. (2023). Complex neurological and multisystem presentations in mitochondrial disease. Handbook of Clinical Neurology. 117–124;
- Мазунин И.О. (2012). Особенности митохондриальных заболеваний. Педиатрический вестник Южного Урала. 1, 86–88;
- Ali Naini, Robert Gilkerson, Sara Shanske, Jiuhong Pang. (2020). Detection of mitochondrial DNA (mtDNA) mutations. Methods in Cell Biology. 383–400;
- Nadee Nissanka, Carlos T Moraes. (2020). Mitochondrial
DNA heteroplasmy in disease and targeted nuclease‐based therapeutic approaches. EMBO Reports. 21; - 12 методов в картинках: секвенирование нуклеиновых кислот;
- 454-секвенирование (высокопроизводительное пиросеквенирование ДНК);
- Важнейшие методы молекулярной биологии и генной инженерии;
- Трое в лодке: о легализации замены митохондрий;
- Бош Э., Броер С., Гризингер Г., Гринберг М., Хумайдан П., Колибианакис Э. и др. (2021). Клинические рекомендации ESHRE: овариальная стимуляция в программах ЭКО и ИКСИ (перевод на русский под ред. проф. В.С. Корсака). Акушерство и гинекология: Новости. Мнения. Обучения, 9, 34–51;
- Малышкина А.И., & Батрак Н.В. (2015). Факторы риска самопроизвольного прерывания беременности у женщин с привычным невынашиванием в анамнезе. Медицинский совет. 20, 46–49;
- Louise A. Hyslop, Emma L. Blakely, Magomet Aushev, Jordan Marley, Yuko Takeda, et. al. (2025). Mitochondrial Donation and Preimplantation Genetic Testing for mtDNA Disease. N Engl J Med. 393, 438–449;
- Nuno Costa-Borges, Eros Nikitos, Katharina Späth, Irene Miguel-Escalada, Hong Ma, et. al. (2023). First pilot study of maternal spindle transfer for the treatment of repeated in vitro fertilization failures in couples with idiopathic infertility. Fertility and Sterility. 119, 964–973;
- «Википедия»: Mitochondrial replacement therapy;
- Tian Wang, Hongying Sha, Dongmei Ji, Helen L. Zhang, Dawei Chen, et. al. (2014). Polar Body Genome Transfer for Preventing the Transmission of Inherited Mitochondrial Diseases. Cell. 157, 1591–1604;
- Пресс-служба Кафедра медицинского права. (2025). Агентство городских новостей «Москва»: Алексей Кубышкин о законодательном регулировании митохондриальной заместительной терапии. Московский государственный юридический университет имени О.Е. Кутафина (МГЮА).
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚