
Почему многие убитые персонажи Агаты Кристи живы и при чем тут сельское хозяйство? Рассказ с перчинкой про «диверсантов» клеточного дыхания
11 марта 2026
Почему многие убитые персонажи Агаты Кристи живы и при чем тут сельское хозяйство? Рассказ с перчинкой про «диверсантов» клеточного дыхания
- 247
- 1
- 3
коллаж автора
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В этой статье мы рассмотрим, что такое электронно-транспортная цепь митохондрий, как она работает и какие ее комплексы можно заблокировать на примере самых популярных ядов.
Многие наверняка читали произведения Агаты Кристи, где жертв убивали с помощью цианистого калия, ингибитора электронно-транспортной цепи митохондрий, или слышали историю про отравление Распутина «вином и пирожными с цианистым калием», но только почему-то Распутин выжил после такого «кушанья», а вот персонажи «королевы детектива» нет…
Какой циклон был назван буквой «Б» и причем тут абрикос? И как «молекулярный почерк» убийцы в точности совпадает с «почерком» препарата, который должен спасать жизни?
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Школьная» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — Благотворительный фонд «Белая лилия», который поддерживает школьников, студентов профильных вузов, научных коллективов врачей и ученых по разработке и созданию прорывных технологий в области медицины.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Ответ на эти, казалось бы, разрозненные загадки лежит не в архивных сводках или сюжетных хитросплетениях, а в самом сердце живой клетки. У этих дел разные жертвы, эпохи и мотивы, но есть одна общая улика: во всех случаях жертва сталкивалась с нарушением клеточного дыхания. Наше расследование начнется с изучения «места преступления» — ЭТЦ и закончится полным раскрытием метода, который используют «молекулярные киллеры»: от антибиотиков до цианида.
Путешествие электрона, которое вы не забудете
Чтобы понять преступление, нужно восстановить исходный, «законный» процесс, который оно нарушает. Внутри митохондрии происходит не производство, а трансформация энергии. Это последовательность окислительно-восстановительных реакций, где электроны, полученные от «сжигания» пищи, передаются по строгому маршруту — электрон-транспортной цепи (ЭТЦ). Чтобы понять, как митохондрии производят энергию, нужно знать их устройство.
У митохондрии есть две мембраны: внешняя (гладкая) и внутренняя, которая образует складки (кристы) для увеличения площади поверхности. Между мембранами есть межмембранное пространство. Пространство митохондрий, ограниченное внутренней мембраной, называется матрикс.
«Место преступления»— электрон-транспортная цепь (ЭТЦ). Это ансамбль из белковых комплексов, встроенных во внутреннюю мембрану. Именно здесь происходит перенос электронов, который в конечном итоге и приводит к производству энергии.
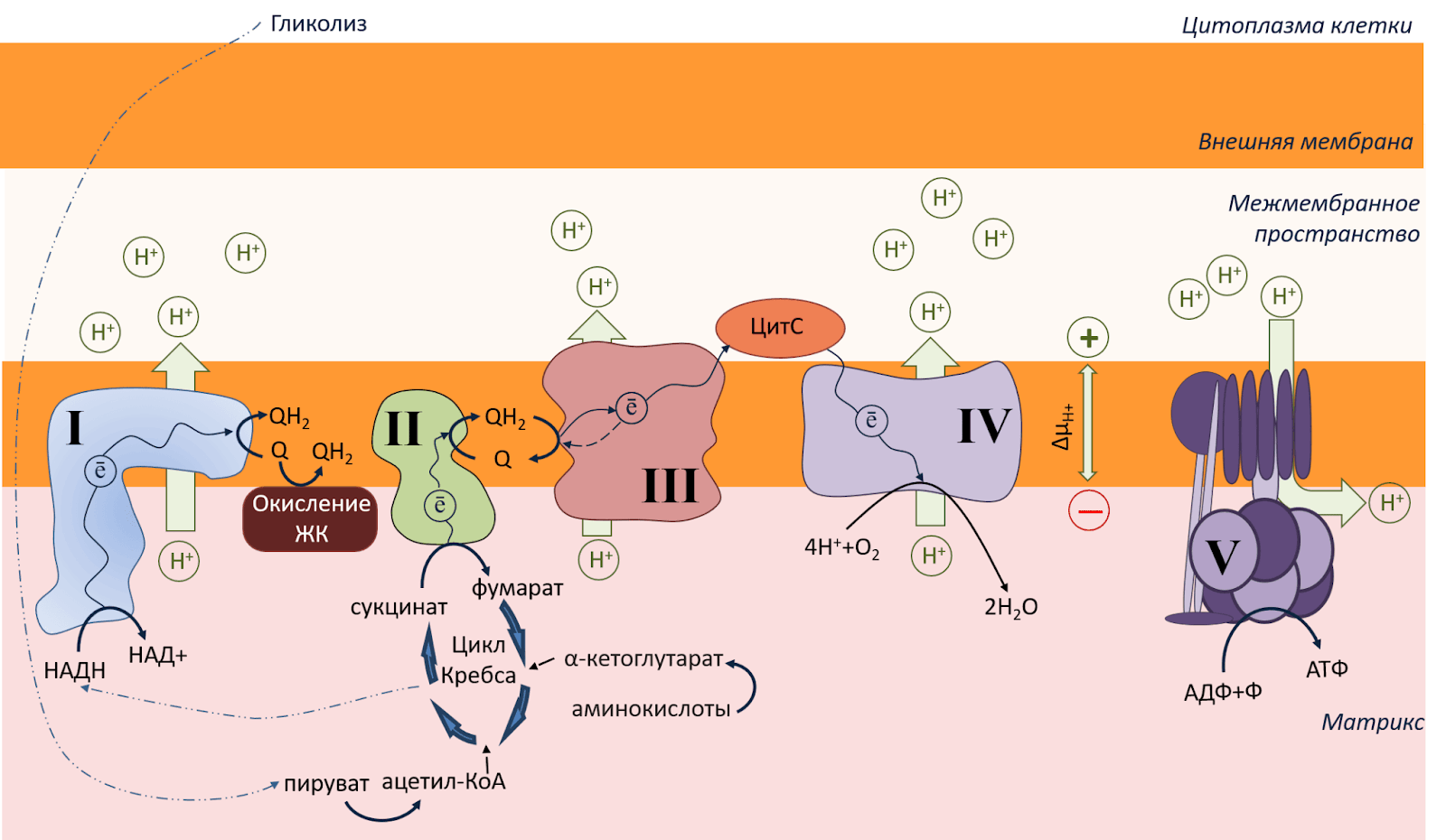
Рисунок 1. Схема работы ЭТЦ.
Электрон-транспортная цепь — это последовательность белков, которые переносят электроны (e). Эти электроны поступают от молекул-доноров: НАДH и сукцината (участника цикла Кребса). Сами же эти доноры образуются в процессе гликолиза (реакции окисления глюкозы до пировиноградной кислоты) и цикла Кребса (центральная часть биохимического процесса распада основных питательных веществ; кроме того, в ходе цикла происходит восстановление коферментов НАД⁺(никотинадениндинуклеотид) и ФАД(флавинадениндинуклеотид) до НАДH и ФАДН₂, которые являются ключевыми переносчиками электронов для цепи дыхания и синтеза АТФ)
Процесс в ЭТЦ начинается, когда НАДH и сукцинат отдают свои электроны (окисляются) первым комплексом дыхательной цепи (I и II). Далее электроны попадают на убихинон (Q) – жирорастворимый кофермент, один из переносчиков электронов на протяжении всего процесса клеточного дыхания.
Заполненный электронами убихинон (теперь он называется убихинол (QH2)) перемещается к комплексу III, где передает электроны на цепочку белков-цитохромов — трансмембранных переносчиков электронов — начиная с цитохрома b.
В комплексе III происходит сложная реакция (Q-цикл), в результате которой один электрон отправляется к новому хинону, а другой — на следующий переносчик, цитохром c. Его задача — «доставить» электрон от III комплекса к финальному IV комплексу.
Именно здесь используется кислород, который мы вдыхаем. Он действует как «финальный пункт приема» для электронов, прошедших всю цепь. Забирая у них энергию и соединяясь с протонами, кислород превращается в воду, что является безопасным способом утилизации отработанных электронов.
А пока наши электроны путешествовали по дыхательной цепи, три ее комплекса (I, III и IV) работали как протонные насосы, перекачивая протоны (H⁺) из внутренней части митохондрии (матрикса) наружу, создавая градиент концентрации протонов.
Так как протоны несут положительный заряд, снаружи внутренней мембраны создается сильный «плюс», а внутри — сильный «минус». Это формирует электронный градиент. Таким образом, протоны участвуют в создании электрохимического градиента на мембране митохондрии.
Протоны «хотят» вернуться внутрь, но не могут пройти через мембрану, так как имеют заряд, а заряженные частицы самостоятельно не могут пройти через гидрофобный участок мембраны.
Единственные «ворота» для их возвращения — это сложный молекулярный мотор АТФ-синтаза. Когда протоны протекают через нее, сила их потока вращает часть фермента, как вода вращает турбину гидроэлектростанции. Эта электрохимическая энергия используется для сборки молекул АТФ — главной энергетической валюты клетки — из энергетически менее богатых молекул, АДФ и фосфата [1].
Важно сказать, что дыхательная цепь может работать только если переносчики и белковые комплексы готовы принять электроны. Сильный электрохимический градиент слегка "тормозит" работу комплексов I, III, IV, уменьшая их способность передавать электроны. Это обеспечивает обратную связь: если градиент слишком велик (АТФ-синтаза перестает прокачивать протоны через мембрану, при большой концентрации АТФ в клетке), перенос электронов замедляется, что предотвращает образование вредных активных форм кислорода (АФК), которые могут буянить и окислять то, что не надо [2].
Про АФК можно отдельно почитать в отдельном разделе на «Биомолекуле» «Активные формы кислорода»
Больше про митохондрии можно прочитать в статье «Тайная жизнь митохондрий» [1].
Вся эта отлаженная система основана на безупречном молекулярном узнавании. Каждый участник — от электрона до кофермента — имеет уникальную «форму», подходящую к определенному сайту в белковом комплексе. Эта необходимость в идеальном совпадении и есть «ахиллесова пята» процесса.
Теперь мы знаем маршрут и ключевые станции. Давайте начнем наше расследование с самой первой и крупной из них — комплекса I. Именно здесь в игру вступает наш первый и, пожалуй, самый древний диверсант, чья история начинается не в лаборатории, а в мутных водах тропических рек.
НАДH-дегидрогеназный комплекс ( I )
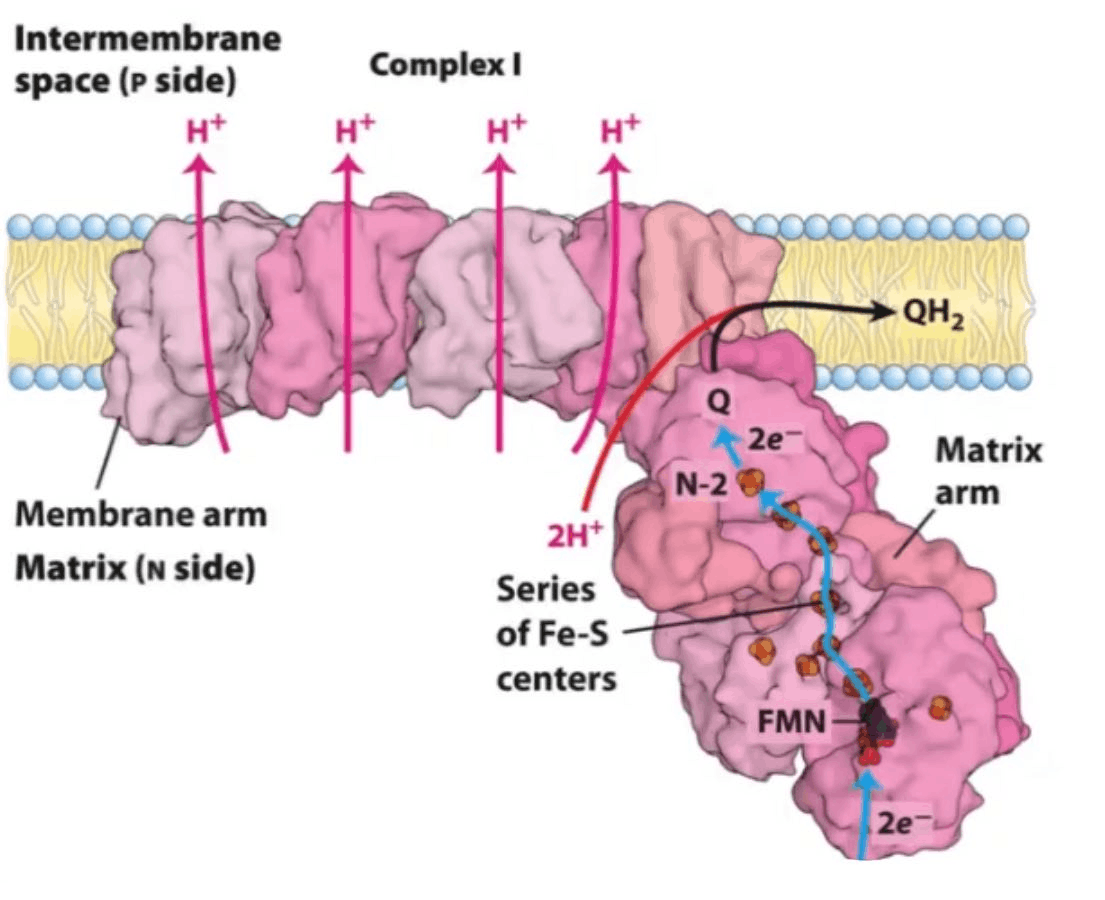
Рисунок 2. Строение НАДH-дегидрогеназного комплекса; intermembrane space (межмембранное пространство), matrix (матрикс), membrane arm («мембранная рука», заякоривающая комплекс в митохондриальной мембране), series of Fe-S centres (железо-серные кластеры), FMN (флавинмононуклеотид), N2 (железо-серный белок из железо-серного кластера).
Комплекс I — начальное звено всего процесса. Он создает около 40% электрохимического потенциала, который затем используется для производства АТФ. Его работа включает два этапа:
-
Химическая реакция: он забирает электроны у НАДH и передает их на ФМН (Флавинмононуклеотид), а затем на комплекс железосерных кластеров (N) и дальше на убихинон, превращая его в убихинол. С НАДH-дегидрогеназным комплексом (комплекс I) связывается хиноновое кольцо (голова) молекулы убихинона. Длинный изопреноидный хвост служит для якорения в мембране и правильного позиционирования, но в самом акте переноса электронов не участвует.
-
Создание градиента: параллельно с этой реакцией комплекс действует как протонный насос, перекачивая 4 протона из матрикса в межмембранное пространство для каждой обработанной молекулы НАДH [3].
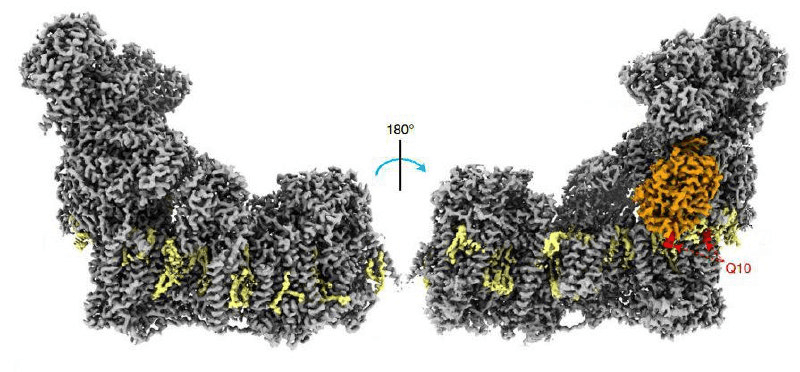
Рисунок 3. Строение НАДH-дегидрогеназного комплекса с двух сторон. Q10 — сайт связывания убихинона.
Эффективность комплекса I критически зависит от его способности связывать убихинон. Эта же особенность делает комплекс уязвимым для специфических ингибиторов. Классический пример — растительный токсин ротенон…
Яд-оборотень. Как растение обманывает рыбу
Ротенон — диверсант-изофлавоноид, широко применяемый как пестицид. Попадая в организм, ротенон взаимодействует с сайтом связывания убихинона, тем самым конкурируя с основным субстратом комплекса I. Ротенон — структурный самозванец. Он не является точной копией убихинона, но виртуозно воспроизводит ключевые элементы, необходимые для связывания в комплексе I.
Его плоская ароматическая часть имитирует хиноновое кольцо. Она попросту занимает пространство в сайте связывания: одна голова-хорошо, но больше-лучше:
-
Его карбонильные группы занимают то же положение, что и карбонильные группы убихинона, и образуют аналогичные водородные связи с аминокислотами в сайте связывания убихинона.
-
Его гидрофобный "хвост" взаимодействует с гидрофобными участками связывающего кармана, подобно изопреноидной цепи самого убихинона.
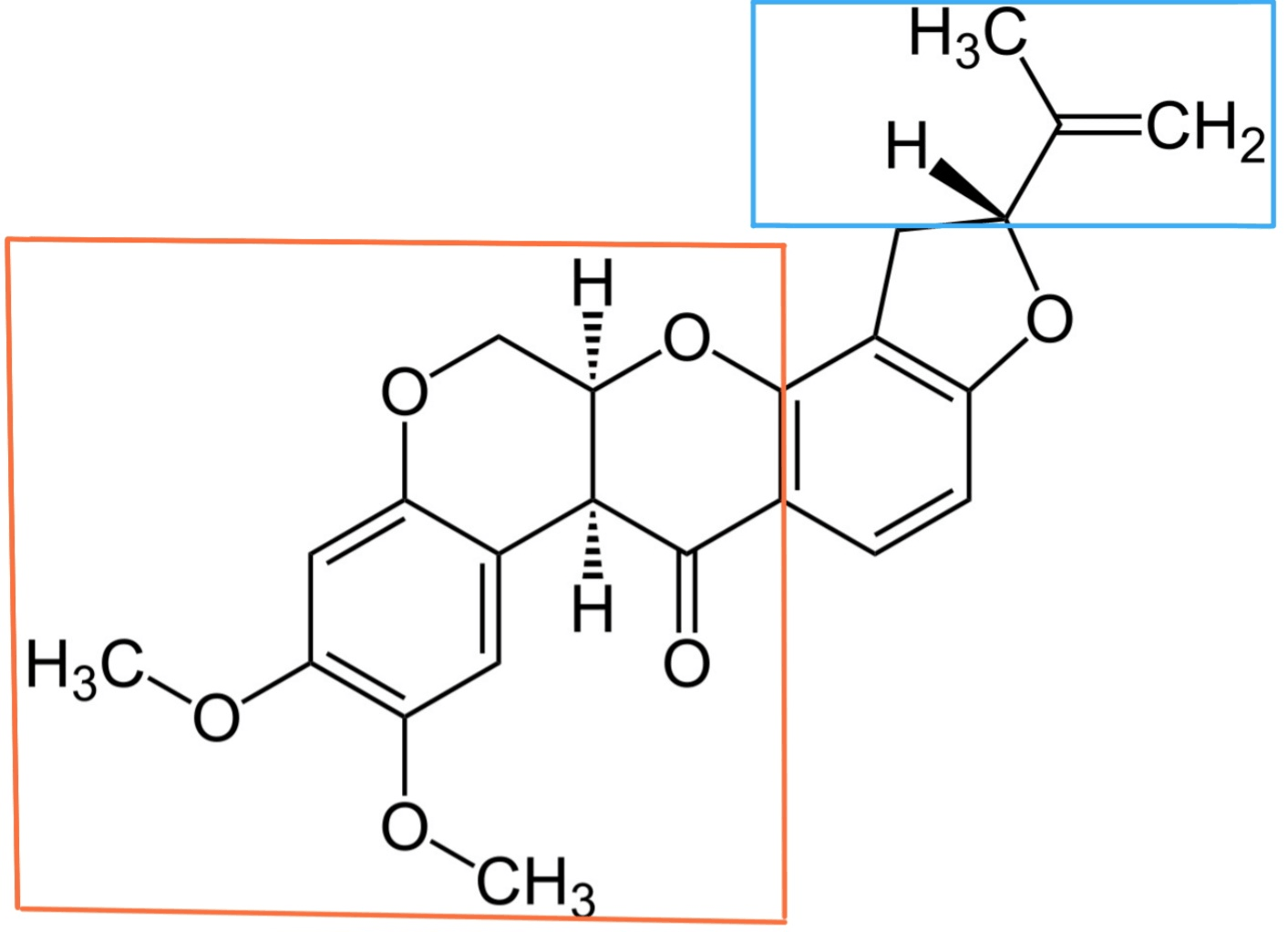
Рисунок 4. Структурная формула ротенона, оранжевым выделена часть молекулы, мимикрирующая под гидрофильную «голову» убихинона, голубым обозначена часть, мимикрирующая под гидрофобный «хвост».
Заняв место убихинона, ротенон не способен выполнять его работу — переносить электроны. Он создает непроходимую пробку в самом начале электрон-транспортной цепи. Цепь переноса электронов обрывается, синтез АТФ прекращается, и клетка, лишенная энергетической валюты, погибает [5].
Интересно, что многие сложные яды работают как молекулярные самозванцы-диверсанты. Они достаточно похожи на естественные молекулы организма, но, заняв чужое место, такой «диверсант» не способен выполнять настоящую работу: он не умеет ни расщеплять нужные субстраты, ни переносить электроны, что просто приводит к ступору работы вначале комплекса, а потом и всего процесса.
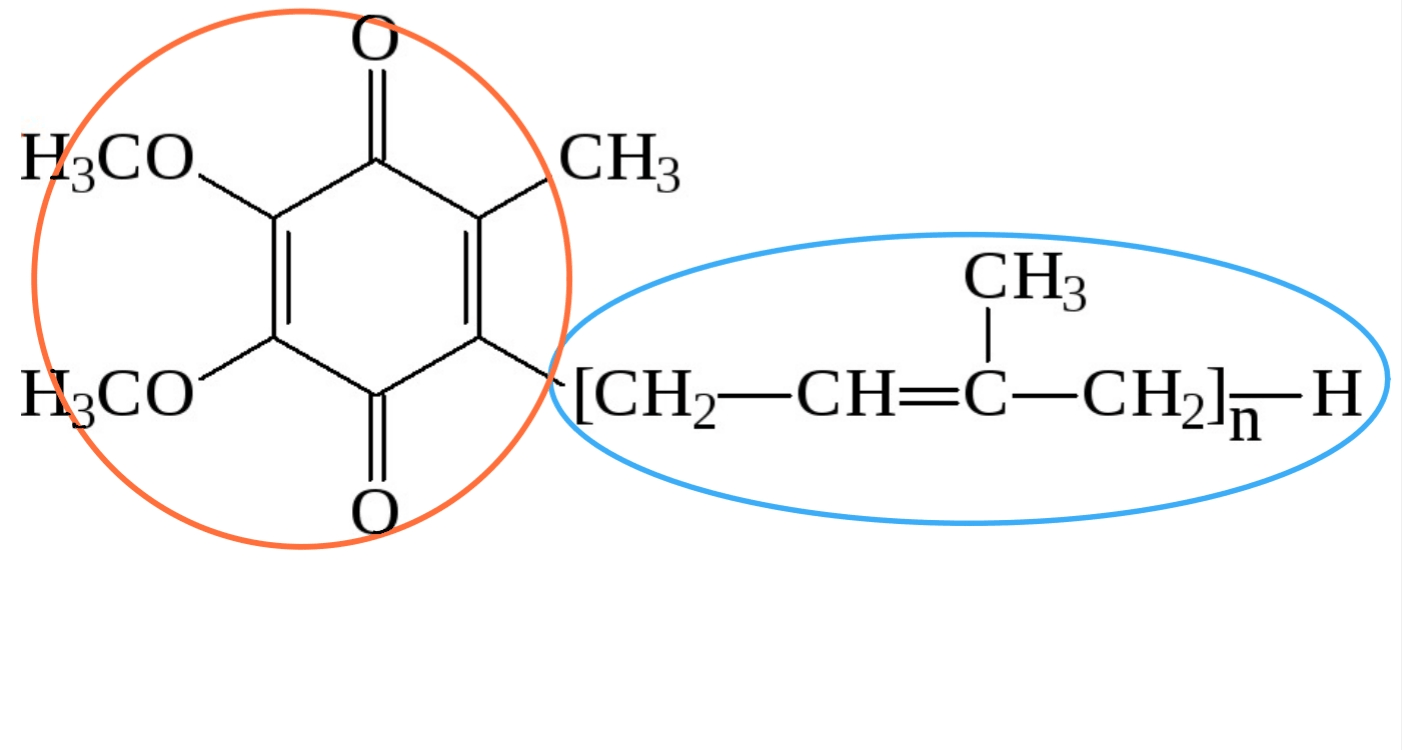
Рисунок 5. Структурная формула убихинона, оранжевым выделена гидрофильная «голова», голубым — гидрофобный «хвост».
Исторический путь этого диверсанта любопытен. Добываемый из растений семейства Логаниевые, он веками использовался индейцами Южной Америки для ловли рыбы. Под действием яда рыба просто всплывает на поверхность. Этот же принцип — в контролируемых, низких дозах — сегодня применяется в ихтиологии для научного мониторинга популяций донных рыб: например, в заранее огороженных сетью местах распыляют раствор ротенона. Рыба, находящаяся в этой зоне, погибает и всплывает на поверхность.
Один и тот же молекулярный диверсант в водной среде становится оружием массового поражения, а на суше — гораздо менее опасным нарушителем, чью атаку наш организм часто способен отразить. Его эффективность в воде объясняется идеальными условиями для проникновения: через жабры — ничем не защищенную поверхность контакта — яд молниеносно попадает в кровоток, достигая цели до того, как сработает какая-либо защита. Концентрация ротенона в крови рыбы быстро достигает смертельного уровня. Млекопитающие, в свою очередь, должны съесть ротенон, чтобы отравиться. В желудочно-кишечном тракте он всасывается медленнее, частично может метаболизироваться или разрушиться печенью (система первого прохождения), прежде чем достигнет митохондрий в критической концентрации. Также у млекопитающих есть мощные изоформы ферментов (например, CYP1A2, CYP2D6, CYP3A4), специализирующиеся на детоксикации широкого спектра ядов. У рыб набор изоформ CYP иной, эволюционно сформированный для решения задач водной среды. Их основные CYP (например, CYP1A) могут быть менее эффективны против специфических наземных токсинов, таких как ротенон [6].
Расследование выявило тревожную закономерность: способность блокировать дыхательную цепь митохондрий — опасный «молекулярный почерк» — характерна не только для классических ядов. Этот же механизм лежит в основе нежелательного побочного действия многих лекарственных препаратов. Учитывая, что разница между терапевтическим и токсическим эффектом зачастую определяется лишь концентрацией и особенностями организма, ученые настаивают на обязательной проверке всех новых соединений на митохондриальную токсичность [7].
Классический пример — метформин, ключевой препарат против диабета. Его действие, как оказалось, тоже включает мягкое ингибирование комплекса I. Одна и та же биохимическая диверсия в высоких дозах убивает, а в строго рассчитанных — лечит. Грань между ядом и лекарством оказалась тоньше, чем можно было предположить [8].
Необычными ингибиторами могут выступать и ванилоиды, особенно ярким представителем которых является капсаицин (то самое жгучее вещество в остром перчике). При более высоких концентрациях (выше 200–300 мкМ) или при длительной инкубации первым делом капсаицин проникает в митохондрию и нарушает протокол безопасности — сбрасывает протонный градиент. Это заставляет ЭТЦ работать в аварийном, «несвязанном» режиме, на максимальных, неуправляемых оборотах, без производства полезного АТФ. Из-за бешеной скорости в системе начинаются сбои. Электроны, не успевшие пройти по штатному маршруту, «просачиваются» с процесса и вступают в реакцию с кислородом. Это приводит к выбросу активных форм кислорода (АФК) — в первую очередь супероксид-радикала. Начавшееся перекисное окисление липидов бушует в самой уязвимой зоне — во внутренней мембране митохондрии. Именно здесь расположены все комплексы дыхательной цепи. Главная ударная волна приходится по комплексу I. Его гигантская, сложнейшая структура, встроенная в мембрану и оснащенная железосерными кластерами, оказывается беззащитна перед АФК. Нарушается целостность его структурного окружения и выводит из строя внутренние цепи передачи электронов [9].
Если диверсия здесь не удалась или цель требует точечного удара, злоумышленники меняют тактику. Они ищут обходной путь, который есть у каждой хорошей системы. И находят его — это тихий и эффективный комплекс II, катализатор реакции из цикла Кребса.
Комплекс II (Сукцинат-дегидрогеназный комплекс) и комплекс III (цитохром bс1-комплекс)
Привет из цикла Кребса или работа комплекса II
После цикла Кребса сукцинат связывается с активным центром комплекса. Происходит реакция, в процессе которой от сукцината отщепляется 2 водорода, и благодаря этому ФАД (такой же кофермент, как и в комплексе 1) принимает электроны и протоны, восстанавливаясь до ФАДH₂. Электроны от ФАДH₂ последовательно передаются через железосерные кластеры ([Fe-S]) на убихинон (Q) в мембране. Убихинон принимает также 2 протона из матрикса, восстанавливаясь до убихинола (QH₂) [4].
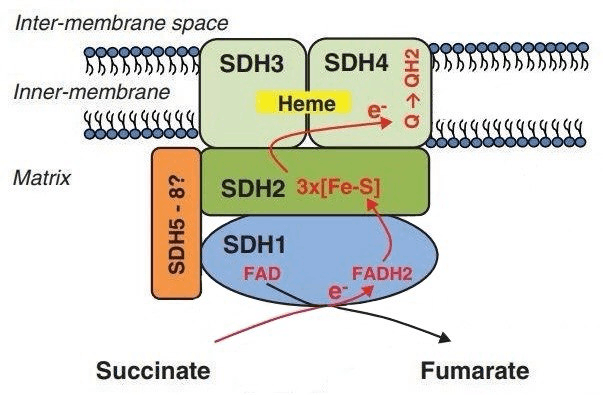
Рисунок 6. Схематичная структура сукцинат-дегидрогеназного комплекса. Данный ферментный комплекс образован четырьмя субъединицами. Две из них (SDH1 и SDH2) являются гидрофильными и каталитическими: SDH1 — это флавопротеин с FAD, а SDH2 — железосерный белок с тремя кластерами. Две другие субъединицы (SDH3 и SDH4) — гидрофобные, интегральные мембранные белки, которые удерживают комплекс в мембране и образуют цитохром b-типа, связывая гем.
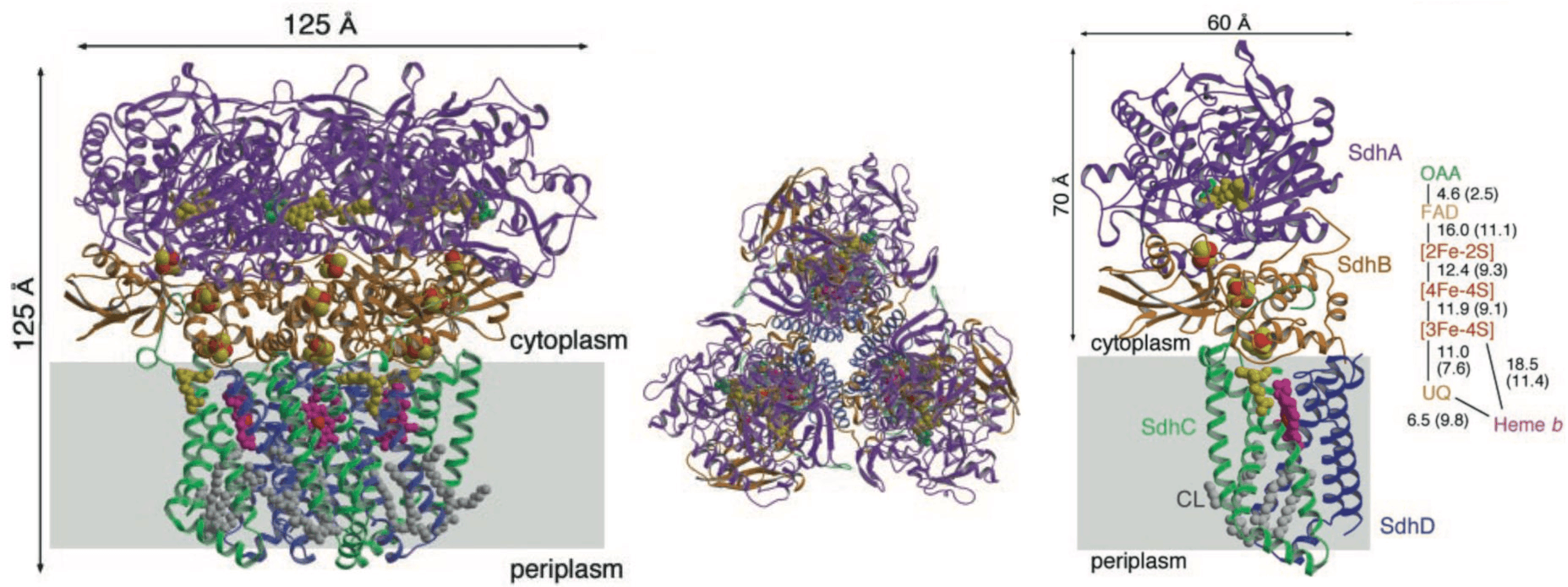
Рисунок 7. Структура сукцинат-дегидрогеназного комплекса с трех сторон. Субъединицы: SdhA, он же SDH 1(фиолетовый), SdhB(2) (оранжевый), SdhC(3) (зеленый), SdhD(4) (синий).Лиганды и субстраты: ФАД (FAD) — золотой, оксалоацетат — зеленый.Окислительно-восстановительные центры: Гем b и убихинон — пурпурный и желтый соответственно. Атомы железа (Fe) и серы (S) в Fe-S кластерах — красный и желтый.
Точное знание структуры и работы комплекса II — это чертеж для создания точечного молекулярного диверсанта. На сцену выходят «умные» ингибиторы.
Умный фунгицид. Почему яд может быть разборчивым
В основном, ингибиторы данного комплекса используются как фунгициды, ингибиторы роста грибов. Это не просто диверсанты, это молекулярные наемники, получившие конкретное задание: уничтожить патогенный гриб, например, серую гниль (Botrytis cinerea)
Они приходят в место связывания убихинонов, ингибируя тем самым транспорт электронов, что в дальнейшем останавливает весь процесс дыхания [12].
Молекулы современных фунгицидов, такие как флуопирам и боскалид, спроектированы как высокоточные инструменты для взлома. У этих «товарищей» есть, как и у других мимикряторов, фальшивая идентичность — общая пиридиновая и амидная группа (выделены оранжевым и голубым соответственно). Пиридиновое кольцо (с неподеленной электронной парой, обладающий основными свойствами) имитирует хиноновую «голову» убихинона, образуя решающую водородную связь N(пиридин)…H-N⁺ с протонированным гистидином в активном центре — точь-в-точь как это делает настоящий субстрат [12,14]. Карбоксамидная группа взаимодействует же с остатком аргинина в сайте связывания [13], [14].
Атомы хлора или фтора — это не просто украшение. Будучи электроноакцепторными, они выполняют две задачи:
-
Повышают липофильность, позволяя молекуле беспрепятственно проникать через восковую кутикулу растения и липидные мембраны гриба.
-
Обеспечивают устойчивость к смыванию дождем и окислению, продлевая время операции.
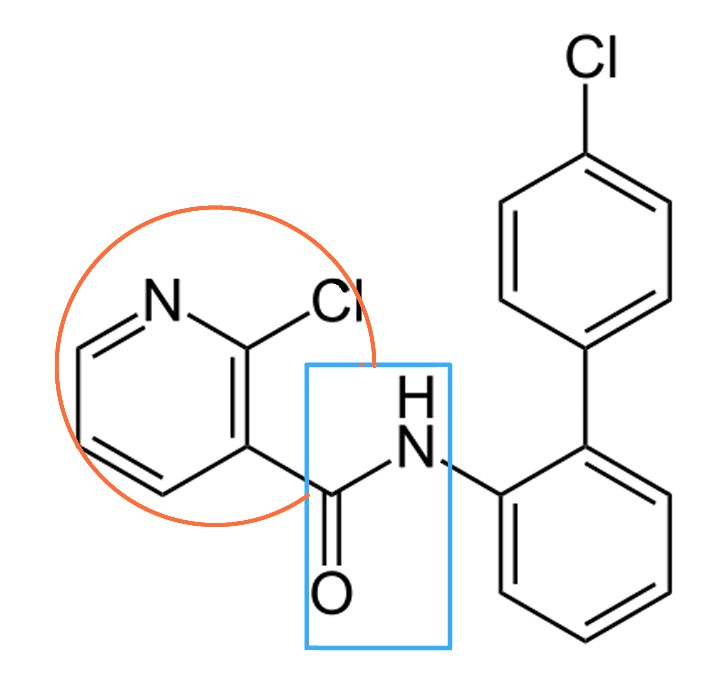
Рисунок 8. Структурная формула боскалида.
Субъединицы SDH1 и SDH2 довольно консервативны у многих эукариот, а вот другие две-нет, и вариабельность аминокислот различна внутри даже родственных групп, а мутации в других комплексах приводят к полнейшей резистентности к фунгицидам, особенно при замене гидрофобного гистидина на гидрофильный тирозин [14]. Криогенно-электронная микроскопия (крио-ЭМ) позволила выяснить, что у грибов (на примере S. cerevisiae) связывающий карман формируется крепко связанными друг с другом аминокислотами. Ключевую роль играет неподвижный триптофан (Trp-90) и окружающие его остатки, создающие узкий, конформационно ригидный карман. Молекула фунгицида, отлитая под эту уникальную форму, входит туда как идеальный ключ. В комплексе II млекопитающих (например, свиньи) на эквивалентной позиции находится подвижный триптофан (Trp-61). Эта гибкость — наша естественная защита. Когда молекула фунгицида пытается в него «встроиться», подвижный остаток может провернуть «незваного гостя», нарушив критическое позиционирование и сделав связывание неэффективным [15].
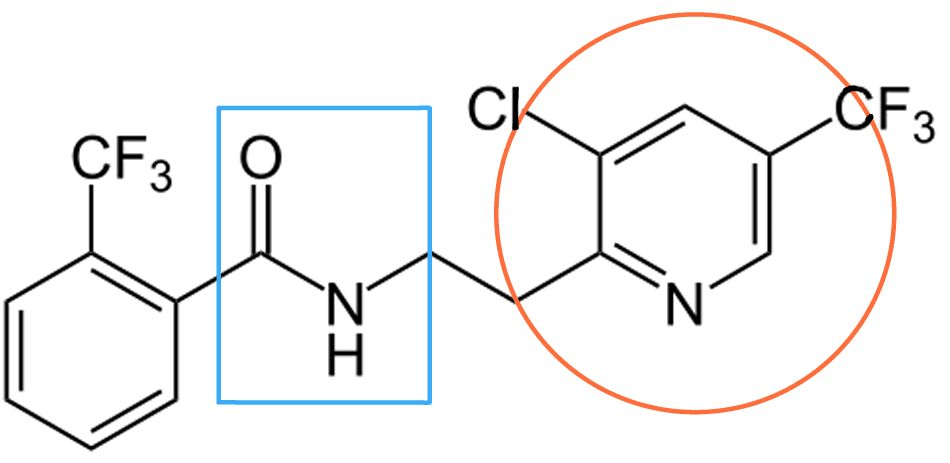
Рисунок 9. Структурная формула флуопирама.
Захватив место связывания убихинона, молекула-самозванец блокирует ключевой этап переноса электронов от сукцината. Это приводит к мгновенному параличу грибной дыхательной цепи и энергетическому коллапсу клетки.
Представим, что диверсантам не удалось сорвать прием электронов на старте (I) или в обходном пути (II). Электроны благополучно сели на убихинон, который превратился в убихинол. Теперь их цель — самый сложный и виртуозный узел всей цепи — комплекс III. Здесь происходит таинственный Q-цикл, и здесь же ждут самые коварные диверсанты, способные вскрыть эту сложнейшую механику.
Нудная и трудная работа комплекса III
Каждая из двух молекул QH₂, получившихся в комплексе I и II, отдает по два электрона: первый электрон по одному пути (через Fe-S-кластер белка Риске и цитохром c₁) передается через Q-out сайт на водорастворимый переносчик цитохром c, который уходит в межмембранное пространство. Мы разошлись, как в море корабли расходятся в тумане.
Второй электрон по другому пути передается на цитохромы bl и bh. После потери электронов каждая молекула QH₂, окисляясь до убихинона (Q), высвобождает по два протона (H⁺) в межмембранное пространство. Электроны, прошедшие через цитохромы b, используются для восстановления новой молекулы Q в сайте Q-in. Эта восстановленная молекула Q, забрав из матрикса два протона, вновь превращается в QH₂ и, как наказанный, возвращаетсв общий пул [16].
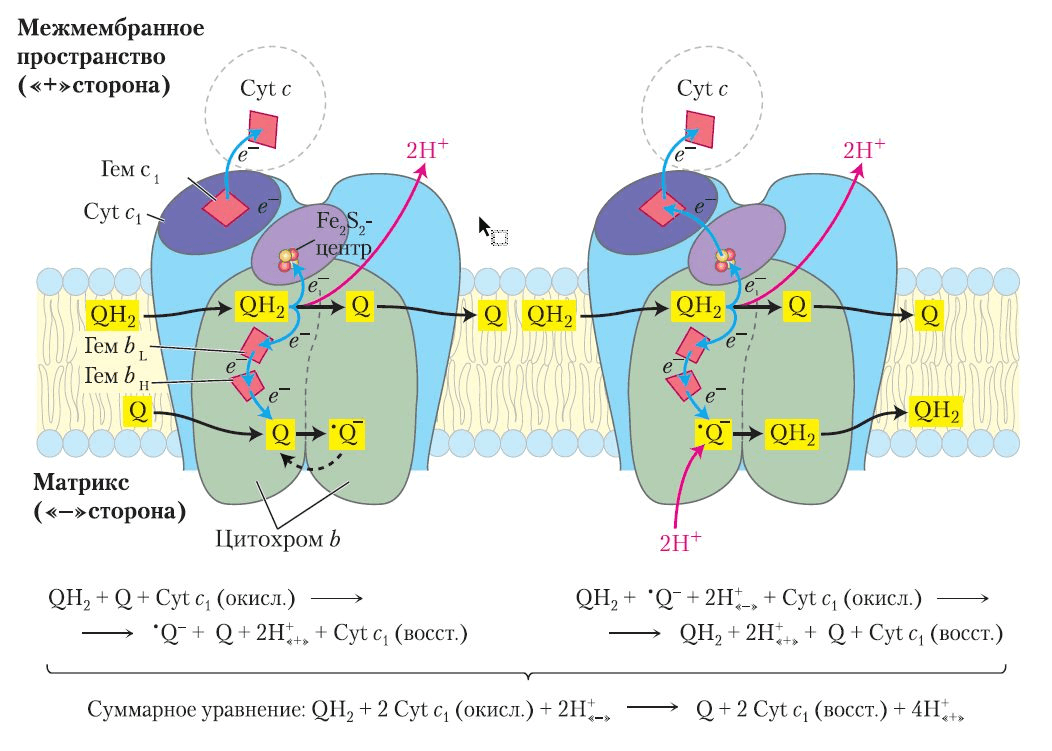
Рисунок 10. Cхема Q-цикла в 2 стадии. Направление движения электронов через комплекс III показано голубыми стрелками.
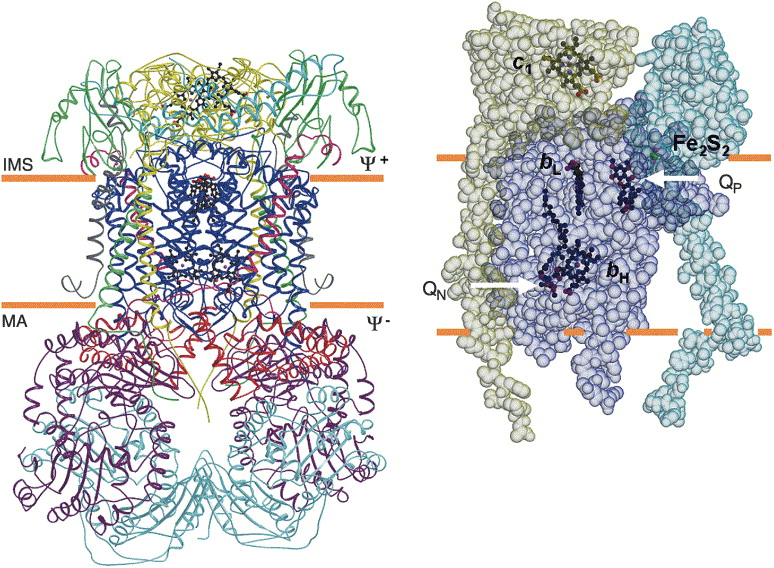
Рисунок 11. Структура цитохром bc1-комплекса. Показан гомодимер, в состав которого входят: каталитические субъединицы: цитохром b (синий), белок Риске (зеленый) и цитохром c1 (желтый) со своими кофакторами.
Ингибиторы комплекса III категорически против болезней
Ингибиторы комплекса III действуют как диверсанты, проникающие в самое сердце энергетического конвейера — Q-цикл. Их стратегия основана на захвате одного из двух критических пунктов: внутреннего (Q-in) или наружного (Q-out) сайта связывания убихинона. Каждая группа использует свою тактику молекулярного шпионажа.
Диверсант внутреннего периметра: антимицин А
Антимицин А проникает в Q-in сайт, предназначенный для окисленного убихинона (Q). Его успех обеспечивает формамидная группа (-NH-CHO) — уникальный пропуск, который образует две прочные водородные связи с остатком аспарагиновой кислоты. Этот аспартат в норме стабилизирует промежуточную форму убихинона, и антимицин, занимая его место, «обманывает» систему. Ароматическое ядро молекулы встраивается в плоскую щель сайта, создавая плотный π-стэкинг с ароматическими аминокислотами, в то время как ее алифатический «хвост» погружается в гидрофобный карман, укрепляя связь [19].
В дальнейшем, блокировка сайта приведет к тому, что гемы b останутся в окисленном состоянии, так как не смогут принять электроны, затормозится Q-цикл, прекратится перекачивание протонов и синтез АТФ, что может привести к смерти [20].
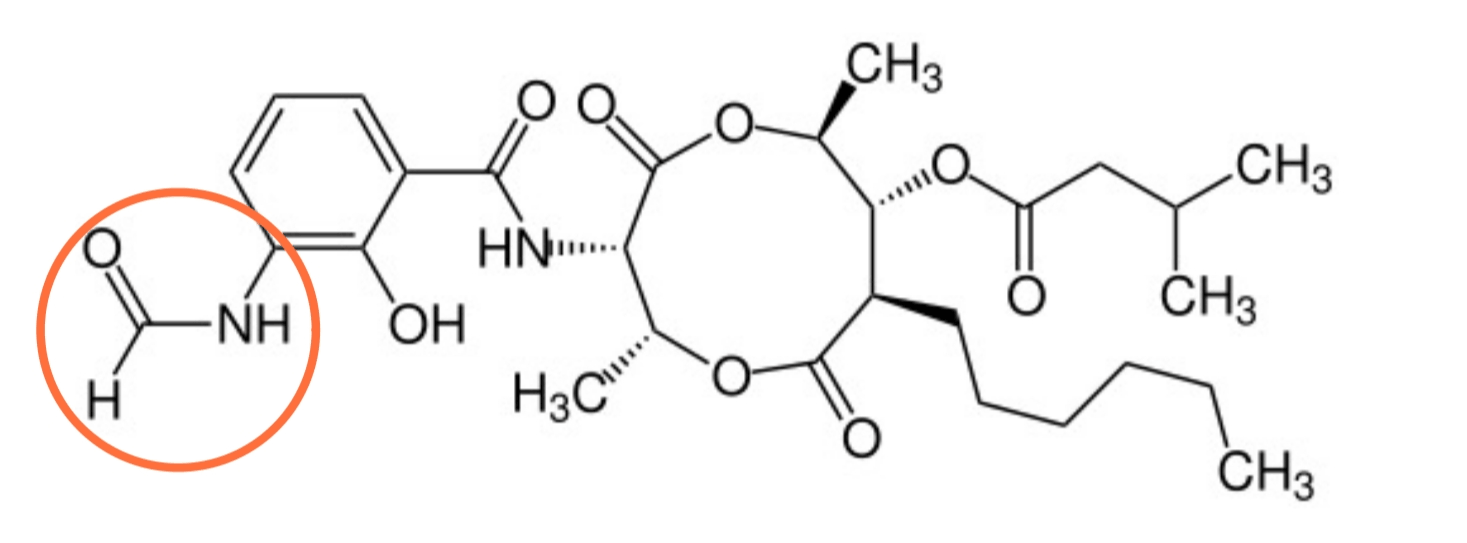
Рисунок 12. Структурная формула антимицина (формамидная группа выделена оранжевым на картинке).
Диверсанты внешнего рубежа: миксотиазол и атовакуон
Вторая группа агентов атакует Q-out сайт, через который убихинол (QH₂) отдает электроны. Антибиотик миксотиазол в арсенале имеет β-Метоксиакрилатную часть, содержащую карбонильную группу (C=O), которая образует водородную связь с остатком гистидина из подвижного домена белка Риске. Это связывание фиксирует критический элемент комплекса, не позволяя ему совершать рабочие движения для переноса электронов. Гидрофобная ароматическая часть при этом надежно заякоривает молекулу в кармане [17].
Комплекс III, высоко консервативен среди эукариот, поэтому такие агенты, как антимицин и миксотиазол, одни из самых опасных диверсантов, и практически не применяются в медицине — их диверсия неизбирательна и может вывести из строя энергосистему как патогена, так и клеток человека. Они применяются только в науке для детального изучения работы ЭТЦ, АФК, митохондриального стресса, а также для создания моделей заболеваний, связанных с митохондриальной дисфункцией (на этих моделях тестируют потенциальные терапевтические средства).
Близкую тактику, но с иным «пропуском», использует противомалярийный препарат атовакуон. Здесь ключевую роль играет нафтохиноновая «голова», которая идеально стыкуется с остатком тирозина-268 в комплексе III малярийного плазмодия. Тирозин создает идеальную стерическую и химическую среду для связывания. У человека на этой позиции находится фенилаланин, лишенный гидроксильной группы, что делает наш комплекс практически нечувствительным к препарату. Плазмодий, пытаясь противостоять атаке, может сменить «код доступа», заменяя тирозин на серин или аспарагин. Эти аминокислоты, хотя и несут гидроксильные группы, располагают их иначе и имеют меньший размер, что нарушает точную подгонку и снижает эффективность связывания яда — классический путь к резистентности[21].
Последствия от блокировки ровно такие же, как и при блокировке Q-in-сайта [22].
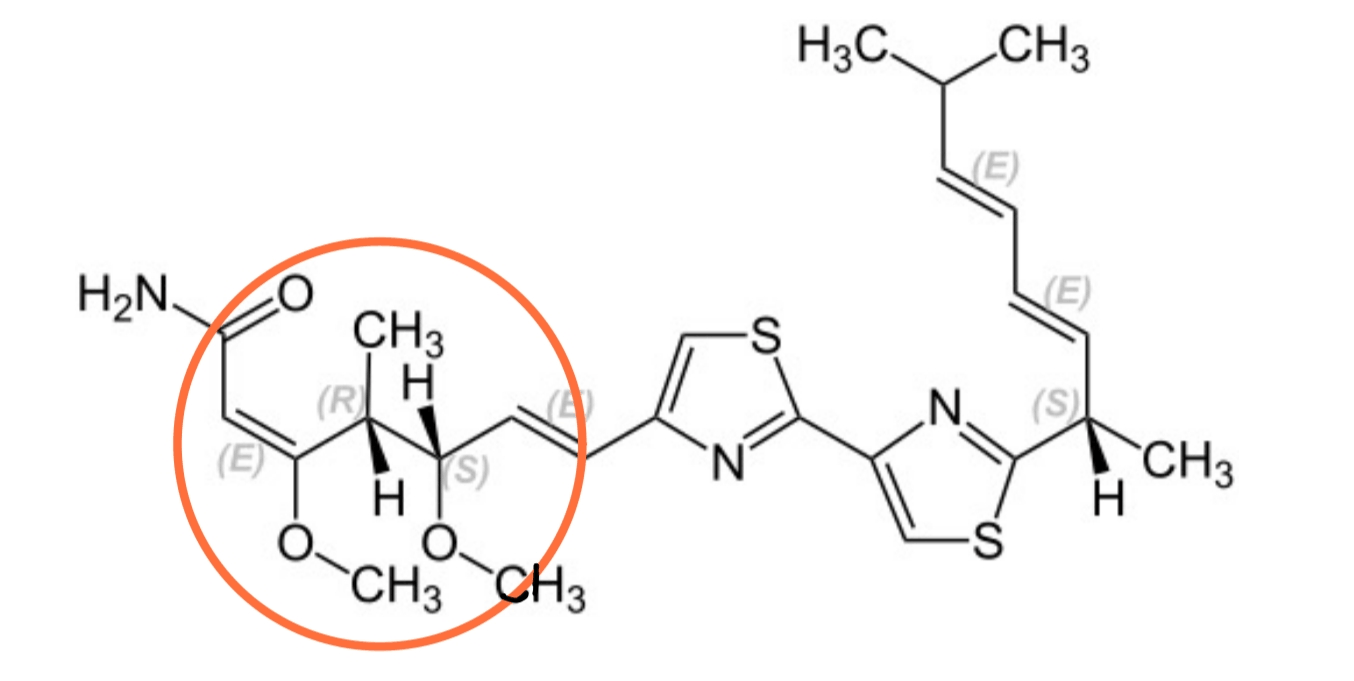
Рисунок 13. Структурная формула миксотиазола (метоксиакрилатная часть выделена оранжевым на картинке).
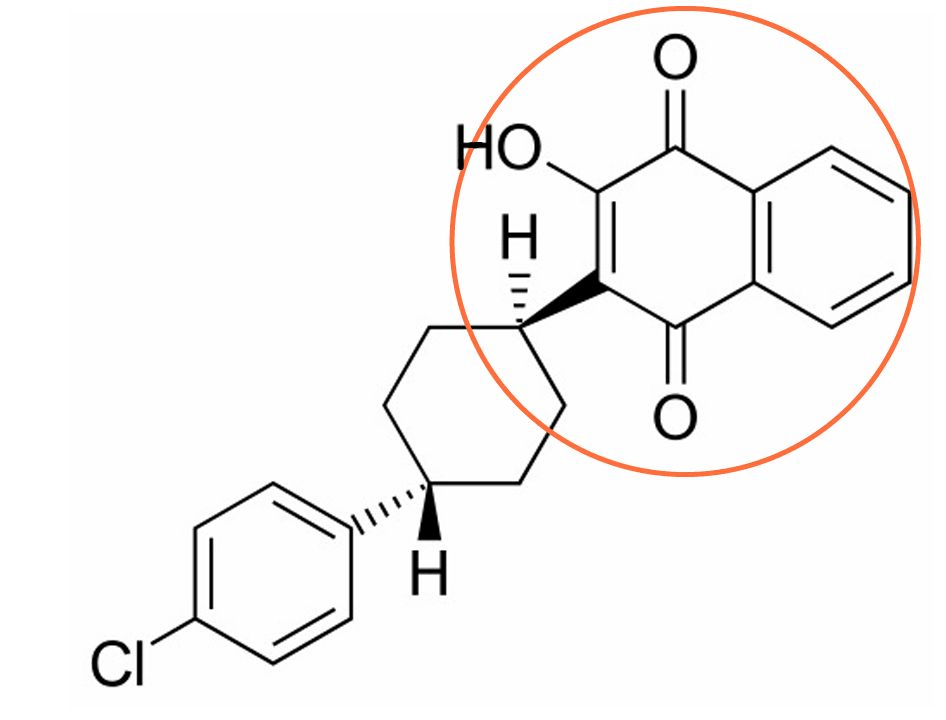
Рисунок 14. Структурная формула атовакуона (нафтохиноновая часть выделена оранжевым на картинке).
«Википедия», доработана автором статьи
Если электрону удалось прорваться, его ждет финальный и самый опасный участок пути. Прямо перед финишем, там, где энергия электрона должна вот-вот превратиться в АТФ, подстерегает самый известный и беспощадный киллер в истории отравлений. Добро пожаловать в комплекс IV — место, где дыхание встречается со смертью, а кислород превращается в воду… или становится орудием убийства.
Цитохром с оксидаза или комплекс IV
Наш заблудший электрон (а точнее два электрона), присев на корабль в виде цитохрома с, плывет к цитохром-с-оксидазе. Путь электрона начинается с торжественной встречи: два электрона от двух молекул цитохрома c поступают на двухъядерный медный центр CuA. Отсюда начинается их финальный спринт. По цепочке гем a они устремляются к самому сердцу комплекса — биядерному Fe-Cu-центру, где их ждет гем a₃ в компании иона меди CuB.
И здесь происходит главное — молекула кислорода (O₂), которую мы когда-то вдохнули, прочно связывается с гемом a₃. Первые два поступивших электрона превращают ее в промежуточный супероксид-радикал (O₂²⁻). Следующая пара электронов, доставленная новыми курьерами-цитохромами, совершает финальное превращение. Четыре электрона в сумме, забрав с собой четыре протона (H⁺) из матрикса (механизм их точной доставки до конца не разгадан), превращают нестабильный радикал в две безобидные молекулы воды (H₂O).
Ну, и в конечном итоге все сводится к выработке АТФ АТФ-синтазой за счет протонов из межмембранного пространства [23].
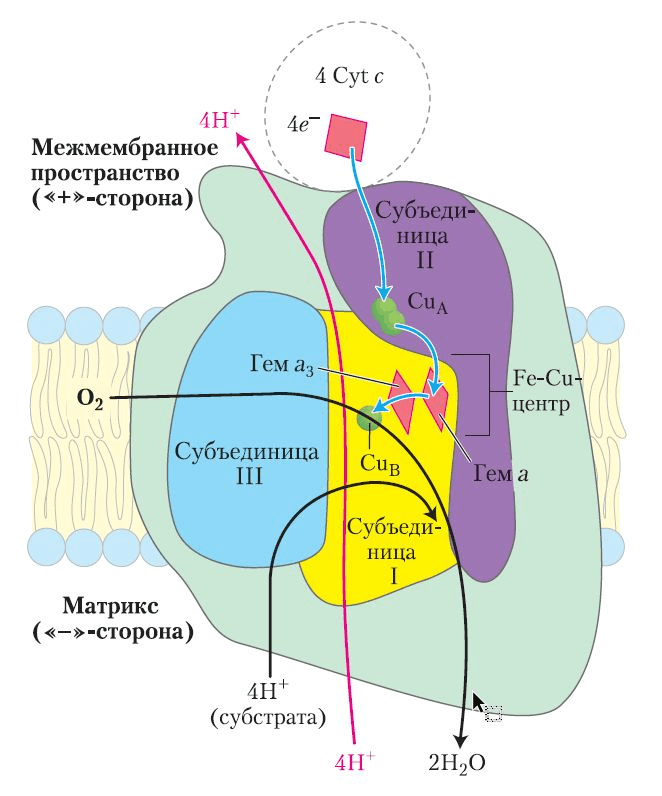
Рисунок 15. Схематичное строение комплекса IV.
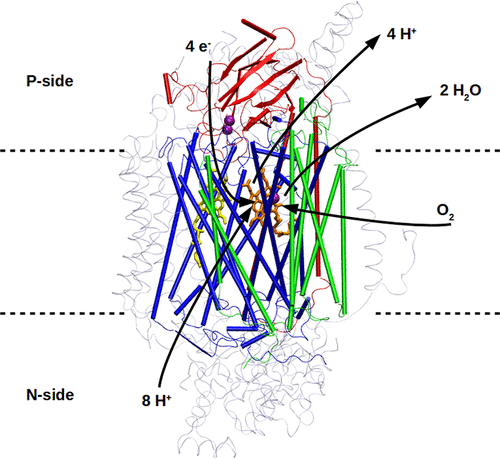
Рисунок 16. Структура цитохром c-оксидазы: каталитические субъединицы I, II и III — синий, красный и зеленый. Активные центры: гем а (желтый), гем а3 (оранжевый) и атомы меди (фиолетовый). Стрелками показано движение электронов, протонов и кислорода. Пунктирные линии обозначают границы липидного бислоя. N-side: матрикс, P-side: межмембранное пространство
Итак, электроны достигли конечной станции — комплекса IV. Если более ранние ингибиторы останавливали их в пути, то следующее вещество (и его производное) бьет точно в цель, навсегда блокируя место встречи электронов с кислородом. Таким убийцей стал компонент пестицида, который по злой иронии попал не в те руки…
Циклон Б или почему немцы так любили абрикосы
«Циклон Б» — это торговая марка препарата-пестицида на основе синильной (цианистоводородной) кислоты (HCN). Эта кислота один из самых известных и быстродействующих ядов в мире, имеющий одновременно промышленное значение и печальную историю, до которой мы обязательно доберемся). У кислоты есть важная улика следствия — ион CN⁻.
Ион CN⁻ обладает исключительным сродством к трехвалентному железу (Fe³⁺) в геме a₃ цитохром-с-оксидазы (комплекс IV). Он прочно связывается с этим атомом железа, входящим в состав биядерного центра a₃/CuB — конечной станции всей дыхательной цепи, где кислород должен превращаться в воду. Заняв это место, ион создает непроходимую блокаду. Электронам больше некуда идти, вся электрон-транспортная цепь замирает, как парализованная. Синтез АТФ прекращается мгновенно. Организм, при всем обилии кислорода в легких, задыхается на клеточном уровне.
Примечательно, что помимо синильной кислоты и ее солей, H2S, CO и NO ингибируют цитохром с-оксидазу, связываясь с комплексом гем a3/CuB. При этом CN⁻ может быть вытеснен NO [25]. Однако взаимодействие зависит от концентрации, поскольку при низких уровнях NO может даже усиливать ингибирование CN⁻-соединений.
Теперь поговорим о той самой печальной истории…
Изначально «циклон Б» разрабатывался для борьбы с вредителями и выпускался в виде пористых гипсовых гранул, что обеспечивало огромную площадь поверхности для испарения. Эти гранулы пропитывались смесью синильной кислоты и слезоточивого газа — бром- или хлорацетона. Последний добавлялся для создания резкого предупреждающего запаха, так как чистая синильная кислота обладает еле уловимым запахом горького миндаля. Однако при контакте с воздухом жидкая кислота активно испаряется, превращаясь в высокотоксичный газ, что и усиливало эффективность препарата. Отравляющее действие проявлялось как при вдыхании этих паров, так и при попадании самого раствора на кожу.

Рисунок 17. Пестицид «циклон Б» в промышленной упаковке.
Но к сожалению, «циклон Б» недолго пробыл только пестицидом. «Изобретательный» Вермахт с 1941 года начал использовать его как отравляющее вещество в концлагерях. По оценкам экспертов, от этого яда умерло свыше 1,1 миллионов человек!
Вообще сама синильная кислота содержится в абрикосовых косточках, но в очень малой дозе, чтобы отравиться данными косточками нужно съесть порядка 200 штук [26]!
Но более известным ядом является соль этой кислоты…
Дыхание смерти. Почему цианид — это клише, которое работает, и почему отравителям стоит хотя бы иногда читать учебник по химии
«Да. Не могу сказать, что именно. Скорее всего, один из цианидов. Но без характерного запаха синильной кислоты - значит, скорее, цианид калия. Действует мгновенно…»— именно к такому заключению приходит доктор Армстронг, персонаж известного произведения «Десять негритят», когда умирает самый первый «негритенок» Энтони Марстон, выпив отравленный алкогольный напиток [27].
Казалось бы, ну да, ведь и вправду цианистый калий очень ядовит. Но есть одно но…
Цианистый калий очень реакционноспособное вещество. Формула его довольна простая — KCN. И тут встречается наш знакомый ион CN⁻, потому что цианиды — соли синильной кислоты. Это соединение может реагировать с очень многими веществами, включая сахар и алкоголь (то есть, выпив растворенный цианид, Марстон с некой долей вероятности мог бы и выжить). Сахар при этом является антидотом. Он связывает цианид в малотоксичный циангидрин. В истории отравления Распутина, ему подавали пирожные с кремом на основе цианистого калия. Получается, ему дали яд с предполагаемым антидотом (мы не знаем достоверное количество веществ, поэтому мы можем только предположить), и после все так удивлялись, почему же его не взял яд [28].
Поскольку синильная кислота слабее угольной (H2O+СО2), все цианиды легко разрушаются углекислым газом (СО2), содержащимся в воздухе, с образованием цианистоводородной кислоты. Хранить этот яд нужно в герметичной таре, без доступа влаги и CO2 иначе диверсант нейтрализуется еще до начала операции.
Детективный штамп о «мгновенном и безотказном» цианиде — это упрощение, не учитывающее его химической нестабильности [26].
Итак, мы прошли весь путь электрона — от первых ворот до финишной черты — и видели, как на каждом этапе его движение могут прервать агенты с разными методами, но одной целью. Картина проясняется. Разрозненные улики — литературные, исторические, сельскохозяйственные — складываются в единое обвинительное заключение против целого класса молекулярных диверсантов
Ключевой вывод таков, что нарушить тонко сбалансированный процесс жизни можно не только грубой силой, но и обманом — создав молекулу, достаточно похожую на ключевую деталь системы, чтобы занять ее место и парализовать работу.
Мы начали наше расследование с загадок Агаты Кристи и закончили его на месте преступления производства энергии. Оказалось, что разгадка самых изощренных литературных и исторических преступлений кроется в тонких молекулярных взаимодействиях, которые ежесекундно поддерживают в нас жизнь.
Так что в следующий раз, читая детективы или разгадывая историческую загадку отравления Распутина, помните — за драматическим сюжетом скрывается глубинная биохимическая драма. Понимание этого плана — ключ не только к раскрытию прошлых дел, но и к созданию инструментов для спасения жизней в будущем. А «циклон Б» — всего лишь печальное свидетельство того, как открытия могут обернуться своей темной стороной.
Дело закрыто.
Это вам краткое досье на всех диверсантов и фигурантов дела.
|
«Диверсант» |
Комплекс |
Метод и место «диверсии» |
Результат |
|
Ротенон |
I |
Молекулярная мимикрия и конкурентное ингибирование. Связывается с Q-сайтом (сайтом убихинона). Ароматическая часть имитирует хиноновое кольцо, карбонильные группы образуют водородные связи, гидрофобный «хвост» занимает соответствующий карман. |
Блокирует перенос электронов от комплекса I к убихинону. Остановка ЭТЦ, прекращение синтеза АТФ, энергетический коллапс клетки |
|
Боскалид, Флуопирам |
II |
Молекулярная мимикрия: связываются в Q-сайте комплекса II. Пиридиновая группа имитирует убихиноновое кольцо, карбоксиамидная группа взаимодействует с аргинином. |
Блокируют перенос электронов от сукцината на убихинон. Остановка этого пути дыхания, прекращение синтеза АТФ. Высокая специфичность к грибному комплексу II. |
|
Антимицин А |
III |
Связывание в Q-in; Критически важная формамидная группа образует водородные связи с аспартатом. |
Блокировка транспорта электронов от гема bH к окисленному убихинону (Q).Прекращает работу Q-цикла, перекачку протонов и синтез АТФ. |
|
Миксотиазол, атовакуон |
III |
Связывание с Q-out-сайтом, β-Метоксиакрилатная (миксотиазол) или нафтохиноновая (атовакуон) части взаимодействуют с белком Риске или тирозином. |
Блокировка окисление убихинола, прерывая Q-цикл. Останавливают перенос электронов на цитохром c,, перекачку протонов и синтез АТФ. Атовакуон специфичен для плазмодия. |
|
Синильная кислота, цианистый калий |
IV |
Необратимое ингибирование. Ион CN⁻ прочно связывается с трехвалентным железом (Fe³⁺) в геме a₃ биядерного центра a₃/CuB. |
Блокирует конечный этап переноса электронов на кислород. Кислород не восстанавливается до воды, вся цепь останавливается, синтез АТФ прекращается. Мгновенное удушение на клеточном уровне. |
Литература
- Тайная жизнь митохондрий;
- Джонсон А., Альбертс Б., Хопкин К. Основы молекулярной биологии клетки. 3-е изд. М.: БИНОМ. Лаборатория знаний, 2023. — 796 с.;
- Попов В.Н., Ругге Э.К., Старков А.А. (2003). Влияние ингибиторов электронного транспорта на образование активных форм. Биохимия 68, 910–916;
- Nelson D.L., Cox M.M. Lehninger Principles of Biochemistry: 6th Edition NY: Macmillan Learning, 2012. — 1198 p.;
- Jiapeng Zhu, Kutti R. Vinothkumar, Judy Hirst. (2016). Structure of mammalian respiratory complex I. Nature. 536, 354-358;
- Tomohide Uno, Mayumi Ishizuka, Takao Itakura. (2012). Cytochrome P450 (CYP) in fish. Environmental Toxicology and Pharmacology. 34, 1-13;
- James A. Dykens, Yvonne Will. (2007). The significance of mitochondrial toxicity testing in drug development. Drug Discovery Today. 12, 777-785;
- Eric Fontaine. (2018). Metformin-Induced Mitochondrial Complex I Inhibition: Facts, Uncertainties, and Consequences. Front. Endocrinol.. 9;
- Prakorn Chudapongse, Withaya Janthasoot. (1981). Mechanism of the inhibitory action of capsaicin on energy metabolism by rat liver mitochondria. Biochemical Pharmacology. 30, 735-740;
- Shaobai Huang, A Harvey Millar. (2013). Succinate dehydrogenase: the complex roles of a simple enzyme. Current Opinion in Plant Biology. 16, 344-349;
- Victoria Yankovskaya, Rob Horsefield, Susanna Törnroth, César Luna-Chavez, Hideto Miyoshi, et. al.. (2003). Architecture of Succinate Dehydrogenase and Reactive Oxygen Species Generation. Science. 299, 700-704;
- Rob Horsefield, Victoria Yankovskaya, Graham Sexton, William Whittingham, Kazuro Shiomi, et. al.. (2006). Structural and Computational Analysis of the Quinone-binding Site of Complex II (Succinate-Ubiquinone Oxidoreductase). Journal of Biological Chemistry. 281, 7309-7316;
- Li-shar Huang, Gang Sun, David Cobessi, Andy C. Wang, John T. Shen, et. al.. (2006). 3-Nitropropionic Acid Is a Suicide Inhibitor of Mitochondrial Respiration That, upon Oxidation by Complex II, Forms a Covalent Adduct with a Catalytic Base Arginine in the Active Site of the Enzyme. Journal of Biological Chemistry. 281, 5965-5972;
- Scalliet G., Boehler M., Bowler J., Green P.S., Kilby P.M. and Fonné-Pfister R. (2010). SDHIs and the Fungal Succinate Dehydrogenase. Modern Fungicides and Antifungal Compounds VI. 16th International Reinhardsbrunn Symposium April 25 – 29, 2010 Friedrichroda, Germany. 171–179;
- Zhi-Wen Li, Yuan-Hui Huang, Ge Wei, Zong-Wei Lu, Yu-Xia Wang, et. al.. (2025). Cryo-EM structure of the yeast Saccharomyces cerevisiae SDH provides a template for eco-friendly fungicide discovery. Nat Commun. 16;
- Нельсон Д. Основы биохимии Ленинджера // учебное изд. в 3 т. / Нельсон Д., Кокс М. пер. с англ. Мосоловой Т.П., Ефременкова О.В. под ред. Богданова А.А., Кочеткова С.Н. М.: БИНОМ. Лаборатория знаний, 2012 Т.2: Биоэнергетика и метаболизм. — Изд. 2-е, испр. — 2015. — 636 с.;
- FLORENZ SASSE, BETTINA BÖHLENDORF, MARTINA HERMANN, BRIGITTE KUNZE, EDGAR FORCHE, et. al.. (1999). Melithiazols, New .BETA.-Methoxyacrylate Inhibitors of the Respiratory Chain Isolated from Myxobacteria. Production, Isolation, Physico-chemical and Biological Properties.. J. Antibiot.. 52, 721-729;
- Carola Hunte, Hildur Palsdottir, Bernard L Trumpower. (2003). Protonmotive pathways and mechanisms in the cytochrome bc1 complex. FEBS Letters. 545, 39-46;
- E.C. Slater. (1973). The mechanism of action of the respiratory inhibitor, antimycin. Biochimica et Biophysica Acta (BBA) - Reviews on Bioenergetics. 301, 129-154;
- Nobuya Tokutake, Hideto Miyoshi, Takashi Satoh, Taku Hatano, Hajime Iwamura. (1994). Structural factors of antimycin A molecule required for inhibitory action. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1185, 271-278;
- Michael Korsinczky, Nanhua Chen, Barbara Kotecka, Allan Saul, Karl Rieckmann, Qin Cheng. (2000). Mutations in Plasmodium falciparum Cytochrome b That Are Associated with Atovaquone Resistance Are Located at a Putative Drug-Binding Site. Antimicrob Agents Chemother. 44, 2100-2108;
- G. von Jagow, Th.A. Link. (1986). [24] Use of specific inhibitors on the mitochondrial bc1 complex. Methods in Enzymology. 253-271;
- Shane A. Watson, Gavin P. McStay. (2020). Functions of Cytochrome c Oxidase Assembly Factors. IJMS. 21, 7254;
- Mårten Wikström, Klaas Krab, Vivek Sharma. (2018). Oxygen Activation and Energy Conservation by Cytochrome c Oxidase. Chem. Rev.. 118, 2469-2490;
- Joanna Izabela Lachowicz, Jan Alexander, Jan O. Aaseth. (2024). Cyanide and Cyanogenic Compounds—Toxicity, Molecular Targets, and Therapeutic Agents. Biomolecules. 14, 1420;
- Как отравить героя. Chemnet;
- Кристи А. Десять негритят. СПб: Антология, 2023. — 192 с.;
- Привалов К. Яды: полная история. От мышьяка до «Новичка» М.: АСТ, 2023. — 432 с..
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚






