
Борьба мозга с нейроинтерфейсами. Что мешает нам попасть в киберпанк?
24 марта 2026
Борьба мозга с нейроинтерфейсами. Что мешает нам попасть в киберпанк?
- 233
- 0
- 0
Рисунок в полном размере.
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Слияние мозга с компьютером — заветная мечта футурологов и центральный образ киберпанка. Но на пути к ней стоит не технический, а биологический барьер: наш собственный мозг. Он воспринимает имплантаты как угрозу и изолирует их непроницаемым рубцом из глиальных клеток, обрекая интерфейсы на короткую жизнь. В этом обзоре мы покажем, что прорыв возможен только на острие нейробиологии, материаловедения и биоинженерии. Будущее — за «невидимыми» ультрамягкими имплантатами, щадящей хирургией и точечным контролем воспаления. Победим ли мы в этой войне с иммунитетом? От ответа зависит не только медицина будущего, но и сама возможность превратить человека в киборга.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
На протяжении десятилетий мечта о прямом общении между мозгом и машиной казалась сюжетом научной фантастики. Первые шаги в этой области были сделаны еще в конце 1990-х — начале 2000-х годов, когда исследователи продемонстрировали, что сигналы мозга, регистрируемые имплантированными электродами, можно декодировать для управления внешними устройствами [1]. Первые эксперименты, часто проводившиеся на лабораторных животных (мышах, крысах, кроликах, шимпанзе, обезьяны Нового Света), заложили фундамент для создания нейроинтерфейсов — технологии, которая создает прямой канал связи между мозгом и внешним миром, минуя традиционные пути через периферические нервы и мышцы. Особый прорыв был связан с разработкой инвазивных интерфейсов, где микрочипы с электродами имплантируются непосредственно в мозговую ткань, что позволяет считывать сигналы нейронов с беспрецедентной точностью (до 95% правильной декодировки мысленных команд) и разрешением (одновременная запись с более чем 1000 отдельных нервных клеток) [1], [2].
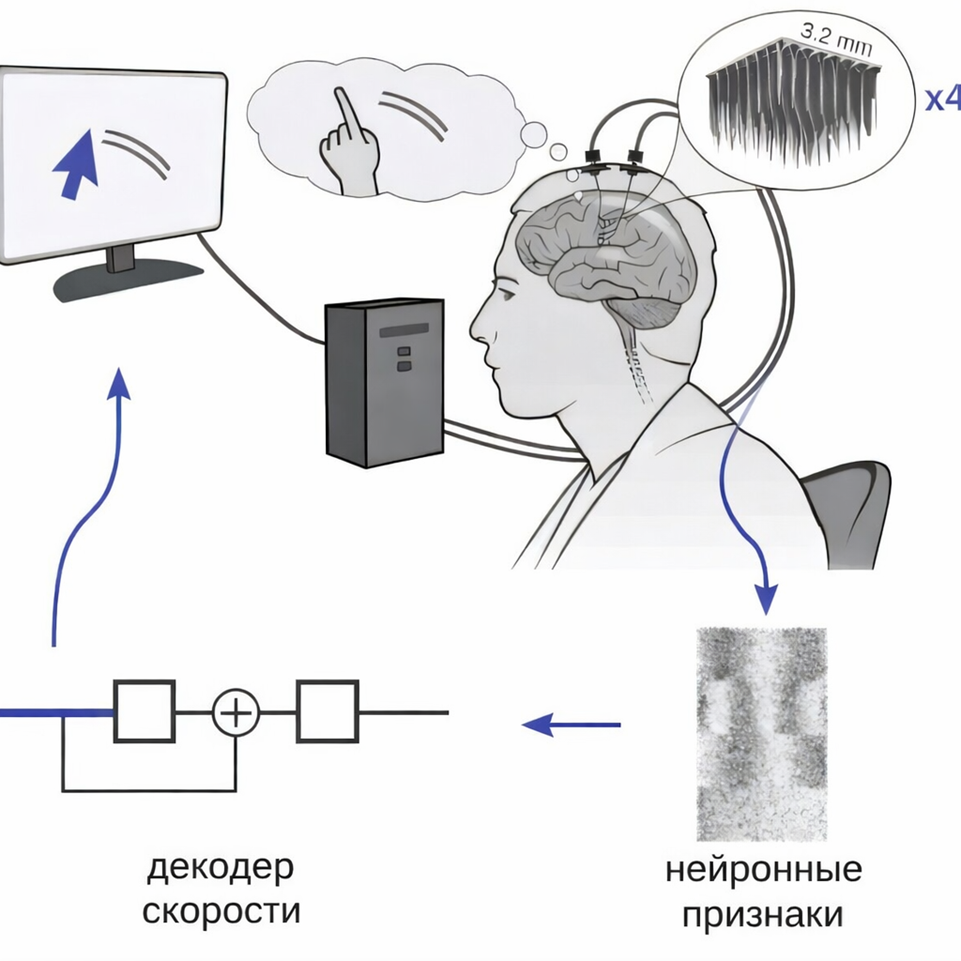
Рисунок 1. Управление курсором силой мысли. Для этого эксперимента в область мозга, отвечающую за движение руки, были имплантированы четыре микрочипа с 64 электродами каждый. Эти миниатюрные сенсоры с высочайшей точностью улавливали импульсы множества нейронов. Специальная компьютерная программа в режиме реального времени расшифровывала эту «беседу» нервных клеток и преобразовывала ее в команды для курсора на экране, позволяя участнику эксперимента перемещать его практически так же, как мысленной рукой.
Сегодня инвазивные нейроинтерфейсы переживают период бурного развития, открывая революционные перспективы, прежде всего в медицине. Например, они уже позволяют парализованным людям управлять роботизированными манипуляторами или даже курсором на экране силой мысли (рис. 1), возвращая им возможность взаимодействовать с окружающим миром [1], [3], [4].
Однако важность этой технологии выходит далеко за рамки восстановления утраченных функций. Современные исследования направлены на преодоление ключевых препятствий, таких как создание полностью имплантируемых биосовместимых устройств.
Но что же мешает хронической имплантации? Исторически применению препятствовала постоянная и серьезная проблема: прогрессирующее снижение качества сигнала и функциональных характеристик в течение нескольких месяцев или лет [5]. Окончательный отказ многих нейронных имплантатов часто является результатом не электронного сбоя (такие как деградация электродов и/или коррозия металлов) [6], а биологического явления — реакции мозговой ткани на инородное тело (foreign body reaction — FBR) на имплантированное устройство [7].
С реакции мозговой ткани начинается каскад воспалений и фиброза, что приводит к образованию плотного глиально-фиброзного рубца, который окружает имплантат [8]. Основные клетки, участвующие в этом процессе — глиальные клетки головного мозга, а именно: микроглия, которая представляет собой резидентные (т.е. постоянно живущие в ткани мозга) макрофаги и астроциты — самые многочисленные клетки глии, выполняющие разнообразные функции (питание, опора, регуляция числа нейромедиаторов в синаптической щели и др.). При повреждении и введении имплантата микроглия активируется и мигрирует к месту имплантации, выделяя провоспалительные цитокины [9]. Это запускает активацию и деление астроцитов, которые претерпевают переход в реактивное состояние, усиливая регуляцию глиального фибриллярного кислого белка (GFAP) (рис. 2) и образуя физический изолирующий барьер между электродами и тканью мозга [5], [8]. Одновременно происходящее разрушение гематоэнцефалического барьера (ГЭБ) позволяет проникать системным (то есть из общего кровотока) иммунным клеткам и фибробластам, что дополнительно способствует отложению богатого коллагеном фиброзного внеклеточного матрикса [10].
Главной причиной этой реакции является механическое несоответствие между жесткими материалами, из которых создают имплантаты (например, кремнием, иридием, вольфрамом) и мягкой желеобразной тканью головного мозга [11]. Модуль упругости (Юнга) нервной ткани в 1 000 000 раз меньше, чем у вышеупомянутых материалов. Это несоответствие в несколько порядков означает, что даже незначительные микродвижения, вызываемые дыханием или пульсацией сердечно-сосудистой системы, постоянно раздражают окружающие ткани, закрепляя состояние хронического воспаления и приводя к образованию рубцов [12]. Как следствие, глиальный рубец действует как изолирующий слой, увеличивая сопротивление электрода и физически отталкивая нейроны от мест записи, что приводит к катастрофическому снижению отношения сигнал/шум и функциональной изоляции имплантата [7].
Таким образом, «борьба мозга с нейроинтерфейсами» — это отторжение мозгом чужеродных структур. Преодоление барьера в виде «рубца» имеет первостепенное значение. Это проблема, требующая комплексного подхода в виде поиска биоматериалов и инженерных решений для повышения биосовместимости.
Ответ головного мозга
Для понимания процессов отторжения имплантатов необходимо разобраться в системах распознавания чужого в мозге и в том, какие клетки за это отвечают.
Науке давно известно, что клетки глии являются главными питающими, опорными клетками нейрональной ткани. Несмотря на свое название (γλοιός — клей), они выполняют многие другие функции, глиальные клетки являются одними из ключевых участников формирования «рубца» [13].
Острая фаза
Имплантация любого устройства неминуемо повреждает гематоэнцефалический барьер (ГЭБ) [14]. Это открывает ворота для белков крови, таких как альбумин и фибронектин, которые запускают воспалительную реакцию в клетках глии — микроглии и астроцитах. В зоне травмы начинается гибель нейронов и других клеток (астроцитов, олигодендроцитов). Содержимое погибших клеток — АТФ, ДНК, белки теплового шока (HSP) — высвобождается в межклеточное пространство. Для иммунной системы это сигнал тревоги: такие молекулы называются DAMP (Damage-Associated Molecular Patterns, или «ассоциированные с повреждением молекулярные паттерны»). Микроглия, резидентные иммунные клетки мозга, мгновенно реагирует на этот хаос. Она повышает выработку специальных рецепторов — Toll-подобных рецепторов (TLR), которые улавливают сигналы опасности (рис. 2).
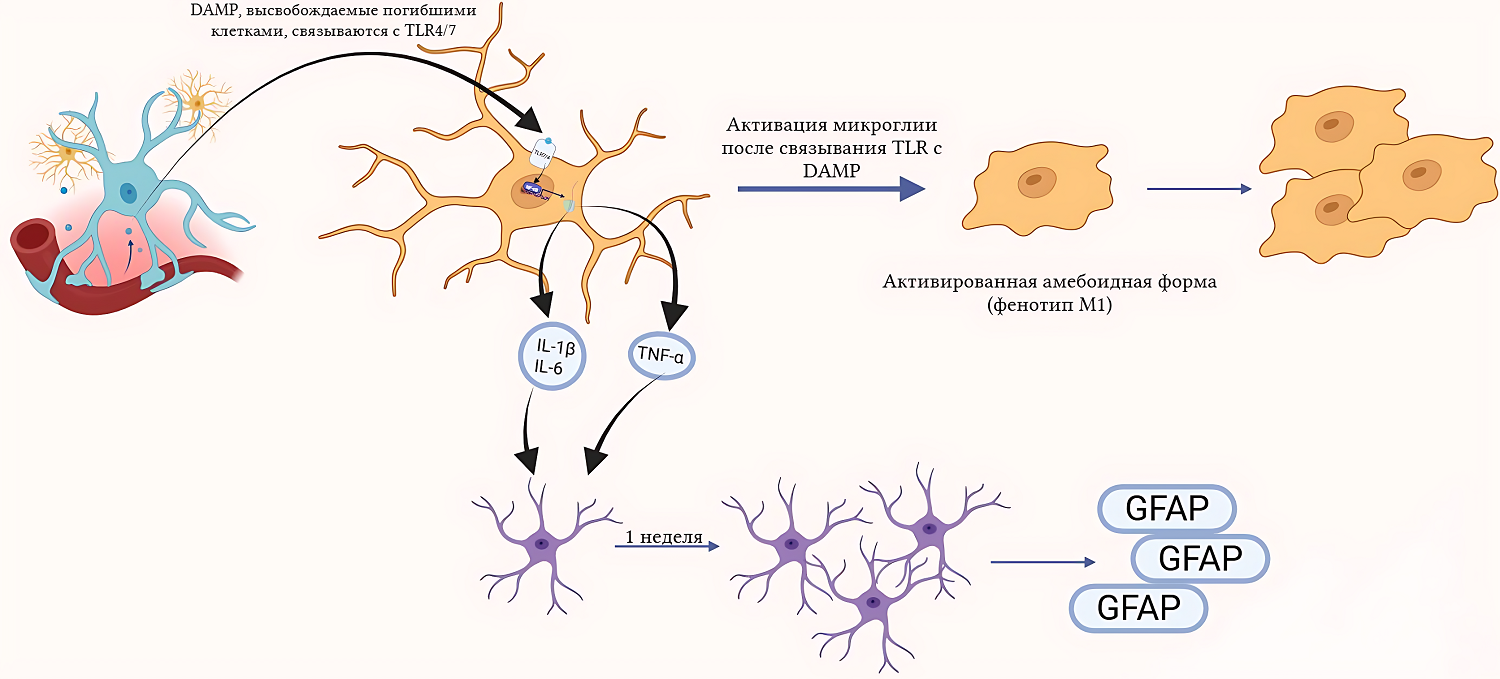
Рисунок 2. Активация микроглии через DAMP: путь от Toll-подобных рецепторов к провоспалительному фенотипу М1. Активация пролиферации астроцитов и синтеза GFAP в ответ на провоспалительные цитокины, выделяемые микроглией в ответ на DAMP.
создано авторами в Biorender
Давайте проследим за двумя ключевыми сигналами:
- Быстрый отклик на АТФ. Молекула АТФ, как хемоаттрактант, через пуринергические рецепторы (P2X4, P2X7) привлекает микроглию и астроциты к месту повреждения [15].
- Запуск воспалительного каскада. Связывание DAMP с рецепторами TLR запускает внутриклеточную цепь реакций. Она приводит к активации главного внутриклеточного «переключателя» воспаления — транскрипционного фактора NF-κB. Тот перемещается в ядро микроглии и включает гены, ответственные за производство провоспалительных цитокинов: фактора некроза опухоли-альфа (TNF-α), интерлейкинов-1β и −6 (IL-1β, IL-6) [16].
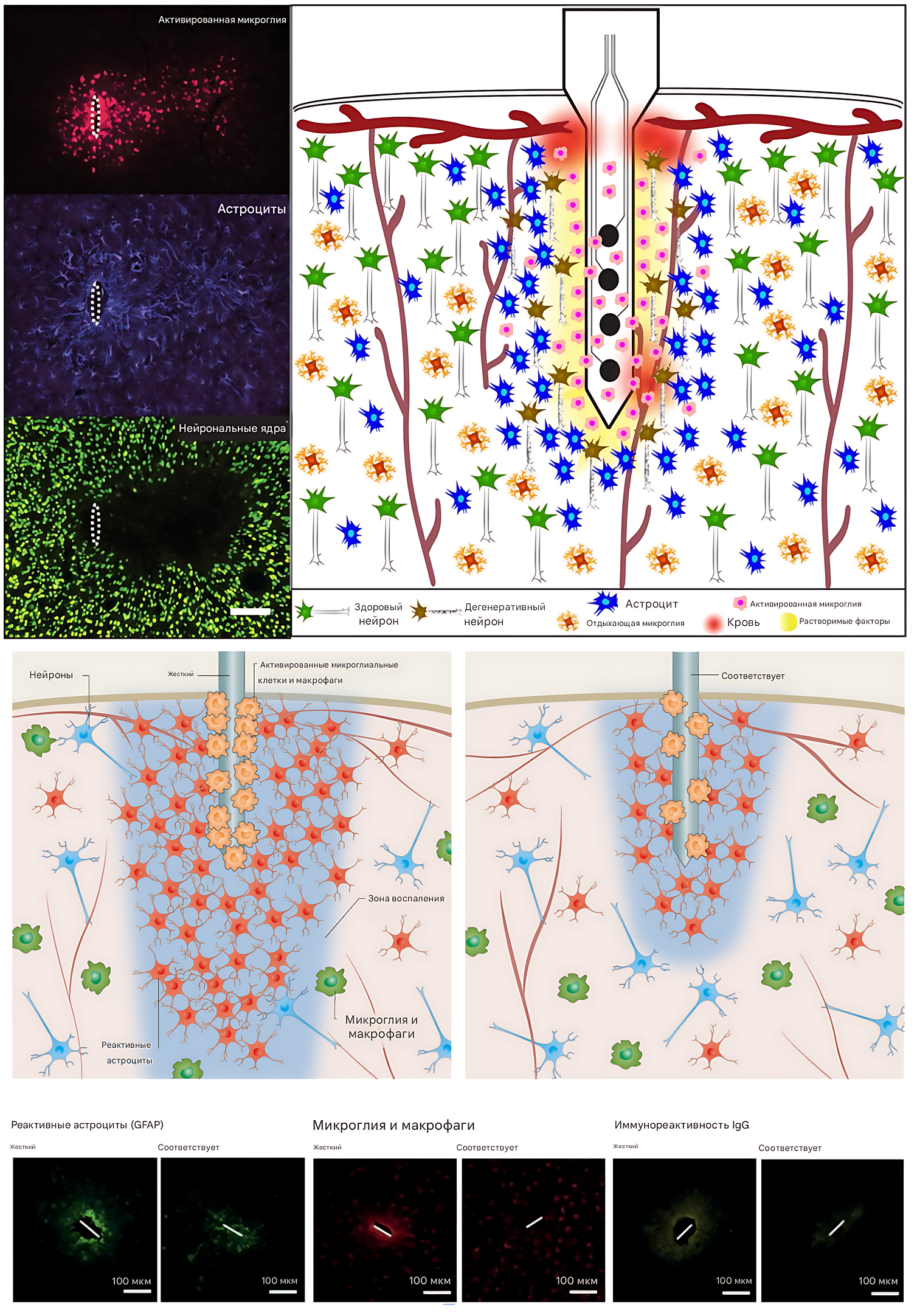
Рисунок 3. Имплантация электрода приводит к локальным провоспалительным клеточным и биохимическим реакциям. Вскоре после имплантации активированная микроглия начинает прикрепляться к поверхности электрода и локально высвобождать провоспалительные факторы. За адгезией глиальных клеток следует астроцитарная инкапсуляция по всей длине электрода (формирование глиального рубца). Было показано, что эти события, а также локальное кровоизлияние, коррелируют с нейродегенерацией в области контакта. Слева представлены репрезентативные ИГХ-изображения доминирующих типов клеток. Масштаб = 100 мкм.
Potter et al., 2012
Под действием этих сигналов клетки микроглии первыми переходят в наступление. Они меняют форму на амебоидную, становясь подвижными (фенотип М1) [17] (рис. 2), начинают быстро размножаться и мигрировать, образуя плотное кольцо вокруг имплантата (рис. 3).
Астроциты присоединяются к реакции примерно через неделю после повреждения, отвечая на цитокиновый «шторм» от микроглии [18]. Они увеличиваются в размерах, наращивают внутренний каркас из белков (например, из уже известного нам GFAP) [19] и активно делятся. Их задача — изолировать угрозу. В течение 4–6 недель астроциты формируют вокруг имплантата плотный глиальный рубец, который может сохраняться годами, создавая непроницаемый барьер между устройством и тканью мозга (рис. 3).
В ответ на выброс цитокинов микроглия начинает активно делиться и мигрирует к месту имплантации. Параллельно (или в ответ на те же сигналы) происходит быстрая пролиферация и активация местных астроцитов, которые также устремляются к имплантату [18].
Активные астроциты начинают массово производить белок коннексин-43 (Cx43) [20]. Он формирует щелевые контакты — своеобразные «тоннели», напрямую соединяющие соседние астроциты. Это создает обширную сеть, по которой ионы и небольшие сигнальные молекулы (включая те самые провоспалительные факторы) могут распространяться из клетки в клетку практически мгновенно. Таким образом, Cx43 не только укрепляет астроглиальный рубец, но и многократно ускоряет и расширяет зону воспалительного ответа [21].
Рассмотрим, как именно активированные клетки атакуют имплантат. Микроглия, перешедшая в провоспалительное состояние (фенотип М1), использует два основных оружия:
- Прямое поглощение (фагоцитоз). Клетки пытаются «съесть» и расчистить зону поражения, поглощая обломки погибших нейронов (клеточный детрит) и мельчайшие частицы материала самого электрода.
- Химическая атака. Микроглия генерирует реактивные формы кислорода (ROS, например, супероксид-анион) — агрессивные молекулы, которые вызывают окислительный стресс и повреждают как чужеродный материал, так и прилегающие клетки мозга [16].
Одновременно с этим микроглия ведет активную сигнальную работу: массово высвобождает провоспалительные цитокины (TNF-α, IL-1β, IL-6). Этот «цитокиновый шторм» выполняет три ключевые задачи:
- усиливает и поддерживает воспаление по принципу положительной обратной связи;
- повреждает гематоэнцефалический барьер (ГЭБ), увеличивая его проницаемость;
- подает сигнал тревоги в кровоток, привлекая к месту имплантации «тяжелую артиллерию» — иммунные клетки из периферической крови (макрофаги, лимфоциты).
Таким образом, единичное повреждение при имплантации запускает мощный и многоуровневый иммунный ответ, направленный на изоляцию и уничтожение угрозы.
Переход в хроническую фазу
Данная стадия обусловлена постоянным присутствием электрода как источника механического и химического раздражения.
Микроглия продолжает продуцировать провоспалительные цитокины. Некоторые исследования показывают, что хронически активированная микроглия может сливаться, образуя многоядерные гигантские клетки, пытающиеся изолировать крупный имплантат [22]. Но ключевую роль здесь играют астроциты, претерпевающие критический переход. Провоспалительные цитокины, выделяемые микроглией, переводят астроциты в фенотип А1 (тип А1 теряет большинство нормальных функций астроцитов, но приобретает новую нейротоксическую функцию, быстро убивая нейроны и зрелые дифференцированные олигодендроциты) [23].
Это ключевое открытие: астроциты теряют часть своих нормальных поддерживающих функций (например, способность способствовать образованию синапсов) и начинают экспрессировать гены, продукты которых вредны для нейронов.
Механизмы формирования плотного глиального рубца
Астроциты резко увеличивают синтез глиального фибриллярного кислого белка (GFAP) [24]. Их цитоплазма заполняется этими промежуточными филаментами, клеточные тела увеличиваются, а отростки утолщаются и разрастаются, физически занимая пространство [25].
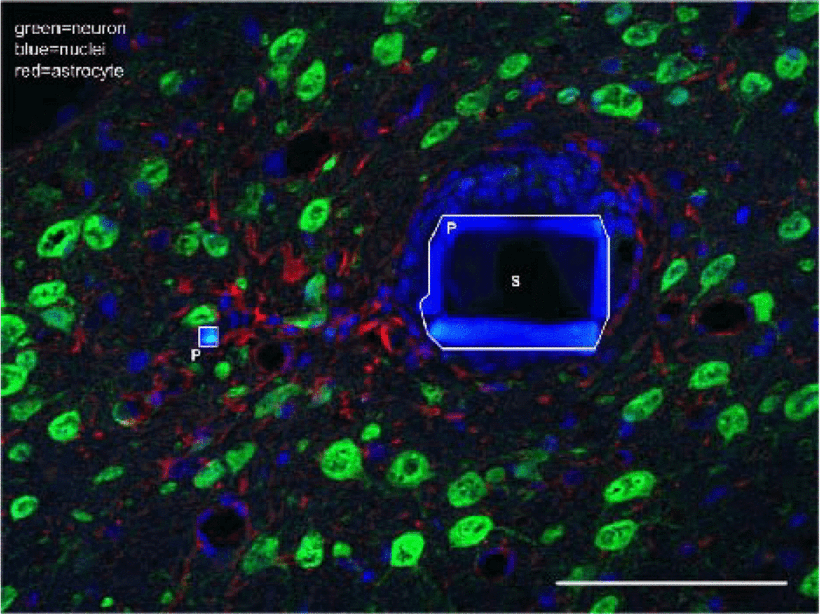
Рисунок 4. Поперечное флуоресцентное конфокальное изображение (400-кратное, погружение в масло). NeuN+ (зеленый, ядра нейронов), GFAP+ (красный, астроциты) и встречное пятно Хехста (синее) вокруг нейронального зонда. Стержень показан справа (белый прямоугольник) и состоит из парилена (P), заключенного в оболочку SU-8 (S). Боковой край размером 4×5 мкм слева представляет собой только парилен. Обратите внимание на разницу в плотности и толщине оболочки, окружающей две структуры. Нейроны также видны вблизи тонкой латеральной структуры, но вокруг хвостовика их нет. Масштабная линейка = 100 мкм.
Активированные астроциты начинают массово производить и секретировать компоненты внеклеточного матрикса, в первую очередь хондроитинсульфат протеогликаны (CSPG). CSPG (например, аггрекан, версикан) являются мощными химическими ингибиторами роста аксонов и синаптической пластичности [8]. Они создают «непроходимый лес» вокруг электрода. Также происходит реорганизация внеклеточного матрикса за счет сдвига концентрации белков клеточного матрикса (тенасцин-С и фибронектин), которые вместе формируют плотную, «рубцовую» ткань. Тела активированных астроцитов и микроглии, переплетенные с уплотненными отростками и внеклеточным матриксом, образуют непрерывный клеточный барьер, отделяющий «здоровую» ткань мозга от поверхности электрода.
А что происходит с нейронами?
«Рубцевание» ткани также влияет на нейроны, ведь происходит потеря опорных контактов, и глиальный рубец разрушает нормальную архитектуру нейропиля — это сложнейшая, плотно переплетенная сеть аксонов, дендритов и глиальных отростков, которая заполняет пространство между нейронами в сером веществе мозга. Это основная ткань, где происходят ключевые процессы обработки информации в нервной системе), нарушая связи нейронов с их естественным окружением. Также сказывается хроническое воздействие TNF-α и IL-1β, которое запускает в нейронах апоптотические пути. ROS напрямую повреждают липиды мембран, белки и ДНК нейронов. Воспалительная среда нарушает ионный гомеостаз (например, концентрацию K+) и нормальную передачу сигналов, что дополнительно угнетает функцию нейронов. В свою очередь, ингибиторные молекулы, такие как CSPG, посылают нейронам сигналы «не приближаться», предотвращая любую попытку реиннервации зоны имплантата [7].
Последствием «рубца» является электрическая изоляция — плотная упаковка клеток и внеклеточного матрикса, которая значительно повышает электрический импеданс вокруг контактов электрода. Это ослабляет регистрируемые сигналы (нейроны «глушатся» рубцом) [14] и требует более высоких токов для стимуляции, что может привести к дальнейшему повреждению ткани. Для успешной регистрации спайка нейрона должен находиться в радиусе ~50—100 мкм от контакта. Глиальный рубец может создать буферную зону в сотни микрометров [26]. Со временем амплитуда регистрируемых нейрональных сигналов неуклонно снижается, а уровень шума растет. В конечном итоге, сигнал становится неотличимым от шума [13], что приводит к функциональному отказу интерфейса мозг-компьютер, даже если электрод физически нетронутый.
Что предпринимают исследователи для продления работоспособности импланта?
Как мы уже выяснили, главным врагом долговечности нейроинтерфейсов является реакция на инородное тело (FBR). Чтобы пробиться через формирующийся вокруг имплантата барьер из глиальных клеток, ученые разрабатывают комплексную стратегию. Ее цель — перехватить и ослабить FBR на разных этапах. Все подходы можно условно разделить на три ключевых направления:
- Инженерные и материаловедческие решения: создание имплантатов, которые меньше травмируют ткань и лучше соответствуют ей по механическим свойствам.
- Биоактивные покрытия и локальная доставка препаратов: модификация поверхности имплантата для «обмана» иммунной системы или точечного подавления воспаления.
- Фармакологические и кондиционирующие методы: подготовка организма или системное воздействие препаратами для снижения реакции отторжения.
Если взглянуть в прошлое, станет очевидна одна из ключевых инженерных проблем. Первые интракортикальные зонды, такие как классические кремниевые Michigan probe и массивы Utah array, делали из очень жестких материалов (например, кремния). Их модуль Юнга (мера жесткости) составлял гигапаскали (ГПа). Для сравнения, мозговая ткань — это нежный гель с жесткостью в районе 0,1–10 килопаскалей (кПа). Разница в десятки тысяч раз! Представьте, что произойдет, если в мягкую подушку воткнуть жесткую щетину — она будет постоянно раздражать ткань. Именно так и работали первые имплантаты: их механическое несоответствие превращало их в источник хронической травмы и воспаления, о чем мы уже подробно говорили (рис. 5) [8], [27–30].

Рисунок 5. Эволюция технологий нейронных интерфейсов на протяжении десятилетий, демонстрирующая переход к повышенной гибкости устройств наряду с растущим использованием более мягких материалов.
Мягкие электроды
Логичным ответом на проблему жесткости стал переход к гибким полимерным электродам из таких материалов, как полиимид и парилен-C.
По своей эластичности они приближались к твердой мозговой оболочке — защитной мембране мозга [31]. Хотя их модуль упругости (все еще измеряемый в мегапаскалях, МПа) оставался выше, чем у мягкой нервной ткани, ключевым преимуществом стала способность изгибаться. Это снижало механическое напряжение вокруг имплантата [32]. Многочисленные эксперименты подтвердили успех: такие гибкие массивы вызывали образование глиального рубца на 40–60% меньше по сравнению с жесткими кремниевыми зондами. Это было значительным, но все еще недостаточным шагом к полной биосовместимости [9].
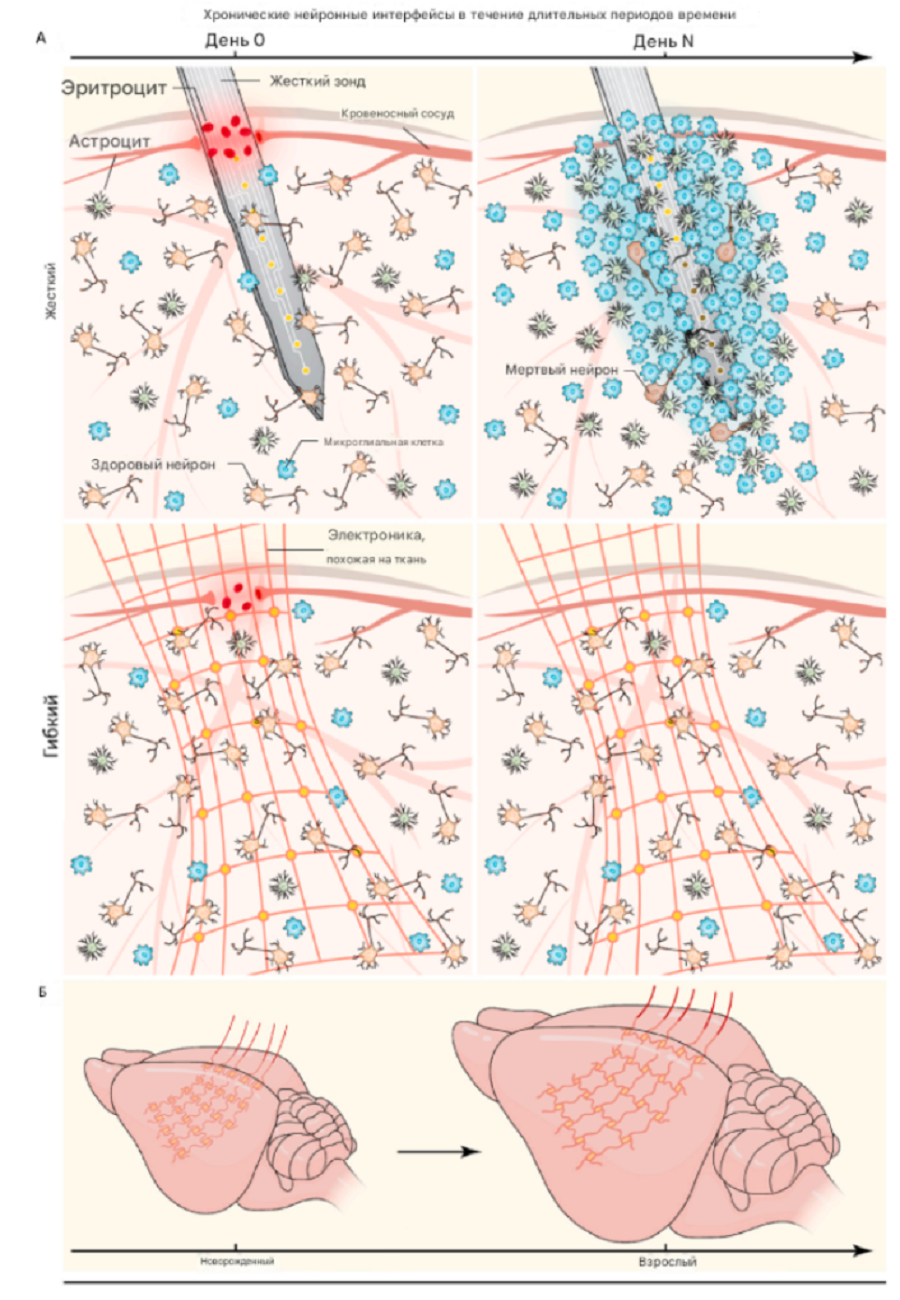
Рисунок 6. Гибкая электроника взаимодействует с нейронной активностью в различных временных масштабах. (а) — гибкая и жесткая электроника вызывает различные реакции тканей в течение длительного времени; (б) — растягиваемая электроника способствует хронической интеграции с растущей нервной тканью.
Следующий прорыв совершили технологии вроде «сетчатой электроники» (mesh electronics). Такие интерфейсы создают из ультрамягких материалов, чьи механические свойства практически неотличимы от свойств мозговой ткани. Это сводит к минимуму повреждения и иммунный ответ, позволяя имплантату работать в мозге годами. Один из самых поразительных примеров — ультрамягкие датчики для эмбрионов. Их имплантируют на ранних стадиях развития мозга, после чего они буквально «растут» вместе с ним. Эта технология впервые позволила непрерывно, в режиме реального времени, отслеживать формирование нейронной активности в масштабе всей жизни эмбриона [33] (рис. 6).
Важно отметить, что главное преимущество мягких электродов выходит далеко за рамки их способности к долгосрочной имплантации без выраженного воспаления. Их ключевая ценность — это возможность создавать настоящие «мультиталантливые» устройства, которые не только считывают электрические сигналы, но и позволяют активно взаимодействовать с мозгом на других уровнях (рис. 7). Например, комбинируя электрофизиологию с оптогенетикой, можно с высочайшей точностью стимулировать только определенные типы нейронов, помеченные светочувствительными белками. Другой мощный метод — хемогенетика, где с помощью встроенных микрофлюидных каналов можно доставлять вещества, избирательно активирующие генетически модифицированные клетки. Эти подходы позволяют не просто регистрировать активность, а точно определять, какие именно клеточные «игроки» и по каким биохимическим правилам участвуют в «сложной игре» высших когнитивных процессов, ведь мозг — это не просто генератор импульсов, а в первую очередь биологический и клеточный объект.
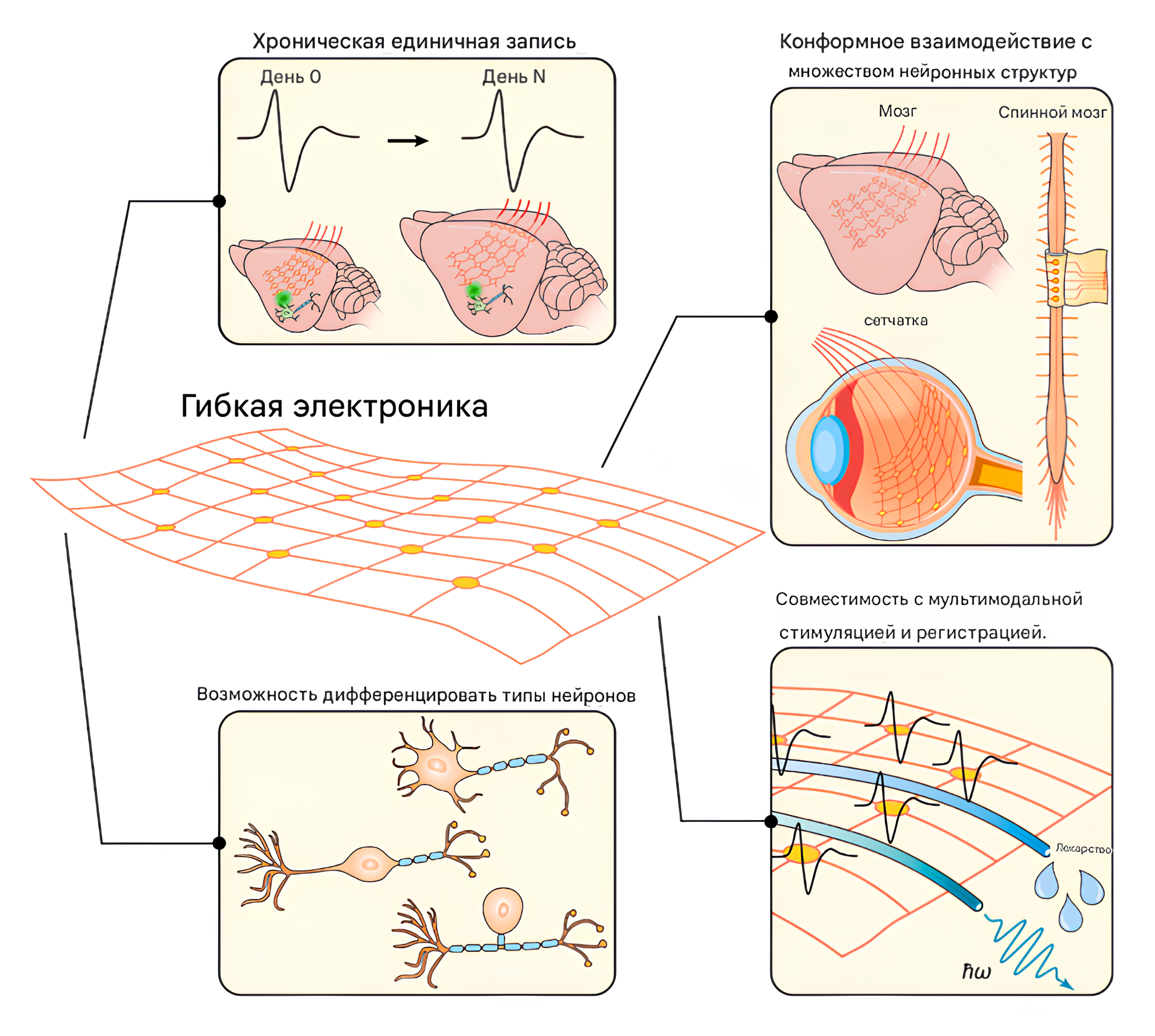
Рисунок 7. Гибкая электроника продвигает исследования в области нейронауки в четырех измерениях: регистрация нейронной активности с хронической стабильностью, доступ к нескольким структурам нервной системы, охват различных модальностей нейронного взаимодействия и предоставление возможности различать различные типы нейронов.
Последние разработки. Гидрогели
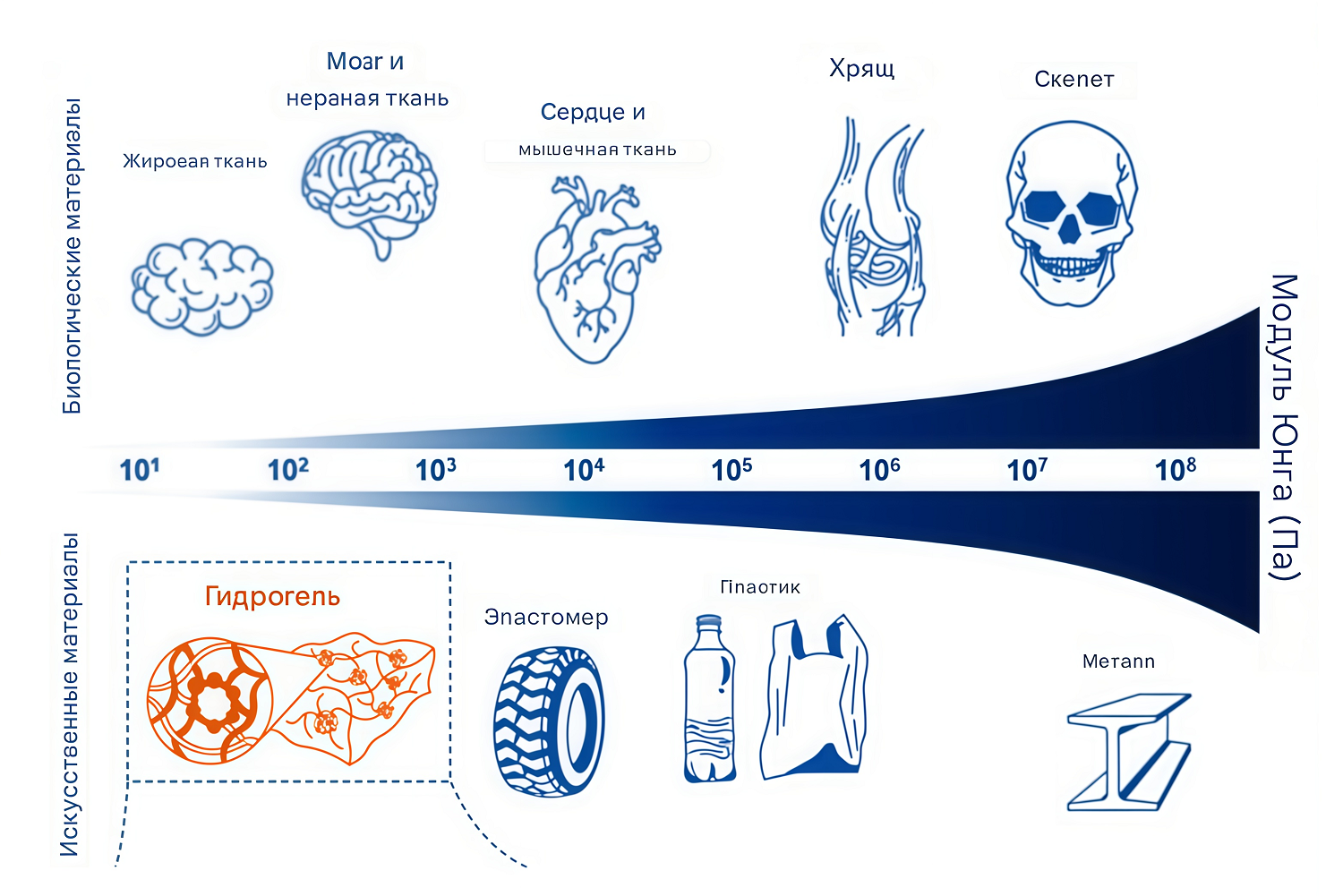
Рисунок 8. Разные значения модуля упругости у биологических тканей и искусственных материалов.
Однако наука не останавливается на поиске лучшего варианта, который будет по своим механическим свойствам не просто похожим, а идентичным головному мозгу. Сегодня наиболее радикальным существующим решением проблемы механического несоответствия являются гидрогелевые электроды, модуль упругости которых равен 1–100 кПа, всего в примерно в 10 раз отличающийся от показателей нейрональной ткани (рис. 8) [34].
Гидрогели открывают новую эру в создании биосовместимой электроники, способной работать внутри человеческого организма. Эти материалы представляют собой 3D [35] полимерные сети, способные удерживать огромное количество воды. Ключевой прорыв заключается в том, что ученые научились наделять эти мягкие влажные матрицы проводимостью [36], [37]. Это достигается за счет введения проводящих полимеров (например, PEDOT:PSS) или наполнителей вроде углеродных нанотрубок, а также за счет использования ионной проводимости, которая естественным образом возникает при движении ионов в пористой структуре геля (рис. 9) [38–40].
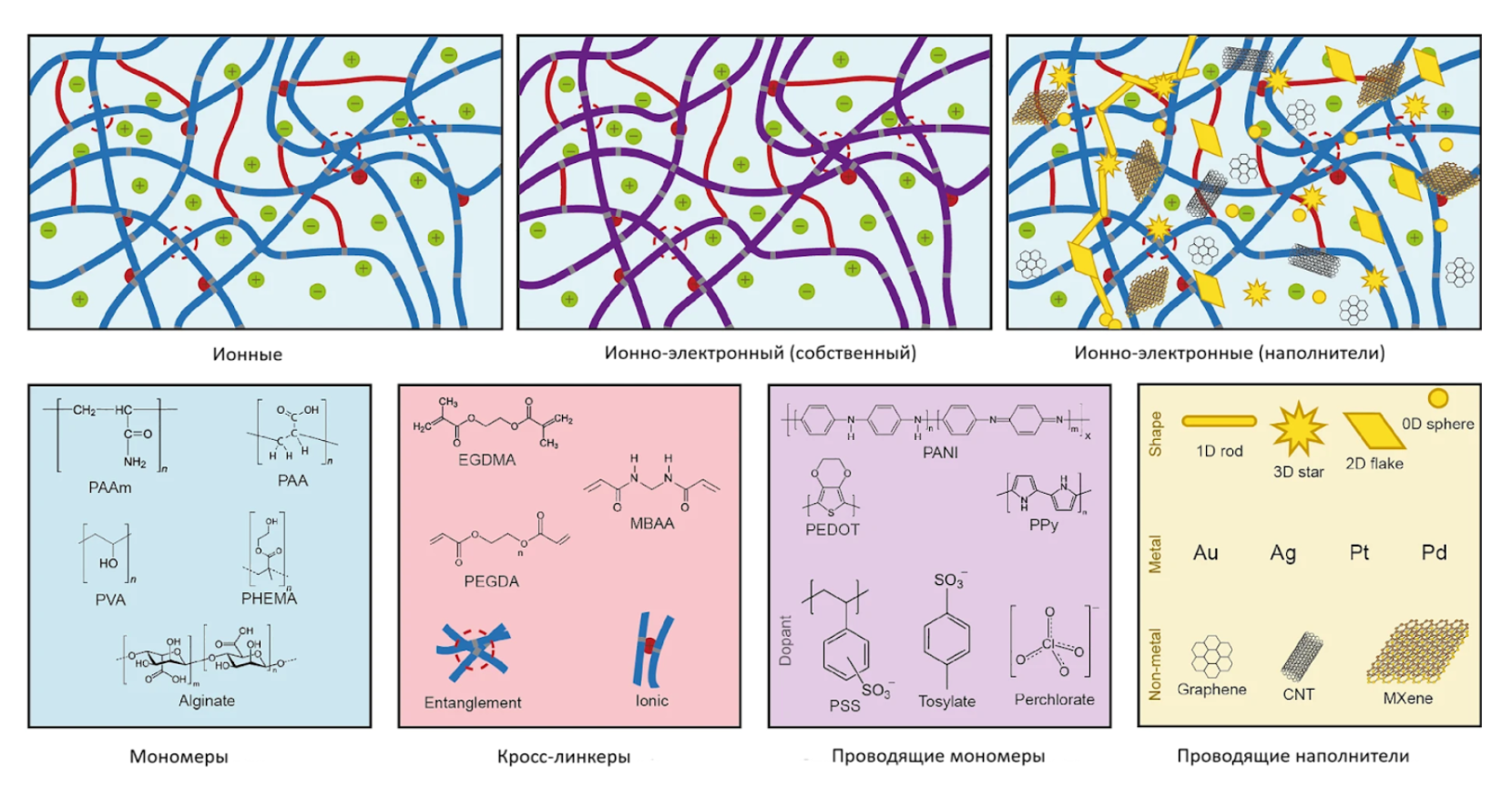
Рисунок 9. Структуры гидрогеля, придающие ему уникальные свойства.
Потенциал таких технологий поистине огромен. В нейроинтерфейсах будущего ультрамягкие электроды на основе гидрогелей смогут минимально инвазивно интегрироваться с тканью мозга, сводя к минимуму воспаление и обеспечивая многолетнюю стабильную запись или стимуляцию [37].
Но на этом их возможности не заканчиваются. Такие материалы открывают путь к принципиально новым типам устройств: полностью имплантируемым, автономным системам, а в перспективе — и к созданию биоразлагаемых имплантатов. Последние могли бы выполнять свою задачу (например, мониторинг или локальную терапию после операции), а затем безопасно рассасываться, не требуя извлечения.
Недостатки мягких электродов
Несмотря на революционный потенциал, мягкая электроника для нейроинтерфейсов сталкивается с рядом серьезных технологических барьеров.
- Ограниченное быстродействие. Гидрогели и полимеры в основном проводят ток за счет движения ионов, что происходит намного медленнее, чем перенос электронов в металлах или кремнии. Это делает их пока непригодными для высокочастотных приложений [1].
- Проблемы долговечности. Поддержание стабильной работы в живом организме — настоящее испытание. Постоянная влажность, агрессивная биохимическая среда и механические нагрузки приводят к деградации материалов и «дрейфу» ключевых параметров устройства [2].
- Сложность интеграции и масштабирования. Создание гибридных систем, где мягкий имплантат соединяется с традиционной «жесткой» микроэлектроникой (КМОП-чипами), — нетривиальная инженерная задача. Она создает препятствия для стандартных производственных процессов и коммерциализации [3].
- Энергопитание. Как эффективно питать автономный мягкий имплантат? Использовать громоздкие внешние элементы или потенциально опасные чрескожные разъемы нежелательно, а надежного встроенного решения пока нет [5].
Несмотря на эти вызовы, уникальное преимущество мягких интерфейсов — их способность к бесшовному контакту с тканью — остается недостижимым для классических технологий. Преодоление текущих ограничений через разработку новых композитных материалов и гибридных архитектур станет главной задачей будущих исследований. Именно от этого зависит воплощение мечты о стирании границ между живым организмом и вычислительной машиной.
Хирургические методы и подходы, уменьшающие травматичность при инвазии
Уже небезызвестные нам проникающие микроэлектродные решетки (Michigan и Utah) долгое время были золотым стандартом для записей нейронной активности с высоким пространственным разрешением в интерфейсах мозг-компьютер (ИМК). Однако их применение сопряжено с фундаментальными проблемами: инвазивность и повреждение тканей увеличиваются с увеличением количества электродов, их крайне сложно удалить или заменить без дополнительного повреждения мозга, а стабильность декодирования нейронных сигналов со временем часто уступает стабильности сигналов с поверхностных электродов. Не до конца ясно, предлагают ли современные подходы с использованием более мягких проникающих электродов принципиально иной компромисс [41].
Однако современные подходы в хирургии электродов уже придумали, как минимизировать последствия на этапе вживления:
- Процедура инъекционного введения. Это операция с использованием методики syringe-injectable electronics (электроники, вводимой шприцом) напоминает стандартную инъекцию. Электронная сетка, которая в расправленном состоянии может достигать сантиметров, за счет своей ультрагибкой и макропористой структуры сворачивается внутри тонкой иглы. При введении в ткань мозга сетка мягко разворачивается, а ее структура позволяет нейронам и другим клеткам свободно мигрировать внутрь, формируя стабильный и биосовместимый интерфейс с минимальным хроническим иммунным ответом [42] (рис. 10).
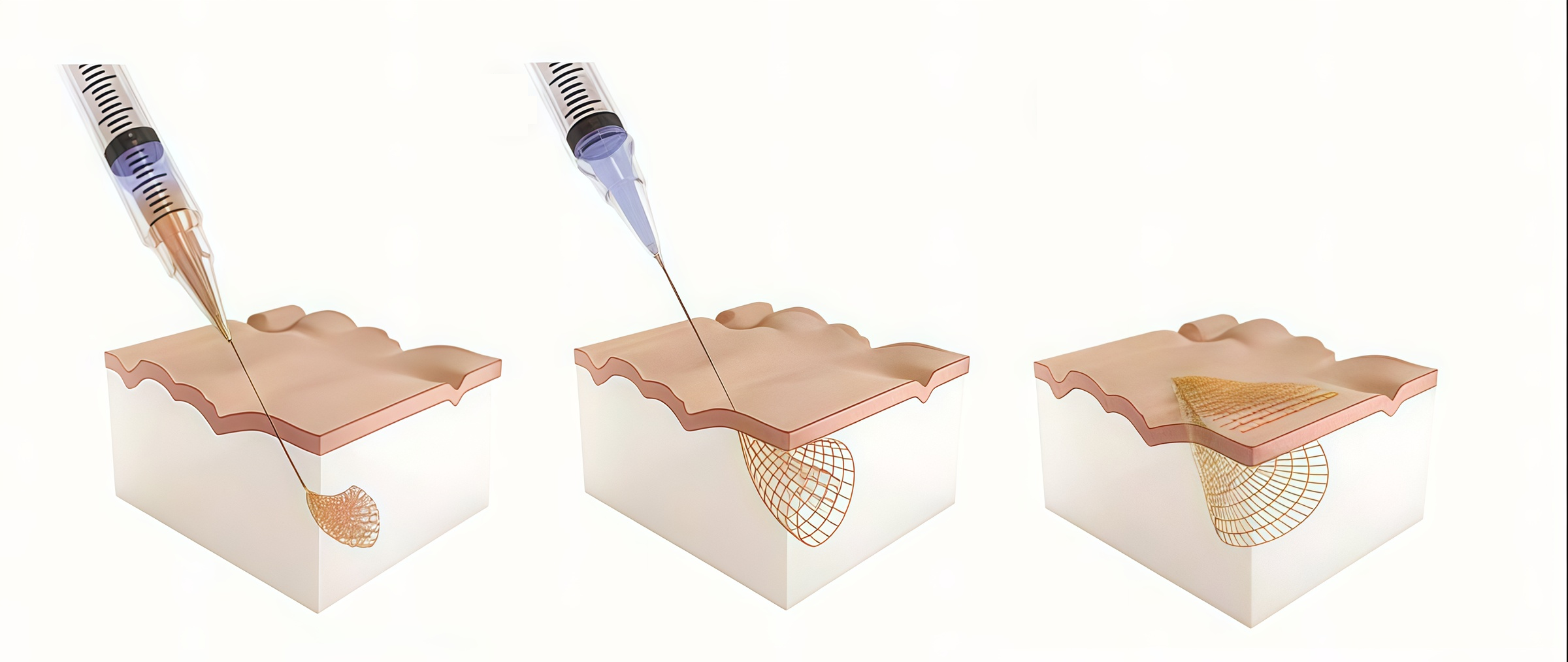
Рисунок 10. Схема и принцип инъекции сетчатых электродов.
- Эндоваскулярные стентроды (Stentrodes) — устройство доставляется через кровеносные сосуды (например, через яремную вену) и фиксируется в вене, проходящей рядом с моторной корой. Это позволяет регистрировать сигналы мозга, не проникая в саму нервную ткань и не требуя трепанации черепа (рис. 11) [42–44], избегая повреждения ГЭБ.
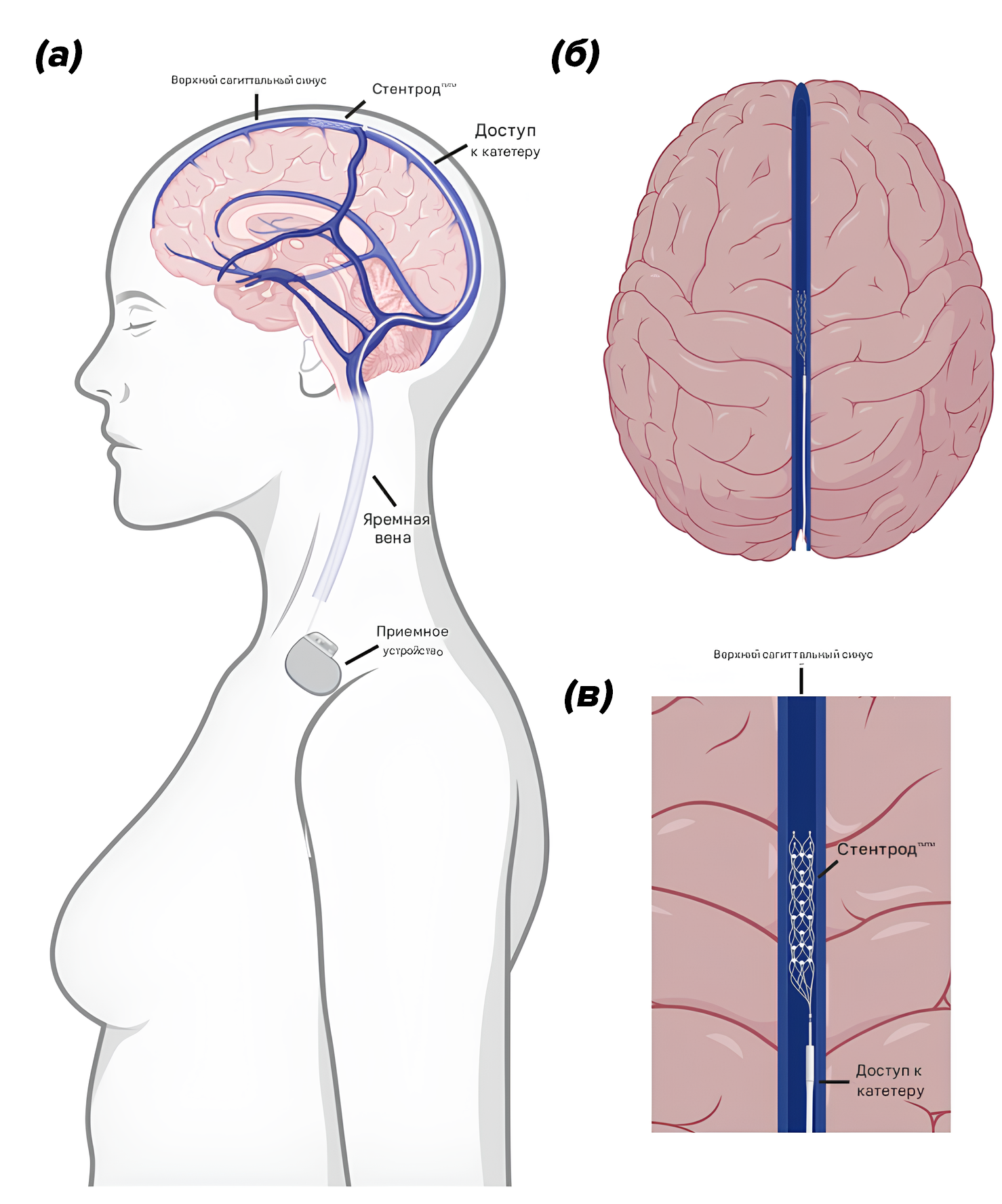
Рисунок 11. Имплантация Stentrode™. (а) — доставка через яремную вену в верхний сагиттальный синус для регистрации активности мозга; (б) — вид сверху: положение Stentrode™ в синусе. (в) — увеличение: Stentrode™ прилегает к ткани мозга.
- «Нейральная пыль» (Neural Dust) — концепция ультраминиатюрных беспроводных датчиков. Эти микромотивы с тончайшими углеродными электродами (тоньше человеческого волоса) имплантируются на поверхность коры, а их электроды проникают в ткань. Они получают питание и передают данные по беспроводной связи, что исключает необходимость в проводах, проходящих через череп (рис. 12).

Рисунок 12. Фотография ультраминиатюрных датчиков Neural Dust.
- Техника «краниальной микрощели» — представляет собой компромиссный подход. Вместо большой трепанации в черепе делаются разрезы шириной менее 1 мм, через которые под контролем нейроэндоскопа вводятся гибкие тонкопленочные электродные массивы. Это значительно менее травматично, чем классическая операция по вживлению цельной пластинки (рис. 13).
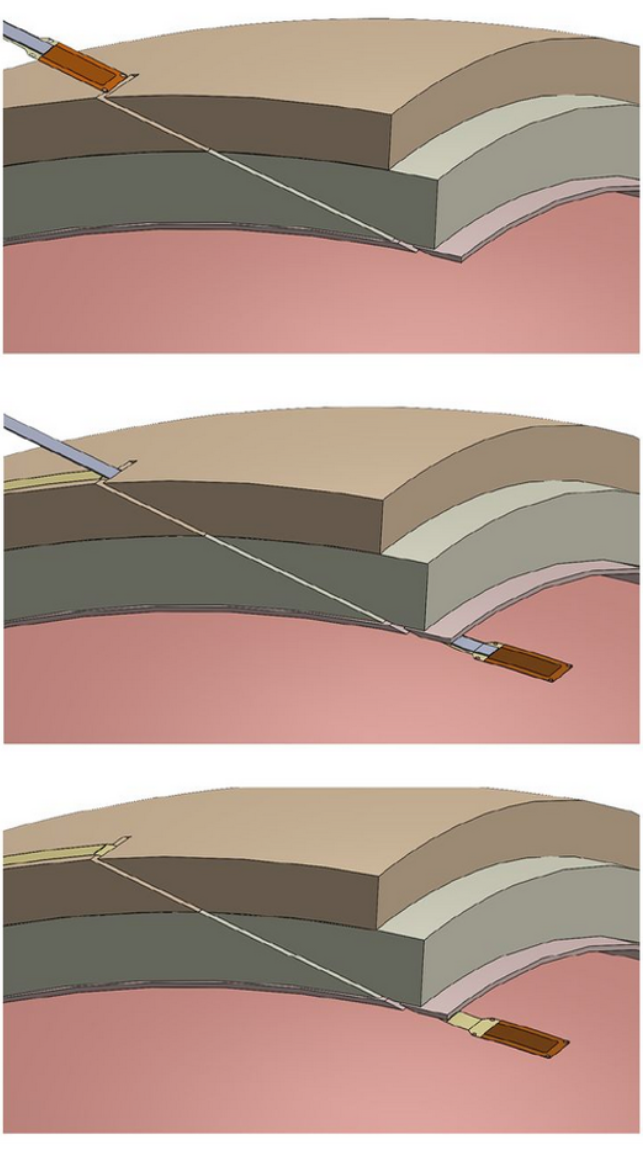
Рисунок 13. Техника введения «краниальной микрощели» от Precision Neuroscience, с демонстрацией введения массива на основе тонкой пленки в субдуральное пространство
изображение из [45], подпись — из «Нейроновости»
Современные тенденции указывают на соединение этих технологий в виде гибридных и «интеллектуальных» систем. К ним относятся устройства с динамическим модулем упругости, которые являются жесткими при имплантации и размягчаются in vivo (наиболее распространенными триггерами для размягчения являются температура тела и контакт с биологическими жидкостями, будучи жестким при комнатной температуре, становится мягким и гибким после имплантации) [46], интерфейсы с интегрированными микрофлюидными каналами для локальной доставки лекарственных средств [47], а также биогибридные системы, содержащие живые клетки (например, мезенхимальные стромальные клетки), которые выделяют паракринные факторы, модулирующие воспалительный ответ и способствующие регенерации [48].
Наконец, системные и упреждающие методы предлагают взаимодополняющий подход. Это включает в себя исследование системных фармакологических методов лечения и новых концепций, таких как диетическое прекондиционирование (например, ограничение калорийности), которое, как было показано, обеспечивает нейропротекцию и усиливает противовоспалительные механизмы [49].
Еще одна нерешенная проблема
В конце хочется обсудить момент электрического снабжения интерфейсов. Если разговор заходит о длительной имплантации, то остается открытым вопрос подзарядки устройства. Нижи приведено сравнение различных методов питания устройств [50]:
| Метод | Принцип работы | Преимущества | Недостатки и риски |
|---|---|---|---|
| Встроенные аккумуляторы | Компактная перезаряжаемая батарея внутри корпуса импланта | Высокая автономность, не требует постоянной связи с внешним миром | Ограниченный срок службы; риск утечки токсичных веществ; необходимость периодической подзарядки |
| Чрескожные соединители | Прямой физический контакт через разъем, выведенный на поверхность кожи | Надежная подача большой мощности; прямая передача данных | Высокий риск инфекции; неудобство для пациента; повреждение соединителя |
| Индукционная зарядка | Беспроводная передача энергии через электромагнитное поле между внешней катушкой и имплантированной катушкой | Удобство для пациента (зарядка через кожу); отсутствие риска инфекции | Низкий КПД; необходимость близкого расположения катушек; нагрев тканей |
| Ультразвуковая зарядка | Передача энергии с помощью ультразвуковых волн, которые преобразуются пьезоэлементом в импланте в электричество | Более глубокое проникновение в ткани; меньшее рассеяние энергии | Относительно новая технология; меньшая эффективная мощность |
| Биотопливные элементы [51] | Генерация электричества из биохимических источников в организме (например, глюкоза и кислород) | Теоретически неограниченный срок службы; полная автономность | Низкая выходная мощность; проблемы с долговечностью и стабильностью в организме |
Выводы
Таким образом, ключевым препятствием для долговечности хронических инвазивных нейроинтерфейсов остается реакция на инородное тело (Foreign Body Reaction, FBR), инициируемая механическим несоответствием между имплантатом и тканью мозга. Этот каскадный процесс, включающий активацию микроглии, переход астроцитов в реактивное состояние и секрецию ингибиторных компонентов внеклеточного матрикса, приводит к формированию плотного глиально-фиброзного рубца. Данная структура вызывает электрическую изоляцию электрода, увеличение расстояния «электрод-нейрон» и прогрессирующую деградацию регистрируемого сигнала.
Перспективы преодоления этого барьера связаны с комплексным междисциплинарным подходом. На первый план выходят стратегии, направленные на минимизацию механического несоответствия за счет разработки ультрамягких материалов, таких как проводящие гидрогели, чей модуль упругости приближается к таковому у нервной ткани. Дополняют эти методы инновационные хирургические техники, снижающие травматичность имплантации, и биоинженерные решения, включающие локальную доставку противовоспалительных препаратов. Дальнейший прогресс в создании стабильных биосовместимых интерфейсов определит возможность их широкого и безопасного клинического применения, открывая новые горизонты в нейрореабилитации и фундаментальных исследованиях работы мозга.
Литература
- Mikhail A. Lebedev, Miguel A.L. Nicolelis. (2006). Brain–machine interfaces: past, present and future. Trends in Neurosciences. 29, 536-546;
- Mikhail Lebedev. (2014). Brain-machine interfaces: an overview. Translational Neuroscience. 5;
- Santosh Chandrasekaran, Matthew Fifer, Stephan Bickel, Luke Osborn, Jose Herrero, et. al.. (2021). Historical perspectives, challenges, and future directions of implantable brain-computer interfaces for sensorimotor applications. Bioelectron Med. 7;
- Tyler Singer-Clark, Xianda Hou, Nicholas S Card, Maitreyee Wairagkar, Carrina Iacobacci, et. al.. (2025). Speech motor cortex enables BCI cursor control and click. J. Neural Eng.. 22, 036015;
- Steven M. Wellman, Takashi D.Y. Kozai. (2018). In vivo spatiotemporal dynamics of NG2 glia activity caused by neural electrode implantation. Biomaterials. 164, 121-133;
- Takashi D. Y. Kozai, Nicolas A. Alba, Huanan Zhang, Nicolas A. Kotov, Robert A. Gaunt, Xinyan Tracy Cui. (2014). Nanostructured Coatings for Improved Charge Delivery to Neurons. Nanotechnology and Neuroscience: Nano-electronic, Photonic and Mechanical Neuronal Interfacing. 71-134;
- Joseph W. Salatino, Kip A. Ludwig, Takashi D. Y. Kozai, Erin K. Purcell. (2017). Glial responses to implanted electrodes in the brain. Nat Biomed Eng. 1, 862-877;
- Mehdi Jorfi, John L Skousen, Christoph Weder, Jeffrey R Capadona. (2015). Progress towards biocompatible intracortical microelectrodes for neural interfacing applications. J. Neural Eng.. 12, 011001;
- Takashi D.Y. Kozai, Zhannetta Gugel, Xia Li, Peter J. Gilgunn, Rakesh Khilwani, et. al.. (2014). Chronic tissue response to carboxymethyl cellulose based dissolvable insertion needle for ultra-small neural probes. Biomaterials. 35, 9255-9268;
- Kelsey A. Potter, Mehdi Jorfi, Kyle T. Householder, E. Johan Foster, Christoph Weder, Jeffrey R. Capadona. (2014). Curcumin-releasing mechanically adaptive intracortical implants improve the proximal neuronal density and blood–brain barrier stability. Acta Biomaterialia. 10, 2209-2222;
- Stéphanie P. Lacour, Grégoire Courtine, Jochen Guck. (2016). Materials and technologies for soft implantable neuroprostheses. Nat Rev Mater. 1;
- Christi L. Kolarcik, Silvia D. Luebben, Shawn A. Sapp, Jenna Hanner, Noah Snyder, et. al.. (2015). Elastomeric and soft conducting microwires for implantable neural interfaces. Soft Matter. 11, 4847-4861;
- Takashi D. Y. Kozai, Andrea S. Jaquins-Gerstl, Alberto L. Vazquez, Adrian C. Michael, X. Tracy Cui. (2015). Brain Tissue Responses to Neural Implants Impact Signal Sensitivity and Intervention Strategies. ACS Chem. Neurosci.. 6, 48-67;
- T D Y Kozai, T C Marzullo, F Hooi, N B Langhals, A K Majewska, et. al.. (2010). Reduction of neurovascular damage resulting from microelectrode insertion into the cerebral cortex usingin vivotwo-photon mapping. J. Neural Eng.. 7, 046011;
- Christopher T. Tsui, Preet Lal, Katelyn V. R. Fox, Matthew A. Churchward, Kathryn G. Todd. (2022). The effects of electrical stimulation on glial cell behaviour. BMC biomed eng. 4;
- Claudia Eder. (2005). Regulation of microglial behavior by ion channel activity. J of Neuroscience Research. 81, 314-321;
- Alejandro Carnicer-Lombarte, Shao-Tuan Chen, George G. Malliaras, Damiano G. Barone. (2021). Foreign Body Reaction to Implanted Biomaterials and Its Impact in Nerve Neuroprosthetics. Front. Bioeng. Biotechnol.. 9;
- Michael V. Sofroniew. (2009). Molecular dissection of reactive astrogliosis and glial scar formation. Trends in Neurosciences. 32, 638-647;
- Baljit S Khakh, Michael V Sofroniew. (2015). Diversity of astrocyte functions and phenotypes in neural circuits. Nat Neurosci. 18, 942-952;
- Joan Y. W. Liu, Maria Thom, Claudia B. Catarino, Lillian Martinian, Dominique Figarella-Branger, et. al.. (2012). Neuropathology of the blood–brain barrier and pharmaco-resistance in human epilepsy. Brain. 135, 3115-3133;
- Shenton S.L. Chew, Cameron S. Johnson, Colin R. Green, Helen V. Danesh-Meyer. (2010). Role of connexin43 in central nervous system injury. Experimental Neurology. 225, 250-261;
- Tarun Saxena, Lohitash Karumbaiah, Eric A. Gaupp, Radhika Patkar, Ketki Patil, et. al.. (2013). The impact of chronic blood–brain barrier breach on intracortical electrode function. Biomaterials. 34, 4703-4713;
- Shane A. Liddelow, Kevin A. Guttenplan, Laura E. Clarke, Frederick C. Bennett, Christopher J. Bohlen, et. al.. (2017). Neurotoxic reactive astrocytes are induced by activated microglia. Nature. 541, 481-487;
- Andrew Campbell, Chengyuan Wu. (2018). Chronically Implanted Intracranial Electrodes: Tissue Reaction and Electrical Changes. Micromachines. 9, 430;
- John P. Seymour, Daryl R. Kipke. (2006). Fabrication of Polymer Neural Probes with Sub-cellular Features for Reduced Tissue Encapsulation. 2006 International Conference of the IEEE Engineering in Medicine and Biology Society. 4606-4609;
- Takashi D Yoshida Kozai, Alberto L Vazquez, Cassandra L Weaver, Seong-Gi Kim, X Tracy Cui. (2012). In vivotwo-photon microscopy reveals immediate microglial reaction to implantation of microelectrode through extension of processes. J. Neural Eng.. 9, 066001;
- K.D. Wise, K. Najafi, R.D. Sacks, E.T. Zellers. (). A wireless integrated microsystem for environmental monitoring. 2004 IEEE International Solid-State Circuits Conference (IEEE Cat. No.04CH37519). 434-537;
- P.K. Campbell, K.E. Jones, R.J. Huber, K.W. Horch, R.A. Normann. (1991). A silicon-based, three-dimensional neural interface: manufacturing processes for an intracortical electrode array. IEEE Trans. Biomed. Eng.. 38, 758-768;
- Vadim S. Polikov, Patrick A. Tresco, William M. Reichert. (2005). Response of brain tissue to chronically implanted neural electrodes. Journal of Neuroscience Methods. 148, 1-18;
- Zezhen Cheng, Manish Shrivastava, Amna Ijaz, Daniel Veghte, Gregory W. Vandergrift, et. al.. (2024). Enhanced light absorption for solid-state brown carbon from wildfires due to organic and water coatings. Nat Commun. 15;
- Ivan R. Minev, Pavel Musienko, Arthur Hirsch, Quentin Barraud, Nikolaus Wenger, et. al.. (2015). Electronic dura mater for long-term multimodal neural interfaces. Science. 347, 159-163;
- Lan Luan, Xiaoling Wei, Zhengtuo Zhao, Jennifer J. Siegel, Ojas Potnis, et. al.. (2017). Ultraflexible nanoelectronic probes form reliable, glial scar–free neural integration. Sci. Adv.. 3;
- Yihang Chen, Nicholas J. Rommelfanger, Ali I. Mahdi, Xiang Wu, Scott T. Keene, et. al.. (2021). How is flexible electronics advancing neuroscience research?. Biomaterials. 268, 120559;
- Hoon Choi, Wan-Sun Choi, Jin-Oh Jeong. (2024). A Review of Advanced Hydrogel Applications for Tissue Engineering and Drug Delivery Systems as Biomaterials. Gels. 10, 693;
- Dingyao Liu, Jing Bai, Xinyu Tian, Yan Wang, Binbin Cui, et. al.. (2025). Increasing the dimensionality of transistors with hydrogels. Science. 390, 824-830;
- Stephanie Fuchs, Kaavian Shariati, Minglin Ma. (2020). Specialty Tough Hydrogels and Their Biomedical Applications. Adv Healthcare Materials. 9;
- Simin Cheng, Ruiqi Zhu, Xiaomin Xu. (2024). Hydrogels for next generation neural interfaces. Commun Mater. 5;
- Janani Sriramakrishnan, Ananya BS, Goutam Thakur, Pradeep Kumar. (2025). Sustainable hydrogels as conductive platforms for neural applications. Reactive and Functional Polymers. 216, 106427;
- Georgios Kougkolos, Muriel Golzio, Lionel Laudebat, Zarel Valdez-Nava, Emmanuel Flahaut. (2023). Hydrogels with electrically conductive nanomaterials for biomedical applications. J. Mater. Chem. B. 11, 2036-2062;
- Kutay Sagdic, Emilio Fernández-Lavado, Massimo Mariello, Outman Akouissi, Stéphanie P. Lacour. (2023). Hydrogels and conductive hydrogels for implantable bioelectronics. MRS Bulletin. 48, 495-505;
- Mark Hettick, Elton Ho, Adam J. Poole, Manuel Monge, Demetrios Papageorgiou, et. al.. (2025). Minimally invasive implantation of scalable high-density cortical microelectrode arrays for multimodal neural decoding and stimulation. Nat. Biomed. Eng;
- Jia Liu, Tian-Ming Fu, Zengguang Cheng, Guosong Hong, Tao Zhou, et. al.. (2015). Syringe-injectable electronics. Nature Nanotech. 10, 629-636;
- Julien Ognard, Gerard El Hajj, Onam Verma, Sherief Ghozy, Ramanathan Kadirvel, et. al.. (2025). Advances in endovascular brain computer interface: Systematic review and future implications. Journal of Neuroscience Methods. 420, 110471;
- Daniel P. Chapman, Jian-Young Wu. (2024). Concept for intrathecal delivery of brain recording and stimulation device. Front. Med. Technol.. 6;
- Mark Hettick, Elton Ho, Adam J. Poole, Manuel Monge, Demetrios Papageorgiou, et. al. The Layer 7 Cortical Interface: A Scalable and Minimally Invasive Brain–Computer Interface Platform — openRxiv;
- Subin Oh, Simok Lee, Sung Woo Kim, Choong Yeon Kim, Eun Young Jeong, et. al.. (2024). Softening implantable bioelectronics: Material designs, applications, and future directions. Biosensors and Bioelectronics. 258, 116328;
- Aydin Bordbar-Khiabani, Michael Gasik. (2022). Smart Hydrogels for Advanced Drug Delivery Systems. IJMS. 23, 3665;
- Philipp Gutruf, John A Rogers. (2018). Implantable, wireless device platforms for neuroscience research. Current Opinion in Neurobiology. 50, 42-49;
- Yuan Liu, Rong Wang, Zhiwei Zhao, Wen Dong, Xu Zhang, et. al.. (2017). Short-term caloric restriction exerts neuroprotective effects following mild traumatic brain injury by promoting autophagy and inhibiting astrocyte activation. Behavioural Brain Research. 331, 135-142;
- Jiahui Wang, Tianyiyi He, Chengkuo Lee. (2019). Development of neural interfaces and energy harvesters towards self-powered implantable systems for healthcare monitoring and rehabilitation purposes. Nano Energy. 65, 104039;
- Ekaterina Vakhnitskaya, Yulia Parunova, Anna Rybakova, Pavel Gotovtsev. (2024). Multi-walled Carbon Nanotubes-based Glucose Biofuel Cell Operating in Rats’ Brains. 2024 IEEE Ural-Siberian Conference on Biomedical Engineering, Radioelectronics and Information Technology (USBEREIT). 273-276.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





