Борьба с солью: решающий удар за сорбентами
07 ноября 2019
Борьба с солью: решающий удар за сорбентами
- 1448
- 7
- 0
Пористая система сорбентов последнего поколения на основе металлорганических каркасов (MOFs)
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Экологическая катастрофа двадцатого столетия — высыхание Аральского моря — привела к тяжелейшему упадку сельского хозяйства в Центральной Азии. Засоление подорвало плодородие почвы, из-за чего растения не приносят ожидаемых урожаев. Что значит солевой стресс для растения? Какие изменения он вызывает? И можно ли с ним бороться, если старые способы не работают? Мы провели исследование по поиску альтернативных методов снижения засоленности почв, изучив динамику роста и развития растений с использованием сорбентов в условиях солевого стресса: от длины корней до активности антиоксидантных ферментов. В этой статье вы узнаете: связано ли засоление с другими видами метаболических стрессов, способны ли растения бороться с ним, и как промышленные сорбенты и отходы ГРЭС могут спасти деградированные почвы.
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Школьная» конкурса «био/мол/текст»-2019.

Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.

Партнер номинации — Некоммерческая школа «Летово».

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступила компания BioVitrum.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Как осушение Аральского моря привело к засолению во всем Казахстане?
Все мы слышали о трагедии Аральского моря (рис. 1), шокирующей своей масштабностью. Высыхание Аральского моря имеет тяжелейшие последствия для экологии, главное из которых — засоление почвы. Пыльные бури разносят соль, пыль и ядохимикаты на расстояние до 500 км. Таким образом засоление коснулось земли далеко за пределами Приаральского региона [1]. Среди трех известных типов засоления (сульфатное, карбонатное, хлоридное) наиболее токсично — хлоридное, вызывающее сильное угнетение ростовых процессов, в крайних случаях и гибель растения [2]. Именно этот вид засоления широко распространен в Кызылординской области (рис. 2).

Рисунок 1. Высыхание Аральского моря. Динамика с 1989 по 2009 годы. Сейчас находится в состоянии еще большего упадка.

Рисунок 2. Засоленные регионы полей Кызылординской области
В плодородных, на первый взгляд, областях пятнами распространены солонцы и солончаки из-за несовершенного орошения сельскохозяйственных угодий. Как итог — страдают все: и фермеры, и животные, и растения, и местные экосистемы.
Что такое солевой стресс и чем он опасен?
Как известно, большинство сельскохозяйственных культур — гликофиты — чувствительные к засолению растения. Это означает, что небольшие колебания в степени засоленности почвы угнетают не только урожайность растений, но и рост, и нормальный метаболизм [3]. Избыток токсичных водорастворимых солей в корневом горизонте почвы — вот что такое солевой стресс для растения.
Однако солевой стресс не так прост, как кажется. Он способен запустить целый каскад других стрессовых реакций, ухудшающих состояние растения [4]:
- Осмотический стресс. В условиях повышенной засоленности растения крайне страдают от недостатка воды, который выливается в «гашение» фотосинтеза, снижение транспирации и деградацию пигментов (хлорофилла) [5].
- Ионный дисбаланс. Ионный стресс напрямую связан с утечкой ионов калия и накоплением токсичных ионов натрия в клетках растений. Также ионы Na+ вызывают выход воды из клеток листьев и корней в межклеточное пространство (рис. 3) [6].
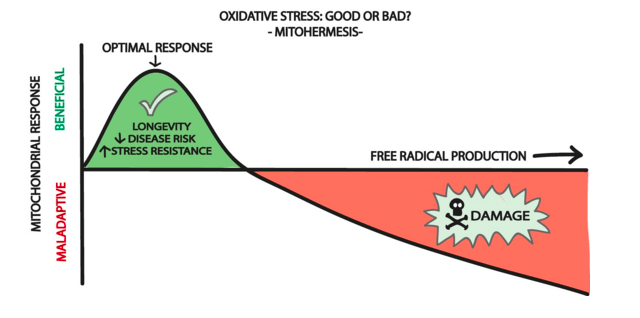
- Окислительный стресс. Самое опасное последствие солевого воздействия. Водорастворимые токсичные соли, такие как хлорид натрия (NaCl), в высоких концентрациях стимулируют синтез активных форм кислорода (АФК) — невероятно активных радикалов, которые нужно незамедлительно обезвредить. Иначе — разрушение клеточных компонентов: липидов мембран, белков, нуклеиновых кислот (ДНК и РНК), пигментов и ядерных элементов (рис. 4) [7].
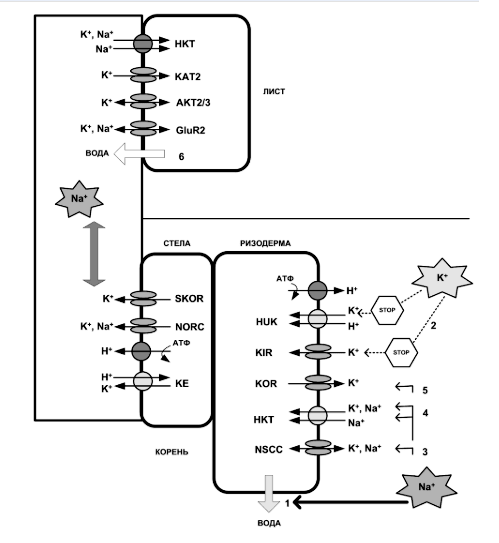
Рисунок 3. Утечка ионов калия с избыточным поглощением ионов натрия транспортировщиками в листе и клетке корней
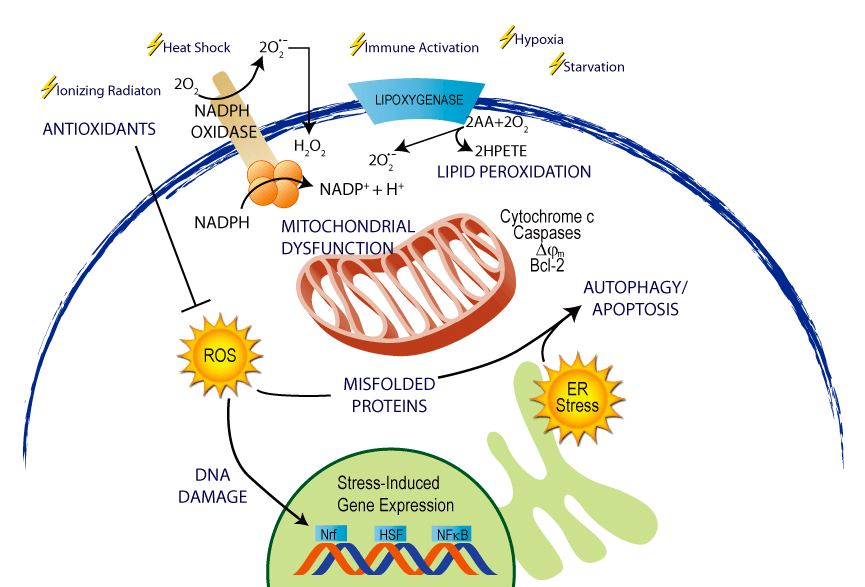
Рисунок 4. Последствия влияния солевого стресса на клетку: разрушение мембран, ДНК, белков активными формами кислорода. Возможный итог — разрушение или апоптоз клетки.
Солевой стресс вызывает специфические изменения в метаболизме растения, сильно влияя на вегетативные параметры роста: сухую массу, высоту растений и длину корней, площадь листьев и т.п. Как правило, растения особенно чувствительны к засолению на ранних этапах роста и появления всходов (рис. 5).

Рисунок 5. Влияние солевого стресса на толерантное растение (слева) и чувствительное (справа)
Как растения противостоят натиску токсичных ионов солей?
За тысячи лет эволюции даже самые чувствительные растения выработали свои защитные механизмы (пусть и краткосрочные) против солевого стресса [8]:
- торможение поглощения солей;
- синтез осмолитов — низкомолекулярных органических соединений, не вызывающих изменений в метаболизме растения, например, пролина;
- накопление солей в вакуолях;
- ионная дискриминация K+, Na+, Cl– и SO42– во время поглощения корнями и транспорта в побеги;
- выработка некоторых ферментов, гормонов, антиоксидантов [10]. Для очистки от АФК и токсичных продуктов распада служат антиоксидантные ферменты: супероксидисмутаза (СОД), каталаза (КАТ), аскорбатпероксидаза (АПО) [9].
Фермент альдегидоксидаза (АО) участвует в биосинтезе «гормона стресса» — абсцизовой кислоты (ABA) [10]. Было обнаружено повышенное содержание альдегидоксидазы в корнях и побегах растения в условиях солевого стресса, в корнях засоленного ячменя содержалось больше всего единиц фермента АО [11].
Что «не так» с засолением?
Как бы ни была эффективна адаптация к солевому стрессу, при длительном воздействии растения неминуемо погибнут. Сейчас решение проблемы засоления разделяется на два направления.
- Агротехническое. Мелиорация — дорогостоящий процесс, зачастую усложненный из-за увеличения засоленности сильнозасоленных почв и солонцов. Глубокое рыхление пашни и промывной полив по-прежнему не гарантирует урожайности культур [12].
- Генноинженерное. Селекция солеустойчивых растений остается критически сложным направлением исследований, так как признак солеустойчивости определен множеством генов (около 8% всего генома), а экспрессия более 25% всех генов, вызывающих неспецифичный комплексный ответ на засоление, зависит от концентрации солей [6].
Поэтому фермеры зачастую ограничиваются лишь малоэффективным севооборотом и простыми дешевыми органическими удобрениями (навозом).
Сорбенты: что, как, и где поглощается, и причем тут засоление?
Сорбенты — твердые тела или жидкости, избирательно поглощающие из окружающей среды определенные вещества. По характеру поглощения делятся на:
- абсорбенты (рис. 6);
- адсорбенты (разветвленная пористая поверхность обеспечивает поглощение веществ на разделе твердой и жидкой фаз) (рис. 7) [13];
- ионообменные смолы (иониты, IXR) — сорбируют ионы одного типа с выделением в раствор эквивалентного количества ионов другого типа (рис. 8).
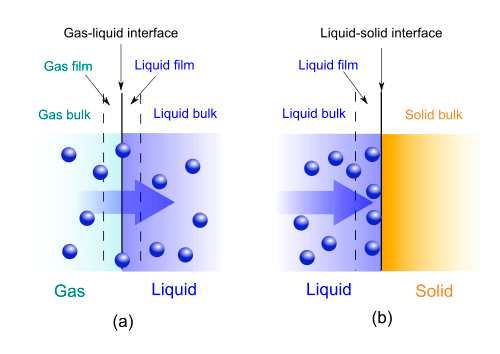
Рисунок 6. Различия между абсорбентами (слева) и адсорбентами (справа). Основное различие заключается в активных фазах (газ/жидкость и жидкость / твердое тело).
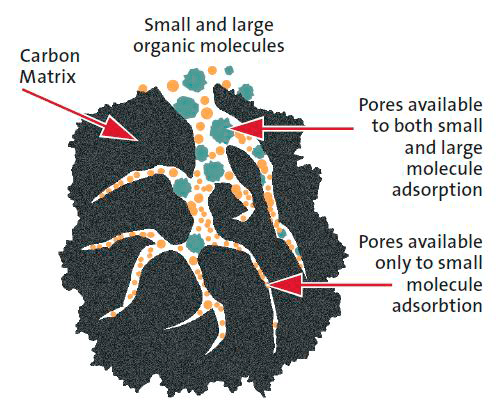
Рисунок 7. Пористая система активированного угля: макропоры захватывают более крупные молекулы, микропоры — более мелкие
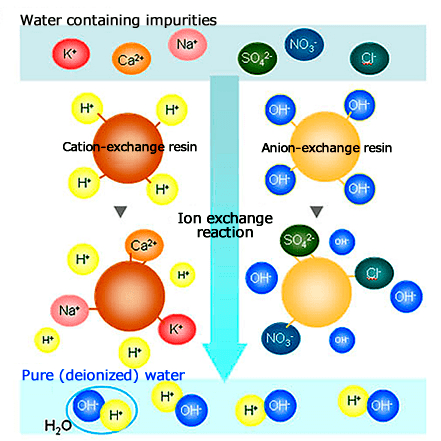
Рисунок 8. Механизм ионообменной реакции между ионообменной смолой и ионами с целью очищения воды. На иллюстрации видно, как группы H+ и OH– замещаются на ионы солей.
Иониты уже сейчас широко используются для удаления ионов из жесткой воды посредством фильтрования или для очистки морской воды (с замещением ионов NaCl на Ca (OH)2) [14]. Активированный уголь используют не только как эндосорбент при интоксикации, но также как фильтр жидкостей и газов (например, внутри противогазов); гранулы активированного угля также удаляют ионы Cl– и органических загрязнителей из технических вод [15].
Таким образом, способность сорбентов связывать другие вещества стала одной из причин их активного применения в промышленности для фильтрации и очистки различных жидкостей [16].
Поэтому мы выбрали объектом наших исследований ионообменные и адсорбирующие сорбенты для исследования их способности удалять ионы солей из среды как метод снижения засоленности почв.
Модельная система, или Как все началось
Как «представителей» ионообменных сорбентов мы взяли органическую смолу Macro-Prep DEAE (МР) и неорганический минерал гидроксиапатит (HA / [Ca5(PO4)3(OH)2]) [17]. Каждый из них обладает своими уникальными свойствами (особая матрица, полимерная структура, лиганды — не будем останавливаться), важнейшее из которых: независимое от молекулярного веса, заряда или изоэлектрической точки поглощение.
Модельной системой — максимально изученной и упрощенной — был выбран яровой ячмень. Мы подвергли заранее подготовленные семена ячменя 15-дневному засолению в 150 mM NaCl.
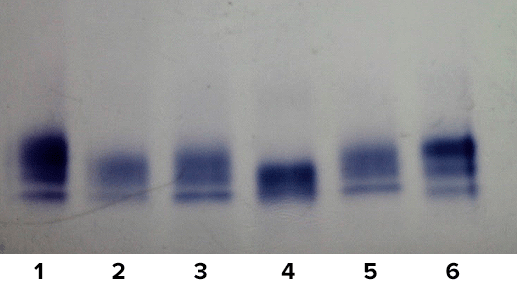
Вот такие результаты мы получили (рис. 9а и 9б):
По фотографиям видно, что образцы, выращенные с использованием сорбентов, практически не отличаются от «нормальных» всходов. Так и есть: образцы, выросшие с сорбентами Macro-Prep DEAE и гидроксиапатитом, незначительно отличаются от здорового растения по своим ростовым параметрам.
Что происходило внутри растений?
После проведения электрофореза в полиакриламидном геле (ПААГ) мы смогли специфически окрасить нужные нам ферменты: альдегидоксидазу и антиоксидантные ферменты.
Мы ожидали очень сильный ответ растения на солевой стресс — развитие окислительного стресса.
Должно было произойти нечто подобное тому, что на рисунке 10.
Рисунок 10. Разрушение клетки под воздействием свободных радикалов (АФК)
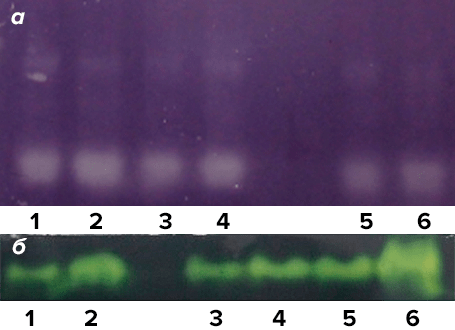
Однако мы получили совершенно противоположный эффект. Все опытные образцы (кроме засоленного) показали минимальное развитие окислительного стресса в клетке (рис. 11 и 12). Это означает, что ферменты-защитники (антиоксиданты) растения в виде каталазы и супероксиддисмутазы смогли выстоять натиск свободных радикалов и противостояли развитию окислительного стресса — спутника солевого (рис.13).
Фермент альдегидоксидаза (голубые полосы) показал умеренную активность, свидетельствуя о поддержании здорового метаболизма. Враг повержен, враг не страшен!
Какой механизм кроется в победе сорбентов над солевым стрессом?
Иониты способны производить ионнообменные реакции как с большими, так и с малыми молекулами. Происходит «товарный обмен» ионами: токсичные ионы Na+ связываются и затормаживаются в сетке сорбентов, взамен безопасные ионы (вид ионов варьирует в зависимости от сорбента: это могут быть, например, K+ и Ca2+) выделяются в среду и не вредят растению. Таким образом, сорбенты блокируют доступ токсичным солям в клетку растения, из-за чего мы наблюдаем минимальное влияние солевого стресса.
Работают ли сорбенты и на обычных овощах?
Да! Мы испытали иониты в аналогичном опыте на овощах разной степени чувствительности: относительно толерантном томате и чувствительной моркови посевной.
Результат оказался практически идентичным с небольшими колебаниями в ростовых показателях (у томата корни длиннее, чем у моркови. Что делать... — особенность вида).
В чем проявляется закон толерантности Шелфорда?
Закон толерантности Шелфорда гласит, что определенный экологический фактор устанавливает границы для развития популяции: процветание в оптимуме, а при избытке или недостатке проявления фактора — упадок в развитии (рис. 14). Мы предположили, что существует некая оптимальная концентрация для ионитов, при значении которых растения будут процветать.
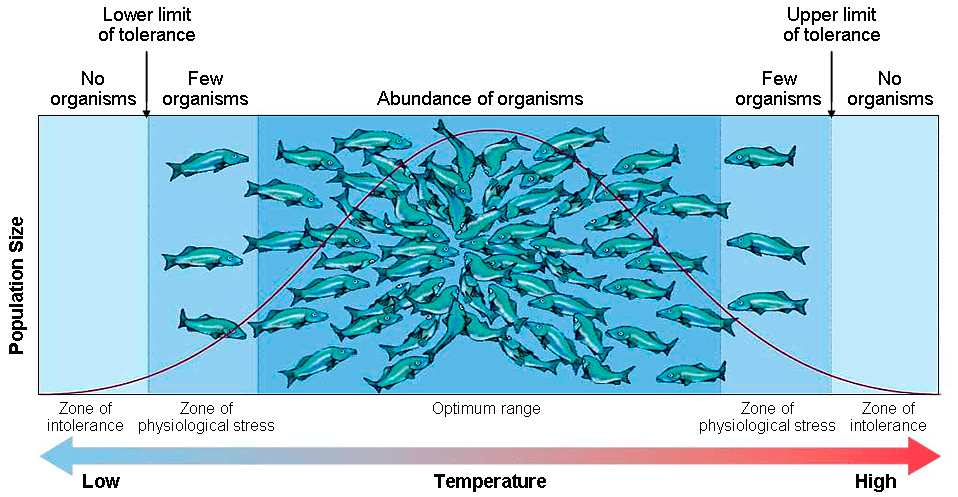
Рисунок 14. Графическое изображение закона толерантности Шелфорда. Количество рыб демонстрируют процветание популяции. Как видно, при оптимальном значении факторов среды (в данном случае температуры), популяция находится в расцвете, при колебаниях в меньшие или большие стороны — уменьшается.
Мы заметили увеличение длины корней и побегов пшеницы при увеличении концентрации сорбентов. Однако это происходило недолго: пик был достигнут в отметке 30%, дальше наступило плато — отсутствие изменений в показателях (рис. 15). Что это значит?
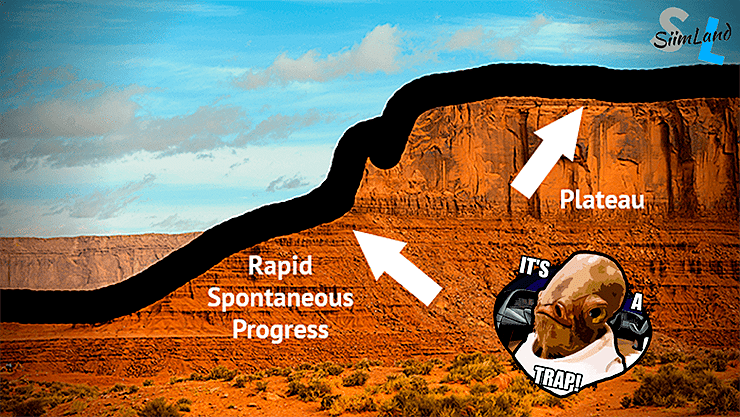
Рисунок 15. Данное природное плато демонстрирует графическое понятие «плато» в зависимости: «увеличения длины побегов от повышения концентрации сорбентов». Как мы видим, был резкий рост, а затем наступила фаза плато — отсутствие изменений. Так как свободные ионы кончились, и больше ничего не угнетало растение.
Существует отметка, при которой максимальное число ионов солей связывается с сайтами обмена в «теле» сорбентов, а значит: нет больше соли — нет угнетения.
С ионитами разобрались — они работают. Как отходы ГРЭС способны помочь деградированным почвам?
После сжигания углей различного происхождения на ГРЭС и ТЭС остается неутилизируемый пылевидный остаток — зола уноса. Зола — неплохое удобрение для растений для получения необходимых микро- и макроэлементов [19]. Также добавление золы есть фактическое добавление мелких дисперсионных частиц в почву (рис. 16).

Рисунок 16. Микрофотография дисперсионных частиц золы уноса
Ученые установили, что зола уноса действует на почву очень благотворно, а именно:
- улучшает текстуру почвы;
- снижает плотность почвы (корням становится легче проникать в более глубокие слои);
- увеличивает водозадерживающую способность почвы;
- оптимизирует кислотность и буферную систему;
- является альтернативой использования известняка и других удобрений;
- способна ингибировать рост и развитие актиномицетов, болезнетворных бактерий и грибков в почве.
Зола с минимальными примесями все же влияет на электропроводимость почвы. Однако эту проблему возможно решить: естественное выщелачивание золы уноса снижает концентрацию в ней растворимых солей и примесей для последующего ее применения в сельском хозяйстве.
Дешево и сердито: и в строй вернули бросовые, деградированные почвы, и справились с отходами производства ГРЭС.
Заключение
Солевой стресс по сей день остается страшной угрозой для многих растений, не успевших приобрести надежные механизмы адаптации к засолению. Однако сорбенты нашли свое новое применение в, казалось бы, далекой области. Ионообменные сорбенты доказали свою эффективность в ликвидации солевого стресса. А использование золы уноса решает сразу две проблемы для экологии: как утилизацию золошлаковых отходов, так и улучшение физического и химико-биологического состояния почвы.
Благодарности
Хотелось бы поблагодарить заведующего, Омарова Рустема Тукеновича, и других сотрудников лаборатории биотехнологии растений ЕНУ им. Л.Н. Гумилева за предоставление собственной лаборатории и реактивов — без них это исследование бы не состоялось. А также моего научного руководителя, Аксенову Инну Валериевну, за искреннюю веру и всестороннюю помощь. Она поддерживала и направляла меня в течение всего пути, не давала опустить руки, первой показала чудеса и красоты науки, показала — что значит быть ученым. И теперь я с уверенностью говорю: наука — это вечность, а мы стоим у ее начала.
Литература
- Боровский В.М. Формирование засоленных почв и галогеохимические провинции Казахстана. Алма-Ата: «Наука», 1982. — 254 с.;
- Удовенко Г.В. (1975). Исследование физиологии устойчивости растений к неблагоприятным условиям среды. «Тр. по прикл. бот., ген. и сел.». 1, 154–161;
- Richards L.A. Origin and nature of saline and alkali soils. In: Diagnosis and Improvement of Saline and Alkali Soils. Washington D.C., 1954. P. 1–6;
- Ashraf M.A., Iqbal M., Rasheed R. et al. Environmental stress and secondary metabolites in plants: an overview. In: Plant Metabolites and Regulation Under Environmental Stress / ed. by P. Ahmad, M.A. Ahanger, V.P. Singh et al. London: Academic Press, 2018. P. 153–167;
- Трухина Ю.О., Шайбе Р., Епринцев А.Т. (2000). Влияние солевого стресса на основные физиолого-биохимические параметры растений картофеля. «Вестник ВГУ. Серия химия, биология». 2, 138–143;
- Битюцкий Н.П. Минеральное питание растений. СПб: Изд. дом С.-Петербургского гос. ун-та, 2014. — 538 с.;
- Franz-Josef Schmitt, Gernot Renger, Thomas Friedrich, Vladimir D. Kreslavski, Sergei K. Zharmukhamedov, et. al.. (2014). Reactive oxygen species: Re-evaluation of generation, monitoring and role in stress-signaling in phototrophic organisms. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1837, 835-848;
- Marschner H. Mineral nutrition of higher plants (2nd Edition). San Diego: Academic Press, 1995;
- Swagat Kumar Das, Jayanta Kumar Patra, Hrudayanath Thatoi. (2016). Antioxidative response to abiotic and biotic stresses in mangrove plants: A review. Internat. Rev. Hydrobiol.. 101, 3-19;
- R. T. Omarov, S. Akaba, T. Koshiba, S. H. Lips. (1999). Aldehyde oxidase in roots, leaves and seeds of barley (Hordeum vulgare L.). Journal of Experimental Botany. 50, 63-69;
- R. T. Omarov, M. Sagi, S. H. Lips. (1998). Regulation of aldehyde oxidase and nitrate reductase in roots of barley (Hordeum vulgare L.) by nitrogen source and salinity. Journal of Experimental Botany. 49, 897-902;
- Карпенко Н.П., Сейтказиев А.С., Маймакова А.К. (2016). Экологическая оценка деградации сероземно-леговых почв Жамбылской области. «Международный научно-исследовательский журнал». 12, 132–135;
- Bansal R.C. and Goyal M. Activated carbon adsorption. Boca Raton: CRC Press, 2005;
- K. Popper, R. J. Bouthilet, V. Slamecka. (1963). Ion-Exchange Removal of Sodium Chloride from Water with Calcium Hydroxide as Recoverable Regenerant. Science. 141, 1038-1039;
- Luong N. Nguyen, Faisal I. Hai, Jinguo Kang, William E. Price, Long D. Nghiem. (2013). Coupling granular activated carbon adsorption with membrane bioreactor treatment for trace organic contaminant removal: Breakthrough behaviour of persistent and hydrophilic compounds. Journal of Environmental Management. 119, 173-181;
- Lygina T.Z., Mikhaiylova O.A., Khatsrinov A.I., Konyukhova T.P. Technology of chemical activation of inorganic natural mineral sorbents: monograph. Kazan: Kazan State Technol. University, 2009. — 120 p.;
- Aziz Fihri, Christophe Len, Rajender S. Varma, Abderrahim Solhy. (2017). Hydroxyapatite: A review of syntheses, structure and applications in heterogeneous catalysis. Coordination Chemistry Reviews. 347, 48-76;
- 12 методов в картинках: очистка молекул и разделение смесей;
- Prem Kishor, A.K. Ghosh, Dileep Kumar. (2010). Use of Flyash in Agriculture: A Way to Improve Soil Fertility and its Productivity. Asian J. of Agricultural Research. 4, 1-14.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚