CAR-NK как новая универсальная альтернатива для CAR-T терапии
02 апреля 2026
CAR-NK как новая универсальная альтернатива для CAR-T терапии
- 278
- 0
- 0
Воздействие NK на раковую клетку.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В современном мире все больше и больше интереса вызывает генная инженерия для лечения рака, то есть болезней, которые основаны на бесконтрольном делении клеток, приводящих к образованию опухолей [1]. Одно из последних решений — CAR-T терапия — генетическая модификация Т-лимфоцитов, превращающая их в метких «снайперов» для раковых клеток [2]. Но каждая опухоль индивидуальна и такая терапия не всегда может быть эффективной, а также имеет большие риски. Поэтому исследователи постоянно ищут новые пути, и один из них — создание нового варианта генной терапии — CAR-NK. В отличие от Т-лимфоцитов NK клеткам не нужно узнавать антиген через антигенпрезентирующие клетки, они реагируют на подозрительные молекулы в мембране клетки. Помимо этого, NK-клетки являются аллогенным продуктом — их можно забирать от здорового донора и вводить пациенту, в отличие от Т-лимфоцитов, которые аутологичны — забираются от пациента, модифицируются и возвращаются ему же. В данной статье рассматривается сравнение обеих терапий, идея CAR-NK и ее перспективы.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Школьная» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — Благотворительный фонд «Белая лилия», который поддерживает школьников, студентов профильных вузов, научных коллективов врачей и ученых по разработке и созданию прорывных технологий в области медицины.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
То, где все начинается
Иммунитет — это свойство организма, при котором обеспечивается сохранение постоянства внутренней среды путем распознавания «своего» и «чужого» благодаря антигенам, которые сохраняются после удаления возбудителей болезни (патогенов) [3]. Антиген — это вещество, которое организм рассматривает как чужеродное или потенциально опасное и против которого активируется иммунный ответ. Благодаря кусочкам антигенов на поверхности патогенов иммунитет определяет агрессора и обеспечивает борьбу с ним. Для слаженной работы клеток против врага нужна система сигналов и тогда на поле выходит новый герой — цитокины — небольшие белковые молекулы, вырабатываемые клетками (например интерлейкины IL-1,2,3 и т. д. В ряд цитокинов входят: хемокины, подающие клетке сигнал о том, куда надо двигаться, факторы роста, помогающие определить какую артиллерию выбрать клетке (например, так появляются гранулоциты и макрофаги) [4]. Еще одним помощником иммунитета являются антенны HLA (человеческий лейкоцитарный антиген — комплекс генов, кодирующий поверхностные белки большинства клеток человека, более современное название MHC) [5]. Находящиеся на поверхности молекулы помогают клеткам распознать своих и чужаков (вирусы, бактерии, раковые клетки) и при необходимости активируют иммунный ответ, благодаря взаимодействию с антиген-распознающим рецептором (TCR) на поверхности Т-хелпера (CD4+).
Иммунитет человека подразделяется на два вида: врожденный и адаптивный. Врожденный обеспечивает быстрый ответ на потенциальные угрозы, но при этом не запоминает чужаков, а одинаково реагирует на все патогены. Адаптивный (приобретенный) требует больше времени на ответ, но при этом он запоминает антигены, с которым сталкивается организм и в будущих встречах с уже знакомыми антигенами способен быстро и эффективно бороться с ними. Подробнее о работе иммунитета можно почитать в «Иммунитет: борьба с чужими и… своими» [4].
Ключевыми клетками иммунитета являются B-лимфоциты, Т-лимфоциты и NK-клетки. Однако в противоопухолевой борьбе наиболее эффективны T-лимфоциты и NK-клетки, происходящие из красного костного мозга. NK-клетки врожденного иммунитета были открыты в середине 1970-х годов, когда исследователи наблюдали лимфоциты, которые могут спонтанно убивать опухолевые клетки без предварительного подготовительного этапа (сенсибилизации). В 1975 году Рольф Кисслинг и его коллеги из Каролинского института определили этот тип клетки как отдельный лимфоцит и назвали его клеткой «естественного убийцы» (натуральные киллеры) [6]. Тем не менее, на протяжении десятилетий основное внимание в борьбе с раком было сосредоточено на Т-лимфоцитах.
Солдаты адаптивного иммунитета
Главной частью армии адаптивного иммунитета являются Т-лимфоциты. Основная функция Т-клеток — это распознавание чужеродных антигенов и активация иммунного ответа. Каждый Т-лимфоцит на своей поверхности имеет Т-клеточный рецептор (TCR), который связывается с антигеном чужака [7]. Но для правильной работы также требуются со-рецепторы — CD4 и CD8 (CD — это «паспорт» на поверхности клетки, по которому она опознается). Эти рецепторы нужны для улучшения взаимодействия Т-клетки и антигена. Важным видом Т-лимфоцитов являются Т-хелперы (CD4+ или Th), которые экспрессируют CD4 на поверхности и руководят другими клетками иммунитета: Т-хелперы замечают антиген, представленный на MHC класса II антигенпрезентирующих клеток и с помощью цитокинов подают сигнал другим клеткам, активируя иммунный ответ [8]. Второй вид клеток — цитотоксические Т-клетки — главное оружие (CD8+ или Т-киллеры), которые экспрессируют CD8 на поверхности и уничтожают патологические клетки: Т-киллеры распознают антигены, представленные на MHC-I, плотно контактируют с мишенью и выпускают цитотоксические гранулы: перфорин — белок, который просверливает отверстия в клетках для их уничтожения и гранзимы, которые входят в клетку и расщепляют ее белки. Таким образом, клетка-мишень умирает [4], [9]. Большинство Т-киллеров также умирают после устранения врага, но те, кто выжил, обретают новую функцию — они переходят в состояние длительной памяти и в будущем, при повторном столкновении с этим патогеном быстро и эффективно реагируют. Но для своей защиты раковые клетки стали «лысеть» — сильно снижать экспрессию MHC-I на своей поверхности, из-за чего становились лысыми (naked cell) и невидимыми для Т-киллеров. Это стимулировало разработку нового терапевтического подхода — CAR-T терапии.
CAR-T терапия
CAR-T терапия (от англ. Chimeric antigen receptor to T-cells) подразумевает собой использование модифицированных клеток пациента, извлеченный с помощью лейкоцитаферез. Полученные клетки изменяют — в них встраивается ген, кодирующий химерный антигенный рецептор (CAR), который узнает специфические белки на опухолевых клетках и активизирует Т-лимфоциты. Далее клетки «размножают» и при достижении нужного количества вводят обратно в организм больного [10]. На «Биомолекуле» уже выходила более подробная статья об этой терапии «Способны ли CAR-Т-клетки уничтожить опухоль?» [11].
Наиболее репрезентативным и успешным примером является терапия Т-клеток CD19 CAR при остром лимфобластном лейкозе B-клеток и неходжкинских лимфомах. CD19 является выгодной мишенью для терапии, так как экспрессируются на поверхности нормальных и злокачественных B-клеток (на ранних и зрелых стадиях), не затрагивая неродственные ткани организма, в результате чего минимизируется повреждение здоровых тканей Т-клеточной терапией [12]. Помимо CD19 для лечения B-клеточных опухолей используют CD20, который экспрессируется на более поздних стадиях B-клеток. После лечения CAR-T-CD20 может начаться рецидив из-за потери экспрессии СD20 на опухолевых клетках (antigen escape), однако экспрессия CD19 сохраняется и CAR-T CD19 становится второй линией атаки опухолевых клеток. Таким образом, CAR-T CD19 стала первой успешной CAR-T терапией, демонстрируя высокие клинические ответы и полные ремиссии [13]. Возвращаясь к обобщенной CAR-T терапии можно выделить серьезные недостатки, из-за которых риск использования терапии возрастает в разы:
-
Ограничение для лечения солидных (уплотненных) опухолей — CAR-T клетки зачастую не могут «просочиться» в опухоль и распознать антиген [14].
-
Цитокиновый шторм и нейротоксичность — значительное выделение цитокинов CAR-Т клетками, которое приводит к нарушению работы иммунитета и повреждению работы центральной нервной системы [15].
Знакомство с киллерами
Не стоит забывать о солдатах врожденного иммунитета — натуральных киллерах. Самые ранние исследования NK-клеток человека и мыши ясно показали, что NK-клетки способны разрушать как сингенные (пересаженные между генетически идентичными особями), так и аллогенные (пересаженные между генетически разными особями) опухоли. То, что NK-клетки преимущественно убивают опухолевые клетки, лишенные MHC класса I, было продемонстрировано Карре путем химической мутагенизации высокозлокачественной лимфомы. Это фундаментальное исследование было революционным и изменило понимание работы иммунитета. Оно раскрыло механизм врожденной иммунной системы, который дополняет функцию CD8+ Т-клеток в борьбе с вирусами и опухолями. Кроме того, оно предсказало существование ингибирующих рецепторов для MHC-I, ответственных за защиту клеток, экспрессирующих собственный MHC-I, от атаки NK-клеток [16].
Продукты киллеров
Одной из функций NK-клеток является выделение цитокинов. Главный продукт киллеров — интерферон гамма (IFN‑γ), который усиливает способность других иммунных клеток бороться с инфекцией. Они стимулируют работу макрофагов — клеток врожденного иммунитета, которые поглощают (фагоцитируют) патоген, увеличивая их способность захватывать и уничтожать микроорганизмы [4]. IFN‑γ также увеличивает экспрессию MHC-молекул на антиген-представляющих клетках, улучшая активацию Т-клеток [17], [18]. Второй продукт киллеров — фактор некроза опухоли-альфа (TNF‑α), который усиливает воспаление для более быстрой реакции иммунной системы на угрозу. Он так же помогает натуральным киллерам в усилении продукции IFN‑γ, при взаимодействии с которым усиливается цитотоксичность NK-клеток [19], [20].
Механизм работы
Большинство здоровых клеток экспрессируют MHC класса I, благодаря своим ингибирующим рецепторам натуральные киллеры распознают MHC-I и не трогают «свои» клетки. Раковые клетки же теряют или уменьшают экспрессию MHC, тогда ингибирующий сигнал ослабевает и киллеры активируются (данный механизм называется missing self т.е. отсутствие своего) [21]. Основные семейства ингибирующих рецепторов: KIR (иммуноглобулиноподобные рецепторы) и CD94/NKG2A распознающие нетипичную молекулу главного комплекса гистосовместимости HLA-E [22]. Помимо этого NK-клетки так же несут активирующие рецепторы, которые распознают стресс-лиганды, появляющиеся на клетке-мишени при стрессовом состоянии, инфекции или опухолевых трансформациях. Главным активирующим рецептором является NKG2D, который распознает лиганды MICA, MICB, ULBP1-6 [23]. Если активирующие превышают ингибирующие, то натуральные киллеры запускают эффекторные функции.
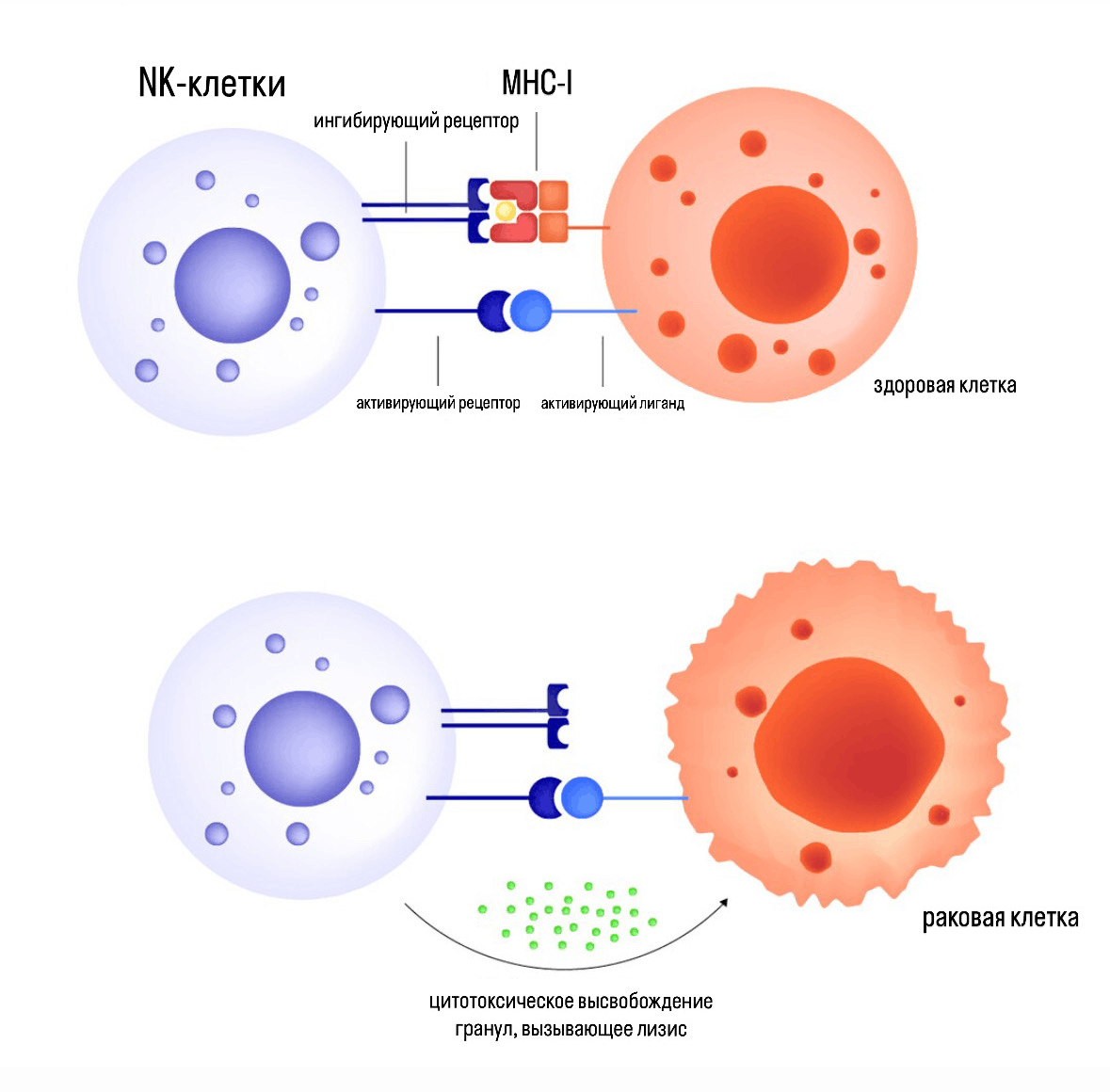
Рисунок 1. Механизм уничтожения раковой клетки.
Распознавание «хорошей» и «плохой» клетки происходит благодаря иммунологическому синапсу — тесному контакту киллеров с клетками-мишенями. На этом этапе происходит сканирование клетки: ингибирующие рецепторы ищут MHC-I, если его нет, то активирующие рецепторы находят стресс-лиганды, после этого сигналы суммируются, и киллеры убивают клетку-мишень направляя свои гранулы в зону контакта, в результате чего выделяется перфорин и гранзимы, которые запускают уничтожение клетки. Таким образом, клетка-мишень умирает. Если ингибирующие рецепторы распознали MHC-I, то они сигнализируют об этом, киллеры отсоединяются от клетки и уходят, не убивая ее. Причем, если есть слабый активирующий сигнал и MHC-I, то киллеры не будут убивать клетку, т. к. ингибирующие сигналы превышают активирующие [25], [26]. Но раковые клетки стараются обходить NKG2D. Они снижают экспрессию лигандов или выделяют их в растворимой форме, чтобы ослепить киллеров и сбить их с правильного пути. Варианты игры в прятки представлены ниже в таблице:
|
Механизм |
Что делает |
Результат |
|---|---|---|
|
Выключение генов [27] |
Подавляет транскрипцию генов, кодирующих лиганды («выключение» генов, которые кодируют MICA/B, ULBP1-6) |
Синтез лиганд замедляется |
|
Шеддинг [28] |
Мембранные металлопротеины ADAM10, ADAM17 расщепляют стресс-лиганды. В результате образуются растворимые формы, которые связывают NKG2D в плазме и вызывают деградацию на поверхности NK-клеток, из-за чего рецептор становится неактивным. |
Растворимые формы стресс-лиганд блокируют NKG2D |
|
Регуляция через экзосомы [29] |
Раковые клетки выделяют экзосомы (маленькие внеклеточные пузырьки), которые содержат стресс-лиганды. Экзосомы взаимодействуют с NKG2D на киллерах и приводят к потере рецепторов с поверхности, либо к потере чувствительности |
Смертельная атака NKG2D с помощью экзосом |
|
Подавление иммунного микроокружения [30] |
Такие сигнальные молекулы как IL-10 подавляют функциональную деятельность NKG2D, а также подавляют экспрессию цитокинов — IFN-γ, TNF-α, которые активируют киллеров [31] |
Потеря цитотоксичности |
|
Альтернативный сплайсинг [32] |
Опухоли экспрессируют усеченные формы MICA, MICAB, которые не транспортируются на мембрану, а остаются в эндоплазматической сети, т.е. внтури клетки. Из-за этого натуральные киллеры не могут их увидеть |
Лиганды не попадают на поверхность клетки, из-за чего остаются незамеченными |
Помимо гранулярной цитотоксичности натуральные киллеры обладают еще двумя механизмами уничтожения клеток:
-
Антиген-зависимая клеточно-опосредованная цитотоксичность (ADCC). B-клетки адаптивной иммунной системы вырабатывают антитела против антигена на клетке-мишени. Происходит опсонизация — антитела маркируют эту клетку, готовят ее для клеток иммунной системы.
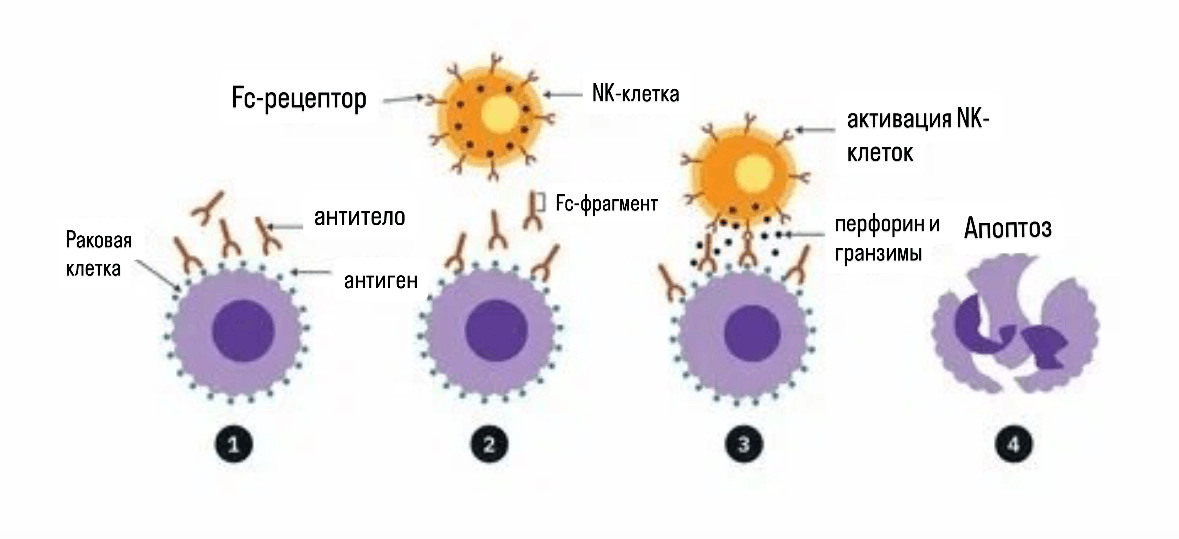
Рисунок 2. Антиген-зависимая клеточно-опосредованная цитотоксичность (ADCC).
NK-клетки имеют на своей поверхности хвостовую часть (Fc-) рецептора CD16, благодаря которому распознается Fc-часть антитела. При связывании CD16 и антитела активируются натуральные киллеры, которые дегранулируют и выделяют перфорин и гранзимы, убивая отмеченную антителами клетку [34]. Увы, CD16 не идеален и хоть он действует мощно, но коротко. После активации рецептор значительно уменьшается на поверхности NK-клеток, так как ADAM17 — основная металлопротеиназа, возбуждает протеолитическое отщепление (расщепление белков, шеддинг) и тем самым уменьшает способность клеток-киллеров выполнять повторные ADCC циклы [24], [35]. Назревает вопрос, почему же нельзя отключить ADAM17? По экспериментам ранние ингибиторы приводили к побочным эффектам (гепатотоксичности, нарушению регенерации) и не прошли дальше, либо были ограничены. Также трудно создать ингибитор, который будет блокировать именно CD16 расщепление без обработки других жизненно важных молекул [35–37]. Как обойти проблему?
-
ex vivo обработка NK-клеток: кратковременное ингибирование ADAM17 при подготовке или активации NK-клеток перед инфузией дает устойчивую повышенную экспрессию CD16 у вводимых клеток, но без системной блокировки у пациента, что снижает риск побочных эффектов.
-
Создание CD16 вариантов с высокой аффинностью и устойчивостью к протеолизу, что позволяет клеткам-киллерам оставаться сильнее к шеддингу и сохранять свою ADCC на более долгий период.
-
Создание моноклональных антител, которые будут блокировать шеддинг. Недавняя работа описала, что антитело F9H4 ингибирует отщепление CD16 и усиливает цикл ADCC в моделях рака легкого в сочетании с «Цетуксимабом» [38–40].
-
-
Убийство клеток-мишеней через лиганд-опосредованные рецепторы смерти. На вражеских клетках есть рецепторы смерти: Fas (CD95) и DR4/DR5, которые распознаются мембранными белками NK-клеток FasL и TRAIL соответственно. При связывании белков и рецепторов смерти запускает сигнальный комплекс, инициирующий гибель (DISC), который ведет к экстремальному (extrinsic) пути апоптоза — саморазрушения клеток, благодаря активации каспазы-8 (фермента, расщепляющий молекулы внутри клетки). Такой способ убийства актуален, когда гранулярный путь, после многократных атак, истощился. [41]
Хоть киллеры и сильные, но они не всегда способны эффективно и предсказуемо уничтожать опухолевые клетки. Чтобы улучшить эффективность клеток их генетически модифицируют с помощью CAR.
Механизм CAR-NK
Наращивание искусственного антиген рецептора (CAR) нужно для более специфичного распознавания антигенов на поверхности раковых клеток. CAR состоит из трех частей:
-
Внеклеточного домена (scFv) распознавания, который связывается с определенным антигеном опухолевой клетки.
-
Трансмембранного домена — фиксирует CAR в мембране киллера и обеспечивает подачу сигнала внутрь.
-
Внутриклеточного сигнального домена (CD3ζ, DAP10, DAP12), который запускает сигнальные каскады, приводящие к активации киллеров и выделению цитокинов. [42]
При связывании scFV с антигеном опухоли вызывается кластеризация CAR: аминокислоты (ITAM) внутриклеточного сигнального домена активируются и с помощью ферментов «отмечаются» (фосфорилируются). Белок-фермент Syk получает сигнал от ITAM и передает его дальше по цепочке к белкам: Vav1 — активирует внутренний скелет клетки, Erk — передает сигнал в ядро клетки, NF-кB — заходит в ядро и «включает» нужные гены, заставляя натуральных киллеров производить цитокины [43]. Таким образом, наличие CAR на поверхности NK-клетки приводит к распознаванию конкретного антигена опухоли, прямому включению цитотоксичных механизмов и позволяет киллерам сохранять свои нативные механизмы распознавания антигена, делая их двухцепочечными убийцами [44].
CAR-NK в практике
Так как наиболее успешный результат среди CAR-T терапии является CD19CAR-T, то предлагаю на этом же примере (CD19) рассмотреть работу терапии натуральных киллеров. В процессе сводили HLA-несоответствующие анти-CD19 CAR-NK клетки, полученные из пуповинной крови, одиннадцати пациентам с рецидивирующим или рефрактерным CD19 раком. Клетки размножали ex vivo и вводили в виде однократной инфузии в трех дозах: (1×105, 1×106, или 1×107 CAR-NK на кг массы тела) . После инфузии NK-клетками не было никаких побочных эффектов (в том числе нейротоксичности, цитотоксического шторма и реакции клеток против хозяина). По сравнению с начальными данными, до инфузии, количества воспалительных цитокинов и IL-6 после введения клеток не повышались. Из 11 пациентов у 8 (73%) был положительный результат — семь пациентов ушли в полную ремиссию, а у одного появилась ремиссия компонента трансформации Рихтера, то есть остановился переход хронического лимфоцитарного лейкоза (ХЛЛ) в более агрессивную форму, но сама болезнь ХЛЛ сохранилась. Реакция на клетки была быстрой — в течение 30 дней после инфузии, введенные CAR-NK размножались и сохранялись на низком уровне как минимум 12 месяцев.
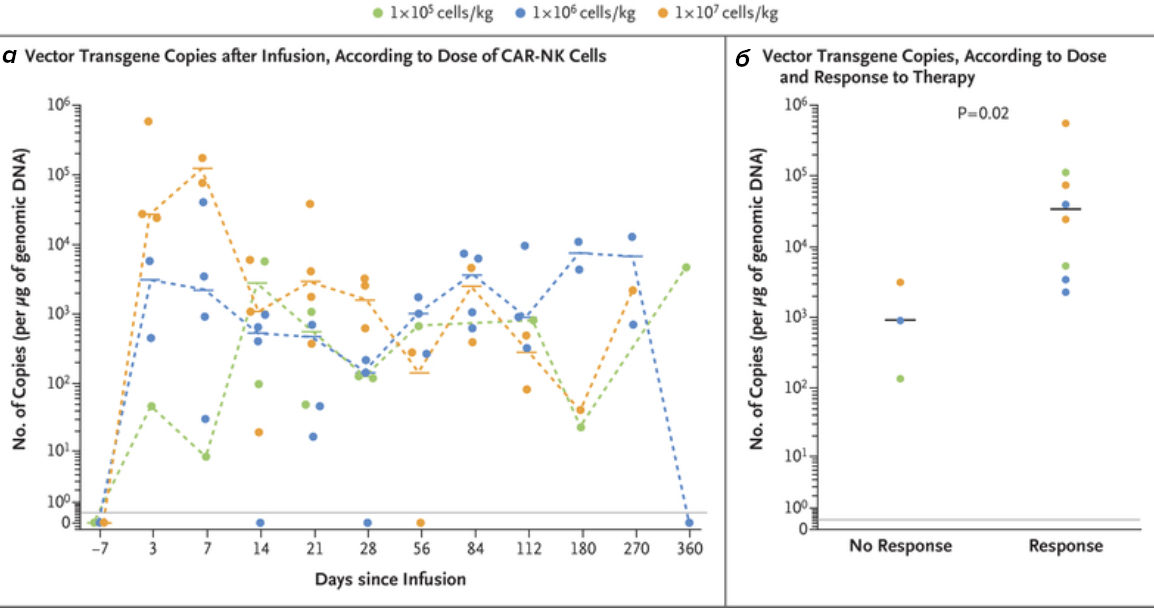
Рисунок 3. Сохранение NK-клеток после инфузии. График а — показатели содержания CAR-NK клеток в периферической крови после инфузий разными дозами. Показатели количества клеток оставались определяемыми в течение года после введения, независимо от дозы. После 14 дня количество клеток не зависело от первоначальной дозы, что говорит о самостоятельном размножении NK-клеток внутри организма. На графике б — максимальное количество клеток на 28 день после инфузии. Пациенты, у которых ответ наблюдался на 30 день имели более высокий пик количества NK-клеток, чем те, у кого ответа не было.
Memory-like NK
Так как классические NK-клетки относятся к врожденному иммунитету, то они не формируют длительную иммунную память. Тогда начали разрабатывать memory-like клетки, которые после предварительного воздействия цитокинов или антигенов сохраняют усиленную функциональность на длительное время. Они демонстрируют повышенную цитотоксичность даже спустя несколько недель, в отличие от оригинальных NK-клеток. Создание memory-like клеток:
-
Кратковременная обработка NK-клеток комбинацией IL-2,15,18. После этого они становятся «обученными» — сохраняют повышенную продукцию IFN и способность уничтожать опухолевые клетки.
-
Экспозиция NK-клеток на определенные опухолевые антигены может формировать специфический memory-like фенотип, что создает селективно активированные клетки-киллеры, которые при повторной встрече с этой же опухолью отвечают быстрее и сильнее.
-
С помощью генной модификации исследуются подходы для усиления памяти NK-клеток, которые будут дольше сохранять свою активность [46], [47].
Перспективы и трудности CAR-NK
Одним из главных минусов CAR-NK клеток является низкая продолжительность жизни — всего несколько недель, в отличие от CAR-T, которые живут десятилетиями. Однако как говорилось ранее, сейчас разрабатывают memory-like NK и, возможно, в будущем это уже не будет проблемой. Также CAR-NK плохо поддаются хранению и заморозке, что усложняет процесс транспортировки терапии до пациента [44].
Однако доклинические и клинические исследования показали, что CAR-NK лишены многих недостатков CAR-T т. к. у них нет Т-клеточного рецептора и это дает им преимущества: не вызывает реакцию «трансплантат против хозяина» (отторжение клеток) и аллогенность [48]. Помимо этого, CAR-NK не вызывают цитокиновый шторм и нейротоксичность, а также в доклинические исследования показали эффективность против солидных опухолей [49]. Также киллеров можно использовать вместе с антителами, чтобы создавать антителозависимый клеточный механизм, при котором CD16 связывается с Fc-фрагментом антител, усиливая уничтожение опухолей [34].
Благодаря прогрессу технологий, маркировки HLA-рецепторов и отсутствию контаминации можно организовать масштабное и безопасное производство CAR-NK терапии [22].
На данном этапе CAR-NK показывает хорошие перспективы и, возможно, в будущем, после многих исследований смогут обойти CAR-T и занять достойное место в противоопухолевой терапии.
Литература
- «Википедия»: Злокачественная опухоль;
- CAR-T-терапия: плюсы и минусы. (2024). ФГБУ «НМИЦ Гематологии» Минздрава России;
- Козыро И.А., Батян Г.М., Сукало А.В. Клиническая иммунология в практике врача педиатра. Минск: БГМУ, 2011. — 41 с.;
- Иммунитет: борьба с чужими и… своими;
- Что такое HLA? (2025). «Лаборатории ЦИР»;
- Lewis L. Lanier. (2024). Five decades of natural killer cell discovery. Journal of Experimental Medicine. 221;
- Будчанов Ю.И. Главный комплекс гистосовместимости. Тверь: Тверская государственная медицинская академия, 2008. — 9 с.;
- CD4 and CD8: Differences, Functions, and Roles in Immunity. (2025). GNA;
- Wissinger E. (2025). Cells T CD8+. British Society for Immunology;
- Хужина Я. (2025). Превратить свои клетки в оружие: как работает CAR-T-терапия рака? интервью с иммунологом Аполлинарией Боголюбовой-Кузнецовой. «Научная Россия»;
- Способны ли CAR-Т-клетки уничтожить опухоль?;
- Robert H. Carter, Douglas T. Fearon. (1992). CD19: Lowering the Threshold for Antigen Receptor Stimulation of B Lymphocytes. Science. 256, 105–107;
- Johannes Duell, Alexander M. Leipold, Silke Appenzeller, Viktoria Fuhr, Hilka Rauert-Wunderlich, et. al. (2024). Sequential antigen loss and branching evolution in lymphoma after CD19- and CD20-targeted T-cell–redirecting therapy. Blood. 143, 685–696;
- Öykü Umut, Adrian Gottschlich, Stefan Endres, Sebastian Kobold. (2021). CAR T cell therapy in solid tumors: a short review. memo. 14, 143–149;
- CAR T-cell Therapy and Its Side Effects. (2025). American Cancer Society;
- Anthony J. Sadler, Bryan R. G. Williams. (2008). Interferon-inducible antiviral effectors. Nat Rev Immunol. 8, 559–568;
- Romina S. Goldszmid, Pat Caspar, Aymeric Rivollier, Sandy White, Amiran Dzutsev, et. al. (2012). NK Cell-Derived Interferon-γ Orchestrates Cellular Dynamics and the Differentiation of Monocytes into Dendritic Cells at the Site of Infection. Immunity. 36, 1047–1059;
- T V Sologub, V V Tsvetkov, E G Deeva. (2014). Interferon Gamma-Cytokine with Antiviral, Immunomodulatory and Antitumor Action. I.P. Pavlov Russian Medical Biological Herald. 22, 56–60;
- Wagdi Almishri, Tania Santodomingo-Garzon, Tyson Le, Danuta Stack, Christopher H. Mody, Mark G. Swain. (2016). TNFα Augments Cytokine-Induced NK Cell IFNγ Production through TNFR2. J Innate Immun. 8, 617–629;
- Eissmann P. (2025). Natural Killer Cells. British Society for Immunology;
- «Википедия»: Killer-cell immunoglobulin-like receptor;
- A.G. Brooks, F. Borrego, P.E. Posch, A. Patamawenu, C.J. Scorzelli, M. Ulbrecht, et al. (1999). Specific recognition of HLA-E, but not classical, HLA class I molecules by soluble CD94/NKG2A and NK cells. Journal of immunology (Baltimore, Md. : 1950). 162, 305–313;
- Естественные киллеры. (2025). РУВИКИ;
- Loïs Coënon, Martin Villalba. (2022). From CD16a Biology to Antibody-Dependent Cell-Mediated Cytotoxicity Improvement. Front. Immunol. 13;
- Natural Killer Cells Overview. (2025). Thermo Fisher Scientific Inc.;
- Sourav Paul, Girdhari Lal. (2017). The Molecular Mechanism of Natural Killer Cells Function and Its Importance in Cancer Immunotherapy. Front. Immunol. 8;
- Shixin Duan, Weihua Guo, Zuxing Xu, Yunbo He, Chuting Liang, et. al. (2019). Natural killer group 2D receptor and its ligands in cancer immune escape. Mol Cancer. 18;
- Michael A. Brehm, Amelia K. Pinto, Keith A. Daniels, Jonathan P. Schneck, Raymond M. Welsh, Liisa K. Selin. (2002). T cell immunodominance and maintenance of memory regulated by unexpectedly cross-reactive pathogens. Nat Immunol. 3, 627–634;
- Anna Gieras, Petra Cejka, Katharina Blatt, Margarete Focke-Tejkl, Birgit Linhart, et. al. (2011). Mapping of Conformational IgE Epitopes with Peptide-Specific Monoclonal Antibodies Reveals Simultaneous Binding of Different IgE Antibodies to a Surface Patch on the Major Birch Pollen Allergen, Bet v 1. The Journal of Immunology. 186, 5333–5344;
- Renato Zambello, Michela Falco, Mariella Della Chiesa, Livio Trentin, Davide Carollo, et. al. (2003). Expression and function of KIR and natural cytotoxicity receptors in NK-type lymphoproliferative diseases of granular lymphocytes. Blood. 102, 1797–1805;
- David E. Ochayon, Stephen N. Waggoner. (2021). The Effect of Unconventional Cytokine Combinations on NK-Cell Responses to Viral Infection. Front. Immunol. 12;
- Won Jin Lee, Mark P. Purdue, Patricia Stewart, Maryjean Schenk, Anneclaire J. De Roos, et. al. (2006). Asthma history, occupational exposure to pesticides and the risk of non‐Hodgkin's lymphoma. Intl Journal of Cancer. 118, 3174–3176;
- Define Antibody-Dependent Cell Cytotoxicity. (2024). Mason Mullan blog;
- «Википедия»: Antibody opsonization;
- Jianming Wu, Hemant K Mishra, Bruce Walcheck. (2019). Role of ADAM17 as a regulatory checkpoint of CD16A in NK cells and as a potential target for cancer immunotherapy. Journal of Leukocyte Biology. 105, 1297–1303;
- Margherita Sisto, Sabrina Lisi. (2024). Updates on Inflammatory Molecular Pathways Mediated by ADAM17 in Autoimmunity. Cells. 13, 2092;
- Anna M. Knapinska, Daniela Dreymuller, Andreas Ludwig, Lyndsay Smith, Vladislav Golubkov, et. al. (2015). SAR Studies of Exosite-Binding Substrate-Selective Inhibitors of A Disintegrin And Metalloprotease 17 (ADAM17) and Application as Selective in Vitro Probes. J. Med. Chem. 58, 5808–5824;
- Emily J. Pomeroy, John T. Hunzeker, Mitchell G. Kluesner, Walker S. Lahr, Branden A. Smeester, et. al. (2020). A Genetically Engineered Primary Human Natural Killer Cell Platform for Cancer Immunotherapy. Molecular Therapy. 28, 52–63;
- Xuan Guo, Srinivas Somanchi, Rohit Mathur, Shuyang He, Qian Ye, et. al. (2019). Engineering High Affinity and Cleavage Resistant CD16 to Augment ADCC of Placental Hematopoietic Stem Cells-Derived Natural Killer Cells. Blood. 134, 1576–1576;
- Bruna Taciane da Silva Bortoleti, Sophia Quasem, Stefanie Maurer, Xiaoxuan Zhong, Ruan Pimenta, et. al. (2025). A monoclonal antibody that inhibits the shedding of CD16a and CD16b and promotes antibody-dependent cellular cytotoxicity against tumors. Nat Commun. 16;
- Christian Sordo-Bahamonde, Seila Lorenzo-Herrero, Ángel R. Payer, Segundo Gonzalez, Alejandro López-Soto. (2020). Mechanisms of Apoptosis Resistance to NK Cell-Mediated Cytotoxicity in Cancer. IJMS. 21, 3726;
- Natalie K. Wolf, Djem U. Kissiov, David H. Raulet. (2023). Roles of natural killer cells in immunity to cancer, and applications to immunotherapy. Nat Rev Immunol. 23, 90–105;
- Yingying Chen, Dan Lu, Alexey Churov, Rong Fu. (2020). Research Progress on NK Cell Receptors and Their Signaling Pathways. Mediators of Inflammation. 2020, 1–14;
- Hamidreza Ebrahimiyan, Amirhossein Tamimi, Bahareh Shokoohian, Neda Minaei, Arash Memarnejadian, et. al. (2022). Novel insights in CAR-NK cells beyond CAR-T cell technology; promising advantages. International Immunopharmacology. 106, 108587;
- Enli Liu, David Marin, Pinaki Banerjee, Homer A. Macapinlac, Philip Thompson, et. al. (2020). Use of CAR-Transduced Natural Killer Cells in CD19-Positive Lymphoid Tumors. N Engl J Med. 382, 545–553;
- Guangyu Lian, Thomas Shiu-Kwong Mak, Xueqing Yu, Hui-Yao Lan. (2021). Challenges and Recent Advances in NK Cell-Targeted Immunotherapies in Solid Tumors. IJMS. 23, 164;
- Pengchao Zhang, Guizhong Zhang, Xiaochun Wan. (2023). Challenges and new technologies in adoptive cell therapy. J Hematol Oncol. 16;
- Jeffrey S. Miller, Yvette Soignier, Angela Panoskaltsis-Mortari, Sarah A. McNearney, Gong H. Yun, et. al. (2005). Successful adoptive transfer and in vivo expansion of human haploidentical NK cells in patients with cancer. Blood. 105, 3051–3057;
- Ewa Wrona, Maciej Borowiec, Piotr Potemski. (2021). CAR-NK Cells in the Treatment of Solid Tumors. IJMS. 22, 5899;
- Прирожденные убийцы: NK-клеточная терапия.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚