Иллюзия уверенности
19 декабря 2017
Иллюзия уверенности
- 16399
- 0
- 2
сайт gomerblog.com
-
Автор
-
Редактор
Вопрос об эффективности ингибиторов нейраминидазы до сих пор не имеет внятного ответа, несмотря на то, что эти препараты — чуть ли не единственная зарекомендовавшая себя сегодня эффективная терапия для больных гриппом. Тем не менее научная журналистика относится к данному факту весьма скептически: все ждут новых исследований, однако, на мой взгляд, даже «старых» вполне достаточно, чтобы усомниться в общепринятой точке зрения.
Нейраминидаза — один из ключевых ферментов, участвующих в репликации вирусов гриппа типов А и В (рис. 1) [1], [2]. Ингибиторы нейраминидазы, как утверждают производители, пресекают возможность проникновения этих вирусов в здоровые клетки, тормозят их выход из инфицированной клетки и снижают устойчивость к инактивирующему действию слизистого секрета дыхательных путей, содержащего иммуноглобулин А (IgA) [3]. Cуществует несколько веществ, обладающих подобными свойствами: осельтамивир («Тамифлю»), занамивир («Реленза»), перамивир и ланинамивир. Если доверять лабораторным тестам, то применение этих препаратов на ранней стадии заболевания должно как минимум сократить время течения болезни и снизить процент осложнений. Однако выводы многих исследований не столь оптимистичны.
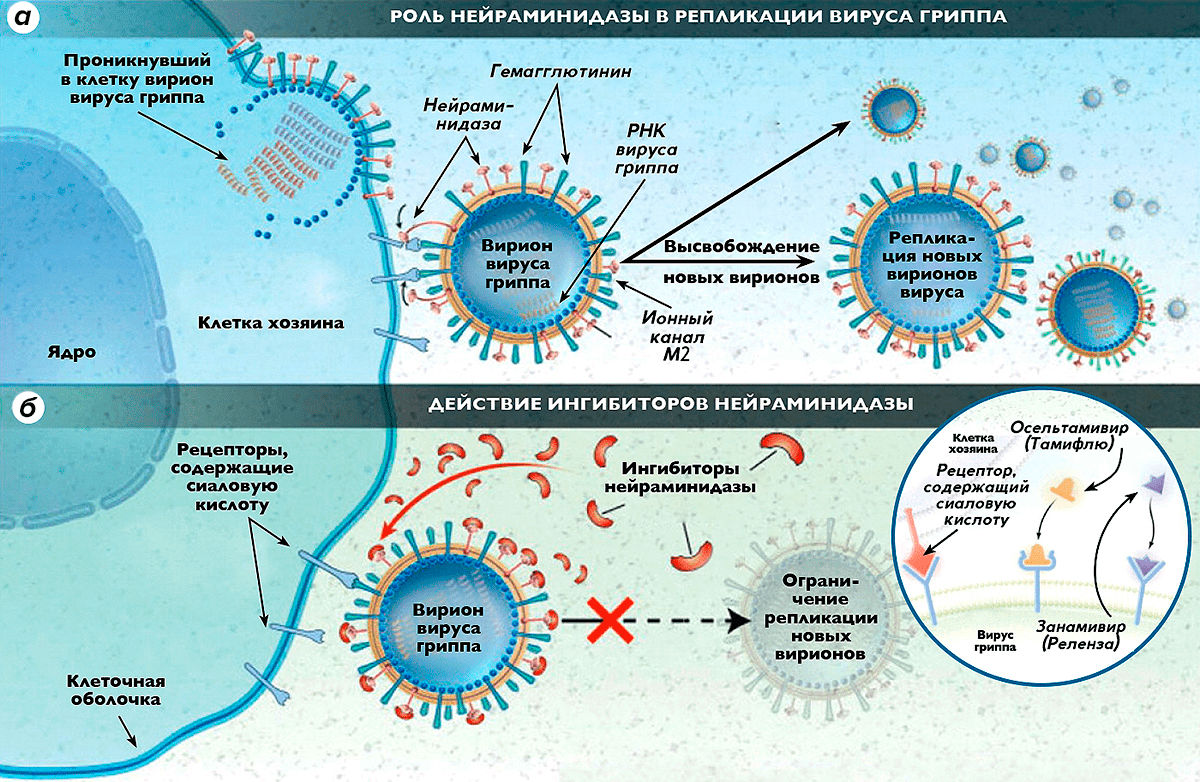
Рисунок 1. Роль нейраминидазы в репликации вируса гриппа и действие ингибиторов нейраминидазы. а — В наружной липидной оболочке вириона вируса гриппа типа А имеются 3 основных белка (гемагглютинин, нейраминидаза и ионный канал М2), играющих основную роль в инфекционном процессе. Шипчики гемагглютинина объединяются с рецепторами восприимчивой клетки хозяина, связываясь с сиаловой кислотой, входящей в состав этих рецепторов. Нейраминидаза отщепляет концевые группы клеточных рецепторов, содержащих сиаловую кислоту, в результате чего клетка теряет способность распознавать антиген, и вирус проникает внутрь нее. Далее в клетке хозяина происходит сборка новых вирионов вируса, которые при помощи нейраминидазы выходят из поврежденной клетки, разносясь с кровотоком и заражая новые клетки. б — Ингибиторы нейраминидазы нарушают способность вирусов гриппа проникать в здоровые клетки, блокируют действие нейраминидазы внутри клетки хозяина, делая невозможным высвобождение из нее новых поколений вирионов вируса гриппа и, соответственно, препятствуя заражению новых клеток.
[2], рисунок адаптирован
Каковы альтернативы?
Исследования этих препаратов делятся на два лагеря: доказавшие эффективность и доказавшие бесполезность. И тех, и других немало. Например, компания Roche — производитель всемирно известного противовирусного препарата «Тамифлю» (осельтамивир) — имеет в своем распоряжении более 70 (спонсируемых ей) клинических испытаний осельтамивира, доказавших его эффективность. Одно из них — рандомизированное контролируемое исследование 2000 года [4] — показало, что ранний прием этого препарата (в течение 36 часов после начала заболевания) способствовал сокращению длительности болезни в среднем на 30%, а степени тяжести — на 38%. Мало того, авторы заключили, что лечение осельтамивиром также будет уменьшать и частоту вторичных осложнений. А между тем уже в 1999 году было известно, что он «снижает длительность гриппозных заболеваний в среднем на 1,3 дня», и директор отдела противовирусных препаратов Управления по санитарному надзору за продуктами и лекарственными средствами США (FDA), доктор Хайди М. Джолсон, описывала его эффективность как весьма «скромную» [5]. Тем не менее осельтамивир не только получил одобрение FDA, но и был внесен ВОЗ сначала в список рекомендованных препаратов, а в 2010 году получил статус «жизненно важного лекарства» [6]. Правда, в 2017 году эксперты ВОЗ перенесли его из основного списка в дополнительный, рекомендовав только для госпитализированных пациентов с тяжелым течением гриппа [7], однако этот факт не умаляет признания его терапевтических свойств.
Обычно цитируют только эту строчку, однако далее в документе доктор Джолсон выражает уверенность, что «сокращение среднетяжелой и тяжелой симптоматики заболевания, включая лихорадку, даже на 1 день может иметь значительную клиническую пользу для многих пациентов. (...) А в случаях тяжелого течения болезни, которые требуют более серьезной терапии, нежели стандартные методы, одобрение осельтамивира даст больному возможность получить эффективное и безопасное лечение» [5].
Разумеется, ингибиторы нейраминидазы — не единственное, что медицина может противопоставить вирусу гриппа. Хотя пока именно они играют решающую роль в терапии, ведь по большому счету «существуют всего два средства, способные смягчить влияние гриппа на население: вакцинация и противовирусные препараты. Вполне вероятно, что при пандемической угрозе, последние будут главным оружием в течение всего периода до момента получения вакцины (ее разработка занимает несколько месяцев — прим. автора). Кроме того, в ситуации, когда штамм циркулирующего вируса отличается от вакцинного, именно противовирусные будут одним из основных средств снижения заболеваемости гриппом», — уверен директор Национального института медицинских исследований ВОЗ (NIMR) Джон Макколи [8].
Тем не менее, кроме ингибиторов нейраминидазы, существуют и другие медикаменты: ингибиторы ионного канала М2 — римантадин и амантадин, — которые еще 15 лет назад широко применяли против вирусов гриппа типа А (тип В не имеет канала М2). Однако сейчас они малоэффективны, так как вследствие широкомасштабного использования (особенно в Китае и России, в том числе в сельском хозяйстве) вирус гриппа развил к ним высокую устойчивость [3], [9]. Кроме того, перспективными считают препараты, воздействующие на гемагглютинин — особый белок, помогающий вирусу гриппа прикрепиться к рецепторам клетки человека [10]. Между прочим, к числу подобных лекарственных средств принадлежит и российский умифеновир («Арбидол»), механизм действия которого сейчас изучают в США [11]. Возможно, эти препараты в ближайшие годы затмят славу ингибиторов нейраминидазы.
Что касается прививок, то в виду высокой антигенной изменчивости циркулирующих штаммов вируса гриппа их эффективность меняется год от года. Например, по промежуточной оценке американских Центров по контролю и профилактике заболеваний (СDC), в США общая эффективность вакцины против гриппа зимой 2016–2017 составила 48%, при этом «вакцинация почти вдвое снизила риск обращения за амбулаторной медицинской помощью» [12].
Эффективно? Нет?
До сих пор ингибиторы нейраминидазы принято считать препаратами с недоказанной эффективностью, обладающими к тому же выраженными побочными эффектами, и многие адепты доказательной медицины уверены в их полной бесполезности. Доказательством этой точки зрения обычно служат выводы метаанализа независимой исследовательской организации Cochrane (бывшая The Cochrane Collaboration). Однако — и это самое странное — именно они окончательно запутывают дело.
Эксперты из Cochrane анализировали ингибиторы нейраминидазы несколько раз (рис. 2), и до 2009 года их отчеты практически ничем не отличались от официальных выводов и информации Roche. Однако в 2009 году грянул гром: японский педиатр Кейдзи Хаяси усомнился в качестве их данных и провел собственное расследование.
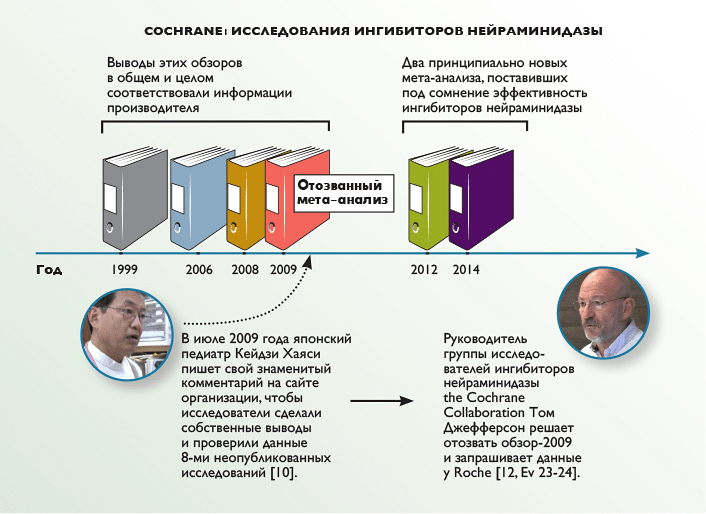
Рисунок 2. Cochrane: исследования ингибиторов нейраминидазы.
Он обнаружил, что выводы об эффективности осельтамивира сделаны на основании десяти исследований, проанализированных профессором Лоурентом Кайзером, которого спонсировал никто иной, как Roche, и лишь два из них были опубликованы в научных журналах (JAMA и The Lancet), остальные восемь видели, наверное, только Кайзер и его коллеги [13], [14]. Тогда под нажимом обвинений в некомпетентности, эксперты из Cochrane были вынуждены отозвать свой обзор-2009 и пообещали заново проанализировать все доступные данные по препаратам, после чего в апреле 2014 года опубликовали сенсационные выводы об их неэффективности: «Оба препарата сокращали продолжительность симптомов гриппоподобного заболевания менее чем на день. Лечение при помощи „Тамифлю“ (осельтамивир) не влияло на количество госпитализаций», тем не менее «достоверные выводы относительно влияния на осложнения, основываясь на данных отчетов, сделать невозможно» . Мало того, исследователи обратили общественное внимание на токсичность «Тамифлю» (повышенный риск тошноты, рвоты, а также головных болей и психических расстройств), и в качестве заключительного аккорда усомнились в необходимости плановых стоковых закупок ингибиторов нейраминидазы, которые проводили правительства США, Великобритании и еще некоторых государств. Также они «не поддерживают присутствие осельтамивира в списке ВОЗ жизненно важных препаратов» [15].
Treatment trials with oseltamivir or zanamivir do not settle the question of whether the complications of influenza (such as pneumonia) are reduced, because of a lack of diagnostic definitions [15]. Мало того, в конце они замечают, что «если предполагать уровень заболеваемости гриппом в 2% (аналогичный тому, который был отмечен в группах, принимавших осельтамивир), для выявления 25-процентного клинически значимого сокращения пневмонии необходимо было исследовать 21 500 участников» [15]. При этом в исследованиях осельтамивира, включенных в обзор, участвовало всего 9623 пациента.
Забегая вперед, скажу, что эксперты из Cochrane, действительно, постарались сделать все возможное, чтобы в конце концов написать качественный отчет (который, кстати, в прессе поторопились окрестить самым «надежным и всеобъемлющим исследованием» противовирусных), но факт в том, что подходящего для анализа материала было недостаточно, и его качество (даже после строгого отбора) оставляло желать лучшего.
Тогда, в 2009 году, пообещав детально разобраться в ситуации, руководитель исследовательской группы ингибиторов нейраминидазы Cochrane — эпидемиолог Том Джефферсон поднял опубликованные материалы и с удивлением обнаружил, что оригиналы данных придется искать в архивах производителя. Тогда он обратился к Roche с просьбой предоставить необходимые материалы. Концерн долго артачился и даже предлагал Джефферсону подписать соглашение о неразглашении (тот, естественно, отказался), но в конце концов уступил и выслал семь небольших документов.
Однако к этому времени исследователи уже успели обнаружить, что существует 123 испытания осельтамивира, при этом 74 из них были в той или иной мере контролируемы производителем, а 23 вообще оказались неполными [16]. Поэтому в 2012 году они опубликовали «предварительный» отчет, для которого тщательным образом отобрали доступные на тот момент исследования, признав, что «не смогли получить полный набор клинических отчетов и данных от производителя, несмотря на то, что в период с июня 2010 года по февраль 2011 года было сделано пять запросов» [17]. Так что дело затянулось еще на два года, когда, наконец, получив документы от Roche и проверив все данные «на вшивость», Джефферсон отобрал для сравнительного анализа всего 20 исследований осельтамивира (9623 пациентов) и 26 занамивира (14 628 пациентов). На основании отобранной столь строгим образом информации он и сделал выводы о неэффективности ингибиторов нейраменидазы [15].
Критика «самого надежного» исследования
Безусловно, исключение из обзоров 2012 и 2014 годов большой части имеющегося материала, аукнулось для Cochrane градом критики [16]. Их обвинили в том, что подобная практика не является «стандартной» [16]. Им пеняли, что они отказались рассматривать не только несостоятельные отчеты , но и все журнальные публикации по ингибиторам нейраминидазы за 2012 год . А ведь правительство Великобритании — заказчик экспертизы-2009 (которую и «исправляли» оба обзора) — ставило своей целью сделать оценку всех доступных материалов, будь то опубликованные или неопубликованные. Кроме того, в отличие от предыдущих работ, исследователи применили «более строгие методы» отбора и анализа данных, что не являлось стандартом для такого рода обзоров [16]. В итоге, ссылаясь на то, что для обзора-2012 использовали всего 37% «потенциально приемлемых исследований», главный санитарный врач Великобритании Сэлли Дейвис констатировала «сомнительную обоснованность оценок» и усомнилась в том, что обзор был полностью готов к публикации. По ее мнению, он являлся лишь «частично завершенным». «Таким образом, он не может дать точные ответы на вопросы об эффективности и безопасности осельтамивира, что, впрочем, признают и сами авторы», — резюмировала Сэлли Дейвис [16].
В пояснительной записке авторы обзора замечают, что они «не исключили» эти несостоятельные исследования (42 документа), а не «смогли их использовать», так как «не получили достаточной информации, чтобы определить их пригодность для включения в метаанализ» [16].
Исследовательская группа объяснила это решение следующим образом: «...мы рассматривали клинические исследования как основную единицу анализа, потому что отчеты о клинических исследованиях часто отправляются национальным регуляторам лекарственных средств (FDA и EMA), а эти организации требуют придерживаться более строгих стандартов полноты и точности отчетности, нежели биомедицинские журналы. Помимо поиска отчетов о клинических исследованиях, мы решили прочитать и просмотреть нормативную документацию» [15].
Что ж, эксперты Cochrane учли это замечание и в апреле 2014 года опубликовали обновленный метаанализ, включавший материалы, которые раньше были недоступны [15]. Но, по большому счету, и он — далеко не последняя точка в разговоре об эффективности ингибиторов нейраминидазы. И когда читаешь его размытые формулировки — «не было достаточно информации, чтобы сравнить эти эффекты», «гриппоподобное заболевание не может быть оценено из-за неполноты данных» [15], — создается впечатление, что либо у авторов действительно было недостаточно данных для более четких выводов, либо предоставленные материалы были крайне некачественными. Кстати, косвенно авторы в этом признаются, замечая, что «были отмечены проблемы в оформлении многих исследований, включенных в обзор, а это, в свою очередь, отразилось на уверенности в их результатах» [15].
И наконец, в метаанализе-2014 есть некоторые двусмысленные выводы. Например, было замечено, что «среди пациентов, принимавших осельтамивир, доля участников с четырехкратным увеличением титров антител была значительно ниже, чем в группе контроля», а «слабый иммунный ответ с низким уровнем провоспалительных цитокинов, вызванный действием препарата, уменьшал симптомы гриппа, не связанные с подавлением размножения (репликации) вируса» [15]. Скорее всего, авторы отнесли это к неблагоприятным эффектам, так как традиционно считается, что снижение активности иммунной системы — это плохо, потому что она должна бороться с инфекцией, но при этом они забывают об обратной связи: воздействии инфекции на иммунную систему. Мало того, они явно считают ингибиторы нейраминидазы иммуносупрессорами, игнорируя факт того, что для увеличения концентрации провоспалительных цитокинов важна репликация вируса [18] — соответственно, чем меньше вируса, тем меньше цитокинов. Таким образом, почему бы не рассмотреть низкий уровень цитокинов и снижение выработки антител через призму косвенного подтверждения эффективности данных препаратов (они быстро уменьшают вирусный титр, а это в свою очередь уменьшает количество цитокинов)?
Развивая теорию о негативном влиянии ингибиторов нейраминидазы на иммунную систему, авторы метаанализа-2014, в основном, ссылаются на три исследовательские работы: Скотта Фритца [18], Ребекки Кокс [19] и Мартина Мура [20]. Первые два исследования проведены на людях — 15 и 40 добровольцев соответственно; работа Мартина Мура [20] посвящена мышам и ингибированию внутриклеточной сиалидазы (гомолога вирусной нейраминидазы, которая, напротив, необходима Т-клеткам для выполнения антивирусных функций). Судя по всему, именно благодаря этому исследованию Том Джефферсон и его коллеги пришли к заключению, что ингибиторы нейраминидазы являются иммуносупрессорами и лишь ослабляют симптоматику, не оказывая влияния на сам вирус (кстати, по идее, это должно задерживать выздоровление и, возможно, влиять на осложнения, однако выводы метаанализа говорят об обратном). В общем, заразив мышей респираторно-синцитиальным вирусом (RSV), у которого отсутствует ген нейраминидазы, доктор Мур пришел к выводу, что «осельтамивир вызывает противовоспалительный эффект, ингибируя сиалидазу (...) Т-клеток, которая способствует антивирусному иммунитету». При этом «если препарат также ингибирует сиалидазу человека (...) есть основания предполагать, что он может продлить пролиферацию вируса, в котором отсутствует ген нейраминидазы» [20]. Тем не менее на каком основании эксперты из Cochrane предполагают, что при гриппе осельтамивир активно воздействует на сиалидазу [15]? Кроме того, данное исследование все-таки проводилось на мышах, и авторы не делают сенсационных заявлений, предлагая альтернативную интерпретацию своих результатов: «возможно, чувствительная к осельтамивиру сиалидаза действует на субстрат, отличный от GSL (гликосфинголипидов), для регуляции антивирусного иммунитета. Например, известно, что активированные Т-клетки обладают повышенной сиалидазной активностью, а также несут молекулы МНС I. В нашей экспериментальной системе лечение осельтамивиром не влияло на активность сиалидазы легочных мононуклеарных клеток, индуцированную вирусом RSV. Причины этого неясны, но могут быть связаны с относительно коротким периодом полураспада активной формы лекарственного средства» [20]. В целом, авторы резюмируют, что этот вопрос надо изучать.
В остальных исследованиях экспериментировали с занамивиром. Например, группа под руководством Скотта Фритца оценивала влияние препарата на цитокины и хемокины: «занамивир предотвращал инфекцию, аннулируя интегрированные ответы всех исследованных цитокинов , за исключением RANTES», без каких-либо выводов о возможной его иммуносупрессорной функции [18].
Таких как IL-6, IL-10, IFN-γ, TNF-α, MIP-1α и −1β, MCP-1.
Ребекка Кокс [19] изучала влияние занамивира на иммунный ответ на противогриппозную вакцину. И это, наверное, единственное исследование, которое может косвенно говорить в пользу теории об иммуносупрессорном действии ингибиторов нейраминидазы. Его авторы отметили, что «группа плацебо показала более высокий антительный ответ к вирусу гриппа H1N1 после вакцинации» [19], однако на второй вакцинный штамм вируса гриппа типа А (H3N2) и к вирусу гриппа типа В обе группы ответили более-менее одинаково (авторы объясняют это тем, что молодые добровольцы были, скорее всего, инфицированы H1N1 в детстве, а «влияние занамивира на иммунный ответ может наблюдаться в ситуации относительно близкого антигенного соответствия между штаммом вакцины и оригинальным прайминг-вирусом» [19]). Так что никаких выводов об угнетении препаратом иммунной системы в исследовании нет, наоборот, в заключении написано, что «вакцинируемым во время эпидемии гриппа желательно проводить профилактику занамивиром в течение 12 дней, пока не разовьется полноценный иммунный ответ на антигены» [19]. В целом этот эффект малоизучен, точнее практически не изучен, так как работе Ребекки Кокс предшествовало всего одно подобное исследование [21], не отметившее, впрочем, разницы в иммунном ответе между исследуемыми группами, а более поздние аналогичные испытания, по всей видимости, не проводились. Получается, что и здесь для далеко идущих выводов о негативной роли ингибиторов нейраминидазы на иммунный ответ необходимы дальнейшие исследования на добровольцах из разных возрастных групп.
И еще кое-что про пониженные титры антител. Не удивительно, что в конечном итоге этот феномен сказывается на риске дальнейшего повторного заражения: Том Джефферсон и его коллеги отмечают, что снижение титров защитных антител у пациентов из групп лечения согласуется с данными испытаний на животных, показавших, что по сравнению с группой контроля, применение препарата у подопытных мышей привело к выделению недостаточного уровня секреторного иммуноглобулина IgA (а также подавлению индукции IgA-образующих клеток) на слизистой носа, но при этом не оказало значительного влияния на системный IgG-ответ [22]. А это может означать, что существует риск повторного заражения пациента, у которого вследствие терапии осельтамивиром выработался недостаточный иммунный ответ слизистой оболочки (IgA) [22]. Однако эти данные не указывают на отсутствие лечебного эффекта. Что же касается риска повторного заражения, то он может быть естественным процессом вследствие низкого уровня выработанных защитных антител.
В общем, чтобы подтвердить негативное действие ингибиторов нейраминидазы на иммунный ответ, необходимо хотя бы изучить различие количества антител при разной концентрации вируса, а также понять, спустя какое время после момента заражения регистрировалось это различие, и как параллельно снижалась вирусная нагрузка (рис. 3 и 4). В целом, снижение указанных параметров по сравнению с группой контроля может быть как следствием иммуносупрессивного действия препаратов, так и результатом быстрого подавления репликации вируса, не позволяющего развиться полноценному иммунному ответу.
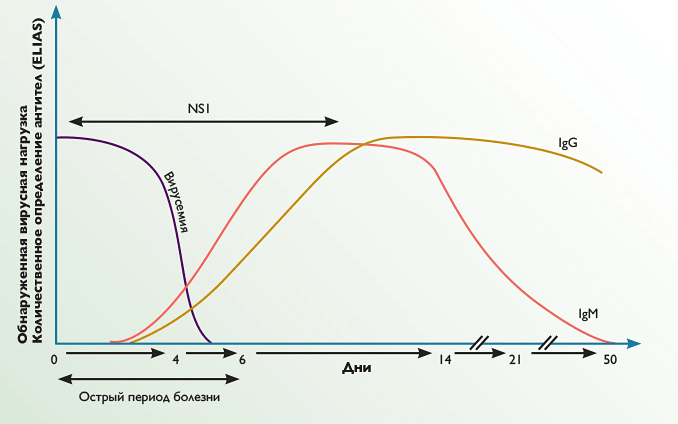
Рисунок 3. Временнáя кривая накопления антител.
сайт nature.com, рисунок адаптирован

Рисунок 4. Титры антител к AAV2/5, обнаруженные у мышей после внутрисосудистой инъекции вируса в различных дозах. Показана зависимость титров антител от дозы вируса: подопытным мышам вводили разное количество вируса AAV2/5 и замеряли количество антител. Оно увеличивалось не равномерно, а начиная с определенного порога.
[31], рисунок адаптирован
Резюме
Истинную правду об эффективности ингибиторов нейроминидазы не знает, наверное, никто. И, несомненно, налицо конфликт интересов производителей. Однако это не отменяет факта, что выводы «самого надежного и всеобъемлющего исследования» выглядят весьма сомнительными и расходятся с международной врачебной практикой в диаметрально противоположные стороны (хотя, исследователи ставят врачебные наблюдения ниже данных клинических испытаний). В любом случае, можно ли выдавать эти выводы за чистую монету? Это — вопрос, ответ на который, боюсь, заставит усомниться не только в авторитетах научно-исследовательского мира, но и в доказательной медицине как таковой, ведь, по большому счету, доказать можно все, что угодно: результат во многом будет зависеть от выборки и качества заполнения отчетности. Мало того, выводы других исследований и метаанализов эффективности ингибиторов нейраминидазы несколько отличаются от тех, к которым Том Джефферсон пришел в 2014 году.
Например, в январе 2015 года The Lancet опубликовал метаанализ рандомизированных контролируемых исследований осельтамивира для лечения взрослых пациентов (4328 человек) под руководством Джоанны Добсон, результаты, которого внушают больше оптимизма [23]. А буквально на днях, в ноябре 2017 года, вышел еще один систематический обзор [24] на эту тему. Что интересно, с каждым годом выводы исследователей все больше смещаются в пользу использования ингибиторов нейраминидазы: «Хотя осельтамивир не ассоциировался с уменьшением риска госпитализаций и пневмоний, препараты, содержащие его (n = 4), последовательно ассоциировались с уменьшением длительности симптомов на 0,5–1 день. (...) Кроме того, лечение при помощи ингибиторов нейраминидазы, вероятно, будет эффективным для снижения смертности среди госпитализированных пациентов (и кажется оправданной мерой), а также для снижения симптоматики на 1 день среди населения в целом» [24].
Интересные факты
- Ингибиторы нейраминидазы имеют направленное действие только против вирусов гриппа и бесполезны при риновирусах, аденовирусах, энтеровирусах и еще 140 их разновидностей, вызывающих сезонные ОРВИ.
- Осельтамивир получила американская компания Gilead Sciences (одним из руководителей которой до 2001 года был Дональд Рамсфельд — министр обороны США при Джордже Буше-младшем) в результате сложных химических опытов со звездчатым анисом (Illicium verum). Против вирусов гриппа осельтамивир продемонстрировал весьма обнадеживающие результаты. В 1996 году патент на его промышленное производство выкупила компания Roche. Несмотря на то, что осельтамивир получен из аниса, употребление этой специи вряд ли поможет при лечении гриппа.
- У подопытных мышей осельтамивир показал свойства ингибитора эндогенной (внутриклеточной) сиалидазы, способного уменьшать ее активность, снижая уровень моносиалоганглиозида GM1 и блокируя GM1-регулируемую гиперальгезию, оказывая болеутоляющий эффект, который позволяет усиливать клиническую эффективность морфина [25].
- Плановые закупки. В начале 2000-х годов правительства некоторых стран под нажимом рекомендаций ВОЗ и положительной оценки привлеченных экспертов закупили огромные партии этих препаратов (в основном, осельтамивира) для стратегических запасов на случай возможной пандемии [16]: США потратили около полутора миллиардов долларов; Великобритания — 424 миллиона фунтов стерлингов (примерно 40 миллионов доз «Тамифлю»), из которых использовали всего 2,4 миллиона, списав остатки на кругленькую сумму в 74 миллиона фунтов в утиль [16]. Когда об этом узнали журналисты, в Великобритании разгорелся жуткий скандал [16], [26], в ходе которого чиновники из Департамента здравоохранения при поддержке научного истеблишмента заявили [16], что они скорее предпочтут объясняться по поводу стоковых закупок, нежели оправдываться, по какой причине «Тамифлю» был недоступен в аптеках во время эпидемии 2009 года.
- Побочные эффекты. Британская газета The Guardian подсчитала, что «если дать „Тамифлю“ миллиону человек, у 45 000 из них будет рвота, у 31 000 — головная боль, а 11 000 столкнуться с проблемами, связанными с психикой» [26].
- Резистентность. Как это ни странно, она уже фиксируется [9], [27], [32]. Правда, количество штаммов вируса гриппа, резистентных и к осельтамивиру, и к занамивиру, статистически незначимо, однако никто не знает, что будет лет через 10. Поэтому во многих странах эти препараты продают строго по рецепту и не рекомендуют принимать для профилактики. В настоящее время ведут исследования о совместной терапии ими [28].
- Существует миф о том, что «Тамифлю» гепатоксичен [29], то есть опасен для печени. Однако выводится он преимущественно почками. Печень участвует лишь в процессе активации карбоксилата осельтамивира.
- В 2013 году эксперты Cochrane оценили эффективность травяных препаратов, применяемых в китайской традиционной медицине, в качестве альтернативы или дополнения к противовирусным средствам (18 испытаний, 2521 пациент; осельтамивир значился в 14 отчетах) и пришли к выводу, что «большинство включенных в обзор лекарственных трав были эффективны, а две даже превосходили противовирусные препараты для профилактики или лечения гриппа. При этом не было зарегистрировано нежелательных побочных эффектов. Однако полученные доказательства являются слабыми из-за низкого качества проведенных исследований. Для подтверждения результатов необходимы более точные испытания» [30].
В этом метаанализе изучали следующие травы: схизонепета (Schizonepeta), корень ледебуриеллы (radix ledebouriellae), корень володушки (radix bupleuri), корень платикодона (radix platycodi), корень имбиря (rhizoma zingiberis recens), плод форсайтии (fructus forsythiae), корень вайды (radix isatidis), корень пуерарии (radix puerariae), листья шелковицы (folium mori), цветы хризантемы (flos chrysanthemi), плоды лопуха (fructus arctii).
Дополнительная литература по теме — [33–38].
Литература
- Гонки с вирусом: эпидемиология и экология вируса гриппа;
- Anne Moscona. (2005). Neuraminidase Inhibitors for Influenza. N Engl J Med. 353, 1363-1373;
- Пилюля от гриппа: современные противовирусные средства;
- John J. Treanor, Frederick G. Hayden, Peter S. Vrooman, Rick Barbarash, Robert Bettis, et. al.. (2000). Efficacy and Safety of the Oral Neuraminidase Inhibitor Oseltamivir in Treating Acute Influenza. JAMA. 283, 1016;
- Wu T.C and Murray J.S. (1999). TamifluTM (oseltamivir) for treatment of influenza. Center for drug evaluation and research;
- The selection and use of essential medicines. World Health Organization, 2014. — 219 p.;
- Zosia Kmietowicz. (2017). WHO downgrades oseltamivir on drugs list after reviewing evidence. BMJ. j2841;
- Еxpert reaction to new meta-analysis investigating effectiveness and side-effects of Tamiflu (oseltamivir) for seasonal influenza. (2015). Science Media Centre;
- Sailen Barik. (2012). New treatments for influenza. BMC Med. 10;
- Универсальная вакцина от гриппа — мечты и реальность;
- Scientists show how drug binds with 'hidden pocket' on flu virus. (2016). ScienceDaily;
- Brendan Flannery, Jessie R. Chung, Swathi N. Thaker, Arnold S. Monto, Emily T. Martin, et. al.. (2017). Interim Estimates of 2016–17 Seasonal Influenza Vaccine Effectiveness — United States, February 2017. MMWR Morb. Mortal. Wkly. Rep.. 66, 167-171;
- D. Cohen. (2009). Complications: tracking down the data on oseltamivir. BMJ. 339, b5387-b5387;
- P. Doshi. (2009). Neuraminidase inhibitors--the story behind the Cochrane review. BMJ. 339, b5164-b5164;
- Jefferson T., Jones M.A., Doshi P., Del Mar C.B., Hama R., Thompson M.J. et al. (2014). Neuraminidase inhibitors for preventing and treating influenza in adults and children. (русскоязычная версия). Cochrane;
- Access to clinical trial information and the stockpiling of Tamiflu (thirty-fifth report of session 2013–14). London: House of Commons, 2013. — 43 p.;
- Tom Jefferson, Mark A Jones, Peter Doshi, Chris B Del Mar, Carl J Heneghan, et. al.. (2012) Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children;
- R. Scott Fritz, Frederick G. Hayden, David P. Calfee, Lindsey M. R. Cass, Amy W. Peng, et. al.. (1999). Nasal Cytokine and Chemokine Responses in Experimental Influenza A Virus Infection: Results of a Placebo‐Controlled Trial of Intravenous Zanamivir Treatment. J INFECT DIS. 180, 586-593;
- Rebecca J Cox, Eva Mykkeltvedt, Håkon Sjursen, Lars R Haaheim. (2001). The effect of zanamivir treatment on the early immune response to influenza vaccination. Vaccine. 19, 4743-4749;
- M. L. Moore, M. H. Chi, W. Zhou, K. Goleniewska, J. F. O'Neal, et. al.. (2007). Cutting Edge: Oseltamivir Decreases T Cell GM1 Expression and Inhibits Clearance of Respiratory Syncytial Virus: Potential Role of Endogenous Sialidase in Antiviral Immunity. The Journal of Immunology. 178, 2651-2654;
- Alison Webster, Malcolm Boyce, Sally Edmundson, Irene Miller. (1999). Coadministration of Orally Inhaled Zanamivir with Inactivated Trivalent Influenza Vaccine Does Not Adversely Affect the Production of Antihaemagglutinin Antibodies in the Serum of Healthy Volunteers. Clinical Pharmacokinetics. 36, 51-58;
- Etsuhisa Takahashi, Kosuke Kataoka, Kazuyuki Fujii, Junji Chida, Dai Mizuno, et. al.. (2010). Attenuation of inducible respiratory immune responses by oseltamivir treatment in mice infected with influenza A virus. Microbes and Infection. 12, 778-783;
- Joanna Dobson, Richard J Whitley, Stuart Pocock, Arnold S Monto. (2015). Oseltamivir treatment for influenza in adults: a meta-analysis of randomised controlled trials. The Lancet. 385, 1729-1737;
- M. K Doll, N Winters, C Boikos, H Kraicer-Melamed, G Gore, C Quach. (2017). Safety and effectiveness of neuraminidase inhibitors for influenza treatment, prophylaxis, and outbreak control: a systematic review of systematic reviews and/or meta-analyses. Journal of Antimicrobial Chemotherapy. 72, 2990-3007;
- Прошин С.Н. (2008). Значение сиалидазной (нейраминидазной) активности клеток в клинической фармакологии. Обзоры по клинической фармакологии и лекарственной терапии. 4, 3–17;
- Goldacre B. (2014). What the Tamiflu saga tells us about drug trials and big pharma (русскоязычная версия). The Guardian;
- О направлении обновленных рекомендаций CDC по использованию противовирусных препаратов. (2016). Роспотребнадзор;
- Camilly P. Pires de Mello, George L. Drusano, Jonathan R. Adams, Matthew Shudt, Robert Kulawy, Ashley N. Brown. (2018). Oseltamivir-zanamivir combination therapy suppresses drug-resistant H1N1 influenza A viruses in the hollow fiber infection model (HFIM) system. European Journal of Pharmaceutical Sciences. 111, 443-449;
- Нестерова Ю. (2016). «Тамифлю»: за и против. MedAboutMe;
- Lanhui Jiang, Linyu Deng, Taixiang Wu. (2013) Chinese medicinal herbs for influenza;
- Christopher M Treleaven, Thomas J Tamsett, Jie Bu, Jonathan A Fidler, S Pablo Sardi, et. al.. (2012). Gene Transfer to the CNS Is Efficacious in Immune-primed Mice Harboring Physiologically Relevant Titers of Anti-AAV Antibodies. Molecular Therapy. 20, 1713-1723;
- «Костыль» для нейраминидазы;
- YogendraKumar Gupta, Meenakshi Meenu, Prafull Mohan. (2015). The Tamiflu fiasco and lessons learnt. Indian J Pharmacol. 47, 11;
- Frederick G. Hayden, John J. Treanor, R. Scott Fritz, Monica Lobo, Robert F. Betts, et. al.. (1999). Use of the Oral Neuraminidase Inhibitor Oseltamivir in Experimental Human Influenza. JAMA. 282, 1240;
- Tamiflu pediatric adverse events: questions and answers. FDA;
- The FDA approves first generic version of widely used influenza drug, Tamiflu. FDA;
- Zheng J.H., Seo S., Lee J.E., Wang Y. (2012). Clinical pharmacology and biopharmaceutics review. Center for drug evaluation and research;
- Ralf Duerrwald, Michael Schlegel, Katja Bauer, Théophile Vissiennon, Peter Wutzler, Michaela Schmidtke. (2013). Efficacy of Influenza Vaccination and Tamiflu® Treatment – Comparative Studies with Eurasian Swine Influenza Viruses in Pigs. PLoS ONE. 8, e61597.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚