«Иммунный след» в нейроэндокринном раке поджелудочной железы
02 марта 2021
«Иммунный след» в нейроэндокринном раке поджелудочной железы
- 1051
- 0
- 4
Рак поджелудочной железы
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Рак поджелудочной железы и в наши дни остается одним из наиболее агрессивных, трудно диагностируемых и плохо поддающихся лечению видов злокачественных опухолей. Возможно, причина кроется в том, что клетки этой опухоли маскируются под здоровые и поэтому плохо распознаются клетками иммунной системы. Однако существует такой вид рака поджелудочной железы, на который иммунная система реагирует. Именно о нем и рассказывает эта статья.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Что такое рак поджелудочной железы?
Поджелудочная железа (ПЖ) — железа смешанной секреции (экзоэндокринная), поскольку она выполняет две разные функции:
- пищеварительную — выделяет панкреатический сок, содержащий пищеварительные ферменты, расщепляющие белки (трипсин и химотрипсин), жиры (панкреатическую липазу), углеводы (амилазу);
- эндокринную — выделяет гормоны инсулин и глюкагон, которые регулируют обмен веществ, главным образом метаболизм глюкозы: глюкагон способствует синтезу глюкозы, а инсулин поддерживает ее концентрацию в крови на оптимальном уровне (3,9–6,1 ммоль/л).
Рак поджелудочной железы — злокачественная опухоль, образующаяся из клеток эпителия поджелудочной железы в результате генетических изменений. В поджелудочной железе выделяют три отдела: головку, тело и хвост. Чаще всего опухоль локализуется в головке железы, прилегающей к луковице двенадцатиперстной кишки, куда открывается общий желчный проток — естественный дренаж для оттока желчи (рис. 1). Опухоль прорастает в этот проток, закупоривая его, вследствие чего отток желчи нарушается, и появляется подозрительный симптом заболевания: желтуха. В этом случае можно выявить рак на ранней стадии и успешно побороть его. При локализации опухоли в теле или хвосте поджелудочной железы желтухи не бывает, что затрудняет проведение диагностики и ухудшает прогноз лечения.
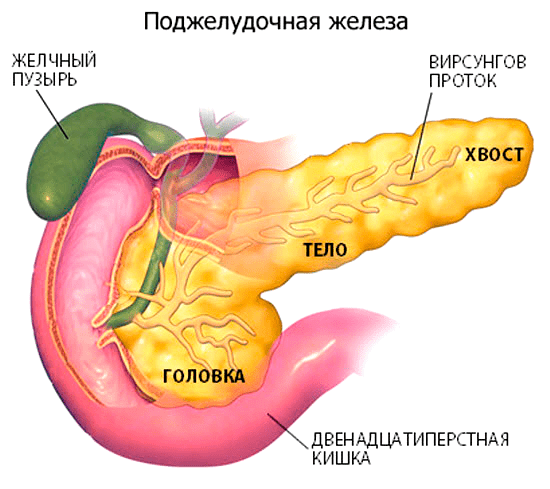
Рисунок 1. Анатомия поджелудочной железы. Головка поджелудочной железы непосредственно прилегает к двенадцатиперстной кишке, в которую открывается общий желчный проток, являющийся естественным дренажем для оттока желчи. Если раковая опухоль локализуется в этом отделе поджелудочной железы, то она глубоко прорастает в проток и закупоривает его, что приводит к нарушению оттока желчи и развитию механической желтухи. Прежде всего окрашиваются желтым цветом белки глаз, затем слизистые оболочки и в последнюю очередь кожа.
Существует множество гистологических форм рака поджелудочной железы, но особое внимание хочется обратить на нейроэндокринный рак. В отличие от «типичного» рака, это опухоль, которая обладает способностью выделять биологически активные вещества, такие как гормоны и нейромедиаторы . Например, такой опухолью является инсулинома — нейроэндокринная опухоль, образующаяся из бета-клеток островков Лангерганса поджелудочной железы, продуцирующих гормон инсулин. Однако клетки инсулиномы генетически изменены, и, в отличие от здоровых бета-клеток, они выделяют инсулин бесконтрольно, что может привести к инсулиновому шоку — крайней степени гипогликемии (снижения концентрации глюкозы в крови ниже 3,9 ммоль/л), при которой в случае несвоевременного или неадекватного лечения нарушаются функции ЦНС (двигательные, когнитивные, слуховые, тактильные, обонятельные, зрительные) вплоть до летального исхода, поскольку при таком состоянии нарушается процесс утилизации глюкозы головным мозгом.
Нейромедиаторы — биологически активные вещества, необходимые для передачи нервных импульсов от клетки к клетке.
Стоит отметить, что нейроэндокринный рак поджелудочной железы встречается редко, является гетерогенным заболеванием и так же, как любой другой рак, взаимодействует с иммунной системой.
Молекулярные подтипы нейроэндокринного рака поджелудочной железы
Современные молекулярно-генетические методы позволяют изучить опухоли на уровне транскриптома, и нередко в результате оказывается, что один вид злокачественного новообразования по своим молекулярным характеристикам может быть разделен на несколько. Это и случилось в недавнем исследовании английских и итальянских ученых, которые провели секвенирование транскриптомов биоптатов нейроэндокринного рака поджелудочной железы [1]. В результате были выявлены 4 молекулярных подтипа, отличавшиеся друг от друга, в первую очередь, активностью определенных генов (рис. 2).
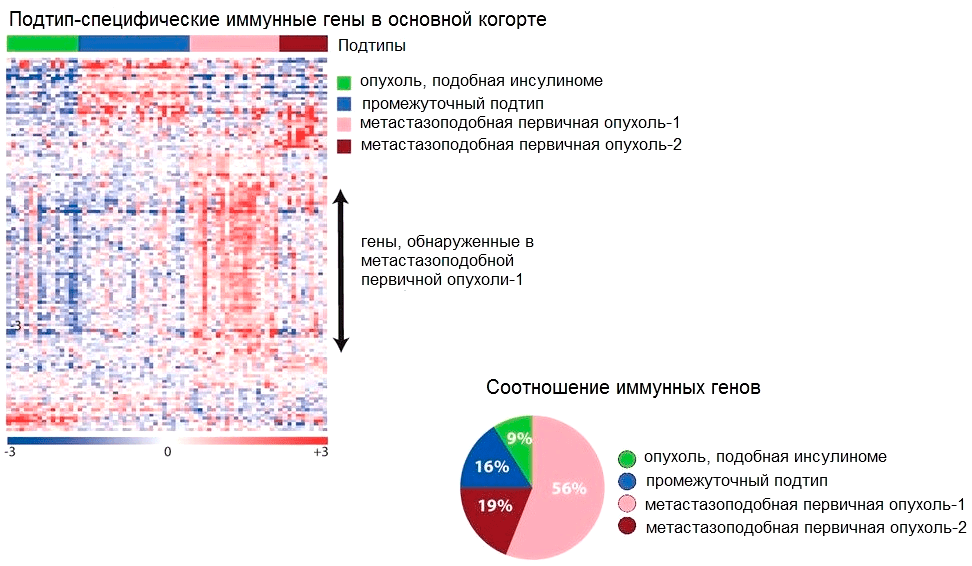
Рисунок 2. Тепловая карта, отображающая уровни экспрессии «иммунных» генов (справа), и диаграмма, отображающая процентное соотношение количества экспрессируемых иммунных генов (слева) в четырех подтипах нейроэндокринных опухолей поджелудочной железы. Самый богатый иммунными генами подтип — метастазоподобная первичная опухоль-1.
Клетки иммунной системы (лейкоциты) мигрируют в нейроэндокринную опухоль, инфильтрируют ее и экспрессируют гены, связанные с иммунитетом.
Самый «иммунный» из всех молекулярных подтипов нейроэндокринных опухолей ПЖ — это метастазоподобная первичная опухоль-1 (metastasis-like primary tumour-1, MLP-1). Встречающиеся в ней иммуноциты экспрессируют 56% иммунных генов (рис. 2), которые ученые разделили на две группы (рис. 3):
Первая группа — гены, кодирующие активированные Т-лимфоциты и белки-цитокины (интерфероны, интерлейкины, стимуляторы интерферонов).
Вторая группа — гены моноцитов/макрофагов и дендритных клеток, необходимые для процессинга (переработки) антигенов.

Рисунок 3. Тепловая карта, отображающая уровни экспрессии 19 идентифицированных иммунных генов в нейроэндокринных опухолях поджелудочной железы. Верхняя полоса указывает на подтип. На радужной шкале под тепловой картой красный цвет (+1 балл) означает высокий уровень экспрессии иммунных генов, синий (–1 балл) — низкий, белый (0 баллов) — отсутствие экспрессии генов. В подтипе MLP-1 наиболее ярко выражена экспрессия генов LAG3, IFI16, SPP1, CCRL2, TREM2, ANXA1.
В ходе гистологического исследования выяснилось, что опухоль MLP-1 менее васкуляризирована (обеднена кровеносными сосудами) по сравнению с другими подтипами нейроэндокринных опухолей поджелудочной железы. Следовательно, она подвержена гипоксии, что в свою очередь стимулирует запрограммированную некротическую гибель клетки — некроптоз . В отличие от апоптоза некроптоз сопровождается сильным иммунным ответом: погибающая клетка высвобождает ассоциированные с повреждениями молекулярные паттерны (образы патогенности, ассоциированные с повреждениями — damage-associated molecular patterns, DAMP), которые активируют каскад иммунных реакций, особенно секрецию цитокинов (интерферонов I и II типов и интерлейкина 18 (IL-18)), имитируя иммунный ответ на вирусную инфекцию (вирусная мимикрия). В итоге, в условиях гипоксии усиливается некроптоз опухолевых клеток, количество DAMP-молекул увеличивается, и усиливается иммунная реакция.
Некроптоз — запрограммированная некротическая гибель клетки, запускаемая через рецепторы смерти (например, через рецептор фактора некроза опухоли) и имеющая, в отличие от некроза, четкую систему регуляции: регулируется протеинкиназами — ферментами, которые модифицируют белки. При некроптозе так же, как и при апоптозе происходит образование активных форм кислорода в митохондриях, но не происходит фрагментации ДНК.
В поисках ответа на вопрос, почему так происходит, исследователи обнаружили, что в организме больных нейроэндокринным раком поджелудочной железы дендритные клетки (клетки, которые знакомят «наивные» Т-лимфоциты с антигенами) интенсивно синтезируют toll-подобный рецептор 3 (TLR3), лигандом которого является двуцепочечная РНК, появляющаяся при некроптозе. Кроме того, увеличивается количество дендритных клеток (рис. 4), следовательно, повышается уровень экспрессии TLR3, и это стимулирует синтез белков DAMP.
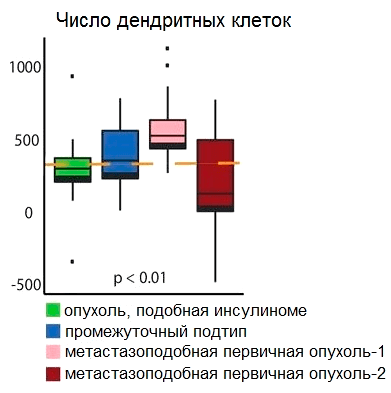
Рисунок 4. Диаграмма, отображающая количество дендритных клеток в четырех различных молекулярных подтипах нейроэндокринных опухолей поджелудочной железы
Исходя из того, что некроптоз является некротической гибелью клеток, для успешного лечения следует исключить те условия, в которых это будет происходить. Опухоль — это живой орган, который питается кислородом. Недостаток кровоснабжения (ишемия) ведет к гипоксии, которая и является условием для возникновения и усиления некроптоза. Клетки опухоли (в том числе и нейроэндокринной) обладают уникальной способностью способствовать появлению новых сосудов (ангиогенезу). Однако такие сосуды дефектны, они не выполняют свою функцию должным образом, вследствие чего опухолевые клетки испытывают стресс. Далее вступает в игру естественный отбор: уязвимые клетки погибают, резистентные клетки мигрируют по сосудам в близлежащие лимфатические узлы, а также в отдаленные органы и ткани, формируя вторичные очаги опухоли — метастазы (клоны опухоли). Этот процесс называется метастазированием. Он является одной из главных стратегий выживания опухоли в организме. Стимуляция же кровотока в опухоли способствует ее интенсивному росту, что ухудшает прогноз. Однако это единственный способ избежать некроптоза, так как DAMP-молекулы вводят иммунную систему в заблуждение, вследствие чего она не может уничтожить опухоль. Замкнутый круг, верно?
В итоге, для того чтобы научиться лечить такие опухоли, нам необходимо более подробно исследовать механизмы ангиогенеза, проанализировать уровень цитокинов, генов, которые экспрессируют различные клетки микроокружения опухоли помимо иммуноцитов. Также можно выявить и новые белки-регуляторы некроптоза. Все это в перспективе поможет победить один из самых агрессивных видов рака.
Литература
- Kate Young, Rita T Lawlor, Chanthirika Ragulan, Yatish Patil, Andrea Mafficini, et. al.. (2020). Immune landscape, evolution, hypoxia-mediated viral mimicry pathways and therapeutic potential in molecular subtypes of pancreatic neuroendocrine tumours. Gut. gutjnl-2020-321016;
- Anguraj Sadanandam, Stephan Wullschleger, Costas A. Lyssiotis, Carsten Grötzinger, Stefano Barbi, et. al.. (2015). A Cross-Species Analysis in Pancreatic Neuroendocrine Tumors Reveals Molecular Subtypes with Distinctive Clinical, Metastatic, Developmental, and Metabolic Characteristics. Cancer Discov. 5, 1296-1313.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚