Когда антибиотики перестают работать...
24 февраля 2023
Когда антибиотики перестают работать...
- 1257
- 1
- 5
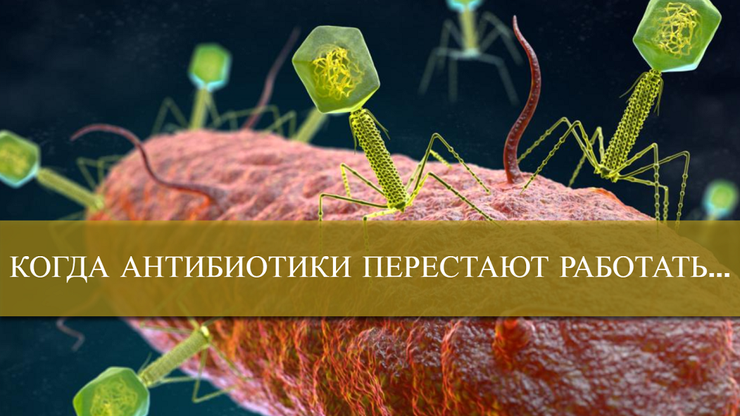
Бактериофаги и бактерия.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В наше время все большее значение приобретает нарастающая проблема антибиотикорезистентности. Все чаще специалисты задумываются о поиске альтернативных антимикробных препаратов, и все чаще в исследовательских работах упоминаются загадочные бактериофаги — микроорганизмы, обнаруженные учеными более 100 лет назад. Кто же это такие? Смогут ли они стать будущей заменой антибиотикам? Если смогут, то как? В этой статье я собрала информацию, которая поможет ответить на эти вопросы, а также узнать о фагах немного больше.
Конкурс «Био/Мол/Текст»-2022/2023
Эта работа опубликована в номинации «Школьная» конкурса «Био/Мол/Текст»-2022/2023.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Кто такой бактериофаг?
Бактериальные вирусы (бактериофаги или фаги) являются одной из самых распространенных форм жизни на планете. Это наиболее часто встречаемые биологические частицы в воде и широко распространенные компоненты биомассы на суше. Кроме этого, фаги были обнаружены в больницах, в сточных водах и везде, где могут жить бактерии, включая ткани животных и человека [1–3].
Бактериофаги — вирусы, которые могут заражать и убивать бактерии без какого-либо негативного воздействия на клетки человека или животных (рис. 1). По этой причине их используют отдельно или в комбинации с антибиотиками для лечения некоторых бактериальных инфекций [1–3].
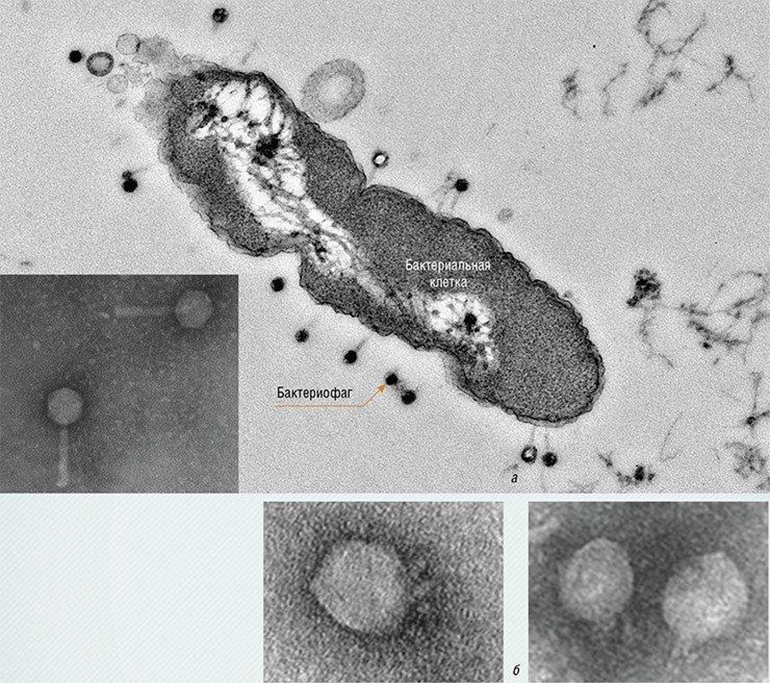
Рисунок 1. Бактериофаг и бактериальная клетка.
О бактериофагах человечество узнало более 100 лет назад. Название микроорганизмам дал франко-канадский микробиолог Ф. Д’Эрелль, и оно означает «пожиратель бактерий». Дальнейшее изучение бактериофагов показало, что существуют фаги с разными особенностями жизненного цикла, не всегда заканчивающимся быстрым уничтожением клетки-хозяина, но название осталось прежним [4].
Строение бактериофагов
Тело бактериофага состоит из головки и отростка (хвоста). Головка несет в себе некоторую генетическую информацию, содержащуюся в молекуле нуклеиновой кислоты (ДНК или РНК), которая защищена белковой оболочкой (капсидом). Хвост бактериофага способствует «программированию» клеток-хозяев. Отросток представляет собой белковую трубку, которая у ряда фагов окружена чехлом, содержащим сократительные белки, благодаря которым он способен сокращаться. На конце отростка у большинства фагов находится базальная пластинка, содержащая тонкие длинные нити и шиповидные выросты, способствующие прикреплению фага к бактерии. Существуют также бесхвостые и нитевидные фаги [3], [5].
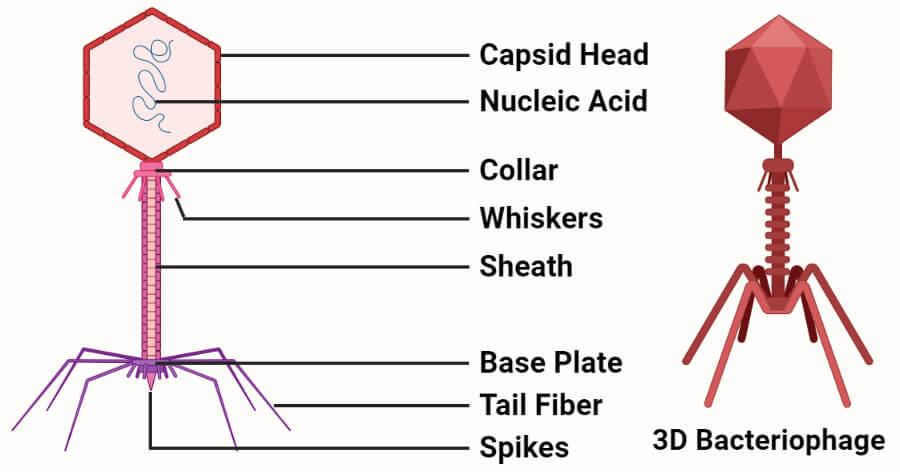
Рисунок 2. Строение бактериофага. Capsid Head — капсидная головка, Nucleic Acid — нуклеиновая кислота, Collar — венчик, Whiskers — усики, Sheath — оболочка, Base Plate — базальная пластинка, Tail Fiber — ножки, Spikes — шипы.
Бактериофаги классифицированы по различным признакам: a) содержанию в них нуклеиновых кислот, б) местам, где они чаще всего встречаются, в) видами бактерий, которые они могут убивать и др. [6].
Наиболее часто используемая классификация разделяет хвостовые компоненты бактериофагов на три морфологические группы :
- Сифовирусы — имеют длинный несократимый хвост, являются самой многочисленной группой (примерно 60% всех бактериофагов).
- Миовирусы — хвост длинный, умеет сокращаться. (на них приходится около 25%).
- Подовирусы — несократимый короткий хвост. (примерно 15% бактериофагов).
На самом деле, таксономическая классификация бактериофагов гораздо сложнее (в ней учитываются такие характеристики, как морфология, физико-химические свойства вириона, структура нуклеиновых кислот, геномные данные), она все еще продолжает претерпевать изменения. Классификация по внешнему виду сейчас применяется для удобства [5].
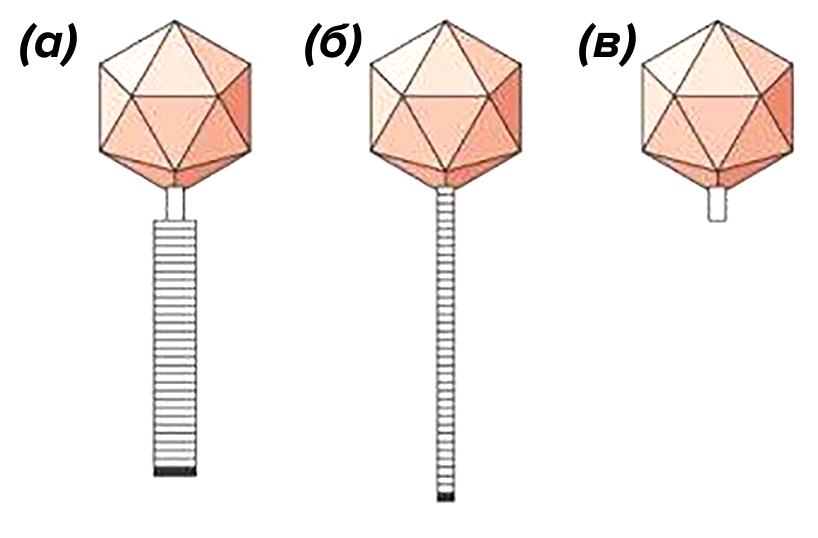
Рисунок 3. Семейства хвостатых фагов: (а) — миовирусы, (б) — сифовирусы, (в) — подовирусы.
Взаимодействие с бактериями
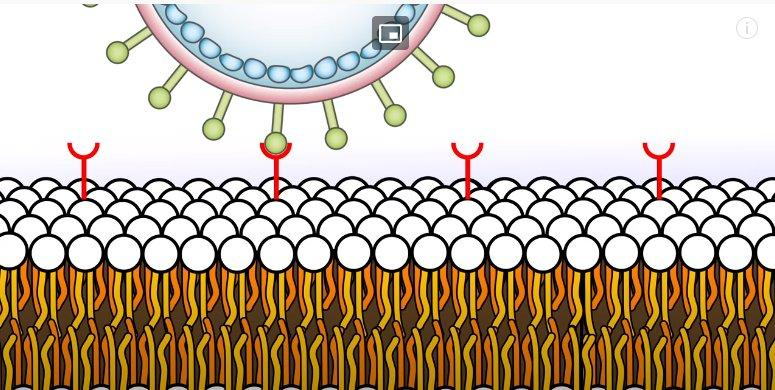
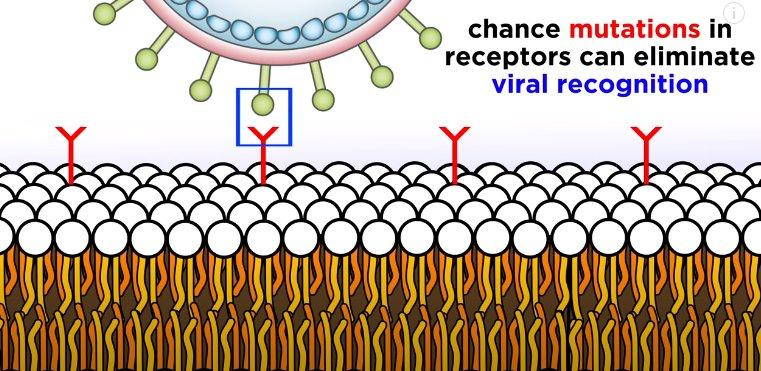
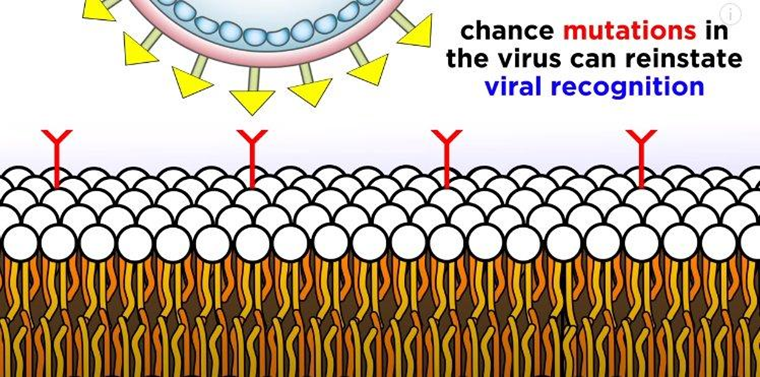
Биологический цикл бактериофагов подразумевает прикрепление к бактерии и введение в нее своего генетического материала. Однако, чтобы инициировать связывание, структуры фагов должны соответствовать штаммоспецифичным вариантам бактериальных рецепторов. Бактерии могут бороться с вирусами, например, изменяя бактериальные клеточные рецепторы. (рис. 4) Учитывая большие и непрерывные мутации как бактериофагов, так и бактериальных структур, один бактериофаг может заразить ограниченное число бактериальных штаммов и видов [1], [3].
Как только бактериофаг попадает в клетку, бактериальный синтетический механизм перенаправляется на производство копий вирусного генома и белков. Наконец, происходит сборка и упаковка фагов, и клетки лизируются с высвобождением новых вирионов, которые могут инфицировать другие бактериальные клетки. Однако размер всплеска может значительно варьироваться в зависимости от характеристик фага, патогенов, против которых он направлен, и среды, в которой происходит взаимосвязь бактериофага и патогена [3], [4].
Циклы развития бактериофагов
У фагов различают два основных (но не единственных) жизненных цикла: литический (разрушение бактериальной клетки фагом) и лизогенный (включение генома бактериофага в геном хозяина и последующее, при определенных условиях, разрушение клетки). Рассмотрим эти циклы чуть подробнее.
Литический цикл. Фаг прикрепляется к бактериальной клетке и вводит внутрь свой генетический материал. Такая бактерия превращается в фабрику по производству новых вирусных частиц. В итоге клетка разрушается, и новые фаги выходят во внешнюю среду. После лизиса вирус без промедления запускает сборку новых фаговых частиц.
Таким образом, фаги приводят к разрушению мембраны инфицированной клетки во время высвобождения вирусных частиц (рис. 5) [3], [4].
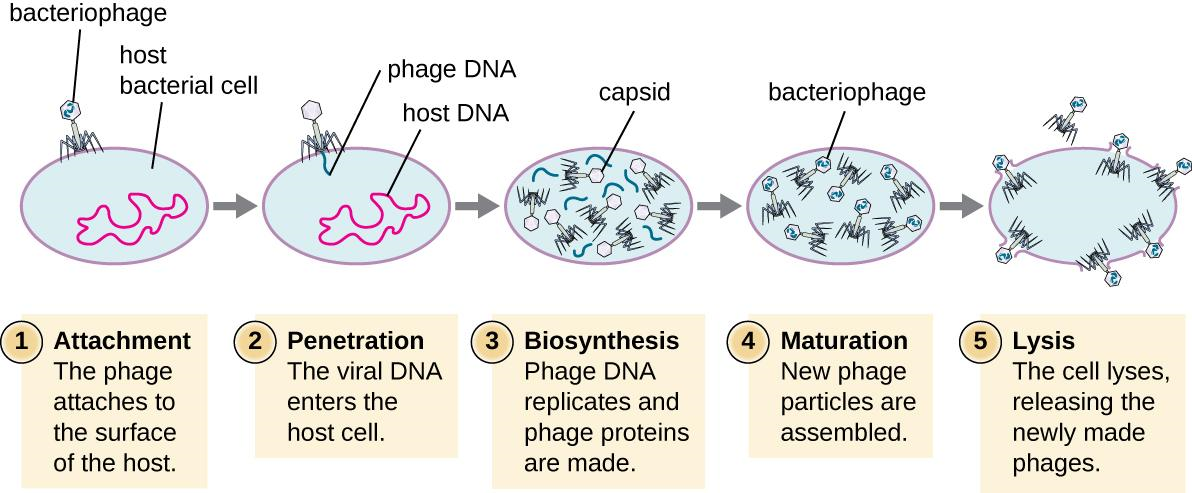
Рисунок 5. Литический цикл.
Лизогенный цикл характеризуется интеграцией вирусного генетического материала в геном хозяина и передачей вирусных хромосом дочерним клеткам при делении. В определенных случаях, например, при наступлении неблагоприятных условий для бактерии, которые могут привести к ее гибели, вирусный геном вырезается из бактериального генома и переключается на литический цикл [1], [7].
Так, в течение лизогенного жизненного цикла бактерии-хозяева продолжают нормально жить и размножаться до момента, пока вирусный геном не перейдет в литическую стадию [3], [4].
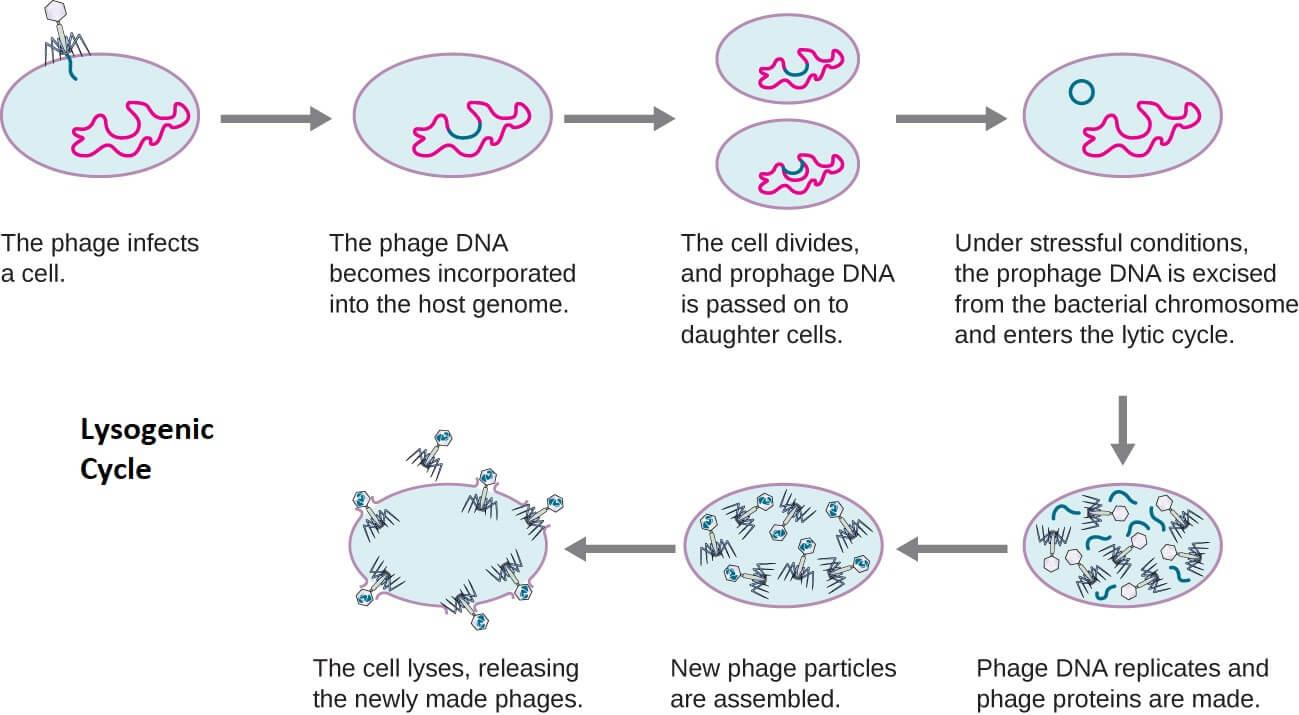
Рисунок 6. Лизогенный цикл.
Заключение
Мир простых, на первый взгляд, бактериофагов оказался гораздо многограннее и интереснее. Несмотря на простоту строения, они являются важным звеном в многообразии организмов. Жизненные стратегии фагов направлены на «программирование» бактериальной клетки производить вирусные частицы, что в конечном итоге приводит к ее гибели. Фаги, паразитируя на бактериях, являются фактором, оказывающим влияние на все живое на нашей планете, в том числе и на человека.
После открытия фаги использовались в медицине при лечении некоторых бактериальных заболеваний, но практически полностью были вытеснены антибиотиками. В настоящее время из-за проблемы быстрой адаптации бактерий к антибиотикам и возникновения устойчивых форм ученые вновь стали интересоваться фагами как средством лечения бактериальных заболеваний.
Таким образом, бактериофаги — это ресурс для борьбы с бактериями, возможности которого нам все еще открываются, и применение которому можно найти во многих областях деятельности человека, таких как медицина, сельское хозяйство и др.
Литература
- Nicola Principi, Ettore Silvestri, Susanna Esposito. (2019). Advantages and Limitations of Bacteriophages for the Treatment of Bacterial Infections. Front. Pharmacol.. 10;
- В.В. Власов, Н.В. Тикунова, В.В. Морозова. (2020). Бактериофаги как терапевтические препараты: что сдерживает их применение в медицине. БМ. 85, 1587-1600;
- Clara Torres-Barceló. (2018). The disparate effects of bacteriophages on antibiotic-resistant bacteria. Emerging Microbes & Infections. 7, 1-12;
- Charlotte Brives, Jessica Pourraz. (2020). Phage therapy as a potential solution in the fight against AMR: obstacles and possible futures. Palgrave Commun. 6;
- Огромный и загадочный мир бактериофагов;
- Потапов С.А. Вирусные сообщества в оз. Байкал: дис. ... канд. биол. наук. — Иркутск, 2021. — 156 с.;
- Stephen T. Abedon, Sarah J. Kuhl, Bob G. Blasdel, Elizabeth Martin Kutter. (2011). Phage treatment of human infections. Bacteriophage. 1, 66-85.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚