
Коварная стройность и безопасная полнота: метаболический синдром и сахарный диабет вне обычных границ индекса массы тела
11 января 2022
Коварная стройность и безопасная полнота: метаболический синдром и сахарный диабет вне обычных границ индекса массы тела
- 7555
- 0
- 10
Иногда наличие избыточного веса не приводит к развитию болезней обмена веществ, а нормальная масса тела не застраховывает от сахарного диабета.
Рисунок в полном размере.
рисунок автора
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Самые распространенные болезни современности связаны с нарушением обмена веществ — сахарный диабет 2 типа, артериальная гипертензия, ишемическая болезнь сердца (стенокардия, инфаркт миокарда). В большинстве случаев они развиваются у людей с явным ожирением, и ожирение у большинства людей со временем приводит к развитию одной или нескольких болезней. Однако эпидемиологические исследования показали, что связь между избыточной массой тела и «букетом» хронических заболеваний не является абсолютной. Среди имеющих инсулинорезистентность (состояние, вызывающее развитие метаболических болезней) — и даже сахарный диабет 2 типа — можно найти людей без ожирения по общепринятым критериям. При этом некоторые полные и очень полные люди живут десятилетиями без развития явных заболеваний. Понимание границ нормы и патологии необходимо врачам и пациентам. Причины столь разной реакции организмов на одинаковые стимулы могут стать ключом к изучению процессов, вызывающих самые распространенные и все же до конца не изученные болезни XXI века.
Конкурс «Био/Мол/Текст»-2021/2022
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2021/2022.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Эпидемия ожирения и метаболический синдром
Двадцатый век кардинально изменил как продолжительность жизни, так и причины смерти людей. Если раньше большей части человечества угрожали инфекции и недостаток питания, то к концу XX века эти опасности отступили в развитых странах. Средняя продолжительность жизни увеличилась с 30–50 до 60–90 лет, а наиболее распространенными причинами смерти стали онкологические заболевания и болезни сердечно-сосудистой системы. Причинами распространенности последних в основном являются два фактора: образ жизни и генетическая предрасположенность. Технологический прогресс принес человечеству дешевые калории: никогда еще пища не была так доступна стольким людям. Многие жители развитых стран съедают намного больше пищи, чем им в среднем требуется для покрытия естественных потребностей организма, а состав этой пищи может кардинально расходиться с потребностями тела [1].
Считается, что предки современных людей были охотниками и собирателями, которые редко питались вдоволь и проходили огромные расстояния в поисках пищи. После успешной охоты можно было наесться с избытком, формируя жировой запас, который быстро тратился при длительных переходах или в менее удачное время. Согласно концепции эволюционного происхождения метаболических болезней, наш обмен веществ принципиально не изменился за короткий с точки зрения эволюции срок, и жировые депо человека приспособлены для хранения питательных веществ только в разумных пределах [2]. Считается, что организм не очень хорошо умеет справляться с избытком жировой ткани. По некоторой договоренности экспертов были проведены границы, отделяющие нормальную массу тела от ожирения, которое можно считать патологическим и опасным для организма. Общепринятая граница проведена по значению индекса массы тела (ИМТ) ≥ 30 кг/м2. ИМТ — производная массы тела и роста, необходимая, чтобы учесть разницу в массе высоких и низких людей. Количество людей с ожирением по этому критерию очень быстро растет со второй половины XX века. По данным ВОЗ, в 2016 году 1,9 млрд людей по всему миру имели ИМТ не ниже 25 кг/м2 (избыточный вес), а 650 млн человек — не ниже 30 кг/м2 (ожирение) [2]. Существенную роль в распространении ожирения отводят так называемой «западной диете», которая содержит много липидов (жиров) с несбалансированным составом, много «быстрых» углеводов и в целом много калорий, но бедна полезными липидами (содержащими полиненасыщенные и сигнальные короткоцепочечные жирные кислоты) [3].
С богатой жирами и калориями диетой, низкой подвижностью и, как следствие, развитием ожирения связывают несколько заболеваний: сахарный диабет 2 типа, артериальную гипертензию и ишемическую болезнь сердца. Эти состояния часто сопровождают друг друга, так как в основе их развития лежит единый комплекс изменений, известный как метаболический синдром. Он включает инсулинорезистентность или повышение концентрации глюкозы в крови натощак, ожирение в той или иной форме, нарушение обмена жиров в крови (дислипидемию) и повышение артериального давления [4], [5]. Концепция метаболического синдрома была сформулирована для удобства выделения подгруппы пациентов с ожирением, имеющих высокий риск развития сахарного диабета 2 типа и артериальной гипертензии. Таким пациентам крайне рекомендовано значительное изменение образа жизни и более частые обследования.
Инсулин, инсулинорезистентность и сахарный диабет
Ключевым фактором развития метаболического синдрома является инсулинорезистентность. Инсулин — основной регулятор обмена глюкозы, гормон поджелудочной железы, заставляющий клетки организма забирать из крови излишки глюкозы. В норме после приема пищи происходит значительный выброс инсулина в кровь, благодаря чему клетки получают источники энергии для текущих нужд и запасания (в печени, мышцах и жировой ткани). Если инсулин не вырабатывается или по каким-то причинам клетки не восприимчивы к его действию, развивается сахарный диабет. Выделяют два основных типа сахарного диабета. Первый тип связан с разрушением из-за патологий иммунной системы клеток поджелудочной железы, выделяющих инсулин, и обычно развивается у детей [6]. Сахарный диабет второго типа в основном связывают с нарушениями обмена веществ, приводящими к нарушенному взаимодействию клеток с инсулином в зрелом возрасте [7]. Нечувствительность клеток к действию инсулина называют инсулинорезистентностью. Как правило, развитие резистентности к инсулину предшествует появлению сахарного диабета 2 типа [8]. Обычно резистентность формируется при значительном избытке калорий в рационе — образно выражаясь, жировые клетки и скелетные мышечные волокна «захлебываются» избытком жиров и глюкозы и пытаются уменьшить приток глюкозы, снижая свою чувствительность к инсулину. В итоге они уменьшают количество рецепторов инсулина на цитоплазматической мембране, либо их активность уменьшается за счет многих возможных путей (например, при активации внутриклеточных сигнальных каскадов, связанных с цитоплазматическими рецепторами — сенсорами обмена веществ). Лишнюю глюкозу поглощают не предназначенные для ее хранения клетки либо она продолжает циркулировать в крови [9].
При сахарном диабете в крови наблюдаются явные излишки глюкозы. Глюкоза хорошо растворяется в жидкостях и она химически активна. При значительном избытке глюкоза вступает в патологические реакции с белками плазмы, клеток крови, межклеточного пространства сосудов. Стенки сосудов утолщаются; из-за этого нарушается транспорт кислорода и питательных веществ в ткани. Крупные сосуды повреждаются в результате дисбаланса липидов, и у пациентов с сахарным диабетом быстро возникает атеросклероз. В результате развиваются осложнения сахарного диабета: ишемия сердца, повреждение почек, сетчатки глаза, формирование незаживающих язв на ногах (диабетическая стопа) [10-13] (рис. 1).
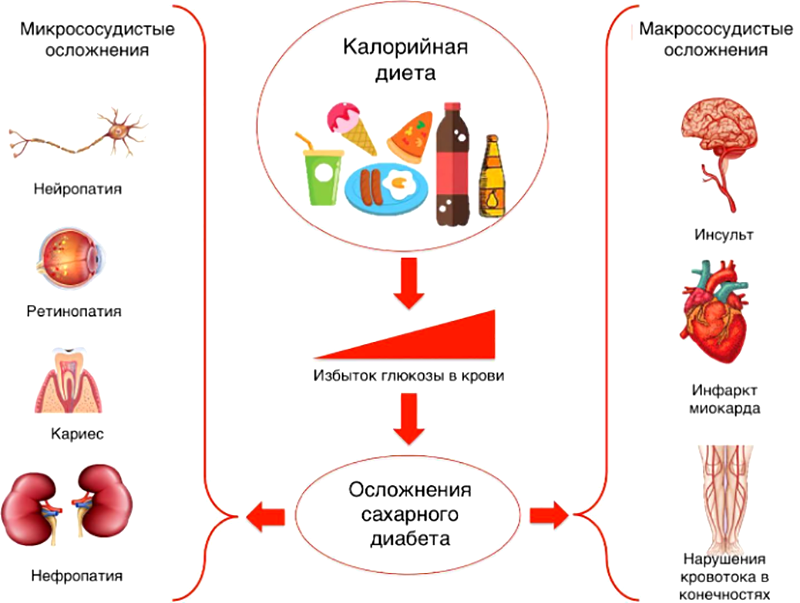
Рисунок 1. Осложнения сахарного диабета. Нейропатия — повреждение нервной системы, ретинопатия — повреждение сетчатки глаза, нефропатия — повреждение почек.
адаптировано из [13]
Метаболический синдром традиционно считается обратимым состоянием и до развития сахарного диабета обычно не сопровождается явными повреждениями органов. Хотя сахарный диабет 2 типа является основным проявлением метаболического синдрома, в некоторых случаях раньше может развиться повышение артериального давления (артериальная гипертензия) или, при наличии дополнительных патологий липидного обмена, ишемическая болезнь сердца (стенокардия) [14]. В целом, обнаружение одного из компонентов метаболического синдрома указывает на необходимость проверки других компонентов. Ранняя обеспокоенность развитием диабета, гипертензии и других болезней обмена веществ очень полезна. Образ жизни и диету легче изменить, когда еще нет клинических проявлений болезней, а эффектом может быть полная нормализация обмена веществ без лекарственных препаратов [1].
«Худой» метаболический синдром
Но что, если развитие инсулинорезистентности и сахарного диабета останутся незамеченными у человека с нормальным или незначительно увеличенным ИМТ? В представлении большинства врачей, ожирение и метаболический синдром — синонимы, но ключевым признаком метаболического синдрома является инсулинорезистентность, а не ожирение. Эпидемиологические исследования показали, что в странах Азии от 15 до 50% от всех пациентов с сахарным диабетом 2 типа не удовлетворяют общим критериям ожирения. Интересно, что для таких пациентов также характерно развитие заболевания в более молодом возрасте, чем у пациентов с ожирением [15]. На наследственные причины развития инсулинорезистентности и диабета у не имеющих ожирения выходцев из Азии указывают данные о столь же высокой распространенности диабета в диаспорах иммигрантов. Исследователи отмечают, что недостаточная представленность иммигрантов в западных эпидемиологических исследованиях препятствует точному сравнению [16].
Выдвигаются различные концепции, объясняющие возможность развития сахарного диабета 2 типа без ожирения. Самое простое объяснение указывает на условность единых критериев избыточной массы тела и ожирения и предлагает концепцию индивидуального порога ожирения [17]. Это утверждение сложно оспорить, но интереснее найти причины, определяющие значительные колебания этого порога.
«Здоровая» полнота
И наоборот: что, если у человека, страдающего ожирением, не наблюдается других признаков метаболического синдрома? В большинстве популяций можно выделить подгруппы людей с избыточной массой тела, которые не имеют проблем со здоровьем. Эта категория крайне дискуссионна, поскольку критерии здоровья можно рассматривать по-разному. По наиболее мягким критериям, в Европе и Северной Америке в эту группу попадает до 50% людей с ожирением, по наиболее строгим — около 7% (рис. 2) [18], [19].
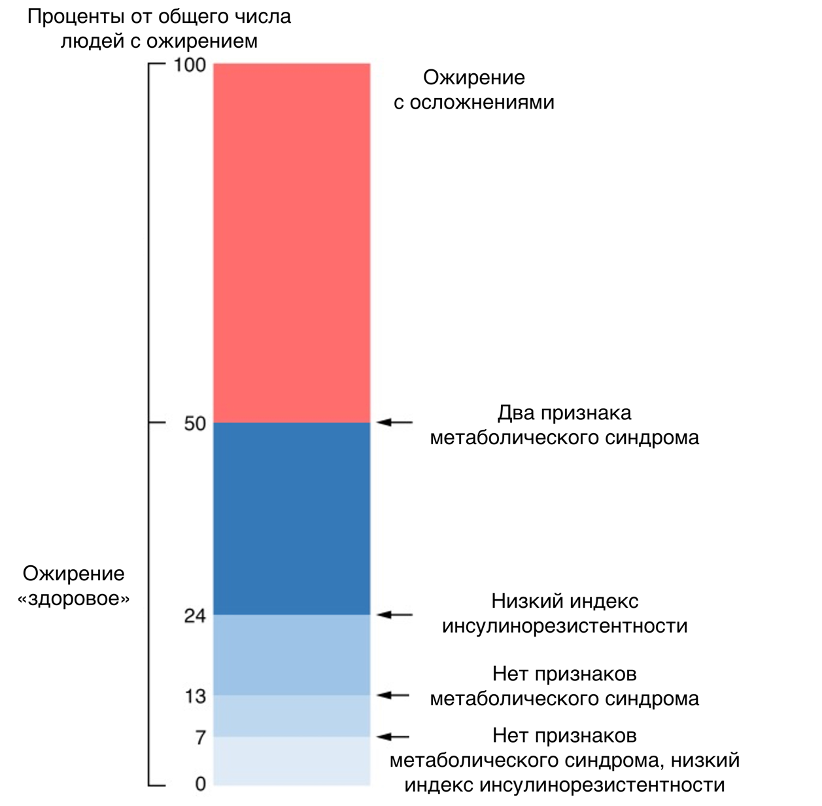
Рисунок 2. Процентное соотношение людей с ожирением и разной выраженностью осложнений.
адаптировано из [19]
По усредненным критериям, минимальное количество таких людей всегда насчитывают в странах Азии (4,2–13,6%); в странах Европы доля «здорового» ожирения составляет 2—19% среди мужчин и 7–28% — среди женщин. Также доля людей с таким типом ожирения падает с возрастом; среди детей ожирение намного чаще не сопровождается развитием метаболических заболеваний (при этом в целом сахарный диабет 2 типа встречается у детей все чаще) [20]. Длительное наблюдение показало, что люди с метаболически здоровым ожирением более устойчивы к его осложнениям, но не защищены от их развития. Наблюдая более 3000 людей, исследователи из США обнаружили, что в течение в среднем 5,6 лет 34,6% людей со «здоровым» ожирением сохранили свой статус, а по сравнению с участниками с нормальным ИМТ риск развития сахарного диабета 2 типа оказался выше в 3,44 раза, нарушений обмена липидов — в 1,5 раза [21]. Поскольку «метаболически здоровое ожирение» становится все более распространенной концепцией, появились некоторые диагностические признаки, позволяющие отделить его от ожирения, сопряженного с метаболическими осложнениями. Их недостатком является отсутствие динамики, поскольку по результатам одного обследования в эту категорию можно отнести как людей с длительно стабильным состоянием обмена веществ, так и только начавших набирать массу тела, но уязвимых к ожирению людей. Исследование 6809 человек с ожирением показало, что чем дольше длится период здорового ожирения, тем ниже риск последующего развития и тяжесть сердечно-сосудистых и метаболических осложнений. Задача определения рисков превращения «здорового» ожирения в «нездоровое» имеет большое практическое значение и требует лучшего понимания механизмов развития нарушений обмена веществ у людей с избыточной массой тела и ожирением [22], [23].
Что может служить причиной такой различной реакции на избыток жиров и калорий?
Что же определяет развитие метаболического синдрома стройных людей или здоровой полноты? Явные отличия встречаемости двух крайних состояний между азиатской и европеоидной расами указывают на генетическую природу различий. Обнаружены полиморфизмы, связанные с двумя этими состояниями, но неясно, как изменения в описанных генах приводят к особому типу обмена веществ на уровне организма [24], [25].
Ключевые различия между двумя группами людей явным образом указывают на существенные особенности работы жировых депо организма. Жировые ткани человека неоднородны. Выделяют подкожные жировые депо (соматические) и висцеральные жировые депо, окружающие органы. Давно известно, что висцеральное ожирение намного более злокачественное, чем соматическое [26]. Увеличение объема подкожной жировой клетчатки — нормальный процесс в периоды избытка калорий, в то время как висцеральные жировые ткани в большей степени нужны для нормального функционирования внутренних органов. Когда человек с нормальной массой тела получает избыток калорий, преимущественно происходит отложение липидов в подкожной жировой ткани. Со временем ее вместимость истощается, липидов становится существенно больше в крови, и их захватывает висцеральная жировая ткань, которая довольно быстро начинает вызывать инсулинорезистентность [27]. В еще более тяжелой ситуации клетки не предназначенных для этого органов (печени, скелетных мышц, поджелудочной железы) начинают откладывать в цитоплазме капли липидов; такое ожирение называют эктопическим, оно является признаком тяжелых нарушений метаболизма [28].
У всех пациентов с метаболическим синдромом утолщается висцеральная жировая ткань, но у пациентов без увеличения ИМТ ее прирост по отношению к подкожной жировой ткани существенно выше [29]. В Азии у пациентов с метаболическим синдромом также значительно чаще встречается эктопическое ожирение. Можно заключить, что подкожные жировые депо у пациентов из Азии заполняются быстрее, и патологические отложения липидов начинаются до того, как масса человека достигнет привычных нам критериев ожирения [30]. У европейских жителей, в особенности у коренных обитателей северных стран, вместимость жировых депо существенно выше среднего, на что указывает распространенность «здорового» ожирения.
Важно отметить, что абсолютный уровень липидных нарушений все же имеет значение. Исследователи из Оксфорда сравнили абсолютную выраженность эктопического и висцерального ожирения при одинаковой длительности заболевания у пациентов с сахарным диабетом 2 типа с ожирением и нормальной массой тела. У последних не только все отложения жировой ткани оказались меньше, но и связанные с ними осложнения со стороны печени и сердца также были менее выражены [31].
Особенности жировых тканей
Клетки жировой ткани (адипоциты) могут реагировать на избыток липидов двумя способами: увеличением размера клеток (гипертрофия) и увеличением количества клеток (гиперплазия) [32]. Здоровая реакция жировой ткани на необходимость запасания калорий — гиперплазия с умеренным увеличением размера клеток. При таком варианте влияние адипоцитов на организм минимально. Если жировая ткань имеет низкую способность к гиперплазии или липидная нагрузка очень велика, размеры адипоцитов увеличиваются многократно. В ответ на такой клеточный стресс развивается местное воспаление в жировой ткани и системное воспаление; развивается инсулинорезистентность; липиды переходят в висцеральные жировые депо (рис. 3) [28]. Возможными причинами низкой способности жировой ткани к гиперплазии являются меньшее число стволовых клеток, измененный баланс факторов роста и низкая чувствительность рецепторов. У пациентов с сахарным диабетом 2 типа без ожирения гипертрофия адипоцитов существенно преобладает над гиперплазией, а размер клеток коррелирует с выраженностью метаболических нарушений [28].
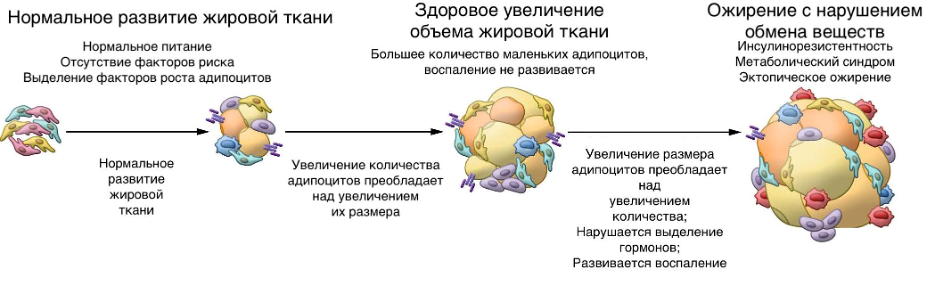
Рисунок 3. Патологическое развитие жировой ткани и его последствия.
с изменениями из [32]
Медицинское значение
У пациентов с нормальной массой тела врачи практически никогда не подозревают наличие сахарного диабета. Многие эндокринологи никогда не встречали таких больных, что не связано с их отсутствием. На ранних этапах и сахарный диабет, и артериальная гипертензия не вызывают явного ухудшения самочувствия. Когда появляются типичные симптомы, от начала заболевания могло уже пройти несколько лет, и за это время развилось клиническое ожирение. В Азии, где до половины пациентов имеют такой фенотип ожирения и где развита профилактическая медицина, этому вопросу уделяют существенное внимание [15].
В дальнейшем отличия в метаболизме влияют на эффективность разных типов терапии сахарного диабета 2 типа. В таком контексте выявление разных вариантов развития и течения диабета может улучшить лечение за счет персонализированного подхода [32]. Пациенты с сахарным диабетом 2 типа без ожирения хуже принимают наличие у них тяжелого заболевания, что может привести к плохой приверженности лечению [33]. Люди со «здоровым» ожирением могут испытывать психологическую нагрузку непропорционально риску развития заболеваний и получать не самое эффективное или ненужное лечение [20].
Кажется, что наиболее доступный способ определения рисков нарушений обмена веществ — определение соотношения соматической и висцеральной жировой ткани. Самый простой метод выявления висцерального ожирения — измерение отношения окружности талии к окружности бедра [25], [30]. Появление «живота» во многом обусловлено увеличением висцеральной жировой ткани брюшной полости, поэтому высокое значение индекса свидетельствует о висцеральном характере ожирения. При крайних случаях «азиатского» типа ожирения этот индекс неинформативен; тогда выявить висцеральное ожирение можно с помощью МРТ [30]. Неясно, требует ли проблема «худого» метаболического синдрома введения скрининговой МРТ, но, на мой взгляд, она увеличивает значимость диспансерных наблюдений, включающих оценку концентрации глюкозы в крови и измерение артериального давления у всех людей вне зависимости от массы тела.
Заключение
Значение наследственных факторов в жизни человека очень велико. Вероятно, устоявшиеся пищевые традиции наших предков продолжают влиять на нашу способность усваивать разные диеты. Традиционная пища восточной Азии — рис и морепродукты, и нужный для их усвоения метаболизм плохо справляется с избытком насыщенных жиров скотоводческой диеты. Рацион северных стран в основном состоял из мясо-молочных продуктов, и потомки северных жителей лучше переносят избыток жиров в пище. Вне зависимости от того, насколько верна эта гипотеза, важно понимать, что несбалансированное и избыточное питание никогда не полезны для организма и могут привести к тяжелым болезням, иногда несмотря на нормальную массу тела или длительную комфортную жизнь с ожирением, у кого-то — быстрее, у кого-то — медленнее.
Литература
- Stéphanie Harrison, Patrick Couture, Benoît Lamarche. (2020). Diet Quality, Saturated Fat and Metabolic Syndrome. Nutrients. 12, 3232;
- Anoop Misra, Shajith Anoop, Seema Gulati, Kalaivani Mani, Surya Prakash Bhatt, Ravindra Mohan Pandey. (2015). Body Fat Patterning, Hepatic Fat and Pancreatic Volume of Non-Obese Asian Indians with Type 2 Diabetes in North India: A Case-Control Study. PLoS ONE. 10, e0140447;
- Yulia K. Denisenko, Oxana Yu Kytikova, Tatyana P. Novgorodtseva, Marina V. Antonyuk, Tatyana A. Gvozdenko, Tatyana A. Kantur. (2020). Lipid-Induced Mechanisms of Metabolic Syndrome. Journal of Obesity. 2020, 1-14;
- Helen H. Wang, Dong Ki Lee, Min Liu, Piero Portincasa, David Q.-H. Wang. (2020). Novel Insights into the Pathogenesis and Management of the Metabolic Syndrome. Pediatr Gastroenterol Hepatol Nutr. 23, 189;
- Christian K. Roberts, Andrea L. Hevener, R. James Barnard. (2013). Metabolic Syndrome and Insulin Resistance: Underlying Causes and Modification by Exercise Training. Comprehensive Physiology. 1-58;
- Tat'yana Yur'evna Shiryaeva, Endocrinology Research Centre, Moscow, Ekaterina Andreevna Andrianova, Yuriy Ivanovich Suntsov. (2013). Type 1 diabetes mellitus in children and adolescents of Russian Federation: key epidemiology trends. DM. 21-29;
- American Diabetes Association. (2017). 2. Classification and Diagnosis of Diabetes. Dia Care. 40, S11-S24;
- Dilek Yazıcı, Havva Sezer. (2017). Insulin Resistance, Obesity and Lipotoxicity. Obesity and Lipotoxicity. 277-304;
- Derek M. Erion, Hyun-Jun Park, Hui-Young Lee. (2016). The role of lipids in the pathogenesis and treatment of type 2 diabetes and associated co-morbidities. BMB Reports. 49, 139-148;
- Renata Libianto, Duygu Batu, Richard J. MacIsaac, Mark E. Cooper, Elif I. Ekinci. (2018). Pathophysiological Links Between Diabetes and Blood Pressure. Canadian Journal of Cardiology. 34, 585-594;
- Masaki Kobayashi, Douglas W Zochodne. (2018). Diabetic neuropathy and the sensory neuron: New aspects of pathogenesis and their treatment implications. J Diabetes Investig. 9, 1239-1254;
- Sher Zaman Safi, Rajes Qvist, Selva Kumar, Kalaivani Batumalaie, Ikram Shah Bin Ismail. (2014). Molecular Mechanisms of Diabetic Retinopathy, General Preventive Strategies, and Novel Therapeutic Targets. BioMed Research International. 2014, 1-18;
- Concetta Schiano, Vincenzo Grimaldi, Michele Scognamiglio, Dario Costa, Andrea Soricelli, et. al.. (2021). Soft drinks and sweeteners intake: Possible contribution to the development of metabolic syndrome and cardiovascular diseases. Beneficial or detrimental action of alternative sweeteners?. Food Research International. 142, 110220;
- Julia Hernandez-Baixauli, Sergio Quesada-Vázquez, Roger Mariné-Casadó, Katherine Gil Cardoso, Antoni Caimari, et. al.. (2020). Detection of Early Disease Risk Factors Associated with Metabolic Syndrome: A New Era with the NMR Metabolomics Assessment. Nutrients. 12, 806;
- Juliana C. N. Chan, Vasanti Malik, Weiping Jia, Takashi Kadowaki, Chittaranjan S. Yajnik, et. al.. (2009). Diabetes in Asia. JAMA. 301, 2129;
- Swapnil Rajpathak. (2009). Diabetes in Asian Immigrant Populations. JAMA. 302, 1646;
- Roy Taylor, Rury R. Holman. (2015). Normal weight individuals who develop Type 2 diabetes: the personal fat threshold. Clinical Science. 128, 405-410;
- Gordon I. Smith, Bettina Mittendorfer, Samuel Klein. (2019). Metabolically healthy obesity: facts and fantasies. Journal of Clinical Investigation. 129, 3978-3989;
- Matthias Blüher. (2020). Metabolically Healthy Obesity. Endocrine Reviews. 41;
- M. Fingeret, P. Marques-Vidal, P. Vollenweider. (2018). Incidence of type 2 diabetes, hypertension, and dyslipidemia in metabolically healthy obese and non-obese. Nutrition, Metabolism and Cardiovascular Diseases. 28, 1036-1044;
- Ling Lai, Miao Wang, Ola J. Martin, Teresa C. Leone, Rick B. Vega, et. al.. (2014). A Role for Peroxisome Proliferator-activated Receptor γ Coactivator 1 (PGC-1) in the Regulation of Cardiac Mitochondrial Phospholipid Biosynthesis. Journal of Biological Chemistry. 289, 2250-2259;
- David J. Mancuso, Harold F. Sims, Kui Yang, Michael A. Kiebish, Xiong Su, et. al.. (2010). Genetic Ablation of Calcium-independent Phospholipase A2γ Prevents Obesity and Insulin Resistance during High Fat Feeding by Mitochondrial Uncoupling and Increased Adipocyte Fatty Acid Oxidation. Journal of Biological Chemistry. 285, 36495-36510;
- Xizhen Wang, Sizhong Zhang, Yuanzhong Chen, Hekun Liu, Cailian Lan, et. al.. (2009). APM1 gene variants −11377C/G and 4545G/C are associated respectively with obesity and with non-obesity in Chinese type 2 diabetes. Diabetes Research and Clinical Practice. 84, 205-210;
- Ayumi TOKUNAGA, Yukio HORIKAWA, Etsuko FUKUDA-AKITA, Kohei OKITA, Hiromi IWAHASHI, et. al.. (2008). A Common P2 Promoter Polymorphism of the Hepatocyte Nuclear Factor-4.ALPHA. Gene Is Associated with Insulin Secretion in Non-Obese Japanese with Type 2 Diabetes. Endocr J. 55, 999-1004;
- Yuji Matsuzawa, Tohru Funahashi, Tadashi Nakamura. (2011). The Concept of Metabolic Syndrome: Contribution of Visceral Fat Accumulation and Its Molecular Mechanism. JAT. 18, 629-639;
- Marie-Eve Piché, André Tchernof, Jean-Pierre Després. (2020). Obesity Phenotypes, Diabetes, and Cardiovascular Diseases. Circ Res. 126, 1477-1500;
- Sonia Caprio, Rachel Perry, Romy Kursawe. (2017). Adolescent Obesity and Insulin Resistance: Roles of Ectopic Fat Accumulation and Adipose Inflammation. Gastroenterology. 152, 1638-1646;
- Juan R. Acosta, Iyadh Douagi, Daniel P. Andersson, Jesper Bäckdahl, Mikael Rydén, et. al.. (2016). Increased fat cell size: a major phenotype of subcutaneous white adipose tissue in non-obese individuals with type 2 diabetes. Diabetologia. 59, 560-570;
- Chatchalit Rattarasarn. (2018). Dysregulated lipid storage and its relationship with insulin resistance and cardiovascular risk factors in non-obese Asian patients with type 2 diabetes. Adipocyte. 1-10;
- Eylem Levelt, Michael Pavlides, Rajarshi Banerjee, Masliza Mahmod, Catherine Kelly, et. al.. (2016). Ectopic and Visceral Fat Deposition in Lean and Obese Patients With Type 2 Diabetes. Journal of the American College of Cardiology. 68, 53-63;
- C. Ronald Kahn, Guoxiao Wang, Kevin Y. Lee. (2019). Altered adipose tissue and adipocyte function in the pathogenesis of metabolic syndrome. Journal of Clinical Investigation. 129, 3990-4000;
- Allan Vaag, Søren S. Lund. (2007). Non-obese patients with type 2 diabetes and prediabetic subjects: distinct phenotypes requiring special diabetes treatment and (or) prevention?. Appl. Physiol. Nutr. Metab.. 32, 912-920;
- Yoshiko Miyawaki, Hiromi Iwahashi, Yukiyoshi Okauchi, Yoshiko Sudo, Yuko Fujiwara, et. al.. (2015). Differences in Emotional Distress among Inpatients with Type 1, Obese Type 2, and Non-Obese Type 2 Diabetes Mellitus. Intern. Med.. 54, 2561-2567.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





