Микрофлюидный биосенсор на основе Helicobacter pylori: может ли патоген приносить пользу?
25 января 2022
Микрофлюидный биосенсор на основе Helicobacter pylori: может ли патоген приносить пользу?
- 1096
- 0
- 2
Бактерия H. pylori и микрофлюидный чип. «Задетектируем это».
рисунок автора статьи
-
Автор
-
Редакторы
Темы
Статья на конкурс «Био/Мол/Текст»: О чем вы думаете, когда слышите слово «биосенсор»? А «микрофлюидные технологии»? Эти слова кажутся таинственными, даже немного пугающими и как будто взятыми из какой-то научно-фантастической книжки. На самом деле первый биосенсор был создан еще в 1975 году, а микрофлюидным технологиям уже более 30 лет. Биосенсоры бывают очень разными по своей структуре и принципу действия. На сегодняшний день клеточные биосенсоры активно используются для экологического мониторинга токсинов в воде, почве и продуктах питания. Чаще всего чувствительным элементом в таких биосенсорах являются условнопатогенные бактерии, например, кишечная палочка или биолюминесцентные бактерии, обитающие в глубинах моря. Однако получение новых специфических, компактных и недорогих биологических сенсоров и выбор оптимальных микроорганизмов, которые могли бы выступать в качестве чувствительных элементов в таких сенсорах, всегда остается актуальной задачей как для экологии, так и в сфере медицинской диагностики. Мы решили подойти к решению этого вопроса нестандартно: взять грозную патогенную бактерию Helicobacter pylori и с использованием микрофлюидных технологий попробовать получить новый биологический сенсор оптического типа. А о том, как и почему мы это делали, и что же из всего этого вышло, читайте ниже.
Конкурс «Био/Мол/Текст»-2021/2022
 Эта работа заняла второе место в номинации «Своя работа» конкурса «Био/Мол/Текст»-2021/2022.
Эта работа заняла второе место в номинации «Своя работа» конкурса «Био/Мол/Текст»-2021/2022.

Партнер номинации — компания Cytiva.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Helicobacter pylori. Кто он такой?
В 1979 году австралийские патологи Робин Уоррен и Барри Маршалл заинтересовались бактерией спиралеобразной формы, которая обнаруживалась в биопсии пациентов, страдающих гастритом и язвой желудка [1]. Они были первыми, кто смог выделить и изолировать Helicobacter pylori из проб слизистой оболочки желудка человека и классифицировать ее как отдельную бактерию. И именно Уоррен и Маршалл предположили, что большинство язв желудка и гастритов вызваны хеликобактерной инфекцией, а вовсе не стрессом или острой пищей [2]. Этим ребятам потребовалось более 10 лет и одна выпитая Маршаллом жидкая культура Helicobacter, вызвавшая у него острый гастрит, прежде чем научное сообщество в 1994 году признало научную значимость их открытия и вручило им Нобелевскую премию.
Этот малыш Helicobacter pylori, из-за которого случился весь сыр-бор, является грамотрицательной бактерией размером всего 3–5 мкм с несколькими хвостиками-жгутиками на одном из концов для быстрого перемещения (рис. 1) [3].
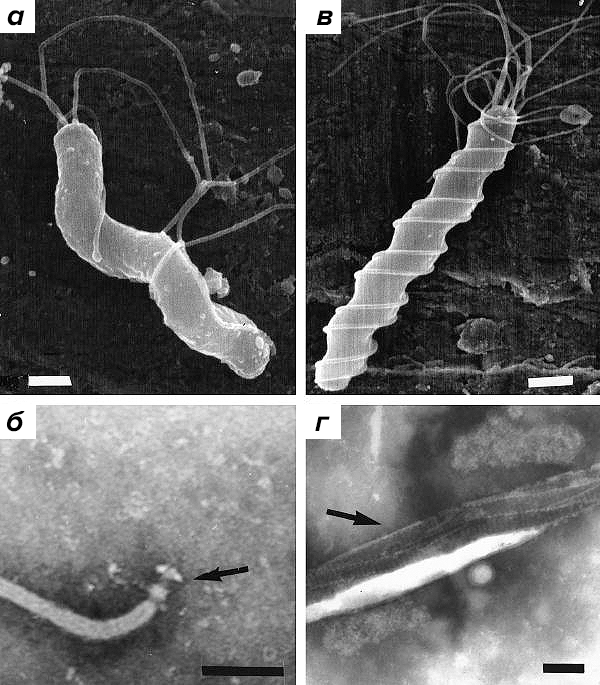
Рисунок 1. Морфология бактерий рода Helicobacter. а — S-форма H. pylori с 5–7 полярными жгутиками. Масштаб поля 0,5 μm. б — Детализация жгутикового крючка. Негативное окрашивание, масштаб 0,05 μm. в — Спиралевидный H. felis с периплазматическими волокнами и биполярными жгутиками. Масштаб 0,5 μm. г — Детализация периплазматического волокна. Негативное окрашивание, масштаб 0,05 μm.
Он микроаэрофил, а значит в очень душной и влажной комнате с 5% содержанием CO2 ему совсем не понадобится форточка. А еще никто не разбирается в длительных и стабильных отношениях так хорошо, как H. pylori. Сосуществование этого патогена с человеческой популяцией насчитывает тысячи лет. Исследования в области филогеографии показали, что он с нами (а точнее в нас) по крайней мере с момента начала миграции людей из Африки — около 60 тыс. лет назад [4]. Вот уж и правда «и в горе, и в радости». И это при том, что условия его проживания в желудке человека далеки от пятизвездочного отеля. Ведь наш желудок, по сути, представляет собой бассейн с соляной кислотой (pH около 2,0) и долгое время считался совершенно стерильным [5]. На сегодняшний день H. pylori является единственным известным микроорганизмом, способным длительно выживать в условиях низких значений pH желудочно-кишечного тракта [6]. Более того, иногда бактерия колонизирует человека на протяжении всей жизни. И кстати, если вы считаете, что вас эта инфекция точно обошла стороной — не спешите с выводами. По статистике, данным микроорганизмом инфицировано более половины человеческой популяции, хотя у 80% инфекция никак себя не проявляет [7], а значит, любой из нас может быть счастливым обладателем этого хвостатого микроба.
Разумеется, на все нужны ресурсы. И такое длительное сосуществование человека и H. pylori обусловило развитие у патогена узкоспециализированных механизмов адаптации [5]. В их основе лежит целый набор белковых факторов и механизмов вирулентности, которые отвечают за подвижность бактерии, способность выживать в кислой желудочной среде, индуцировать синтез провоспалительных цитокинов, нарушать структуру контактов эпителиальных клеток [6].
Белки — всегда продукт экспрессии соответствующих генов. И для того, чтобы сожительствовать с человеком так долго, H. pylori развил в себе специализированные механизмы генетической регуляции, заточенные на то, чтобы «замечать» малейшие изменения в желудке человека (диета, лекарственная терапия, иммунный ответ) и адаптироваться к ним. Что если использовать это умение H. pylori «чувствовать» в наших интересах?
Клеточные биосенсоры. Удивительные факты из жизни некоторых бактерий
Любая бактериальная клетка — это удивительная мини-фабрика, которая, исходя из своей природной ниши, выработала внутри себя ряд механизмов выживания и адаптации, основой которых являются гены, белки (продукты экспрессии генов) и промоторы, управляющие всеми этими процессами. Промотор — это уникальная последовательность перед геном, которую «узнает» фермент полимераза, взаимодействует с ней и запускает каскад таких процессов, как транскрипция (наработка РНК) и трансляция (наработка белкового продукта) этого гена. Все это называется экспрессией гена, а промотор регулирует эту экспрессию и ее уровень (рис. 2).
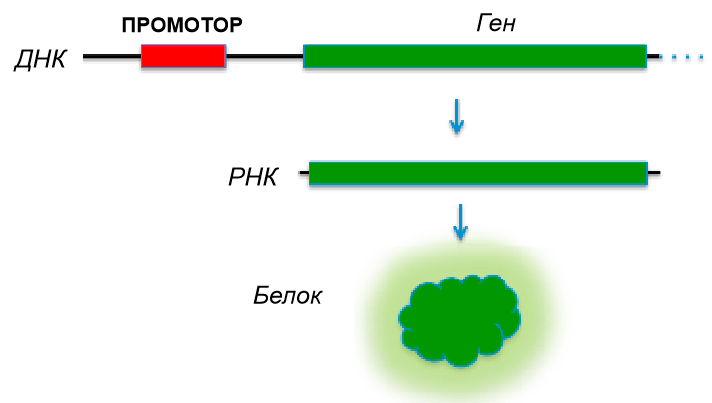
Рисунок 2. Схематическое изображение процесса экспрессии гена. Экспрессия гена регулируется промотором. ДНК-последовательность гена служит в качестве матрицы для процесса транскрипции (наработка РНК с ДНК-последовательности гена) и последующей трансляции (образование белкового продукта).
рисунок автора статьи
Есть гены, чьи продукты нужны клетке всегда, поэтому они экспрессируются на постоянном уровне (их называют генами «домашнего хозяйства»). А есть гены, чья экспрессия нужна только в некоторых случаях, например, для защиты клетки от неблагоприятного внешнего воздействия. Такое воздействие называют индуктором промотора. И у одного промотора таких индукторов может быть сразу несколько. Иногда изменение количества белкового продукта в клетке в ответ на индуктор можно легко зарегистрировать, например визуально. Именно это характерно для природных люминесцентных бактерий, таких как Vibrio, Photobacterium, Shewanella (Altermonas) и Photorhabdus (Xenorhabdus), встречающихся, главным образом, в море [8]. В их клетках с помощью целого оперона (несколько объединенных генов), называемого lux-опероном, закодирован белок-фермент люцифераза и его вспомогательные белки, которые, управляя сложным каскадом реакций, инициируют свечение клетки голубовато-зеленым светом — люминесценцию [8]. За регуляцию этого lux-оперона в клетке отвечают стресс-чувствительные промоторы. Соответственно, факторы, воздействующие на эти промоторы, изменяют экспрессию lux-оперона и, как следствие, уровень свечения клетки. А поскольку у хорошей хозяйки все в хозяйстве сгодится, то ученые решили, что негоже таким бактериям просто так пропадать на дне морском и сделали их частью биологического сенсора [9].
Биосенсор — это устройство, в котором чувствительный слой представлен биологическим объектом: клеткой (клеточный биосенсор), ферментом (ферментный биосенсор), антителом (иммуносенсор) или нуклеиновой кислотой (сенсоры на основе ДНК-аптамеров). Этот чувствительный слой реагирует на присутствие определенного компонента в анализируемой смеси и генерирует сигнал (например, в случае люминесцентных бактерий, свечение), пропорциональный количеству этого компонента или факту его наличия/отсутствия [10]. Для каждого вида чувствительного элемента есть свои преимущества и ограничения. Но сенсоры на основе живых клеток значительно стабильнее и дешевле. К тому же уникальная комбинация всех клеточных компонентов позволяет создавать систему, которую невозможно воспроизвести, используя отдельные составляющие. Поэтому уже сейчас в экологии для определения токсичности водных сред на основе люминесцентных бактерий активно используются такие биосенсорные системы, как Microtox в США, LUMItox в Великобритании, ToxAlert в Германии и BioTox в Финляндия [9], [10]. Это клеточные биосенсоры на основе нативных (то есть естественных) бактериальных клеток.
Но что делать, если у бактерии есть специфические промоторы, которые чувствительны к специфическим факторам и были бы полезны в биосенсоре, но продукт экспрессии этих генов не удобно регистрировать? Ну не светятся они в обычной жизни. Не хочешь? Поможем.
Именно здесь на сцену выходит великая и ужасная генная инженерия, благодаря которой, кстати, человечество получило устойчивую к засухе пшеницу и холодоустойчивые томаты, более крупный картофель и устойчивые к паразитам яблоки и бананы [11]. Как? Если кратко, то с помощью генно-инженерных методов мы можем внести в клетку дополнительные гены или целые гибридные последовательности таким образом, чтобы клетка производила нужные нам белки в большем объеме или приобретала благодаря им новые качества [12]. Кстати, именно генномодифицированные бактерии производят для нас в огромных масштабах гормоны инсулин и эритропоэтин, а также различные витамины и антибиотики, которые многим людям просто жизненно необходимы [12].
На сегодняшний день вариантов и подходов к модификации растений и микроорганизмов в генной инженерии существует очень много. Но в нашем случае, для получения клеточного биосенсора на основе генетически модифицированных бактерий, наиболее простым подходом является использование репортерной конструкции (рис. 3) [7], [13–16]. Чаще всего репортерная конструкция представляет собой кольцевую ДНК (плазмиду), которая может быть внесена в клетку и существовать в ней автономно. В состав такой плазмиды мы можем поместить выбранный нами чувствительный к специфическим воздействиям промотор данного микроорганизма таким образом, чтобы он регулировал экспрессию выбранного нами гена-репортера (это ген, продукт которого легко регистрируется — например, зеленая или красная флуоресценция или люминесценция).
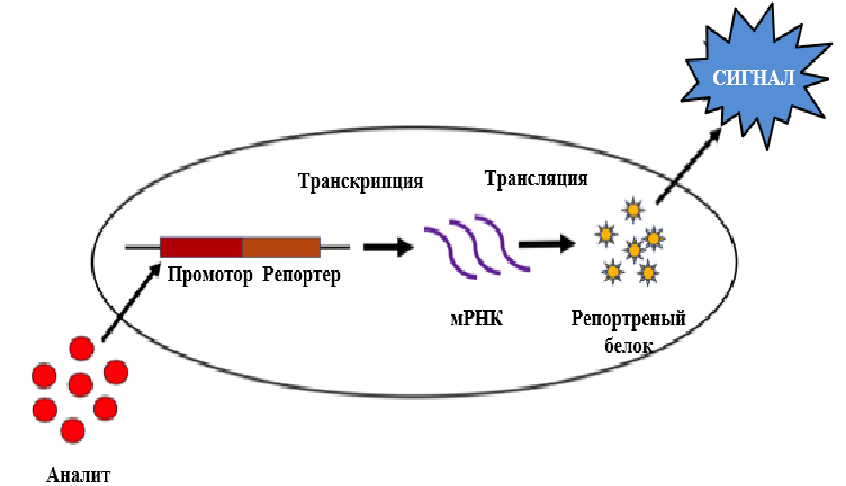
Рисунок 3. Упрощенная схема принципа действия биосенсора на основе модифицированных клеток с использованием репортерной конструкции. В составе конструкции чувствительный промотор объединен с геном-репортером, контролируя его экспрессию. Конструкция внесена в клетки путем клеточной трансформации. В результате внешнего воздействия на такие модифицированные конструкцией клетки происходит активация стресс-чувствительного промотора, экспрессия гена-репортера и последующая продукция репортерного белка.
[7], рисунок изменен и адаптирован
Итак, резюмируем. Мы выбираем интересный микроорганизм с необычным, специфическим промотором, чувствительным к определенному веществу, которое нам хотелось бы детектировать. Затем мы «собираем» для него репортерную конструкцию, которая содержит ген-репортер под контролем стресс-чувствительного промотора и вносим эту конструкцию в клетки (генетически модифицируем наш микроорганизм). Если в среде оказывается вещество-индуктор, к которому чувствителен наш промотор, — промотор активирует экспрессию гена-репортера, в клетке происходит продукция репортерного белка, и мы видим клеточный сигнал — вуаля! Мы детектируем данное вещество в среде благодаря тому, что модифицированные клетки меняют свою флуоресценцию/люминесценцию в ответ на вещество-индуктор. На основе таких модифицированных микроорганизмов уже получен ряд биосенсоров, с помощью которых успешно детектируют тяжелые металлы в среде и почве, токсины в подземных водах, ядовитые соединения в воде и антибиотики в почве и в продуктах питания.
Наиболее популярным микроорганизмом для модификации и использования в таких биосенсорах является условно патогенная бактерия E. coli или кишечная палочка [17]. Однако потребности человечества в новых специфических системах детекции и новых микроорганизмах для этих целей с каждым днем только растут. Каждый микроорганизм уникален, и чем необычнее его биологическая ниша и способы адаптации к ней, тем специфичнее его промоторы. Вот так мы и решили заставить нашего грозного патогенного малыша H. pylori приносить пользу, генетически модифицировав его с помощью репортерной конструкции и сделав его частью клеточного биосенсора.
«ГМОшная» бактерия. Как и зачем научить H. pylori флуоресцировать
Как мы знаем, H. pylori сам по себе не умеет светиться в темноте подобно люминесцентным бактериям. Это, конечно, очень досадно, ведь тогда в желудке его бы было отлично видно. Но нам в нем интересно другое. У него есть ряд уникальных стресс-чувствительных промоторных последовательностей, которые мы могли бы использовать. Гены, которые регулируются этими промоторами, кодируют белки вирулентности H. pylori, помогают ему колонизировать желудок и реагируют на присутствие самых разнообразных факторов. Здесь и снижение кислотности среды, и осмотический и окислительный стрессы и изменение концентрации ионов металлов (таких как никель и железо), и взаимодействие с эпителиальными клетками [5]. Из этого многообразия мы решили выбрать для нашей последующей работы промоторы двух генов, кодирующих белки, критически важные для колонизации H. pylori: субъединицу А фермента уреазы и вакуолизирующий цитотоксин [3], [4].
Уреаза и есть тот философский камень, который синтезируется в клетке H. pylori и помогает ему выживать внутри нас. Только превращает он не металл в золото, а мочевину в аммиак и СО2. Аммиак защелачивает pH до значений 6,0–7,0 вблизи бактерии, делая окружающую среду пригодной для выживания. Промотор гена, кодирующего субъединицу А уреазы, Pure, чувствителен к снижению pH и повышению концентрации ионов никеля. В ответ на эти воздействия экспрессия гена возрастает [18].
И если уреаза — щит H. pylori, то вакуолизирующий цитотоксин VacA — один из его мечей. Это уникальный и очень агрессивный белок, активность которого может быть высокой или низкой в зависимости от штамма [3]. Кстати, в том числе и с вариативностью VacA в разных штаммах связана разнородность симптоматических проявления инфекции у пациентов [19]. В своем самом агрессивном варианте, цитотоксин, секретируемый H. pylori, «дырявит» клетки желудочного эпителия, образуя в них анионные каналы. В результате этого эпителиоциты из-за разницы осмотического давления разбухают (вакуолизируются), лопаются и гибнут [20]. Промотор гена, кодирующего этот цитотоксин, Pvac, чувствителен к осмотическому стрессу (повышение соли в среде) и к снижению концентрации ионов железа [21].
Итак, мы выбрали промоторы и то, что будем детектировать с их помощью. Затем, для того, чтобы сделать генно-инженерную репортерную конструкцию, мы позаимствовали из клеток H. pylori его же природную плазмиду, которая встречается в клетках примерно 50% штаммов H. pylori [22]. С ее помощью мы решили научить нашего H. pylori светиться зеленым светом. Для этого, используя генно-инженерные методы, мы интегрировали в плазмиду ген-репортер gfp, продуктом экспрессии которого является тот самый зеленый белок GFP, благодаря которому светятся медузы Aequorea victoria [23]. А для того, чтобы ген экспрессировался (то есть чтобы происходила продукция GFP в клетках и они светились), мы «поставили» перед ним два наших промотора H. pylori Pvac и Pure.
Итак, на основе нашей одной природной плазмиды мы сделали для H. pylori целых две репортерные конструкции, содержащие ген gfp под контролем двух критически важных промоторов H. pylori. В одной конструкции Pure, в другой Pvac. Затем мы внесли эти конструкции в клетки H. pylori (модифицировали их) и получили два генно-модифицированных штамма, которые светятся зеленым светом благодаря продукции GFP в клетках. Теперь один штамм (с Pure) должен детектировать повышение кислотности и повышение ионов никеля, флуоресцируя сильнее. Другой штамм (с Pvac), по тому же принципу, должен определять повышение соли в среде и снижение концентрации ионов железа. Но как нам проверить их работоспособность? И каким вообще может быть биосенсор на основе таких клеток?
H. pylori + микрофлюидный чип: «Задетектируем это!»
В случае с H. pylori не все так просто. Для этой бактерии важно анализировать единичные клетки, так как известно, что данная бактерия высоко гетерогенна [3]. Это понятие означает, что внутри клеточной популяции каждая клетка индивидуальна и отвечает на внешний стимул по-своему, со своей интенсивностью. То есть если мы будем просто регистрировать общую флуоресценцию клеточной популяции, то результат будет чем-то вроде средней температуры по больнице — не достоверным. К тому же важной характеристикой биосенсора является не только его чувствительность и специфичность, но и его компактность. Поэтому, для решения этой комплексной задачи, мы решили использовать микрофлюидные технологии [24]. Этот подход позволяет не только миниатюризировать инструменты исследования (ведь масштабы микрофлюидики это 1–1000 микрон, а 1000 микрон = 1 мм) (рис. 4), но и, как следствие, сократить объем пробы, а также во многом автоматизировать весь эксперимент [25].
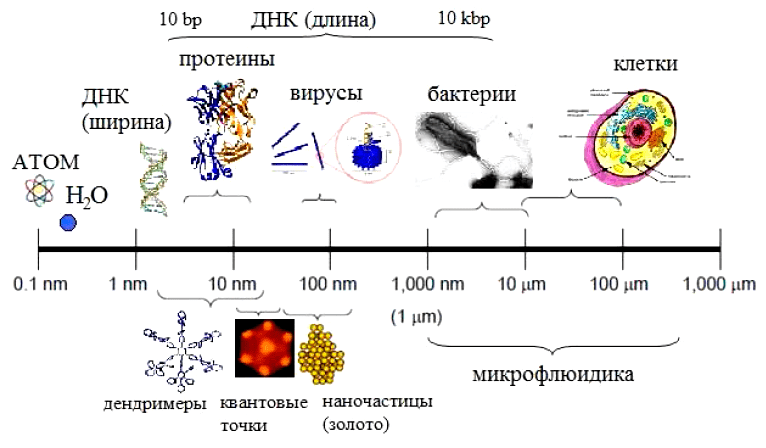
Рисунок 4. Упрощенная шкала масштабов применения нано- и микрофлюидных технологий. С помощью нанотехнологий ученые работают с ДНК, белками и вирусами, в то время как микрофлюидика позволяет анализировать прокариотические и эукариотические единичные клетки.
рисунок автора статьи
Кроме того, мы сможем анализировать ответ единичных клеток, наблюдать их морфологию и очень тонко регулировать условия воздействия на клетку. Такие технологии уже активно используются для различных фундаментальных и прикладных исследований.
Поэтому мы решили, что наш биосенсор на основе флуоресцентных клеток H. pylori будет представлять собой микрофлюидный чип с закрепленными в контрольном и индуцированном каналах единичными клетками. Добавляя в индуцируемые каналы анализируемую смесь (аналит), мы сможем детектировать изменение флуоресценции единичных клеток с помощью микроскопа и сравнивать с контрольным каналом. Увеличение интенсивности флуоресценции будет говорить нам о присутствии определенного фактора в аналите. То есть клетки будут его детектировать.
Важно, чтобы себестоимость биосенсора была невысокой. Поэтому наш чип, заточенный специально под малыша H. pylori, представлял собой трехслойную конструкцию (рис. 5), состоящую из: i) слоя ПММА (полиметилметакрилата), в котором с помощью углекислотного лазера были сформированы два канала; ii) промежуточной «склеивающей» прокладки из композитных материалов; iii) покровного стекла, которое обеспечивало защиту каналов. Размер финальной конструкции составлял всего лишь 7,5×2,5 см (рис. 5). Все эти материалы имеют очень невысокую себестоимость и отлично подходят для одноразового использования. Так, ПММА активно применяют при изготовлении одноразовой лабораторной посуды для культивирования клеточных культур, а покровные стекла знакомы нам еще со школы, и их широко используют при различных микроскопических исследованиях.
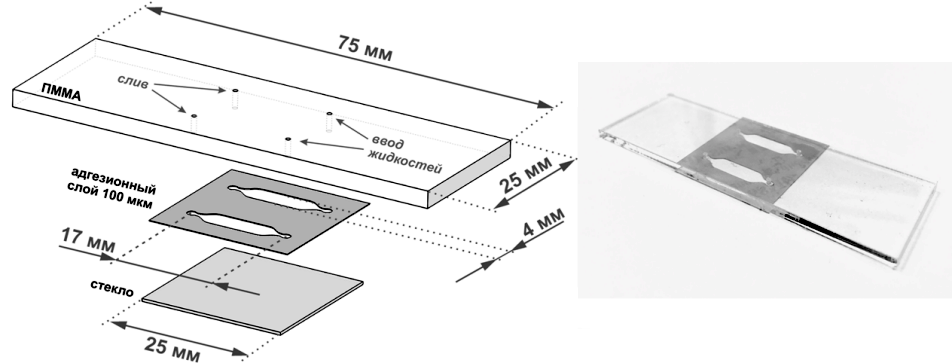
Рисунок 5. Оригинальная конструкция микрофлюидного чипа (слева) и его фотография в собранном виде (справа). На изображении слева сверху вниз показаны ПММА-основа, «склеивающая» прокладка и покровное стекло.
рисунок автора статьи
Мы помнили, что H. pylori очень подвижен благодаря жгутикам на одном из его концов, а скорость его движения превышает таковую у других бактерии [26]. Это препятствует фокусировке микроскопа на единичных клетках. Поэтому чтобы легко регистрировать флуоресценцию неподвижных единичных клеток в канале чипа, мы модифицировали каналы таким образом, чтобы бактериальная клетка была закреплена. Мы использовали свойство адгезии H. pylori, благодаря которому он активно прикрепляется к эпителиоцитам [20], и сделали многослойную модификацию каналов с помощью полиалиламина, глутарового альдегида и затем смеси белков клеточной адгезии (конканавалина и фибронектина). Такая «мягкая перинка» в канале чипа с одной стороны была довольно естественным окружением для H. pylori, а с другой обеспечила нам неподвижность клеток и удобство наблюдения в микроскоп. Один канал чипа служил нам в качестве контроля, а в другой мы добавляли среду, содержащую индукторы наших промоторов для проверки эффективности биосенсора. Для регистрации флуоресценции клеток в каналах мы использовали EMCCD-камеру и эпифлуоресцентный микроскоп с системой поддержания автофокуса. Мы получали фотографии клеток в канале. Далее мы выбирали клетки «вручную» с помощью компьютерной мыши в программном обеспечении микроскопа и нормировали значения флуоресценции единичной клетки на ее площадь (рис. 6). Полученные значения в индуцированном канале мы сравнивали с контрольным каналом. Так как мы выбирали только те клетки, которые характеризовались нормальной морфологией и были в фокусе, то успешно учитывали гетерогенность нашей клеточной популяции и регистрировали флуоресценцию только «здоровых» и живых клеток.
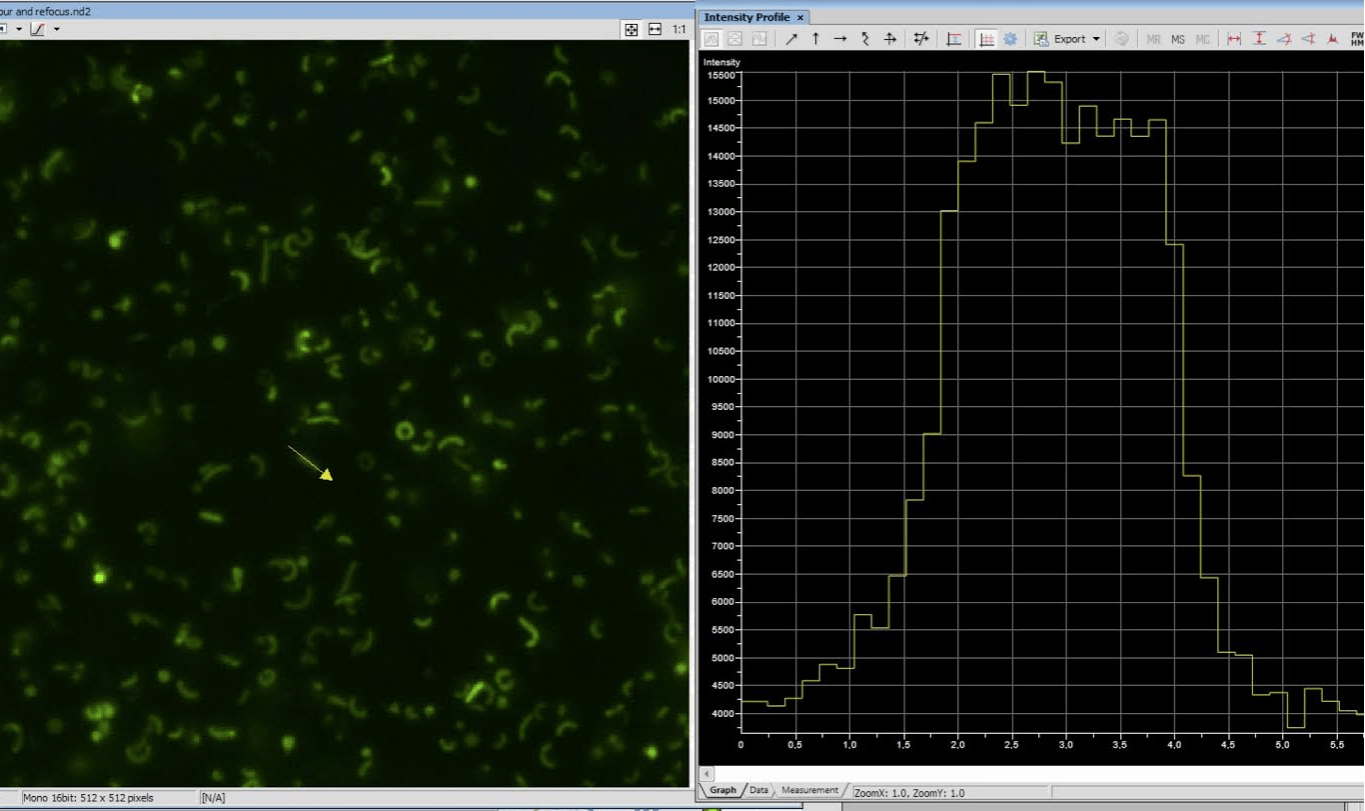
Рисунок 6. Иллюстрация обработки данных, полученных с помощью EMCCD-камеры в программном обеспечении эпифлуоресцентного микроскопа. Снимок компьютерного экрана. Слева единичные клетки H. pylori в одной из областей в канале чипа, на которой сфокусирован микроскоп. Справа график распределения интенсивности клеточной флуоресценции в канале чипа для выбранной области поля. На графике видно, что клеточная флуоресценция представляет собой не единичное значение, а множество различных значений интенсивности от каждой клетки (распределение Гаусса), что подтверждает неоднородность (гетерогенность) клеточной популяции.
изображение получено автором статьи
В результате, полученные нами модифицированные клетки H. pylori не только стабильно флуоресцировали в каналах чипа, но уже через два часа значительно увеличивали уровень флуоресценции в ответ на различные факторы, которые мы добавляли в среду (рис. 7).
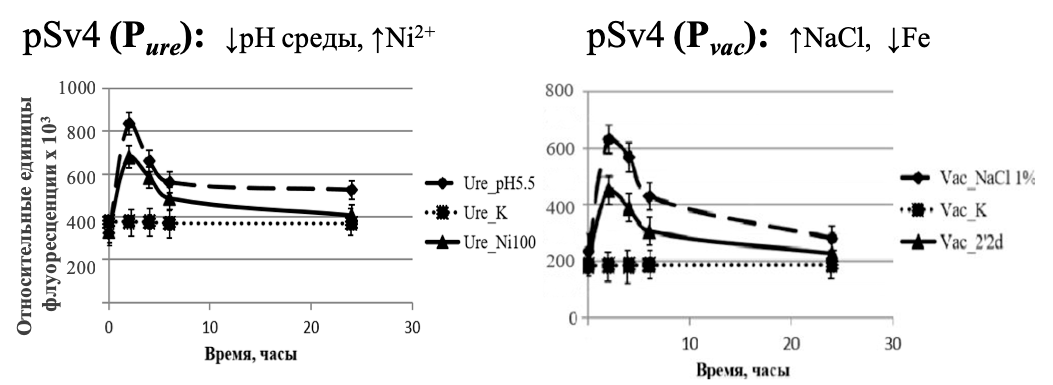
Рисунок 7. Изменение флуоресценции клеток H. pylori, трансформированных репортерными конструкциями в ответ на присутствие индуктора в аналите. Слева: Изменение флуоресценции клеток, содержащих gfp под контролем Pure в ответ на pH 5,5 (добавление HCl) и добавление 100 µМ NiCl2 в течении 24 часов после добавления индукторов. Справа: Изменение флуоресценции клеток, содержащих gfp под контролем Pvac в ответ на осмотический стресс (добавление 1% NaCl) и снижение концентрации железа (добавление 75 µM 2′2-дипиридила) в течение 24 часов после добавления индукторов.
рисунок автора статьи
Причем изменение клеточной флуоресценции можно было зафиксировать даже визуально (рис. 8). Кроме того, наблюдая за клетками в канале чипа на протяжении 24 часов, мы видели, что все это время они сохраняли нормальную морфологию.
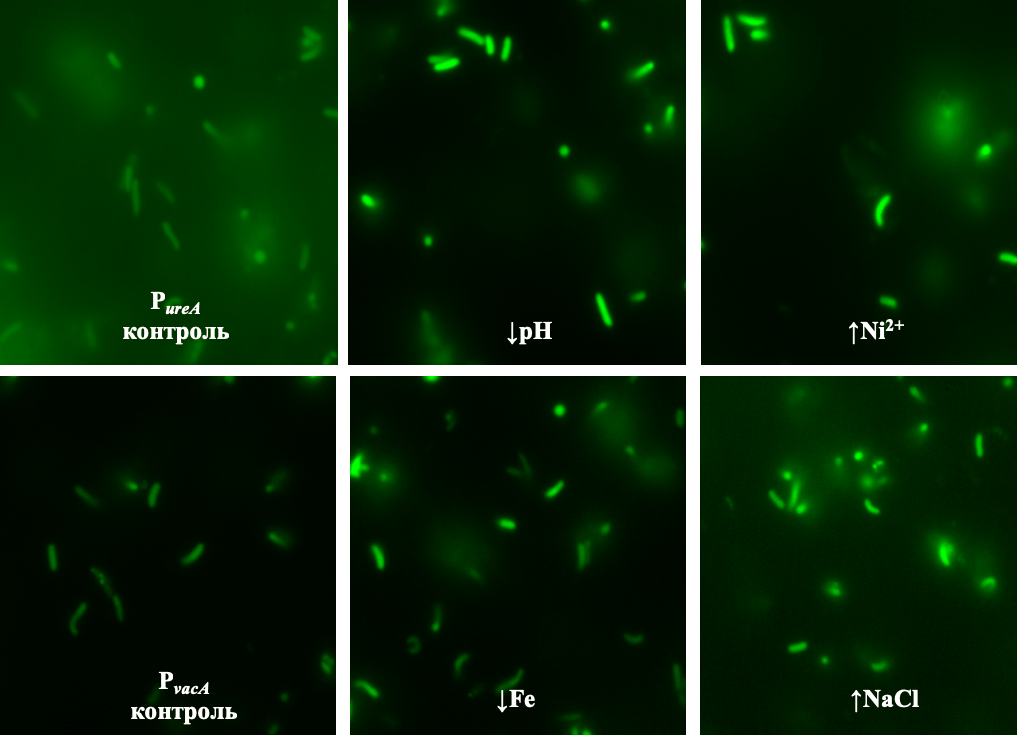
Рисунок 8. Микрофотография зафиксированных единичных флуоресцирующих клеток H. pylori в каналах чипа, содержащих gfp под контролем Pure и Pvac. В каждом случае показаны клетки в контрольных и индуцированных каналах.
изображение получено автором статьи
Итак, нам удалось собрать оригинальный микрофлюидный чип, который позволяет успешно закреплять и длительно культивировать клетки H. pylori, изучая поведение единичной бактериальной клетки [27], [28]. Более того, в случае использования модифицированных флуоресцентных клеток H. pylori такая система «чип + клетки» может служить прототипом биосенсора. Мы успешно детектировали с помощью этой системы такие факторы, как снижение pH, увеличение концентрации ионов никеля, снижение концентрации ионов железа, а также осмотический стресс.
Такой подход открывает удивительные возможности в дальнейшем. Благодаря использованию микрофлюидных технологий, вся механика эксперимента на чипе может быть доведена практически до полного автоматизма, что также значительно увеличит скорость и упростит систему. При этом сам процесс изготовления чипа, себестоимость его составляющих и небольшой расход реактивов обеспечивает системе дешевизну. Бактерия H. pylori обладает большим спектром специфических промоторов, а значит, в дальнейшем, можно собирать самые разные репортерные конструкции и получать модифицированные штаммы H. pylori, способные детектировать еще большее количество различных специфических факторов в области низких концентраций. Потенциально, такую систему можно адаптировать для использования в ранней диагностике следовых маркеров иммунитета человека. Помимо этого, ничто не мешает успешно применять ее для тестирования лекарственных препаратов и совершенствования подходов в антихеликобактерной терапии. Сколько же еще заманчивых перспектив нам откроется в случае таких биосенсоров на основе H. pylori? Время покажет.
Литература
- Marshall B.J. (2005). Autobiography. Nobel Prize;
- Barry J. Marshall, David B. McGechie, Peter A. Rogers, Ross J. Clancy. (1985). Pyloric Campylobacter infection and gastroduodenal disease. Medical Journal of Australia. 142, 439-444;
- Mobley H.L.T., Mendz G.L., Hazell S.L. Helicobacter pylori: physiology and genetics. Washington (DC): ASM Press, 2001;
- Sebastian Suerbaum, Christine Josenhans. (2007). Helicobacter pylori evolution and phenotypic diversification in a changing host. Nat Rev Microbiol. 5, 441-452;
- Behnam Kalali, Raquel Mejías-Luque, Anahita Javaheri, Markus Gerhard. (2014). H. pyloriVirulence Factors: Influence on Immune System and Pathology. Mediators of Inflammation. 2014, 1-9;
- John C. Atherton. (1999). Vacuolating Cytotoxin ( vacA ) Alleles of Helicobacter pylori Comprise Two Geographically Widespread Types, m1 and m2, and Have Evolved Through Limited Recombination. Current Microbiology. 39, 211-218;
- Angela Keane, Pauline Phoenix, Subhasis Ghoshal, Peter C.K. Lau. (2002). Exposing culprit organic pollutants: A review. Journal of Microbiological Methods. 49, 103-119;
- Jonathan D. Van Hamme, Ajay Singh, Owen P. Ward. (2003). Recent Advances in Petroleum Microbiology. Microbiol Mol Biol Rev. 67, 503-549;
- Понаморева О.Н. (2010). Бактериальные биосенсоры для экологического мониторинга углеводородов нефти: мини-обзор. «Известия Тульского государственного университета. Естественные науки». 2, 273–280;
- Oleg N. Kompanets. (2004). Portable optical biosensors for the determination of biologically active and toxic compounds. Usp. Fiz. Nauk. 174, 686;
- Вальдхольц М. (2017). Трансформеры. «В мире науки». 5–6, 126–135;
- Alberts B., Johnson A., Lewis J., Raff M., Roberts K., Walter P. Molecular biology of the cell (5th Edition). USA: Garland Science, 2008. — 1392 p.;
- Søren J Sørensen, Mette Burmølle, Lars H Hansen. (2006). Making bio-sense of toxicity: new developments in whole-cell biosensors. Current Opinion in Biotechnology. 17, 11-16;
- L.H. Hansen, S.J. S rensen. (2001). The Use of Whole-Cell Biosensors to Detect and Quantify Compounds or Conditions Affecting Biological Systems. Microbial Ecology. 42, 483-494;
- Amy Cheng Vollmer, Tina K. Van Dyk. (2004). Stress Responsive Bacteria: Biosensors as Environmental Monitors. Advances in Microbial Physiology. 131-174;
- Hauke Harms, Mona C. Wells, Jan Roelof van der Meer. (2006). Whole-cell living biosensors—are they ready for environmental application?. Appl Microbiol Biotechnol. 70, 273-280;
- Hani A. Alhadrami. (2018). Biosensors: Classifications, medical applications, and future prospective. Biotechnology and Applied Biochemistry. 65, 497-508;
- B E Dunn, G P Campbell, G I Perez-Perez, M J Blaser. (1990). Purification and characterization of urease from Helicobacter pylori.. Journal of Biological Chemistry. 265, 9464-9469;
- John C. Atherton, Ping Cao, Richard M. Peek, Murali K.R. Tummuru, Martin J. Blaser, Timothy L. Cover. (1995). Mosaicism in Vacuolating Cytotoxin Alleles of Helicobacter pylori. Journal of Biological Chemistry. 270, 17771-17777;
- Nayoung Kim, Elizabeth A. Marcus, Yi Wen, David L. Weeks, David R. Scott, et. al.. (2004). Genes of Helicobacter pylori Regulated by Attachment to AGS Cells. Infect Immun. 72, 2358-2368;
- Chun-Hao Huang, Shyh-Horng Chiou. (2011). Proteomic analysis of upregulated proteins in Helicobacter pylori under oxidative stress induced by hydrogen peroxide. The Kaohsiung Journal of Medical Sciences. 27, 544-553;
- S. S. Penfold, A. J. Lastovica, B. G. Elisha. (1988). Demonstration of Plasmids in Campylobacter pylori. Journal of Infectious Diseases. 157, 850-851;
- Yueh-Fen Li, Feng-Yin Li, Chen-Lung Ho, Vivian Hsiu-Chuan Liao. (2008). Construction and comparison of fluorescence and bioluminescence bacterial biosensors for the detection of bioavailable toluene and related compounds. Environmental Pollution. 152, 123-129;
- Bruus H. Theoretical microfluidics. Oxford University Press, 2008;
- Hilde de Reuse, Stefan Bereswill. (2007). Ten years after the firstHelicobacter pylorigenome: comparative and functional genomics provide new insights in the variability and adaptability of a persistent pathogen: Table 1. FEMS Immunol Med Microbiol. 50, 165-176;
- M. L. DePamphilis, Julius Adler. (1971). Attachment of Flagellar Basal Bodies to the Cell Envelope: Specific Attachment to the Outer, Lipopolysaccharide Membrane and the Cytoplasmic Membrane. J Bacteriol. 105, 396-407;
- Белова А.М., Басманов Д.В., Прусаков К.А., Лазарев В.Ф., Клинов Д.В. (2018). Микрофлюидная платформа для создания биосенсора на одиночных генетически модифицированных клетках Helicobacter pylori. «Биофизика». 5, 923–932;
- A.M. Belova, D.V. Basmanov, V.V. Babenko, O.V. Podgorny, T.V. Mitko, et. al.. (2019). Two novel transcriptional reporter systems for monitoring Helicobacter pylori stress responses. Plasmid. 106, 102442.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚