Мир под оболочкой: как микрокапсулы научились хранить, лечить и думать
23 марта 2026
Мир под оболочкой: как микрокапсулы научились хранить, лечить и думать
- 123
- 0
- 2
Изображение биодеградируемых полимерных микрокапсул, полученное с помощью электронной сканирующей микроскопии.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Микрокапсулы — полые полимерные сферы размером от десятков нанометров до десятков микрометров — превратились из экзотической лабораторной технологии в универсальный инструмент для медицины, диагностики и биотехнологии. О том, что это за технология и как исследователям удалось превратить микрокапсулы в миниатюрные хранилища, лекарственные носители и элементы химического «мышления», читайте в этой статье.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Микрокапсулы — это крошечные полые «шарики» с тонкой полимерной оболочкой, внутри которых можно спрятать почти что угодно: ферменты, лекарства, красители, датчики. Это фактически новая форма для работы с хрупкими молекулами.
Потенциал использования у микрокапсул впечатляющий: это и фармакология с необходимостью адресной доставки препаратов , и диагностика, где важна стабилизация ферментов, и биотехнология — от инкапсуляции живых клеток и пробиотиков для защиты их в агрессивной среде до иммобилизации ферментов в биореакторах, и много чего еще.
Об использовании микрокапсул в фарме можно подробнее почитать в статье «Биомиметические наночастицы: как природа помогает доставлять лекарства», опубликованной на «Биомолекуле» [1].
Микрокапсулы становятся «умными системами», которые могут одновременно «хранить», «лечить» и «думать» — о том, как они это делают, поговорим в этой статье.
Что такое полиэлектролитные микрокапсулы и как их собирают?
Микрокапсулы представляют собой полые структуры с оболочками из полимеров-электролитов, в которых можно инкапсулировать активные вещества (ферменты, лекарственные молекулы и др.), обеспечивая их защиту, удержание и контролируемое высвобождение. Они всегда небольшого размера — он варьируется от 50 нм до 20 мкм. Полимеров, пригодных для создания микрокапсул, существует множество [2].
При выборе материала, из которого будет состоять микрокапсула, ученые обычно ориентируются на такие свойства, как биосовместимость, нетоксичность, а также насыщенность функциональными группами (–OH, –NH2, –COOH), которые делают их удобными для сшивания слоев между собой и конъюгации биоактивных молекул [3].
Чтобы микрокапсула появилась на свет, мало одних лишь материалов — ее нужно собрать. Для этого исследователи применяют метод послойной сборки (layer-by-layer, LbL) (рис. 1). Такой конструктор позволяет довольно тонко регулировать параметры микрокапсул, важные для адресной доставки препаратов: например, проницаемость, толщину стенки, буферную емкость [4]. Именно их необходимо учитывать при построении системы, рассчитанной на доставку, например, ферментов, поскольку любая ферментная молекула работает только в узком диапазоне условий — ей нужен определенный pH, доступ субстрата и защита от инактивации.
Настроив стенку так, чтобы субстрат легко проникал внутрь, а сам фермент был надежно удержан и изолирован от резких сдвигов среды, можно добиться стабильной активности в течение длительного времени. А управляя толщиной и плотностью слоев, исследователь задает, насколько быстро капсула «откликнется» на сигнал и при каких условиях начнет высвобождать содержимое — это критично для терапевтических систем, где важны и место, и момент действия [5].
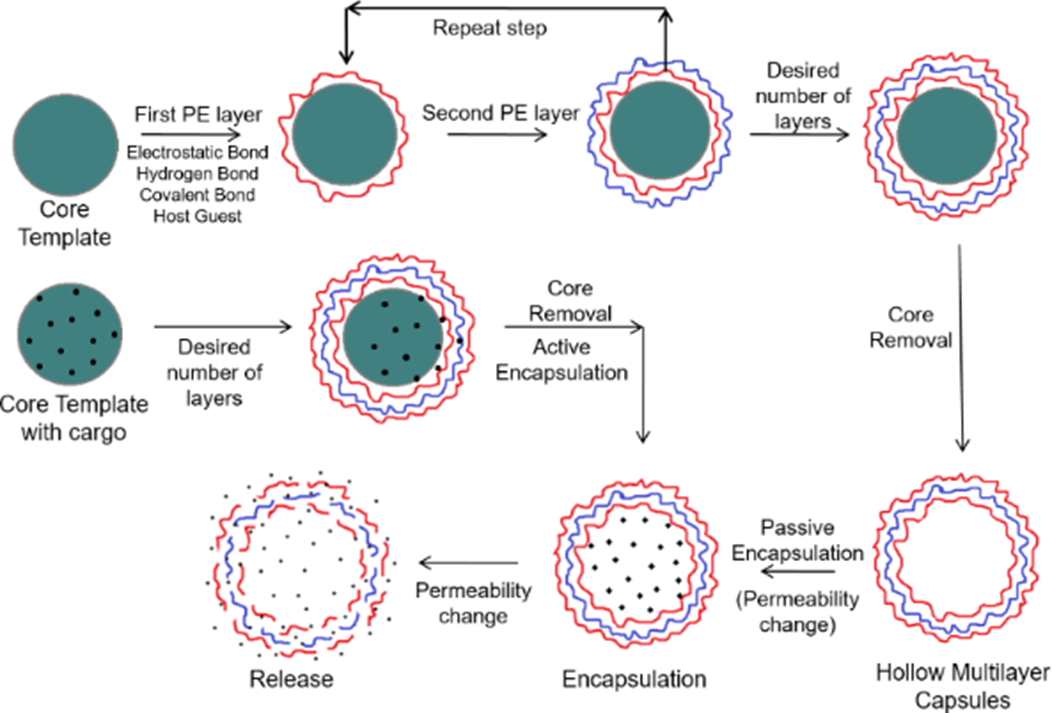
Рисунок 1. На схеме показан полный цикл получения полиэлектролитных микрокапсул методом послойной сборки (LbL). Процесс начинается с шаблонной частицы — твердого ядра, на поверхности которого — инкапсуляция. Заключительный этап — управляемое высвобождение: изменение проницаемости многослойной оболочки позволяет контролировать, как быстро и в каком объеме содержимое покидает капсулу. Так формируются полые или загруженные микрокапсулы с заданными свойствами для диагностики, доставки молекул или сенсорных систем.
Как капсулы научились «хранить»
Мы иногда даже не подозреваем, как много важных для здоровья анализов делаются ферментными методами — а ведь на самом их очень много (табл.1). Микрокапсулы в рассматриваемых системах выступают не как вспомогательный элемент, а как функциональный модуль, определяющий стабильность, воспроизводимость и режим работы анализа.
| Метод | Суть метода | Примеры анализов | Ссылки |
|---|---|---|---|
| Ферментный колориметрический метод (уреаза–Berthelot и аналоги) | Фермент (например, уреаза) специфически расщепляет мочевину до NH3 и CO2. Освободившийся аммиак далее определяется цветной реакцией (Berthelot): аммиак реагирует с фенолом/салицилатом и гипохлоритом в присутствии катализатора, образуя окрашенный комплекс; оптическая плотность пропорциональна концентрации мочевины | Мочевина в сыворотке и моче; аналогичные ферментные колориметрические тесты используют для аммиака и ряда других метаболитов | academic.oup.com |
| Общие ферментные колориметрические/спектрофотометрические тесты в клин. биохимии | Оксидазы, дегидрогеназы и другие ферменты превращают аналит в продукт, который либо сам имеет характерную абсорбцию, либо включен в каскад (например, изменение концентрации НАДH при 340 нм). По изменению оптической плотности рассчитывают концентрацию аналита или активность фермента | Глюкоза, холестерин, триглицериды, лактат, ряд печеночных и сердечных маркеров (через сопряженные ферментные реакции) | pmc.ncbi.nlm.nih.gov, researchgate.net |
| Электрохимические ферментные биосенсоры (глюкоза, лактат и др.) | Фермент (чаще оксидаза или дегидрогеназа) иммобилизован на электроде вместе с проводящими материалами (наночастицы, нанотрубки и т.п.). При взаимодействии субстрата образуются электроактивные продукты или происходит прямая электронная передача к электроду; измеряемый ток/потенциал коррелирует с концентрацией аналита | Глюкоза (глюкометры), лактат (в крови, поте), холестерин, этанол, мультимодальные сенсоры (глюкоза + лактат) | pubs.rsc.org, mdpi.com |
Одна из ключевых проблем в таких аналитических ферментных системах — их стабильность, так как ферменты очень чувствительны ко внешним факторам. Но если их заключить в микрокапсулу, то система становится значительно удобнее — возрастают ее стабильность и срок жизни: инкапсулированный фермент работает дольше и ведет себя более предсказуемо. Многослойная оболочка защищает ферменты от резких изменений pH, температуры и действия протеаз, при этом пропуская внутрь низкомолекулярные субстраты и выведенные продукты реакции [7].
Конечно же, исследователи довольно быстро разработали инструменты на основе микрокапсул, которые помогали бы оптимизировать лабораторные анализы. Удачный пример тому — тест на мочевину от команды С.Тихоненко [8]. Ученые из его группы заключили фермент уреазу в микрокапсулы из противоположно заряженных полиаллиламина и полистиролсульфоната — и разработали две системы тестирования. Одна из них представляла собой просто суспензию микрокапсул (ее назвали «микродиагностикумом»), а вторая — закрепленные на подложке микрокапсулу (ее назвали «диагностической пластинкой»). Диагностика в обоих случаях происходила по стандартной схеме за счет работы уреазы (рис. 2).
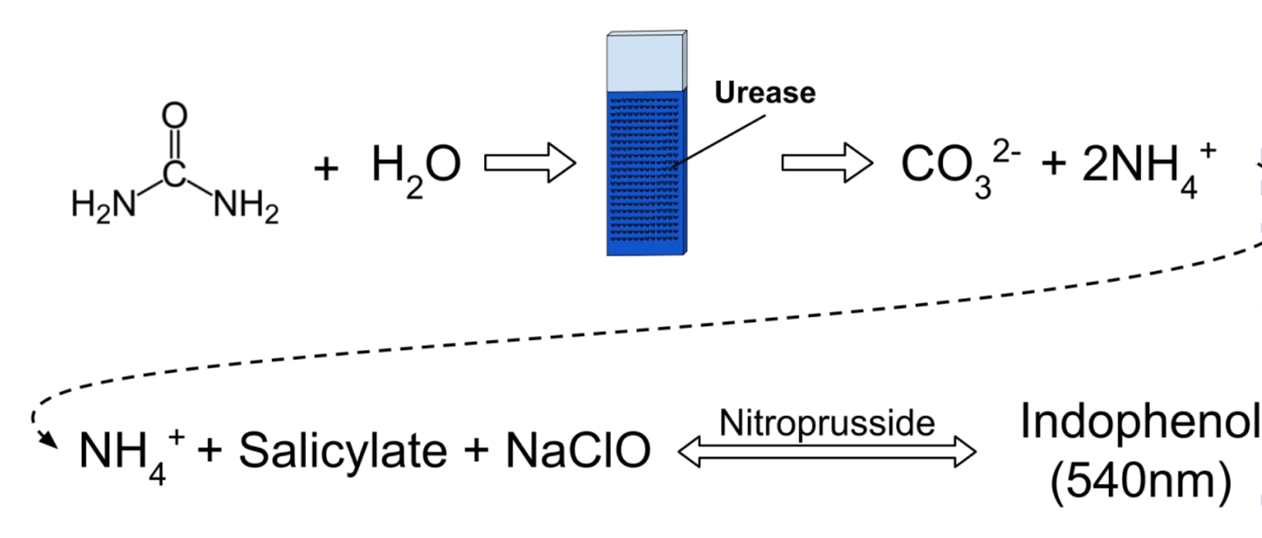
Рисунок 2. Схема ферментативного гидролиза мочевины уреазой с образованием карбонат-иона и аммония и последующего колориметрического определения ионов NH4+ по реакции Бертло с образованием индофенола, регистрируемого при 540 нм.
Оба теста по точности и чувствительности оказались сопоставимы с классическим тестом, но имели одно существенное преимущество. И диагностикум, и диагностическую пластинку можно использовать неоднократно — фермент не разрушается и точность измерения не снижается [8].
Такой подход очень принципиален для промышленных тест-систем, где нужно проводить огромное количество анализов — например, при тестировании качества удобрений в случае с мочевиной. Превратив «раствор фермента» в капсульный модуль, можно потенциально удлинять срок годности диагностической системы, снизить требования к условиям ее хранения и получать результаты с меньшими усилиями.
Как капсулы научились «лечить»
Лекарства (будь то простой ибупрофен или серьезная химиотерапия) действуют на организм системно, циркулируя в кровотоке, куда попадают через слизистые или напрямую через катетеры. В случае с нурофеном это большого урона организму не наносит, а вот в случае с химиотерапией здоровые клетки могут сильно пострадать. Ученые давно ищут способы доставлять препараты адресно — конкретно к тому органу или ткани, где они требуются.
Помимо токсичной противоопухолевой терапии, направленная доставка лекарств важна в случае, когда лекарство требуется донести в целости и сохранности — например, при введении в организм инсулина. Оболочка капсул способна удерживать его в агрессивной среде желудка, защищая его от ферментов и повышенной кислотности, и становиться проницаемой или разрушаться уже в кишечнике, где pH и ферментная активность иные [10]. Еще более продвинутый дизайн микрокапсул позволяет делать их чувствительными к глюкозе — например, с ферментами или «глюкозочувствительными» полимерами на поверхности, так что при повышении сахара оболочка «открывается» и инсулин высвобождается [11]. Такая подача препарата минимизирует риск гипогликемии и снижает нагрузку на печень. Не говоря уже об удобстве пациента, которому не нужно в таком случае постоянно носить с собой шприц и отслеживать уровень сахара в крови.
Похожим образом дела обстоят в случае с заболеваниями ЖКТ — язвенным колитом, болезнью Крона, локальными опухоли толстой кишки — препараты при этих патологиях требуют доставки препаратов точно «на место», потому что системная терапия малоэффективна и дает много побочных эффектов. Микрокапсулы пригождаются и здесь — pH-чувствительные оболочки уверенно «переживают» желудок, где среда сильно кислая, и раскрываются уже в кишечнике, где pH выше. Другой подход для таргетной доставки в кишечник — капсулы на основе полисахаридов (например, альгината, пектина, хитозана), которые разрушаются под действием микрофлоры толстой кишки и тем самым высвобождают препарат именно там, где он нужен [12].
Помимо рН чувствительных оболочек, существуют окислительно-восстановительные и АФК-чувствительные системы, где в полимер или сшивающие агенты встраивают дисульфидные или перекисно-чувствительные фрагменты: в воспаленной ткани или опухолевой микросреде с высоким уровнем H2O2 и восстановителей эти связи рвутся, и капсула раскрывается [13].
Вариант попроще — ион-чувствительные оболочки, которые теряют устойчивость при росте ионной силы или при изменении концентрации определенных ионов. Одним из первых наглядных примеров ион-чувствительного разрушения многослойных капсул стал эксперимент с оболочками, собранными из ДНК и спермидина — полианиона и поликатионного биомолекулярного лиганда. Эти два компонента легко формируют плотные многослойные структуры за счет сильного электростатического притяжения: отрицательно заряженная ДНК взаимодействует с положительно заряженным спермидином, создавая устойчивый комплекс, который можно «наслаивать» друг на друга в режиме слой за слоем [14]. Если поместить такую капсулу в концентрированный солевой раствор (например, 5M NaCl, раствор хлорида натрия с молярной концентрацией 5 моль/л), ситуация меняется: огромное количество ионов натрия и хлора экранируют заряды ДНК и спермидина. Электростатическое взаимодействие резко ослабевает, и многослойная структура просто «рассыпается» — слои теряют сцепление, оболочка дезинтегрирует, а капсула распадается.
Еще один из наиболее востребованных сегодня механизмов — ферментативное разрушение, когда капсулы делают из полисахаридов, пептидов или нуклеиновых кислот, расщепляемых ферментами, типичными для целевой зоны: протеазами опухоли, ферментами микрофлоры толстой кишки в случае с заболеваниями ЖКТ и т. д. [15].
Наконец, один из самых очевидных способов организовать адресную доставку капсул — «пометить» их поверхностным лигандом, который узнает нужные клетки или ткани. В этом случае логика проста: сначала капсула должна прийти именно туда, где требуется терапия, а уже затем — раскрыться под действием локальных триггеров. На поверхность многослойных капсул легко «навешивают» антитела или их фрагменты, нацеленные на опухолевые или воспалительные маркеры [16]; пептиды-лиганды, узнающие рецепторы на эндотелии и быстро пролиферирующих опухолевых клетках [17]; или гиалуроновую кислоту, обеспечивающую точное попадание в CD44-положительные клетки (клетки, на поверхности которых присутствует белок CD44, играющий ключевую роль в прикреплении клетки к окружающему матриксу и регуляции ее поведения в ткани), типичные для ряда опухолей и воспаленных тканей [18].
Как капсулы научились «думать»
Если взять набор капсул с разными ферментами внутри, то можно построить целый биопроцессор, в котором каждая капсула реагирует только на свои молекулы — свой метаболит — и дает свой вклад в общий сигнал. Если специально спроектировать оболочку, такая система начинает вести себя как логический элемент. Например, в работе Krishna Radhakrishnan 2013 года микрокапсулы из протамина и хондроитинсульфата разрушались и высвобождали груз, если в растворе присутствовал либо трипсин, либо гиалуронидаза — любого из двух ферментов было достаточно, чтобы «активировать» выход [19]. По сути, исследователи создали биохимический аналог логического элемента OR и реализовали его на капсулах.
Если хочется использовать логический элемент AND, то схему надо строить иначе. Например, разделить несколько ферментов по разным «карманам» внутри одной многокамерной капсулы и связать их каскадом, в котором продукт первой реакции служит субстратом для второй, и так далее [20]. В такой схеме заметный сигнал возникает только если запущены все ступени каскада, то есть присутствуют сразу несколько необходимых субстратов — поведение уже ближе к логике AND.
Чтобы превратить получившиеся операторы в микролабораторию, «биологическую логику» нужно связать с электроникой. Здесь появляются многостенные углеродные нанотрубки (MWCNT) и микроэлектроды. В работе Александра Решетилова полимерные микрокапсулы PAH/PSS с глюкозооксидазой встроили в проводящую сеть из MWCNT и нанесли на электрод. В результате сопротивление структуры упало почти на два порядка, а чувствительность к глюкозе заметно выросла: ток на единицу концентрации оказался значительно выше, чем у системы с капсулами без нанотрубок [21]. Капсула в таком случае перестает быть просто «коробочкой с ферментом» и превращается в интерфейс между химической реакцией внутри и углеродной проводящей матрицей снаружи.
Такой гибрид хорошо ложится на архитектуру современных носимых и портативных сенсоров: тонкий или гибкий электрод, покрытый углеродными наноматериалами, и сверху — биомодуль. Если на одном маленьком чипе разместить несколько таких «биомодулей» — капсулы с глюкозооксидазой, уреазой, лактатоксидазой и так далее, — можно снимать уже не один показатель, а целую панель метаболитов. Именно к таким мультиплексным, часто носимым системам сейчас движутся электрохимические сенсоры для пота [22], межтканевой жидкости и капли крови [23].
Что дальше
Капсульный картридж очень удобно было бы применять в отделении нефрологии или эндокринологии, где он сможет работать как многофункциональный «глюкометр». К примеру, в одном одноразовом картридже — панель микрокапсул с уреазой, глюкозооксидазой, лактатоксидазой и другими ферментами по запросу. Пациент с хронической болезнью почек или диабетом приносит каплю крови, сыворотки или фильтрат — а картридж за минуту выдает профиль: мочевина, креатинин, глюкоза, лактат, и т.д. Такой подход уже пробуют в мультиплексных сенсорных платформах для онкологии [23] и кардиологии [24], где под каждую клиническую задачу собирают свою комбинацию биомаркеров.
Если все это получится довести до рутины, для врача и пациента капсульный картридж будет всего лишь еще одним привычным прибором на столе. Однако за простой кнопкой «измерить» окажется сложная архитектура из микрокапсул и ферментов, которая сейчас только формируется в лабораториях. И чем лучше ученые научатся собирать такие системы сегодня, тем надежнее и точнее будет выглядеть повседневная медицина завтра.
Литература
- Биомиметические наночастицы: как природа помогает доставлять лекарства;
- Miju Kim, Seon Ju Yeo, Christopher B. Highley, Jason A. Burdick, Pil J. Yoo, et. al.. (2015). One-Step Generation of Multifunctional Polyelectrolyte Microcapsules via Nanoscale Interfacial Complexation in Emulsion (NICE). ACS Nano. 9, 8269-8278;
- Wenyan Li, Xuejiao Lei, Hua Feng, Bingyun Li, Jiming Kong, Malcolm Xing. (2022). Layer-by-Layer Cell Encapsulation for Drug Delivery: The History, Technique Basis, and Applications. Pharmaceutics. 14, 297;
- Alexey V. Dubrovskii, Aleksandr L. Kim, Sergey A. Tikhonenko. (2024). The Buffer Capacity of Polyelectrolyte Microcapsules Depends on the Type of Template. Polymers. 16, 2261;
- Katsuhiko Ariga, Mike McShane, Yuri M Lvov, Qingmin Ji, Jonathan P Hill. (2011). Layer-by-layer assembly for drug delivery and related applications. Expert Opinion on Drug Delivery. 8, 633-644;
- Varsha Sharma, Anandhakumar Sundaramurthy. (2020). Multilayer capsules made of weak polyelectrolytes: a review on the preparation, functionalization and applications in drug delivery. Beilstein J. Nanotechnol.. 11, 508-532;
- Gayong Shim, Gunwoo Kim, Junhyeok Choi, TacGhee Yi, Yun Kyoung Cho, et. al.. (2015). Biomimetic chimeric peptide-tethered hydrogels for human mesenchymal stem cell delivery. Colloids and Surfaces B: Biointerfaces. 136, 634-640;
- Aleksandr L. Kim, Egor V. Musin, Alexey V. Dubrovskii, Sergey A. Tikhonenko. (2019). Determination of urea concentration using urease-containing polyelectrolyte microcapsules. Anal. Methods. 11, 1585-1590;
- Yashdeep Mukheja, Santhosh Nayak Kethavath, Linga Banoth, Sandip V. Pawar. (2024). Lignin: The green powerhouse for enzyme immobilization in biocatalysis and biosensing. International Journal of Biological Macromolecules. 280, 135940;
- Büşra Arpaç, Burcu Devrim Gökberk, Berrin Küçüktürkmen, Işıl Özakca Gündüz, İsmail Murat Palabıyık, Asuman Bozkır. (2023). Design and in vitro/in vivo Evaluation of Polyelectrolyte Complex Nanoparticles Filled in Enteric-Coated Capsules for Oral Delivery of Insulin. Journal of Pharmaceutical Sciences. 112, 718-730;
- Yanguang Yang, Xiangqian Wang, Xiaopeng Yuan, Qiwei Zhu, Shusen Chen, Donglin Xia. (2022). Glucose-activatable insulin delivery with charge-conversional polyelectrolyte multilayers for diabetes care. Front. Bioeng. Biotechnol.. 10;
- Anil Philip, Betty Philip. (2010). Colon Targeted Drug Delivery Systems: A Review on Primary and Novel Approaches. OMJ. 25, 70-78;
- Edurne Marin, Neha Tiwari, Marcelo Calderón, Jose-Ramon Sarasua, Aitor Larrañaga. (2021). Smart Layer-by-Layer Polymeric Microreactors: pH-Triggered Drug Release and Attenuation of Cellular Oxidative Stress as Prospective Combination Therapy. ACS Appl. Mater. Interfaces. 13, 18511-18524;
- Corinna Schüler, Frank Caruso. (2001). Decomposable Hollow Biopolymer-Based Capsules. Biomacromolecules. 2, 921-926;
- Egor V. Musin, Aleksandr L. Kim, Sergey A. Tikhonenko. (2022). Substance Release from Polyelectrolyte Microcapsules. Encyclopedia. 2, 428-440;
- Angus P. R. Johnston, Marloes M. J. Kamphuis, Georgina K. Such, Andrew M. Scott, Edouard C. Nice, et. al.. (2012). Targeting Cancer Cells: Controlling the Binding and Internalization of Antibody-Functionalized Capsules. ACS Nano. 6, 6667-6674;
- Stefaan De Koker, Liesbeth J. De Cock, Pilar Rivera-Gil, Wolfgang J. Parak, Rachel Auzély Velty, et. al.. (2011). Polymeric multilayer capsules delivering biotherapeutics. Advanced Drug Delivery Reviews. 63, 748-761;
- Fatih Ciftci, Ali Can Özarslan, İmran Cagri Kantarci, Aslihan Yelkenci, Ozlem Tavukcuoglu, Mansour Ghorbanpour. (2025). Advances in Drug Targeting, Drug Delivery, and Nanotechnology Applications: Therapeutic Significance in Cancer Treatment. Pharmaceutics. 17, 121;
- Krishna Radhakrishnan, Jasaswini Tripathy, Ashok M. Raichur. (2013). Dual enzyme responsive microcapsules simulating an “OR” logic gate for biologically triggered drug delivery applications. Chem. Commun.. 49, 5390;
- Qingli Qu, Xiaoli Zhang, Anquan Yang, Jing Wang, Weixia Cheng, et. al.. (2022). Spatial confinement of multi-enzyme for cascade catalysis in cell-inspired all-aqueous multicompartmental microcapsules. Journal of Colloid and Interface Science. 626, 768-774;
- Anatoly Reshetilov, Yulia Plekhanova, Sergei Tarasov, Sergei Tikhonenko, Alexey Dubrovsky, et. al.. (2019). Bioelectrochemical Properties of Enzyme-Containing Multilayer Polyelectrolyte Microcapsules Modified with Multiwalled Carbon Nanotubes. Membranes. 9, 53;
- Fupeng Gao, Chunxiu Liu, Lichao Zhang, Tiezhu Liu, Zheng Wang, et. al.. (2023). Wearable and flexible electrochemical sensors for sweat analysis: a review. Microsyst Nanoeng. 9;
- Connor O’Brien, Chun Keat Khor, Sina Ardalan, Anna Ignaszak. (2024). Multiplex electrochemical sensing platforms for the detection of breast cancer biomarkers. Front. Med. Technol.. 6;
- Nandhinee Radha Shanmugam, Sriram Muthukumar, Ambalika Sanjeev Tanak, Shalini Prasad. (2018). Multiplexed Electrochemical Detection of Three Cardiac Biomarkers cTnI, Ctnt and Bnp Using Nanostructured ZnO-sensing Platform. Future Cardiol.. 14, 131-141.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚