
Рак щитовидной железы — всё не так страшно, как мы привыкли думать!
28 ноября 2019
Рак щитовидной железы — всё не так страшно, как мы привыкли думать!
- 75724
- 1
- 5
-
Авторы
-
Редакторы
Статья на конкурс «био/мол/текст»: Рак — та проблема, которая так или иначе волнует каждого из нас, а некоторых, к сожалению, коснулась напрямую. Сегодня заболеваемость онкологическими патологиями неуклонно растет. Однако сейчас мы бы хотели поговорить с вами о том виде рака, который бояться в большинстве случаев совсем не нужно! Это рак щитовидной железы. Заинтригованы? Читайте эту статью.
Конкурс «био/мол/текст»-2019
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2019.

Генеральный спонсор конкурса и партнер номинации «Сколтех» — Центр наук о жизни Сколтеха.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступила компания BioVitrum.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Несомненно, XXI век — время развития научно-технического прогресса. Вместе с совершенствованием технологий приходит и их доступность в повсеместном использовании. Медицина не является исключением. Благодаря развитию технологий диагностики и лечения самых разных заболеваний мы стали спасать тех пациентов, которые когда-то входили в число неизлечимых. Однако не на все сферы медицины прогресс повлиял так положительно. Поэтому сегодня мы бы хотели познакомить вас с такими животрепещущими вопросами медицины, как гипердиагностика и гиперлечение. Сейчас мы остановимся лишь на одной, но весьма значимой стороне данной проблемы — гипердиагностика узлов щитовидной железы, а также гиперлечение этих узлов и рака щитовидной железы.
Что мы знаем сегодня про узлы щитовидной железы?
26 сентября 2019 года в группе «Медфронт» во «ВКонтакте» появилась небольшая статья Александра Циберкина, врача-эндокринолога, создателя блога «Занимательная эндокринология» [1]. Проблема, которая поднималась в статье, достаточно проста: многим из нас когда-то предлагали сделать УЗИ щитовидной железы на всякий случай. На наш взгляд, Александр рассказывает о проблеме гипердиагностики и гиперлечения для того, чтобы врачи всерьез задумались, правильно ли назначать не всегда нужные анализы всем, и насколько серьезной проблемой является обнаружение узла в щитовидной железе в процессе такого скрининга.
Однако то, что эта проблема была озвучена совсем недавно, не значит, что о ней больше не надо писать. Мы не хотим загружать вас медицинской терминологией, вновь писать о TI-RADS и разбирать по кусочкам, что может написать функциональный диагност в заключении. Мы обращаемся к вам в качестве потенциальных пациентов и хотим донести мысль, что не всегда узел в щитовидной железе опасен, а рак априори смертелен.
База, с которой нам нужно познакомиться: щитовидная железа
Немножко о щитовидной железе (ЩЖ). Это орган эндокринной системы человека, который располагается на передней поверхности шеи в области гортани, прямо перед щитовидным хрящом. Состоит железа из левой и правой долей и перешейка. ЩЖ богато кровоснабжается разными артериями, а иннервируется гортанными нервами.
Главной функцией щитовидной железы (лат. glandula thyroidea) является синтез тиреоидных гормонов, необходимых нашему организму. Под тиреоидными гормонами мы подразумеваем два соединения: тироксин (Т4) и трийодтиронин (Т3). Основной функцией Т4 и Т3 является увеличение потребления клетками кислорода. Иначе говоря, эти гормоны стимулируют все энергетические процессы в клетке и обмен веществ, причем их влияние распространяется на все клетки организма.
Также клетки ЩЖ производят кальцитонин, ответственный за обмен кальция в организме.
Прямо за щитовидной железой располагаются четыре небольшие паращитовидные железы. Последние производят паратиреоидный гормон, который также отвечает за поддержание уровня кальция в организме, причем в большей степени, чем кальцитонин.
Откуда берется столько случаев рака щитовидки?
Рак щитовидной железы (РЩЖ) — наиболее распространенное злокачественное новообразование эндокринной системы [2]. Все чаще мы слышим, что заболеваемость РЩЖ неуклонно растет. И звучит это ужасающе, однако так ли всё просто на самом деле? Возможно, вы будете шокированы, какая правда скрывается за этими, на первый взгляд, однозначными научными фактами. И прежде, чем мы разберемся с истинной причиной роста заболеваемости РЩЖ, необходимо ознакомиться с тем, какие виды рака щитовидки существуют.
Итак, начнем. Сейчас нам понадобится привести немного численных данных, но не пугайтесь их, всё крайне просто. В научном сообществе выделяют пять типов РЩЖ:
- Папиллярный (80–85% случаев).
- Фолликулярный (10–15% случаев).
- Медуллярный (5% случаев).
- Низкодифференцированный (1% случаев).
- Недифференцированный (0,1–0,2% случаев).
Наиболее благоприятными принято считать два первых типа РЩЖ. И как мы можем заметить, они встречаются наиболее часто. Их также называют высокодифференцированными типами рака. Медуллярный, низкодифференцированный и недифференцированный типы считаются агрессивными формами РЩЖ. В нашей статье мы сделаем акцент лишь на первых двух типах РЩЖ, так как они являются наиболее распространенными.
Что означает понятие «дифференцировка»?
Когда-то давно, еще до нашего рождения, каждый из нас представлял собой одну-единственную клетку. Во время внутриутробного развития клеток стало в триллионы раз больше! И каждая из них обрела свою собственную функцию: одни отвечают за биение нашего сердца, другие защищают наш организм от внешних и внутренних опасностей, а третьи отвечают за когнитивные функции. И таких видов клеток более 230! Путь, который проходит клетка от той единственной, стоявшей в начале нашего пути, до высоко специализированной клетки, у которой есть четкие обязанности, и называется «дифференцировка».
Что касается рака — если клетки, из которых состоит опухоль, являются высокодифференцированными, в большинстве случаев врачи считают исход благоприятным. Однако если опухоль состоит из низкодифференцированных клеток, то с большой вероятностью она склонна к агрессивному течению. Как уже было сказано, наиболее часто выявляемые РЩЖ являются высокодифференцированными.
Папиллярный РЩЖ — наиболее распространенная форма: 80–85%. И с самым хорошим прогнозом. Пятилетняя выживаемость пациентов с РЩЖ — 98,1% [2]. Что это значит для пациента? Что наиболее часто выявляемые случаи РЩЖ имеют благоприятный исход!
Рак, ушедший в себя
Наше традиционное понимание РЩЖ, а именно его развития, в корне изменилось благодаря трем исследованиям 2014 года (Thyroid cancer trilogy) [3–5]. Казалось бы, все злокачественные образования по мере развития подвергаются прогрессии, а потому нуждаются в ранней диагностике и оперативном лечении. Впервые за всю историю человека было обнаружено существование «самоограничивающихся раков» (self-limiting cancers), которые являются злокачественными, но при этом не прогрессируют в летальные формы из-за ограниченной способности к делению клеток, составляющих опухоль. Конечно же, существуют и так называемые летальные РЩЖ (lethal thyroid cancers). Различие между ними заключается в происхождении раковых клеток, что и определяет развитие заболевания и его исход. Во втором случае клетки как бы затаиваются на долгий срок, на годы и даже на десятилетия, а потом по невыясненным еще причинам внезапно начинают делиться и приводят к неблагоприятному исходу. Однако на данный момент считается, что именно «самоограничивающиеся» типы РЩЖ составляют большинство.
Подбираемся к корню проблемы: статистика и диагностика
Вернемся к распространенности РЩЖ. Теперь мы готовы понять, что возросшее число случаев данной патологии не является поводом для беспокойства.
В 1975 году заболеваемость РЩЖ составляла 4,9 на 100 000 человек и оставалась относительно стабильной до начала 1990-х годов [6]. За последние 25 лет заболеваемость РЩЖ выросла более чем в 3 раза, то есть на 300% (рис. 1) [7], [8], причем в большинстве случаев за счет высокодифференцированного папиллярного РЩЖ. При этом очень важно понимать, что, несмотря на такой значительный рост, смертность от РЩЖ остается стабильной, примерно 0,5 случаев на 100 000 человек [6].
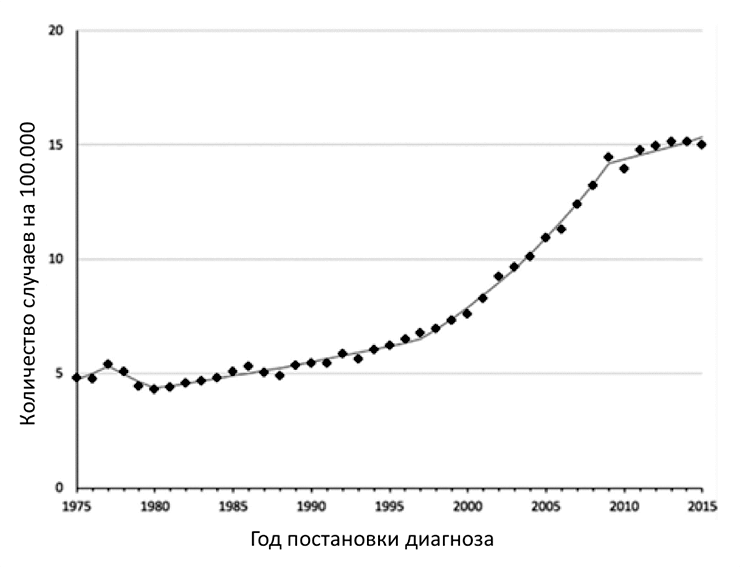
Рисунок 1. Данные заболеваемости раком щитовидной железы в период с 1975 по 2015 годы
Чувствуете, что тут что-то не так? Нет связи между возросшим числом случаев РЩЖ и смертностью от этой патологии! Среди врачей и ученых до сих пор продолжаются дебаты, почему так происходит. Сейчас выделяют несколько теорий. Наиболее вероятная — широкое распространение методов ультразвуковой диагностики (УЗИ). Пусть корни УЗИ уходят к Леонардо да Винчи и XV веку, широкое медицинское распространение данный метод получил с 50-х годов XX века [9], [10]. Сегодня УЗИ является наиболее простым, дешевым, неинвазивным и информативным методом выявления опухолевых образований щитовидной железы. Поэтому, как вы можете догадаться, УЗИ стали делать почти всем, причем независимо от показаний.
Сейчас научное сообщество активно дискутирует на тему, связаны ли такие показатели с истинным увеличением заболеваемости РЩЖ, или же проблема в гипердиагностике тех небольших образований ЩЖ, которые не требуют никакого вмешательства со стороны человека [11], [12].
Для более полного понимания проблемы вернемся на чуть более ранний этап диагностики РЩЖ.
Что такое узлы и как их найти?
Узлы ЩЖ — это радиологически различимые объемные образования в ЩЖ, которые могут быть доброкачественными и злокачественными. Узлы можно найти в 50% случаев всех проводимых УЗИ ЩЖ. При этом только 5% выявляемых образований будут злокачественными [13], [14].
Весомый вклад УЗИ в возросшее количество диагностированных узлов и РЩЖ можно показать на примере одного нашумевшего исследования в Южной Корее [3], [15], [16]. В 1999 году там была утверждена национальная программа, направленная на скрининг злокачественных заболеваний. Под программу попала и щитовидная железы. В результате повсеместного внедрения УЗИ щитовидки частота выявления рака выросла в 15 (!) раз с 1993 по 2011 год. И это мы еще не говорим просто об узлах, которые также могут быть психологической проблемой пациента. Большинство выявляемых случаев — папиллярный РЩЖ. Как вы помните, этот вид рака имеет весьма благоприятный исход. Однако простому населению идея жить с раком настолько чужда и неприятна, что было проведено огромное число полного удаления щитовидных желез, причем часто без видимой на то необходимости! А такая операция имеет серьезные последствия, о которых мы расскажем чуть ниже.
Врачи, осознав свою ошибку, убрали УЗИ щитовидки из списка обязательных скрининговых тестов. И результат не заставил себя ждать. В последней на эту тему публикации 2015 года сказано, что на 30% снизилась заболеваемость РЩЖ, а число операций на щитовидной железе снижалось на 35% ежегодно. Вывод напрашивается сам собой: в основе увеличения числа диагностированных случаев узлов щитовидки (в том числе и РЩЖ) является ставшее таким доступным УЗИ.
Думаем, следует также сказать, что образования ЩЖ выявляются не только при выполнении УЗИ, но и при использовании других методов лучевой диагностики (КТ, МРТ, ПЭТ), что стало возможным благодаря улучшению разрешающей способности оборудования. Следовательно, увеличилось чисто случайно выявляемых образований щитовидной железы (в том числе, рака) — инциденталóм (от англ. incidence — случайность) [17]. Инциденталомы клинически никак себя не проявляют и могут оставаться в организме бессимптомно всю жизнь. И многие из таких инциденталом обнаруживались лишь посмертно, случайно, и не являлись причиной кончины человека. Это позволяет говорить нам о существовании резервуара пациентов с узлами или раком щитовидной железы, который клинически является скрытым и никак себя не проявляет до его случайного обнаружения [18].
Приведенные данные обобщены на рисунке 2.

Рисунок 2. Что даст нам УЗИ щитовидки на самом деле?
рисунок авторов статьи
Напомним, что в нашей статье мы делаем акцент на наиболее распространенных типах РЩЖ (папиллярный, фолликулярный). Агрессивные формы РЩЖ (медуллярный, низкодифференцированный, недифференцированный и редко папиллярный) требуют дальнейшего более детального изучения
Самое главное: почему гипердиагностика и гиперлечение РЩЖ являются проблемой?
Является ли столь чрезмерное выявление объемных образований ЩЖ проблемой? Да, и очень даже серьезной. И она получила свое название — гипердиагностика (overdiagnosis) [19], [20]. И проблема состоит в том, что следствием ее становится гиперлечение. На самом деле она касается не только ЩЖ и представляет более серьезную опасность, чем может казаться на первый взгляд, а по мере развития методов диагностики приобретает все более и более масштабный характер, о чем говорит в своей статье «На всякий случай...» врач-эндокринолог В.В. Фадеев [28]. Говоря о ЩЖ, большинство пациентов с папиллярным РЩЖ подвергаются оперативному лечению — тотальной тиреоидэктомии или гемитиреоидэктомии [21]. Тем не менее в некоторых исследованиях [22], [23] показано, что при выборе лечения в пользу «активного наблюдения» (active surveillance) у пациентов с папиллярным РЩЖ (который относится к low-risk РЩЖ) диаметром менее одного сантиметра обнаруживались такие же исходы заболевания, как и при выполнении хирургических операций. В связи с этим в 2015 году в клинических рекомендациях Американской тиреоидологической ассоциации (American thyroid association, ATA) впервые была принята стратегия «активного наблюдения» для пациентов с low-risk cancers [24].
В связи с выявленным фактом, что в оперативном лечении таких РЩЖ, вполне возможно, нет необходимости (а ведь удаление ЩЖ сопровождается серьезными последствиями, о чем мы расскажем далее), с 2015 года в США уже принимаются меры по снижению частоты гипердиагностики и гиперлечения [24]. Например, уже настоятельно рекомендовано не проходить скрининг РЩЖ пациентам, у которых нет никаких симптомов, поскольку выявление агрессивных типов рака в этом случае крайне маловероятно.
Еще одной мерой предотвращения гиперлечения является изменение классификации типов РЩЖ, которые ведут себя как доброкачественные. Иначе говоря, их больше не называют «рак». Зачем? Все дело в психологической реакции пациента. Инстинкт самосохранения — самый живучий инстинкт человека и животных. И реализуется он во многом благодаря страху. Благодаря страху антилопа убегает ото льва, а змея жалит потенциальный объект угрозы — животные стремятся выжить. То же и с человеком. Всеми способами человек хочет продлить свое существование на этой земле. И диагноз «рак», который социум привык ассоциировать c мучительным завершением жизни, заставляет человека сделать все, чтобы от этого самого рака избавиться. В нашем случае, если у человека нашли РЩЖ, самая стойкая мысль — избавиться от этого мучения. И в большинстве случаев выбор падает на полное удаление щитовидной железы, вне зависимости от того, необходимо ли это. Как говорится, на всякий случай. И во многих случаях это не оправдано.
В одном из исследований [25] было выяснено, что люди, как правило, имеют общее представление о РЩЖ, но не знают о его диагностике и лечении, полагая, что по распространенности и смертности РЩЖ схож с другими типами рака. Страх дальнейшего прогрессирования заболевания заставляет пациента выбирать радикальное лечение. Так, недавно проведенные исследования неинвазивного рака груди [24], [25], а впоследствии и папиллярного РЩЖ [25], показали влияние терминологии на выбор лечения: замена термина «рак» в описании обоих патологических состояний способствовала выбору пациентом нехирургического лечения. Таким образом, данная стратегия оказывает влияние на психологическое состояние пациентов, тем самым предотвращая гиперлечение. Возможно ли жить с диагнозом «рак»? Как бы ответили на этот вопрос вы?
Что врачи думают о данной проблеме?
Проблема гиперлечения РЩЖ существует не только среди пациентов, но и среди медицинского сообщества.
Конечно, выбор, удалять ли щитовидную железу или нет, стоит больше перед пациентом, нежели перед лечащим врачом. И пациент вполне может выбрать хирургическую тактику лечения. А врач должен определять, сколько ткани щитовидной железы в конкретном случае нужно убирать.
В качестве уменьшения гипердиагностики Американская тиреоидологическая ассоциация рекомендует воздержаться от скрининга и биопсии мелких образований щитовидной железы при отсутствии на то иных клинических симптомов [6].
Как вообще лечат рак щитовидной железы?
Давайте разберемся, какие существуют пути лечения РЩЖ [26].
- Полное удаление ЩЖ, тотальная тиреоидэктомия, вместе с окружающей клетчаткой, а иногда и рядом лежащими лимфатическими узлами.
- Терапия радиоактивным йодом I131 после тотальной тиреиодэктомии. Не пугайтесь — это не опасно! Такой йод влияет только на клетки щитовидной железы и убивает их.
Почему мы, авторы, так не хотим, чтобы щитовидную железу удаляли без серьезных на то причин? Казалось бы, мы уберем орган, где сидит рак, и будем жить себе спокойно, только лишь принимая препараты гормонов щитовидной железы. Это ведь лучше, чем жить с раком. Или все-таки нет? Так вот, сама сложность вопроса заключается в операции.
Чем чревато полное удаление щитовидки (или, как говорят врачи, тотальная тиреоидэктомия)?
Существует два серьезных осложнения тотальной тиреоидэктомии [27].
- Стойкое снижение функции щитовидной железы (гипопаратиреоз). Наиболее серьезное и жизнеугрожающее осложнение. Итак, прямо за щитовидной железой располагаются четыре паращитовидные железы. Они производят паратиреоидный гормон, который отвечает за обмен кальция в нашем организме (а из него состоит бóльшая часть наших костей!). Паращитовидные железы совсем маленькие: диаметром 5 мм и весом 0,5 г. Их легко не заметить во время операции и удалить вместе с щитовидной железой. К тому же, даже если сохранить эти железы, высока вероятность повреждения питающих их кровеносных сосудов и нервов. А значит, железы просто перестанут работать, и в организм перестанет поступать паратиреиодный гормон. Это чревато возникновением тетанических приступов (подергиваний, которые могут переходит в судороги), нарушением питания волос и ногтей, кожи, эмали зубов, а также отложением кальция вне костей, например, между нервными клетками, что может проявляться в виде паркинсонизма или хореоатетоза — комбинации быстрых порывистых движений с медленными судорожными.
- Повреждение возвратного гортанного нерва и парез гортани. Щитовидная железа располагается прямо перед гортанью. Там же рядом находятся голосовые связки. Все эти структуры иннервируются гортанными нервами. И в случае повреждение некоторых из них — возвратных гортанных нервов — у пациента будет наблюдаться уменьшение активности гортанных мышц, что влечет за собой проблемы работы голосовых связок (в основном, осиплость голоса) и нарушения функций дыхания.
Согласитесь, последствия не из приятных. Поэтому главный вопрос заключается в следующем: оправдывают ли риски тиреоидэктомии ее пользу? На данном этапе развития науки и медицины нельзя дать однозначный ответ. Но важно понимать, что диагноз «Рак щитовидной железы» ничего не говорит о прогнозе для пациента и смертность от него крайне низка. А вот неоправданное агрессивное лечение, а именно удаление щитовидной железы, может повлечь за собой инвалидизацию и значительное ухудшение качества жизни. Поэтому сейчас в научном сообществе наблюдается тенденция органосохраняющей тактики в отношении высокодифференцированных РЩЖ. А показания к УЗИ щитовидной железы касаются только специфических групп пациентов. Ведь обнаружение раковых клеток в организме не означает смерть, а вот риск невротизации значительно возрастает.
Какой существует выход?
Одним из наиболее перспективных выходов из ситуации является частичное удаление ткани ЩЖ, а именно поврежденной доли. В таком случае пациент, во-первых, избавляется от необходимости принимать пожизненную заместительную терапию гормонами щитовидной железы, а во-вторых, избегает тех серьезных последствий, которые несет за собой операция полного удаления ЩЖ. Однако стоит понимать, что такой вариант не касается опухолей большого размера, а также тех новообразований, которые потенциально могут быть агрессивными (это решает врач!).
Сейчас терапевты и хирурги, которые занимаются патологией щитовидной железы, разделились на два лагеря: те, кто считает, что лучше перестраховаться, и при выявлении даже самой маленькой опухоли удалить всю щитовидную железу, и те, кто считает, что лучшим выходом будет частичное удаление ткани железы, а именно поврежденной ее доли. К сожалению, этот вопрос до сих пор остается открытым. Врачи все еще не могут прийти к единому знаменателю в данном вопросе. Проблема в том, что достоверная объективная доказательная база, на которую врачи могли бы опираться в качестве актуального клинического руководства, вовсе отсутствует. Существуют лишь отдельные исследования, которые обозревают вопрос лишь с одной субъективной стороны [21]. Оптимальным решением данной проблемы, на наш взгляд, стало бы объединение всех существующих статей с объективным и всесторонним взглядом на этот вопрос. Однако подобное исследование лишь ожидает нас в будущем.
Финальный аккорд
Итак, вот мы и подошли к последним строкам нашей статьи. Могло показаться, что мы и вовсе против УЗИ щитовидной железы, однако это не так. Существует группа риска пациентов, которым необходимо сделать УЗИ щитовидки (например, РЩЖ у кого-то из членов семьи). Также нельзя игнорировать тот факт, что УЗИ сильно продвинуло врачей в ранней диагностике агрессивных быстротекущих форм РЩЖ. Однако бóльшая часть врачей-эндокринологов, особенно за границей, против того, чтобы делать УЗИ щитовидки тогда, когда нет никаких симптомов болезни! Необходимой к прочтению, на наш взгляд, является работа профессора Фадеева В.В. «На всякий случай...» [28].
В этой статье высококвалифицированный врач обращает внимание читателя на то, что часто врачи оценивают результаты лабораторных и инструментальных анализов только на основании общепринятых границ норм. В случае несоответствия данной «норме» пациент признается больным. Очень важно понимать, что человек — индивидуальность, и показатель нормы у каждого может варьировать в зависимости от особенностей организма. Поэтому и лечить мы должны не анализы, не болезнь, а пациента. Врачу необходимо оценивать не только цифры в листе анализов, но и состояние пациента, а также качество жизни, которое ждет человека после лечения. Это и называется клиническим мышлением, которое, к сожалению, зачастую отсутствует у врачей в век, когда мы хотим слепо довериться цифрам, а машина начинает думать за человека.
С этими и другими мыслями вы можете ознакомится по оставленной нами ссылке [26].
Итак, дорогие наши читатели! Опираясь на всё, о чем мы рассказали выше, мы бы хотели, чтобы вы сделали три главных вывода:
- Не делайте УЗИ щитовидной железы «на всякий случай», без каких-либо симптомов! Ни по совету подруги, ни потому, что так сказали по телевизору, ни даже если вам сказал так врач (только если он четко объяснит, зачем нужно делать УЗИ).
- Если у вас нашли узел — 90%, что он доброкачественный.
- Если вы попали в оставшиеся 10%, помните, что бóльшая часть РЩЖ хорошо поддается лечению и имеет благоприятный прогноз.
Всем хорошего дня, и берегите свои щитовидки и нервы. :)
Литература
- Циберкин А. (2019). Всегда ли нужна биопсия узлов щитовидной железы? «Медфронт»;
- Carolyn Dacey Seib, Julie Ann Sosa. (2019). Evolving Understanding of the Epidemiology of Thyroid Cancer. Endocrinology and Metabolism Clinics of North America. 48, 23-35;
- Hyeong Sik Ahn, Hyun Jung Kim, H. Gilbert Welch. (2014). Korea's Thyroid-Cancer “Epidemic” — Screening and Overdiagnosis. N Engl J Med. 371, 1765-1767;
- Yasuhiro Ito, Akira Miyauchi, Minoru Kihara, Takuya Higashiyama, Kaoru Kobayashi, Akihiro Miya. (2014). Patient Age Is Significantly Related to the Progression of Papillary Microcarcinoma of the Thyroid Under Observation. Thyroid. 24, 27-34;
- S. Suzuki. (2016). Childhood and Adolescent Thyroid Cancer in Fukushima after the Fukushima Daiichi Nuclear Power Plant Accident: 5 Years On. Clinical Oncology. 28, 263-271;
- Alexandria D. McDow, Susan C. Pitt. (2019). Extent of Surgery for Low-Risk Differentiated Thyroid Cancer. Surgical Clinics of North America. 99, 599-610;
- Toru Takano. (2017). Natural history of thyroid cancer [Review]. Endocr J. 64, 237-244;
- Noone A.M., Howlader N., Krapcho M., Miller D., Brest A., Yu M. et al. SEER cancer statistics review, 1975-2015. Bethesda: National Cancer Institute, 2018;
- A. Kurjak. (2000). Ultrasound scanning – Prof. Ian Donald (1910–1987). European Journal of Obstetrics & Gynecology and Reproductive Biology. 90, 187-189;
- Ian Donald, R.E. Steiner. (1953). RADIOGRAPHY IN THE DIAGNOSIS OF HYALINE MEMBRANE. The Lancet. 262, 846-849;
- Louise Davies, H. Gilbert Welch. (2014). Current Thyroid Cancer Trends in the United States. JAMA Otolaryngol Head Neck Surg. 140, 317;
- Hyeyeun Lim, Susan S. Devesa, Julie A. Sosa, David Check, Cari M. Kitahara. (2017). Trends in Thyroid Cancer Incidence and Mortality in the United States, 1974-2013. JAMA. 317, 1338;
- Antonino Belfiore, Dario Giuffrida, Giacomo L. La Rosa, Orazio Ippolito, Giovanna Russo, et. al.. (1989). High frequency of cancer in cold thyroid nodules occurring at young age. Acta Endocrinologica. 121, 197-202;
- S. Ezzat. (1994). Thyroid incidentalomas. Prevalence by palpation and ultrasonography. Archives of Internal Medicine. 154, 1838-1840;
- Carolyn Dacey Seib, Julie Ann Sosa. (2019). Evolving Understanding of the Epidemiology of Thyroid Cancer. Endocrinology and Metabolism Clinics of North America. 48, 23-35;
- Hyeong Sik Ahn, H. Gilbert Welch. (2015). South Korea’s Thyroid-Cancer “Epidemic” — Turning the Tide. N Engl J Med. 373, 2389-2390;
- Louise Davies, H. Gilbert Welch. (2006). Increasing Incidence of Thyroid Cancer in the United States, 1973-2002. JAMA. 295, 2164;
- A.T. Grady, J.A. Sosa, T.P. Tanpitukpongse, K.R. Choudhury, R.T. Gupta, J.K. Hoang. (2015). Radiology Reports for Incidental Thyroid Nodules on CT and MRI: High Variability across Subspecialties. AJNR Am J Neuroradiol. 36, 397-402;
- Hirsch E.F. (1947). Unnecessary operations. Ill. Med. J. 5;
- Horwitz A. (1947). Unnecessary surgery. Med. Ann. Dist. Columbia. 11, 605–608;
- H. Gilbert Welch, Gerard M. Doherty. (2018). Saving Thyroids — Overtreatment of Small Papillary Cancers. N Engl J Med. 379, 310-312;
- Akira Miyauchi, Yasuhiro Ito, Hitomi Oda. (2018). Insights into the Management of Papillary Microcarcinoma of the Thyroid. Thyroid. 28, 23-31;
- Iwao Sugitani, Kazuhisa Toda, Keiko Yamada, Noriko Yamamoto, Motoko Ikenaga, Yoshihide Fujimoto. (2010). Three Distinctly Different Kinds of Papillary Thyroid Microcarcinoma should be Recognized: Our Treatment Strategies and Outcomes. World J Surg. 34, 1222-1231;
- Benjamin R. Roman, Luc G. Morris, Louise Davies. (2017). The thyroid cancer epidemic, 2017 perspective. Current Opinion in Endocrinology & Diabetes and Obesity. 24, 332-336;
- Brooke Nickel, Caitlin Semsarian, Ray Moynihan, Alexandra Barratt, Susan Jordan, et. al.. (2019). Public perceptions of changing the terminology for low-risk thyroid cancer: a qualitative focus group study. BMJ Open. 9, e025820;
- Дедов И.И. и Мельниченко Г.А. Эндокринология: национальное руководство (2-е изд.). М.: «ГЭОТАР-Медиа», 2019. — 1112 с.;
- Дедов И.И., Мельниченко Г.А., Фадеев В.В. Эндокринология: учебник (3-е изд.). М.: «Литтерра», 2015. — 416 с.;
- Фадеев В.В. (2017). На всякий случай... «Клиническая и экспериментальная тиреоидология». 2.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





