Тихий убийца: открытая или эндоваскулярная операция? Как правильно бороться с аневризмой брюшной аорты
06 апреля 2026
Тихий убийца: открытая или эндоваскулярная операция? Как правильно бороться с аневризмой брюшной аорты
- 959
- 0
- 1
Рисунок в полном размере.
создано с помощью perplexity.ai
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Аневризма брюшной аорты (АБА) представляет собой целый ряд противоречий: с одной стороны, болезнь, изучаемая более полувека, с известными факторами риска и проверенными методами лечения; с другой — загадка, которая продолжает убивать людей тысячами ежегодно, несмотря на наличие эффективного скрининга.
В настоящее время медикаментозных методов лечения АБА не существует, поэтому хирургическое вмешательство остается единственным решением этой проблемы. К тому же в сосудистой хирургии до сих пор сохраняется дилемма выбора между открытой резекцией аневризмы (OAR) — классическим подходом с проверенной эффективностью — и эндоваскулярной репарацией (EVAR) — современным минимально инвазивным методом. Оба подхода имеют свои преимущества и недостатки, поэтому итоговое решение хирург всегда должен принимать на основе индивидуальных характеристик пациента. В данной статье мы бы хотели рассказать о патогенезе АБА, сравнить профили риск-выгоды обоих методов лечения и обосновывать необходимость персонализированного подхода к выбору оптимальной хирургической стратегии для каждого пациента, как делают это настоящие хирурги в своей практике.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Когда секунда — жизнь
Все изменилось за считанные минуты. Обычное утро у 67-летнего Джона Уолмсли (Великобритания) началось как всегда, но внезапно пронзительная боль в животе и стремительная слабость повергли его в шок. Не понимая, что происходит, он едва успел позвать жену и почти тут же потерял сознание. Позже врачи объяснили: у него произошел разрыв аневризмы брюшной аорты — самого крупного сосуда живота. Спасти Джона удалось лишь благодаря молниеносной доставке на вертолете и слаженной работе сосудистых хирургов, которые за считанные минуты заменили разорванный участок аорты искусственным протезом. Подобная операция — всегда гонка со смертью: из-за любого промедления человек может расстаться с жизнью.
История Джона далеко не единственная. Ранее 54-летняя австралийка Эмили Бенхэм внезапно почувствовала резкую слабость и головокружение во время похода по магазинам. Как выяснилось позже — это был тот самый «гром среди ясного неба»: разрыв аневризмы. Ближайшая подруга, оказавшаяся рядом, немедленно вызвала скорую. Благодаря быстрой диагностике и экстренной операции женщину удалось спасти.
Статистика неумолима: около 30% пациентов с разрывом аневризмы брюшной аорты умирают еще по дороге в больницу, а из прибывших в стационар выживает от 40% до 50% [1]. Каждый прошедший час снижает шанс на спасение. Сосудистая катастрофа, с которой ежегодно сталкиваются тысячи людей, превращает «невидимую» болезнь в отчаянное испытание для целых семей.
Тихий убийца, о котором вы не знаете
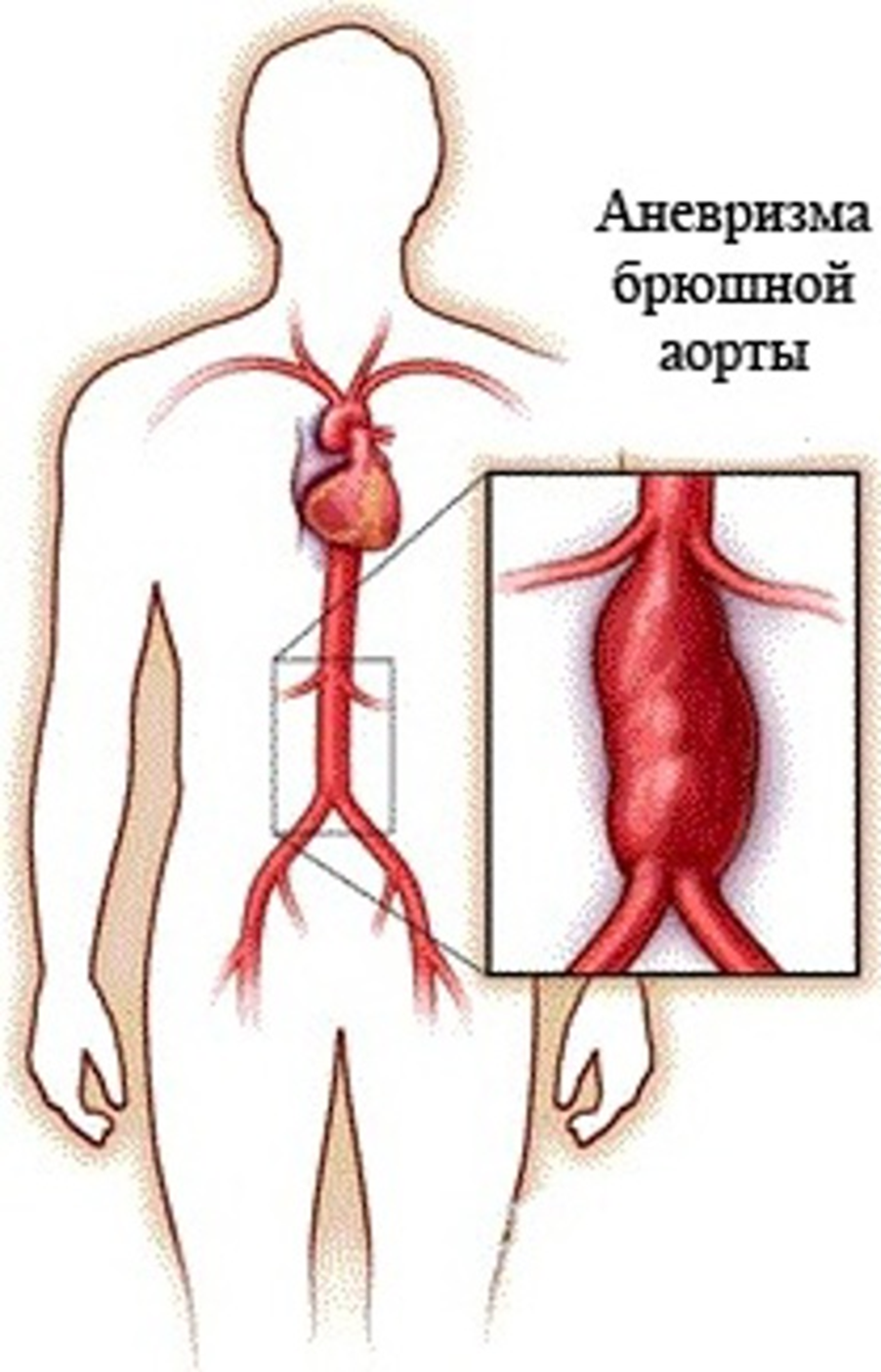
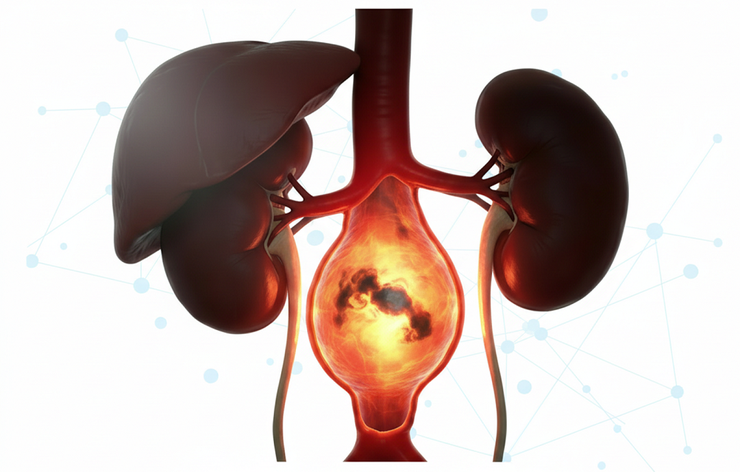
Рисунок 1. Аневризма брюшной аорты (АБА) — это локализованное расширение брюшной аорты , при котором диаметр превышает 3 см или превышает норму более чем на 50%.
Аневризма брюшной аорты (АБА) (рис. 1) широко известна как «тихий убийца» из-за того, что зачастую она развивается бессимптомно и долгое время не вызывает никаких явных изменений в состоянии человека [2]. Большинство пациентов не подозревают о заболевании до тех пор, пока аневризма не достигнет значительных размеров или не произойдет разрыв, который грозит смертельным исходом [2]. Врачи отмечают, что АБА достаточно часто становится случайной находкой при обследованиях по другим причинам, например, при ультразвуковом исследовании или рентгене брюшной полости [3].
При этом масштаб проблемы весьма серьезен. В России ежегодно регистрируется от 10 до 40 случаев аневризмы брюшной аорты на 100 тысяч населения, что отражает значительное распространение заболевания. Это заболевание занимает десятое место среди причин смертности, что подчеркивает его опасность и необходимость ранней диагностики.
К группе высокого риска относятся преимущественно мужчины старше 65 лет, особенно курящие и страдающие гипертонией или атеросклерозом. Возраст и пол являются ключевыми факторами: у мужчин вероятность развития АБА в четыре раза выше, чем у женщин. Также при патологоанатомических исследованиях аневризмы выявляются в 0,16–1% случаев, причем частота их увеличивается с возрастом.
Проблема скрытности заболевания заключается в том, что на ранних стадиях аневризма не вызывает болевых ощущений или других симптомов. При прогрессировании болезни могут появиться такие признаки, как чувство тяжести или пульсации в животе, но они часто принимаются за другие, менее серьезные недуги. Болевой синдром может проявляться в виде ноющих или пульсирующих болей в животе или пояснице, иногда боль иррадиирует в паховую область или крестец, что часто приводит к ошибочной диагностике. Кроме того, растущая аневризма может создавать давление на соседние органы, вызывая запоры, снижение аппетита, тошноту, а в некоторых случаях нарушения мочеиспускания. Однако эти симптомы проявляются уже на поздних стадиях, когда риск разрыва значительно возрастает [2], [3].
Строение стенки аорты и патогенез аневризмы
Архитектура сосудистой стенки
Стенка аорты состоит из трех слоев: интимы (внутренний эндотелиальный слой), медии (средний слой) и адвентиции (наружный соединительнотканный слой) [4–6]. Основную часть стенки составляет медия, занимающая около 80% ее толщины и образованная гладкомышечными клетками (ГМК), коллагеновыми и эластичными волокнами и протеогликанами (рис. 2) [5], [6].
Ключевыми структурными белками являются эластин и коллаген. Эластин организован в волокна в медиальном слое и обеспечивает растяжимость сосуда, тогда как коллаген — преимущественно типов I (в интиме и адвентиции) и III (в медии) — придает стенке механическую прочность. Взаимодействие эластиновых и коллагеновых волокон с ГМК формирует функциональную единицу, необходимую для поддержания структурной целостности и эластических свойств аорты [4–7].
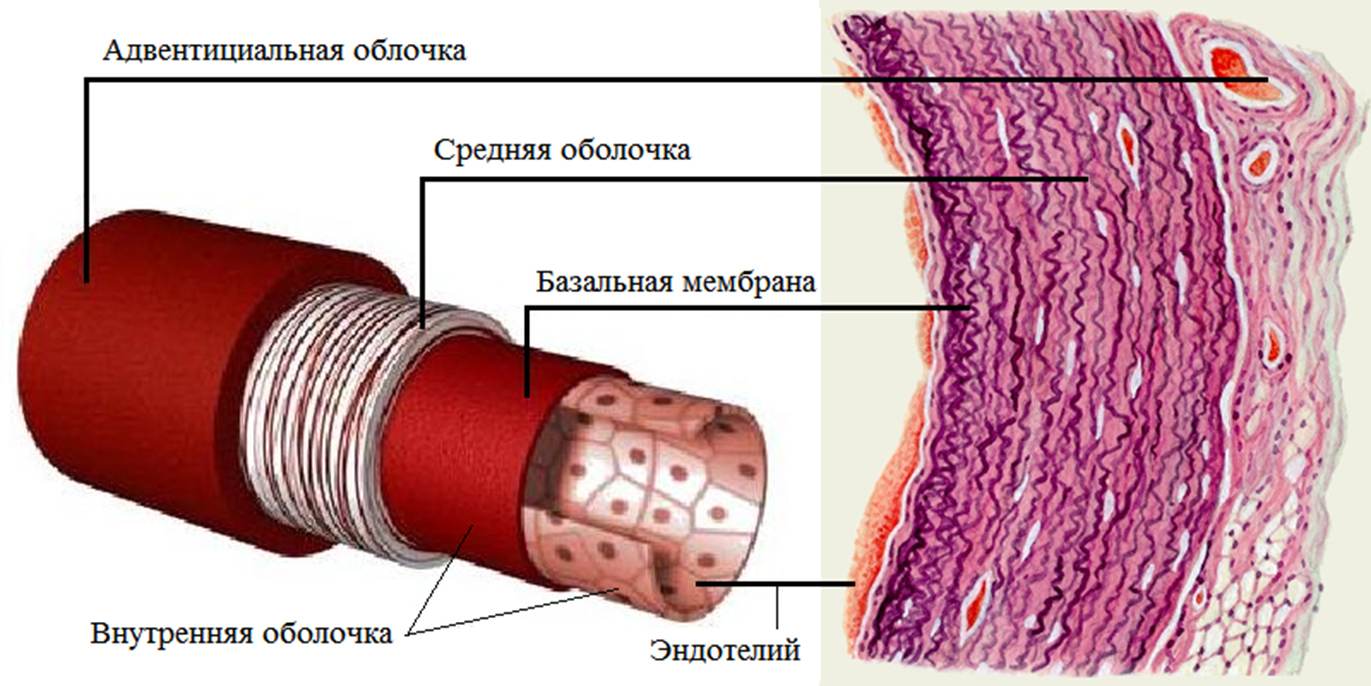
Рисунок 2. Строение стенки аорты.
Патогенез
Ведущую роль в патогенезе АБА играет дисбаланс между протеолитической активностью матриксных металлопротеиназ (ММП) [8] и их ингибиторами (ТIMP), приводящий к прогрессирующей деградации внеклеточного матрикса (ВКМ). Потеря эластина и коллагена обусловливает дилатацию и нестабильность стенки аорты, поэтому наследственные заболевания, такие как синдром Марфана (нарушение синтеза эластина) и сосудистый тип синдрома Элерса—Данлоса (нарушение синтеза коллагена), являются серьезным фактором риска [9], [10].
Также при дисфункции гладкомышечных клеток (апоптоз, фенотипическое переключение) снижается синтез ВКМ и увеличивается продукция ММП, что замыкает порочный круг (рис. 3). Инициирующим и поддерживающим фактором этих процессов служит хроническое воспаление, сопровождаемое инфильтрацией макрофагов, Т-лимфоцитов и генерацией активных форм кислорода (АФК) [11], [12].
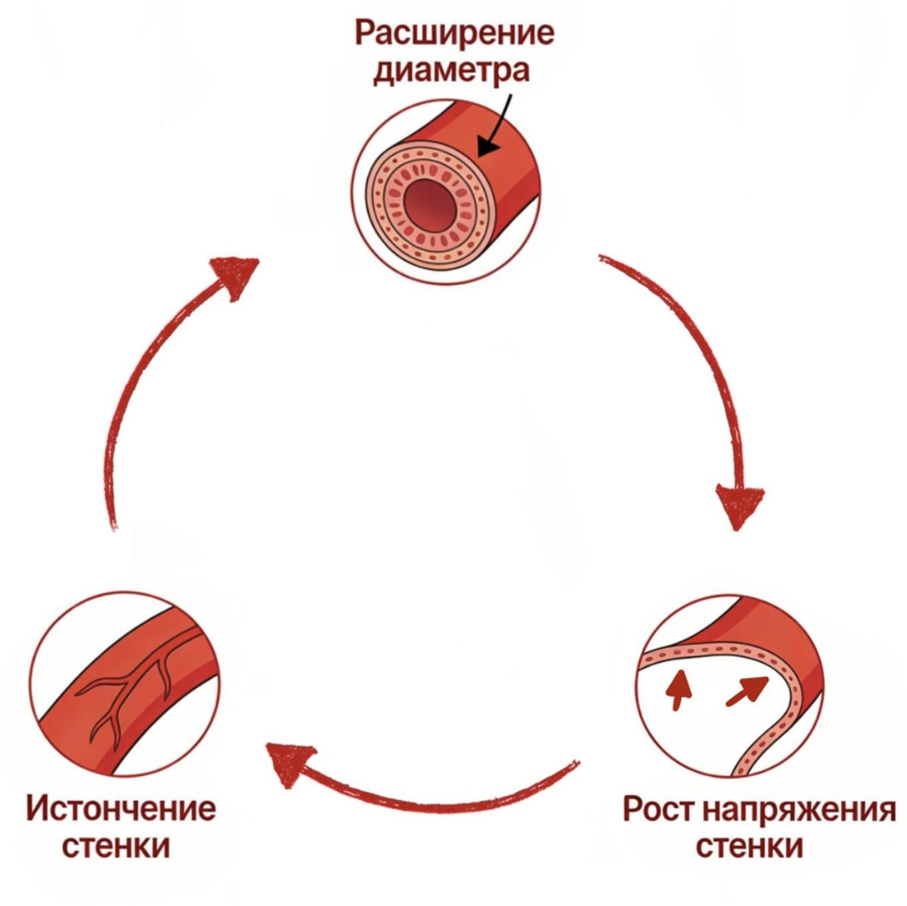
Рисунок 3. Порочный круг аневризмы.
создано с помощью Perplexity.ai
Мужчины с длительным стажем курения, атеросклерозом и артериальной гипертензией в анамнезе имеют повышенные риски возникновения АБА. Женские половые гормоны оказывают протективное действие на сосудистую стенку, поэтому аневризма возникает реже, однако в постменопаузе риски значительно возрастают, а вероятность разрыва становится больше, чем у мужчин [13]. Курение считается главным и наиболее сильным предиктором АБА, а также темпов ее роста и риска разрыва; связь имеет дозозависимый характер и ослабевает по мере увеличения стажа отказа от курения [14]. При атеросклерозе у пациентов с АБА часто выявляются пристеночные тромбы, которые могут поддерживать локальное воспаление и ремоделирование стенки, однако связь АБА и атеросклероза больше рассматривают как частично «параллельные процессы» на фоне общих факторов риска, а не как простую прямую причинность [15]. Артериальная гипертензия ассоциирована с риском формирования АБА, а повышение среднего АД относится к факторам, связанным с риском разрыва; клинически это согласуется с тем, что рост давления увеличивает механическое напряжение стенки и «подталкивает» дилатацию при уже ослабленном ВКМ [16].
К тому же по мере роста аневризмы увеличивается напряжение стенки согласно закону Лапласа, что ускоряет прогрессирование до критического размера (обычно диаметр ≥5,5 см), при котором риск разрыва превышает риски хирургического вмешательства [17–19].
Выбор оружия: две операции, разные судьбы
На протяжении последних 30 лет сосудистая хирургия переживает парадигматический сдвиг. Если традиционная открытая операция была единственным методом лечения аневризмы брюшной аорты в течение полувека, то внедрение эндоваскулярного подхода в 1991 году кардинально изменило тактику лечения. Сегодня сосудистые хирурги столкнулись с дилеммой: два эффективных метода с диаметрально противоположными профилями риск-выгода (отношение вероятности осложнений и/или летальности к ожидаемой пользы для пациента) [20], [21]. Понимание их различий критично для правильного выбора стратегии лечения каждого пациента (рис. 4).
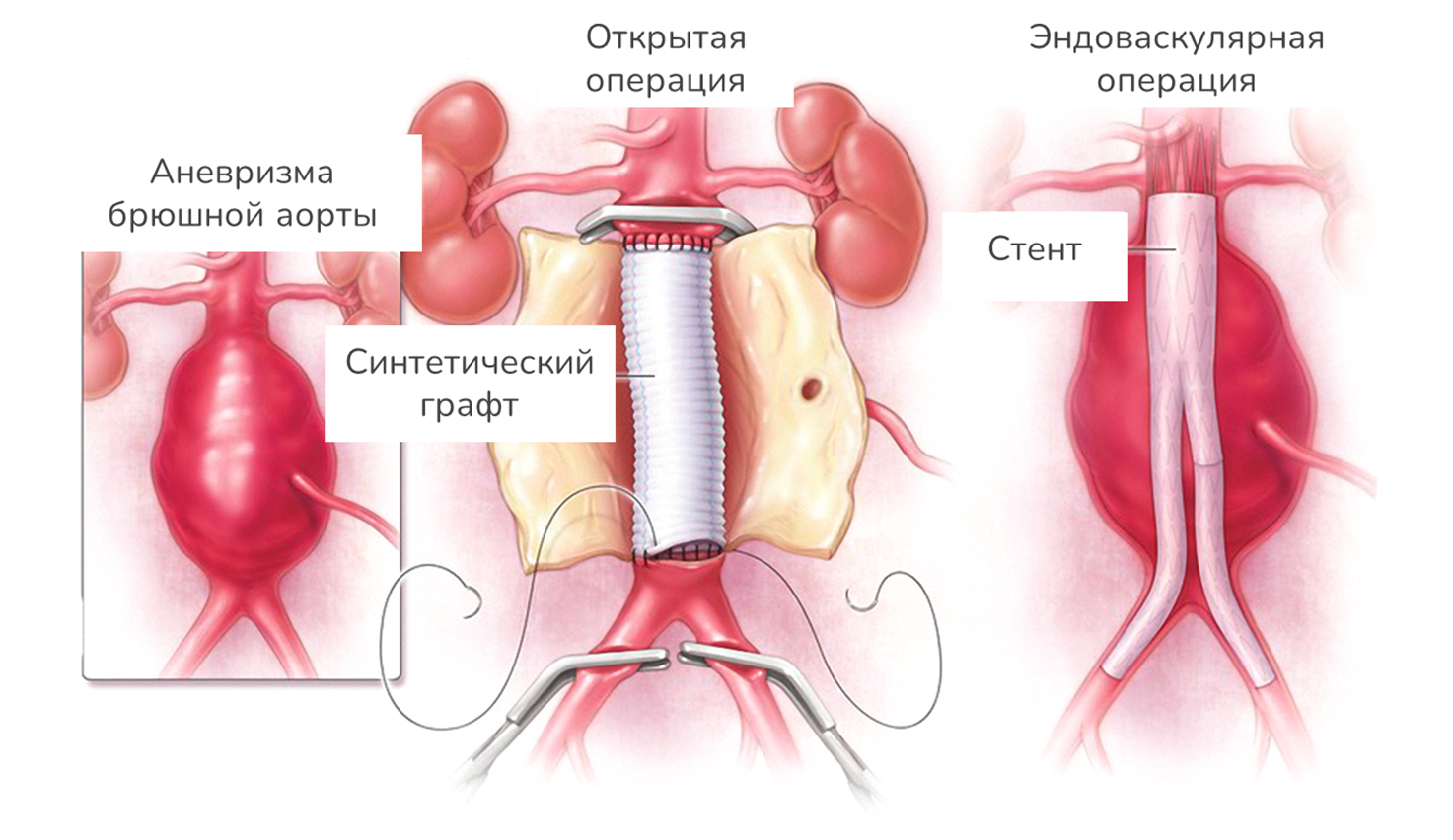
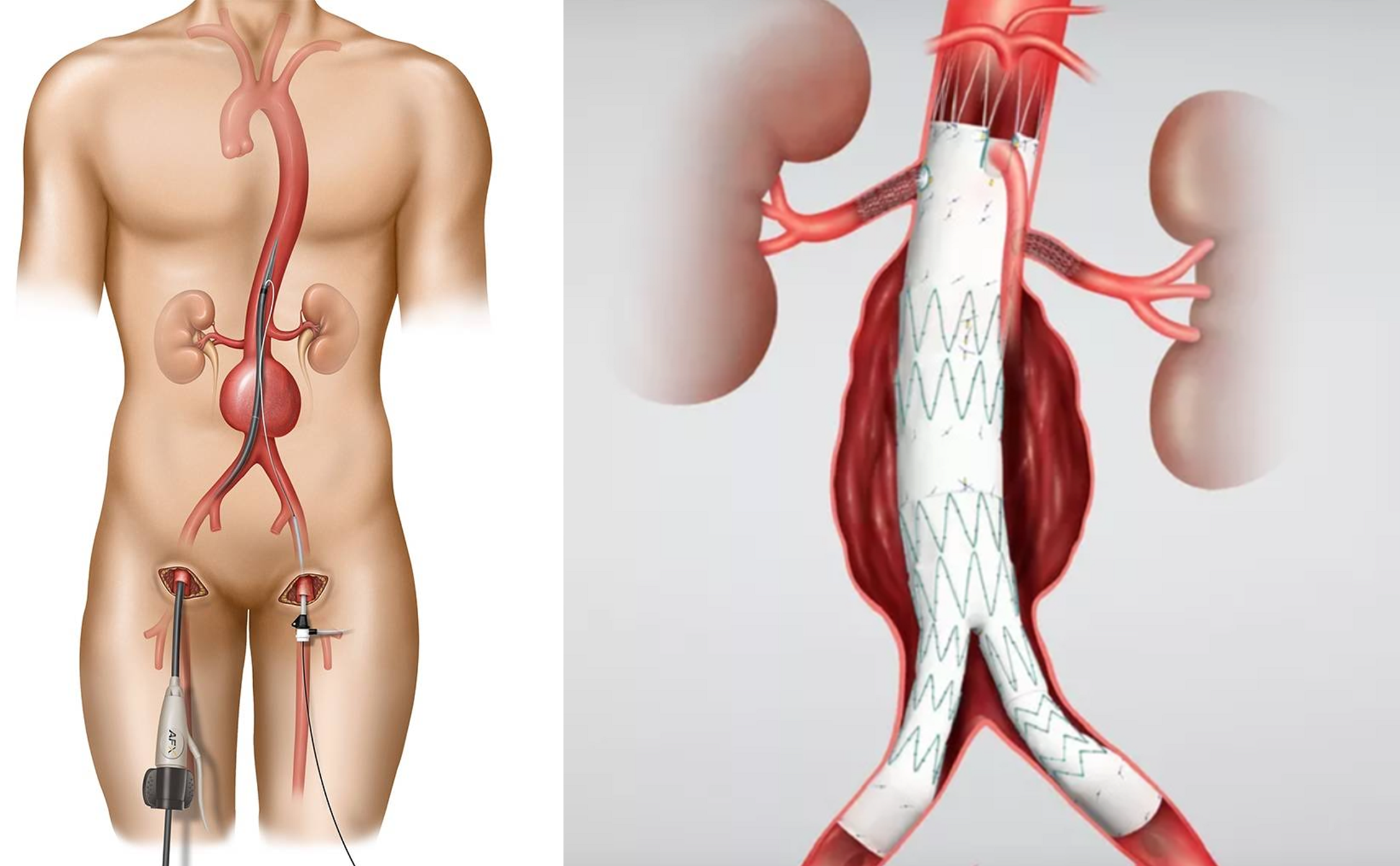
Рисунок 4. Два способа операций на АБА.
адаптировано из aafp.org
Открытая операция (OAR)
Открытая резекция аневризмы с протезированием — методика, которая остается в арсенале сосудистых хирургов более полувека. Суть операции заключается в полном удалении пораженного участка аорты и замене его синтетическим протезом (обычно из дакрона или политетрафторэтилена). Это прямой, анатомически полный подход, который обеспечивает восстановление целостности аорты с надежным механическим укреплением ее стенки [22].
Методика предполагает выполнение лапаротомии (разреза брюшной полости) или забрюшинного доступа, мобилизацию аневризмы, мобилизацию и контроль проксимального и дистального концов аорты, вскрытие аневризмы, удаление пристеночного тромба и последующее наложение анастомозов (соединений) синтетического протеза с здоровыми участками аорты (рис. 5). В зависимости от анатомии аневризмы, операция может сопровождаться вовлечением висцеральных и почечных артерий (так называемые сложные аневризмы), что требует высочайшего мастерства хирурга [22–24].
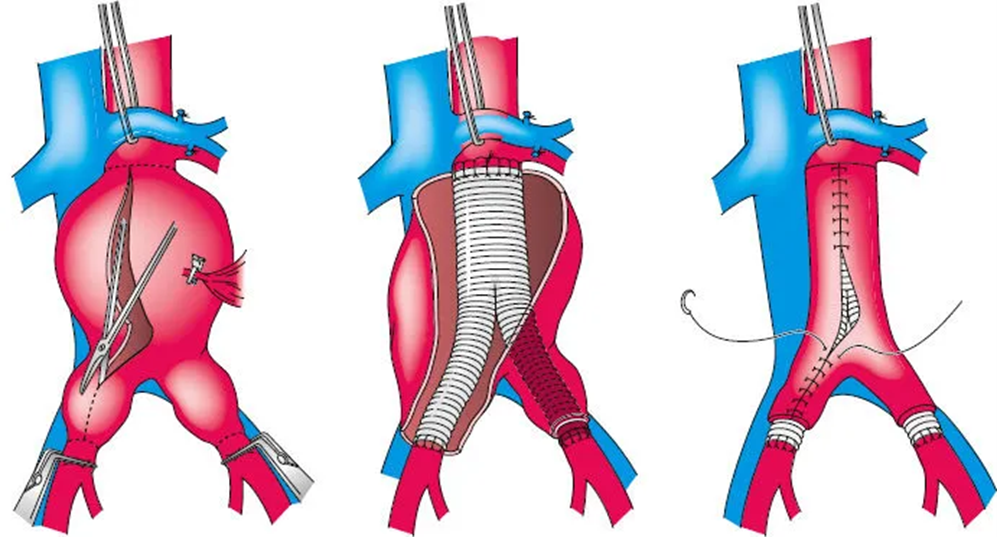
Рисунок 5. Открытая операция на АБА.
Эндоваскулярная операция (EVAR)
Эндоваскулярная репарация аневризмы (EVAR — Endovascular Aneurysm Repair) представляет собой принципиально иной подход к лечению аневризмы. Операция выполняется через малые пункции в области бедренных артерий под рентгенологическим (ангиографическим) контролем. Через сосуды к аневризме аорты ретроградно подводятся катетеры и направляющие устройства, по которым устанавливается стент-графт — каркасная конструкция из нитинола, нержавеющей стали или кобальт-хромового сплава, покрытая непроницаемым материалом из полиэстера или политетрафторэтилена (рис. 6А) [25–27].
Стент-графт изолирует патологически расширенный участок аорты от кровотока, предотвращая его разрыв и обеспечивая надежную герметизацию. Давление внутри аневризмального мешка снижается, что позволяет остановить дальнейшее расширение и разрыв (рис. 6Б) [28–30]. Ключевое преимущество — отсутствие необходимости в лапаротомии, что значительно снижает операционную травму [31], [32].
Сравнительный анализ: когда выбирать каждый метод
Хотя открытая операция (OAR) и EVAR имеют принципиально различные профили риск-выгода, правильный выбор между ними не является просто следованием строгим алгоритмам.
На этапе оперативного вмешательства OAR требует лапаротомии, длится 2–4 часа и сопровождается кровопотерей 500–1500 мл. EVAR выполняется через чрескожные пункции бедренных артерий, занимает менее 2 часов с минимальной кровопотерей (менее 200 мл) [33], [34]. Эта разница напрямую влияет на ранние осложнения: 30-дневная летальность при EVAR составляет 1,2% против 3,8–4.0% при OAR, периоперационные осложнения возникают в 2–5% при EVAR и в 5–15% при OAR. Это делает EVAR значительно предпочтительнее для высокорисковых пациентов [35–37].
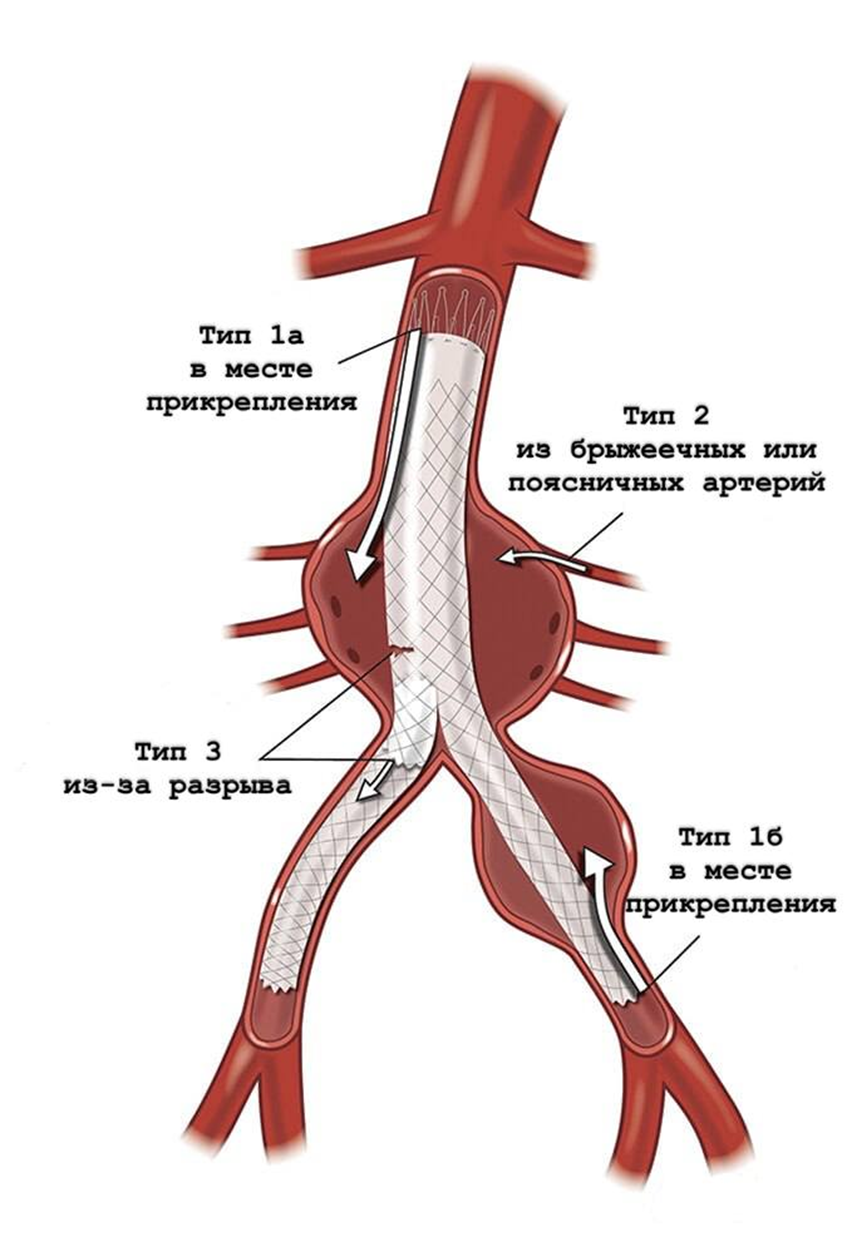
Рисунок 7. Иллюстрация эндоликов типов I, II и III. Эндолики определяются как постоянный кровоток между трансплантатом и стенкой аорты (т.е. внутри исключенного аневризматического мешка) после эндоваскулярной реконструкции аневризмы. Тип IV обусловлен пористостью эндопротеза, но в настоящее время встречается редко. Эндолики типа V представляет собой расширение мешка без видимого эндолика. Типы IV и V не изображены
адаптировано из [30]
Однако долгосрочные результаты рисуют иную картину. OAR обеспечивает дефинитивное решение — аневризма полностью удалена и больше не требует наблюдения. EVAR же требует обязательного долгосрочного контроля минимум 2 года, поскольку у 15–30% пациентов возникают эндолики (утечки вокруг стент-графта), требующие переоперации (рис. 6А). В результате 30–40% пациентов после EVAR нуждаются в повторном вмешательстве, против 9,8% при OAR [30], [35], [36], [38], [39].
Через 6 лет смертность составляет 35,6% при OAR и 41,2% при EVAR — OAR обеспечивает на 17% меньший риск смерти. Риск разрыва аневризмы также ниже при OAR (5,6% vs 7,7%) [35], [39]. Парадокс EVAR заключается в том, что, несмотря на более низкую 30-дневную летальность, долгосрочная выживаемость хуже, предположительно вследствие осложнений, требующих переоперации. При этом успешно пролеченные пациенты требуют пожизненного мониторирования. После OAR показано ежегодное клиническое обследование с периодическим КТ Q (компьютерная томография) исследованием; после EVAR требуется более интенсивный контроль — КТ-ангиография в течение первого месяца, затем в 6 и 12 месяцев, далее ежегодно для выявления эндоликов («подтеканий» стент‑графта), миграции стента и роста аневризматического мешка [24]. Также независимо от типа реконструкции пациентам рекомендуется продолжить прием статинов, антитромбоцитарных препаратов (аспирин), бета-блокаторов при их показаниях, а также строгий контроль артериального давления и полный отказ от курения, так как эти меры снижают периоперационную смертность и улучшают долгосрочный прогноз [29], [33].
| Параметр | OAR | EVAR |
|---|---|---|
| Оперативные характеристики | ||
| Доступ | Лапаротомия/забрюшинный | Чрезкожная пункция |
| Длительность | 2–4 часа | <2 часов |
| Кровопотеря | 500–1500 мл | <200 мл |
| Операционная травма | Высокая | Минимальная |
| Ранние осложнения (0–30 дней) | ||
| 30-дневная смертность | 3,8–4,0% | 1,2% |
| Периоперационные осложнения | Выше (5–15%) | Ниже (2–5%) |
| Кровотечение | Часто | Редко |
| Ишемия кишечника | Есть риск | Низкий |
| Ишемия нижних конечностей | Возможна | Выше (миспозиция) |
| Поздние осложнения (>30 дней) | ||
| Осложнения разреза | 8,4% | 0% |
| Грыжи, инфекции ран | Да | Нет |
| Эндолики | Нет | 15–30% |
| Миграция стент-графта | Нет | Возможна |
| Долгосрочные результаты (6 лет) | ||
| Смертность | 35,6% | 41,2% |
| Разрыв аневризмы | 5,6% | 7,7% |
| Необходимость переоперации | 9,8% | 15,3% |
| Требуется наблюдение | Редко | Обязательно (2+ года) |
Заключение: когда решение должно быть персонализированным
Аневризма брюшной аорты — это болезнь контрастов. С одной стороны, она развивается бессимптомно, скрываясь за обыденными жалобами на боль в спине или дискомфорт в животе, рискуя долгие годы оставаться необнаруженной. С другой — один момент может перевернуть жизнь пациента и его семьи, когда стенка аневризмы разрывается и превращается в смертельное осложнение. История Джона Уолмсли и Эмили Бенхэм — это не исключения, а иллюстрация суровой реальности: каждый день врачи сталкиваются с пациентами, для которых каждая секунда имеет значение.
Понимание патогенеза АБА как сложного порочного круга, инициированного хроническим воспалением и поддерживаемого дисбалансом между протеолитической активностью и защитными механизмами, может послужить толчком к развитию фармакологического подхода к лечению заболевания. Однако на современном этапе развития медицины хирургия остается единственным эффективным методом лечения симптоматической и растущей асимптоматической аневризмы.
При этом в современной сосудистой хирургии нет единого «правильного» выбора между открытой операцией и EVAR. Правильный выбор — это тот, который соответствует индивидуальным особенностям конкретного пациента, его ожиданиям и жизненным целям. Молодому здоровому пациенту открытая операция предоставляет десятилетия безопасной жизни без необходимости в дополнительных вмешательствах. Пожилому пациенту со множественной коморбидностью при условии подходящей анатомии EVAR обеспечивает возможность перенести операцию и вернуться к нормальной жизни. Ключ к успеху — это поделенное с пациентом принятие решения, основанное на доказательствах, индивидуальной оценке риск-выгоды и уважении к его предпочтениям.
Литература
- Saira Mauland Mansoor, Jørgen Joakim Jørgensen, Jonny Hisdal, Toril Rabben. (2024). Thirty-Nine Percent of Patients with a Ruptured Abdominal Aortic Aneurysm (AAA) Have an Incidentally Detected AAA Prior to Rupture. Annals of Vascular Surgery. 108, 148-156;
- Aggarwal S., Qamar A., Sharma V., Sharma A. (2011). Abdominal aortic aneurysm: A comprehensive review. Exp Clin Cardiol. 16, 11–15;
- Vicente Riambau, Francisco Guerrero, Xavier Montañá, Rosa Gilabert. (2007). Aneurisma de aorta abdominal y enfermedad vascular renal. Revista Española de Cardiología. 60, 639-654;
- Eijiro Maeda, Yoriko Ando, Kazuhiro Takeshita, Takeo Matsumoto. (2022). Through the cleared aorta: three-dimensional characterization of mechanical behaviors of rat thoracic aorta under intraluminal pressurization using optical clearing method. Sci Rep. 12;
- Xiaochen Wang, Harry J. Carpenter, Mergen H. Ghayesh, Andrei Kotousov, Anthony C. Zander, et. al.. (2023). A review on the biomechanical behaviour of the aorta. Journal of the Mechanical Behavior of Biomedical Materials. 144, 105922;
- Joseph Brunet, Baptiste Pierrat, Pierre Badel. (2021). Review of Current Advances in the Mechanical Description and Quantification of Aortic Dissection Mechanisms. IEEE Rev. Biomed. Eng.. 14, 240-255;
- Louise Neave, Maria Tahir, Miriam Nightingale, Anshul S. Jadli, Vaibhav B. Patel, et. al.. (2022). Medial Collagen Type and Quantity Influence Mechanical Properties of Aneurysm Wall in Bicuspid Aortic Valve Patients. Front. Mech. Eng.. 8;
- Что такое внеклеточный матрикс и почему его все изучают;
- Georgia Atkinson, Rosaria Bianco, Karina Di Gregoli, Jason L. Johnson. (2023). The contribution of matrix metalloproteinases and their inhibitors to the development, progression, and rupture of abdominal aortic aneurysms. Front. Cardiovasc. Med.. 10;
- Shuo Wang, Dan Liu, Xiaolin Zhang, Xiaoxiang Tian. (2023). Regulation of Matrix Metalloproteinase-2 and Matrix Metalloproteinase-9 in Abdominal Aortic Aneurysm. Cardiology Discovery. 3, 212-220;
- Matthew Kazaleh, Rachel Gioscia-Ryan, Gorav Ailawadi, Morgan Salmon. (2023). Oxidative Stress and the Pathogenesis of Aortic Aneurysms. Biomedicines. 12, 3;
- Jun Li, Yang Liu, Zhitao Wei, Jie Cheng, Yongfa Wu. (2024). The occurrence and development of abdominal aortic aneurysm may be related to the energy metabolism disorder and local inflammation. Heliyon. 10, e27912;
- Кузнецов М. Р., Папышева О. В. (2018). Менопаузальная гормональная терапия и сосудистые события: какова взаимосвязь? Доктор.Ру. 10, 51–55;
- Dagfinn Aune, Sabrina Schlesinger, Teresa Norat, Elio Riboli. (2018). Tobacco smoking and the risk of abdominal aortic aneurysm: a systematic review and meta-analysis of prospective studies. Sci Rep. 8;
- Jonathan Golledge, Paul E. Norman. (2010). Atherosclerosis and Abdominal Aortic Aneurysm. ATVB. 30, 1075-1077;
- J. Cornuz. (2004). Risk factors for asymptomatic abdominal aortic aneurysm: Systematic review and meta-analysis of population-based screening studies. The European Journal of Public Health. 14, 343-349;
- Nikolaos Kontopodis, Dimitrios Pantidis, Athansios Dedes, Nikolaos Daskalakis, Christos V. Ioannou. (2016). The – Not So – Solid 5.5 cm Threshold for Abdominal Aortic Aneurysm Repair: Facts, Misinterpretations, and Future Directions. Front. Surg.. 3;
- Kristina Grassl, Thomas C. Gasser, Florian K. Enzmann, Alexandra Gratl, Josef Klocker, et. al.. (2024). Early Prediction of Abdominal Aortic Aneurysm Rupture Risk Using Numerical Biomechanical Analysis. Diagnostics. 15, 25;
- Radek Vitásek, Luboš Kubíček, David Schwarz, Robert Staffa, Stanislav Polzer. (2024). Tension-based abdominal aortic aneurysm rupture risk assessment improves its accuracy and reduces the time of analysis. Journal of Biomechanics. 176, 112328;
- Andres Schanzer, Louis Messina. (2012). Two Decades of Endovascular Abdominal Aortic Aneurysm Repair: Enormous Progress With Serious Lessons Learned. JAHA. 1;
- Piotr Kulig, Krzysztof Lewandowski, Damian Ziaja, Maciej Zaniewski, Jan Kulig. (2016). Endovascular Aneurysm Repair or Open Aneurysm Repair for the Treatment of Abdominal Aortic Aneurysm – The Latest Update. Polish Journal of Surgery. 88;
- Christopher D. Blackstock, Benjamin M. Jackson. (2020). Open Surgical Repair of Abdominal Aortic Aneurysms Maintains a Pivotal Role in the Endovascular Era. Semin intervent Radiol. 37, 346-355;
- Yousef Yousef, Claire Dawkins. (2024). Innovations in abdominal aortic aneurysm repair: a comprehensive overview. Surgery (Oxford). 42, 327-334;
- Vinamr Rastogi, Christina L. Marcaccio, Priya B. Patel, Rens R.B. Varkevisser, Virendra I. Patel, et. al.. (2022). A retroperitoneal operative approach is associated with improved perioperative outcomes compared with a transperitoneal approach in open repair of complex abdominal aortic aneurysms. Journal of Vascular Surgery. 76, 354-363.e1;
- Niamh Hynes, Yogesh Acharya, Sherif Sultan. (2022). The contemporary design of endovascular aneurysm stent-graft materials: PTFE versus polyester. Front. Surg.. 9;
- Stéphane Avril, Michael W. Gee, André Hemmler, Sandra Rugonyi. (2021). Patient‐specific computational modeling of endovascular aneurysm repair: State of the art and future directions. Numer Methods Biomed Eng. 37;
- Ali Abdul Jabbar, Arijit Chanda, Christopher J. White, James Stephen Jenkins. (2020). Percutaneous endovascular abdominal aneurysm repair: State‐of‐the art. Cathet Cardio Intervent. 95, 767-782;
- Atsushi Aoki, Kazuto Maruta, Tomoaki Masuda, Tadashi Omoto. (2023). Factors Influencing on the Aneurysm Sac Shrinkage after Endovascular Abdominal Aortic Aneurysm Repair by the Analysis of the Patients with the Aneurysm Sac Shrinkage and Expansion. Annals of Vascular Diseases. 16, 245-252;
- Quan Chen, Yuan Zhang, Kangqing Lei, Liangyin Fu, Dengxiao Zhang, et. al.. (2023). Efficacy and safety of prophylactic intraoperative sac embolization in EVAR for abdominal aortic aneurysm: A meta-analysis. Front. Surg.. 9;
- Tyler Smith, Keith B. Quencer. (2020). Best Practice Guidelines: Imaging Surveillance After Endovascular Aneurysm Repair. American Journal of Roentgenology. 214, 1165-1174;
- Giuseppe Sena, Rossella Montemurro, Francesco Pezzo, Rosario Gioffrè, Giuseppe Gallelli, Paolo Rubino. (2023). Contralateral Snare Cannulation vs. Retrograde Gate Cannulation during Endovascular Aortic Repair in Difficult Iliac Artery Anatomy: A Single Center Experience. JCM. 13, 175;
- Jin Hyun Joh. (2024). Novel Strategies for the Hostile Iliac Artery during Endovascular Aortic Aneurysm Repair. Vasc Specialist Int. 40;
- James R Vienneau, Camden I Burns, Anto Boghokian, Varun Soti. (2024). Endovascular Aneurysm Repair Versus Open Surgical Repair in Treating Abdominal Aortic Aneurysm. Cureus;
- Amrita M Cherian, Rakshaya Venu, Pavithra Ishita Raja, Sabanantham Saravanan, Usman Khan, et. al.. (2024). Outcomes of Endovascular Aneurysm Repair (EVAR) Compared to Open Repair in Abdominal Aortic Aneurysm: An Umbrella Meta-Analysis. Cureus;
- Georgios Loufopoulos, Panagiotis Tasoudis, Georgios Koudounas, Ioannis Zoupas, Nikolaos Madouros, et. al.. (2025). Long-Term Outcomes of Open Versus Endovascular Treatment for Abdominal Aortic Aneurysm: Systematic Review and Meta-Analysis With Reconstructed Time-to-Event Data. J Endovasc Ther. 32, 946-956;
- Marwan Y. Abdulkadder, Roda Rashid Bin Sultan Alshamsi, Hanadi Mohamad Al Hussami, Meera Ahmed Mohamed Othman Ali, Nabaa Shakir Mahmood, et. al.. (2025). Comparison of Endovascular vs Open Repair for Abdominal Aortic Aneurysm: Mortality and Morbidity Outcomes. J Surg Res. 72-86;
- Nikolaos Kontopodis, Nikolaos Galanakis, Stavros Charalambous, Miltiadis Matsagkas, Athanasios D. Giannoukas, et. al.. (2022). Editor's Choice – Endovascular Aneurysm Repair in High Risk Patients: A Systematic Review and Meta-Analysis. European Journal of Vascular and Endovascular Surgery. 64, 461-474;
- Laura E. Newton, Aravind Ponukumati, Gabrielle Zwain, Caroline Korves, Jialin Mao, et. al.. (2025). Imaging Surveillance Adherence After Endovascular Abdominal Aortic Aneurysm Repair at VA Hospitals. JAMA Netw Open. 8, e256852;
- Zachary J. Wanken, J. Aaron Barnes, Spencer W. Trooboff, Jesse A. Columbo, Tarun K. Jella, et. al.. (2020). A systematic review and meta-analysis of long-term reintervention after endovascular abdominal aortic aneurysm repair. Journal of Vascular Surgery. 72, 1122-1131.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚