Бактериоцины — ноухау биомедицины
19 октября 2017
Бактериоцины — ноухау биомедицины
- 3567
- 0
- 9
Бактериоцин субтилозин.
-
Автор
-
Редактор
Статья на конкурс «био/мол/текст»: Распространение устойчивости к антибиотикам у бактерий, вызывающих инфекционные заболевания, привело к необходимости разработки новых методов лечения. Одним из перспективных является создание препаратов на основе бактериоцинов — небольших пептидов, подавляющих рост бактерий. Многие научные группы занимаются исследованием этих веществ, и в обозримом будущем возможно их становление в качестве альтернативы антибиотикам.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Биомедицина сегодня и завтра» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Считается, что нерациональное использование антибиотиков в сочетании с самолечением привело к развитию бактерий, устойчивых к наиболее распространенным препаратам. В последние годы люди стали уделять большее внимание данной проблеме [2].
Ученые пытаются разрабатывать новые виды антибиотиков для борьбы с болезнями бактериального происхождения. Однако из всех синтезируемых молекул лишь 0,01% имеют антимикробную активность. И зачастую эти новые соединения имеют высокую себестоимость или оказывают высокотоксичное действие на человека [3].
Ознакомление с проблемой
Ярким примером бактерий, устойчивых к антибиотикам, могут служить представители рода энтерококков. Раньше они считались безобидными членами нашей микрофлоры, потом оказалось, что они являются одной из главных причин внутрибольничных инфекций, и значит, с ними надо бороться. Чаще всего против энтерококков применяли антибиотик ванкомицин. Если в 2000 году в США зафиксировали 9820 случаев заболеваний, вызванных ванкомицинустойчивыми энтрекококками, то в 2006-м их стало 21 352 [4].
Возможные пути решения
Одним из перспективных альтернативных методов борьбы с патогенными бактериями долгое время считали фаготерапию — лечение больных бактериальными инфекциями введением в организм бактериофагов. Бактериофаги — это вирусы, способные уничтожать бактерий. Более подробно о них вы можете почитать в другой статье — «Пожиратели бактерий: убийцы в роли спасителей» [5]. В поисках бактериофагов, которые будут бороться с патогенными бактериями, достигли определенных успехов, но при всех преимуществах данного способа нашли и ряд минусов. Самый главный — это то, что бактериофаги являются очень специфичными к определенному штамму бактерий. Получается, что даже если будет подобран бактериофаг для лечения какой-то болезни, не факт, что он сможет справиться со всем разнообразием бактерий, ее вызывающих [6]. Однако бактериофаги применяют уже несколько лет в стоматологии, причем довольно успешно, и это дает шанс фаготерапии найти более широкое применение [7].
Другим популярным способом в попытках заменить антибиотики является использование бактериоцинов. Бактериоцины — большое семейство секретируемых бактериями пептидов, обладающих антимикробной активностью и действующих против других штаммов того же вида или близкородственных видов [8]. Вы можете прочитать еще две статьи на сайте «Биомолекулы», посвященные данной теме: «Антимикробные пептиды — возможная альтернатива традиционным антибиотикам» [9] и «Антибиотики прямо под нашим носом» [10].
Бактериоцины синтезируют почти все известные бактерии. Известно, что бактерии бывают грамположительные и грамотрицательные. И те, и другие подавляют близкородственные виды и тем самым прекращают их рост согласно механизмам, описанным на рисунке 1.
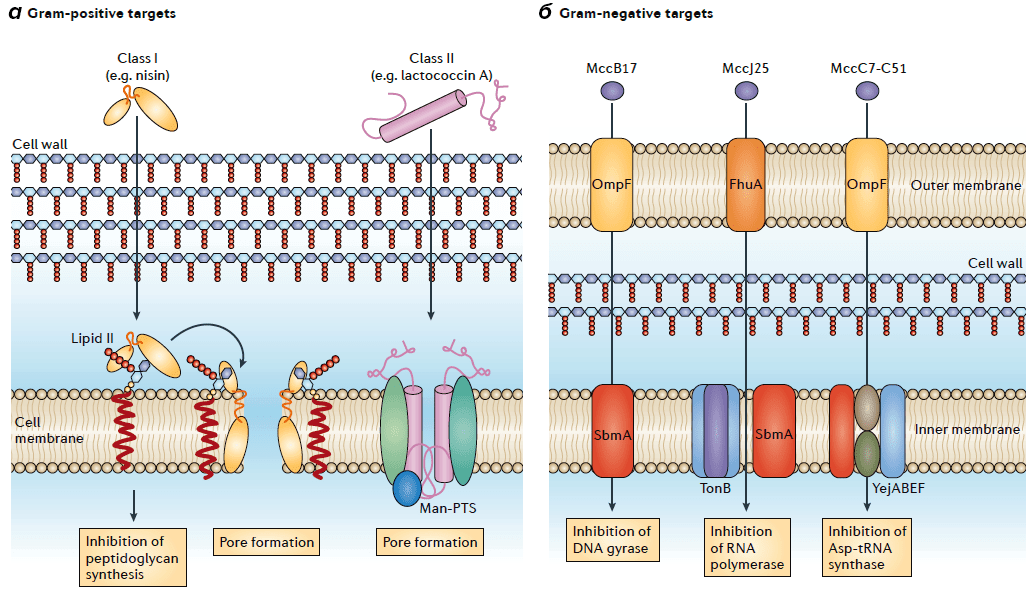
Рисунок 1. Механизмы действия бактериоцинов. а — Механизм действия бактериоцинов грамположительных бактерий: низин и некоторые другие бактериоцины класса I ингибируют синтез пептидогликана, связываясь с липидом II, и образуют поры; бактериоцины класса II, такие как лактококцин А, связываются с порообразующей рецепторной маннозо-фосфотрансферазной системой (Man-PTS). б — Механизм действия бактериоцинов грамотрицательных бактерий: микроцин B17 (MccB17) ингибирует ДНК-гиразу, MccJ25 ингибирует РНК-полимеразу, а MccC7-C51 ингибирует аспартил-тРНК-синтетазу.
Чтобы увидеть рисунок в полном размере, нажмите на него.
Рисунок можно объяснить и более простым образом. В левой части изображено действие бактериоцинов грамположительных бактерий: по сути, они приводят к образованию дырок в мембране, и клетка просто погибает. В правой — показан механизм действия бактериоцинов, продуцируемых грамотрицательными бактериями: они блокируют синтез каких-либо важных ферментов, что также приводит к гибели клетки.
Бактериоцины обладают рядом преимуществ, позволяющим заявить — они являются жизнеспособной альтернативой антибиотикам [11]:
- антимикробная активность (как определено in vitro и in vivo);
- низкая токсичность;
- широкий и узкий спектр действия разных пептидов;
- возможность производства in situ пробиотиками;
- возможность создания на их основе биоинженерных конструкций.
Субтилозин
Один из недавно открытых бактериоцинов — субтилозин. Его продуцирует Bacillus spp. Данный пептид, как и многие другие, проявляет активность по отношению к близкородственным видам и Listeria monocytogenes (чей рост подавляют многие бактериоцины). Как и все бактериоцины грамположительных бактерий, субтилозин убивает путем образования пор в мембранах чувствительных клеток [12]. Штаммы, продуцирующие этот бактериоцин, считаются потенциальными пробиотиками, так как способны подавлять рост болезнетворных бактерий, которые могут разрушать нашу кишечную микрофлору [13].
Однако, как и другие бактериоцины, он должен быть подвергнут подробному анализу, поскольку до сих пор не проводили клинических испытаний бактериоцинов или препаратов на их основе.
Альтернативное использование
Считается, что бактериоцины можно использовать в качестве естественных консервантов продуктов питания. Один из них, а именно низин, выделяют из бактерии Streptococcus lactis [14] и уже используют в коммерческих целях. Его можно встретить в составе на этикетках под именем E234.
В последнее время также появляется много информации на тему возможности использования бактериоцинов в борьбе с раком. Что может сделать их почти панацеей нашего времени в случае успешного внедрения в медицинскую практику [15].
В заключение можно сказать о том, что, вероятно, в скором будущем появятся новые способы борьбы с инфекционными бактериальными заболеваниями в случае успешного изучения особенностей функционирования бактериоцинов. Что станет достойной альтернативной антибиотикам в будущем.
Литература
- Vijaya R. Pattabiraman, Jeffrey W. Bode. (2011). Rethinking amide bond synthesis. Nature. 480, 471-479;
- Kai Li, Lici A. Schurig-Briccio, Xinxin Feng, Ashutosh Upadhyay, Venugopal Pujari, et. al.. (2014). Multitarget Drug Discovery for Tuberculosis and Other Infectious Diseases. J. Med. Chem.. 57, 3126-3139;
- Ville Ojala, Jarkko Laitalainen, Matti Jalasvuori. (2013). Fight evolution with evolution: plasmid-dependent phages with a wide host range prevent the spread of antibiotic resistance. Evol Appl. 6, 925-932;
- Cesar A. Arias, Barbara E. Murray. (2012). The rise of the Enterococcus: beyond vancomycin resistance. Nat Rev Micro. 10, 266-278;
- Пожиратели бактерий: убийцы в роли спасителей;
- Alessandra C. Rios, Carla G. Moutinho, Flávio C. Pinto, Fernando S. Del Fiol, Angela Jozala, et. al.. (2016). Alternatives to overcoming bacterial resistances: State-of-the-art. Microbiological Research. 191, 51-80;
- Mor Shlezinger, Leron Khalifa, Yael Houri-Haddad, Shunit Coppenhagen-Glazer, Grégory Resch, et. al.. (2017). Phage Therapy: A New Horizon in the Antibacterial Treatment of Oral Pathogens. CTMC. 17, 1199-1211;
- Luc De Vuyst, Frédéric Leroy. (2007). Bacteriocins from Lactic Acid Bacteria: Production, Purification, and Food Applications. J Mol Microbiol Biotechnol. 13, 194-199;
- Антимикробные пептиды — возможная альтернатива традиционным антибиотикам;
- Антибиотики прямо под нашим носом;
- Paul D. Cotter, R. Paul Ross, Colin Hill. (2012). Bacteriocins — a viable alternative to antibiotics?. Nat Rev Micro. 11, 95-105;
- Sathiah Thennarasu, Dong-Kuk Lee, Alan Poon, Karen E. Kawulka, John C. Vederas, Ayyalusamy Ramamoorthy. (2005). Membrane permeabilization, orientation, and antimicrobial mechanism of subtilosin A. Chemistry and Physics of Lipids. 137, 38-51;
- Nalisa Khochamit, Surasak Siripornadulsil, Peerapol Sukon, Wilailak Siripornadulsil. (2015). Antibacterial activity and genotypic–phenotypic characteristics of bacteriocin-producing Bacillus subtilis KKU213: Potential as a probiotic strain. Microbiological Research. 170, 36-50;
- Ana Andréa Teixeira Barbosa, Hilário Cuquetto Mantovani, Sona Jain. (2017). Bacteriocins from lactic acid bacteria and their potential in the preservation of fruit products. Critical Reviews in Biotechnology. 37, 852-864;
- Sumanpreet Kaur, Sukhraj Kaur. (2015). Bacteriocins as Potential Anticancer Agents. Front. Pharmacol.. 6.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚