Две крепости одного организма: вагинальная и кишечная микробиота
08 апреля 2026
Две крепости одного организма: вагинальная и кишечная микробиота
- 759
- 0
- 3
Иллюстрация показывает взаимное влияние вагинального и кишечного микробиома. Взаимодействие между этими двумя ключевыми микробными сообществами может влиять на общее состояние здоровья.
Рисунок в полном размере.
рисунок Олеси Иванковой, сделан с использованием инструментов искусственного интеллекта
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Кишечная и вагинальная микробиоты долгое время считались изолированными системами. Однако исследования показывают, что между ними существует тесная связь. Наша статья расскажет о механизмах этого удивительного диалога и о том, как его нарушение приводит к болезням.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Две микробные вселенные внутри нас
В человеческом организме существует множество микробных сообществ, начиная от ротовой полости, заканчивая микрофлорой кожи стоп. Самое крупное и изученное сообщество находится в кишечнике, а одно из самых немногочисленных — сообщество репродуктивного тракта женщин. При этом, несмотря на четкое анатомическое разделение, кишечный и влагалищный микробиомы находятся в постоянном взаимодействии, обмениваясь микроорганизмами и продуктами их метаболизма.
Эта связь, обозначаемая в научной литературе как ось «кишечник—влагалище», пока уступает по изученности знаменитой оси «кишечник—мозг» [1]. Но по степени влияния на женское здоровье и исход беременности, предрасположенность к инфекциям и воспалительным состояниям, она может оказаться не менее значимой.
Та двусторонняя связь, которая существует между кишечником и влагалищем, приводит к тому, что состояние одной микробиоты напрямую влияет на здоровье другой [2]. Нарушение баланса микробиоты (дисбиоз) в кишечнике может «эхом» отозваться во влагалище, спровоцировав инфекцию, и, наоборот, заболевания репродуктивной системы и их лечение могут усугубить течение заболеваний кишечника [3]. В этой статье мы отправимся в путешествие по этой удивительной оси — «кишечник-влагалище», чтобы разобраться, как именно наши внутренние «вселенные» общаются друг с другом, и почему поддержание мира в одной из них так важно для процветания другой (рис. 1).
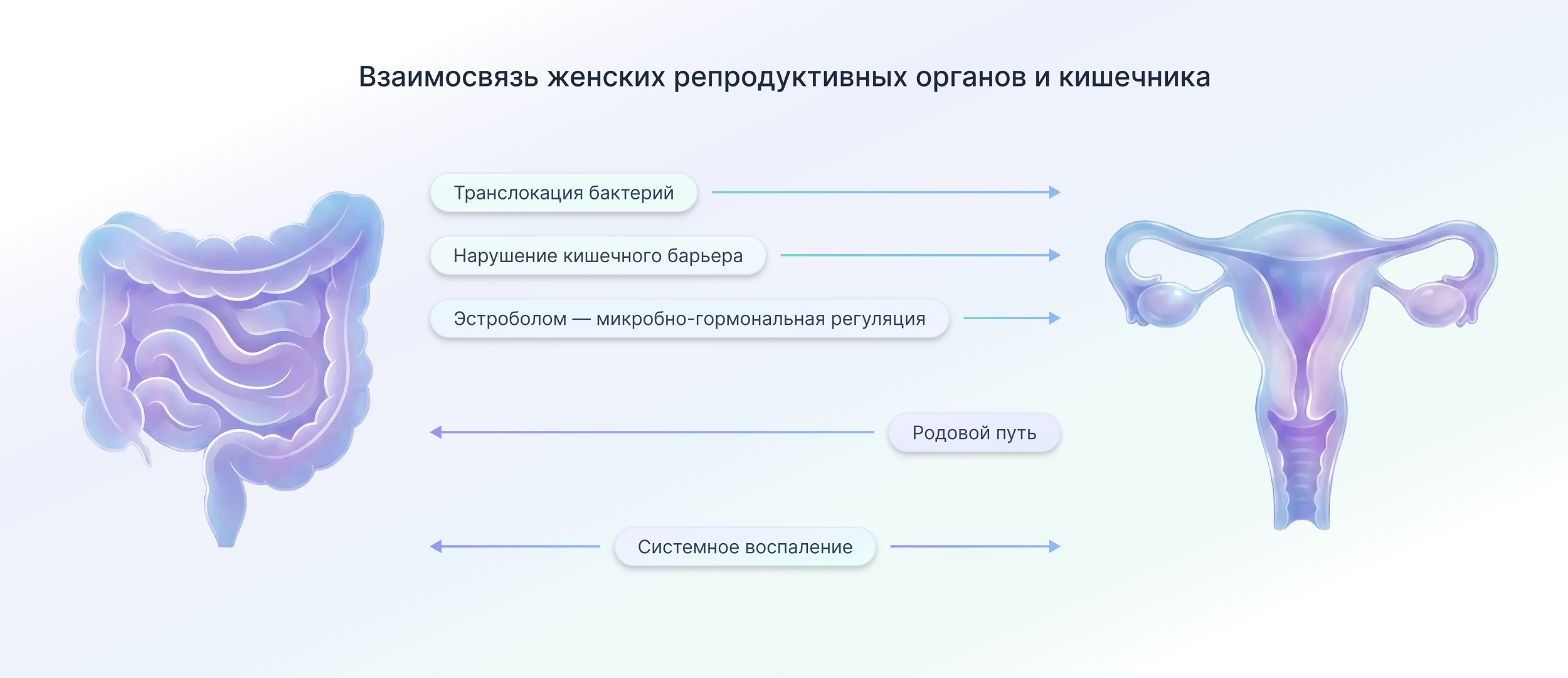
Рисунок 1. Основные механизмы взаимодействия между кишечником и женской репродуктивной системой.
рисунок Софьи Цветиковой
От кишечника к влагалищу
Говоря о микробиоме человека, мы чаще всего имеем в виду кишечный, — ему посвящено больше всего научных работ, и он представляет собой самый масштабный резервуар микроорганизмов в нашем теле [2]. Для сравнения, общая биомасса бактерий урогенитального тракта составляет лишь около 5–10% от всей микробиоты человека, тогда как на кишечную микробиоту приходится до 70–80% всех микробов организма [2], [4].
Основу влагалищного микробиома в норме составляют лактобациллы — они, как правило, хорошо растут в лабораторных условиях. Но за этим «лактобацилльным фоном» скрываются десятки, если не сотни, других видов — часто анаэробных, медленно растущих или требовательных к специфическим условиям. Именно этих «невидимых» участников микробного сообщества сложнее всего выделить и охарактеризовать культуральными методами [2].
То, что бактерии способны мигрировать из кишечника во влагалище, достаточно давно известно. В обоих микробиомах наиболее часто встречаются бактерии типов Firmicutes, Bacteroidetes, Proteobacteria, Actinobacteria и Fusobacteria. Яркий пример — грамположительные палочки Lactobacillus, которые обычно доминируют в здоровой вагинальной микробиоте. Ученые полагают, что их прародина — кишечник. И это логично, ведь лактобациллы активно живут и в пищеварительном тракте, где играют ключевую роль в функционировании микробного сообщества. Исследования показывают, что у значительной части женщин одни и те же штаммы бактерий (включая лактобациллы и другие виды) обнаруживаются одновременно в прямой кишке и во влагалище [2], [5]. Это значит, что кишечник может являться резервуаром для условно-патогенных бактерий, например, Gardnerella vaginalis и Atopobium vaginae, вызывающих бактериальный вагиноз [6].
Однако связь между кишечником и репродуктивной системой — это не только прямое физическое переселение бактерий. Существует и другой канал связи, где кишечные бактерии управляют ключевыми сигналами организма, влияя на здоровье женщины на уровне гормонов. Речь идет об эстроболоме.
Гормональный регулятор: что такое эстроболом?
Представьте, что печень «упаковывает» избыток эстрогенов для вывода из организма — прикрепляет к ним молекулу глюкуроновой кислоты, делая их водорастворимыми и неактивными. Но некоторые кишечные бактерии «распаковывают» эти гормоны обратно с помощью фермента β-глюкуронидазы — и тогда эстрогены снова всасываются и попадают в кровь: так микробиом регулирует гормональный фон изнутри через механизм энтерогепатической циркуляции эстрогенов. К микроорганизмам, имеющим β-глюкуронидазную активность, относятся, например, Clostridium, Escherichia, Bacteroides, Lactobacillus [7], а совокупность бактериальных генов в кишечнике, отвечающих за метаболизм эстрогенов, называется эстроболомом [8]. Когда микробиом сбалансирован, бактерии поддерживают физиологические уровни циркулирующего эстрогена. При нарушении баланса микробиоты количество и активность эстроген-метаболизирующих бактерий меняется, что приводит либо к гиперэстрогенизму — избытку активного эстрогена, либо к его недостатку — гипоэстрогенизму.
Например, исследование с участием более 2300 женщин показало, что в постменопаузе снижается активность бактериальной β-глюкуронидазы в кишечнике. Это снижение коррелирует с изменением уровня метаболитов прогестина в сыворотке крови, что указывает на роль микробиома в реактивации половых гормонов. Это особенно важно во время менопаузы, когда естественное снижение выработки эстрогенов яичниками делает энтерогепатическую циркуляцию значимым механизмом поддержания их системного уровня [9].
И наоборот, патологически повышенная активность β-глюкуронидазы является фактором влияния на эстроген-зависимые состояния. Например, исследование эндометрия у женщин с бесплодием и повторными неудачами имплантации показало, что в условиях дисбиоза (снижения доли лактобацилл менее 90%) активность β-глюкуронидазы в ткани эндометрия была достоверно выше, чем в норме, и коррелировала с увеличением экспрессии рецептора эстрогена и маркеров воспаления IL-1β. Это позволяет предположить, что локальная гиперпродукция β-глюкуронидазы в эндометрии на фоне дисбиоза может способствовать избыточной реактивации эстрогенов, усилению воспаления и нарушению восприимчивости слизистой оболочки матки [10].
Большой интерес представляют данные о влиянии эстроболома на онкологию. Так, в ходе исследования, которое напрямую сравнивало состав кишечной микробиоты у здоровых женщин и пациенток с раком молочной железы (РМЖ), была обнаружена характерная «микробная подпись» болезни. У пациенток с РМЖ были более распространены бактерии, продуцирующие β-глюкуронидазу, такие как Citrobacter, Bacteroides, Enterobacter и Bifidobacterium. В то же время, в контрольной группе здоровых женщин, особенно в возрасте старше 40 лет, была значительно выше доля бактерий рода Staphylococcus. Интересно, что выделенные из этой бактерии внеклеточные везикулы усиливали действие гормональной терапии тамоксифеном на раковые клетки, вероятно, через модуляцию внутриклеточных сигнальных путей. Эти результаты предлагают новую перспективу: бактериальные везикулы в будущем могут быть рассмотрены как потенциальные адъюванты (вспомогательные средства) для лечения РМЖ [11].
Учитывая важность таких результатов, ученые активно разрабатывают и исследуют ингибиторы β-глюкуронидазы как потенциальный терапевтический подход для модуляции эстрогена [12]. В настоящее время эти соединения находятся на доклинической стадии разработки, и для перехода в клиническую практику необходимы дальнейшие масштабные исследования для подтверждения эффективности и безопасности этих соединений у человека.
Однако нарушение работы эстроболома — лишь один, хотя и чрезвычайно важный, пример того, как дисбаланс в кишечнике может «отозваться» на гинекологической сфере. Дисбиоз способен влиять на репродуктивное здоровье не только через эндокринную регуляцию, но и более прямым путем — ослабляя защитные барьеры организма и нарушая работу иммунитета. Давайте рассмотрим, как именно это происходит.
Разлад в кишечнике — угроза репродуктивной системе
Нарушения в составе кишечной микробиоты — это не локальная проблема, а системный сбой, последствия которого ощущаются во всем организме, включая репродуктивную систему.
Дисбаланс микробиоты кишечника является не диагнозом, а состоянием. Вокруг его определения много споров, однако в целом исследователи сходятся во мнении, что он может проявляться снижением микробного разнообразия, избыточным ростом или отсутствием отдельных групп бактерий (пробиотических, условно-патогенных), наличием патогенных бактерий [13], [14]. Так к чему приводит кишечный дисбиоз, помимо дисрегуляции метаболизма эстрогенов [15]?
- Нарушение кишечного барьера («дырявый кишечник») из-за снижения выработки короткоцепочечных жирных кислот (КЦЖК), особенно бутирата, приводит к попаданию липополисахаридов (ЛПС) в кровоток и метаболической эндотоксемии. Например, у пациенток с эндометриозом наблюдается повышенная кишечная проницаемость, что приводит к хроническому воспалению и росту эндометриоидных очагов [16].
- Также на животных моделях было показано, что кишечная микробиота при эндометриозе может не только нарушать проницаемость кишечного эпителия, но и приводить к бактериальной транслокации в жидкость брюшной полости, что также является важным драйвером воспаления [17].
- Нарушение регуляции синтеза иммуноглобулина А (IgA) под влиянием дисбиотической микробиоты приводит к ослаблению местного иммунитета. IgA не только регулирует состав микробиоты, но и ограничивает взаимодействие патогенов с иммунной системой. При дефиците IgA нарушается целостность слизистого барьера, что приводит к бактериальной транслокации и дисрегуляции иммунных ответов [18]. В вагинальных секретах пациенток с бактериальным вагинозом отмечается достоверное снижение как IL-33, так и IgA [19]. Некоторые патогенные микроорганизмы, такие как Ureaplasma urealyticum (уреаплазма) секретирует IgA-белок, расщепляющий защитный иммуноглобулин IgA1 на фрагменты, позволяя бактерии ослаблять местный иммунитет [20].
Но на самом деле, все эти сложные механизмы взаимодействия микробиоты, о которых мы говорили, закладываются гораздо раньше. Если кишечный микробиом активно влияет на здоровье генитального тракта взрослого человека, то вагинальный микробиом матери, в свою очередь, играет ключевую роль в самом начале жизни, фактически передавая эстафету микробного здоровья следующему поколению. Именно во время родов происходит первое и самое масштабное «знакомство» новорожденного с микробным миром, что определяет фундамент его будущего здоровья. Чтобы в полной мере оценить эту фундаментальную взаимосвязь, обратимся к самому началу — процессу рождения.
Важность родов: как вагинальные бактерии матери влияют на кишечный микробиом младенца
Влияние вагинальных микроорганизмов на состояние кишечника — процесс, начинающийся в самый первый момент нашей жизни. Наиболее масштабное и значимое переселение микробов из одного организма в другой происходит во время рождения, когда ребенок, проходя через родовые пути, получает от матери уникальный микробный «стартовый набор», во многом определяющий будущее здоровье его собственного кишечника и иммунитета [21]. Давайте рассмотрим этот процесс детальнее.
Итак, самый первый способ путешествия бактерий, населяющих человеческий организм, — это роды. При естественном родоразрешении младенец контактирует с микробиомом влагалища и промежности матери, и эти микробы, в том числе пробиотические Lactobacillus, являются первыми колонизаторами организма ребенка [22].
А вот дети, рожденные с помощью кесарева сечения, не подвергаются такому первоначальному контакту и в основном колонизируются бактериями кожи и окружающей среды (Staphylococcus, Corynebacterium и Streptococcus spp [22], [23]), что может привести к неоптимальному развитию микробиома ребенка. Из-за этого такие дети подвержены повышенному риску воспалительных, метаболических и неврологических нарушений в более позднем возрасте [22].
Однако этот исходный дисбаланс может быть в значительной степени скорректирован. Исследования указывают на то, что нарушения в развитии микробиоты у детей после кесарева сечения могут со временем сглаживаться благодаря грудному вскармливанию, контакту с матерью и окружающей средой [24]. Так, грудное вскармливание может повысить уровень пробиотических бактерий, таких как L. johnsonii, L. gasseri, L. paracasei, L. casei и B. longum, которых так не хватает после кесарева сечения. Также в некоторых случаях для поддержки формирования здоровой микробиоты у таких детей могут применяться пробиотические препараты с Bifidobacterium и Lactobacillus, хотя их необходимость определяется индивидуально [25].
Помимо вагинальной микробиоты, важную роль играет и фекальная микробиота матери, которая также передается ребенку в процессе родов [26]. Бактерии, которые массово заселяют кишечник младенцев при вагинальных родах, — это Bacteroides. Причем их успешное и долговременное закрепление в кишечнике младенца, рожденного вагинально, зависит от сложившейся поддерживающей микробной сети (включающей, например, Collinsella, Ruminococcus и Veillonella). Bacteroides обладают уникальными молекулами на своей поверхности, которые «обучают» иммунную систему новорожденного не атаковать полезные бактерии и отличать их от патогенов [27]. Отсутствие или низкое количество этих бактерий связывают с «необученной», склонной к аллергическим реакциям иммунной системой [28]. Колонизация кишечника бифидобактериями в раннем младенческом возрасте также имеет решающее значение для здоровья ребенка, так как Bifidobacterium важны для усвоения грудного молока, формирования иммунитета, укрепления кишечного барьера и защиты от патогенов [29–31]. Но, в отличие от Bacteroides, Bifidobacterium часто удается «добрать» с помощью пробиотиков и грудного молока, если все-таки было проведено кесарево сечение [32].
Понимая, насколько глубоко и многообразно связаны две эти экосистемы — кишечный и влагалищный микробиомы, и как их дисбаланс ведет к заболеваниям, закономерно возникает вопрос: что мы можем с этим сделать?
Терапевтические перспективы: восстановление баланса в обеих экосистемах
Мы убедились, что нарушение баланса внутри оси «кишечник–влагалище» может привести к печальным последствиям. К счастью, существуют целенаправленные стратегии для одновременного восстановления и поддержания гармонии в этих взаимосвязанных микромирах. Давайте вместе рассмотрим их (рис. 2).
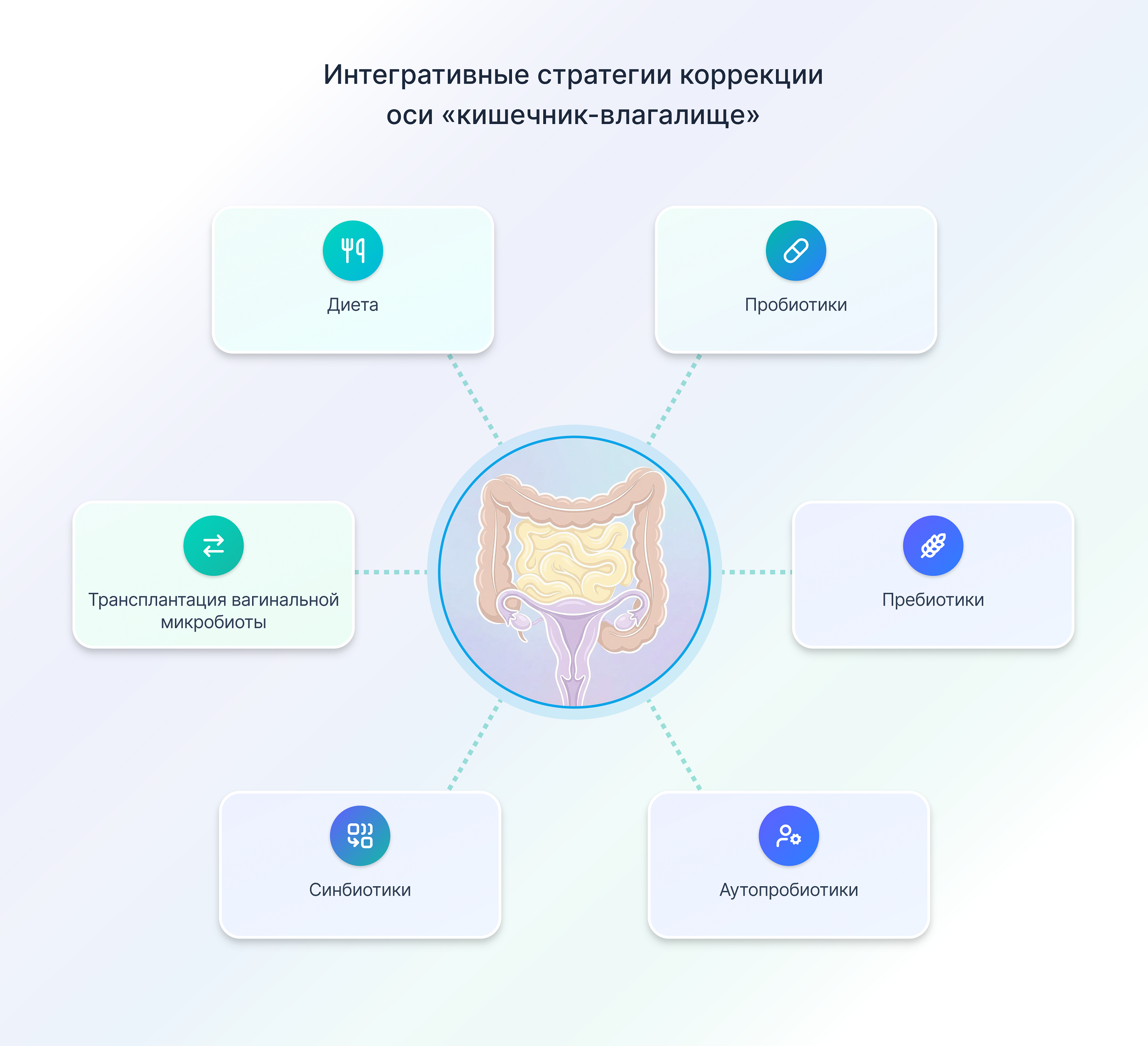
Рисунок 2. Визуализация ключевых подходов к коррекции оси «кишечник–влагалище»: от питания и пробиотиков до передовых методов вроде трансплантации микробиоты и аутопробиотиков.
рисунок Софьи Цветиковой
Диета для здоровья микробиоты
Здоровье нашего кишечника, а через него и всего тела, начинается с рациона, богатого клетчаткой. Овощи, фрукты, бобовые и цельнозерновые продукты являются лакомством для наших полезных бактерий-сожителей, которые перерабатывают эту клетчатку с образованием КЦЖК.
Эти кислоты можно назвать настоящими телохранителями нашего организма. Они подавляют воспалительные процессы и укрепляют кишечный барьер, обеспечивая защиту против проникновения токсинов и патогенов в кровоток. Такой стабильный и здоровый кишечник, как мы уже знаем, помогает сохранять равновесие и в микробном сообществе влагалища [33]. Интересно, что рацион с высоким содержанием пищевых волокон во время беременности был связан с большей численностью L. crispatus — одного из главных защитников влагалищной среды [34].
Другими союзниками нашего микробиома можно назвать омега-3 жирные кислоты, которые в изобилии содержатся в жирной рыбе и орехах, а также полифенолы из ягод, кофе, какао и чая. Эти компоненты питания оказывают комплексное благотворное влияние на кишечную микрофлору, мягко способствуя росту полезных бактерий.
В кросс-секционном исследовании были проанализированы данные 2345 женщин, оценивалось потребление пищевых волокон и наличие воспалительных заболеваний органов малого таза. Высокое потребление клетчатки у них было ассоциировано с модуляцией вагинальной микробиоты и снижением риска бактериального вагиноза. Было установлено, что пищевые волокна через ось «кишечник—репродуктивный тракт» способствуют росту полезных бактерий (Lactobacillus, Bifidobacterium), производящих КЦЖК. Клетчатка также влияет на метаболизм эстрогена через кишечную β-глюкуронидазу, что усиливает защитные функции вагинальной среды за счет повышения кислотности и утолщения эпителия. Был определен пороговый эффект в 19,45 г/день клетчатки, при превышении которого значительно снижается риск воспалительных заболеваний органов малого таза [35].
Итак, мы убедились, что правильное питание создает основу для здоровья микробиоты, но иногда для восстановления баланса необходима целенаправленная поддержка. Здесь на помощь приходят специальные биологически активные добавки.
Пробиотики, пребиотики и синбиотики
Для восстановления нарушенной микробиоты применяются пробиотики, пребиотики и их комбинации — синбиотики.
- Пробиотики — это живые микроорганизмы, которые при поступлении в достаточном количестве приносят пользу здоровью хозяина. Эффекты пробиотиков являются штаммоспецифичными. Например, определенные штаммы лактобацилл (такие как Lactobacillus rhamnosus GR-1 и L. fermentum RC-14) демонстрируют способность к транслокации — они могут мигрировать из кишечника во влагалище, оказывая защитное действие в обеих экосистемах [36]. Эти бактерии подавляют рост патогенов, вырабатывая молочную кислоту, бактериоцины и перекись водорода, а также укрепляют местный иммунитет [36].
Но, кроме пробиотиков, возможно и расширение рациона ферментированными продуктами — в них тоже обитают полезные бактерии. Йогурт, кефир, квашеная капуста и комбуча напрямую поставляют в ЖКТ полезные живые штаммы. Например, исследования влияния употребления комбучи с инулином на здоровых людях на протяжении 6 недель показало, что ферментированный напиток меняет состав микробиоты: снижает количество бактерий Ruminococcus torques (ассоциированы с воспалительными заболеваниями кишечника) и увеличивает Bifidobacterium (род бактерий, известных своими преимуществами для здоровья кишечника и иммуномодулирующими эффектами) [37]. Другой ферментированный продукт — йогурт, содержащий живые лактобактерии Lactobacillus acidophilus, в испытании на 33 женщинах с рецидивирующим вагинальным кандидозом в течение 6 месяцев показал, что в «йогуртовый» период частота острых инфекций снизилась в три раза. Если без йогурта женщины болели в среднем 2,5 раза за полгода, то во время «йогуртовой» диеты этот показатель упал до менее чем одного случая [38]. - Пребиотики — это компоненты пищи (например, инулин, фруктоолигосахариды), которые не перевариваются и не усваиваются в верхних отделах желудочно-кишечного тракта, а служат «топливом» для пробиотических бифидо- и лактобактерий и других полезных бактерий. Потребление продуктов, богатых пребиотиками (бананы, чеснок, лук, отруби, цикорий), помогает поддерживать иммунитет и способствует производству КЦЖК.
Интересным примером «нетрадиционного» применения пребиотика служит лактулоза. Лактулоза — это искусственно созданный из молочного сахара пребиотик, который наш организм не переваривает, но который служит «удобрением» для полезных бактерий в кишечнике, стимулируя их рост и выработку полезных веществ. При интравагинальном использовании она создает питательную среду, избирательно стимулирующую рост лактобацилл, которые конкурируют с патогенами, такими как Candida albicans, и восстанавливают кислую среду влагалища за счет выработки молочной кислоты [39].
Кроме того, в недавнем клиническом исследовании, проведенном российскими учеными, было выявлено, что комбинация антибиотика натамицина и лактулозы интровагинально обеспечивает более быстрое достижение клинической ремиссии при остром кандидозном вульвовагините по сравнению с монотерапией натамицином. Уже на 7-й день лечения количество пациенток без симптомов в группе комбинированного препарата было на 25% больше, чем в контрольной группе. Кроме того, через месяц после начала терапии у женщин, получавших эту комбинацию, отмечался в 100 раз более высокий уровень лактобацилл во влагалище, что способствует восстановлению нормального микробиоценоза и предотвращению рецидивов заболевания [40]. - Синбиотики представляют собой синергическую комбинацию про- и пребиотиков. Такой подход обеспечивает более эффективное и долгосрочное восстановление микробного сообщества, ведь синбиотики и поставляют полезные бактерии (пробиотик), и обеспечивают их идеальным питанием (пребиотик). Например, у женщин с синдромом поликистозных яичников прием синбиотика, содержащего лакто- и бифидобактерии с инулином, за 12 недель статистически значимо улучшил сразу несколько показателей: уровень глобулина, связывающего половые гормоны, и индекс свободных андрогенов. У пациенток также снизился гирсутизм (состояние, при котором у женщины появляется избыточный рост темных густых волос на лице, груди, животе и других «мужских» зонах, обычно из-за повышенного уровня мужских гормонов в организме), снизился инсулин и индекс инсулинорезистетности HOMA-IR, а также маркер воспаления (С-реактивный белок) [41].
Трансплантация вагинальной микробиоты
Подобно тому, как трансплантация фекальной микробиоты (ТФМ) произвела революцию в лечении некоторых кишечных инфекций, появился и новый метод — трансплантация вагинальной микробиоты (ТВМ). Эта процедура предполагает перенос вагинальной жидкости от здорового донора с высоким содержанием лактобацилл реципиенту, страдающему от дисбиоза, например, рецидивирующего бактериального вагиноза [42].
Как это работает? Существует два основных подхода:
- Прямой перенос подготовленной вагинальной жидкости.
- Выделение, культивирование и очистка микробиоты донора с ее последующим введением пациенту в форме капсул или суппозиториев.
Хотя ТВМ рассматривается как многообещающий метод лечения бактериального вагиноза, который плохо поддается стандартной антибиотикотерапии (рецидивы в 30–60% случаев), важно подчеркнуть, что эта технология все еще находится на стадии активных исследований. Как и при ТФМ, критически важным является тщательный скрининг доноров для исключения передачи инфекций [42].
Аутопробиотики
Иногда искать подходящего донора вариант непростой и небыстрый, поэтому возникла идея использования собственных пробиотических бактерий для создания индивидульного пробиотика — аутопробиотика.
В отличие от стандартных пробиотиков, содержащих промышленные штаммы, технология аутопробиотиков предполагает забор образца микрофлоры здорового человека, выделение из него индивидуальных штаммов лактобацилл, их культивирование в лабораторных условиях и последующее возвращение пациенту в виде капсул или суппозиториев. Такой метод особенно перспективен в акушерстве и гинекологии для лечения рецидивирующих заболеваний репродуктивной системы, связанных с нарушением влагалищной микробиоты. Поскольку микроорганизмы являются частью собственной микробиоты женщины, они легко приживаются во влагалище и эффективно восстанавливают защитную кислую среду, предотвращая развитие патогенов [43], [44]. Несмотря на перспективность персонализированного подхода, использование аутопробиотиков для лечения урогенитальных заболеваний пока остается экспериментальной технологией, не закрепленной в официальных клинических рекомендациях.
Заключение
Мы выяснили, что ось «кишечник—влагалище» представляет собой важную систему двусторонней связи, где дисбиоз в кишечнике способен провоцировать нарушения в микробиоте влагалища, влияя на него как напрямую (транслокация бактерий), так и опосредованно — через иммунитет, гормональный фон и общее состояние здоровья. Поддержание баланса микробиоты с помощью питания, пробиотиков, пребиотиков и новых методов терапии — важное направление в профилактике и лечении гинекологических и системных заболеваний, а изучение оси «кишечник—влагалище» открывает новые возможности для персонализированной медицины и комплексного подхода к женскому здоровью.
Литература
- Carabotti M., Scirocco A., Maselli M., Severi C. (2015). The gut-brain axis: interactions between enteric microbiota, central and enteric nervous systems. Ann Gastroenterol. 28, 203–209;
- Emmanuel Amabebe, Dilly O. C. Anumba. (2020). Female Gut and Genital Tract Microbiota-Induced Crosstalk and Differential Effects of Short-Chain Fatty Acids on Immune Sequelae. Front. Immunol.. 11;
- Hoda Elkafas, Melinique Walls, Ayman Al-Hendy, Nahed Ismail. (2022). Gut and genital tract microbiomes: Dysbiosis and link to gynecological disorders. Front. Cell. Infect. Microbiol.. 12;
- Попова Е. Н., Гордеев И. Г. (2019). Современные представления о микробиоте человека. Микробиота. 1, 5–19;
- Nabil Abdullah El Aila, Inge Tency, Geert Claeys, Hans Verstraelen, Bart Saerens, et. al.. (2009). Identification and genotyping of bacteria from paired vaginal and rectal samples from pregnant women indicates similarity between vaginal and rectal microflora. BMC Infect Dis. 9;
- Jeanne M. Marrazzo, Tina L. Fiedler, Sujatha Srinivasan, Katherine K. Thomas, Congzhou Liu, et. al.. (2012). Extravaginal Reservoirs of Vaginal Bacteria as Risk Factors for Incident Bacterial Vaginosis. The Journal of Infectious Diseases. 205, 1580-1588;
- Patricia Escorcia Mora, Diana Valbuena, Antonio Diez-Juan. (2025). The Role of the Gut Microbiota in Female Reproductive and Gynecological Health: Insights into Endometrial Signaling Pathways. Life. 15, 762;
- James M. Baker, Layla Al-Nakkash, Melissa M. Herbst-Kralovetz. (2017). Estrogen–gut microbiome axis: Physiological and clinical implications. Maturitas. 103, 45-53;
- Brandilyn A. Peters, Juan Lin, Qibin Qi, Mykhaylo Usyk, Carmen R. Isasi, et. al.. (2022). Menopause Is Associated with an Altered Gut Microbiome and Estrobolome, with Implications for Adverse Cardiometabolic Risk in the Hispanic Community Health Study/Study of Latinos. mSystems. 7;
- Giorgia Scarfò, Simona Daniele, Elisa Chelucci, Francesca Papini, Francesco Epifani, et. al.. (2024). Endometrial Dysbiosis: A Possible Association with Estrobolome Alteration. Biomolecules. 14, 1325;
- Jeongshin An, Hyungju Kwon, Woosung Lim, Byung-In Moon. (2022). Staphylococcus aureus-Derived Extracellular Vesicles Enhance the Efficacy of Endocrine Therapy in Breast Cancer Cells. JCM. 11, 2030;
- M. Leonor Fernández-Murga, Fernando Gil-Ortiz, Lucía Serrano-García, Antonio Llombart-Cussac. (2023). A New Paradigm in the Relationship between Gut Microbiota and Breast Cancer: β-glucuronidase Enzyme Identified as Potential Therapeutic Target. Pathogens. 12, 1086;
- Wenli Cao, Xiayan Fu, Jing Zhou, Qing Qi, Feijun Ye, et. al.. (2023). The effect of the female genital tract and gut microbiome on reproductive dysfunction. BST. 17, 458-474;
- Ailim Margarita Carías Domínguez, Dimas de Jesús Rosa Salazar, Juan Pablo Stefanolo, Maria Claudia Cruz Serrano, Isabel Cristina Casas, Julio Ricardo Zuluaga Peña. (2025). Intestinal Dysbiosis: Exploring Definition, Associated Symptoms, and Perspectives for a Comprehensive Understanding — a Scoping Review. Probiotics & Antimicro. Prot.. 17, 440-449;
- Efthalia Moustakli, Sofoklis Stavros, Periklis Katopodis, Anastasios Potiris, Peter Drakakis, et. al.. (2025). Gut Microbiome Dysbiosis and Its Impact on Reproductive Health: Mechanisms and Clinical Applications. Metabolites. 15, 390;
- D. Viganó, F. Zara, S. Pinto, E. Loddo, L. Casula, et. al.. (2020). How is small bowel permeability in endometriosis patients? a case control pilot study. Gynecological Endocrinology. 36, 1010-1014;
- Xiangguang Wu, Mingfu Wu, Huawen Li, Yang Yang, Huimin Shen, et. al.. (2025). Intraperitoneal translocation of gut microbiota induces NETosis and promotes endometriosis. Gut. gutjnl-2025-336185;
- Emma Slack, Maria Luisa Balmer, Jörg H. Fritz, Siegfried Hapfelmeier. (2012). Functional Flexibility of Intestinal IgA – Broadening the Fine Line. Front. Immun.. 3;
- Min Zhou, Lili Zhou, Junbo Liu, Shaohui Yu. (2025). IL-33 Participates in G. Vaginalis-Induced Bacterial Vaginosis: Involvement of Intravaginal IgA. JIR. Volume 18, 8005-8013;
- J A Robertson, M E Stemler, G W Stemke. (1984). Immunoglobulin A protease activity of Ureaplasma urealyticum. J Clin Microbiol. 19, 255-258;
- Suchitra K. Hourigan, Maria Gloria Dominguez-Bello. (2023). Microbial seeding in early life. Cell Host & Microbe. 31, 331-333;
- Phoebe LaPoint, Keona Banks, Mickayla Bacorn, Ruhika Prasad, Hector N. Romero-Soto, et. al.. (2025). Can Vaginal Seeding at Birth Improve Health Outcomes of Cesarean Section-Delivered Infants? A Scoping Review. Microorganisms. 13, 1236;
- Jing He, Lijuan Wang, Ying Ruan, Xinyan Yan, Qingju Liu, et. al.. (2024). Comparison of intestinal and pharyngeal microbiota in preterm infants on the first day of life and the characteristics of pharyngeal microbiota in infants delivered by cesarean section or vaginally. Front. Pediatr.. 12;
- Cheng Guo, Qian Zhou, Muxia Li, Letian Zhou, Lei Xu, et. al.. (2020). Breastfeeding restored the gut microbiota in caesarean section infants and lowered the infection risk in early life. BMC Pediatr. 20;
- Diana Montoya-Williams, Dominick J. Lemas, Lisa Spiryda, Keval Patel, O’neshia Olivia Carney, et. al.. (2018). The Neonatal Microbiome and Its Partial Role in Mediating the Association between Birth by Cesarean Section and Adverse Pediatric Outcomes. Neonatology. 114, 103-111;
- Debby Bogaert, Gina J. van Beveren, Emma M. de Koff, Paula Lusarreta Parga, Carlos E. Balcazar Lopez, et. al.. (2023). Mother-to-infant microbiota transmission and infant microbiota development across multiple body sites. Cell Host & Microbe. 31, 447-460.e6;
- Osagie A. Eribo, Nelita du Plessis, Novel N. Chegou. (2022). The Intestinal Commensal, Bacteroides fragilis, Modulates Host Responses to Viral Infection and Therapy: Lessons for Exploration during Mycobacterium tuberculosis Infection. Infect Immun. 90;
- Dollwin Matharu, Alise J. Ponsero, Evgenia Dikareva, Katri Korpela, Kaija-Leena Kolho, et. al.. (2022). Bacteroides abundance drives birth mode dependent infant gut microbiota developmental trajectories. Front. Microbiol.. 13;
- Isabelle Laforest-Lapointe, Marie-Claire Arrieta. (2017). Patterns of Early-Life Gut Microbial Colonization during Human Immune Development: An Ecological Perspective. Front. Immunol.. 8;
- Raz Abdulqadir, Jessica Engers, Rana Al-Sadi. (2023). Role of Bifidobacterium in Modulating the Intestinal Epithelial Tight Junction Barrier: Current Knowledge and Perspectives. Current Developments in Nutrition. 7, 102026;
- Hiroshi MAKINO. (2018). Bifidobacterial strains in the intestines of newborns originate from their mothers. Bioscience of Microbiota, Food and Health. 37, 79-85;
- Стражи микробиома;
- Shana M. Miles, Britney L. Hardy, D.Scott Merrell. (2017). Investigation of the microbiota of the reproductive tract in women undergoing a total hysterectomy and bilateral salpingo-oopherectomy. Fertility and Sterility. 107, 813-820.e1;
- Corrie Miller, Kira Morikawa, Paula Benny, Jonathan Riel, Marie K. Fialkowski, et. al.. (2024). Effects of Dietary Quality on Vaginal Microbiome Composition Throughout Pregnancy in a Multi-Ethnic Cohort. Nutrients. 16, 3405;
- Hongyu Jin, Zhaoyuan Niu, Xinyue Zhao. (2025). The association between dietary fiber intake and pelvic inflammatory disease in women: findings from the NHANES 2015–2018. BMC Women's Health. 25;
- Gregor Reid, Duane Charbonneau, Julie Erb, Barbara Kochanowski, Dee Beuerman, et. al.. (2003). Oral use ofLactobacillus rhamnosusGR-1 andL. fermentumRC-14 significantly alters vaginal flora: randomized, placebo-controlled trial in 64 healthy women. FEMS Immunology & Medical Microbiology. 35, 131-134;
- Beatriz Arce-López, Guadalupe X. Bazan, Susana Molina, Maria Carmen Crespo, María García-Beccaria, et. al.. (2025). Effect of fiber-modified kombucha tea on gut microbiota in healthy population: A randomized controlled trial (RCT). Current Research in Food Science. 11, 101130;
- Eileen Hilton, Henry D. Isenberg, Phyllis Alperstein, Kenneth France, Michael T. Borenstein. (1992). Ingestion of Yogurt Containing Lactobacillus acidophilus as Prophylaxis for Candidal Vaginitis. Ann Intern Med. 116, 353-357;
- Jacques Ravel, Sheri Simmons, Eleni Greenwood Jaswa, Sara Gottfried, Miriam Greene, et. al.. (2025). Impact of a multi-strain L. crispatus-based vaginal synbiotic on the vaginal microbiome: a randomized placebo-controlled trial. npj Biofilms Microbiomes. 11;
- Кротин П. Н., Кириленко О. В. (2019). Комбинация противогрибкового препарата и пребиотика в терапии острого кандидозного вульвовагинита. РМЖ. 2, 120–125;
- Khadijeh Nasri, Mehri Jamilian, Elham Rahmani, Fereshteh Bahmani, Maryam Tajabadi-Ebrahimi, Zatollah Asemi. (2018). The effects of synbiotic supplementation on hormonal status, biomarkers of inflammation and oxidative stress in subjects with polycystic ovary syndrome: a randomized, double-blind, placebo-controlled trial. BMC Endocr Disord. 18;
- Javad Nezhadi, Manouchehr Fadaee, Somayeh Ahmadi, Hossein Samadi Kafil. (2024). Microbiota transplantation. Heliyon. 10, e39047;
- Barinova V.V. Barinova, Bushtyreva I.O. Bushtyreva, Kuznetsova N.B. Kuznetsova, Suvorov A.N. Suvorov, Botasheva T.L. Botasheva, et. al.. (2023). Experience of using vaginal autoprobiotics in a patient with spontaneous triplet pregnancy with recurrent vaginal anaerobic dysbiosis. Akusherstvo i ginekologiia. 10_2023, 184-192;
- Блинов А. И., Глушанова Н. А., Бахаев В. В., Левченко В. Г. (2007). Принципы использования пробиотических лактобацилл в акушерстве и гинекологии. Acta Biomedica Scientifica. 3, 16–18.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚