Как раскрыть секреты цитохрома с
06 декабря 2015
Как раскрыть секреты цитохрома с
- 4871
- 0
- 6
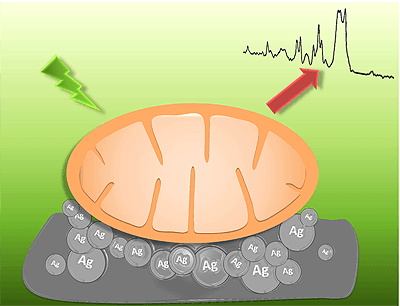
Помещение митохондрий на серебряную наноструктурированную поверхность позволяет регистрировать спектр гигантского комбинационного рассеяния цитохрома с.
Рисунок в полном размере.
-
Автор
-
Редактор
Статья на конкурс «био/мол/текст»: «Только ленивый не занимался митохондриями!» — сказал один профессор. И действительно, митохондрии — очень популярный объект исследования, ведь в них происходит множество сложнейших биохимических и биофизических процессов, обусловливающих широкий набор функций данных органелл. Но, несмотря на активность исследователей, многие механизмы этих процессов и свойства отдельных компонентов митохондрий остаются загадкой. Это связано в первую очередь с отсутствием подходящих неинвазивных методик. В ходе междисциплинарного проекта, проводимого группой биофизики клетки Биологического ф-та МГУ и лабораторией неорганического материаловедения химического ф-та МГУ совместно с коллегами из Германии и Дании, удалось создать методику на основе спектроскопии гигантского комбинационного рассеяния для селективного исследования цитохрома с непосредственно в живых митохондриях. Статья опубликована в журнале Scientific reports.
Конкурс «Био/Мол/Текст»-2015
 Эта работа заняла первое место в номинации «Своя работа» конкурса» конкурса «био/мол/текст»-2015.
Эта работа заняла первое место в номинации «Своя работа» конкурса» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
О, эти спектры! О, эти пики!
В тайны молекул можем мы заглянуть.
Так и работаем мы в этом ЛИКе ,
И не напрасно избрали свой путь!
Лаборатория искусственного климата (ЛИК) — прежнее название корпуса каф. Биофизики биофака МГУ.
Жалюзи опущены. Выключен свет. Мы погружены во мрак. Капля мутной жидкости падает на серебряную подложку. Вспышка зеленого света. 30 секунд. Спектр. Так начинается наш длинный день. А теперь обо всем по порядку.
Эти важные органеллы
Как вы уже (наверное) догадались, капля мутной жидкости — не что иное, как суспензия митохондрий. Митохондрии — это клеточные органеллы размером около 1 микрона. Основная функция митохондрий — это окисление питательных веществ и производство молекул АТФ — универсального источника энергии для большинства биологических процессов в клетках. Кроме того, митохондрии участвуют в инициации апоптоза, старении клеток, продукции активных форм кислорода (АФК) [1], метаболизме лекарств, выработке тепла, запасают в себе ионы кальция, синтезируют некоторые гормоны и т.д. [2]. Митохондрии обладают столь широким спектром функций, что нарушение их работы является причиной многих заболеваний: различных видов миопатий, сердечно-сосудистых заболеваний, диабета и многих других [3]. Большинство из них связаны с мутациями в генах, кодирующих белки митохондрий . Но может быть и наоборот: некоторые заболевания или неправильный образ жизни могут привести к нарушению работы митохондрий, например ожирение [4] или употребление наркотиков [5]. С другой стороны, митохондрии как преобразователи энергии и, фактически, белковый электропровод представляют большой интерес для физиков — биоников [6].
Органеллами митохондрии стали не сразу: согласно теории симбиогенеза, они появились в эукариотических клетках как бактерии-симбионты. И за миллиарды лет обросли множеством функций [7].
Т.к. митохондрии передаются по наследству от матери, то потомство получает все генетические нарушения, которые присутствовали в материнских митохондриях, но в перспективе эту проблему можно будет решить с помощью донорских митохондрий [8].
Митохондрии: как все устроено
Митохондрии состоят из двух мембран: внешней, проницаемой для ионов и некоторых белков, и внутренней, ограничивающей внутреннее пространство митохондрий — матрикс. Пространство между мембранами так и называется — межмембранное пространство (ММП). Внутренняя мембрана образует множество инвагинаций (так называемых крист). В матриксе митохондрий расположены ферменты цикла Кребса, а во внутренней мембране митохондрий находится четыре белковых комплекса дыхательной цепи (электрон-транспортной цепи, ЭТЦ) и АТФ-синтаза (рис. 1). Также в митохондриях есть подвижные элементы дыхательной цепи: убихинон во внутренней мембране и цитохром с в ММП. Принцип работы дыхательной цепи — окисление субстратов, поступающих из цикла Кребса, и перенос электронов от этих субстратов по кофакторам ЭТЦ на конечный акцептор — кислород. Есть определенная закономерность в последовательности переноса электрона: электроны поступают от донора с более отрицательным редокс-потенциалом (Еred/ox) к акцептору с более положительным Еred/ox. Таким образом, электрон как будто движется вниз по течению (рис. 2). Во время переноса электронов некоторые комплексы дыхательной цепи закачивают протоны из матрикса в ММП, тем самым создавая электрохимический потенциал на внутренней мембране митохондрий, который используется для синтеза АТФ (рис. 1) [2].
Окислительно-восстановительный потенциал — синоним редокс-потенциала (от англ. reduction — восстановление, oxidation — окисление).
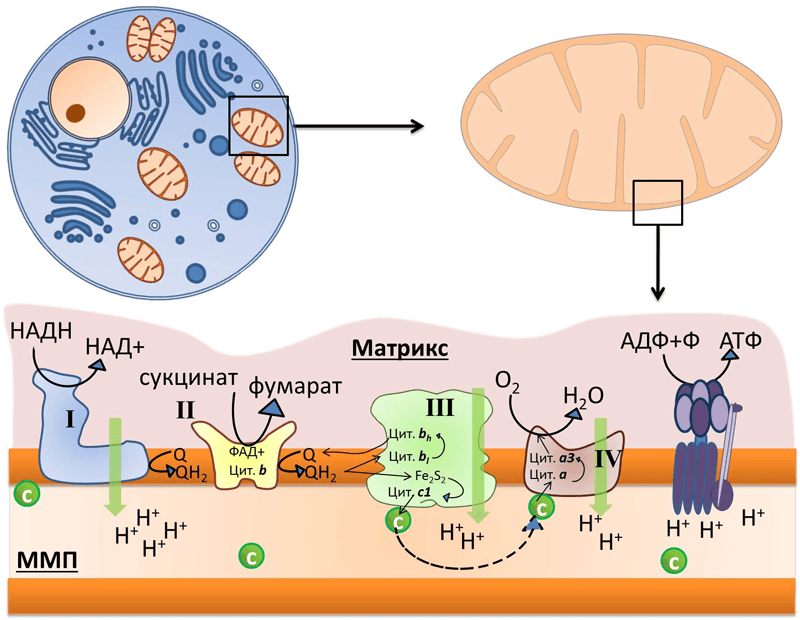
Рисунок 1. Во внутренней мембране митохондрий локализованы комплексы дыхательной цепи:
I — НАДН-дегидрогеназа, II — сукцинат-дегидрогеназа, III — цитохром b–c1-комплекс, или цитохром с-редуктаза, IV — цитохром а–а3, или цитохромоксидаза, и фермент АТФ-синтаза. Q — убихинон, «с» в зеленом кружке — цитохром с. Черными стрелками показан транспорт электрона, пунктирной стрелкой — диффузия цитохрома с от комплекса III к IV, зелеными стрелками — перенос протона.
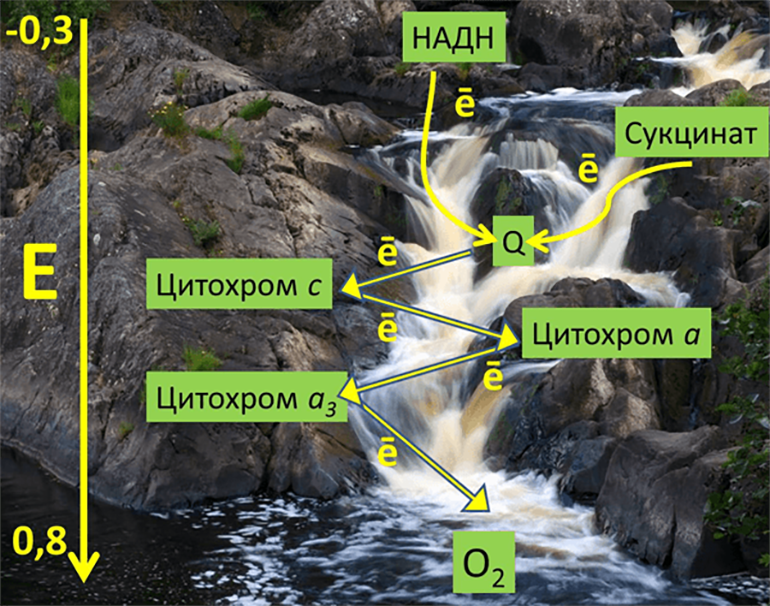
Рисунок 2. Метафорическое изображение среднеточечных редокс-потенциалов различных переносчиков ЭТЦ митохондрий в энергетической шкале (вольт) на фоне реки Тохмайоки в Карелии.
Несмотря на то, что с митохондриями работали корифеи науки, такие как Кребс, Митчелл, Ленинджер, Чанс, Скулачёв и многие другие, благодаря которым мы столько знаем об этих органеллах, все же многие митохондриальные процессы и свойства переносчиков электронов до сих пор не изучены. Это связано в первую очередь с отсутствием подходящих неинвазивных методик. В этом году нашей лабораторией в сотрудничестве с коллегами из других факультетов МГУ, а также из Дании и Германии, удалось создать методику для селективного исследования конформации гема цитохрома с непосредственно в живых митохондриях [9].
Что такое конформация гема и почему она важна?
Если приглядеться к комплексам дыхательной цепи (рис. 1), то в трех из них можно увидеть цитохромы — гем-содержащие белки, которые являются кофакторами, участвующими в переносе электронов. А еще один цитохром диффундирует в ММП. Всего в митохондриях имеется три типа цитохромов: а, b и с. Они очень похожи и отличаются только боковыми радикалами (рис. 3).
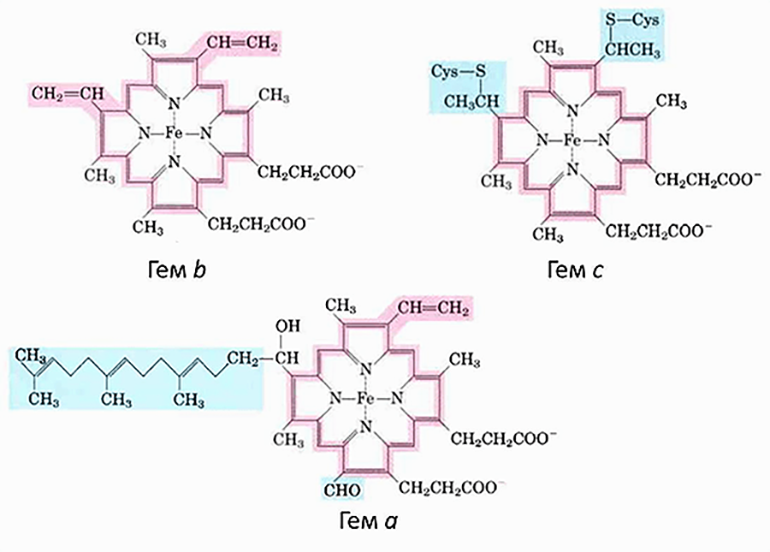
Рисунок 3. Гемы цитохромов разных типов. Каждый гем состоит из четырех пятичленных азотосодержащих циклов, связанных между собой. Это т.н. порфирины. Атомы азота координируют атом железа (Fe). Гемы отличаются боковыми группами, и только гем типа с связан с белком ковалентно.
Во время переноса электрона меняется редокс-состояние гемового железа цитохромов Fe3+/Fe2+, что приводит к изменению конформации всего гема. Эти два параметра (Еred/ox и конформация) всегда связаны друг с другом. Кроме того, изменение в белковом окружении тоже приводит к изменению конформации гема [10], [11]. А так как Еred/ox определяет эффективность переноса электрона, то конформация гема — вещь важная. К тому же, чтобы произошел перенос электрона с одного цитохрома на другой, нужно, чтобы гемы этих цитохромов находились на определенном расстоянии друг от друга и были правильно ориентированы (рис. 4). Поэтому любые изменения в цитохромах могут отражаться на эффективности переноса электрона, т.е. на работе всей дыхательной цепи и, как следствие, энергообеспечении клеток [12], [13].
Наиболее интересен в этом отношении цитохром с, так как это единственный мобильный переносчик электронов, курсирующий в ММП (все остальные цитохромы заякорены в комплексах ЭТЦ), поэтому он наиболее подвержен изменениям, которые могут происходить в митохондриях. Помимо этого выход цитохрома с запускает каскад реакций, ведущих к апоптозу, и в этом процессе тоже важен его редокс-потенциал [14].
Возникает вопрос, как понять, в какой конформации и в каком редокс-состоянии находится гем цитохрома с в митохондриях?
Как увидеть конформацию гема и оценить Еred/ox?
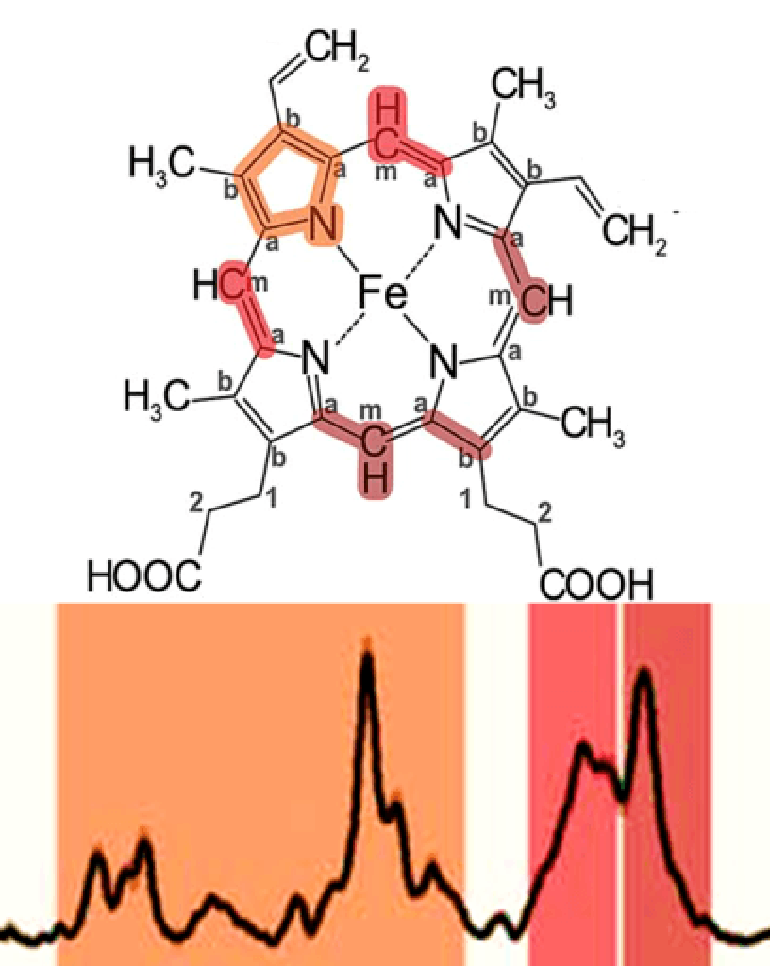
Рисунок 5. Сверху показан гем типа b, который содержится в эритроцитах, снизу — спектр КР эритроцита. Различные группы атомов и соответствующие им пики обозначены одним цветом.
Численно можно определить Еred/ox с помощью электрохимических методов. Однако для этого нужные комплексы дыхательной цепи изолируют и помещают в совершенно иные условия среды, что может само по себе изменить их свойства. Благодаря таким мощным методам как ЯМР и рентгеноструктурный анализ, мы знаем, в какой конформации находятся белки и кофакторы дыхательной цепи в окисленной и восстановленной форме. Но нас интересует их состояние в максимально естественных условиях, а также соотношение этих состояний при работе дыхательной цепи. Есть несколько неинвазивных методов для определения окислительно-восстановительного состояния цитохромов. Например, абсорбционная спектроскопия. Спектр поглощения митохондрий — это суммарный спектр всех имеющихся цитохромов в митохондриях, а также ФАД. Но из-за того, что все типы цитохромов очень похожи и, соответственно, обладают схожими спектрами поглощения, а их окислительно-восстановительное состояние все время меняется при нормальной работе дыхательной цепи, становится сложно оценить вклад различных цитохромов в спектр [15].
По спектрам флуоресценции НАДН и ФАД+ можно примерно оценить редокс-состояние только комплексов I и II. А по потенциалу на внутренней мембране митохондрий можно судить только о работе митохондрии в целом [16].
Напрямую получение информации о конформации и редокс-состоянии цитохрома с в интактной (целой и функционирующей) митохондрии — это крайне сложная задача, ведь его конформация постоянно меняется при работе ЭТЦ, он диффундирует и взаимодействует с мембранными комплексами. Наличие метода, который бы позволял это сделать, значительно расширило бы наши знания о влиянии цитохрома с на активность дыхательной цепи и его вкладе в развитие митохондриальных патологий.
К митохондриям от чистого сердца
Несколько лет назад в работах нашей группы вопрос о неинвазивном методе исследования цитохромов митохондрий в клетках уже поднимался. На тот момент сотрудники лаборатории исследовали влияние окислительного стресса на кардиомиоциты (клетки сердечной мышцы), методом комбинационного рассеяния света (КР, Raman spectroscopy) [17]. Подробно об этом рассказывается в статье «Спектроскопия КР: новые возможности старого метода» [18].
Спектр комбинационного рассеяния молекулы представляет собой колебательный спектр, пики которого характеризуют нормальные частоты колебаний молекулы. Отдельные группы атомов вносят свой вклад в различные колебания молекулы, поэтому можно сказать, что каждый пик на спектре КР характеризует колебания определенной группы атомов (рис. 5) [19], [20]. Таким образом, спектр КР — нечто вроде «отпечатков пальцев» молекулы. И так же, как по отпечаткам пальцев можно отличить родных братьев, по спектрам КР можно отличить схожие по строению молекулы. Кроме того, спектры КР чувствительны к изменениям конформации молекул, ведь если конформация меняется, то меняются и нормальные частоты колебаний.
В ходе работы с кардиомиоцитами было показано, что спектры КР разных типов цитохромов и миоглобина (который, как и гемоглобин, содержит гем типа b) можно различать по спектрам КР интактных клеток и даже определять их окислительно-восстановительное состояние. Позже Н.А. Браже с другими сотрудниками успешно провели подобное исследование на целом сердце, т.е. in situ (рис. 6) [21].
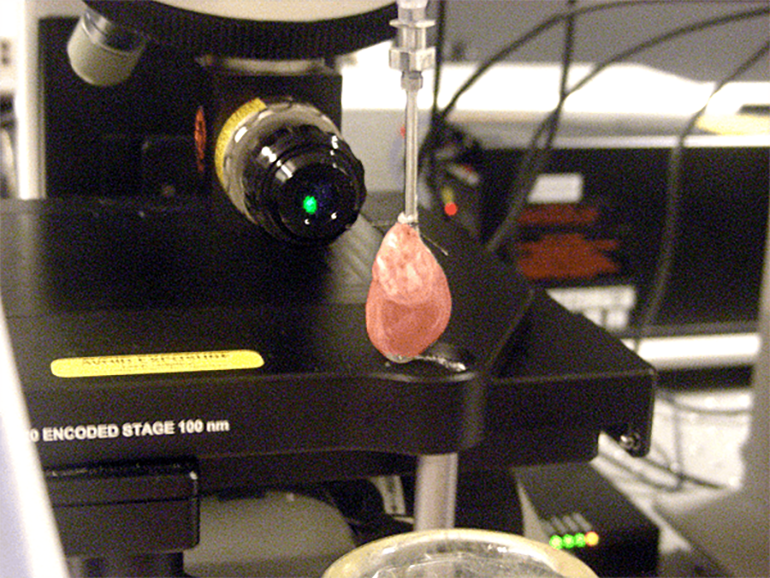
Рисунок 6. Регистрация спектра КР целого сердца.
Однако у цитохромов есть одна особенность — спектр КР интенсивен только для восстановленных их форм, тогда как спектр окисленных состояний обладает очень низкой интенсивностью. Поэтому основным критерием определения восстановленности цитохромов является интенсивность сигнала. Но если мы ориентируемся только на интенсивность, то можем потерять важную информацию об изменениях в исследуемой системе! Ведь интенсивность зависит и от количества молекул, и от выраженности тех или иных колебаний, и от других параметров. К тому же, для определения точного положения пиков большинство исследователей, имеющих дело с цитохромами, вынуждены искусственно восстанавливать образцы, что заведомо нарушает их нативность.
Отчасти проблему решили японские ученые. Они определили, какие пики на спектре КР характерны только для восстановленных, а какие — только для окисленных цитохромов [22]. Однако проблема интенсивности спектров по-прежнему сохранялась. Нужно было ее решать!
Усиливая сигнал
Один из способов усилить сигнал КР — это поместить исследуемую молекулу вблизи наночастицы благородного металла, например, золота или серебра. Эти металлы обладают свободными поверхностными электронами, а квант коллективных колебаний таких электронов называется плазмон. Если частота падающего света входит в резонанс с частотой колебаний поверхностных электронов металла, то возникает эффект плазмонного резонанса, который приводит к многократному усилению электромагнитного излучения вблизи наночастицы. Этот эффект используют в методе поверхностного плазмонного резонанса (surface plasmon resonance, SPR), в абсорбционной и флуоресцентной спектроскопии [23]. Но нас интересует способ усилить именно сигнал КР. И для этого существует спектроскопия гигантского комбинационного рассеяния (ГКР, англ. Surface enhanced Raman spectroscopy, SERS) .
Подробности КР- и ГКР-спектроскопии даны в предшествующей статье: «Спектроскопия КР: новые возможности старого метода» [18].
Спектры КР и ГКР цитохрома с хорошо известны [24], [25]. И что самое замечательное, в отличие от спектров КР, спектры ГКР окисленного и восстановленного цитохрома с практически не отличаются по интенсивности. Так почему бы не зарегистрировать спектр ГКР митохондрий?
Идея пришла от О.В. Сосновцевой, профессора Копенгагенского университета, с которой наша лаборатория сотрудничает не первый год. Она даже предложила «подсобить» с митохондриями, так как с ними работали в соседней лаборатории, и они готовы были поделиться.
На тот момент было только две работы по изучению митохондрий методом ГКР и его разновидностью TERS (когда плазмонная частица находится на острие иглы кантилевера атомно-силового микроскопа, и сигнал ГКР регистрируют при сканировании поверхности образца). В первой работе [26] исследователи регистрировали спектр ГКР только от белков и липидов митохондрий, но не от цитохромов. А во второй работе [27] использовали не нативные, а высушенные митохондрии. Но как применить метод ГКР для изучения цитохромов живых митохондрий? Прежде чем ответить на этот вопрос, следует слегка переместиться в прошлое...
Междисциплинарность — залог успеха
В 2010 году, когда интерес к нанотехнологиям был на высоте, академик Юрий Дмитриевич Третьяков, в то время декан факультета наук о материалах (ФНМ) МГУ, решил начать межфакультетское сотрудничество с биологами для проведения совместных исследований методом ГКР. В итоге сотрудничество было установлено с лабораторией биофизики клетки под руководством Г.В. Максимова. Так наша лаборатория познакомилась с заместителем декана ФНМ химиком-материаловедом член-корр. Е.А. Гудилиным. Совместно с группой Гудилина начались активные исследования по применению ГКР в биологии.
Дело в том, что ГКР — метод непростой и требует исключительно междисциплинарного подхода. Каждый биообъект уникален, и чтобы регистрировать от него сигнал ГКР, нужно разрабатывать уникальные наноструктуры, которые бы усиливали сигнал от нужного объекта, не повреждали его и выдерживали «атаку» физиологических многокомпонентных буферов.
Большинство работ, связанных с ГКР, предполагают адсорбцию молекул на поверхности наноструктур, пусть даже введенных внутрь клетки [28]. Это связано с тем, что усиление сигнала КР наблюдается только на очень небольшом расстоянии от поверхности металла [29]. Однако такой подход не всегда удовлетворяет запросам биологов. В идеале усиление сигнала должно распространяться на достаточно большое расстояние, чтобы можно было работать с целыми клетками и органеллами, при этом не повреждая их, и желательно не вводить ничего внутрь. Для этой цели нужно разрабатывать специфический дизайн наноструктур и придумывать методы их синтеза, чем и занималась группа под руководством Гудилина.
Наконец, длительные и упорные попытки разработать такие структуры для исследования живых клеток увенчались успехом. В 2012-м году дебютировали наноструктурированные подложки для усиления сигнала от примембранного гемоглобина в интактных эритроцитах [20]. За счет определенной морфологии наноструктур удалось получить усиление сигнала на расстоянии более 10 нм, т.е. больше толщины мембраны эритроцита.
Раз это удалось сделать для эритроцитов, то можно сделать и для митохондрий!
Долгожданный спектр ГКР митохондрий
Жалюзи опущены. Выключен свет. Комната погружена во мрак. Капля суспензии падает на серебряную подложку. Вспышка зеленого света. 30 секунд. Спектр. Тот самый долгожданный спектр ГКР от изолированных сердечных митохондрий был получен! Оставалось только понять, от каких именно структур в митохондриях исходит сигнал.
С учетом размеров компонентов митохондрий (рис. 7) и того, что усиление наблюдается на расстоянии нескольких нанометров от наноструктур, можно было предположить, что спектр ГКР митохондрий будет преимущественно спектром цитохрома с, так как этот цитохром наиболее близко подходит ко внешней мембране митохондрий и, соответственно, к наноструктурам. В то же время остальные цитохромы закреплены в комплексах внутренней мембраны.
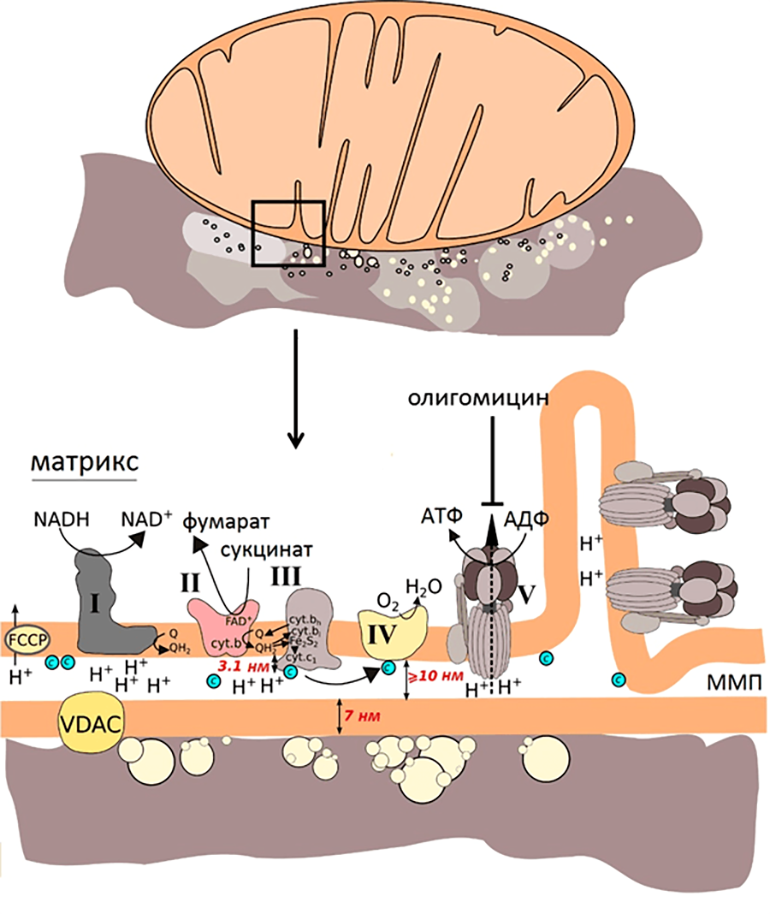
Рисунок 7. Схема эксперимента: изолированные сердечные митохондрии помещают на серебряную наноструктурированную поверхность и облучают зеленым лазером. На рисунке показаны размеры мембраны, межмембранного пространства (ММП) и участков комплексов ЭТЦ. VDAC — потенциал зависимый анионный канал, FCCP — протонофор, разобщающий электронный транспорт и синтез АТФ, олигомицин — ингибитор АТФ-синтазы, в синем кружке — цитохром с.
Это утверждение также подтверждалось при моделировании эффектов усиления КР серебряными наноструктурами, которые были использованы в работе. Группа наших коллег из лазерного центра Ганновера показала, что сложная морфология подложки со множеством углублений, в которые могут попадать митохондрии, позволило получать усиление на большом расстоянии (более 10 нм). А иерархическое устройство самих наноструктур увеличивало число мест контакта с мембраной митохондрий и, следовательно, число молекул цитохрома с, от которых можно было зарегистрировать сигнал ГКР. Если использовать те же наночастицы серебра, просто присоединенные к плоской подложке, то особого усиления не произойдет, что и подтверждалось в эксперименте (рис. 8).
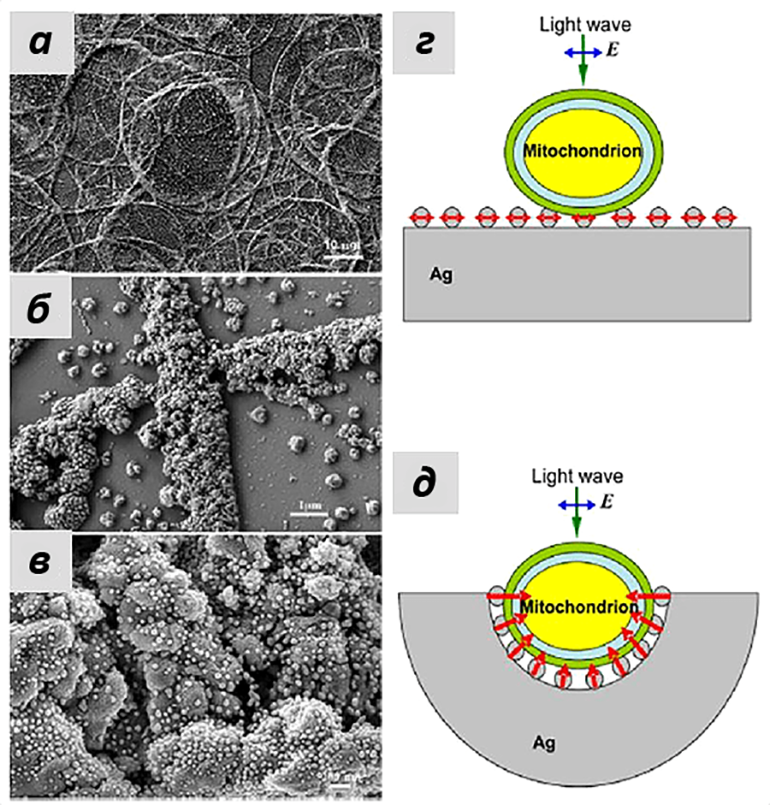
Рисунок 8. а—в — Изображения наноструктур, полученные на сканирующем электронном микроскопе. а — масштаб 10 мкм; б — 1 мкм, в — 0,2 мкм. На изображениях хорошо видна иерархическая морфология серебряных наноструктур. г—д — две модели, которые использовались для математического моделирования эффекта усиления электрического поля наноструктурами. г — в случае, когда митохондрии помещают на плоскую поверхность с наночастицами серебра, не происходит значительного усиления сигнала. д — при использовании структур, образующих полости, покрытые наночастицами серебра, число мест контакта между митохондрией и наночастицами увеличивается, а усиление электрического поля направлено перпендикулярно поверхности, т.е. внутрь митохондрии. За счет этого достигается многократное усиление сигнала ГКР цитохрома с.
[9], с изменениями
И действительно, полученный спектр ГКР митохондрий соответствовал спектрам цитохрома с! При использовании зеленого лазера в качестве возбуждающего света можно регистрировать сигнал только от цитохромов b и с, но не от цитохрома а, что облегчает задачу расшифровки спектров. Несмотря на схожесть структуры цитохромов типа b и с, они имеют ключевые пики на спектре, благодаря которым их нельзя перепутать. Таким образом, используемые наноструктуры давали усиление на достаточно большом расстоянии, чтобы зарегистрировать спектры от цитохрома с, но недостаточно большом, для того чтобы увидеть пики цитохромов b. И это как раз то, что нужно! Благодаря методу ГКР теперь можно исследовать селективно редокс-состояние и конформацию именно цитохрома с в живых функционирующих митохондриях.
Как и ожидалось, спектры ГКР цитохрома с митохондрий оказались очень чувствительны к изменению его окислительно-восстановительного состояния. Для этого было исследовано два воздействия: внесение протонофора FCCP и ингибитора АТФ-синтазы олигомицина.
FCCP встраивается во внутреннюю мембрану митохондрий и начинает переносить протоны из ММП в матрикс, минуя протонные каналы АТФ-синтазы. В результате этого исчезает электрохимический потенциал и прекращается синтез АТФ. Это явление называют разобщением дыхания и фосфорилирования. В результате разобщения количество АТФ снижается, а АДФ увеличивается [30]. В этом случае возрастает количество поглощенного кислорода и скорость окисления субстратов, а, следовательно, и количество окисленных молекул цитохрома с, что очень хорошо видно на спектрах ГКР. И наоборот, добавление ингибитора синтеза АТФ — олигомицина, который приводит к увеличению электрохимического градиента на фоне снижения скорости дыхания, увеличивает количество восстановленных молекул цитохрома с, что также выражено на спектрах ГКР митохондрий.
Таким образом, спектры ГКР митохондрий, являясь спектрами исключительно цитохрома с, оказались чувствительны к изменениям его конформации и редокс-состояния в процессе работы митохондрий.
Видео 1. Схема всей работы в одном ролике.
Итоги
Спектроскопия гигантского комбинационного рассеяния позволяет многократно усилить сигнал КР от молекул вблизи наночастиц металла. Однако для проведения успешных экспериментов необходимо учитывать свойства как биологического объекта, так и наноструктур. «Ключевым моментом нашего достижения стал междисциплинарный подход к работе, в которую были вовлечены биологи, химики и физики», — поясняет одна из главных авторов проекта к.б.н. Надежда Браже, ставшая осенью 2015 года лауреатом премии L’Oreal Unesco для женщин в науке. — «Результатом такого подхода стало создание уникальной методики селективного определения редокс-состояния и конформации цитохрома с в живых функционирующих митохондриях, помещенных на специальную наноструктурированную поверхность. Разработанная методика поможет восполнить пробелы наших знаний о свойствах и поведении переносчиков электрона в митохондриях, а также может быть использована для разработки диагностических тестов для раннего выявления патологий митохондрий, чем и планируется заниматься в ближайшее время».
Литература
- Активный кислород: друг или враг, или О пользе и вреде антиоксидантов;
- Nelson D.L., Cox M.M. Lehninger Principles of Biochemistry (5th Edition). NY: W.H. Freemanand Company, 2008;
- Scott B. Vafai, Vamsi K. Mootha. (2012). Mitochondrial disorders as windows into an ancient organelle. Nature. 491, 374-383;
- В ооцитах мышей с ожирением нарушается работа митохондрий;
- Пробило на хавчик;
- Moore L., Gust D., Moore T.A. (2007). Bio-inspired constructs for sustainable energy production and use. L’Actualité Chim. 308–309, 50–56;
- Как появились митохондрии (рассказ, похожий на сказку);
- Трое в лодке: о легализации замены митохондрий;
- Nadezda A. Brazhe, Andrey B. Evlyukhin, Eugene A. Goodilin, Anna A. Semenova, Sergey M. Novikov, et. al.. (2015). Probing cytochrome c in living mitochondria with surface-enhanced Raman spectroscopy. Sci Rep. 5;
- Gianantonio Battistuzzi, Marco Borsari, James A. Cowan, Antonio Ranieri, Marco Sola. (2002). Control of Cytochrome c Redox Potential: Axial Ligation and Protein Environment Effects. J. Am. Chem. Soc.. 124, 5315-5324;
- 10.1016/0300-9084(94)90171-6Dolla A., Blanchard L., Guerlesquin F., Bruschi M. (1994). The protein moiety modulates the redox potential in cytochromes c. Biochimie. 76, 471–479;
- Sozanne R.N. Solmaz, Carola Hunte. (2008). Structure of Complex III with Bound Cytochrome c in Reduced State and Definition of a Minimal Core Interface for Electron Transfer. Journal of Biological Chemistry. 283, 17542-17549;
- Jian-Guo Ma, Jun Zhang, Ricardo Franco, Song-Ling Jia, Isabel Moura, et. al.. (1998). The Structural Origin of Nonplanar Heme Distortions in Tetraheme Ferricytochromes c3. Biochemistry. 37, 12431-12442;
- Guy C. Brown, Vilmante Borutaite. (2008). Regulation of apoptosis by the redox state of cytochrome c. Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1777, 877-881;
- David J. Chess, Eric Billings, Raúl Covian, Brian Glancy, Stephanie French, et. al.. (2013). Optical spectroscopy in turbid media using an integrating sphere: Mitochondrial chromophore analysis during metabolic transitions. Analytical Biochemistry. 439, 161-172;
- Anatoly A. Starkov, Gary Fiskum. (2003). Regulation of brain mitochondrial H2O2 production by membrane potential and NAD(P)H redox state. Journal of Neurochemistry. 86, 1101-1107;
- Nadezda A. Brazhe, Marek Treiman, Alexey R. Brazhe, Ninett L. Find, Georgy V. Maksimov, Olga V. Sosnovtseva. (2012). Mapping of Redox State of Mitochondrial Cytochromes in Live Cardiomyocytes Using Raman Microspectroscopy. PLoS ONE. 7, e41990;
- Спектроскопия КР: новые возможности старого метода;
- Горелик В. (1997). Комбинационное рассеяние света. Соросовский образовательный журнал. 6, 91–96;
- Semenova А.А., Goodilin E.А., Brazhe N.А., Ivanov V.K., Baranchikov A.E., Lebedev V.A. et al. (2012). Planar SERS nanostructures with stochastic silver ring morphology for biosensor chips. J. Mater. Chem. 22, 24530;
- Nadezda A. Brazhe, Marek Treiman, Barbara Faricelli, Jakob H. Vestergaard, Olga Sosnovtseva. (2013). In Situ Raman Study of Redox State Changes of Mitochondrial Cytochromes in a Perfused Rat Heart. PLoS ONE. 8, e70488;
- Kakita M., Kaliaperumal V., Hamaguchi H. (2012). Resonance Raman quantification of the redox state of cytochromes b and c in-vivo and in-vitro. J. Biophotonics. 5, 20–24;10.1002/jbio.201100087;
- Миграция энергии плазмонного резонанса: вторая жизнь оптической спектроскопии;
- Hu S., Morris I.K., Singh J.P., Smith K.M., Spiro T.G. (1993). Complete assignment of cytochrome c resonance Raman spectra via enzymic reconstitution with isotopically labeled hemes. J. Am. Chem. Soc. 115, 12446–12458;
- Ines Delfino, Anna Rita Bizzarri, Salvatore Cannistraro. (2005). Single-molecule detection of yeast cytochrome c by Surface-Enhanced Raman Spectroscopy. Biophysical Chemistry. 113, 41-51;
- Ömer Faruk Karataş, Erdinç Sezgin, Ömer Aydın, Mustafa Çulha. (2009). Interaction of gold nanoparticles with mitochondria. Colloids and Surfaces B: Biointerfaces. 71, 315-318;
- Elina A. Vitol, Zulfiya Orynbayeva, Michael J. Bouchard, Jane Azizkhan-Clifford, Gary Friedman, Yury Gogotsi. (2009). In Situ Intracellular Spectroscopy with Surface Enhanced Raman Spectroscopy (SERS)-Enabled Nanopipettes. ACS Nano. 3, 3529-3536;
- Janina Kneipp, Harald Kneipp, Burghardt Wittig, Katrin Kneipp. (2010). Novel optical nanosensors for probing and imaging live cells. Nanomedicine: Nanotechnology, Biology and Medicine. 6, 214-226;
- M. Moskovits. (1978). Surface roughness and the enhanced intensity of Raman scattering by molecules adsorbed on metals. The Journal of Chemical Physics. 69, 4159-4161;
- Северин С. Е. Биохимия. Москва: ГЭОТАР-МЕД, 2003. — 779 с..
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚