Какие молекулы полезны в диагностике болезни Крона?
18 марта 2026
Какие молекулы полезны в диагностике болезни Крона?
- 163
- 0
- 1
Кишечник — орган, который чаще всего поражается болезнью Крона.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Болезнь Крона необходимо начать лечить как можно раньше, чтобы предотвратить возникновение серьезных осложнений. Лечение подбирается индивидуально и зависит от многих факторов. Чтобы посмотреть на состояние кишечника, врачи используют эндоскопию — смотрят на кишечник изнутри. Но могут ли анализы крови и кала что-либо сказать о возможном наличии болезни Крона, рисках осложнений и состоянии слизистой кишечника?
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Что такое болезнь Крона и почему ее стоит изучать?
Болезнь Крона (БК) — это хроническое воспалительное заболевание желудочно-кишечного тракта, причины которого до сих пор не ясны. Известно, что оно возникает при взаимодействии генетических, иммунологических, микробиологических и экологических факторов [1]. Это заболевание характеризуется воспалением, которое затрагивает всю толщину стенки кишечника. Течение болезни не всегда можно предсказать — она то обостряется, то стихает. При болезни Крона в воспалительный процесс могут вовлекаться любые отделы желудочно-кишечного тракта (ЖКТ), но чаще всего поражаются тонкая и/или толстая кишка, в большинстве случаев — отдел, где две эти кишки соединяются. Частота встречаемости БК в последние годы растет. Болезнь Крона значительно влияет на качество жизни пациентов, проявляясь такими симптомами, как слабость, боль в животе и диарея. Нередко при этом заболевании встречаются кишечные осложнения, такие как стриктуры (патологические сужения просвета кишки), свищи (патологические каналы), абсцессы (полости с гноем), а также внекишечные осложнения — поражения суставов, кожи, глаз и так далее [2].
Механизм развития болезни Крона
Факторами, предрасполагающими к развитию БК являются генетические особенности, изменение состава микробиоты кишечника, дефекты врожденного и приобретенного иммунитета и различные факторы окружающей среды.
Наибольшую роль в развитии БК играют такие гены, как NOD2, ATG16L1, LRRK2, IRGM, IL23R, HLA, STAT3, JAK2, участвующие в работе Th17-лимфоцитов (T-хелперов 17 типа, которые играют ключевую роль в иммунной защите от внеклеточных бактерий и грибковых инфекций), MUC2, который кодирует муцин (один из основных компонентов слизи) и ряд других генов. Также наличие некоторых вариаций гена HLA (кодирует белки, которые участвуют в распознавании антигенов), таких как HLA-A2, HLA-DR1 и HLA-DQw5, может указывать на вероятность развития внекишечных осложнений.
Генетическая детерминированность ассоциирована с нарушением врожденного иммунитета, изменением реакции на микроорганизмы — гиперактивацией сигнальных провоспалительных путей, нарушением аутофагии (например, нарушением ее инициации из-за дефекта в гене, кодирующем белок NOD2 — один из рецепторов иммунокомпетентных клеток), нарушением функции эпителиального барьера (снижение количества и целостности плотных контактов между эпителиальными клетками, увеличение апоптоза эпителиальных клеток и т.д.). Определяющим фактором в развитии БК является нарушение распознавания частей бактериальных клеток иммунными клетками человека.
Пусковыми факторами могут выступить курение, нервный стресс, недостаточное употребление клетчатки и чрезмерное употребление животного белка в пищу, дефицит витамина D и кишечные инфекции.
В результате активации Т-лимфоцитов, таких как Т-хелперы 1, 2, 17 типов и Т-регуляторные лимфоциты, происходит гиперэкспрессия фактора некроза опухоли альфа, интерлейкинов 1, 12, 23, 17 типов и других провоспалительных цитокинов. В результате каскада реакций возникает воспаление, которое затрагивает всю толщину стенки кишечника, и образуются гранулемы — компактные скопления иммунных клеток [2–4] (рис. 1).
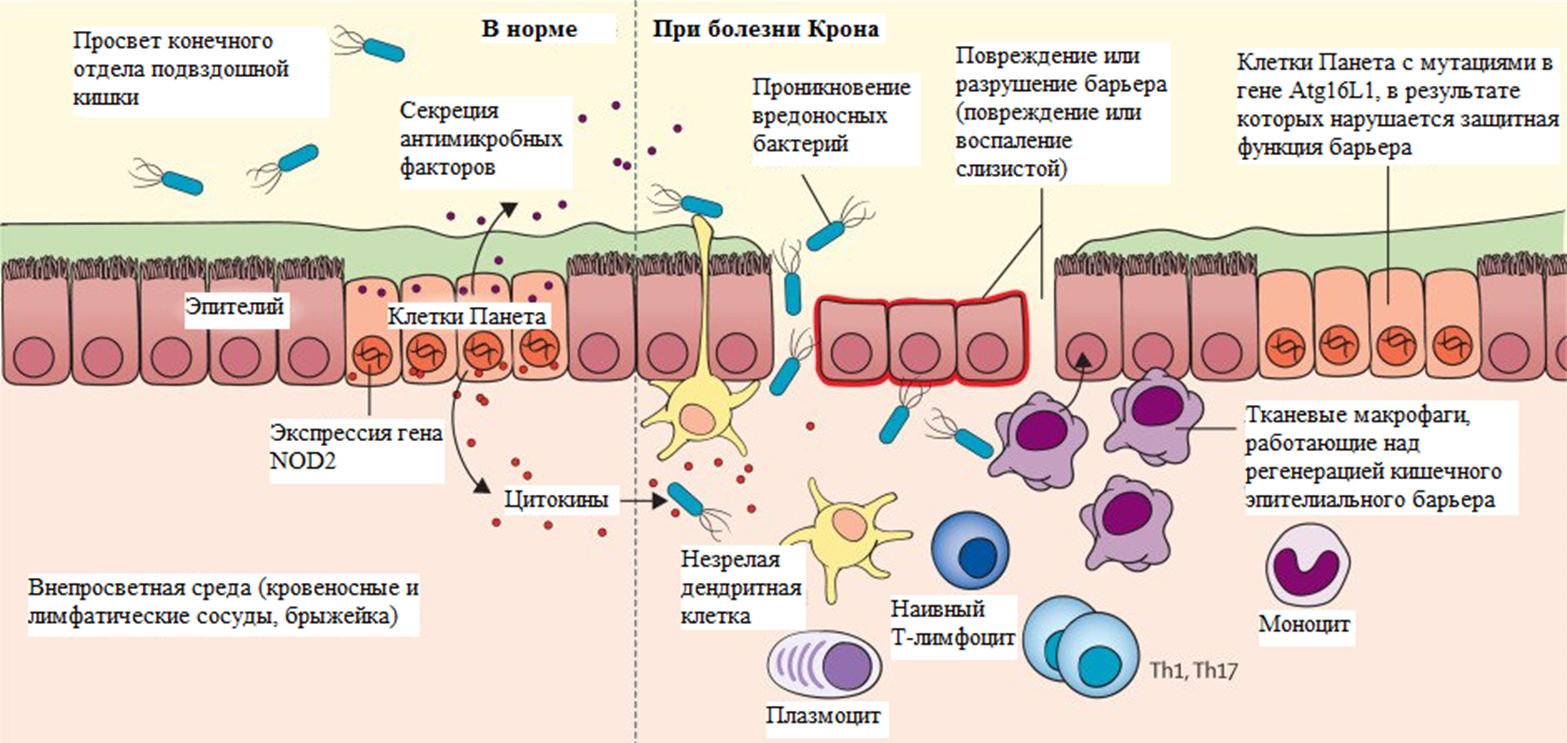
Рисунок 1. Кишечный эпителиальный барьер в норме и при болезни Крона. Клетки Панета, являющиеся местом концентрации белка NOD2 в конечном отделе подвздошной кишки, играют центральную роль в контроле над прохождением бактерий через барьер — они секретируют антимикробные факторы. Клетки Панета используют аутофагию для регулирования способности к секреции и объема секреции. Нарушение этого сигнального пути вследствие мутаций в таких генах, как Atg16L1, приводит к нарушению функции клеток Панета, дисрегуляции микробиоты и снижению целостности барьера. Тканевые макрофаги важны для регенерации клеток кишечного эпителия и для поддержания постоянства внутренней среды в кишечнике.
Антитела — белки, созданные для поддержания порядка
Так как БК и язвенный колит во многом похожи, бывают случаи, когда сложно различить эти заболевания. В таких случаях может помочь определение в крови пациента ASCA и ANCA — антител классов иммуноглобулины А (IgA) и/или иммуноглобулины G (IgG). ASCA — это антитела к пивным и пекарским дрожжам Saccharomyces cerevisiae. ASCA перекрестно распознают дрожжевые грибки Candida albicans — распространенных представителей кишечной микробиоты. При БК они встречаются в 39–70% случаев, тогда как при язвенном колите — в 10–15% случаев, у родственников больных воспалительными заболеваниями кишечника (ВЗК) — в 20–25%, а у здоровых лиц — в 1–2%. Такое соотношение объясняется различиями в характере воспаления кишечной стенки при этих двух заболеваниях. У больных БК воспаление проходит через всю стенку кишки, что позволяет проникать через стенку большому количеству антигенов. При язвенном колите воспаление ограничено слизистой оболочкой толстой кишки, и это препятствует проникновению грибков и возникновению на них иммунного ответа. Помимо этого, возникновение ASCA связано с наследственной предрасположенностью, и это объясняет более частое выявление ASCA у здоровых родственников пациентов с ВЗК. Кроме того, больные ВЗК и их родственники зачастую подвергаются общим экологическим факторам, которые нарушают кишечную микробиоту и способствуют избыточной колонизации кишечника дрожжевыми грибками. Для выявления ASCA классов IgA и IgG чаще всего используют непрямую реакцию иммунофлюоресценции (нРИФ) — выявление антител в крови с помощью специальной метки, светящейся в ультрафиолетовом свете, и иммуноферментный анализ — когда антитела выявляют с помощью реакции антигена с антителом и ферментного усиления сигнала [5–8]. ANCA — антинейтрофильные цитоплазматические антитела, чаще встречаются при язвенном колите [5], [8]. Помимо дифференциальной диагностики, анализ на ASCA также можно использовать для подтверждения диагноза БК в комплексе с другими методами диагностики [9]. ASCA являются стабильным показателем, не меняясь на протяжении заболевания. Также они могут служить прогностическим маркером: у ASCA-позитивных пациентов наблюдается более тяжелое течение заболевания по эндоскопическим и клиническим признакам [9].
У пациентов с БК часто встречаются панкреатические аутоантитела (PAB) классов IgA и IgG — антитела к гликопротеину 2 (GP2). GP2 наиболее известен как белок, входящий в состав мембран гранул ацинарных клеток поджелудочной железы — это клетки, которые отвечают за выработку пищеварительных ферментов. Однако GP2 также экспрессируется эпителием Пейеровых бляшек — лимфоидных узелков, расположенных в слизистой и подслизистой оболочках тонкой кишки, преимущественно подвздошной, которая, в свою очередь, является наиболее частой локализацией БК. GP2 регулирует воспалительные процессы и выполняет антибактериальную функцию. При БК синтез GP2 увеличивается под действием провоспалительных цитокинов. Нарушение барьера и хроническое воспаление приводят к утрате толерантности к GP2 и формированию аутоантител. У пациентов с БК частота встречаемости антител к GP2 составила 27–42%, у больных язвенным колитом — 0–5%, целиакией — 13%, аутоиммунным панкреатитом и у здоровых людей — 5%. Антитела к гликопротеину 2 чаще всего определяют с помощью нРИФ [2], [5], [10].
При БК определяется более высокий уровень антител к цитокину GM-CSF, чем у больных язвенным колитом и у здоровых. GM-CSF синтезируется иммуноцитами слизистой оболочки кишечника и участвует в работе лейкоцитов и процессах репарации тканей [8], [11].
Также при БК выявляются антитела к антигенным пептидам — коротким цепочкам аминокислот, таким как CDP-1, 3, 4, 5 и ТСР-353. Антитела выявляются в 57–62% случаев против 0–7% случаев при язвенном колите. В проведенном исследовании было показано, что ТСР-353 участвует в патогенезе БК, индуцируя выработку провоспалительных цитокинов [8].
Врач не сможет поставить диагноз лишь по уровню антител, но это не значит, что исследование уровня антител — пустая трата времени. Антитела помогают отличить БК от похожих заболеваний, в частности, от другого воспалительного заболевания кишечника — язвенного колита, особенно если определять не один вид, а целый спектр антител. Кроме того, антитела полезны в прогнозировании характера течения заболевания, и это может помочь врачу выбрать тактику ведения пациента. Изучая же причины и механизмы появления антител, можно лучше понять различные аспекты механизмов возникновения и развития заболевания.
Биомаркеры — лабораторные характеристики организма
Рисунок 2. Кальпротектин — наследие лейкоцитов.
Наиболее важным биомаркером, указывающим на воспалительные процессы в кишечнике при ВЗК, считается фекальный кальпротектин. Кальпротектин является продуктом нейтрофилов, сохраняется в кале на протяжении 7 дней и равномерно в нем распределен. Уровень кальпротектина коррелирует с уровнем воспаления в стенке кишки, поэтому фекальный кальпротектин может использоваться для наблюдения за динамикой заболевания и эффективностью лечения. Определяется с помощью иммуноферментного анализа. Нормальный уровень кальпротектина — 50 мкг/гр, 50–120 мкг/гр считается умеренным повышением, а уровень выше 120 мкг/гр указывает на наличие воспалительного заболевания кишечника. Помимо БК фекальный кальпротектин может повышаться при язвенном колите, инфекциях ЖКТ, приеме нестероидных противовоспалительных препаратов, таких как ибупрофен, диклофенак, аспирин, дивертикулите и онкологии. Среди людей с уровнем кальпротектина в кале выше 120 мкг/гр ВЗК есть у 74% — это чувствительность метода в диагностике ВЗК, а среди людей с уровнем ниже 120 мкг/гр 87% не больны ВЗК — это специфичность метода (рис. 2). Еще один продукт нейтрофилов, определяемый в кале и являющийся стабильным показателем — фекальный лактоферрин. Однако он уступает кальпротектину в чувствительности при диагностике ВЗК — 62% против 74% [11].
Фекальный альфа1-антитрипсин — молекула, которая блокирует ферменты, расщепляющие белки — увеличивается при обострениях БК и может использоваться врачами для прогнозирования обострений и определения тактики ведения пациентов [11], [12].
В наблюдении за динамикой течения БК и эффективностью лечения также может помочь определение уровня С-реактивного белка (СРБ) в сыворотке крови. СРБ синтезируется в печени в ответ на провоспалительные цитокины и играет роль во врожденном иммунитете. Уровень СРБ повышается почти при любых воспалительных процессах, но в сочетании с оценкой симптомов и уровня фекального кальпротектина оценка уровня СРБ может использоваться для определения активности заболевания. Исчезновение симптомов в сочетании с уровнем фекального кальпротектина менее 150 мкг/гр и нормальным уровнем СРБ позволяет не проводить эндоскопическую оценку активности заболевания.
Скорость оседания эритроцитов (СОЭ) — скорость, с которой эритроциты оседают на дно пробирки с кровью в течение часа — повышается при многих заболеваниях, но может быть использована для того, чтобы отличить БК от заболеваний ЖКТ, при которых отсутствуют органические изменения, например, от синдрома раздраженного кишечника, так как повышение СОЭ свидетельствует о наличии воспалительных процессов в организме — она повышается при увеличении концентрации фибриногена, который участвует в образовании тромбов, и IgG. Также существует значительная корреляция между СОЭ и активностью БК, но для СРБ корреляция с активностью БК более выражена, т.к. СОЭ медленнее достигает пика, а снижение СОЭ может продолжаться до 5 дней из-за долгого снижения концентрации фибриногена [13], [14] (рис. 3). Уровень лейкоцитов также принимается во внимание как маркер воспаления.
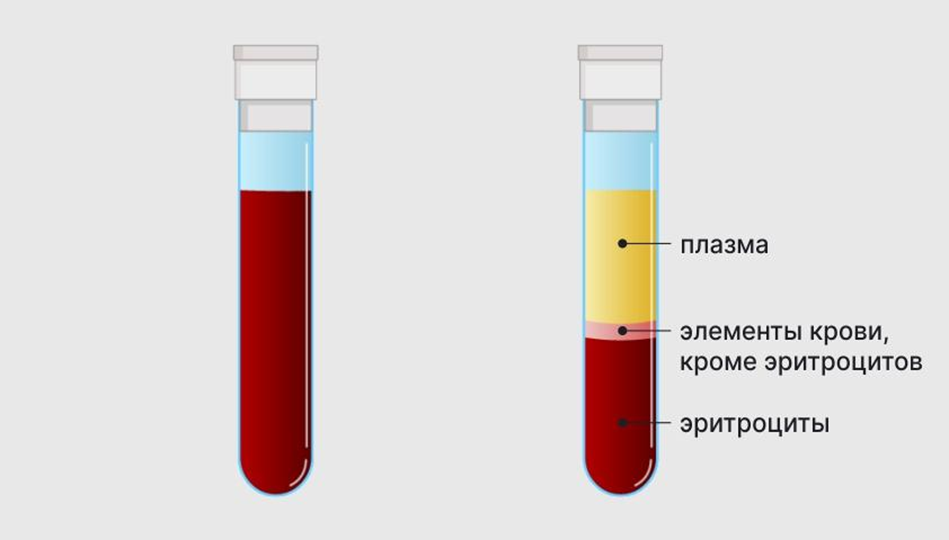
Рисунок 3. Измерение СОЭ. Слева — цельная кровь, справа — кровь, которая разделилась на плазму, эритроциты и остальные элементы крови.
Уровень витамина D в крови может предсказывать активность заболевания. При его низком уровне чаще встречается развитие осложнений БК [15].
Дополнительный метод исследования при БК — исследование желчных кислот в кале. Желчные кислоты — это молекулы, которые играют ключевую роль в переваривании и всасывании жиров. Так как наибольшее количество желчных кислот всасывается в конечном отделе тонкой кишки, при локализации БК в данном отделе всасывание желчных кислот нарушается и их количество в кале может увеличиваться. С помощью фотометрии — измерении интенсивности света, проходящего через образец — определяют суммарное количество желчных кислот: холевой, хенодезоксихолевой, литохолевой, дезоксихолевой и урсодезоксихолевой. Однако повышение содержания желчных кислот в кале может наблюдаться не только при БК, но и при других патологиях ЖКТ, в том числе тех, при которых отсутствуют органические изменения.
При БК часто встречаются такие явления, как анемия — снижение уровня гемоглобина (белка, содержащегося в эритроцитах и обеспечивающего транспорт кислорода и углекислого газа) и/или эритроцитов в крови, мальнутриция — недостаточное поступление питательных веществ в организм, дегидратация — недостаточное количество воды в организме, гипопротеинемия — сниженное количество белка в крови. Чтобы не пропустить эти состояния и отличить их от других патологий, в крови пациентов определяются уровень гемоглобина, эритроцитов, железа, ферритина — белка, который накапливает и хранит железо внутри клеток, необходимых для кроветворения витамина B12 и фолиевой кислоты, общего белка в крови и альбумина — основного белка плазмы крови. Также при активных симптомах БК необходимо проведение иммуноферментного анализа кала на токсины А и В Clostridioides difficile. Эти токсины являются крупными белками, которые бактерия выделяет, попадая в организм. Их определение позволяет обнаружить или исключить Clostridioides difficile-инфекцию, риск которой при ВЗК повышается [2], [14].
Биомаркеры широко используются в диагностике БК, и не зря: они позволяют без больших рисков и затрат получить объективную информацию о состоянии пациента, наличии и активности заболевания и эффективности лечения. Врач определяет биомаркеры комплексно, чтобы получить наиболее полную информацию, а также сочетает анализ уровней биомаркеров с другими методами обследования.
Заключение
На данный момент ведется множество исследований болезни Крона. Лабораторная диагностика этого заболевания постоянно совершенствуется. Несмотря на то, что анализ на антитела не входит во все протоколы диагностики при БК, его нередко используют для того, чтобы отличить БК от похожих заболеваний, а также он может использоваться для подтверждения диагноза. Биомаркеры, такие как фекальный кальпротектин и СРБ, широко используются в диагностике БК и могут быть полезны не только для того, чтобы отличить БК от похожих заболеваний, но и для оценки активности болезни, определения тактики лечения и оценки его эффективности.
Литература
- Першко А. М., Гриневич В. Б., Соловьев И. А., Шотик А. В., Курило Д. П. (2018). Частные вопросы патогенеза воспалительных заболеваний кишечника. Экспериментальная и клиническая гастроэнтерология. 153, 140–149;
- Gary R. Lichtenstein, Edward V. Loftus, Anita Afzali, Millie D. Long, Edward L. Barnes, et. al.. (2025). ACG Clinical Guideline: Management of Crohn's Disease in Adults. Am J Gastroenterol. 120, 1225-1264;
- Michael Dolinger, Joana Torres, Severine Vermeire. (2024). Crohn's disease. The Lancet. 403, 1177-1191;
- Иммунитет: борьба с чужими и… своими;
- Кузнецова Д. А., Лапин С. В., Щукина О. Б. (2020). Диагностическая и прогностическая значимость серологических маркеров воспалительных заболеваний кишечника (обзор литературы). Альманах клинической медицины. 48, 364–374;
- M H Giaffer, A Clark, C D Holdsworth. (1992). Antibodies to Saccharomyces cerevisiae in patients with Crohn's disease and their possible pathogenic importance.. Gut. 33, 1071-1075;
- Boualem Sendid, Marjorie Cornu, Camille Cordier, Julie Bouckaert, Jean Frederic Colombel, Daniel Poulain. (2024). From ASCA breakthrough in Crohn's disease and Candida albicans research to thirty years of investigations about their meaning in human health. Autoimmunity Reviews. 23, 103486;
- E. N. Aleksandrova, A. A. Novikov, G. V. Lukina, A. I. Parfenov. (2021). Clinical value of antibodies in inflammatory bowel diseases. Terapevticheskii arkhiv. 93, 228-235;
- Abin Chandrakumar, Michael Georgy, Prasoon Agarwal, Geert W. ‘t Jong, Wael El‐Matary. (2019). Anti‐Saccharomyces cerevisiae Antibodies as a Prognostic Biomarker in Children With Crohn Disease. J. pediatr. gastroenterol. nutr.. 69, 82-87;
- Michael Shpoliansky, Dirk Roggenbuck, Marina Pinsker, Naomi Salamon, Batia Weiss, et. al.. (2021). Antibodies Against Glycoprotein 2 Are Specific Biomarkers for Pediatric Crohn’s Disease. Dig Dis Sci. 66, 2619-2626;
- Anette Kraemer, Tatiana Bulgakova, Oksana Schukina, Aleksandra Kharitidis, Andrei Kharitonov, et. al.. (2020). Automated Fecal Biomarker Profiling - a Convenient Procedure to Support Diagnosis for Patients with Inflammatory Bowel Diseases. Clin. Lab.. 66;
- Livia Biancone, Massimo Fantini, Claudio Tosti, Rosamaria Bozzi, Piero Vavassori, Francesco Pallone. (2003). Fecal α1-antitrypsin clearance as a marker of clinical relapse in patients with Crohn's disease of the distal ileum. European Journal of Gastroenterology & Hepatology. 15, 261-266;
- Katarzyna Akutko, Barbara Iwańczak. (2022). Evaluation of Fecal Calprotectin, Serum C-Reactive Protein, Erythrocyte Sedimentation Rate, Seromucoid and Procalcitonin in the Diagnostics and Monitoring of Crohn’s Disease in Children. JCM. 11, 6086;
- Что они делают с нашей кровью? Это уже клиника!;
- John Gubatan, Naomi D. Chou, Ole Haagen Nielsen, Alan C. Moss. (2019). Systematic review with meta‐analysis: association of vitamin D status with clinical outcomes in adult patients with inflammatory bowel disease. Aliment Pharmacol Ther. 50, 1146-1158.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚