
Хромосомная мимикрия
19 марта 2026
Хромосомная мимикрия
- 250
- 0
- 0
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В мире животных мимикрия — искусный трюк, чтобы выжить. Оказывается, подобный принцип обмана существует и в наших хромосомах. Мимикрирующие транслокации — это редкие перестройки, при которых морфология хромосом под микроскопом выглядит как клинически значимая транслокация, но на генном уровне ожидаемая перестройка отсутствует, соответствующий химерный ген не образуется. Рассмотрим этот феномен на примере онкогематологических заболеваний.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Идеальный обман, или в чем суть мимикрии хромосом
Многие помнят с уроков биологии бабочку, которая маскируется под сову (рис. 1). В статье «Биомолекулы» [1] подробно разбирается феномен «халтурной» мимикрии у животных, когда подражание неидеально.

Рисунок 1. Бабочка Сова.
Мимикрирующая транслокация как эта бабочка — под микроскопом она идентична значимой рекуррентной транслокации, но не содержит истинной перестройки на уровне генов, т.е. врач получает ложноположительный результат (рис. 2) [2].
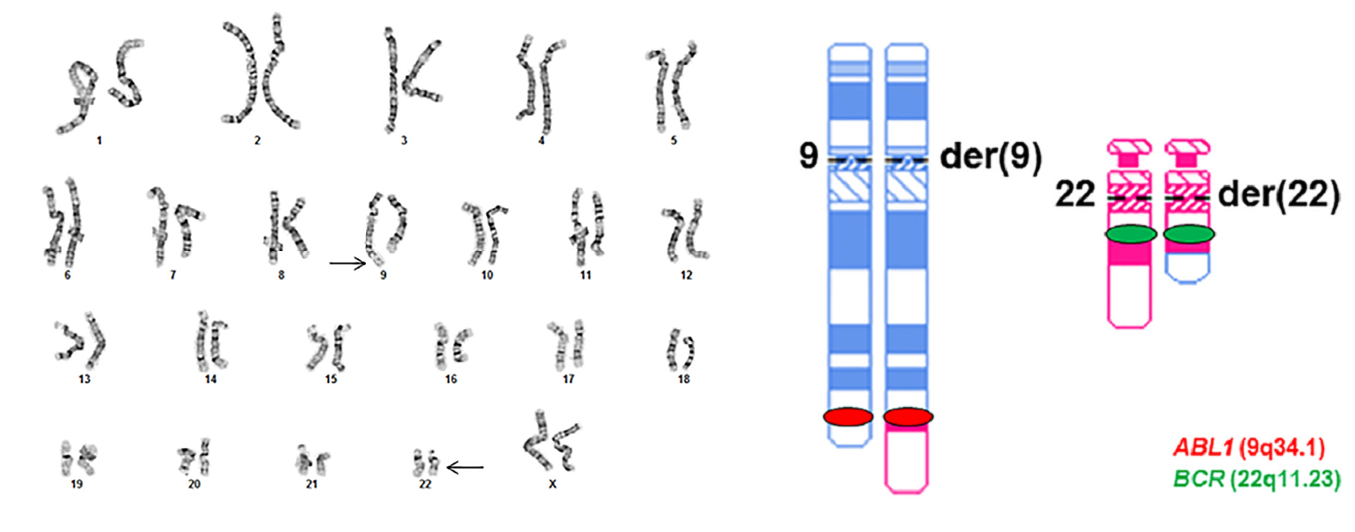
Рисунок 2. Кариограмма и идиограмма пациента с мимикрирующей транслокацией t(9;22), хромосомы меняются участками, но точки разрывов расположены за пределами критических генов BCR и ABL.
Рекуррентная транслокация — это устойчиво повторяющаяся хромосомная перестройка, при которой участки двух разных хромосом обмениваются местами. В онкогематологии такие транслокации часто являются маркерами определенных видов лейкозов и лимфом и помогают поставить диагноз, выбрать терапию, оценить прогноз. Они возникают не случайно, а у пациентов с конкретным заболеванием. Например, классическая транслокация t(9;22), известная как «филадельфийская хромосома», встречается почти у всех пациентов с хроническим миелолейкозом (ХМЛ). В результате такой перестройки образуется химерный ген BCR::ABl, который запускает бесконтрольное деление клеток (рис. 3).
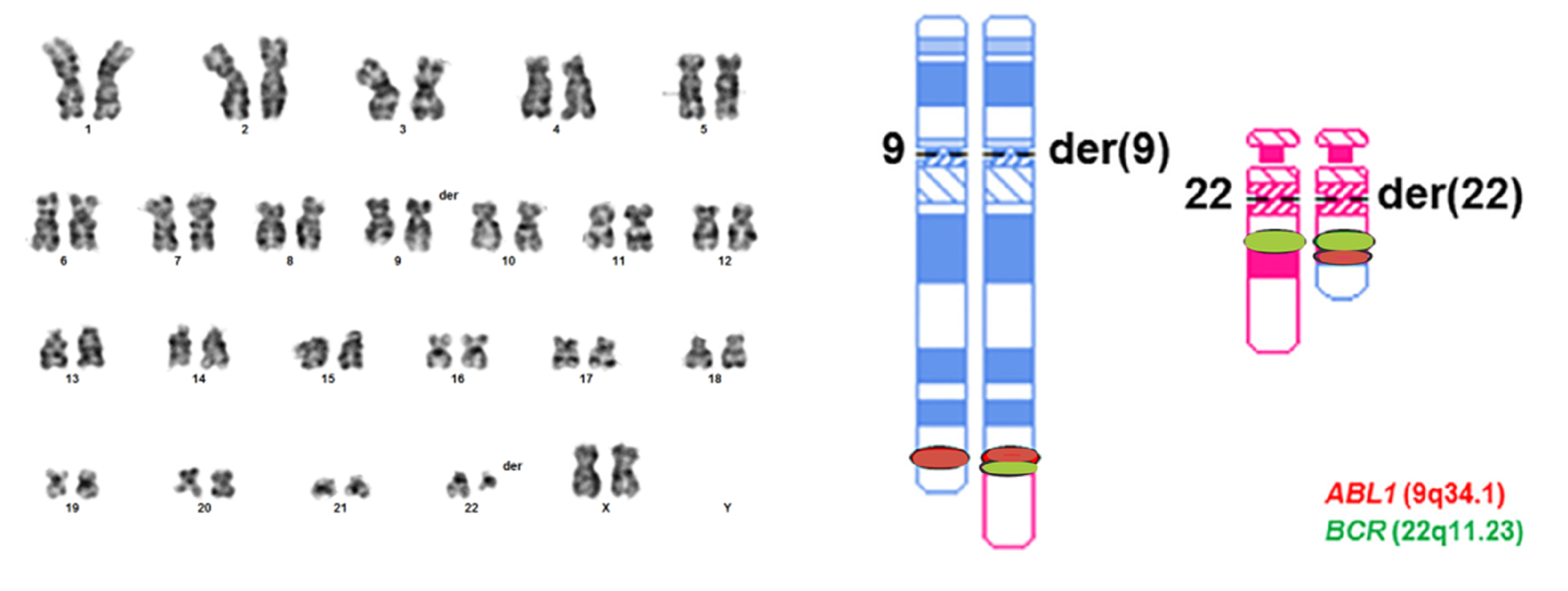
Рисунок 3. Кариограмма и идиограмма пациентки с хроническим миелолейкозом, хромосомы 9 и 22 меняются сегментами, содержащими, соответственно, гены ABL и BCR, в результате чего на производной хромосомы 22 (der(22)) формируется новый функционально активный ген BCR::ABl.
Диагностика лейкозов в настоящее время не обходится без стандартного цитогенетического анализа (кариотипирования), при котором цитогенетик на каждой хромосоме под микроскопом изучает уникальный узор из светлых и темных полос (бэндов). У этого метода есть предел разрешения — около 10 миллионов пар нуклеотидов. Представьте, что вы рассматриваете карту города с высоты птичьего полета. Вы увидите, если две крупные улицы поменяются местами, но не заметите, переехало ли конкретное кафе (ген) на новое место (улицу).
Две маски одного явления: врожденная и приобретенная мимикрия
Мимикрирующие транслокации можно разделить на два разных типа, что критически важно для течения заболевания.
- Врожденные (конституциональные) двойники. Это особенность, с которой человек родился, такая перестройка присутствует во всех клетках организма и сама по себе не вызывает рак. Главная проблема носителей таких транслокаций — это высокий риск невынашивания беременности или рождения детей с хромосомными нарушениями [2], [3]. Первый пример такой конституциональной транслокации t(9;22)(q34;q11.2) был описан в работе 2011 года [4]. У женщины при профилактическом осмотре обнаружили необъяснимое повышение лейкоцитов в крови. Когда ей сделали цитогенетический анализ костного мозга (кариотип) — увидели «филадельфийскую хромосому», которую видят при хроническом миелолейкозе (ХМЛ). Дополнительно выполненные молекулярные тесты показали, что это всего лишь «безобидный двойник» опасной транслокации. Химерного гена BCR::ABL1 в данном случае не образовалось, так как хромосомы обменялись немного другими участками. Здесь и кроется ловушка. Если бы диагноз поставили только на основе кариотипа, то это привело к ненужной и токсичной таргетной терапии. История данной пациентки — яркий пример, что за результатами цитогенетики должна следовать молекулярная диагностика.
- Приобретенные (соматические) двойники. Перестройка возникает только в опухолевых клетках, но копирует морфологию более частого и изученного варианта. Яркий пример из свежего исследования 2025 года — транслокация t(8;21) без характерного химерного гена RUNX1::RUNX1T1 [5]. В этом случае ошибка диагностики приведет к неверной классификации подтипа лейкоза, что может повлиять на протокол лечения и оценку прогноза.
Эволюция методов: от распознавания рисунка к чтению текста
Как же бороться с этими искусными подделками? Эволюция диагностических методов — это история повышения разрешающей способности.
- Эра кариотипирования. Кариотипирование (цитогенетический анализ) позволяет визуализировать полный набор хромосом в одной клетке и выявлять крупные аномалии — дополнительные хромосомы или их потерю, транслокации и маркерные хромосомы. Основа — человеческий глаз, снабженный микроскопом, и опыт. Метод глобальный, но с ограниченной разрешающей способностью. Мимикрия здесь непобедима. При этом, многие современные классификации опухолей прямо опираются на цитогенетические данные.
- Эра FISH (флуоресцентной in situ-гибридизации). Введение FISH стало прорывом, но не панацеей. FISH повышает разрешение за счет флуоресцентных ДНК-зондов, нацеленных на конкретные гены. Это же и его ограничение, видны изменения только в конкретной точке, а не вся картина целиком. FISH также может дать ложноположительный сигнал «слияния», если разрыв при мимикрии попадает внутри зонда, а не между зондами к разным генам [3]. В статье «От хромосом к молекулам: молекулярная цитогенетика» [6] подробно описана методика проведения кариотипирования и FISH- анализа.
- Молекулярная эра (ПЦР-полимеразной цепной реакции). Здесь мимикрия начинает раскрываться. ПЦР прицельно ищет химерную РНК. Нет продукта ПЦР, нет и химерного гена, как бы ни выглядели хромосомы. Подробнее про метод можно прочитать в статье «12 методов в картинках: полимеразная цепная реакция» [7].
- Эра «геномной картографии». Современные методы, например, оптическое картирование генома (OGM) и полногеномное секвенирование позволяют не гадать, а с разрешением в несколько тысяч пар нуклеотидов точно видеть все точки разрывов и соединений, разоблачая мимикрию, какой бы искусной она ни была. Секвенирование всего генома — это самый распространенный подход. ДНК разбивается на миллионы мелких фрагментов (около 150 «букв»-нуклеотидов), которые прочитываются параллельно. Мощные компьютеры затем собирают этот пазл обратно, попутно находя ошибки. Оптическое геномное картирование — это не секвенирование! Здесь ДНК не «читают», а «рассматривают». Длинные молекулы ДНК растягивают в наноканалах и метят флуоресцентными метками в определенных последовательностях. Получается уникальный «штрихкод» для каждой молекулы. Компьютер сравнивает штрихкоды здоровой и опухолевой ДНК, находя разрывы, перевороты и лишние копии. Следует отметить, что все новые технологии работают с «усредненной» ДНК из миллионов клеток. Они могут не уловить малочисленный, но агрессивный клон, который в будущем вызовет рецидив. Кариотипирование же, несмотря на низкое разрешение, позволяет анализировать геном отдельной клетки.
История выявления мимикрирующих транслокаций — это история прогресса в медицине. Мы движемся от доверия к внешней, иногда обманчивой, форме, к пониманию глубинной сути. Чтобы разгадать любую загадку, необходимо посмотреть на нее со всех сторон, иначе может получиться как в притче «слон и слепые». Только комбинация методов обеспечит надежную, доступную и клинически интерпретируемую генетическую картину онкогематологических заболеваний.
Литература
- Имитаторы-халтурщики;
- Jess F. Peterson, Beth A. Pitel, Stephanie A. Smoley, James B. Smadbeck, Sarah H. Johnson, et. al.. (2019). Constitutional chromosome rearrangements that mimic the 2017 world health organization “acute myeloid leukemia with recurrent genetic abnormalities”: A study of three cases and review of the literature. Cancer Genetics. 230, 37-46;
- Zimeng Gao, Stephanie M. Rice, Sascha Wodoslawsky, Sara C. Long, Zi-Xuan Wang, et. al.. (2022). A Systematic Review of Reproductive Counseling in Cases of Parental Constitutional Reciprocal Translocation (9;22) Mimicking BCR-ABL1. Front. Genet.. 13;
- David R. Czuchlewski, Haleh Farzanmehr, Sheldon Robinett, Skip Haines, Kaaren K. Reichard. (2011). t(9;22)(q34;q11.2) is a recurrent constitutional non-Robertsonian translocation and a rare cytogenetic mimic of chronic myeloid leukemia. Cancer Genetics. 204, 572-576;
- Melissa Zhao, Scott Ryall, Samuel J. Brody, Amyah C. Harris, Kristin Cabral, et. al.. (2025). Integrative cytogenetic and molecular studies unmask “chromosomal mimicry” in hematologic malignancies. Blood Advances. 9, 1003-1012;
- От хромосом к молекулам: молекулярная цитогенетика;
- 12 методов в картинках: полимеразная цепная реакция.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





