
Коронованные особы, троянские кони и будущее человечества: как использовать белковую корону
12 марта 2026
Коронованные особы, троянские кони и будущее человечества: как использовать белковую корону
- 275
- 0
- 1
Рисунок в полном размере.
рисунок Зои Черновой
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Попав в биологическую среду — например, в кровь — наночастица тут же покрывается белковой короной. Такая корона кардинально меняет поведение и характеристики частицы: у нее появляется новая идентичность. Ученые, работающие с наночастицами, попали в сложную ситуацию: то ли попытаться помешать формированию короны, то ли пойти другим путем — использовать корону в собственных целях. О том, какой путь они выбрали, мы расскажем в нашей статье.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Жители Бодэга Бэй не были к этому готовы. Только выходишь за порог, и на тебя со всех сторон налетают они: черные птицы, влекомые неизвестной силой и яростью. Зазеваешься, и они покроют тебя с головы до ног — что тогда с тобой будет?
Примерно так чувствуют себя, попав в кровоток или любую другую физиологическую жидкость, наночастицы. Попадают они туда с какой-то целью, но их тут же окружают белки, формируя белковую корону — прямо как птицы облепляют жителей Бодэга Бэй. Исходные свойства частицы при этом меняются: она может стать более или менее токсичной для организма, стать невидимой для клеток иммунной системы, потерять способность связываться с нужными клетками или покрыться белками-опсонинами и... покинуть свой пост, вообще не выполнив задачу. Неудивительно, что с момента обнаружения феномена короны усилия ученых были брошены на то, чтобы от нее избавиться. Но есть и еще одна идея: в последнее время всё чаще предлагается использовать корону во благо — например, для направления наночастиц в нужные органы, повышения эффективности направленной доставки препаратов или снижения токсичности наночастиц.
О тонкостях коронации
Перед тем как понять, как победить «нечто», недурно понять, как это «нечто» устроено. В случае белковой короны путь к ее постижению был труден (и нельзя сказать, что он завершен).
Корона наночастицы имеет две стадии формирования — можно представить это как двойную корону Древнего Египта (рис. 1). Сразу после попадания в биологическую среду наночастицы покрываются первичными белками — первичной «мягкой» короной [1], [2]. Одним из первых с поверхностью связывается альбумин, самый распространенный белок плазмы крови [1], [2].
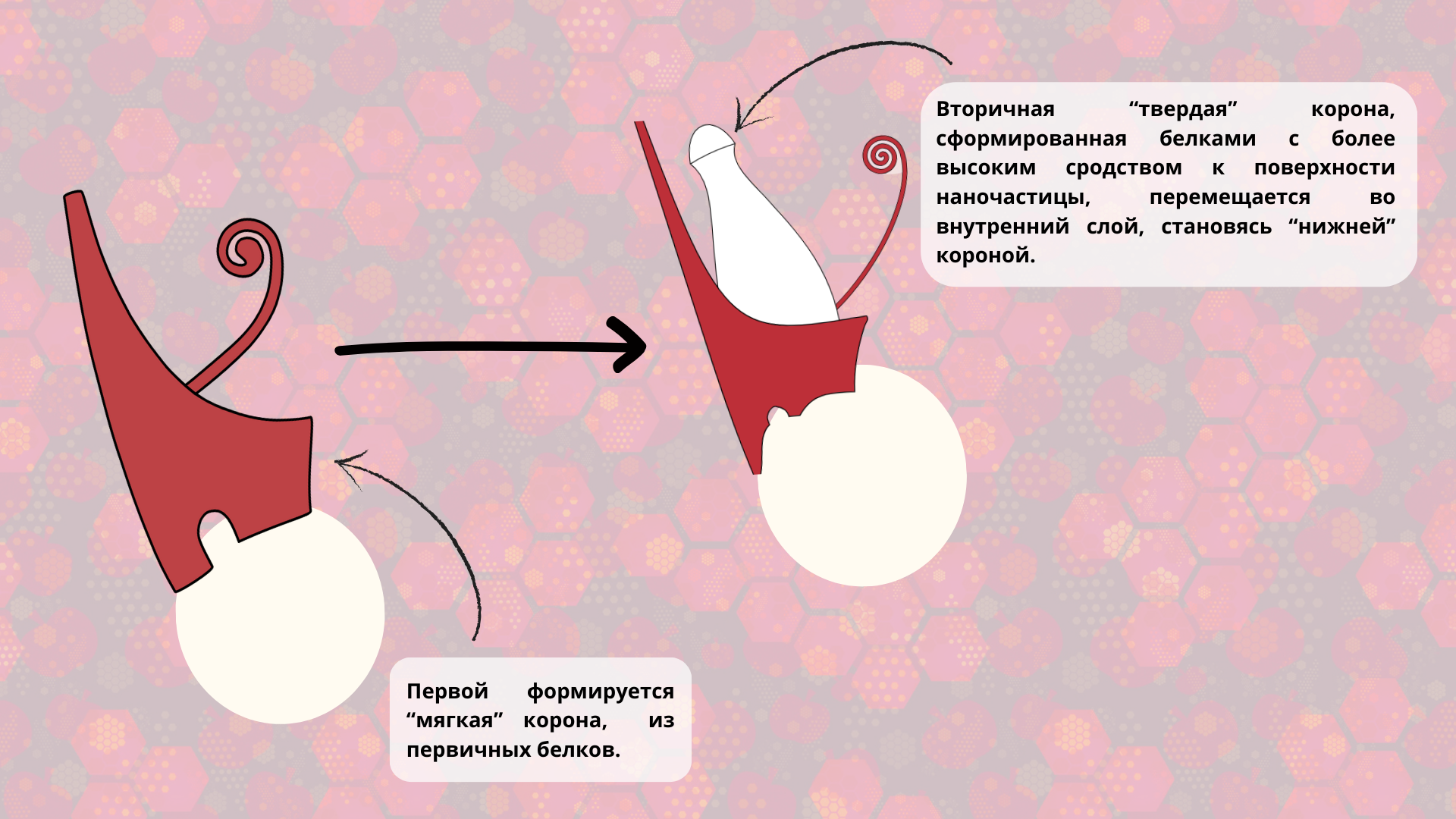
Рисунок 1. Корона наночастицы имеет две стадии формирования — можно представить это как двойную корону Древнего Египта, где «мягкая» корона формируется первой, а под ней с течением времени формируется «твердая» корона.
рисунок Зои Черновой
Через какое-то время белки с более низким сродством к поверхности вытесняются белками, обладающими более высоким сродством. Этот процесс называется «эффектом Вромана», и он приводит к формированию стабильного внутреннего слоя «твердой» короны [1]. Белки «твердой» короны прочно связаны непосредственно с поверхностью наночастицы, в то время как белки «мягкой» короны связаны с белками «твердой» короны более слабыми белок-белковыми взаимодействиями (рис. 2) [3]. Более того, белки «мягкой» короны находятся в динамическом равновесии с окружающей средой, то есть постоянно обмениваются со свободными белками плазмы. «Твердую» корону формируют уже более активные белки: иммуноглобулины [4], [5], фибриноген [5], белки системы комплемента [4], аполипопротеины [6], витронектин [6], [7]. Белков-участников «коронации» на самом деле немало — были замечены даже аристократичные гистоны [1], [2], [4], [6].
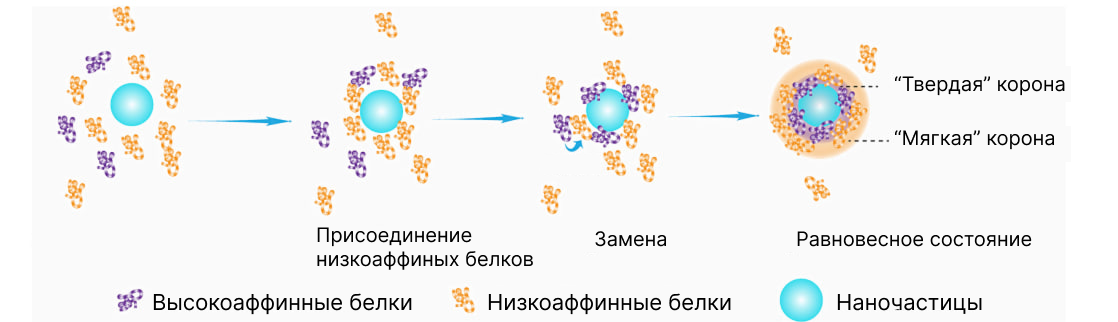
Рисунок 2. Постепенный процесс формирования белковой короны вокруг наночастицы.
адаптировано из [1]
Но почему белки вообще налипают на, казалось бы, неинтересную для них наночастицу? Основная причина крайне проста: взаимодействие между поверхностью наночастиц и биомолекулами. Здесь «работают» и электростатические силы (частицы с высоким положительным зарядом активно взаимодействуют с белками, имеющими изоэлектрическую точку ниже 5,5, тогда как отрицательно заряженные частицы притягивают белки с изоэлектрической точкой выше 5,5), и гидрофобно-гидрофильные связи, и силы Ван-дер-Ваальса с водородными связями [1].
На состав короны влияет множество факторов: и свойства самих наночастиц, их заряд и химический состав поверхности, и конкретная биологическая среда, куда попала наночастица, и даже индивидуальные особенности организма (одна и та же наночастица, попав в кровоток мыши или, например, здорового или больного человека, покроется разными коронами) [1], [5].
При этом «коронация» наночастицы похожа на то, как в мифологических историях людям раздают судьбы. Белки, формирующие корону, формируют и дальнейшую судьбу наночастицы — и поменять ее уже практически невозможно. А влияет корона колоссально: она буквально меняет идентичность наночастицы, заставляет выглядеть и действовать совершенно другим образом.
С одной стороны, корона маскирует исходную поверхность частицы, меняя заряд, размеры, гидрофобность и так далее [5–7]. С другой, меняет и взаимоотношения частицы с клетками: например, богатая альбумином корона снижает поверхностную энергию частиц, и взаимодействие с поверхностью клеток снижается [5–7]. В некоторых случаях клеточное поглощение, наоборот, усиливается: например, корона, обогащенная витронектином, усиливает связывание частиц раковыми клетками — они экспрессируют рецепторы к этому белку [7].
Но самое важное влияние — это влияние на то, как иммунная система видит частицу. Белки-опсонины (например, иммуноглобулины или факторы комплемента), адсорбируясь на поверхности, работают как сигналы для клеток иммунной системы [1], [8] — «Эй, — говорят они, — мы нашли что-то странное, давайте удалим это из организма!». С другой стороны, есть белки, которые, наоборот, ингибируют активацию комплемента и мешают клеткам иммунной системы делать свою работу.
Решаем проблему
Итак, корона меняет все. Ты вводишь наночастицу для решения какой-то проблемы, а вокруг нее образуется корона, которую трудно четко предсказать и которая мешает всей работе. Что делать? Решение кажется очевидным: помешать ей формироваться. Так борьба с формированием короны стала одной из ключевых задач наномедицины.
На заре исследований этого феномена ученые пытались установить взаимосвязь между физико-химическими свойствами частиц и характеристиками образующейся на них короны — количественными и качественными. Идея состояла в том, чтобы, установив эту взаимосвязь, создавать частицы с оптимальными свойствами, и таким образом контролировать ее. Взаимосвязь установить удалось, но параметров оказалось слишком много, чтобы делать однозначный прогноз. Слишком много характеристик: и размер, и форма, и заряд, и жесткость частицы, и химический состав, не говоря уже о разнообразии сочетания этих факторов. Можно сказать, что белковый «отпечаток» на каждой наночастице уникален, хотя его формирование и подчиняется каким-то общим законам.
Тогда они придумали плащ-невидимку: на поверхность наночастицы наносят тонкий слой полиэтиленгликоля (этот процесс называют ПЭГилированием) [4], [9] (рис. 3). Гидрофильные цепи ПЭГ притягивают молекулы воды, которые создают вокруг частицы плотный слой, отталкивающий белки и мешающий им взаимодействовать с поверхностью частицы напрямую. Это в литературе называется стеллс-эффектом: частица будто покрывается заклинаниями невидимости. Но работал плащ из полиэтиленгликоля неидеально: во-первых, не давал 100%-ой гарантии «невидимости», а во-вторых, иногда и вовсе мешал нормальной работе — сам вызывал иммунный ответ и образование анти-ПЭГ-антител [4], [9].
Тогда в игру вступили другие полимеры: в первую очередь, поли-2-оксазолины (POx), цвиттер-ионные материалы и другие молекулы (в том числе биополимеры — хитозан и гиалуроновая кислота) [1], [4]. Все они показали неплохую эффективность в создании щита и снижали адсорбцию белков — но полной защиты все еще не было.
Последним появился немного безумный, но потенциально идеальный подход — «клокинг», или маскировка наночастиц... биомембранами собственных клеток организма [4] (рис. 3). Такой волк в овечьей шкуре, по идее, полностью укрытый клеточной мембраной, не должен вообще вызывать подозрения у клеток иммунной системы, да и белкам будет менее интересен. Такая биомиметика предполагает сложную процедуру: сначала нужно выделить клетки нужного типа (чаще всего выбирают мембрану эритроцитов), затем разрушить их, сохранив полностью стабильные мембраны, а потом «надеть» мембраны на наночастицы. В идеальном мире, где мембрана действительно сохранила полную структуру, наночастица выглядит для организма как эритроцит, со всеми необходимыми рецепторами и сигналами. Звучит как гениальный план, но на практике и у этого пути множество недостатков: от сложности и высокой стоимости создания таких «перевертышей» до огромных проблем с масштабируемостью [4], [8].
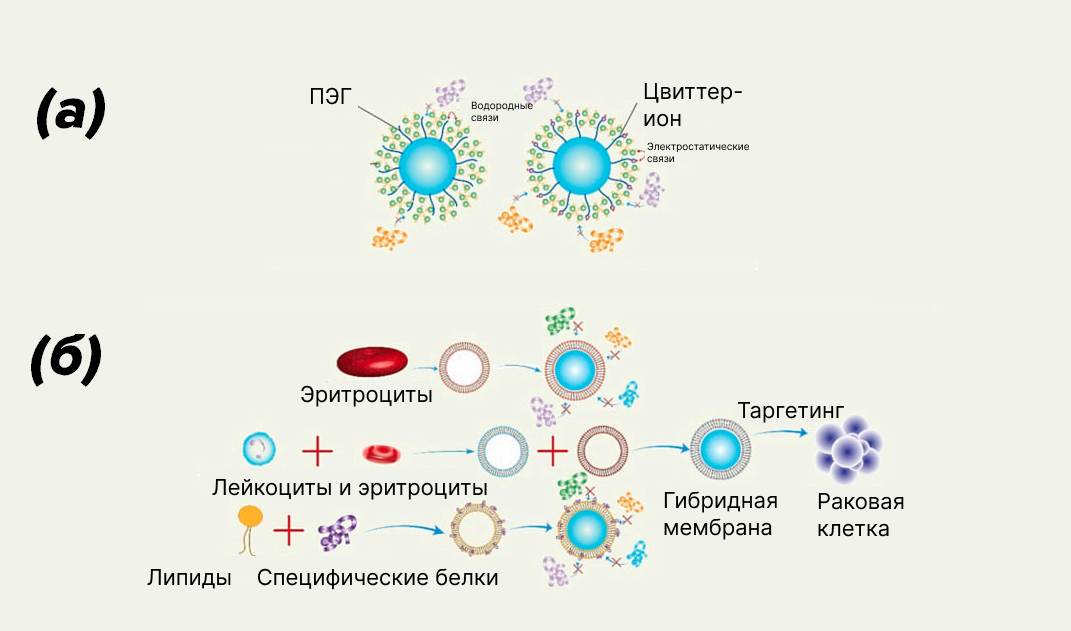
Рисунок 3. Способы борьбы с белковой короной: (а) — модифицирование с помощью ПЭГ и цвиттер-ионов; (б) — «клокинг» — биомиметическая мембрана.
адаптировано из [1]
Не можешь победить — возглавь!
Итак, методов борьбы с формированием короны много. Но ряд ученых, посмотрев на корону, пришли к выводу, что можно пойти вообще другим путем — сменить парадигму борьбы на использование в своих целях. Что, если белковая корона — это отличный способ управлять наночастицей? Что, если не бороться с короной, а заставить ее работать на наши человеческие нужды?
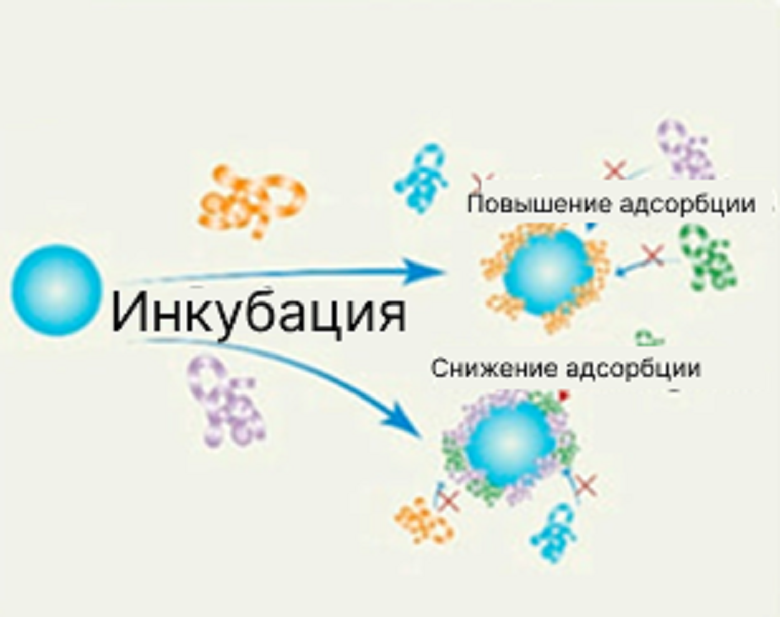
Рисунок 4. Пре-коатинг, или предварительное покрытие наночастицы белковой короной.
адаптировано из [1]
Стратегия предварительного покрытия предполагает, что еще до введения в организм, наночастицу коронуют в искусственную корону из заранее выбранных белков [1], [4], [8], [9] (рис. 4). Такая методика предполагает довольно длительный процесс. Сначала выбирают белки. Чаще всего для короны берут многострадальный альбумин — он и распространен в плазме, и может мешать иммунным клеткам. Также довольно часто используют аполипопротеины — некоторые из этих белков, например, аполипопротеин J, он же кластерин, способны уменьшать захват частиц клетками [10]. У других белков этого семейства, например, аполипопротеина E, есть еще одна суперспособность — направлять частицу в клетки мозга, что тоже можно использовать для создания систем доставки [11]. Но наночастицы мало просто смешать с нужным белком, им нужно еще и сделать для этого рандеву определенные условия. В случае наночастиц, предназначенных для работы в организме человека, это должна быть инкубация при температуре около 37 oC. На третьем этапе счастливые парочки частиц и белка чистят от одиночек — это этап центрифугирования и очистки.
При этом нужно очень осторожно выбирать метод предварительного «укрывания» частиц выбранными белками. Если в процессе нанесения белок потеряет свою исходную структуру, в организме его встретят беспощадные макрофаги, на поверхности которых есть специальные рецепторы-«мусорщики» (scavenger receptors), узнающие «испорченные» белки [12]. Несмотря на все сложности, к настоящему моменту есть примеры успешного применения этой стратегии.
Предварительная адсорбция аполипопротеина E на поверхности графеновых и золотых наночастиц позволила замедлить выведение частиц из организма, что также способствовало их накоплению в опухоли [13]. «Укрывание» поверхности наночастиц кремния с помощью фактора комплемента H привело к снижению количества адсорбирующихся из плазмы белков и препятствовало активации системы комплемента [14]. Белковые наночастицы для доставки, конъюгированные с аптамерами [15], несущие на поверхности белок казеин, показали высокую эффективность доставки в опухоль [16]. Также было показано уменьшение цитотоксичности полимерных наночастиц после адсорбции на их поверхности белков — лизоцима, бычьего сывороточного альбумина и иммуноглобулина G [17]. В эксперименте на мышах золотые наностержни, предварительно покрытые белками сыворотки крови, смогли доставить в опухоль фотосенсибилизатор [9]. При облучении лазером это позволило одновременно и фототермически «сжечь» опухоль, и запустить химическую атаку, что привело к полному излечению у мышей. Это показывает, что естественная корона может быть биосовместимым и функциональным инструментом. Причем современные методики предполагают инкубацию наночастиц прямо в сыворотке, что сделает такую предварительную коронацию куда легче.
Предварительно созданная корона действительно довольно сильно влияет на поведение белков: и это хорошая новость, потому что у наночастицы и ее судьбы появляется предсказуемость. Помимо покрытия частиц белками для «маскировки», можно придумать и более интересное практическое применение: вместо альбумина использовать другой белок — глутатионтрансферазу — для защиты, а к ней прикрепить специальные белки нацеливания, аффибоди — искусственно созданные молекулы, распознающие клетки опухоли [8] (рис. 5). А это уже прямой путь в сторону таргетной доставки.
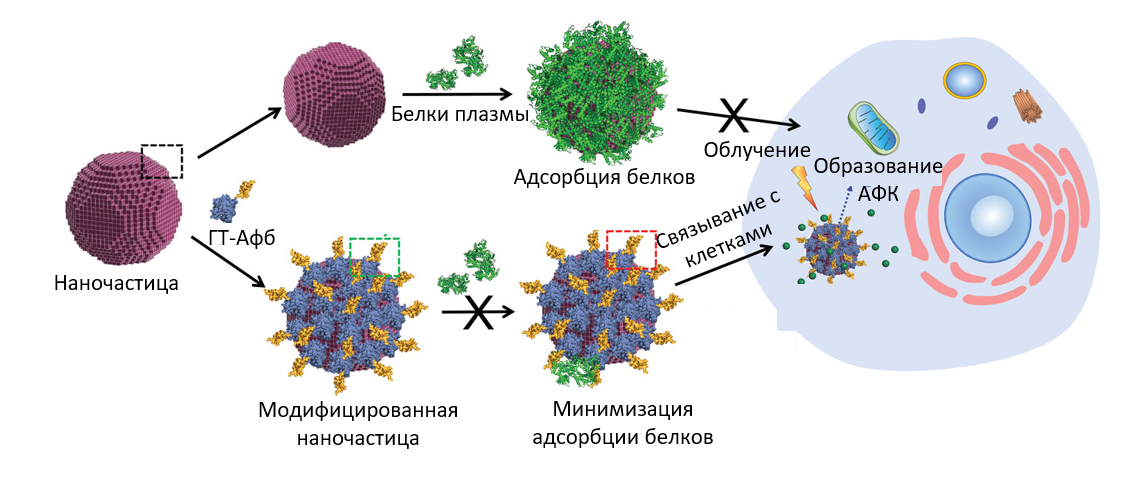
Рисунок 5. Доставка наночастиц с помощью предварительно сформированной белковой короны. ГТ — глутатионтрансфераза, Афб — аффибоди, АФК — активные формы кислорода.
адаптировано из [8]
Perfect match
Существуют две основные стратегии доставки наночастиц с противоопухолевыми препаратами — пассивный и активный таргетинг. При пассивном нацеливании частицы попадают в опухоль за счет эффекта повышенной проницаемости и задержания (ERP, enhanced permeability and retention). Однако белки сыворотки крови, покрывающие частицу — иммуноглобулины, фибриноген и факторы комплемента — могут способствовать выведению частицы из организма клетками иммунной системы. Следовательно, уменьшение адсорбции этих белков на поверхности частиц может улучшить эффективность их доставки. С другой стороны, усиление адсорбции «полезных» белков, например, альбумина, может помочь частицам остаться невидимыми для иммунной системы.
Например, методом молекулярного импринтинга были созданы наногели, поверхность которых при попадании в кровоток «узнавала» альбумин, и за счет этого наногели дольше оставались в организме мыши и накапливались в опухоли [18]. Другая группа ученых использовала похожую идею для создания наночастиц, несущих противоопухолевый препарат: к их поверхности «пришили» химические группы, прочно связывающие альбумин после попадания частиц в кровь. Такие частицы медленнее выводились из кровотока и эффективно проникали в клетки опухоли, что в результате усилило эффект от лекарства [19]. Белки семейства аполипопротеинов также могут помогать наночастицам достичь опухолевых клеток, потому что некоторые из них экспрессируют на поверхности рецепторы к этим белкам. А заставить частицу связывать именно аполипопротеины можно, регулируя ее состав — например, соотношение положительно и отрицательно заряженных групп в липидах, из которых она состоит [6].
Активный таргетинг, или направленная доставка, основан на модификации поверхности наночастиц распознающими молекулами, например, антителами, пептидами или биополимерами, которые узнают рецепторы на поверхности клеток-мишеней и избирательно связываются с ними: это и увеличивает эффективность лечения, и снижает побочные эффекты. Белковая корона в разработке таких «идеальных» систем доставки обычно рассматривается как преграда, ведь молекулы белков плазмы крови могут маскировать те же антитела на поверхности частиц и мешать им связываться со своими мишенями. Однако, и тут ученые смогли придумать, как использовать адсорбцию белков на пользу дела. Например, липидные частицы спонтанно формируют корону с высоким содержанием витронектина: это позволяет им эффективно связываться с раковыми клетками, экспрессирующими витронектиновый рецептор [7].
Используя результаты этого и других исследований, другая научная группа создала ряд липосом с разным составом, а потом проанализировала их взаимодействие с белками плазмы. Потом отбирали те липосомы, которые связывали максимальное количество витронектина, аполипопротеинов и других белков, потенциально улучшающих доставку в раковые клетки. И действительно, именно эти липосомы показали высокий уровень связывания с клетками аденокарциномы поджелудочной железы и инсулиномы. Причем эффективность такой таргетной доставки значительно превосходила связывание липосомального химиотерапевтического препарата «Онивайд», уже применяющегося в клинической практике [20].
Более сложный подход применили для направленной доставки олигонуклеотида в клетки печени для лечения фиброза. Полимерные частицы синтезировали с ретинолом на поверхности, благодаря чему при попадании в кровь с их поверхностью связывались не случайные белки плазмы, а вполне определенный — RBP4 (ретинол-связывающий белок 4), что обеспечивало специфическое связывание с клетками печени, а связывание альбумина уменьшало неспецифические взаимодейстивия [2] (рис. 6).
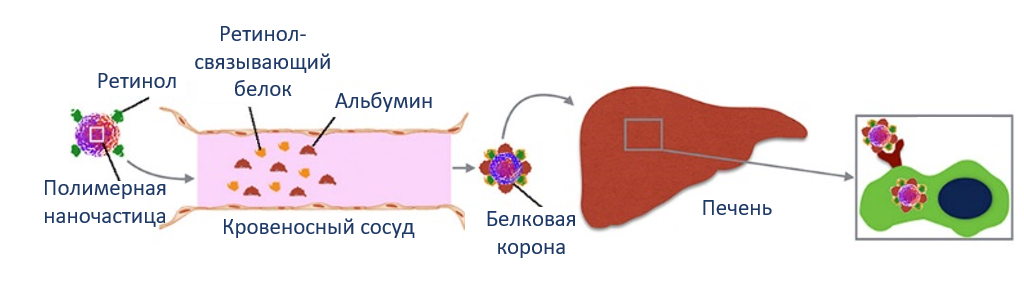
Рисунок 6. Доставка наночастиц в клетки печени за счет избирательного связывания белков в плазме крови.
адаптировано из [2]
Умная медицина будущего
Манипулирование наночастицами и их взаимодействием с белками организма дает обширное поле для экспериментов. Теоретически, в будущем можно будет брать анализ крови пациента, определять его уникальный белковый состав и создавать наночастицы, которые сформируют «идеальную» корону именно в его организме для максимальной эффективности лечения.
Способность наночастиц притягивать к себе уникальный набор белков, попадая в плазму, недавно уже начали использовать для диагностики различных заболеваний. Дело в том, что состояние организма влияет на состав белков крови, а «поймать» специфические маркеры традиционными методами не всегда получается. Например, «отпечаток» белков, образовавшийся на липосомах в образцах крови, позволил отличить пациентов с опухолями центральной нервной системы от здоровых доноров [21]. Также был создан набор магнитных наночастиц для глубокого анализа протеома плазмы крови человека — тут пригодились знания о влиянии физико-химических свойств частиц на состав белковой короны [22].
А еще можно вполне подключить компьютеры: например, для моделирования процесса формирования короны, чтобы предсказывать его и создавать наночастицы с заранее заданными свойствами. Например, модель NPCoronaPredict, представленная в 2024 году, позволяет предсказывать взаимодействие наночастиц и других материалов со смесью биомолекул (в основном, белков) с известными свойствами [23]. Модель предсказания белковой короны на основе машинного обучения показала коэффициент корреляции с экспериментальными данными от 0,45 до 0,88, что выглядит довольно обнадеживающе [24].
В будущем подходы к использованию белковой короны, вероятно, полностью сместятся к активному и целенаправленному управлению ее составом. Одной из самых перспективных стратегий является уход в персонализированную медицину. Идея заключается в том, что уникальный состав белков плазмы крови каждого человека формирует такую же уникальную «персонализированную корону». А анализ этой короны с помощью протеомики и машинного обучения может стать мощным инструментом для ранней диагностики рака и других заболеваний, выявляя специфические именно для конкретного человека биомаркеры. Потом, на основе полученных данных, можно будет делать индивидуальные, эффективные только для пациента, нанолекарства [25] (рис. 7).
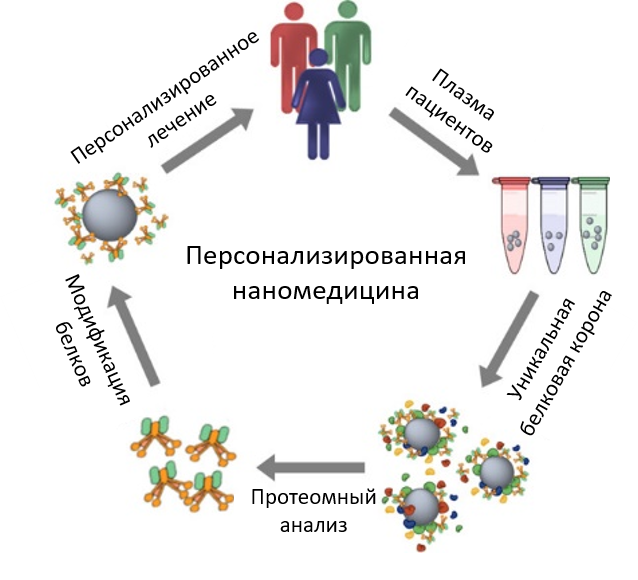
Рисунок 7. Стратегия применения белковой короны в персонализированной медицине.
адаптировано из [25]
Термин «белковая корона» появился только в 2007 году [3], и меньше чем за 20 лет человечество прошло путь от «избегать любым путем» до «использовать себе на благо». Из непредсказуемого препятствия она превратилась в ключевой элемент для разработки «умных» и индивидуально настроенных терапевтических и диагностических платформ: их появление — это лишь вопрос времени.
Литература
- Fangyuan Guo, Shuai Luo, Lianyi Wang, Mengqi Wang, Fang Wu, et. al.. (2024). Protein corona, influence on drug delivery system and its improvement strategy: A review. International Journal of Biological Macromolecules. 256, 128513;
- Zhengping Zhang, Chunming Wang, Yinhe Zha, Wei Hu, Zhongfei Gao, et. al.. (2015). Corona-Directed Nucleic Acid Delivery into Hepatic Stellate Cells for Liver Fibrosis Therapy. ACS Nano. 9, 2405-2419;
- Арчаков А.И. (2019). Эволюция концепции белковой короны наночастиц. Биомедицинская химия. 65, 5–8;
- Woojun Kim, Nhu Ky Ly, Yanying He, Yongzhe Li, Zhongyue Yuan, Yoon Yeo. (2023). Protein corona: Friend or foe? Co-opting serum proteins for nanoparticle delivery. Advanced Drug Delivery Reviews. 192, 114635;
- Burcu Önal Acet, Désirée Gül, Roland H. Stauber, Mehmet Odabaşı, Ömür Acet. (2024). A Review for Uncovering the “Protein-Nanoparticle Alliance”: Implications of the Protein Corona for Biomedical Applications. Nanomaterials. 14, 823;
- Dongyu Chen, Neha Parayath, Shanthi Ganesh, Weimin Wang, Mansoor Amiji. (2019). The role of apolipoprotein- and vitronectin-enriched protein corona on lipid nanoparticles forin vivotargeted delivery and transfection of oligonucleotides in murine tumor models. Nanoscale. 11, 18806-18824;
- Giulio Caracciolo, Francesco Cardarelli, Daniela Pozzi, Fabrizio Salomone, Giuseppe Maccari, et. al.. (2013). Selective Targeting Capability Acquired with a Protein Corona Adsorbed on the Surface of 1,2-Dioleoyl-3-trimethylammonium Propane/DNA Nanoparticles. ACS Appl. Mater. Interfaces. 5, 13171-13179;
- Jun Yong Oh, Eunshil Choi, Batakrishna Jana, Eun Min Go, Eunji Jin, et. al.. (2023). Protein‐Precoated Surface of Metal‐Organic Framework Nanoparticles for Targeted Delivery. Small. 19;
- Woojun Kim, Nhu Ky Ly, Yanying He, Yongzhe Li, Zhongyue Yuan, Yoon Yeo. (2023). Protein corona: Friend or foe? Co-opting serum proteins for nanoparticle delivery. Advanced Drug Delivery Reviews. 192, 114635;
- Susanne Schöttler, Greta Becker, Svenja Winzen, Tobias Steinbach, Kristin Mohr, et. al.. (2016). Protein adsorption is required for stealth effect of poly(ethylene glycol)- and poly(phosphoester)-coated nanocarriers. Nature Nanotech. 11, 372-377;
- Roberta Dal Magro, Barbara Albertini, Silvia Beretta, Roberta Rigolio, Elisabetta Donzelli, et. al.. (2018). Artificial apolipoprotein corona enables nanoparticle brain targeting. Nanomedicine: Nanotechnology, Biology and Medicine. 14, 429-438;
- Hyesun Hyun, Joonyoung Park, Kiela Willis, Ji Eun Park, L. Tiffany Lyle, et. al.. (2018). Surface modification of polymer nanoparticles with native albumin for enhancing drug delivery to solid tumors. Biomaterials. 180, 206-224;
- Xiang Lu, Peipei Xu, Hong-Ming Ding, You-Sheng Yu, Da Huo, Yu-Qiang Ma. (2019). Tailoring the component of protein corona via simple chemistry. Nat Commun. 10;
- Jae Hyeon Park, Joshua A. Jackman, Abdul Rahim Ferhan, Jason N. Belling, Natalia Mokrzecka, et. al.. (2020). Cloaking Silica Nanoparticles with Functional Protein Coatings for Reduced Complement Activation and Cellular Uptake. ACS Nano. 14, 11950-11961;
- Аптамеры: графический гайд;
- Zicheng Zhong, Senbiao Fang, Yan Li, Yuan Huang, Yue Zhang, et. al.. (2021). Quantitative Analysis of Protein Corona on Precoated Protein Nanoparticles and Determined Nanoparticles with Ultralow Protein Corona and Efficient Targeting in Vivo. ACS Appl. Mater. Interfaces. 13, 56812-56824;
- Fernando A. de Oliveira, Lindomar J.C. Albuquerque, Carlos E. Castro, Karin A. Riske, Ismael C. Bellettini, Fernando C. Giacomelli. (2022). Reduced cytotoxicity of nanomaterials driven by nano-bio interactions: Case study of single protein coronas enveloping polymersomes. Colloids and Surfaces B: Biointerfaces. 213, 112387;
- Toshifumi Takeuchi, Yukiya Kitayama, Reo Sasao, Takuya Yamada, Kazuko Toh, et. al.. (2017). Molecularly Imprinted Nanogels Acquire Stealth In Situ by Cloaking Themselves with Native Dysopsonic Proteins. Angew Chem Int Ed. 56, 7088-7092;
- Zhenbao Li, Dan Li, Qingsong Li, Cong Luo, Jing Li, et. al.. (2018). In situlow-immunogenic albumin-conjugating-corona guiding nanoparticles for tumor-targeting chemotherapy. Biomater. Sci.. 6, 2681-2693;
- Sara Palchetti, Damiano Caputo, Luca Digiacomo, Anna Laura Capriotti, Roberto Coppola, et. al.. (2019). Protein Corona Fingerprints of Liposomes: New Opportunities for Targeted Drug Delivery and Early Detection in Pancreatic Cancer. Pharmaceutics. 11, 31;
- Massimiliano Papi, Valentina Palmieri, Sara Palchetti, Daniela Pozzi, Luca Digiacomo, et. al.. (2019). Exploitation of nanoparticle-protein interactions for early disease detection. Applied Physics Letters. 114;
- John E. Blume, William C. Manning, Gregory Troiano, Daniel Hornburg, Michael Figa, et. al.. (2020). Rapid, deep and precise profiling of the plasma proteome with multi-nanoparticle protein corona. Nat Commun. 11;
- Ian Rouse, David Power, Julia Subbotina, Vladimir Lobaskin. (2024). NPCoronaPredict: A Computational Pipeline for the Prediction of the Nanoparticle–Biomolecule Corona. J. Chem. Inf. Model.. 64, 7525-7543;
- Nicole Vijgen, Karsten M. Poulsen, Gustavo Sosa Macias, Christine K. Payne. (2025). Predicting the protein corona on nanoparticles using random forest models with nanoparticle, protein, and experimental features. Nanoscale Adv.. 7, 5612-5624;
- Jiayu Ren, Rong Cai, Jing Wang, Muhammad Daniyal, Didar Baimanov, et. al.. (2019). Precision Nanomedicine Development Based on Specific Opsonization of Human Cancer Patient-Personalized Protein Coronas. Nano Lett.. 19, 4692-4701.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





