
«Метаболизм и шизофрения»: поиск ассоциаций удается вузам России
10 октября 2018
«Метаболизм и шизофрения»: поиск ассоциаций удается вузам России
- 1697
- 0
- 6
-
Авторы
-
Редактор
Темы
Статья на конкурс «био/мол/текст»: Шизофрения — настоящая «живая легенда» на той «Аллее Звезд», которую могли бы составить людские недуги. Пожалуй, любому из нас она, как «двойное послание», кажется и по-своему давно знакомой, и по-своему же до сих пор непонятной. Нивелируя маленькие человеческие слабости и сомнения, «большая наука» давно взялась за шизофрению не только со всей особенностью ее психиатрического лечения, но и глубиной, затаенной на уровне генов. Всплеск аналогичного интереса ученых сегодня вызывают и те генетические механизмы, которые скрываются за целым комплексом девиаций, классифицируемых как метаболический синдром. И вот где раскрывается настоящее «исследовательское чутье»: ведь и такие вроде чужеродные напасти, тем не менее, вполне способны пролить свет друг на друга! Например, при сравнительных исследованиях, которые позволяет такой относительно новый метод биомедицины, как полногеномный поиск ассоциаций (GWAS). Именно поэтому и данная статья, помимо «болезненного дуэта», посвящается одному из вероятных прорывов в рамках таких исследований за авторством наших соотечественников: шаг за шагом, «снип за снипом» — генная подоплека метаболического синдрома «выходит из тени».
Конкурс «био/мол/текст»-2018
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2018.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
МикроРНК и атлас: болезни становятся нагляднее
За последние годы ученые успели выяснить, что сбои работы микроРНК приводят к появлению легендарных «голосов в голове» у шизофреников, раскрыли связь таких сбоев с раком, диабетом и другими девиациями [1–4].
Исходя из такой перспективы, международный консорциум FANTOM5 с участием РАН и МФТИ проанализировал сотни ранее неизвестных молекул и составил атлас микроРНК, помогающий прояснить механизмы регуляции генов и роль микроРНК в «историях болезней» того или иного рода. Этот «рисеч-кейс» ценен не только сам по себе — и принципы регуляции генов, и шизофрения с диабетом, и усилия представителей российских университетов в 2018 году складываются во вполне цельную сюжетную линию, один из витков которой мы решили раскрыть подробнее.
ДНК и GWAS: высокая обучаемость сближает с шизофренией?..
Но для начала напомним о таком приеме сегодняшней биомедицины, как GWAS (Genome-Wide Association Studies — «полногеномный поиск ассоциаций») — направлении исследований, основанном на статистике и сравнительном анализе геномных вариантов и фенотипических признаков (рис. 1).
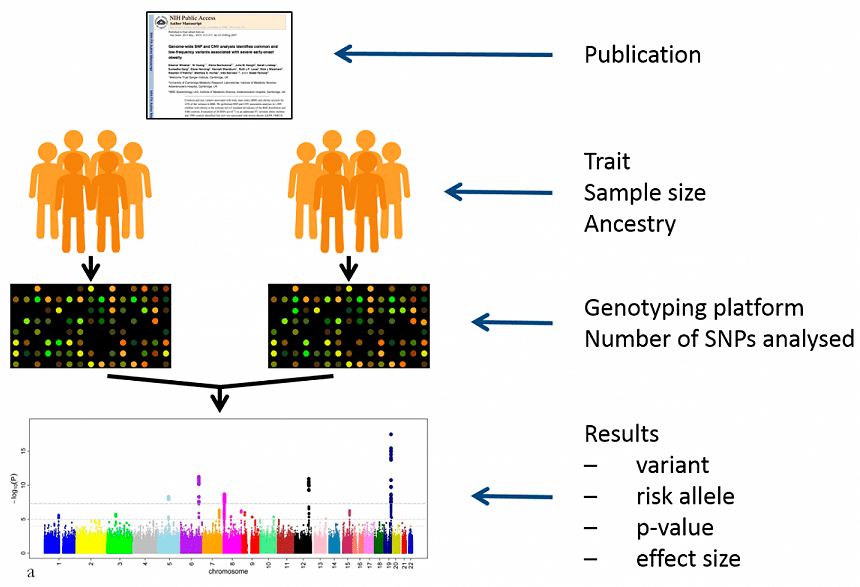
Рисунок 1. Иллюстрация метода GWAS в действии: публикация (вверху) не обходится без выборки, платформы для генотипирования и манхэттенского графика (внизу).
Обычно выборка GWAS весьма обширна и разбивается на две группы: «носителей» определенного заболевания и контрольную. Экспериментальными данными выступают образцы полной ДНК каждого участника выборки. Часто GWAS проводится как поиск связей между заболеваниями и единичными мутациями / различиями аллелей в последовательности ДНК, которые называются однонуклеотидными полиморфизмами (SNP, или снипами).
Подобный анализ генетической предрасположенности к заболеваниям серьезно двигает вперед развитие персональной медицины, но результаты применения GWAS в целом довольно вариативны. Мы уже писали [5] о консорциуме SSGAC, который в 2016 году задействовал метод, чтобы прояснить роль генетики в обучении людей [6]. Тогда ученые нашли статистически значимые корреляции «образованности» не только с ростом когнитивных функций и увеличением внутричерепного объема, но и с выросшим риском биполярных расстройств, а также шизофрении [7]. А другой международный коллектив с участием исследователей из США, Германии и Великобритании выявил связь между серьезными психическими расстройствами и нарушениями иммунитета [8]. Ученые подчеркивают, что среди лиц с психическими расстройствами чаще встречаются аутоиммунные заболевания. Более того, у многих из них наличествует сразу несколько хронических заболеваний данной группы.
...А шизофрения — приближает разгадку метаболического синдрома?
В 2018 году российские ученые из Балтийского федерального университета им. И. Канта, Национального исследовательского Томского политехнического университета и Томского национального исследовательского медицинского центра РАН с коллегами из Германии успешно выявили связь между метаболическим синдромом и геном NOS3 (кодирующим эндотелиальную синтазу оксида азота). И сделали это они — что особо важно в контексте данной статьи — именно при проведении GWAS с группами страдающих не только собственно синдромом, но и шизофренией [9].
- Метаболический синдром
- (далее, для краткости, МС) комплекс гормональных, обменных и клинических нарушений, к признакам которого относятся абдоминальное ожирение, повышенное артериальное давление, гипергликемия. Изучение молекулярно-генетических механизмов МС крайне важно для современной биомедицины по целому ряду причин. Например, из-за его широкого распространения на фоне роста заболеваемости ожирением в мировых масштабах, и вследствие этого же — повышенного риска развития сахарного диабета и сердечно-сосудистых заболеваний.
Исходной предпосылкой в данном случае стал обзор, опубликованный в 2014 году журналом Frontiers in Physiology, — тогда ученые в деталях зафиксировали нарушения всех форм NO-синтазы при метаболическом синдроме [10].
Это отклонение само по себе сегодня очень распространено — в целом ряде стран им страдает уже более 80% населения [2]. При этом синдром — как и смертность из-за сердечно-сосудистых заболеваний — значительно чаще по сравнению с остальным населением отмечают у людей, больных шизофренией.
Поэтому важными для проведения собственной экспериментальной работы россиян оказались исследования зарубежных коллег, опубликованные в 2014 году Journal of Pharmacology. Тогда ученые обратили особое внимание на вероятный защитный характер того влияния, которое оказывает один из снипов NOS3 на развитие МС среди больных шизофренией [7].
Учтя эти нюансы, россияне организовали свое новое исследование в два основных этапа. Последовательность ДНК выявляли у выборки из 515 пациентов, разбитой на четыре группы [9]:
- группа а — больные и шизофренией, и метаболическим синдромом;
- группа б — больные шизофренией;
- группа в — больные метаболическим синдромом;
- группа г — здоровые люди (контрольная группа).
Метаболический синдром определяли на базе критериев, предложенных Международной федерацией диабета (International Diabetes Federation, IDF). Авторы проводили измерения антропометрических, клинических, биохимических параметров и концентраций нитрита в сыворотках крови во всех образцах.
Ученые продемонстрировали связь между функционированием эндотелия (пласта клеток, выстилающего внутреннюю поверхность кровеносных и лимфатических сосудов) и одним из снипов гена NOS3.
Такое пристальное внимание ученых к гену обусловлено тем, что он отвечает за синтез оксида азота в кровеносных сосудах. У пациентов с метаболическим синдромом его производство нарушается, делая невозможной релаксацию мускулатуры в стенках сосудов, что, в свою очередь, приводит к повышению артериального давления и увеличивает риск развития сердечно-сосудистых заболеваний.
«Виновником» оказалась мутация одного звена нуклеотидной цепи — снип Т-786С. Исследование вскрыло взаимосвязь его гаплотипов с повышенным риском возникновения МС (рис. 2).
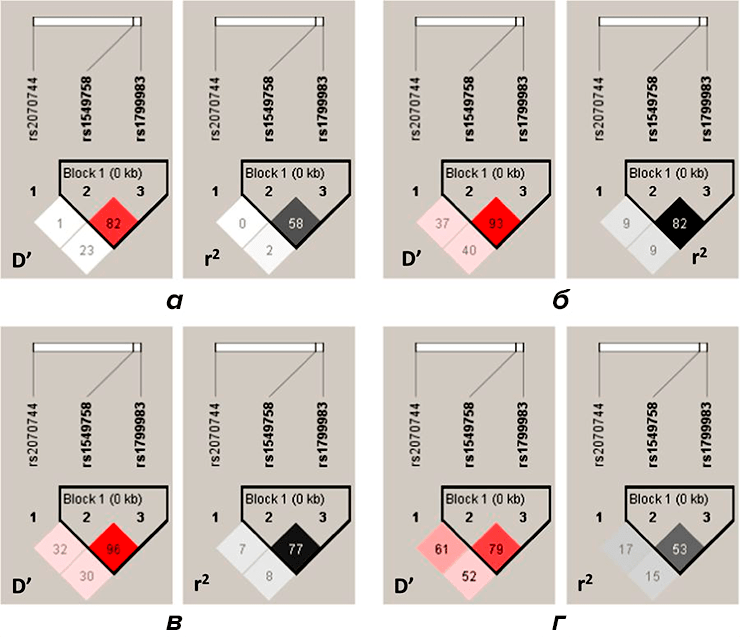
Рисунок 2. Анализ гаплотипов генетических вариантов NOS3 и МС у здоровых людей и пациентов с шизофренией, показывающий положения трех полиморфизмов NOS3 у группы пациентов с МС и шизофренией одновременно (а), пациентов с нормальным весом (б), пациентов с МС (в) и контрольной группы (г).
В процессе: «сегодня GWAS найдет среди снипов ассоциации даже с лебедем, раком и щукой из басни Крылова»
Важно, что это исследование впервые оценило уровни концентрации нитрита у шизофреников с МС и с нормальным индексом массы тела. Сравнив концентрации у двух этих групп (а и б), ученые отметили усиленный — относительно группы б — синтез плазматических нитритов у группы больных обоими заболеваниями [9].
По словам Ларисы Литвиновой — руководителя лаборатории иммунологии и клеточных технологий БФУ, где прошла весомая часть исследований — снип T-786C, наличие или отсутствие которого взаимосвязано с регуляцией уровня холестерина в крови, имеет выраженную защитную роль. Она проявилась в случае группы а и развития МС с ожирением у больных шизофренией: оказывается, за счет усиленного синтеза нитритов этот снип нейтрализует молекулярные вещества, губительные для эндотелия.
При этом свежие данные россиян разошлись с рядом важных предположений предшественников — например, о том, что аллель Т-786C может сохранить эндотелиальное функционирование только у тех пациентов с шизофренией, которые не больны метаболическим синдромом [7].
Помимо T-786C, ученые описали два других полиморфизма NOS3 (C774T и G894T), которые совокупно увеличивают риск нарушения обмена веществ у здоровых людей. Однако общее влияние всех трех мутаций на уровень концентрации нитритов при наличии МС не подтвердилось, как не обнаружилось и доказательств совместного вклада T-786C и G894T в уровень циркуляции нитрита у здоровых людей.
Отсутствие «единства влияния» всех трех снипов на концентрации нитритов подвело авторов к мысли о том, что эти снипы могут «содействовать» МС какими-то другими механизмами.
Снип T-786C пока остается определяющим: ученые последовательно показали, что этот промоторный полиморфизм, влияющий на скорость транскрипции NOS3, связан с холестерином. Обнаруженная связь представляется исследователям именно тем самым механизмом, с помощью которого T-786C провоцирует развитие признаков МС у шизофреников.
В итоге: «ложка дегтя в бочке сахарного диабета», «луч света» на горизонте медицины будущего?
Тем не менее авторы отдельно отмечают предварительность своих результатов. К базовым недостаткам исследования, вероятно, можно причислять и относительно скромную выборку, и отсутствие определенной диеты у испытуемых до взятия крови.
Однако, по мнению специалистов, перспективность дальнейших шагов в данном направлении неоспорима. Сами представители этого исследовательского коллектива продолжают активно изучать тканевую специфику с особенностями развития сахарного диабета. Выявляемые молекулярно-генетические аспекты углеводного обмена могут выступать основанием для выбора лечения и назначения оптимальной фармакотерапии. В 2018 году ученые БФУ уже успели защитить патентом свой способ генетической диагностики риска развития сахарного диабета 2-ого типа.
Возможно, все это уже в ближайшем будущем подведет генную инженерию вплотную к тому, чтобы полностью заглушить довольно мрачную «одышку», неизменно сопровождающую метаболический синдром в его распространении по всему земному шару.
Изначальная версия материала подготовлена для РИА «Новости» при содействии Балтийского федерального университета и непосредственно авторов исследования.
Литература
- Tiffany A. Greenwood, Neal R. Swerdlow, Raquel E. Gur, Kristin S. Cadenhead, Monica E. Calkins, et. al.. (2013). Genome-Wide Linkage Analyses of 12 Endophenotypes for Schizophrenia From the Consortium on the Genetics of Schizophrenia. AJP. 170, 521-532;
- Genovefa D. Kolovou, Katherine K. Anagnostopoulou, Klelia D. Salpea, Dimitri P. Mikhailidis. (2007). The Prevalence of Metabolic Syndrome in Various Populations. The American Journal of the Medical Sciences. 333, 362-371;
- S H Witt, F Streit, M Jungkunz, J Frank, S Awasthi, et. al.. (2017). Genome-wide association study of borderline personality disorder reveals genetic overlap with bipolar disorder, major depression and schizophrenia. Transl Psychiatry. 7, e1155;
- Болезнь потерянных связей;
- GWAS и психогенетика: консорциумы в поисках ассоциаций;
- Aysu Okbay, LifeLines Cohort Study, Bart M L Baselmans, Jan-Emmanuel De Neve, Patrick Turley, et. al.. (2016). Genetic variants associated with subjective well-being, depressive symptoms and neuroticism identified through genome-wide analyses. Nat Genet. 48, 624-633;
- KJ Burghardt, TB Grove, VL Ellingrod. (2014). Endothelial nitric oxide synthetase genetic variants, metabolic syndrome and endothelial function in schizophrenia. J Psychopharmacol. 28, 349-356;
- Daniel S. Tylee, Jiayin Sun, Jonathan L. Hess, Muhammad A. Tahir, Esha Sharma, et. al. Genetic correlations among psychiatric and immune-related phenotypes based on genome-wide association data. — Cold Spring Harbor Laboratory;
- Nikolai Fattakhov, Liudmila Smirnova, Dmitriy Atochin, Daria Parshukova, Daria Skuratovskaia, et. al.. (2018). Haplotype analysis of endothelial nitric oxide synthase (NOS3) genetic variants and metabolic syndrome in healthy subjects and schizophrenia patients. Int J Obes;
- Larisa Litvinova, Dmitriy N. Atochin, Nikolai Fattakhov, Mariia Vasilenko, Pavel Zatolokin, Elena Kirienkova. (2015). Nitric oxide and mitochondria in metabolic syndrome. Front. Physiol.. 6.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





