Между бактериями и археями, окисляющими метан, обнаружена «электропроводка»
22 декабря 2015
Между бактериями и археями, окисляющими метан, обнаружена «электропроводка»
- 931
- 2
- 5
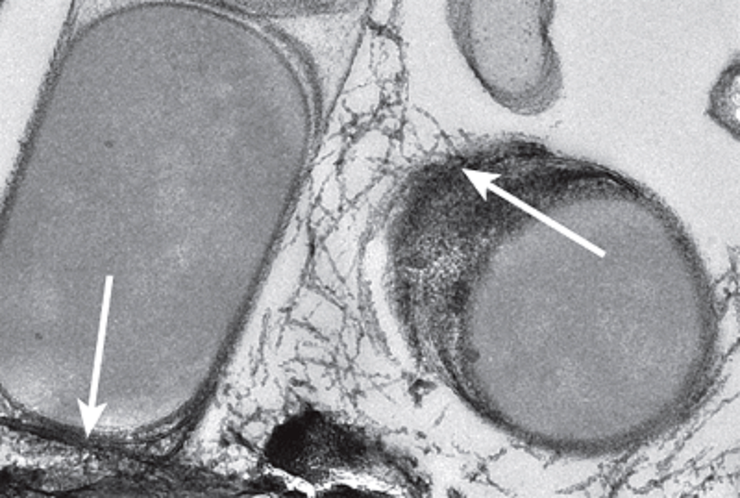
Нанопроводка в микромире.
Рисунок в полном размере.
-
Автор
-
Редакторы
Темы
Чтобы окислять метан, бактериям и археям приходится объединять усилия. Два разных организма проводят необходимые для этого процесса реакции. Из одной стадии в другую, от археи к бактерии должны течь электроны, но до сих пор не было понятно, как именно микроорганизмы их друг другу передают. Теперь выяснилось, что напрямую — по своеобразным биопроводам.
Общественная жизнь микроорганизмов очень развита — одноклеточные существа могут обмениваться метаболитами, а среди бактерий очень распространена прямая передача генов (горизонтальный перенос) [1]. Но недавно в бактериальных сообществах обнаружили еще более экзотический способ отношений — передачу электронов [2]. Электрические импульсы, как известно, могут течь и по нейронным цепочкам многоклеточных, однако в их случае никакого переноса заряженных частиц между клетками цепочки не происходит. Нейрон, по которому пришел электрический сигнал, посылает следующему нейрону сигнальные молекулы [3], благодаря которым в нём тоже возникает возбуждение. При этом электрический ток хотя и идет по цепочке, но прерывается в каждом месте контакта нервных клеток. А бактерии, как оказалось, могут непосредственно передавать друг другу электроны, так что между микроорганизмами возникает настоящий ток.
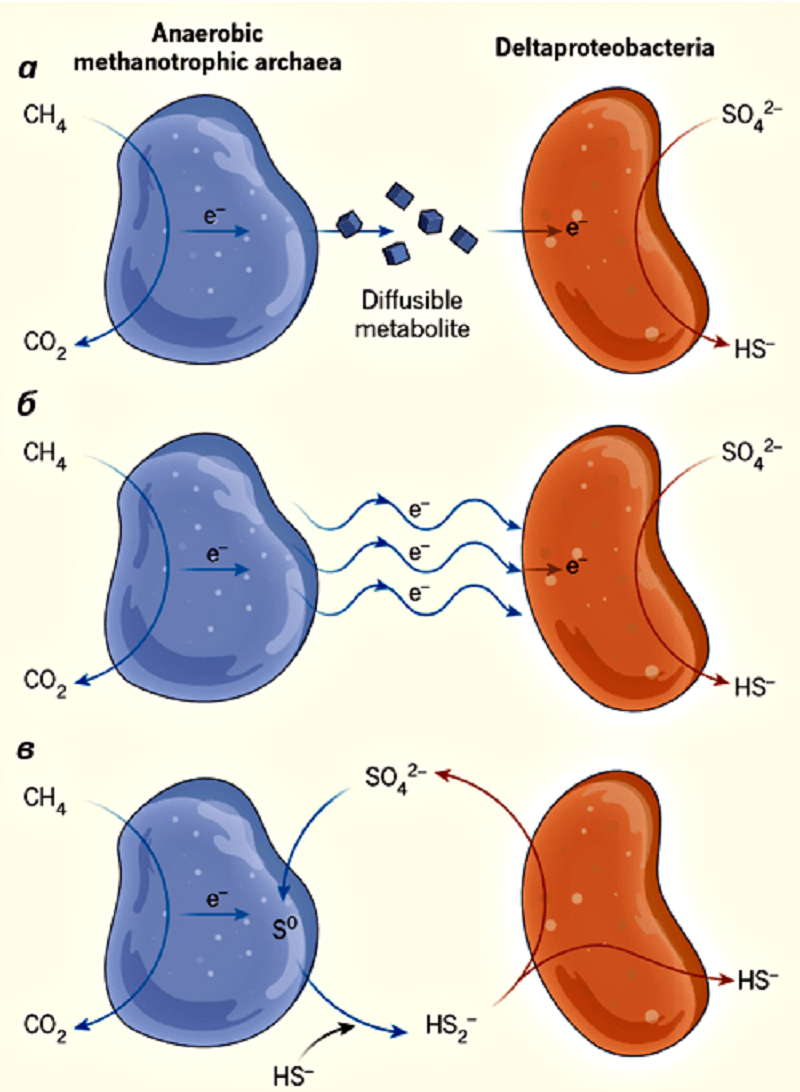
Рисунок 1. Археи, способные окислить метан до углекислого газа, и бактерии, способные восстановить сульфат до сульфида, нужны друг другу. Эти процессы можно провести с «выигрышем» энергии, только если археи будут сбрасывать бактериям электроны, образовавшиеся в процессе окисления метана. На рисунке показаны теоретические варианты кооперации бактерий и архей: a — передача электронов в составе молекул, б — передача электронов напрямую, в — восстановление сульфата до нейтрально заряженной серы и ее передача. Оказалось, что все восстановленные молекулы, кроме водорода, бактериям никак не помогают, но водород ингибирует окисление метана и потому не подходит для коммуникации микроорганизмов (при этом восстанавливать сульфат сами археи никак не могут). Остается прямой транспорт электронов.
Пример такой живой проводки обнаружился на дне океана — в сообществах окисляющих метан прокариот. Окисляясь, метан превращается в углекислый газ, а образующиеся в ходе этого процесса электроны необходимо куда-то пристроить, чтобы поддерживать ход процесса в этом направлении. Окисление метана будет приносить скромную энергетическую прибыль только в том случае, если будет сопряжено с выгодным присоединением электронов к достаточно окисленным молекулам. Подходящий вариант — восстановление сульфата до серы или сульфида — доступен бактериям группы сульфатредукторов. А микроорганизмы, окисляющие метан, не способны образовывать ферменты для восстановления сульфата. Поэтому было понятно, почему бактериальные сообщества, живущие у источников метана, состоят из двух типов микроорганизмов. Метанокисляющим археям этих сообществ удается использовать этот скудный источник энергии, но только если другие бактерии помогают им вести процесс, постоянно забирая и утилизируя образующиеся электроны [4]. Схема выглядела разумно, но было непонятно, как она реализуется на практике (рис. 1).
Микроорганизмы часто передают друг другу восстановительные эквиваленты — те же электроны, но в составе молекул, из которых электроны можно в нужный момент извлекать. С нейтрально заряженными молекулами обычно удобнее иметь дело — они не склонны реагировать со всем, что попадется на пути. Поэтому, исследуя работу микробных сообществ, живущих за счет окисления метана, ученые стали в первую очередь искать между микробами потоки восстановленных метаболитов. На эту роль подходит много молекул-кандидатов, и найти подходящую можно, если с ее помощью удастся заменить бактериям — акцепторам электронов коллег по сообществу. Исследователи перепробовали много молекул, и оказалось, что только водород может заменить сульфатредукторам их метанокисляющих товарищей: только при добавлении водорода сульфатредукторы могли приступить к своему любимому восстановлению сульфата, остальные типы восстановленных молекул им не подходили.
Однако оказалось, что метанокисляющие археи не выделяют водород в таких количествах, чтобы за счет него обеспечить своим товарищам нормальный уровень восстановления сульфата. Более того, водород подавляет процесс окисления метана, и как только он появляется в среде в достаточных количествах, сообщество перестает перерабатывать метан. Значит, использовать водород как сигнальную молекулу окисляющие метан археи никак не могут. Против использования каких-либо выделяемых во внешнюю среду молекул говорило и отсутствие зависимости эффективности, с которой сообщество окисляет метан, от расстояний между микроорганизмами. Если бы клетки передавали друг другу электроны в составе молекул, которые должны были бы диффундировать между ними в воде, эффективность процесса окисления резко падала бы с расстоянием между членами сообщества.
Итак, микроорганизмы несомненно как-то передавали друг другу электроны, но при этом было неважно, какое расстояние разделяет их клетки. Оставалось только предположить, что между членами сообщества есть «проводка» , по которой электроны идут напрямую [5]. Что самое интересное, ученым даже удалось увидеть эту проводку (рис. 2). Она состояла из трубочек диаметром 10 нм и длиной более 1 мкм и представляла собой выросты сульфатредукторов, образующиеся только при совместном росте бактерий с коллегами, окисляющими метан. У обоих участников сообщества обнаружились гены, кодирующие внеклеточные цитохромы. Эти белки используются для передачи электронов в процессе клеточного дыхания. Активность генов этих цитохромов у участников сообщества усиливалась по мере роста активности генов, необходимых для окисления метана и восстановления сульфата. Вероятно, молекулы цитохромов располагаются на выростах сульфатредукторов, а также в местах контактов выростов с поверхностями метанокисляющих архей, и по цепочке этих белков электроны переходят от одной клетки к другой.
То, что для бактериальных пилей характерна проводимость металлического типа, было подтверждено в оригинальном эксперименте с бактерией Geobacter sulfurreducens: «Металлическая проводимость биологических структур» [6]. К вящей радости творцов биоэлектронных устройств, оказалось, что проводимостью «пилевых» нанопроводов можно управлять. — Ред.
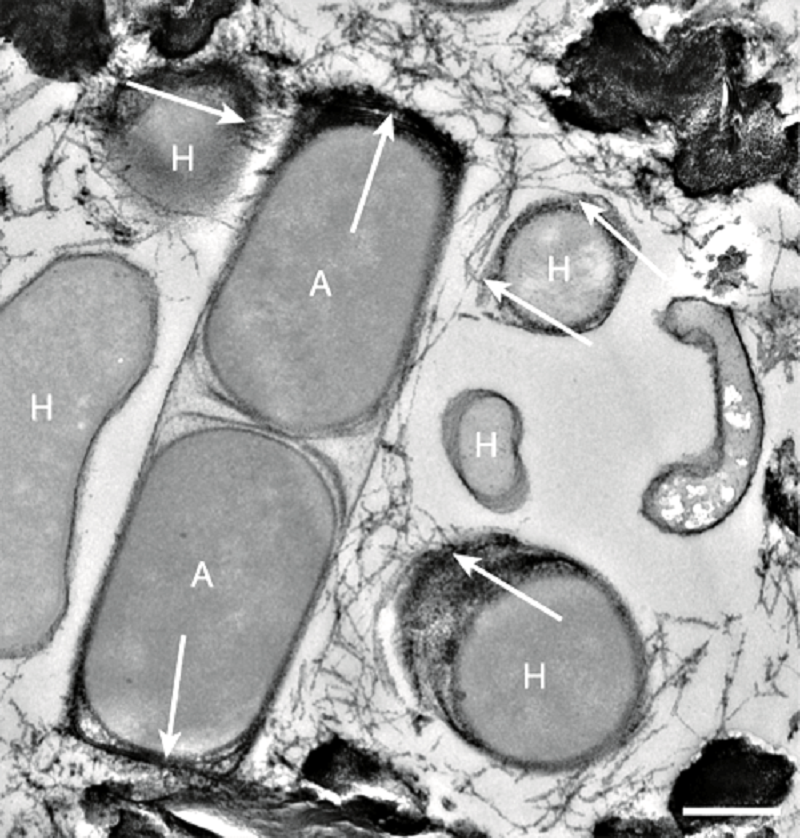
Рисунок 2. «Электропроводка» образуется между бактериями и археями, совместно окисляющими метан. К «источнику тока» подключается бактерия. Масштабная линейка — 300 нм.
Прокариоты не устают удивлять ученых богатством своих возможностей. В случае с окислением метана им, вероятно, не оставалось ничего другого, кроме как изобрести способ передавать друг другу электроны напрямую, потому что в присутствии восстановленных молекул процесс окисления метана может либо подавляться, либо становиться невыгодным. Совместно окисляющие метан сообщества прокариот — интересный пример гибкости микроорганизмов, способных на пути к выживанию решить самые фундаментальные проблемы. Последующие микробиологические исследования прямой передачи электронов покажут, насколько распространен этот интересный способ взаимодействия в мире прокариот.
Литература
- Мобильные генетические элементы прокариот: стратификация «общества» бродяжек и домоседов;
- Тысячекратная полиплоидия гигантской бактерии Epulopiscium;
- Как происходит выделение нейромедиатора;
- Michael Wagner. (2015). Conductive consortia. Nature. 526, 513-514;
- Gunter Wegener, Viola Krukenberg, Dietmar Riedel, Halina E. Tegetmeyer, Antje Boetius. (2015). Intercellular wiring enables electron transfer between methanotrophic archaea and bacteria. Nature. 526, 587-590;
- Металлическая проводимость биологических структур.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚