
Объяснена различная вирулентность вирусов гриппа — возбудителей «испанки»
28 февраля 2008
Объяснена различная вирулентность вирусов гриппа — возбудителей «испанки»
- 18956
- 18
- 6
На картине «Семья» умирающий художник Эгон Шиле (1890–1918 гг.) изобразил трёх жертв «испанки» — себя, свою беременную жену и её нерождённого ребёнка. (Масло, холст.)
-
Автор
-
Редактор
В 1918–1919 годах пандемия гриппа — «испанки» — унесла, по меньшей мере, 20–50 миллионов жизней. Болезнь была вызвана особым штаммом вируса H1N1, предположительно произошедшим от вируса, распространённого среди диких птиц. Недавно выяснено, что такая «пересадка» вируса с животных на человека была обусловлена мутацией всего двух остатков в гемагглютинине — белке оболочки вируса, участвующего в заражении. Изучив структурные особенности «взлома» гликорецепторов эпителия дыхательных путей человека гемагглютининами различных штаммов вируса, учёные объясняют биохимию этого трагического «нашествия».
Пандемия гриппа-«испанки» [1] прогремевшая по всей земле в 1918–1919 годах и унесшая около 50 миллионов человеческих жизней, была вызвана вирусом гриппа серотипа N1H1 (для объяснения классификации см. врезку), «перекинувшегося» с диких птиц — своих природных носителей — на человека. Случившись однажды, такое может случиться и теперь: ведь уже известны случаи (в том числе и смертельные) заражения людей «более современной» модификацией птичьего гриппа — H5N1, зарегистрированного преимущественно в восточной Азии. До сих пор эти случаи заражения не перешли в эпидемию, однако чтобы встретить опасность во всеоружии, необходимо знать механизм, который однажды превратил вполне безопасный для человека вирус в настоящую угрозу всему человечеству.
Ключевой этап заражения вирусом гриппа — связывание белка вирусной оболочки гемагглютинина (ГА) с сиалогликорецепторами на поверхности клеток дыхательного эпителия организма-носителя. (Сиалогликорецепторами будем называть интегральные мембранные рецепторы, модифицированные олигосахаридными молекулами, в частности — остатками сиаловой кислоты.) Вслед за связыванием гемагглютинин «вскрывает» мембрану эпителиальной клетки, и содержимое вирусной капсулы переходит в заражаемую клетку.
Считается, что передача вируса от птиц людям обусловлена адаптацией гемагглютинина вируса «птичьего» штамма к гликанам (углеводным составляющим сиалогликорецепторов) человеческих клеток, а именно — «переключением» с α2–3 сиалогликанов («птичий тип») на отличающиеся типом гликозидной связи α2–6 сиалогликаны («человеческий тип»), преобладающие на поверхности эпителиальных клеток верхних дыхательных путей человека.
Учёным из Массачусетского технологического института удалось связать топологию углеводов на поверхности сиалогликорецепторов со способностью взаимодействовать с гемагглютининами из различных штаммов вируса [3], а также дать биохимическое объяснение распространению птичьего вируса гриппа среди людей, ставшего причиной трагедии 1918-го [4]. Оказалось, что способность связываться (а, значит, и заражать) с «человеческими» α2–6 рецепторами появилась у штамма H1N1 вируса птичьего гриппа после... всего двух мутаций в молекуле гемагглютинина. «Сродство вирусного гемагглютинина к человеческим сиалогликорецепторам, судя по всему, — важнейшая составляющая вирулентности. Две мутации драматическим образом влияют на сродство гемагглютинина к рецепторам, находящимся в верхних дыхательных путях человека», — говорит Рэм Сасисекаран (Ram Sasisekharan), ведущий автор обеих публикаций.
Изучив структурные особенности гликанов в α2–3 и α2–6 рецепторах, исследователи пришли к выводу, что гликан на поверхности рецептора может находиться в разных топологических формах: «конусоподобной» — когда «разрешённая» область для углеводных цепей описывается конусом) — и «зонтикообразной» — когда вытянутые углеводные цепи могут разворачиваться шире, наподобие раскрытого зонтика (рис. 2). Одним из главных наблюдений стало, что «конусоподобная» форма характерна для α2–3 рецепторов (что связано с топологией 2–3-гликозидной связи) и для α2–6 рецепторов с короткой углеводной цепью. В α2–6 рецепторах с более длинной цепью (>4 углеводных остатков) гликан приобретает «зонтикообразную» форму, отличающуюся способом связывания с гемагглютинином.
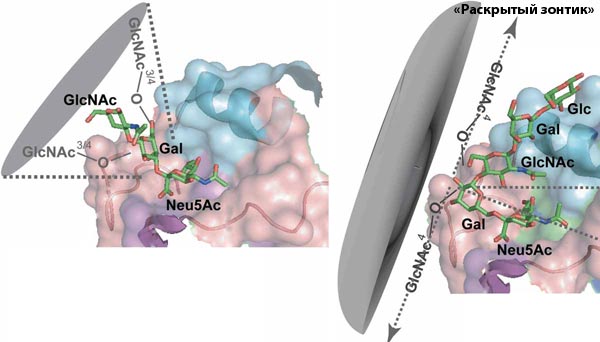
Рисунок 2. «Конусообразная» (слева) и «зонтикоподобная» (справа) топологии α2–3 и α2–6 сиалогликанов. Соответствующая топология определяется торсионными углами в трисахаридах Neu5Ac-α2–3-Gal-β1–3/4-GlcNAc и Neu5Ac-α2–6-Gal-β1–4-GlcNAc (где Neu5Ac — N-ацетилнейраминовая кислота, Gal — галактоза и GlcNAc — N-ацетилглюкозамин). Конформационный анализ этих трипептидов подтверждает, что для α2–3-молекулы характерная только «конусообразная» форма гликана (этому способствует сама геометрия 2–3-гликозидной связи), а α2–6-молекулы могут принимать обе формы (топология «раскрытого зонтика» характерна для сравнительно длинных олигосахаридов (>4 углеводных остатков)).
Учёные называют найденное различие основной причиной, по которой птичий вирус гриппа не может (пока ещё?) «перекинуться» на человека. В специализированном эксперименте исследователи изучили связывание гемагглютининов различных типов с сиалосахаридами типов α2–3 и α2–6. «Птичий» гемагглютинин из штаммов H1N1, H3N8 и H5N3 практически не связывался с α2–6-гликанами, отлично взаимодействуя с «родным» для себя α2–3 типом; гемагглютинины человеческих вирусов связывались с обоими типами гликанов, отдавая «предпочтение» молекулам с «зонтикоподобной» топологией — то есть, α2–6-гликанам со сравнительно длинной углеводной цепью. Основываясь на этих наблюдениях, учёные делают вывод, что «человеческие» гемагглютинины H1 и H3 произошли от своих «птичьих» предков, приобретя способность эффективно взаимодействовать с «зонтикоподобными» α2–6 рецепторами и, следовательно, заражать людей.
Установив, как топология углеводной «шапки» сиалогликорецепторов влияет на связывание с гемагглютинином, исследователи сосредоточились на сравнении вирулентности нескольких штаммов вируса гриппа, существовавших во время пандемии 1918–1919 гг. и различающихся только гемагглютинином — что чрезвычайно удобно для такого исследования [4]. Вирулентность изучали на хорьках — обнаружилось, что их дыхательный эпителий устроен практически так же, как и человеческий — с точки зрения распространённости сиалогликорецепторов. В работе сравниваются:
- «тот самый» A/South Carolina/1/1918 (SC18), крайне заразный для человека и селективно связывающийся с α2–6-рецепторами с длинными углеводными цепями;
- NY18, ГА которого отличается от SC18 лишь одним аминокислотным остатком, слабо вирулентный и демонстрирующий смешанное α2–3/6 связывание, и
- AV18, содержащий две мутации в ГА (ещё одну, кроме аналогичной в NY18), не опасный для человека — видимо, по причине неспособности связываться с α2–6-рецепторами (избирательно связывается с α2–3-типом).
Чтобы понять структурный механизм, обуславливающий избирательность взаимодействия гемагглютининов с гликанами рецепторов, исследователи основывались на уже существующих кристаллографических структурах H1-ГА в комплексе с гликанами [5]. Анализ комплексов показал, что гемагглютинин штамма SC18 идеально подходит для связывания гликана в топологии α2–6 (рис. 3А) — образуя специфические взаимодействия как с его «базовой» областью (или областью «рукояти зонтика»), так и в «распрямлённой» области. По сравнению с наиболее вирулентным штаммом, комплекс NY18-ГА с гликаном отличается отсутствием специфического стабилизирующего взаимодействия с ASP225 (в NY18 этот остаток заменён на GLY, см. рис. 2Б, Г) в области «базы». AV18-ГА содержит ещё одну мутацию: ASP190GLU, которая заключается в потере ещё одной ключевой точки контакта с гликаном — на этот раз, с распрямлённой областью (рис. 3В) — что, видимо, является, причиной того, что AV18-ГА избирательно связывает «конусообразные» гликаны α2–3 «птичьих» рецепторов (и «коротких» α2–6-рецепторов), но не имеет сродства к «длинным» α2–6 гликанам, топологически организованным на манер «зонтика».
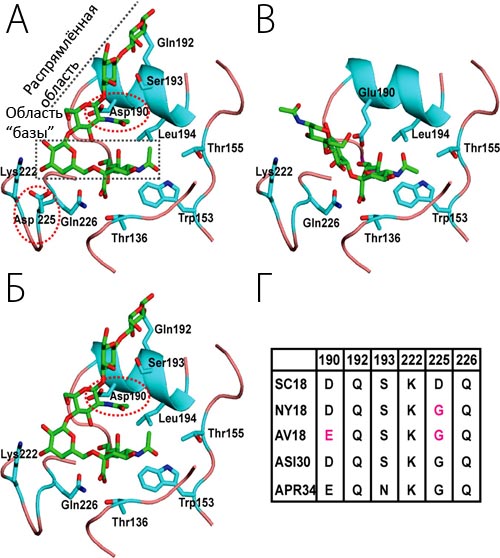
Рисунок 3. Молекулярные взаимодействия гемагглютининов вируса гриппа штаммов SC18, NY18 и AV18 (голубым цветом) с гликанами в топологии α2–3 и α2–6 (зелёным цветом). В сайте связывания гликанов на поверхности гемагглютинина показаны важнейшие остатки, включая «якорную» область для N-ацетилнейраминовой кислоты олигосахарида (T136, W153, T155 и L194). Консервативные остатки K222 и Q226 обеспечивают фиксацию остатка галактозы в «базовой» области. А — Взаимодействие SC18-ГА с длинноцепочечным α2–6 олигосахаридом в «зонтикоподобной» топологии. Остатки K222, D225 и Q226 стабилизируют молекулу гликана в «базовой» области, а D190, Q192 и S193 — в области распрямления молекулы (область «раскрытого зонтика»). Б — В случае комплекса NY18-ГА с длинной α2–6 молекулой заметно отсутствие стабилизирующего «базовую» область контакта с D225 (по сравнению с SC18 на А). В — Взаимодействие AV18-ГА с α2–3 гликаном с конической топологией отличается от механизма связывания на А и Б. Остатки E190 и Q226 оптимально координируют олигосахарид в конической топологии. Г — Сравнение ключевых аминокислотных остатков гемагглютининов Sc18, NY18 и AV18 (нумерация на всём рисунке дана по H1N1-ГА). Цветом выделены мутации NY18 и AV18 по сравнению со штаммом SC18.
Проделанная работа позволяет понять, как именно всего две мутации в безопасном для человека вирусе стоили миллионов человеческих жизней. Однако цена, заплаченная за адаптацию «птичьего» H1N1 вируса, ставшего для выживших после пандемии 1918-го уже «человеческим», может быть запрошена вновь: аналогичные адаптации могут произойти и с естественной популяцией современного птичьего вируса H5N1, пока очень слабо распространяющегося среди людей. Проделанная работа послужит основой мониторинга природных очагов вируса птичьего гриппа на предмет того, не появилась ли у них способность к «пересадке» на человека, которая может привести к новой пандемии.
Литература
- Википедия: «Испанский грипп»;
- Википедия: «Грипп»;
- Aarthi Chandrasekaran, Aravind Srinivasan, Rahul Raman, Karthik Viswanathan, S Raguram, et. al.. (2008). Glycan topology determines human adaptation of avian H5N1 virus hemagglutinin. Nat Biotechnol. 26, 107-113;
- A. Srinivasan, K. Viswanathan, R. Raman, A. Chandrasekaran, S. Raguram, et. al.. (2008). Quantitative biochemical rationale for differences in transmissibility of 1918 pandemic influenza A viruses. Proceedings of the National Academy of Sciences. 105, 2800-2805;
- S. J. Gamblin. (2004). The Structure and Receptor Binding Properties of the 1918 Influenza Hemagglutinin. Science. 303, 1838-1842.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




