
«Осторожно, двери закрываются! Следующая станция — внешняя среда» или бактериальные системы секреции
31 марта 2026
«Осторожно, двери закрываются! Следующая станция — внешняя среда» или бактериальные системы секреции
- 161
- 0
- 1
Бактерии могут поставлять во внешнюю среду различные белковые молекулы с помощью специализированных систем секреции.
рисунок автора статьи
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Бактерии всегда окружены большим количеством различных молекул. Одни нужны для «коммуникации» с другими бактериями и формирования биопленок, вторые — для подавления роста конкурентов, третьи — для поражения эукариотических клеток и процесса инфекции. Они невероятно разнообразны как по структуре, так и по своим функциям. Но возникает вопрос, как же они проходят бактериальные мембраны и попадают во внешнюю среду?
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Транспорт различных веществ жизненно необходим для любой клетки, и бактерии — не исключение. Как мы все прекрасно знаем, в строении бактериальных клеток, помимо мембраны, присутствует еще и клеточная стенка. В зависимости от ее организации, бактерии делятся на грамположительных и грамотрицательных. Первые окрашиваются кристаллвиолетом из-за того, что краситель не вымывается из толстого слоя пептидогликана. Вторые же при промывке спиртом утрачивают краситель, а потом их окрашивают фуксином или сафранином. Для них характерно наличие тонкого слоя пептидогликана и внешней мембраны [1]. Очевидно, что как и в первом, так и во втором случае, никакая молекула сама не сможет преодолеть такие сложные структуры. Как же тогда осуществляется транспорт?
В бактериальных клетках функционируют специализированные системы секреции. Основная их функция — транспорт веществ из клетки в окружающую среду. Причины могут быть различны: «коммуникация» с другими бактериями (например, конъюгация при горизонтальном переносе генов) или же наоборот — конкуренция. Кроме того, системы секреции играют большую роль и в патогенезе. Секретируемые вещества могут использоваться для подавления иммунного ответа организма-хозяина. Особо интересна роль систем секреции в грамположительных бактериях, которую мы чуть позже рассмотрим в этой статье. Важно отметить, что под транспортом подразумевают транспорт именно во внешнюю среду. У грамположительных бактерий веществам необходимо преодолеть одну мембрану и клеточную стенку, а у грамотрицательных — еще и внешнюю мембрану.
Впервые системы секреции были обнаружены у грамотрицательных бактерий: Escherichia coli, Neisseria gonorrhoea, Klebsiella pneumoniae, Yersinia enterocolitica и Pseudomonas aeruginosa. Пути секреции у этих бактерий настолько сильно различались, что казалось, что у каждой бактерии должен быть свой неповторимый механизм. Однако вскоре выяснилось, что у Klebsiella pneumoniae белки PulL и PulM, участвующие в секреции пуллулуназы (фермента, гидролизующего крахмал), гомологичны белкам XcpY и XcpZ Pseudomonas aeruginosa. У Pseudomonas aeruginosa система Xcp участвует в транспорте различных веществ, например, экзотоксина А, фосфолипазы, щелочной фосфатазы. Таким образом, стало понятно, что идея об уникальном механизме для каждого вида бактерий неправильна. А системы секреции вполне можно разделить на конкретные группы. Так, приведенную в пример систему Pul/Xcp отнесли к типу II или Т2SS. Секрецию гемолизина у E. coli — к типу I (T1SS), IgA у Klebsiella pneumoniae — к типу V (T5SS) [2]. Далее мы детально разберем строение и особенности основных существующих типов систем секреции.
Система секреции T1SS
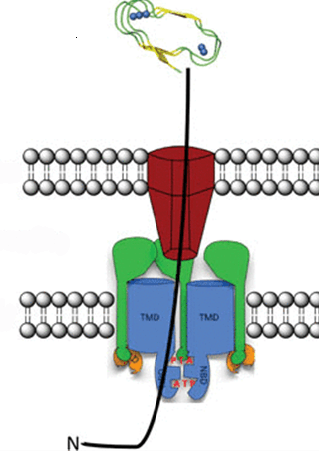
Рисунок 1. Строение T1SS на примере системы секреции гемолизина А у Escherichia coli.
Гемолизин взаимодействует с HlyB — ABC транспортером (окрашен синим) и HlyD — MFP (окрашен зеленым). Формируется канал, через который синтезирующаяся молекула начинает выходить во внешнюю среду. HlyD отвечает за взаимодействие этой конструкции с компонентом внешней мембраны — TolC (окрашен красным). В результате, гемолизин выходит во внешнюю среду, минуя периплазматическое пространство.
Система секреции T1SS — один из самых распространенных типов систем секреции среди грамотрицательных бактерий, включая патогенов. С их помощью секретируются адгезины, липазы, протеазы и различные токсины. Главная особенность этой системы заключается в том, что вещества преодолевают обе мембраны фактически за один раз, то есть без образования промежуточных продуктов в периплазматическом пространстве. Хотя существуют и исключения, при которых промежуточные продукты все-таки образуются.
Классический пример системы секреции T1SS — система секреции гемолизина у Escherichia coli. Это первая и наиболее детально описанная система этого типа. Гемолизин А белок, обладающий гемолитическими и цитотоксическими свойствами. Он экспрессируетсв больших количествах при инфекции мочевыводящих путей уропатогенными штаммами Escherichia coli (UPEC) [3]. Интересно, что изначально гемолизин А синтезируется в неактивной, нетоксичной форме. Для его перехода в активную форму необходима посттрансляционная модификация — ацилирование, которое осуществляет ацилтрансфераза HlyC [4]. Такой интересный механизм наблюдается не только у гемолизина А, но и у других белков семейства RTX (сокращение от repeats in toxin). У семейства такое название, потому что для всех его белков характерно наличие повторов глицина и аспартата на С-концевом домене. Интересно, что активация после синтеза требуется только для токсинов грамотрицательных бактерий. Токсины грамположительных бактерий синтезируются сразу в готовой форме. Гемолизин А обладает массо110 кДа. Но известно, что системы секреции этого типа способны транспортировать субстраты совершенно различных размеров, начиная от 20 кДа (HasA из Serratia marcescens [5]) и заканчивая огромным адгезионным белком массой в 900 кДа (LapA из Pseudomonas fluorescens [6]).
Итак, процесс секреции HlyA начинается, конечно же, с синтеза субстрата на рибосоме. Интересно, что непосредственно секреция начинается с того момента, как на C концевом домене белка появляются всего 50–100 аминокислот. На этом этапе возникает вопрос, почему синтезированное вещество не успевает подвергнуться деградации до того, как будет транспортировано во внешнюю среду. Но, к сожалению, ответа на этот вопрос пока не найдено. После начала синтеза белок взаимодействует с двумя белками внутренней мембраны — ABC транспортером и MFP (membrane fusion proteins) [7]. В системе секреции гемолизина А в качестве ABC транспортера участвует HlyB, MPF — HlyD. Формируется канал, через который синтезируемая молекула начинает выходить во внешнюю среду. HlyD отвечает за взаимодействие этой конструкции с компонентом внешней мембраны — TolC (рис. 1). Такая структура позволяет веществу преодолеть периплазматическое пространство без выхода в него (рис.) [8].
Перед тем, как перейти к следующей системе секреции, нужно разобраться, как молекулы могут преодолевать цитоплазматическую мембрану. В случае с T1SS никакого дополнительного механизма не требуется. Однако T2SS, T5SS, T8SS и T9SS работают по двустадийному принципу. Молекулы сначала выходят в периплазматическое пространство, а потом уже происходит взаимодействие с конкретной системой. Итак, перенос субстрата через цитоплазматическую мембрану осуществляет либо система Sec, либо Tat.
Системы Sec и Tat
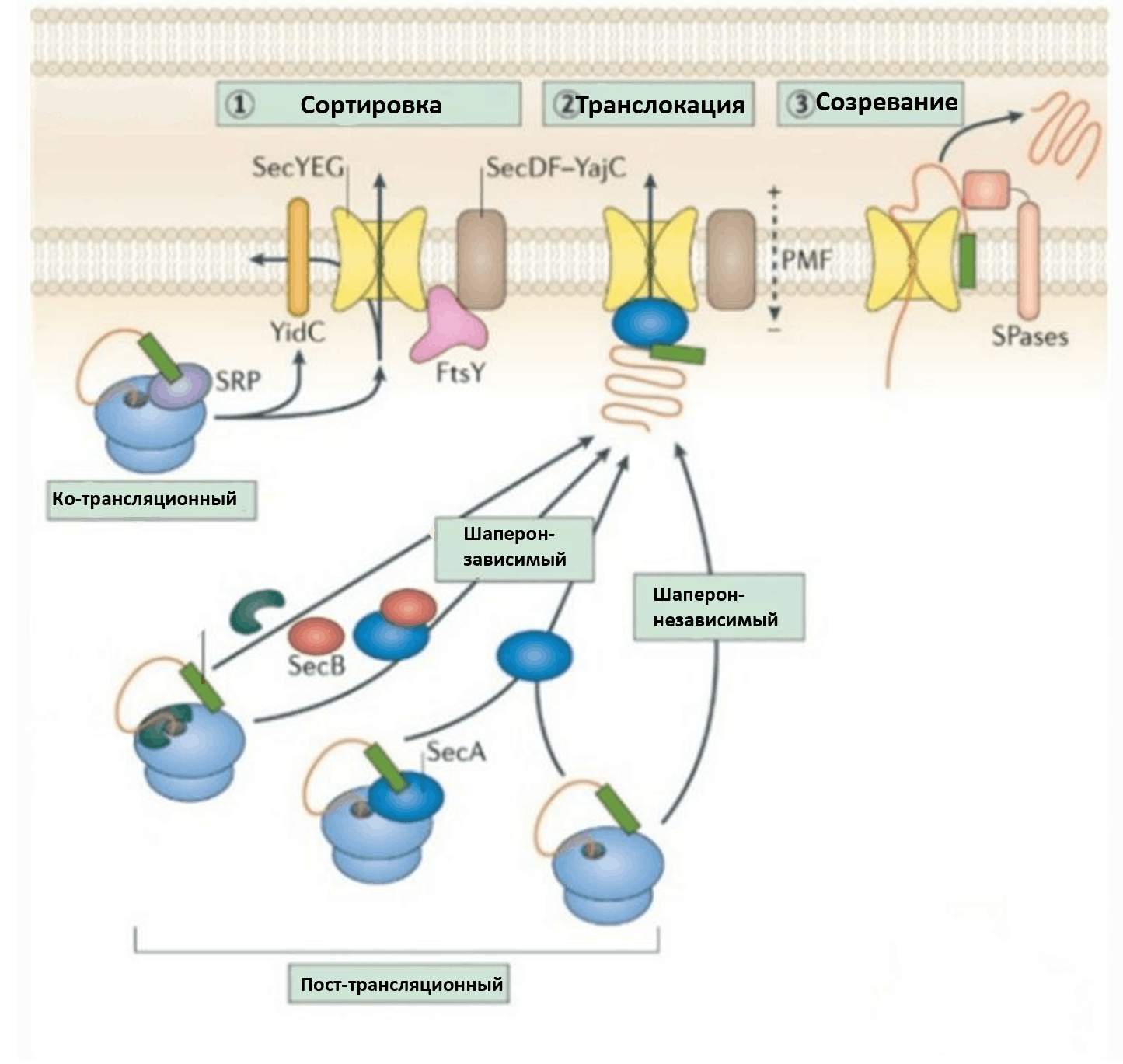
Рисунок 2. Схема работы системы секреции Sec.
Существует два варианта работы системы Sec: белки транспортируются либо сразу с начала их синтеза, либо уже в полностью готовой форме. В первом случае после распознавания сигнальной последовательности белка частицей SRP, он направляется к транспортеру SecYEG. Во втором случае шаперон SecB не дает белку свернуться, а SecA обеспечивает энергией процесс его переноса через комплекс SecYEG в периплазматическое пространство.
Начнем рассмотрение способов переноса молекул через цитоплазматическую мембрану с системы Sec. Белки могут транспортироваться либо сразу с начала их синтеза, либо уже в полностью синтезированном варианте. В первом случае сигнальная последовательность белка распознается частицей SRP, которая направляет белок к транспортеру SecYEG. Во втором случае шаперон SecB не дает белку свернуться, а SecA обеспечивает энергией процесс его переноса через тот же SecYEG (рис. 2). В периплазме уже происходит правильное сворачивание белка и некоторые дополнительные модификации [9].
В отличие от системы Sec, через систему Tat происходит секреция уже свернутых белков. Еще интересно отметить, что для ее работы не нужна АТФ. Работа системы начинается со связывания целевого белка с комплексом TatB/TatC. Сигнальная последовательность, с помощью которой белок узнается мембранным комплексом, представляет собой два остатка аргинина. Далее с помощью протонного градиента происходит полимеризация TatA и формирование канала (рис. 3). Через него свернутый целевой белок выходит в периплазматическое пространство [10].
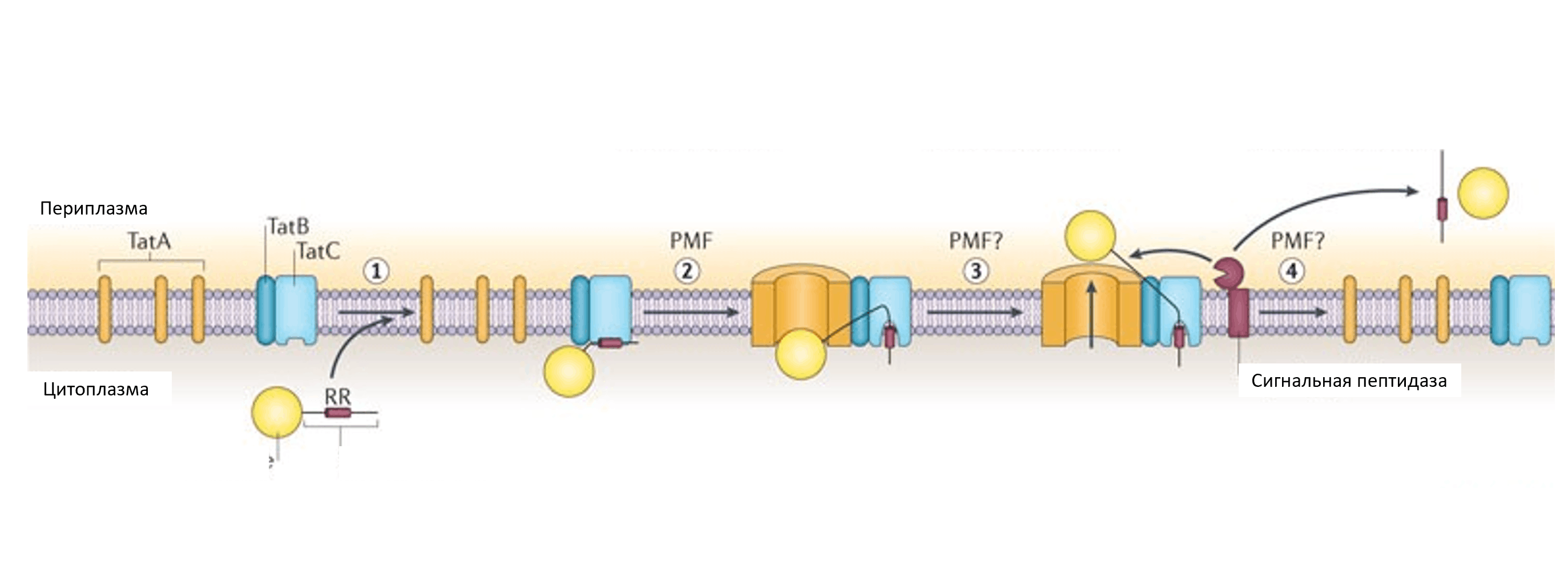
Рисунок 3. Схема работы системы секреции Tat. Сначала происходит узнавание сигнальной последовательности целевого белка комплексом TatB/TatC и связывание с ним. Далее с помощью протонного градиента идет процесс полимеризации TatA, и формируется канал. Через него свернутый целевой белок выходит в периплазматическое пространство.
T2SS
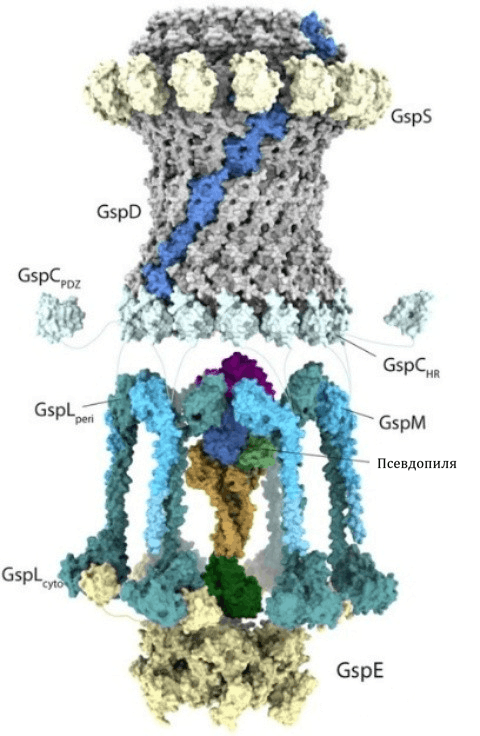
Рисунок 4. Строение системы секреции T2SS.
T2SS состоит из основных 4 белковых комплексов. Один из них образует пору для выхода субстрата располагается на внешней мембране (GspD). Второй — на внутренней мембране, его главная функция — связь с комплексом внешней мембраны (состоит из GspL, GspM). АТФаза GspE осуществляет выработку энергии, необходимую для транспортировки субстрата. Псевдопиля состоит из различных белков псевдопилинов и работает как поршень. В результате, белки выталкиваются во внешнюю среду.
Система секреции T2SS широко распространена у представителей альфа-, бета-, гамма-, дельтапротеобактерий, Bacteroidetes, Deferribacteres. Она является одним из факторов вирулентности патогенов человека группы ESKAPE. Такое название дано по первым буквам наименований ее представителей: Enterococcus faecium, Staphylococcus aureus, Klebsiella pneumoniae, Acinetobacter baumannii, Pseudomonas aeruginosa и Enterobacter sp. ESKAPE опасны своей высокой множественной устойчивостью к различным группам антибиотиков. Обычно с ними связывают внутрибольничные инфекции [11]. Было показано, что у микроорганизмов, мутантных по T2SS , существенно снижается вирулентность. Работа этой системы приводит к гибели клеток организма-хозяина, нарушает работу системы комплемента и подавляет врожденный иммунитет. Кроме того, увеличивается адгезия к эпителиальным клеткама некоторые вещества способствуют образованию биопленок [12].
Данная система секреции характерна для широкого круга патогенов. Так, помимо группы ESKAPE T2SS участвует в секреции холерного токсина у Vibrio cholerae и секреции энтеротоксина у Escherichia coli. Выше были упомянуты, в основном, патогены человека, но T2SS характерна и для фитопатогенов — патогенов растений. К ним относятся такие микроорганизмы, как Burkholderia gladioli, Erwinia amylovora и Xanthomonas campestris. Burkholderia gladioli поражает плодовые деревья, а Erwinia amylovora и Xanthomonas campestris — важные сельскохозяйственные культуры [13]. Из всего вышеописанного у вас может сложиться впечатление, что T2SS характерна только для патогенов и участвует исключительно в инфекционных процессах. Но это совсем не так. T2SS может использоваться и для поддержания симбиотических связей между микроорганизмом и каким-либо макроорганизмом. Интересный пример — симбиоз Aeromonas veronii и медицинской пиявки Hirudo verbana. В пищеварительном тракте пиявок Aeromonas veronii является одним из доминирующих видов бактерий. «В чем же заключается симбиоз и причем тут опять система секреции?» — спросите вы. Как всем известно, пиявки — паразиты и питаются кровью, и ее нужно как-то переваривать. Тут на помощь и приходят микроорганизмы. С помощью T2SS Aeromonas veronii секретируют аэролизин, который относится к классу гемолизинов. Аэролизин вызывает выход калия и глюкозы из эритроцитов, что, в свою очередь, приводит к осмотическому лизису, высвобождению гемоглобина и, собственно, разрушению эритроцитов. Эти микроорганизмы используют гемоглобин, а конкретно, гем в качестве источника железа. Стоит отметить, что Aeromonas veronii может вызывать и некоторые инфекции человека, однако в данном случае он рассматривается как свободноживущий микроорганизм [14].
У некоторых свободноживущих бактерий T2SS служит для секреции ферментов, необходимых для их типа метаболизма. Так, для Geobacter sulfurreducens — это мультимедная оксидаза ( в активном центре содержит несколько атомов меди, которые участвуют в процессах окисления различных субстратов). Для Gluconacetobacter diazotrophicus — левансахараза (участвует в синтезе левана). Для Pseudomonas putida — Mn-окисляющие ферменты [15].
Обсудив возможности использования T2SS в бактериальных клетках, перейдем к ее структуре. В отличие от T1SS, в T2SS секреция субстрата происходит в два этапа. Сначала вещество проходит через внутреннюю мембрану и попадает в периплазматическое пространство с помощью описанных выше Sec или Tat. Там белки подготавливаются к дальнейшей транспортировке: происходит их укладка в третичную структуру, а также могут протекать некоторые дополнительные модификации. Сама система состоит из 12 белков, которые входят в состав 4 белковых комплексов. Один из них образует пору для выхода субстрата и располагается на внешней мембране. Второй — на внутренней мембране, его главная функция — связь с комплексом внешней мембраны. АТФаза осуществляет выработку энергии, необходимую для транспортировки субстрата. И наконец, самая важная часть — так называемая псевдопиля, состоящая из различных белков псевдопилинов. Она работает как поршень, выталкивая белки из периплазматического пространства и проталкивая через пору наружу (рис. 4). Этот процесс происходит с использованием энергии АТФ [16].
T3SS
Переходим к следующему типу систем секреции — T3SS. T3SS интересна своей структурой. В отличие от двух описанных выше систем, тут происходит высвобождение субстрата не во внешнюю среду, а его прямое введение в целевую клетку. Эта система внешне и по своему действию напоминает шприц. Впервые ее работа была описана на Yersinia pestis.

Рисунок 5. Строение системы секреции T3SS. Система секреции T3SS состоит из 4 главных компонентов: основания или мембранных колец; иглы; аппарата, непосредственно осуществляющего секрецию; цитозольных компонентов. Секреция субстрата осуществляется внутрь клетки-мишени.
В состав T3SS входят более 20 различных белков. Система состоит из 4 главных компонентов: основания или мембранных колец; иглы; аппарата, непосредственно осуществляющего секрецию; цитозольных компонентов (рис. 5). В зависимости от вида микроорганизма, в ее структуре могут наблюдаться некоторые различия. Так, например, у фитопатогенов роль иглы играет специализированная пиля. Интересно, что у всех микроорганизмов на конце иглы или пили располагается белок, который блокирует секрецию субстрата. При контакте с целевой клеткой он деградирует, и секреция начинается.
T3SS характерна для широкого круга патогенов человека, животных и растений. Она встречается у Bordetella pertussis — основного возбудителя коклюша, Chlamydia trachomatis — возбудителя урогенитальных инфекций, Pseudomonas aeruginosa — условного патогена, ответственного за инфекции дыхательной системы. В случае фитопатогенов, Dickeya dadantii — возбудителя мягкой гнили, Pseudomonas syringae — пятнистость на листьях, Xanthomonas campestris — возбудителя черной гнили [17].
T4SS

Рисунок 6. Строение системы секреции T4SS. «Минимальная» система секреции T4SS содержит белки VirB1–VirB11 и VirD4. Количество белков в «расширенной» системе секреции может достигать 25 штук.
Следующая система секреции — T4SS. Она интересна тем, что используется бактериальными клетками в двух случаях. Первый случай нам уже хорошо знаком — для доставки во внешнюю среду каких-либо белковых молекул. Но кроме этого, T4SS может использоваться и для передачи ДНК между клетками. Этот механизм лежит в основе процесса конъюгации и горизонтального переноса генов (ГПГ). ГПГ — важное явление, потому что благодаря нему бактерии могут передавать друг другу гены устойчивости к антибиотикам и другим неблагоприятным для них веществ и адаптироваться к изменяющимся условиям среды [18]. Проблема роста антибиотикорезистентности очень актуальна, она заставляет ученых постоянно искать новые антибиотики.
В структуру T4SS входят 12 основных белков VirB1–VirB11 и VirD4. Если система состоит только из них, то она считается «минимальной». Минимальные системы используются в процессе конъюгации. Если же в состав входят дополнительные элементы (общее количество белков тогда достигает до 25), то она называется «расширенной». Расширенные системы приобретают новые функции и могут осуществлять секрецию различных белков-эффекторов и токсинов (рис. 6). Причем у них может как сохраняться способность к переносу ДНК, так и не сохраняться [19].
Еще один интересный пример применения T4SS — выделение токсинов, направленных не на эукариотические клетки, а на бактериальные. Известно, что у Xanthomonas citri белок VirD4 взаимодействует с рядом еще не описанных белков, характерных для этого микроорганизма. Эти белки токсичны для других бактерий, что было доказано при смешивании клеток Xanthomonas citri и Escherichia coli. Наблюдался лизис клеток кишечной палочки. Этот пример показывает, что бактериальные системы секреции могут применяться и для устранения конкурентов [20].
T5SS
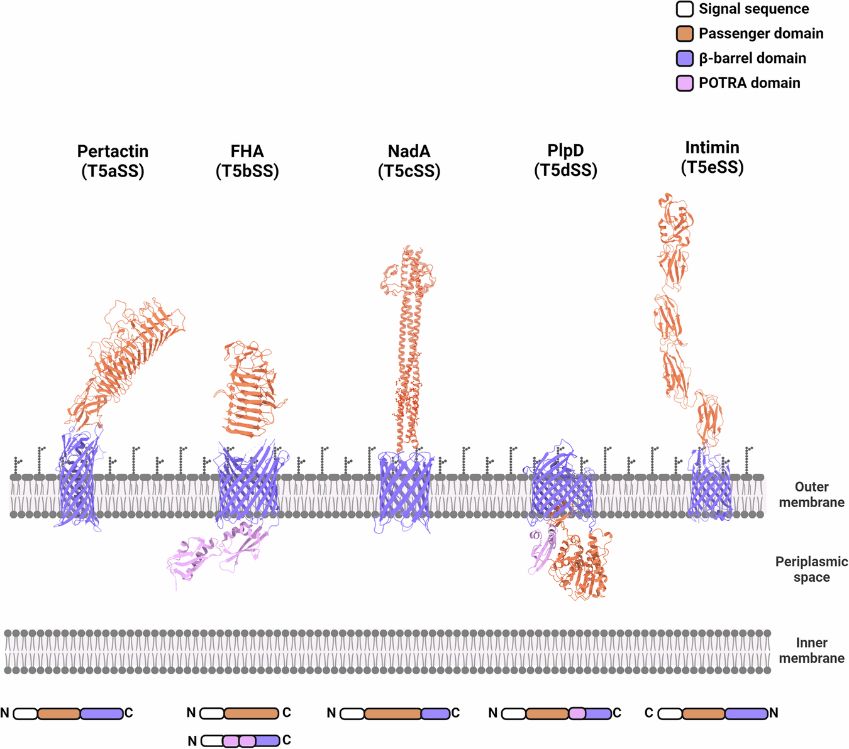
Рисунок 7. Подсистемы T5SS и секретируемые ими субстраты. Система секреции T5SS делится на 5 подсистем: a, b, c, d, e. T5aSS Bordetella pertussis секретирует белок пертактин, а T5cSS Neisseria meningitidis — NadA. Эти белки можно использовать при создании субъединичных вакцин.
Мы подходим к 5 типу систем секреции — T5SS. Эта система так же, как и T2SS работает поэтапно в две стадии. Сначала молекулы субстрата поставляются в периплазматическое пространство с помощью Sec, а через внешнюю мембрану проходят уже с помощью T5SS. Но в отличие от T2SS, она устроена гораздо проще, и состоит всего из одного комплекса, расположенного на внешней мембране. Он представляет собой полипептид, свернутый в конформацию бета-бочонка. Как и T2SS в периплазматическом пространстве происходит правильное сворачивание белка-субстрата с помощью шаперонов. В данном случае эту роль играют белки Skp, SurA и DegP [21].
По структуре полипептида T5SS делится на 5 подсистем: a, b, c, d, e (рис. 7). Но в данной статье рассматривать их различия в структуре мы не будем. Каждая из этих систем секретирует какой-то свой тип белков.
Интересно, что белки, секретируемые T5SS можно использовать для создания субъединичных вакцин. На основе белка пертактина была предложена вакцина против Bordetella pertussis — возбудителя коклюша. А на основе белка-адгезина NadA — против возбудителя менингита Neisseria meningitidis. Однако субъединичные вакцины показывают низкую эффективность, поэтому необходимо использовать несколько белков [22].
T6SS
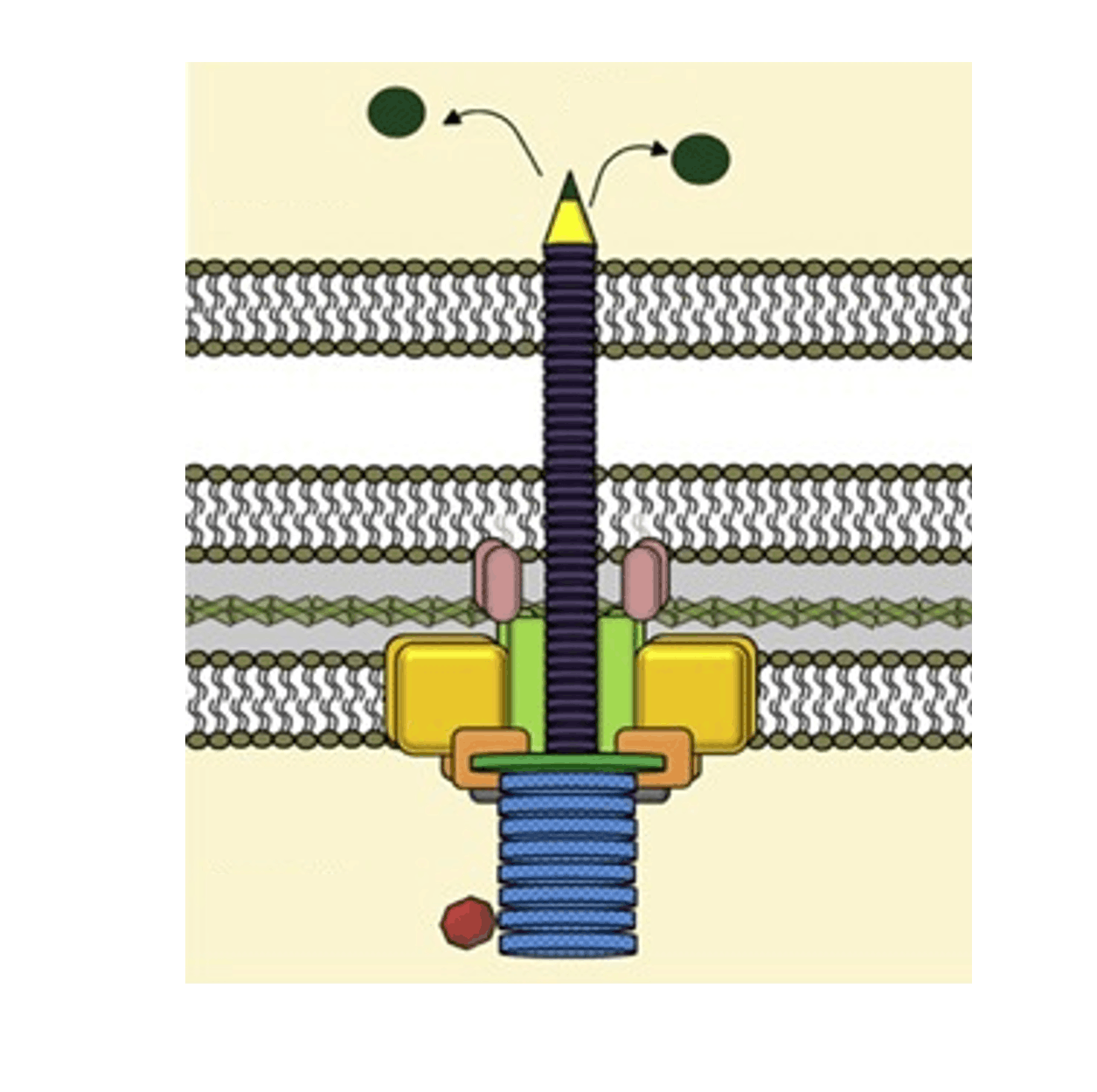
Рисунок 8. Структура системы секреции T6SS. Система секреции T6SS состоит из: основания, располагающегося на внутренней мембране, трубки и иглы. Трубка представляет собой кольца белка Hcp, окруженные двумя белками TssB и TssC. Они отвечают за ее сокращение и проталкивание субстрата через нее к клетке-мишени.
T6SS обнаружена более, чем у 25 % грамотрицательных бактерий. Она нужна для прямого введения токсичных соединений как в эукариотические, так и в прокариотические клетки. Ее часто сравнивают с бактериофагом T4.
T6SS состоит из 13 основных компонентов. Она включает в себя несколько важных частей: основание, располагающееся на внутренней мембране, трубку и иглу. Трубка представляет собой кольца белка Hcp, окруженные двумя белками TssB и TssC. Они отвечают за ее сокращение и проталкивание субстрата через нее к клетке-мишени (рис. 8). «Это очень напоминает механизм действия T3SS» — подумаете вы, и будете правы. Сходство определенно есть, но T3SS, как мы помним, используется, в основном, для инфицирования эукариотических клеток. Здесь же ситуация другая, по мимо того, что T6SS может действовать и на бактериальные клетки, ее функция отличается. T6SS нужна скорее для «уничтожения конкурентов» в борьбе за субстрат, а не для инфекции [23].
В пример приведем такую интересную бактерию как Pseudomonas putida. Это непатогенный микроорганизм, который часто обитает в ассоциации с растениями. Он не только не приносит им вреда, но еще и приносит пользу, защищая их офитопатогенов. Как же ему это удается? Как раз с помощью системы T3SS. Было показано, чтпри совместном культивирование с Pseudomonas putida рост Pseudomonas syringae , Xanthomonas campestris , Pectobacterium carotovorum и Agrobacterium tumefaciens существенно снижается. Все они — страшные фитопатогены, которые приводят к гибели важных сельскохозяйственных растений. Причиной угнетения роста является токсин Tke2. Такая антибактериальная активность T6SS у Pseudomonas putida — перспективное свойство для использования в биотехнологии.
T7SS
Мы переходим к очень интересной системе секреции — T7SS. Она характерна для грамположительных бактерий. Впервые T7SS была обнаружена у Mycobacterium tuberculosis, поэтому мы начнем рассмотрение этой системы именно с микобактерий.
ESX (early antigenic secretion systems) или T7SS — один из факторов вирулентности у микобактерий. Всего выделяют 5 систем ESX (ESX1 — ESX5), различающихся по структуре и своим функциям (рис. 9). Но для всех них характерно наличие компонентов, необходимых для синтеза субстрата, собственных секретируемых белков и вспомогательных элементов. Все это закодировано в геноме в консервативной последовательности генов. Наиболее изученной и хорошо описанной системой секреции является ESX-1, характерная для Mycobacterium tuberculosis. Данная система обуславливает выживаемость микроорганизмов при инфекции организма-хозяина. Это достигается с помощью ингибирования процесса закисления внутри фагосомы, что приводит к ее последующему разрыву и попаданию бактерий в цитозоль. Интересно, что у непатогенного представителя этого рода Mycobacterium smegmatis ESX-1 вместе с ESX-4 осуществляют процесс конъюгации. Причем при таком горизонтальном переносе генов происходит передача больших фрагментов геномной ДНК [24]. Точная функция ESX-4 у других микобактерий еще плохо описана. Но, например, у Mycobacterium abscessus (условный патоген, характеризующийся множественной антибиотикорезистентностью к различным группам антибиотиков) ESX-4 также участвует в процессе разрыва фагосомы и выходе бактерий в цитозоль.
ESX-2 еще плохо изучена, ее функции неизвестны. Известно только, что эта система присутствует у медленнорастущих микобактерий и участвует в поддержании выживаемости. Тут стоит сделать уточнение, что глобально род микобактерий можно разделить на две большие группы: медленнорастущие и быстрорастущие микобактерии. Так, из названных выше представителей, к первой группе относится Mycobacterium tuberculosis, а ко второй — Mycobacterium abscessus и Mycobacterium smegmatis [25].
ESX-3 же участвует в обмене железа и цинка. Она помогает клеткам выживать в условиях дефицита этих элементов. С такими условиями бактерии сталкиваются внутри организма-хозяина при инфекции [26]. И наконец, ESX-5 — система секреции, характерная только для медленнорастущих представителей [27]. Она участвует в поддержании вирулентности микобактерий. Через нее секретируются белки PE (содержат последовательность пролин-глутамат на N-концевом домене) и PPE (содержат последовательность пролин-пролин-глутамат на N-концевом домене) [28]. Эти белки модулируют иммунный ответ организма-хозяина [29].
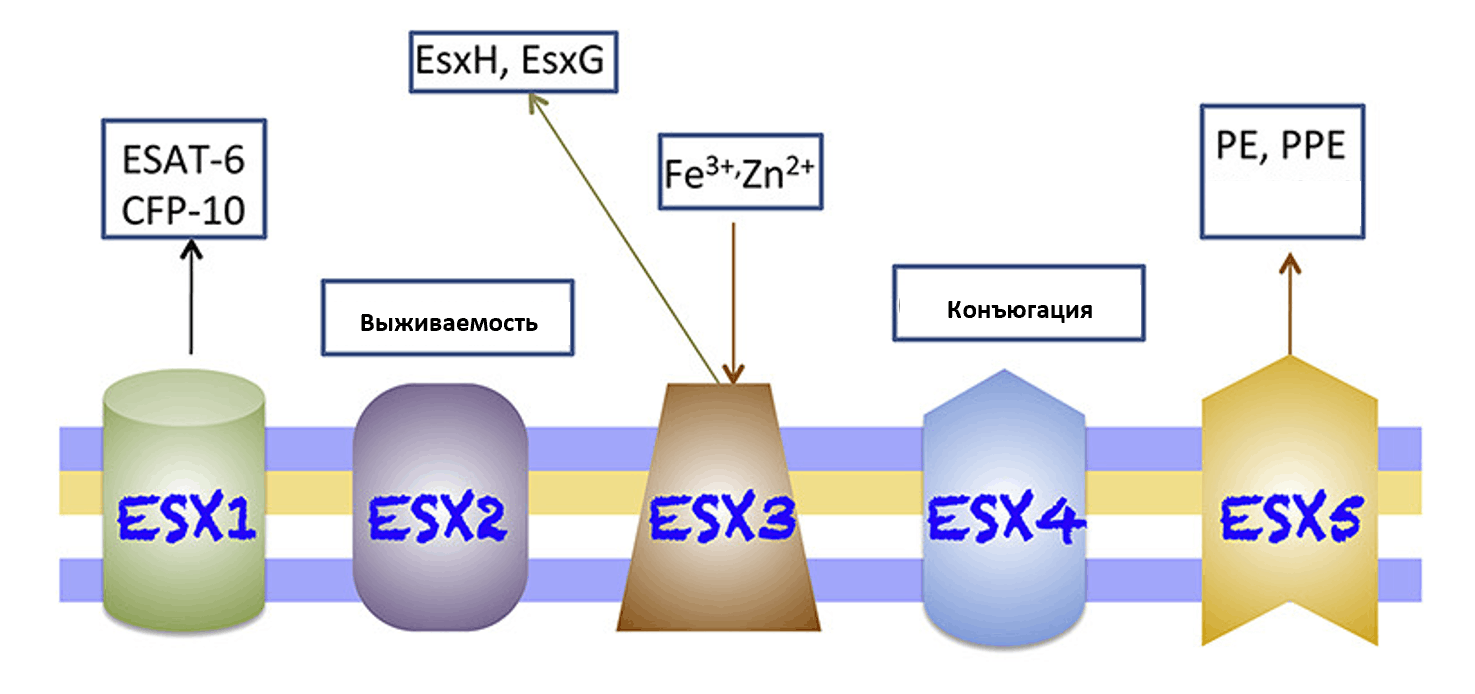
Рисунок 9. Системы секреции ESX1-5, характерные для рода Mycobacterium.
Cистемы секреции ESX относятся к T7SS. ESX-1 секретирует белки (ESAT-6 и CFP-10, повреждающие мембрану фагосомы. Нарушается процесс созревания фагосомы. В результате, закисления и последующего уничтожения патогенов не происходит. ESX-2 способствует выживаемости бактерий в организме-хозяине, остальные ее функции еще не описаны. ESX-3 участвует в обмене железа и цинка. ESX-4 вместе с ESX-1 принимают участие в процессе конъюгации. ESX-5 секретирует белки PE (содержат последовательность пролин-глутамат на N-концевом домене) и PPE (содержат последовательность пролин-пролин-глутамат на N-концевом домене).
T7SS встречается и у других грамположительных бактерий. Например, Staphylococcus aureus, Bacillus anthracis, Streptococcus pneumonia, Corynebacterium diphtheria и Streptococcus agalactiae. В отличие от микобактерий, у Staphylococcus aureus нет деления на подсистемы внутри T7SS. В этом случае через систему секретируются два белка EsxA и EsxB. Вместе они помогают бактериям выйти из эпителиальных клеток организма-хозяина. Интересно, что у Staphylococcus aureus через эту систему секретируется еще и токсин EsaD. В бактериальных клетках он связывается с EsaG и становится безвредным. EsaD действует на клетки S. aureus, у которых мало белка-антитоксина, для снижения конкуренции за субстрат при большом скоплении бактерий. Потенциально этот белок можно использовать для создания субъединичных вакцин [30].
T8SS
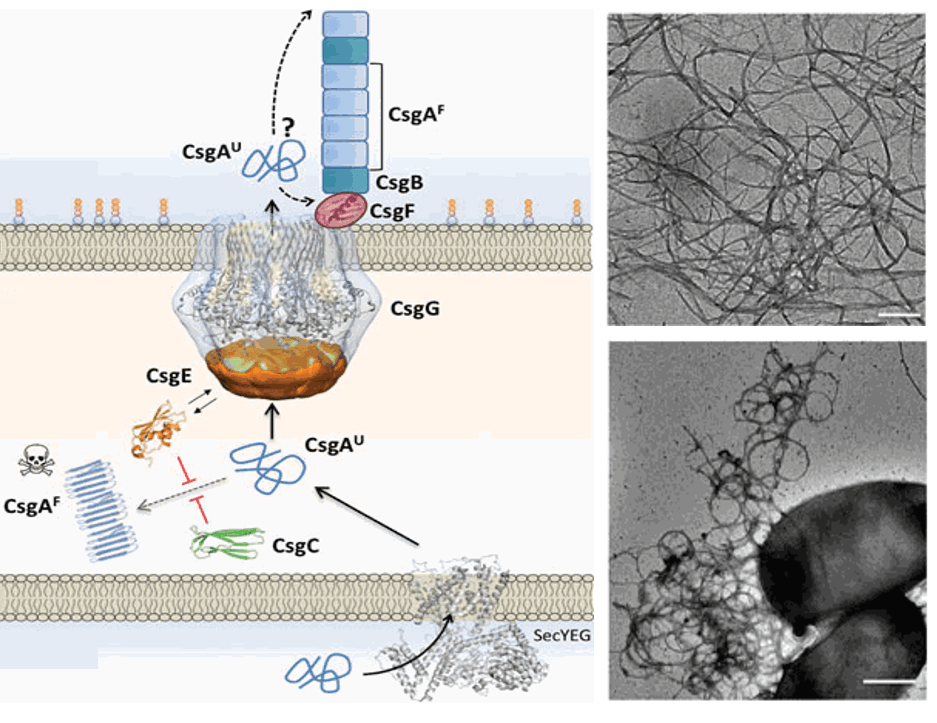
Рисунок 10. Строение системы секреции T8SS и биогенез волокон Curly у Escherichia coli.
В системе секреции T8SCsgA и CsgB, основные компоненты волокон Curly, в периплазматическом пространстве взаимодействуют с белком CsgE, который доставляет их к комплексу на внешней мембране CsgG. Шаперон CsgC защищает CsgA от преждевременной полимеризации. Пройдя через CsgG, белки CsgA и CsgB оказываются во внешней среде. Происходит формирование волокон Curly.
Возвращаемся к грамотрицательным бактериям и переходим к системе секреции T8SS. Она используется некоторыми энтеробактериями, например, Escherichia coli для биогенеза амилоидных волокон или так называемых волокон Curly. Они располагаются на поверхности бактериальных клеток, улучшают адгезию клеток к различным поверхностям и способствуют образованию биопленок.
При упоминании амилоидов у вас скорее всего возникла ассоциация с их участием в развитии некоторых нейродегенеративных заболеваний: болезни Альцгеймера или Паркинсона. Действительно, причинами этих тяжелых заболеваний является неправильное сворачивание белков-амилоидов. Волокна Curly по своей структуре очень похожи на амилоиды человека. Есть предположение, что Curly не только обладают похожими на них свойствами, но и сами участвуют в развитии нейродегенеративных заболеваний, например, болезни Паркинсона.
В организме человека существует ось «кишечник-мозг», с помощью которой бактерии из ЖКТ могут влиять на нервную систему и развитие нейродегенеративных заболеваний [31]. Так, есть предположение, что белки Curly могут взаимодействовать с амилоидным белком α-синуклином — его неправильное сворачивание напрямую влияет на развитие болезни Паркинсона [32].
T8SS работает в два этапа: сначала молекулы поставляются в периплазматическое пространство с помощью Sec, а потом в действие вступает уже непосредственно T8SS. Основные компоненты волокон Curly — белки CsgA и CsgB. CsgE помогает им преодолеть периплазматическое пространство, а шаперон CsgC защищает CsgA от преждевременной полимеризации. CsgG образует комплекс на внешней мембране, через который белки попадают во внешнюю среду (рис. 10) [33].
T9SS
Мы близимся к концу обзора бактериальных систем секреции и переходим к T9SS. Это четвертая по счету система, которая работает по двухэтапному механизму. Снова молекулы должны сначала преодолеть внутреннюю мембрану с помощью Sec, а потом уже встретиться с самой T9SS. Она характерна для представителей Bacteroides. Например, для очень интересной бактерии Porphyromonas gingivalis — патогена человека, вызывающего пародонтит (заболевание десен). Было показано, что данная бактерия может быть одной из причин возникновения болезни Альцгеймера [34]. Свои основные токсичные элементы — гингипаины, этот микроорганизм секретирует как раз с помощью T9SS. Еще один хорошо изученный представитель с этой системой — Flavobacterium johnsoniae [35]. Секретируемые им белки используются для его передвижения с помощью скольжения [36].
По структуре T9SS похожа на описанные выше системы. Из периплазматического пространства молекулы попадают во внешнюю среду благодаря комплексу, расположенному на внешней мембране. Структура T9SS постоянно уточняется, и довольно часто выходят статьи, описывающие конкретные белковые взаимодействия, которые там происходят. Так, долгое время функция белка PorZ оставалась неизвестной. Оказалось, что это один из основных элементов системы T9SS (рис. 11). Его главная функция — распознавание белковых субстратов и их доставка к основному комплексу, который осуществляет секрецию во внешнюю среду [37].
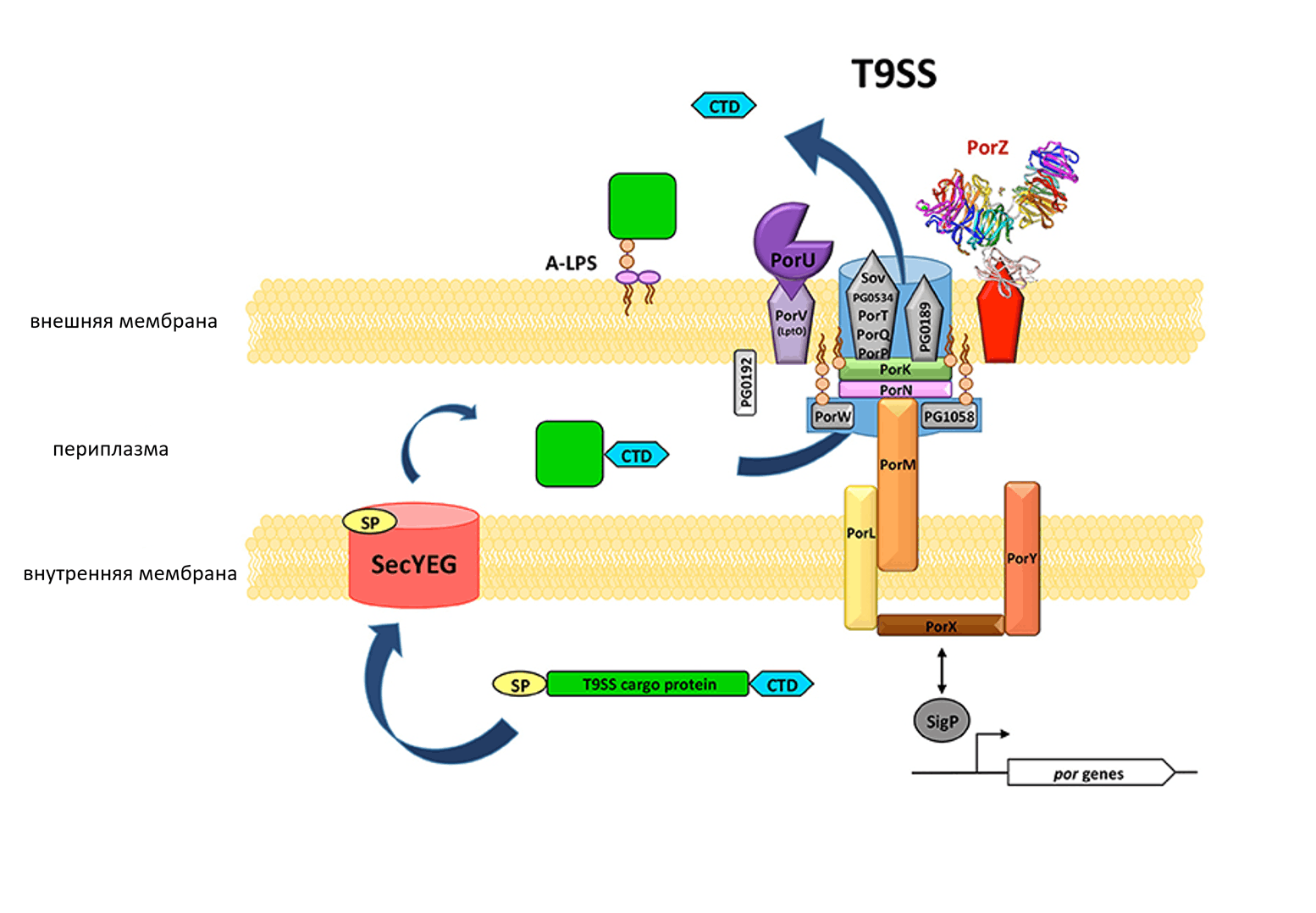
Рисунок 11. Строение системы секреции T9SS. На внешней мембране располагается белковый комплекс T9SS. Рядом с ним — белок PorZ, один из основных элементов системы T9SS. Его главная функция — распознавание белковых субстратов и их доставка к основному комплексу, который осуществляет секрецию субстрата во внешнюю среду.
На этом обзор основных классических бактериальных систем секреции заканчивается. Однако не так давно были обнаружены еще две системы: T10SS и T11SS.
T10SS
На сегодняшний день механизмы секреции описаны далеко не для всех существующих веществ. Так, например, долгое время оставалось непонятным, как осуществляется секреция больших молекул в некоторых патогенах. Очевидно, что существующие системы явно для этого не подходили. Ответ на этот вопрос был найден в 2020 году. Вышла статья, в которой группа ученых предложила систему, работающую на основе двух основных белков. Один белок — мембранный белок холин, а главная функция второго — изменение структуры клеточной стенки (второй белок различается у разных видов микроорганизмов). Так, они описали механизмы секреции хитиназы у Serratia marcescens и тифоидного токсина Salmonella enterica. В статье показано, что первый микроорганизм использует фермент эндопептидазу в связке с холином, а второй — мурамидазу. Эта новая система секреции получила название T10SS [38].
Уже в 2024 году вышла статья, в которой показано, что система T10SS работает и в случае секреции токсина Tc в патогене насекомых Yersinia entomophaga. Этот токсин очень большой, размером с рибосому [39] !
T11SS
Долгое время механизм секреции липопротеинов во внешнюю среду оставался неописанным. В 2021 году была предложена система, осуществляющая эту функцию. Она характерна для всех протеобактерий [40]. Например, у Neisseria meningitidis, Acinetobacter baumanii, Haemophilus haemolyticus, и Proteus vulgaris — патогенов человека. Сначала был определен лишь один входящий в нее компонент — белок из семейства DUF560 (domain of unknown function) [41]. Впоследствии вышло несколько статей с уточнением структуры этой новой системы, но полный механизм действия все еще остается неизвестным [42].
Заключение
Бактериальные системы секреции — важный элемент бактериальных клеток. Каждая из них обладает своей функцией, уникальной структурой и своим механизмом действия. Практически каждый год происходит описание новых элементов в уже существующих системах и даже открытие новых систем секреции. Многие из них представляют имеют потенциал для их использования в биотехнологии, например, при разработке вакцин.
Литература
- Антибиотики vs Бактерии. «Война Бесконечности» или всему есть предел?;
- Alain Filloux. (2022). Bacterial protein secretion systems: Game of types. Microbiology. 168;
- Laura C. Ristow, Rodney A. Welch. (2016). Hemolysin of uropathogenic Escherichia coli: A cloak or a dagger?. Biochimica et Biophysica Acta (BBA) - Biomembranes. 1858, 538–545;
- Peter Stanley, Vassilis Koronakis, Colin Hughes. (1998). Acylation ofEscherichia coliHemolysin: A Unique Protein Lipidation Mechanism Underlying Toxin Function. Microbiol Mol Biol Rev. 62, 309–333;
- S Létoffé, J M Ghigo, C Wandersman. (1994). Secretion of the Serratia marcescens HasA protein by an ABC transporter. J Bacteriol. 176, 5372–5377;
- Shannon M. Hinsa, Manuel Espinosa‐Urgel, Juan L. Ramos, George A. O'Toole. (2003). Transition from reversible to irreversible attachment during biofilm formation by Pseudomonas fluorescens WCS365 requires an ABC transporter and a large secreted protein. Molecular Microbiology. 49, 905–918;
- Olivia Spitz, Isabelle N. Erenburg, Tobias Beer, Kerstin Kanonenberg, I. Barry Holland, Lutz Schmitt. (2019). Type I Secretion Systems—One Mechanism for All?. Microbiol Spectr. 7;
- Sabrina Thomas, I. Barry Holland, Lutz Schmitt. (2014). The Type 1 secretion pathway — The hemolysin system and beyond. Biochimica et Biophysica Acta (BBA) - Molecular Cell Research. 1843, 1629–1641;
- Alexandra Tsirigotaki, Jozefien De Geyter, Nikolina Šoštaric´, Anastassios Economou, Spyridoula Karamanou. (2017). Protein export through the bacterial Sec pathway. Nat Rev Microbiol. 15, 21–36;
- Tracy Palmer, Ben C. Berks. (2012). The twin-arginine translocation (Tat) protein export pathway. Nat Rev Microbiol. 10, 483–496;
- William R. Miller, Cesar A. Arias. (2024). ESKAPE pathogens: antimicrobial resistance, epidemiology, clinical impact and therapeutics. Nat Rev Microbiol. 22, 598–616;
- Биопленки. Как живется в бактериальных многоэтажках?;
- Silindile Maphosa, Lucy N. Moleleki, Thabiso E. Motaung. (2023). Bacterial secretion system functions: evidence of interactions and downstream implications. Microbiology. 169;
- Michele Maltz, Joerg Graf. (2011). The Type II Secretion System Is Essential for Erythrocyte Lysis and Gut Colonization by the Leech Digestive Tract Symbiont Aeromonas veronii. Appl Environ Microbiol. 77, 597–603;
- Souvik Naskar, Michael Hohl, Matteo Tassinari, Harry H. Low. (2021). The structure and mechanism of the bacterial type II secretion system. Molecular Microbiology. 115, 412–424;
- Sophie S. Abby, Jean Cury, Julien Guglielmini, Bertrand Néron, Marie Touchon, Eduardo P. C. Rocha. (2016). Identification of protein secretion systems in bacterial genomes. Sci Rep. 6;
- Andrea Puhar, Philippe J. Sansonetti. (2014). Type III secretion system. Current Biology. 24, R784-R791;
- РНК-полимераза, горизонтальный перенос генов и связь поколений в лаборатории молекулярной генетики микроорганизмов ИМГ РАН;
- Tiago R. D. Costa, Jonasz B. Patkowski, Kévin Macé, Peter J. Christie, Gabriel Waksman. (2024). Structural and functional diversity of type IV secretion systems. Nat Rev Microbiol. 22, 170–185;
- Diorge P. Souza, Gabriel U. Oka, Cristina E. Alvarez-Martinez, Alexandre W. Bisson-Filho, German Dunger, et. al. (2015). Bacterial killing via a type IV secretion system. Nat Commun. 6;
- Yi Luo, Ziyue Chen, Siqi Lian, Xingduo Ji, Chunhong Zhu, et. al. (2023). The Love and Hate Relationship between T5SS and Other Secretion Systems in Bacteria. IJMS. 25, 281;
- Rochelle M. Da Costa, Jessica L. Rooke, Timothy J. Wells, Adam F. Cunningham, Ian R. Henderson. (2024). Type 5 secretion system antigens as vaccines against Gram-negative bacterial infections. npj Vaccines. 9;
- Patricia Bernal, Luke P Allsopp, Alain Filloux, María A Llamas. (2017). The Pseudomonas putida T6SS is a plant warden against phytopathogens. The ISME Journal. 11, 972–987;
- Todd A. Gray, Ryan R. Clark, Nathalie Boucher, Pascal Lapierre, Carol Smith, Keith M. Derbyshire. (2016). Intercellular communication and conjugation are mediated by ESX secretion systems in mycobacteria. Science. 354, 347–350;
- Mae Newton-Foot, Robin Mark Warren, Samantha Leigh Sampson, Paul David van Helden, Nicolaas Claudius Gey van Pittius. (2016). The plasmid-mediated evolution of the mycobacterial ESX (Type VII) secretion systems. BMC Evol Biol. 16;
- M. Sloan Siegrist, Meera Unnikrishnan, Matthew J. McConnell, Mark Borowsky, Tan-Yun Cheng, et. al. (2009). Mycobacterial Esx-3 is required for mycobactin-mediated iron acquisition. Proc. Natl. Acad. Sci. U.S.A. 106, 18792–18797;
- Swati Shah, Volker Briken. (2016). Modular Organization of the ESX-5 Secretion System in Mycobacterium tuberculosis. Front. Cell. Infect. Microbiol. 6;
- Louis S. Ates. (2020). New insights into the mycobacterial PE and PPE proteins provide a framework for future research. Molecular Microbiology. 113, 4–21;
- Mae Newton-Foot, Robin Mark Warren, Samantha Leigh Sampson, Paul David van Helden, Nicolaas Claudius Gey van Pittius. (2016). The plasmid-mediated evolution of the mycobacterial ESX (Type VII) secretion systems. BMC Evol Biol. 16;
- Yongjin Wang, Yang Zhou, Chaowei Shi, Jiacong Liu, Guohua Lv, et. al. (2022). A toxin-deformation dependent inhibition mechanism in the T7SS toxin-antitoxin system of Gram-positive bacteria. Nat Commun. 13;
- Влияние бактериальных внеклеточных везикул на нейродегенеративные заболевания;
- Chenyin Wang, Chun Yin Lau, Fuqiang Ma, Chaogu Zheng. (2021). Genome-wide screen identifies curli amyloid fibril as a bacterial component promoting host neurodegeneration. Proc. Natl. Acad. Sci. U.S.A. 118;
- Sujeet Bhoite, Nani van Gerven, Matthew R. Chapman, Han Remaut. (2019). Curli Biogenesis: Bacterial Amyloid Assembly by the Type VIII Secretion Pathway. EcoSal Plus. 8;
- Porphyromonas gingivalis — Дракула в мире бактерий;
- Maelle Paillat, Caterina Comas Hervada, Stéphane Audebert, Eric Cascales, Thierry Doan. (2025). Specialized shuttle proteins recognize Type IX secretion signals and target effectors to their final destinations in Flavobacterium johnsoniae. Commun Biol. 8;
- Движение бактерий;
- Frédéric Lauber, Justin C. Deme, Susan M. Lea, Ben C. Berks. (2018). Type 9 secretion system structures reveal a new protein transport mechanism. Nature. 564, 77–82;
- Tracy Palmer, Alexander J. Finney, Chayan Kumar Saha, Gemma C. Atkinson, Frank Sargent. (2021). A holin/peptidoglycan hydrolase‐dependent protein secretion system. Molecular Microbiology. 115, 345–355;
- Oleg Sitsel, Zhexin Wang, Petra Janning, Lara Kroczek, Thorsten Wagner, Stefan Raunser. (2024). Yersinia entomophaga Tc toxin is released by T10SS-dependent lysis of specialized cell subpopulations. Nat Microbiol. 9, 390–404;
- Alex S. Grossman, Terra J. Mauer, Katrina T. Forest, Heidi Goodrich-Blair. (2021). A Widespread Bacterial Secretion System with Diverse Substrates. mBio. 12;
- Alex S. Grossman, Nicholas C. Mucci, Sarah J. Kauffman, Jahirul Rafi, Heidi Goodrich-Blair. (2025). Bioinformatic discovery of type 11 secretion system (T11SS) cargo across the Proteobacteria. Microbial Genomics. 11.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





