Porphyromonas gingivalis — Дракула в мире бактерий
19 февраля 2021
Porphyromonas gingivalis — Дракула в мире бактерий
- 8139
- 2
- 9
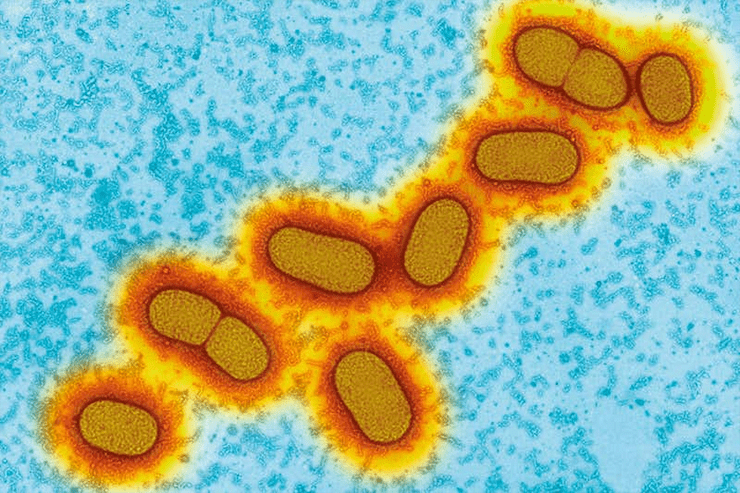
Porphyromonas gingivalis
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Бывает ли у вас такое, что после тяжелого дня по возвращении домой хочется просто рухнуть на любимую кровать, даже не почистив зубы? Если ваш ответ положительный, то стоит пересмотреть эту привычку, ведь она может привести не только к кариесу и заболеваниям полости рта, но и к деменции! За это может отвечать микроорганизм под названием Porphyromonas gingivalis.
Конкурс «Био/Мол/Текст»-2020/2021
 Эта работа заняла второе место в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Эта работа заняла второе место в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
P. gingivalis (см. заглавную картинку) — палочковидная анаэробная патогенная бактерия, широко известная способностью вызывать пародонтит и многие другие болезни ротовой полости. За последние несколько лет появились сведения о том, что порфиромонада играет немаловажную роль и в развитии таких заболеваний, как рак поджелудочной железы, ревматоидный артрит, системные болезни сердечно-сосудистой системы (в том числе инфаркт и инсульт) и нейродегенеративные заболевания. В этой статье мы обсудим необычные способности P. gingivalis и откуда они берутся, а также каким образом этот микроорганизм относится к появлению болезни Альцгеймера.
Цикл функционирования в организме: от десен до мозга
Первый контакт
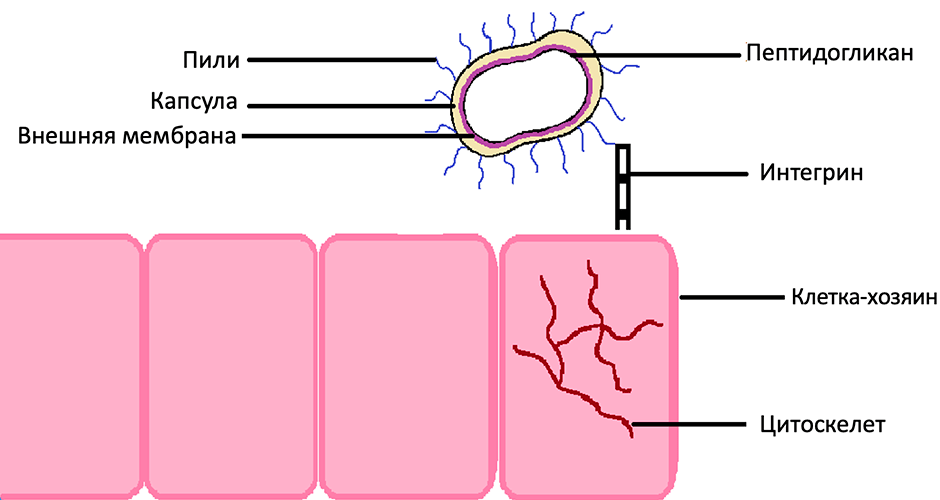
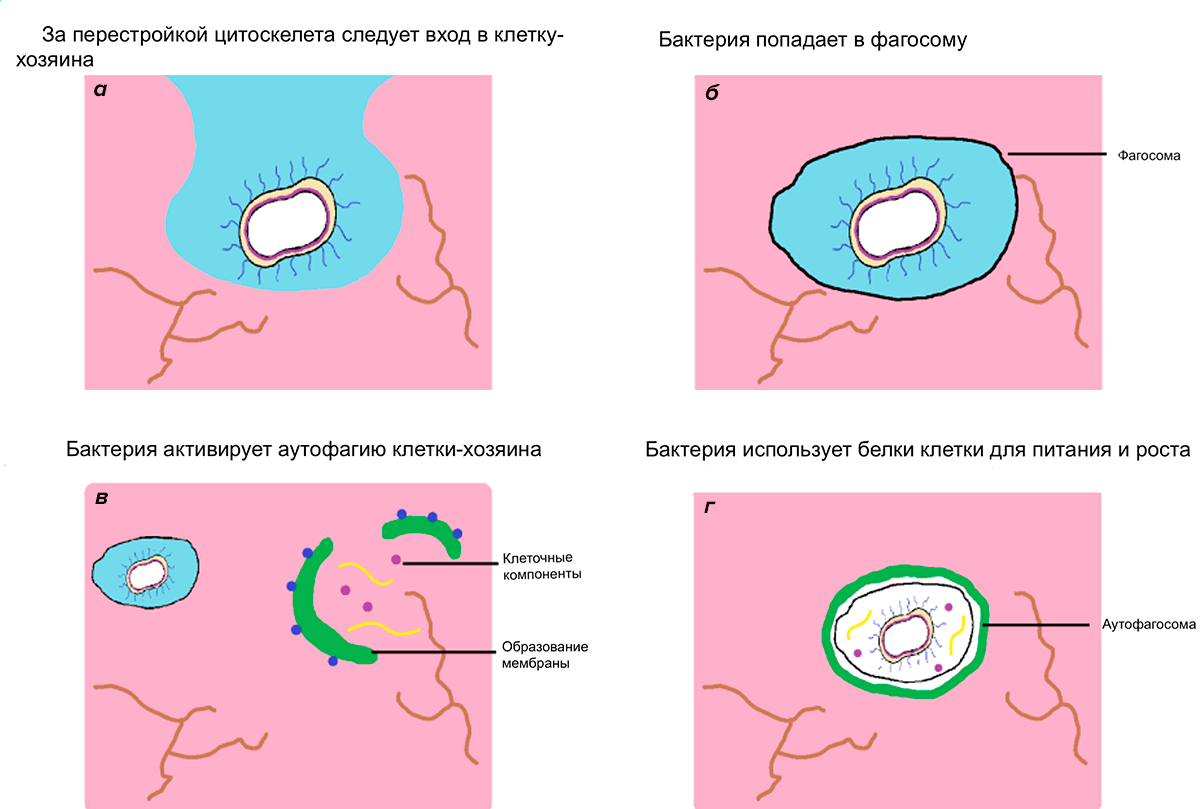
P. gingivalis обычно попадает в ротовую полость от другого человека [1]. В этот момент перед порфиромонадой встает сложное испытание — удержаться здесь. Механические движения челюсти и языка, слюна и содержащиеся в ней бактерицидные агенты — всё это противостоит колонизации полости рта бактерией. Поэтому микроорганизм объединяется при помощи пилей с другими бактериями [2]. Межвидовые связи не только помогают микробу в колонизации ротовой полости, но и способствуют получению питательных элементов [3]. Для прикрепления к клеткам хозяина бактерия использует поверхностный белок гемагглютинин [4], который связывается с рецепторами на мембране человеческой клетки (в основном с интегрином β1) [5]. Однако бактерия не останавливается на прикреплении к эпителиальным клеткам: она проникает и самовоспроизводится в них (рис. 1). Сама клетка служит транспортом в другие органы через кровоток и ресурсным местом для роста и размножения.
На грани жизни и смерти
Бактерия находится в выгодном положении и старается остаться в клетке хозяина как можно дольше. Чтобы удержаться внутри, порфиромонада частично замедляет апоптоз (клеточное самоубийство) в деснах, который провоцируют молекулы АТФ [6]. P. gingivalis выборочно выдерживает равновесие между про- и антиапоптозными ферментами и ингибирует «невыгодные» ей ферменты [7]. Однако такое поведение зарегистрировано не во всех типах клеток. В некоторых случаях микроорганизму наоборот удобнее ускорять клеточную смерть. Этот факт указывает на прекрасный баланс в механизмах работы бактерии, что является огромным преимуществом в выживании. В случаях подавления гибели клетки хозяина она запускает способность распространяться к другим клеткам с помощью актинового скелета. Так микроб может проникать в глубокие слои эпителия, кровяные клетки и заражать другие органы (рис. 2) [8].
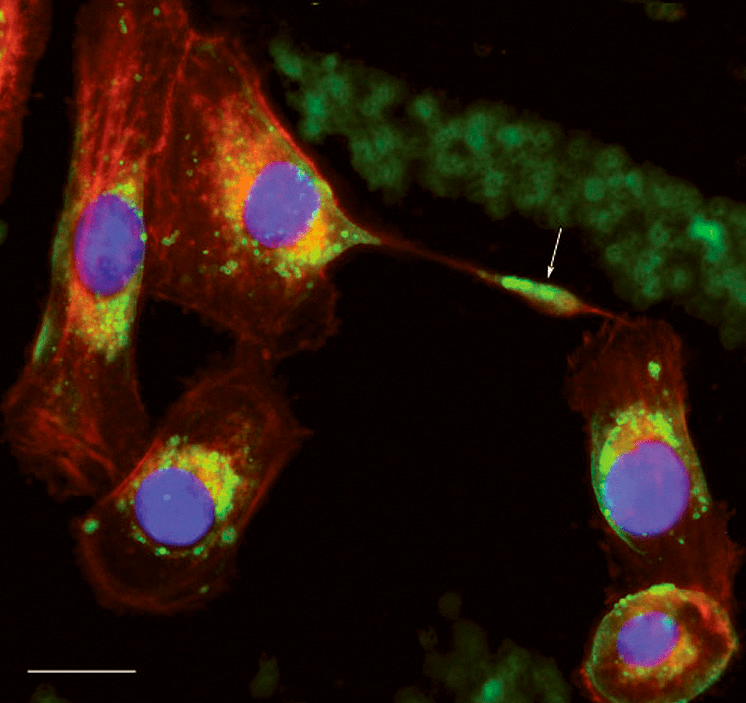
Рисунок 2. На фотографии красным выделены актиновые филаменты, зеленым — сама Porphyromonas gingivalis. Белая стрелка указывает на актин и бактериальное перемещение между клетками-хозяевами. Такое перемещение упрощает распространение по организму хозяина.
Осторожное перемещение в основном характерно для более ранних фаз заражения. Скорее всего, это дает порфиромонаде достаточно времени для адаптации к новой среде и распространения по всему телу хозяина. В других случаях микроб подталкивает клетку к самоубийству, особенно если эта клетка — часть иммунитета организма хозяина. P. gingivalis убивает лимфоциты и Т-клетки, чтобы в первую очередь защищать своих соседей и не терять питательные связи [9]. Сама бактерия устойчива к нашему иммунитету благодаря липополисахариду (LPS) на своей поверхности.
LPS нашего патогена отличается от липополисахаридов большинства других бактерий из-за измененного липидного состава. Липополисахарид порфиромонады включает рецепторы опознавания паттерна (PRR) на поверхности иммунных клеток хозяина. PRR — это белки, задача которых — опознавать специфичные для патогенов структуры. Представители PRR — толл-подобные рецепторы, как раз реагирующие на патогенные бактерии. На LPS порфиромонады реагирует в основном TLR-2. На этом моменте P. gingivalis подключает свое главное оружие — протеазы гингипаины. В распоряжении патогена есть два вида гингипаинов: лизинспецифичные Kgp и аргининспецифичные RgpA и RgpB [10]. С помощью них микроб может контролировать другую часть врожденного иммунитета — систему комплемента.
Система комплемента состоит из большого количества различных белков плазмы, которые взаимодействуют друг с другом и покрывают поверхность патогенов, что облегчает фагоцитоз и вызывает воспаление. Гингипаины расщепляют один из белков — C5 — на C5a и C5b [11], [12]. C5a взаимодействует с TLR2 на поверхности нейтрофилов, что приводит к подавлению фагоцитоза и воспалению (рис. 3) [13], [14]. Так порфиромонада утоляет жажду крови из поврежденных тканей и спасает себя и своих сожителей.
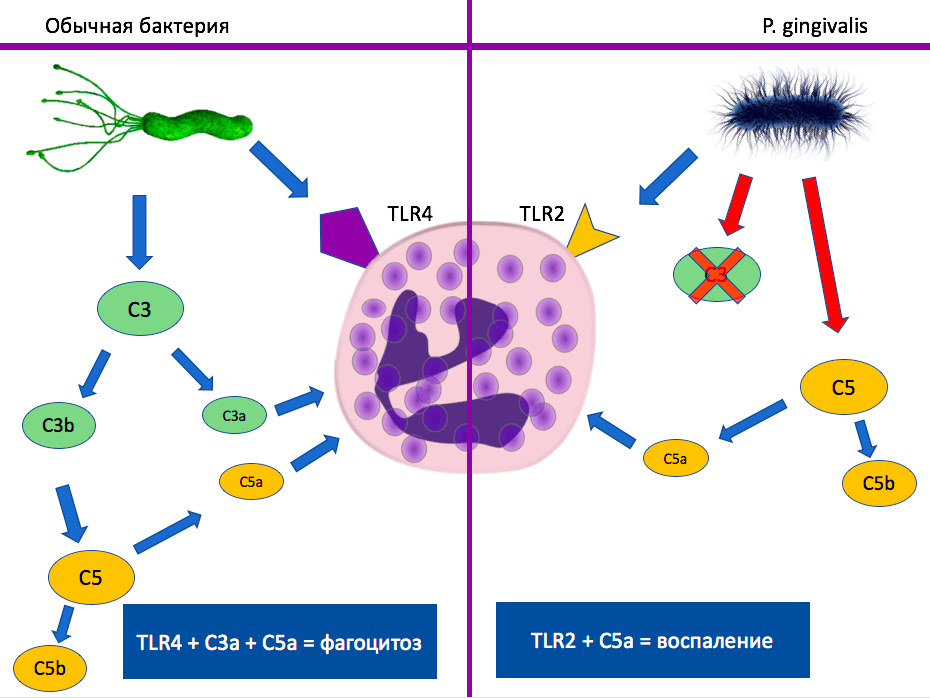
Рисунок 3. Сравнение путей активации системы комплемента обычной бактерией и Porphyromonas gingivalis. Клетка по центру — нейтрофил. Синие стрелки обозначают обычные для организма реакции. Красными стрелками показаны гингипаины.
Но кровь нужна микробу не только, чтобы ее пить. Через кровеносную систему бактерия распространяется по телу хозяина и попадает в мозг [15]. Пока точно не известно, каким образом патоген попадает туда, ведь мозг тщательно охраняется гематоэнцефалическим барьером (ГЭБ). Скорее всего, бактерия проникает туда через сосуды, которые со старостью становятся проницаемыми (рис. 4). В мозговой ткани P. gingivalis (внезапно!) вызывает нейродегенеративные заболевания.

Рисунок 4. P. gingivalis может проникать в ткани пародонта через бороздчатый эпителий, попадая в микроциркуляцию пародонта, где затем может распространяться через кровоток и колонизировать мозг
[15], рисунок адаптирован
P. gingivalis и болезнь Альцгеймера
Биофармацевтическая компания Cortexyme (США) в сотрудничестве с лабораториями в Австралии, Великобритании, Европе и Новой Зеландии опубликовала новые подтверждения того, что P. gingivalis — возможная причина болезни Альцгеймера (БА) [16] (предположения о такой связи высказывали и до этого). Исследователи Cortexyme изучили связь новой гипотезы с уже существующими: тау- и амилоидной гипотезами. Команда исследовала 54 образца мозговой ткани людей с БА и сравнила со здоровыми экземплярами. Материалы были взяты post mortem (у мертвых людей). Более чем в 90% образцов мозга с БА исследователи нашли следы гингипаинов и бета-амилоида (Aβ) с наибольшей концентрацией в гиппокампе — области мозга, ответственной за память. Aβ — пептид, из которого образуются токсичные амилоидные бляшки — основной признак БА [17]. Однако в некоторых здоровых экземплярах тоже обнаружили гингипаины и Aβ, но в меньших концентрациях. Также мы знаем, что болезни нужно аж 10–20 лет, чтобы появились первые симптомы. Этот факт может значить, что бактерия попадает в мозг не в результате самой болезни, заявляет глава Cortexyme и соавтор статьи Кейси Линч.
Спинномозговая жидкость (ликвор) считается брешью в защите мозга, которая может стать проходом для патогенов и токсинов, поэтому группа решила проверить и ее на наличие P. gingivalis. Ликвор и слюну взяли у живых людей с подозрением на БА с легкими или умеренными умственными нарушениями. Семь образцов спинномозговой жидкости из 10 и все образцы слюны содержали порфиромонаду. Эти данные подкрепляют предположение о связи P. gingivalis и БА.
Так как бактерия может быть причиной деменции?
Чтобы понять влияние бактерии на мозг и связь с гипотезами о появлении БА, команда проводила эксперименты на мышах и культуре нейробластомы и пришла к следующим результатам:
- Повышение уровня Aβ. При появлении порфиромонады в мозге сильно увеличивалась концентрация Aβ. Амилоид эффективно устранял порфиромонаду, хотя с этим не могли справиться антибиотики широкого спектра. Но, к сожалению, при большой концентрации амилоид отравлял не только микроба, но и нейроны мозга. Этот факт подтверждает догадки о том, что Aβ — часть врожденного иммунитета [18].
- Нарушение конформации тау-белка. В норме тау-белок стабилизирует микротрубочки в аксонах нейронов и отвечает за транспорт веществ внутри клетки. При БА белок гиперфосфорилирован и входит в состав опасных для мозга нейрофибриллярных клубков. Гингипаины расщепляли тау-белок на небольшие фрагменты. После фрагментации протеазой RgpB образовывалась последовательность, которую можно обнаружить во всех изоформах тау. Концентрация этой последовательности повышена у людей с БА. После нарезки Kgp образовывались пептиды, склонные к гиперфосфорилированию и слипанию в клубки.
- Прямое разрушение нейронов и межклеточных связей. Гингипаины разрушали синапсы, нарушали работу межклеточного транспорта и метаболизма клеток. Такие эффекты связаны с повреждением микротрубочек и цитоскелета. Изменения приводили к воспалениям и дальше нарушали деятельность мозга, продолжая порочный круг.
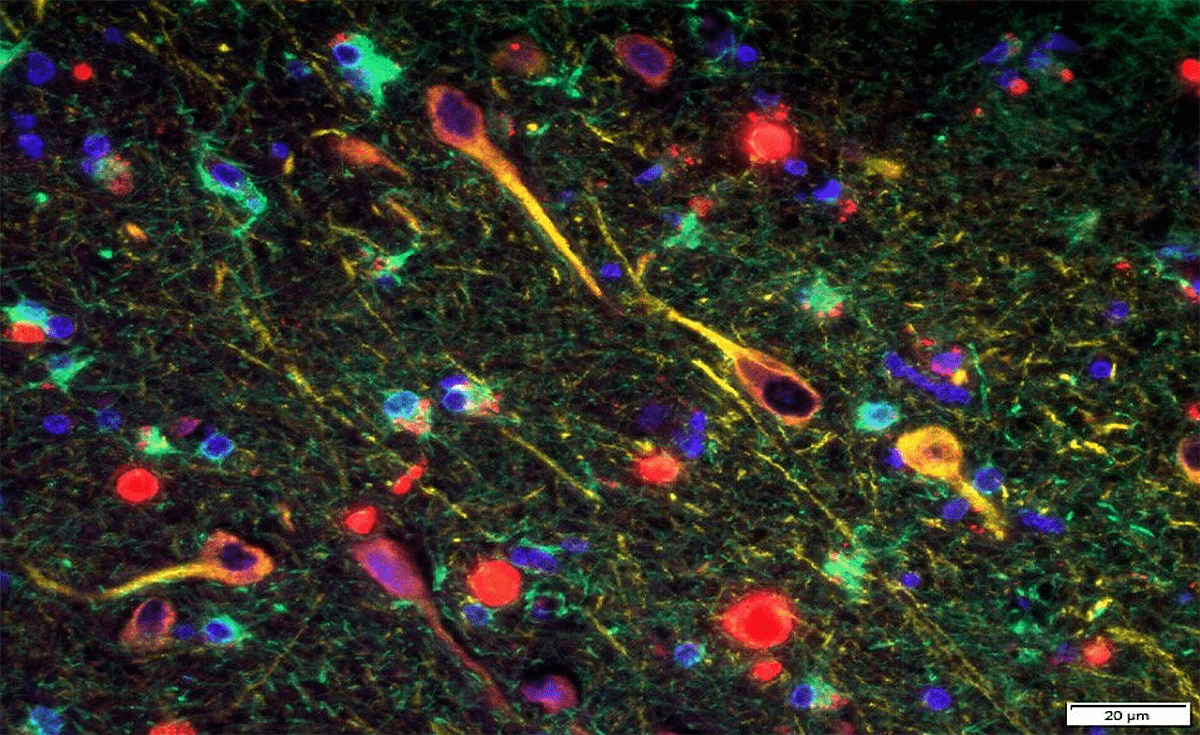
Рисунок 5. Экземпляр мозговой ткани одного из исследуемых образцов. Гингипаины Porphyromonas gingivalis (красный) среди нейронов в мозге пациента с БА. Желтым цветом отмечены нейроны, зеленым — глиальные клетки.
Другие исследования поддерживают предположения о ключевой роли P. gingivalis в появлении деменции. Ученые из Швеции показали, как бактерия связана с генетическим фактором БА [19]. Считается, что риск развития нейродегенеративных заболеваний повышен у людей с аллелем E4 гена ApoE, который кодирует одноименную форму аполипопротеина ApoE4 (подробнее про ApoE читайте в статье «Болезнь Альцгеймера: ген, от которого я без ума» [20]). Исследователи выяснили, что гингипаины нарезают аполипопротеин на аминокислоты, которые могут вредить нейронам. В результате фрагментации варианта ApoE4 появляется больше опасных аминокислот, что может ускорять развитие БА и других заболеваний мозга. Вдобавок P. gingivalis не щадит ни кровеносную, ни пищеварительную,. ни даже дыхательную систему. Такое воздействие делает организм более уязвимым, в том числе мозг и ГЭБ.
Возможное лечение
За почти весь ущерб отвечают гингипаины, поэтому Cortexyme решили разобраться в первую очередь с ними. Компания разрабатывает ингибиторы гингипаинов Kgp под названием COR388, или «Атузагинстат». Исследования эффективности ингибитора уже проводились в лаборатории и на животных. «Атузагинстат» замедлял рост и распространение P. gingivalis, уменьшал концентрацию Aβ в мозговой ткани, нейровоспаление и нейродегенерацию и предотвращал потерю синапсов. Порфиромонада не вырабатывала устойчивость к COR388, в отличие от антибиотиков. Ученые предполагают, что ингибитор может помочь в лечении других болезней, связанных с P. gingivalis, например — пародонтита [21]. Сейчас проводятся клинические исследования на 570 пациентах с БА. Команда исследователей планирует опубликовать результаты тестирований в конце 2021 года.
Заключение
Новая гипотеза, хоть и может показаться неожиданной и даже неоднозначной, основана на убедительных фактах и множестве исследований, а доказательная база стремительно растет. Особенно смотря на сильные пагубные способности Porphyromonas gingivalis и ее «кровожадность», такое громкое заявление звучит не так сомнительно. Многие ученые, фармацевтические компании и все люди, которые сталкивались с этой болезнью, надеются на эту теорию и верят в ее успех.
Однако стоит помнить, что БА — комплексное заболевание, и вряд ли можно объяснить все случаи одной причиной. Само исследование было относительно небольшим, и делать точные выводы пока еще рано. Но пока что исследования себя оправдывают, а многие инвесторы всё чаще посматривают в сторону разработок Cortexyme. В любом случае эта гипотеза — свежий глоток воздуха за многие годы для многих исследователей, а ингибитор гингипаинов может стать прорывом в лечении этого заболевания.
Литература
- Gary Greenstein, Ira Lamster. (1997). Bacterial Transmission in Periodontal Diseases: A Critical Review. Journal of Periodontology. 68, 421-431;
- Howard F. Jenkinson, Richard J. Lamont. (2005). Oral microbial communities in sickness and in health. Trends in Microbiology. 13, 589-595;
- G. Lépine, A. Progulske-Fox. (1996). Duplication and differential expression of hemagglutinin genes in Porphyromonas gingivalis. Oral Microbiol Immunol. 11, 65-78;
- Rieko Ito, Kazuyuki Ishihara, Mikio Shoji, Koji Nakayama, Katsuji Okuda. (2010). Hemagglutinin/Adhesin domains ofPorphyromonas gingivalisplay key roles in coaggregation withTreponema denticola. FEMS Immunol Med Microbiol. 60, 251-260;
- Ichiro Nakagawa, Atsuo Amano, Masae Kuboniwa, Takayuki Nakamura, Shigetada Kawabata, Shigeyuki Hamada. (2002). Functional Differences among FimA Variants of Porphyromonas gingivalis and Their Effects on Adhesion to and Invasion of Human Epithelial Cells. IAI. 70, 277-285;
- Özlem Yilmaz. (2008). The chronicles of Porphyromonas gingivalis: the microbium, the human oral epithelium and their interplay. Microbiology. 154, 2897-2903;
- Simin F Nakhjiri, Yoonsuk Park, Ozlem Yilmaz, Whasun O Chung, Kiyoko Watanabe, et. al.. (2001). Inhibition of epithelial cell apoptosis byPorphyromonas gingivalis. FEMS Microbiology Letters. 200, 145-149;
- Özlem Yilmaz, Philippe Verbeke, Richard J. Lamont, David M. Ojcius. (2006). Intercellular Spreading of Porphyromonas gingivalis Infection in Primary Gingival Epithelial Cells. IAI. 74, 703-710;
- D. R. Geatch, J. I. Harris, P. A. Heasman, J. J. Taylor. (1999). In vitro studies of lymphocyte apoptosis induced by the periodontal pathogen Porphyromonas gingivalis. J Periodontal Res. 34, 70-78;
- Jan Potempa, Aneta Sroka, Takahisa Imamura, James Travis. (2003). Gingipains, the Major Cysteine Proteinases and Virulence Factors of Porphyromonas gingivalis: Structure, Function and Assembly of Multidomain Protein Complexes. CPPS. 4, 397-407;
- Дареному коню в дёсны не смотрят;
- J.A. Wingrove, R.G. DiScipio, Z Chen, J Potempa, J Travis, T.E. Hugli. (1992). Activation of complement components C3 and C5 by a cysteine proteinase (gingipain-1) from Porphyromonas (Bacteroides) gingivalis.. Journal of Biological Chemistry. 267, 18902-18907;
- Joshua C. Cyktor, Joanne Turner. (2011). Interleukin-10 and Immunity against Prokaryotic and Eukaryotic Intracellular Pathogens. Infect. Immun.. 79, 2964-2973;
- Tomoki Maekawa, Jennifer L. Krauss, Toshiharu Abe, Ravi Jotwani, Martha Triantafilou, et. al.. (2014). Porphyromonas gingivalis Manipulates Complement and TLR Signaling to Uncouple Bacterial Clearance from Inflammation and Promote Dysbiosis. Cell Host & Microbe. 15, 768-778;
- Mark I. Ryder. (2020). Porphyromonas gingivalis and Alzheimer disease: Recent findings and potential therapies. J Periodontol. 91;
- Stephen S. Dominy, Casey Lynch, Florian Ermini, Malgorzata Benedyk, Agata Marczyk, et. al.. (2019). Porphyromonas gingivalisin Alzheimer’s disease brains: Evidence for disease causation and treatment with small-molecule inhibitors. Sci. Adv.. 5, eaau3333;
- На руинах памяти: настоящее и будущее болезни Альцгеймера;
- Возможно, β-амилоид болезни Альцгеймера — часть врождённого иммунитета;
- J. Lönn, S. Ljunggren, K. Klarström-Engström, I. Demirel, T. Bengtsson, H. Karlsson. (2018). Lipoprotein modifications by gingipains ofPorphyromonas gingivalis. J Periodont Res. 53, 403-413;
- Болезнь Альцгеймера: ген, от которого я без ума;
- I'm testing an experimental drug to see if it halts Alzheimer's. (2019). New Scientist.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚