
Тканевая инженерия — окно в современную медицину
19 октября 2011
Тканевая инженерия — окно в современную медицину
- 20112
- 16
- 7
В перспективе тканевая инженерия, если и не приведет к бессмертию, то уж точно сделает решение многих современных проблем медицины более чем реальным.
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Петр I мечтал «прорубить окно в Европу», а ученые нашего времени — окно в современную медицину. Сочетание «медицина + биотехнология» нашло свое отражение в тканевой инженерии — технологии, открывающей возможность восстановления утраченных органов без трансплантации. Методы и результаты тканевой инженерии поражают: это получение живых (а не искусственных!) органов и тканей; регенерация тканей; печать кровеносных сосудов на 3D-принтере; использование «тающих» в организме хирургических шовных нитей и многое другое.
Конкурс «био/мол/текст»-2011
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2011 в номинации «Лучшая обзорная статья».
В последние десятилетия стали отчетливо проявляться тревожные тенденции старения населения, роста количества заболеваний и инвалидизации людей трудоспособного возраста, что настоятельно требует освоения и внедрения в клиническую практику новых, более эффективных и доступных методов восстановительного лечения больных. На рисунке 1 показано, как изменяется структура заболеваний в настоящее время.
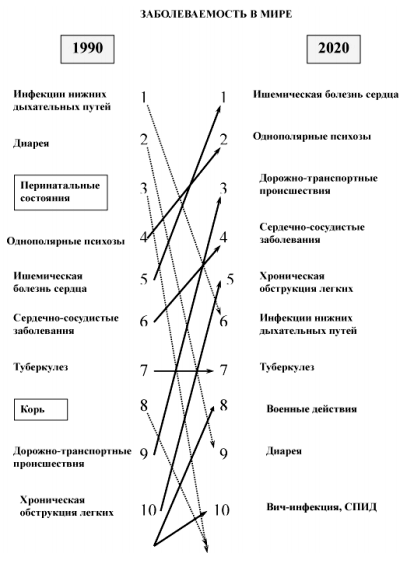
Рисунок 1. Мировая динамика частоты заболеваний.
На сегодняшний день наука и техника предлагает несколько альтернативных путей восстановления или замены поврежденных или пораженных патологией тканей и органов:
- трансплантацию;
- имплантацию;
- тканевую инженерию.
В рамках данной статьи мы подробнее остановимся на возможностях и перспективах тканевой инженерии.
Тканевая инженерия — современная инновационная технология
Принципиально новый подход — клеточная и тканевая инженерия — является последним достижением в области молекулярной и клеточной биологии. Этот подход открыл широкие перспективы для создания эффективных биомедицинских технологий, с помощью которых становится возможным восстановление поврежденных тканей и органов и лечение ряда тяжелых метаболических заболеваний человека.
Цель тканевой инженерии — конструирование и выращивание вне организма человека живых, функциональных тканей или органов для последующей трансплантации пациенту с целью замены или стимуляции регенерации поврежденных органа или ткани. Иными словами, на месте дефекта должна быть восстановлена трехмерная структура ткани.
Важно отметить, что обычные имплантаты из инертных материалов могут устранить только физические и механические недостатки поврежденных тканей, — в отличие от тканей, полученных методом инженерии, которые восстанавливают, в том числе, и биологические (метаболические) функции. То есть, происходит регенерация ткани, а не простое замещение ее синтетическим материалом.
Однако для развития и совершенствования методов реконструктивной медицины на базе тканевой инженерии необходимо освоение новых высокофункциональных материалов. Эти материалы, применяемые для создания биоимплантатов, должны придавать тканеинженерным конструкциям характеристики, присущие живым тканям:
- способность к самовосстановлению;
- способность поддерживать кровоснабжение;
- способность изменять строение и свойства в ответ на факторы окружающей среды, включая механическую нагрузку.
Клетки и матриксы — основа основ для тканевой инженерии
Наиболее важным элементом успеха является наличие необходимого количества функционально активных клеток, способных дифференцироваться, поддерживать соответствующий фенотип и выполнять конкретные биологические функции. Источником клеток могут быть ткани организма и внутренние органы. Возможно использование соответствующих клеток от пациента, нуждающегося в реконструктивной терапии, или от близкого родственника (аутогенных клеток). Могут быть использованы клетки различного происхождения, в том числе первичные (рис. 2) и стволовые клетки (рис. 3).
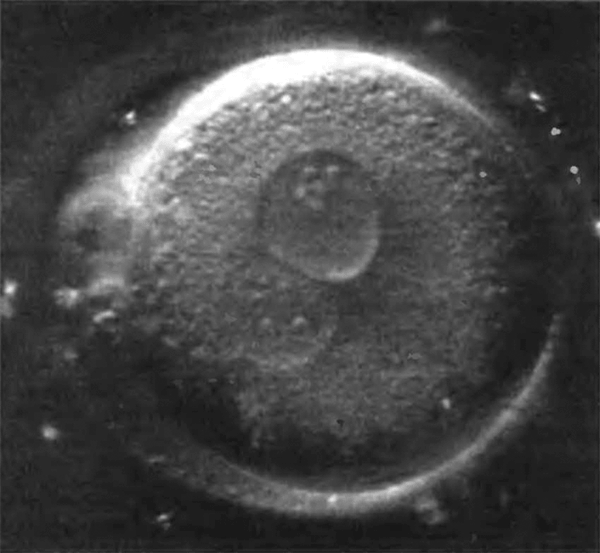
Рисунок 2. Первичная клетка человека.
библиотека Федерации Киокушинкай г. Южноуральска
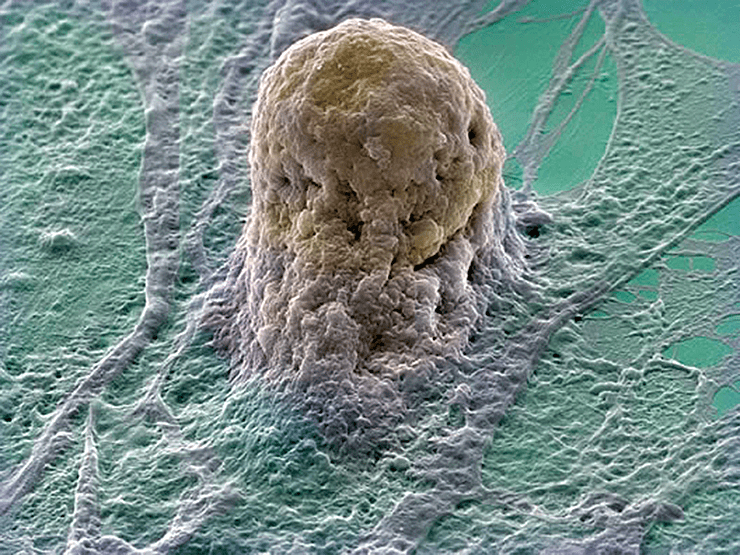
Рисунок 3. Стволовая клетка человека.
Первичные клетки — это зрелые клетки определенной ткани, которые могут быть взяты непосредственно от организма-донора (ex vivo) хирургическим путем. Если первичные клетки взяты у определенного организма-донора, и впоследствии необходимо имплантировать эти клетки ему же в качестве реципиента, то вероятность отторжения имплантированной ткани исключается, поскольку присутствует максимально возможная иммунологическая совместимость первичных клеток и реципиента. Однако первичные клетки, как правило, не способны делиться — их потенциал к размножению и росту низок. При культивировании таких клеток in vitro (посредством тканевой инженерии) для некоторых типов клеток возможна дедифференцировка, то есть потеря специфических, индивидуальных свойств. Так, например, хондроциты, вводимые в культуру вне организма, часто продуцируют фиброзный, а не прозрачный хрящ.
Поскольку первичные клетки не способны делиться и могут потерять свои специфичные свойства, возникла необходимость альтернативных источников клеток для развития технологий клеточной инженерии. Таковой альтернативой стали стволовые клетки.

Рисунок 4. Биокерамические изделия из ортофосфатов кальция.
сайт biomaster.co
Стволовые клетки — недифференцированные клетки, которые имеют способность к делению, самообновлению и дифференцировке в различные типы специализированных клеток под воздействием конкретных биологических стимулов (см.: «Была клетка простая, стала стволовая» [3]). Стволовые клетки подразделяются на «взрослые» [2] и «эмбриональные». Эмбриональные стволовые клетки образуются из внутренней клеточной массы развития зародыша на ранней стадии, а взрослые — из тканей взрослого организма, пуповины или даже плодных тканей. Однако существует этическая проблема, связанная с неизбежным разрушением человеческого эмбриона при получении эмбриональных стволовых клеток [4]. Поэтому предпочтительнее «добыча» клеток из тканей взрослого организма. Так, например, в 2007 году Шинью Яманакой (Shinya Yamanaka) из Киотского университета Японии были открыты индуцированные плюрипотентные стволовые клетки (ИПСК), получаемые из покровных тканей человека (в основном, из кожи). ИПСК открывают поистине невиданные возможности для регенеративной медицины, хотя, прежде чем они всерьез войдут в медицинскую практику, предстоит решить еще немало проблем (см.: «Снежный ком проблем с плюрипотентностью» [5]).
Для направления организации, поддержания роста и дифференцировки клеток в процессе реконструкции поврежденной ткани необходим специальный носитель клеток — матрикс, представляющий из себя трехмерную сеть, похожую на губку или пемзу (рис. 4). Для их создания применяют биологически инертные синтетические материалы, материалы на основе природных полимеров (хитозан, альгинат, коллаген) и биокомпозиты. Так, например, эквиваленты костной ткани получают путем направленной дифференцировки стволовых клеток костного мозга, пуповинной крови или жировой ткани в остеобласты, которые затем наносят на различные материалы, поддерживающие их деление (например, донорскую кость, коллагеновые матрицы и др.).
«Фирменная» стратегия тканевой инженерии
На сегодняшний день одна из стратегий тканевой инженерии такова:
- Отбор и культивирование собственных или донорских стволовых клеток.
- Разработка специального носителя для клеток (матрицы) на основе биосовместимых материалов.
- Нанесение культуры клеток на матрицу и размножение клеток в биореакторе со специальными условиями культивирования.
- Непосредственное внедрение тканеинженерной конструкции в область пораженного органа или предварительное размещение в области, хорошо снабжаемой кровью, для дозревания и формирования микроциркуляции внутри конструкции (префабрикация).
Матриксы через некоторое время после имплантации в организм хозяина полностью исчезают (в зависимости от скорости роста ткани), а в месте дефекта останется только новая ткань. Также возможно внедрение матрикса с уже частично сформированной новой тканью («биокомпозит»). Безусловно, после имплантации тканеинженерная конструкция должна сохранить свои структуру и функции в течение периода времени, достаточного для восстановления нормально функционирующей ткани в месте дефекта, и интегрироваться с окружающими тканями. Но, к сожалению, идеальные матриксы, удовлетворяющие всем необходимым условиям, пока не созданы.
Кровеносные сосуды из принтера
Перспективные тканеинженерные технологии открыли возможность лабораторного создания живых тканей и органов, но перед созданием сложных органов наука пока бессильна. Однако сравнительно недавно ученые под руководством доктора Гунтера Товара (Gunter Tovar) из Общества Фраунгофера в Германии сделали огромнейший прорыв в сфере тканевой инженерии — они разработали технологию создания кровеносных сосудов. А ведь казалось, что капиллярные структуры создать искусственно невозможно, поскольку они должны быть гибкими, эластичными, малой формы и при этом взаимодействовать с естественными тканями. Как ни странно, но на помощь пришли производственные технологии — метод быстрого прототипирования (другими словами, 3D-печать). Подразумевается, что сложная трехмерная модель (в нашем случае кровеносный сосуд) печатается на трехмерном струйном принтере с использованием специальных «чернил» (рис. 5).

Рисунок 5. Технология «печати» искусственного кровеносного сосуда.
Принтер наносит материал послойно, и в определенных местах слои соединяются химически. Однако заметим, что для мельчайших капилляров трехмерные принтеры пока недостаточно точны. В связи с этим был применен метод многофотонной полимеризации, используемый в полимерной промышленности. Короткие интенсивные лазерные импульсы, обрабатывающие материал, так сильно возбуждают молекулы, что они взаимодействуют друг с другом, соединяясь в длинные цепочки. Таким образом, материал полимеризуется и становится твердым, но эластичным, как естественные материалы. Эти реакции настолько управляемы, что с их помощью можно создавать мельчайшие структуры по трехмерному «чертежу».
А для того, чтобы созданные кровеносные сосуды могли состыковаться с клетками организма, при изготовлении сосудов в них интегрируют модифицированные биологические структуры (например, гепарин) и «якорные» белки. На следующем этапе в системе созданных «трубочек» закрепляются клетки эндотелия (однослойный пласт плоских клеток, выстилающий внутреннюю поверхность кровеносных сосудов) — для того, чтобы компоненты крови не приклеивались к стенкам сосудистой системы, а свободно транспортировались по ней.
Однако прежде чем действительно можно будет имплантировать выращенные в лаборатории органы с собственными кровеносными сосудами, пройдет еще какое-то время.
Давай, Россия, давай вперед!
Без ложной скромности скажем, что и в России создана научная основа для практического применения биомедицинских материалов нового поколения. Интересную разработку предложила молодой учёный из Красноярска Екатерина Игоревна Шишацкая (рис. 6) — растворимый биосовместимый полимер биопластотан [7]. Суть своей разработки она объясняет просто: «в настоящее время практические медики испытывают большой дефицит материалов, способных заменить сегменты человеческого организма. Нам удалось синтезировать уникальный материал, который в состоянии заменить элементы органов и тканей человека». Разработка Екатерины Игоревны найдет применение, прежде всего, в хирургии. «Самое простое — это, например, шовные нити, сделанные из нашего полимера, которые растворяются после того, как зарастает рана, — говорит Шишацкая. — Также можно делать специальные вставки в сосуды — стенты. Это маленькие полые трубки, которые используют, чтобы расширить сосуд. Через некоторое время после операции сосуд восстанавливается, а полимерный заменитель растворяется» [8].

Рисунок 6. Лауреат премии Президента РФ Екатерина Игоревна Шишацкая.
Первый опыт трансплантации тканеинженерной конструкции в клинике

Рисунок 7. Паоло Маккиарини, мастер-класс которого «Клеточные технологии для тканевой инженерии и выращивания органов» прошел в Москве в 2010 году.
Осенью 2008 года руководитель клиники Университета Барселоны (Испания) и Медицинской школы Ганновера (Германия) профессор Паоло Маккиарини (Paolo Macchiarini; рис. 7) провел первую успешную операцию по трансплантации биоинженерного эквивалента трахеи пациентке со стенозом главного левого бронха на протяжении 3 см (рис. 8) [11].
В качестве матрикса будущего трансплантата был взят сегмент трупной трахеи длиной 7 см. Чтобы получить природную матрицу, по свойствам превосходящую все то, что можно сделать из полимерных трубок, трахею очистили от окружающей соединительной ткани, клеток донора и антигенов гистосовместимости. Очищение заключалось в 25 циклах девитализации с применением 4%-деоксихолата натрия и дезоксирибонуклеазы I (процесс занял 6 недель). После каждого цикла девитализации проводили гистологическое исследование ткани для выявления количества оставшихся ядросодержащих клеток, а также иммуногистохимическое исследование на наличие в ткани антигенов гистосовместимости HLA-ABC, HLA-DR, HLA-DP и HLA-DQ. Благодаря биореактору собственной разработки (рис. 9) ученые на поверхность медленно вращающегося отрезка трахеи равномерно нанесли шприцем суспензию клеток. Затем трансплантат, наполовину погруженный в среду для культивирования, вращался вокруг своей оси с целью попеременного контакта клеток со средой и воздухом.
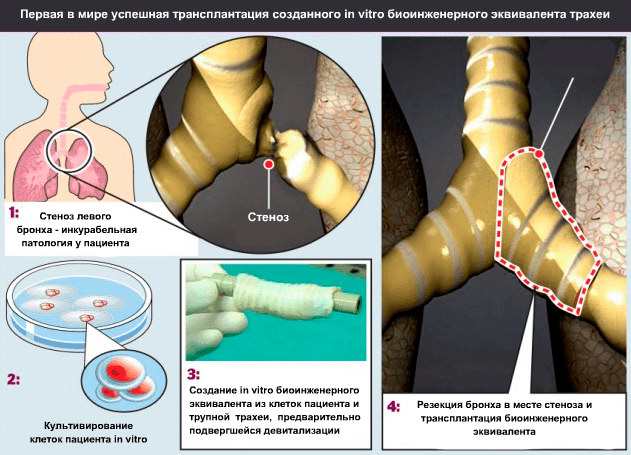
Рисунок 8. Операция по пересадке пациентке трахеи.
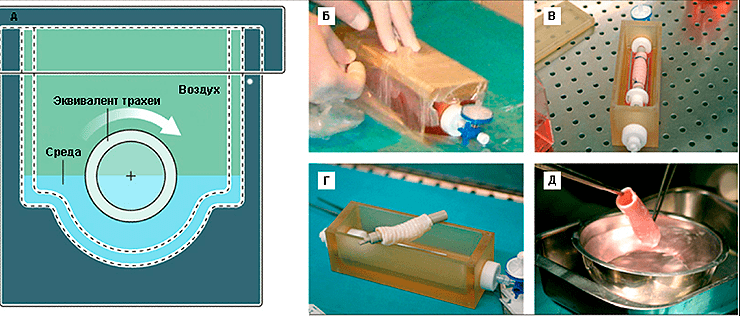
Рисунок 9. Биореактор для создания тканеинженерного эквивалента трахеи. А — схема биореактора, вид с боку. Б — герметизация биореактора. В — биореактор с тканеинженерным эквивалентом трахеи in situ. Г — биореактор после удаления эквивалента трахеи. Д — вид эквивалента трахеи непосредственно перед операцией.
Эквивалент трахеи находился в биореакторе 96 часов; затем его трансплантировали пациентке. При операции был полностью удален главный левый бронх и участок трахеи, к которому он примыкал. В образовавшийся промежуток вшили трансплантат, а некоторое несоответствие диаметров просветов тканеинженерного эквивалента и бронха реципиента было преодолено благодаря эластичности донорской ткани.
По истечении десяти суток после операции пациентка была выписана из клиники без признаков дыхательной недостаточности и иммунной реакции отторжения трансплантата. По данным компьютерной томографии, с помощью которых была сделана виртуальная 3D реконструкция дыхательных путей, тканеинженерный эквивалент был практически неотличим от собственных бронхов пациентки (рис. 10).
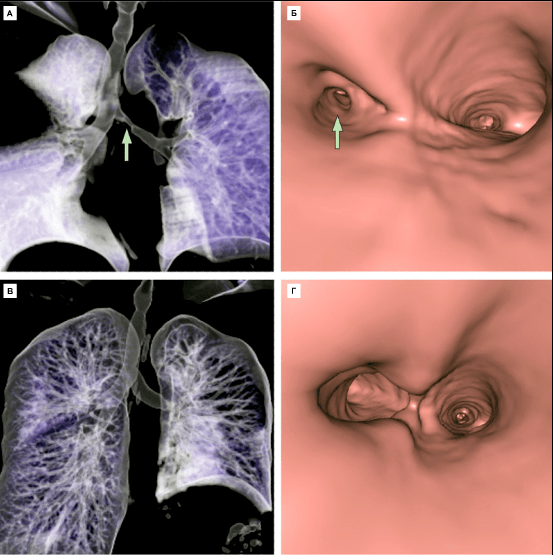
Рисунок 10. Виртуальная 3D-реконструкция дыхательных путей по данным компьютерной томографии и бронхоскопии перед операцией (А, Б) и через 1 месяц и после замены стенозного участка левого главного бронха тканеинженерным эквивалентом (В, Г). Стрелкой указан стеноз.
Литература
- Волова Т.Г. Материалы для медицины, клеточной и тканевой инженерии. Красноярск: ИПК СФУ, 2009;
- «Взрослые стволовые клетки». RusDocs;
- Была клетка простая, стала стволовая;
- Щадящие стволовые клетки;
- Снежный ком проблем с плюрипотентностью;
- Woollacott E. (2011). Artificial blood vessels made through 3D printing. TechGuru Daily;
- Шишацкая Е. И. (2010). «БИОПЛАСТОТАН: совместим с жизнью». «Наука из первых рук»;
- «Научная разработка, созданная молодой красноярской ученой, вызвала большой интерес среди медиков». (2010). Medvestnik.ru;
- Трофимов И. (2010). «Лауреат премии Президента РФ Екатерина Шишацкая: „Премиальные потрачу на себя и свою семью“». «Комсомольская правда»;
- Bates C. (2012). Patients will 'grow' new organs from their own cells to replace failing body parts, says pioneering surgeon. DailyMail;
- «Первая успешная трансплантация тканеинженерной трахеи в клинике». (2008). «Гены и клетки».
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





