ВКонтакте на молекулярном уровне, или как органеллы общаются между собой
24 марта 2026
ВКонтакте на молекулярном уровне, или как органеллы общаются между собой
- 164
- 0
- 2
Мембранные контакты во многом напоминают транспортные пути, соединяющие различные пункты в огромном клеточном «городе».
Рисунок в полном размере.
сгенерировано Gemini 3.0
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Представление об органеллах как о независимых друг от друга клеточных «органах» доминировало в биологической науке на протяжении нескольких десятков лет. Однако последние исследования показывают, что органеллы не выполняют свои функции изолированно, а активно координируют свою деятельность, общаясь друг с другом посредством так называемых «мембранных контактов» (MCSs, от англ. membrane contact sites). В этой статье мы разбираемся, как устроена сложная сеть взаимодействий между органеллами, какую роль она играет во внутриклеточных процессах и почему нарушение ее работы может иметь серьезные последствия не только на уровне клетки, но и целого организма.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Что представляют собой мембранные контакты?
Несмотря на многочисленные работы об организации, функционировании и разнообразии мембранных контактов, не так просто дать точное определение этому понятию. Основная сложность заключается в том, что необходимо отличать реальные, функционально значимые контакты от простых стохастических взаимодействий между компартментами, которые в клетках происходят постоянно. Итак, что же мы все-таки понимаем под этим термином? Прежде всего, это некая специализированная область, в пределах которой мембраны двух органелл находятся на достаточно близком расстоянии (в среднем около 30 нм) друг от друга, позволяя тем самым обоим «участникам» обмениваться между собой различными соединениями (ионами, липидами, метаболитами) и координировать свою деятельность. Кроме того, подразумевается, что слияния между органеллами не происходит, а везикулярный транспорт не является основным механизмом обмена веществ [1], [2].
Тем не менее, даже это довольно широкое определение не охватывает всего многообразия мембранных контактов, известных на сегодняшний день. В качестве наглядных примеров можно привести следующие факты [3–5]:
- Подобные контакты могут существовать как между одинаковыми, так и различными органеллами (так называемые «гомотипные» и «гетеротипные» контакты, соответственно);
- Мембранные контакты «вездесущи» — каждая органелла внутри клетки «касается» хотя бы одной другой органеллы (а чаще всего нескольких одновременно);
- Хотя, как отмечалось выше, классические контакты формируются парой органелл, известны менее распространенные случаи образования «тройных» мембранных контактов (другими словами, подобные MCSs включают три различные органеллы в одном и том же физическом сайте);
- MSCs не являются статичными структурами (примерное время их существования колеблется от доли секунд до нескольких минут); более того, характер их образования тесно взаимосвязан с клеточной регуляцией и может меняться в зависимости от различных условий. Один из примеров такой «динамичности» — образование контактов между ЭПР и плазматической мембраной в ответ на истощение ионов кальция — мы подробно рассмотрим ниже;
- Мембранные контакты играют огромную роль в процессах аутофагии («поедания» клеткой находящихся внутри нее «мусорных» компонентов) и деления органелл;
- Наконец, близкие к такому типу контакты могут формироваться внутри органелл (например, в пределах эндоплазматического ретикулума) или же включать немембранный компартмент! Примером последнего может служить взаимодействие телец включения (т. е. маленьких частиц, состоящих в основном из «неправильно» свернутых белков) с липидными каплями.
Разумеется, теоретически число органелл, формирующих один контакт, может быть неограниченным, однако на практике экспериментальные свидетельства образования «мульти-органелльных» контактов (четыре и более органелл) очень скудны.
Как же возможно охарактеризовать такое разнообразное множество?
Чаще всего органеллы соблюдают дистанцию. Но есть и исключения…
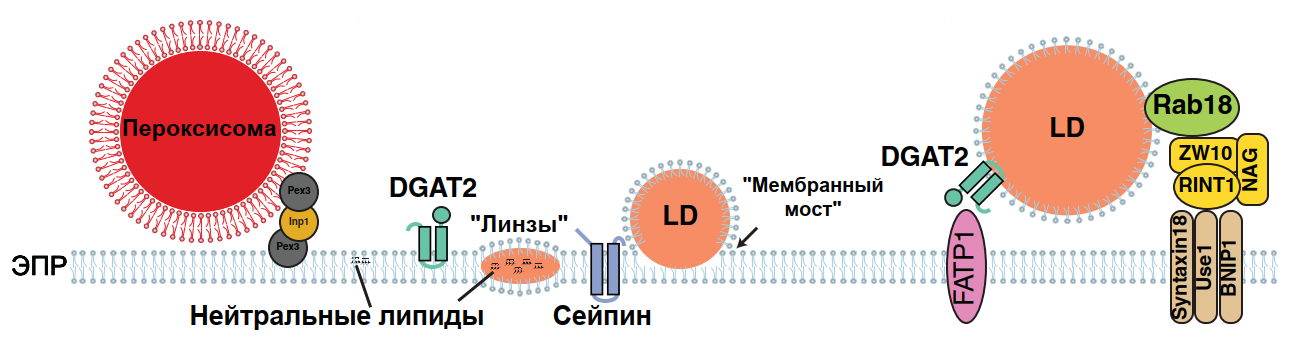
Рисунок 1. Мембранные контакты между эндоплазматическим ретикулумом (ЭПР) и органеллами-производными ЭПР. В процессе биогенеза предшественники липидных капель (так называемые «липидные линзы») аккумулируются в мембране ЭПР, прежде чем трансформироваться в полноценную каплю (в чем принимают участие различные белки вроде сейпина). Липидные капли, связанные с мембраной ЭПР посредством «мембранного моста», могут вскоре отпочковаться и образовать обычный контакт (с участием белков FATP1, DGAT2, а также белков семейства SNARE). Также показаны контакты между ЭПР и пероксисомами.
адаптировано из [7]
Для начала определим основные черты, характерные для «истинных» мембранных контактов [6]. Пока ограничимся рассмотрением лишь того случая, когда во взаимодействие вступают только две органеллы (хотя сказанное может быть легко обобщено и на другие примеры). В первую очередь, как было отмечено выше, при образовании контактов не происходит слияния компартментов. Такой критерий позволяет нам отсеять различные интермедиаты этого процесса, поскольку их природа носит иной характер. Тем не менее, есть одно очень важное исключение из этого правила: специфическое взаимодействие между липидными каплями и эндоплазматическим ретикулумом (рис. 1) [7]. Образование такого неканонического контакта возможно благодаря особенности строения липидных капель, содержащих монослой фосфолипидов вместо привычного бислоя. В результате образования подобных контактов (часто называемых «мембранными мостами», англ. membrane bridges) мембрана липидной капли плавно переходит во внешний слой мембраны ЭПР. Такой «мост» позволяет осуществить передачу нейтральных липидов в формирующуюся каплю в процессе биогенеза (механизм которого еще недостаточно изучен) и может сохраниться в течение всей ее жизни. Некоторая часть липидных капель, тем не менее, благополучно отпочковывается от ЭПР, но может впоследствии реинтегрироваться и снова сформировать аналогичный мембранный контакт [7]. Отметим также, что липидные капли также могут «касаться» мембраны ЭПР каноническим способом, к описанию которого мы и возвращаемся.
«Якорные» белки — главный способ молекулярного «рукопожатия» в мире органелл
Кроме отсутствия слияния, мембранные контакты, по определению, должны характеризоваться наличием физических взаимодействий, удерживающих органеллы на определенном расстоянии друг от друга и имеющих белок-белковую либо же белок-липидную природу (такое явление часто обозначают как «тетеринг», англ. tethering). При этом конкретное расстояние между мембранами варьируется от 10 до 80 нм, однако в некоторых случаях может превышать 300 нм. В связи с этим разумно отмечают, что близкое расположение органелл друг относительно друга само по себе не определяет мембранных контактов [6]. Как же именно связаны между собою обе органеллы? Главными (но не единственными) «посредниками» таких взаимодействий являются определенные группы белков (так называемые «белки-якоря», англ. tethering proteins), поскольку именно они играют основную роль в удержании двух органелл на определенной дистанции (хотя, разумеется, определенный вклад вносят и электростатические взаимодействия между липидами и белками, структуры цитоскелета и другие факторы). Ниже мы познакомимся с несколькими примерами таких белков, а пока ограничимся перечислением минимальных критериев, позволяющих классифицировать данный белок как «якорь»:
- очевидно, изучаемый белок должен быть в рассматриваемом мембранном контакте;
- «якорный» белок, кроме того, характеризуется наличием:
- структурных черт (доменов или мотивов), позволяющих ему взаимодействовать с обеими мембранами;
- функциональной активности, которая выражается в «удержании» двух мембран, составляющих контакт.
Польза данных критериев заключается в том, что наличие каждого из них может быть показано экспериментально. Заметим, что некоторые мембранные контакты вовсе не содержат четкого, специализированного «якоря», но «удерживаются» благодаря множественным белок-белковым и белок-липидным взаимодействиям. Кроме того, функция «удерживания» может оказаться для данного белка вторичной, существующей наряду с его основной функцией, которая никак не связана с организацией контакта. Например, как мы увидим ниже, белок OSBP, отвечающий за транспорт липидов между ЭПР и аппаратом Гольджи, также «подрабатывает» в качестве «якоря» для сцепления данных органелл друг с другом [8].
Общение между органеллами не может быть безрезультатным!
Наконец, какой бы контакт ни рассматривался, он должен выполнять специфическую функцию. Поскольку большинство мембранных контактов первоначально было изучено на примере ЭПР, долгое время в качестве основных функций называли кальциевый и липидный обмен между органеллами. С течением времени спектр исследованных контактов заметно расширился, в связи с чем наше представление о функциональной значимости этих структур претерпело серьезные изменения. На данный момент мы можем с уверенностью утверждать, что мембранные контакты принимают непосредственное участие не только в транспорте липидных молекул или ионов кальция, но и в таких значимых для клетки процессах, как [11]:
- передача сигналов между компартментами;
- деление, позиционирование (т. е. «закрепление» органелл в определенном месте внутри клетки) и трафик органелл;
- поддержание физической и структурной организации клетки;
- адаптация к клеточному стрессу (включая воспаление, апоптоз, формирование аутофагосомы, образование и регуляция активных форм кислорода) и др.
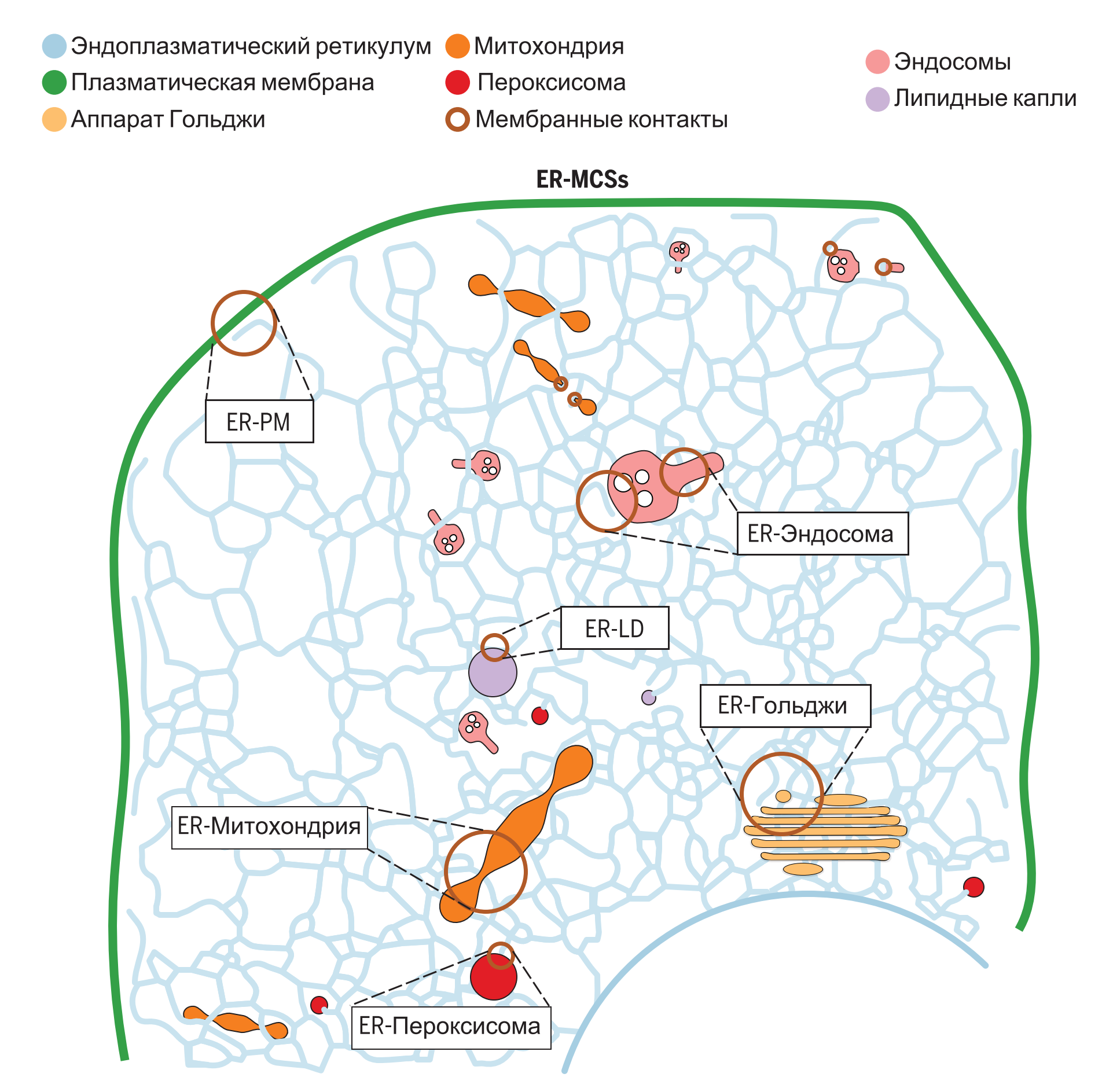
Рисунок 3. Разнообразие ЭПР-опосредованных контактов. Как изображено на рисунке, эндоплазматический ретикулум (ER) образует мембранные контакты с митохондриями, аппаратом Гольджи, эндосомами, пероксисомами и другими органеллами, а также с плазматической мембраной (PM). Эти контакты играют незаменимую роль в таких внутриклеточных процессах, как обмен липидами и ионами, позиционирование органелл и их биогенез.
адаптировано из [7]
Значимость мембранных контактов дополнительно подтверждается тем, что нарушение функционирования контактома (т. е. совокупности всех мембранных контактов как единого целого) может быть вовлечено в развитие разного рода заболеваний, включая паркинсонизм, болезнь Альцгеймера и некоторые вирусные инфекции (эту тему мы вкратце затронем ниже) [12].
После некоторого знакомства с общей организацией мембранных контактов перейдем к более детальному обсуждению их роли в жизнедеятельности клеток, рассмотрев некоторые наиболее значимые примеры.
| Парные контакты с участием ЭПР или митохондрий | |
| Эндоплазматический ретикулум — ... | — Митохондрия |
| — Липидная капля | |
| — Аппарат Гольджи | |
| Митохондрия — ... | — Пероксисома |
| — ПМ | |
| — Лизосома | |
| Другие типы контактов | |
| Парные контакты без участия ЭПР и митохондрий | Пероксисома — липидная капля |
| Лизосома — пероксисома | |
| Лизосома — ПМ | |
| Тройные контакты | ЭПР — митохондрия — ПМ |
| ЭПР — митохондрия — липидная капля | |
| ЭПР — митохондрия — аппарат Гольджи | |
| Ядро — вакуоль — липидная капля | |
ПМ — плазматическая мембрана |
|
Эндоплазматический ретикулум формирует обширную сеть контактов с органеллами клетки
Среди всего множества органелл клетки эндоплазматический ретикулум (ЭПР) занимает особое место: будучи представленным сетью внутриклеточных трубочек и цистерн, «разбросанных» по всей цитоплазме, ЭПР способен формировать мембранные контакты практически с каждым своим «соседом» (рис. 3). Схожим свойством обладают и митохондрии, вследствие чего обе органеллы могут быть положены в основу классификации всех мембранных контактов на несколько отдельных категорий (см. таблицу) [13]. (Как мы помним, единой терминологии в данной области пока нет, однако обозначенного подхода в рамках данного обзора будет вполне достаточно). Согласно данной таблице, ниже речь пойдет об ЭПР-опосредованных двунаправленных контактах, т. е. о MSCs, сформированных двумя органеллами, одна из которых представлена эндоплазматическим ретикулумом. Н
Мембранные контакты позволяют органеллам осуществлять липидный обмен
Обмен липидными молекулами между различными компартментами играет неотъемлемую роль в клеточном метаболизме: он крайне необходим для формирования полноценных мембран, распределения липидов между органеллами от места их синтеза (ЭПР, собственно, и является таким источником), регуляции сигнальных путей и многих других процессов. Однако передача «голого» липида через цитоплазму является энергетически невыгодной вследствие гидрофобности этих молекул, в связи с чем существуют два принципиальных пути липидного обмена между компартментами: везикулярный (т. е. задействующий везикулу в качестве «посредника») и невезикулярный. Зачем клеткам понадобился альтернативный механизм липидного трафика в обход везикулярного?
Тому есть несколько причин. Во-первых, невезикулярный путь может выполнять множество функций, не реализуемых при участии везикул (к примеру, это может быть доставка липидов с минимальным количества белка, корректировка «нежелательного» обмена липидами, происходящего при везикулярном транспорте, быстрое изменение липидома при определенных условиях и др.). Во-вторых, для таких жизненно важных органелл, как митохондрии (а также хлоропласты в растительных клетках), которые не способны синтезировать большую часть необходимых липидов самостоятельно, везикулярный транспорт принципиально невозможен, и в этом случае альтернативный путь является единственным доступным вариантом (заметим, что именно путем невезикулярного транспорта осуществляется большая часть липидного обмена) [14]. Именно мембранные контакты являются основным местом протекания невезикулярного транспорта [15].
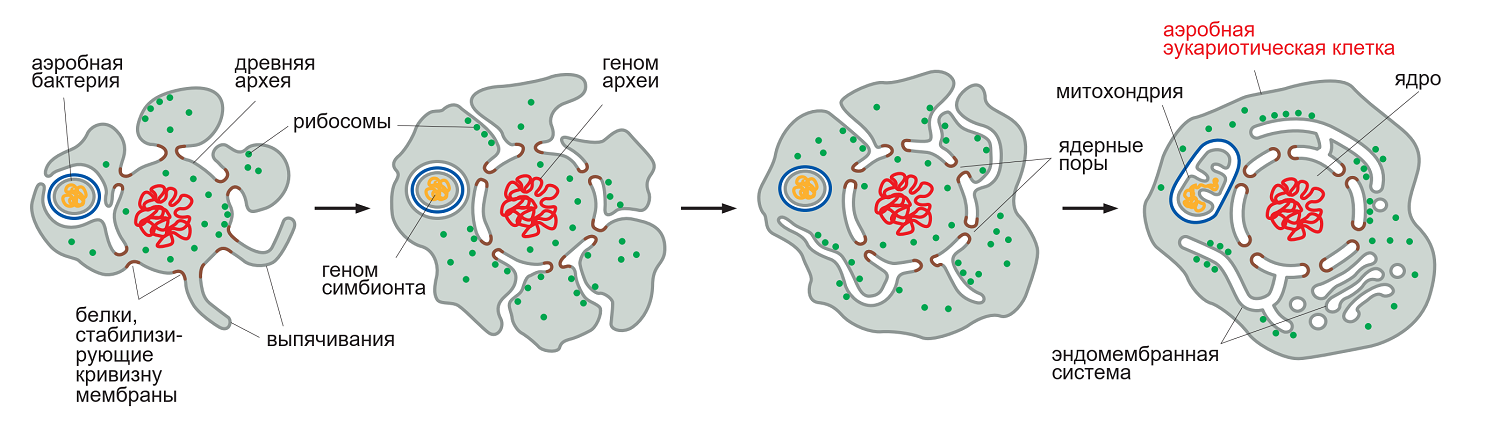
Рисунок 4. Эволюционное происхождение эндомембранной системы в клетках эукариот. Пояснения в тексте.
адаптировано из [15]
Липид-транспортирующие белки — основной «туннель» для пересечения липидами опасной дистанции
Одну из главных ролей в невезикулярном транспорте липидов играют так называемые липид-транспортирующие белки, или LTPs (англ. lipid transport proteins), большая часть которых локализована в мембранных контактах. Данная группа белков содержит в своей структуре гидрофобную поверхность, благодаря которой липидная молекула «изолируется» от водного окружения в процессе транспорта между компартментами. Несмотря на огромное разнообразие LTPs (описано более двух десятков семейств), их можно разделить на три группы в зависимости от механизма переноса липидных молекул: белки-«челноки» (наиболее распространенная подгруппа LTPs, переносящих липиды между мембранами «челночным» способом, см. рис. 5), белки-«мосты» и белки-«трубки» (оба типа представляют собой «каналы» или «туннели», по которым липиды перемещаются между органеллами, при этом только белки последней подгруппы имеют полностью замкнутую полость) [17].
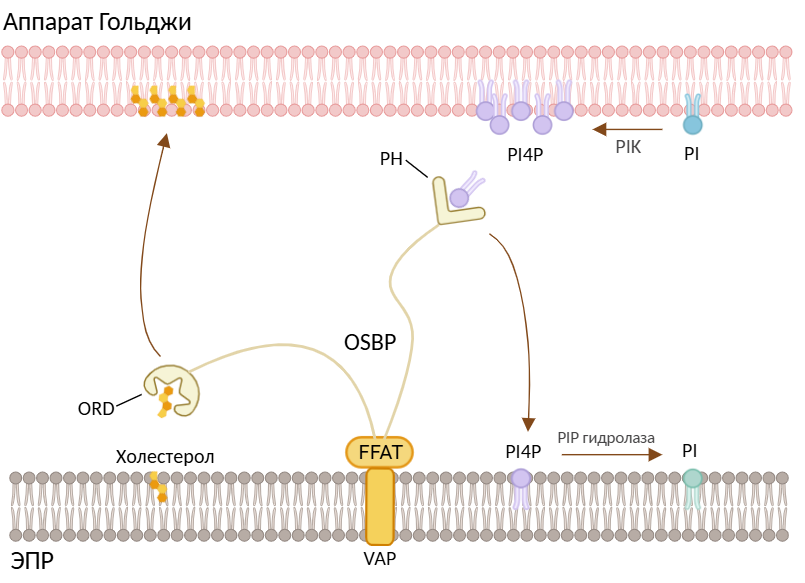
Рисунок 6. Транспорт холестерола от аппарата Гольджи к мембране ЭПР с помощью белка OSBP. Пояснения в тексте.
рисунок создан с помощью BioRender на основе статьи [1]
Многие белки, переносящие липиды, имеют в своей структуре несколько дополнительных доменов для «коммуникации» с мембраной. Так, в мембранных контактах между ЭПР и плазматической мембраной часто находятся белки, имеющие специфический домен для взаимодействия с трансмембранными белками VAPs (англ. vesicle-associated membrane-protein-associated proteins), а также отдельный домен для связывания с фосфатидилинозитолом-4,5-бисофосфатом — липидом, локализованным в плазматической мембране. Наглядным примером может служить упоминавшийся ранее белок OSBP (англ. oxysterol-binding protein), который «катализирует» один из этапов метаболизма фосфоинозитидов (небольшого семейства липидов, играющих важную роль в передаче клеточных сигналов) в мембранных контактах между ЭПР и ПМ, а также ЭПР и комплексом Гольджи (рис. 6). Источником фосфатидилинозитола (PI) — предшественника остальных фосфоинозитидов — является ЭПР, откуда он транспортируется к обеим органеллам и претерпевает фосфорилирование соответствующими киназами (с образованием фосфатидилинозитол-4-фосфата, PI4P). Перенос липидов опосредуется различными LTPs, такими как Nir2 (у млекопитающих) или Sec14 (у дрожжей), причем некоторые из них (тот же OSBP) способны одновременно транспортировать несколько различных липидных молекул в противоположных направлениях. Так, PI4P мигрирует в эндоплазматический ретикулум, гидролизуясь там до исходного фосфатидилинозитола, в то время как другой липид (например, фосфатидилсерин, PS) перемещается в плазматическую мембрану.
Белок OSBP, в свою очередь, играет важную роль в переносе холестерола от ЭПР (места его синтеза) к аппарату Гольджи (откуда он может, например, встраиваться в плазматическую мембрану посредством везикулярного транспорта), параллельно транспортируя второго «пассажира» в лице PI4P в противоположном направлении (см. рис 6). С этой целью OSBP задействует несколько ключевых доменов: ORD (связывает холестерол и его производные), FFAT (взаимодействует с VAP мембраны ЭПР) и PH (распознает PI4P в мембране комплекса Гольджи). Цикл транспорта холестерола в общих чертах состоит из нескольких стадий [18]:
- Мембраны обеих органелл при помощи OSBP сближаются на необходимое расстояние (это обеспечивается взаимодействиями FFAT с VAP и PH с PI4P);
- Домен ORD «вытаскивает» холестерол из мембраны ЭПР и транспортирует его к аппарату Гольджи;
- Тот же домен ответственен за противоположный транспорт PI4P от мембраны комплекса Гольджи к ЭПР;
- На заключительной стадии PI4P претерпевает гидролиз (катализируемый ферментом Sac1) с образованием фосфатидилинозитола.
Итак, мы снова вернулись к PI, с которого, фактически, и начали нашу беседу. Для чего же, собственно, необходимо было задействовать циклическое перемещение этого липида? Дело в том, что изначальные уровни холестерола в мембранах аппарата Гольджи и ЭПР кардинально различаются: первый содержит гораздо больше молекул холестерола чем последний. По этой причине холестерол не может перемещаться к аппарату Гольджи без дополнительной затраты энергии. В этом ему как раз и помогает PI: поскольку после миграции в мембрану комплекса Гольджи фосфатидилинозитол сразу же претерпевает фосфорилирование до PI4P, то уровень последнего в данном месте быстро накапливается. Но выше мы отметили, что каждая молекула PI4P при своем «возвращении» в ЭПР тут же гидролизуется, регенерируя PI. Другими словами, количество PI4P в мембране эндоплазматического ретикулума предельно мало по сравнению с таковым для аппарата Гольджи, что и является основным «драйвером» транспорта холестерола в необходимом направлении.
Схожие принципы реализуется в трафике других видов липидов. Так, мембранный контакт ЭПР-Гольджи, кроме OSBP, также содержит белки CERT (ответственен за транспорт церамида) и FAPP2 (транспортирует гликозилцерамид), причем оба LTP структурно близки к разобранному выше OSBP (хоть и не задействуют PI4P в ходе транспорта). Разумеется, известно множество примеров липид-транспортирующих белков, расположенных в других типах контактов. Примерами могут служить дрожжевые комплексы ERMES (между ЭПР и митохондриями) и vCLAMP (между митохондриями и вакуолью), которые являются хорошими моделями для изучения принципов организации и функционирования LTPs [19].
Мембранные контакты являются динамическими хабами кальциевого сигналинга
О незаменимой роли ионов кальция в самых разнообразных клеточных процессах было сказано предостаточно [20] . В частности, Ca2+ является одним из главных участников в механизме сокращения скелетных мышц: его взаимодействие с тропониновым комплексом запускает процесс связывания «головки» миозина с актином, инициируя тем самым процесс сокращения. Основным «донором» ионов кальция для этого процесса является эндоплазматический ретикулум (в случае скелетных мышц также называемый «саркоплазматическим ретикулумом», СПР), из которого Ca2+ буквально «выкачивается» при достижении потенциалом действия мышечной клетки. Что же произойдет, если скелетные мышцы будут испытывать постоянную нагрузку (например, в ходе выполнения сложных физических упражнений)? Очевидно, подобные тренировки приведут к истощению пула ионов кальция в саркоплазматическом ретикулуме, в связи с чем должен существовать специальный механизм его пополнения. Принципиальный путь восстановления уровня Ca2+ связан с работой SERCA (англ. Sarcoplasmic/Endoplasmic Reticulum Ca2+-ATPase) — помпы (или «насоса»), локализованной в мембране СПР, которая активно «закачивает» кальций обратно, пытаясь восполнить его потери в ходе сокращения [21]. Но что, если интенсивность выполняемых упражнений превосходит возможности транспортера (который имеет ограниченную скорость работы даже при оптимальной доступности АТФ)?
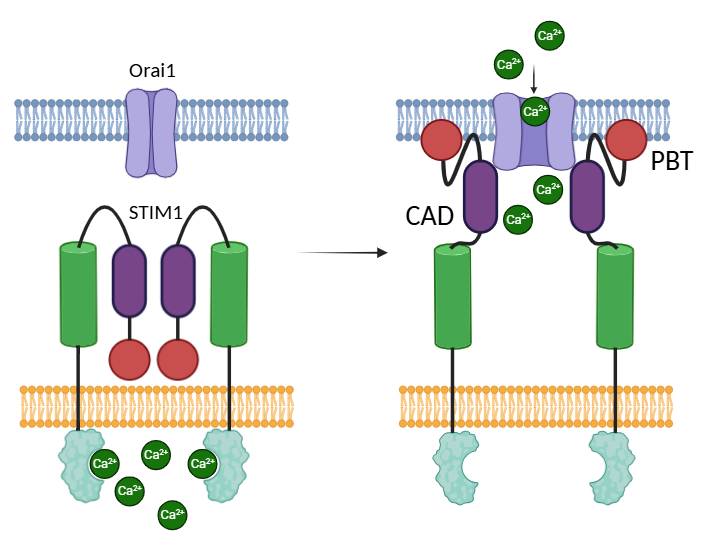
Рисунок 7. Молекулярный механизм пополнения пула ионов кальция в эндоплазматическом ретикулуме. Желтым цветом обозначена мембрана ЭПР, синим — плазматическая мембрана. Пояснения в тексте.
рисунок создан с помощью BioRender на основе статьи [21]
По этой причине требуется некий дополнительный механизм пополнения пула ионов кальция в саркоплазматическом ретикулуме, причем, как можно догадаться, в качестве источника Ca2+ должно выступать внеклеточное пространство. Мы можем сделать вывод, что состояние дефицита ионов кальция в СПР обязано каким-то путем «передаваться» через плазматическую мембрану для инициации поступления Ca2+ извне. Именно здесь вспоминаются известные нам контакты ЭПР-ПМ, которые, судя по всему, должны быть задействованы в механизме восстановления уровня ионов кальция. И в самом деле, было показано, что интенсивная нагрузка приводит к ремоделированию саркоплазматической системы с образование дополнительных контактов между СПР и Т-трубочками (участкам ПМ, ответственных за один из этапов «передачи» сигнала к сокращению) [22].
Дополнительный механизм, о котором только что шла речь, носит название SOCE (англ. store-operated Ca2+ entry); основные участники этого процесса изображены на рисунке 7. Механизм этого процесса довольно прост: в обычных условиях (ЭПР содержит достаточное количество ионов кальция) димерный белок STIM1, располагающийся в мембране эндоплазматического ретикулума, образует комплекс с Ca2+ и в этом состоянии не соприкасается с компонентами плазматической мембраны. Когда же в ЭПР ионов кальция недостаточно, STIM1 меняет свою конформацию, олигомеризуется (на рисунке не показано) и взаимодействует посредством цитозольных доменов с кальциевым каналом Orai1. Последний при контакте с белком STIM1 открывается, в результате чего дополнительные количества ионов кальция поступает в цитозоль и тут же «закачиваются» в ЭПР при помощи SERCA [21].
Как их вообще изучать?
Итак, теперь мы имеем некоторое представление о том, как мембранные контакты устроены и насколько они важны для правильного функционирования «клеточного организма». Однако понимание важности этих структур, равно как и детали их строения, пришло к ученым не сразу.
Что есть случайность, а что выбор?
Как мы видели выше, контакты между мембранами вообще бывают разными, от случайных взаимодействий до чего-то более организованного. Как же их отличать и изучать?
Исторически именно биохимические методы позволили ученым впервые заметить, что органеллы способны «контактировать» друг с другом. Классическим примером является обнаружение участков ЭПР, содержащих митохондриальную фазу. Однако анализ белков в этой смеси показал, что фракции были насыщены ферментами, участвующими в синтезе и переносе липидов. Так были описаны одни из первых функциональных MCS.
Получение высокоочищенных фракций — задача нетривиальная, поскольку она полностью зависит как от тех протоколов, которые мы выберем (лизиса клеток, условий центрифугирования), так и условий, в которых проводится выделение; все это влияет на стабильность и степень очистки контактов. Дальнейший же анализ может проводиться при помощи распространенных аналитических методов. Так, с помощью вестерн-блоттинга можно описать тип изучаемых контактов, а присутствие новых, не охарактеризованных белков можно подтвердить при помощи ко-иммунопреципитации, аффинной хроматографии, масс-спектрометрии и других известных методов.
Чтобы понять, где находится сам контакт, разработано много методов, которые в полной мере реализуют свой потенциал при помощи различных неординарных подходов. Например, для детекции расположения контакта внутри клетки и подтверждения того, что контакт не является случайным, используется реакция присоединения биотина к белку, или же биотинилирование (рис. 8). Фермент, «привязанный» к белку-якорю на изучаемой мембране, при добавлении биотинового фенола и перекиси водорода модифицирует все белки в радиусе 10–20 нм, присоединяя метку (молекулу биотина). Потом дело останется за малым: выделил и идентифицировал белки с меткой и карта контакта готова [2].
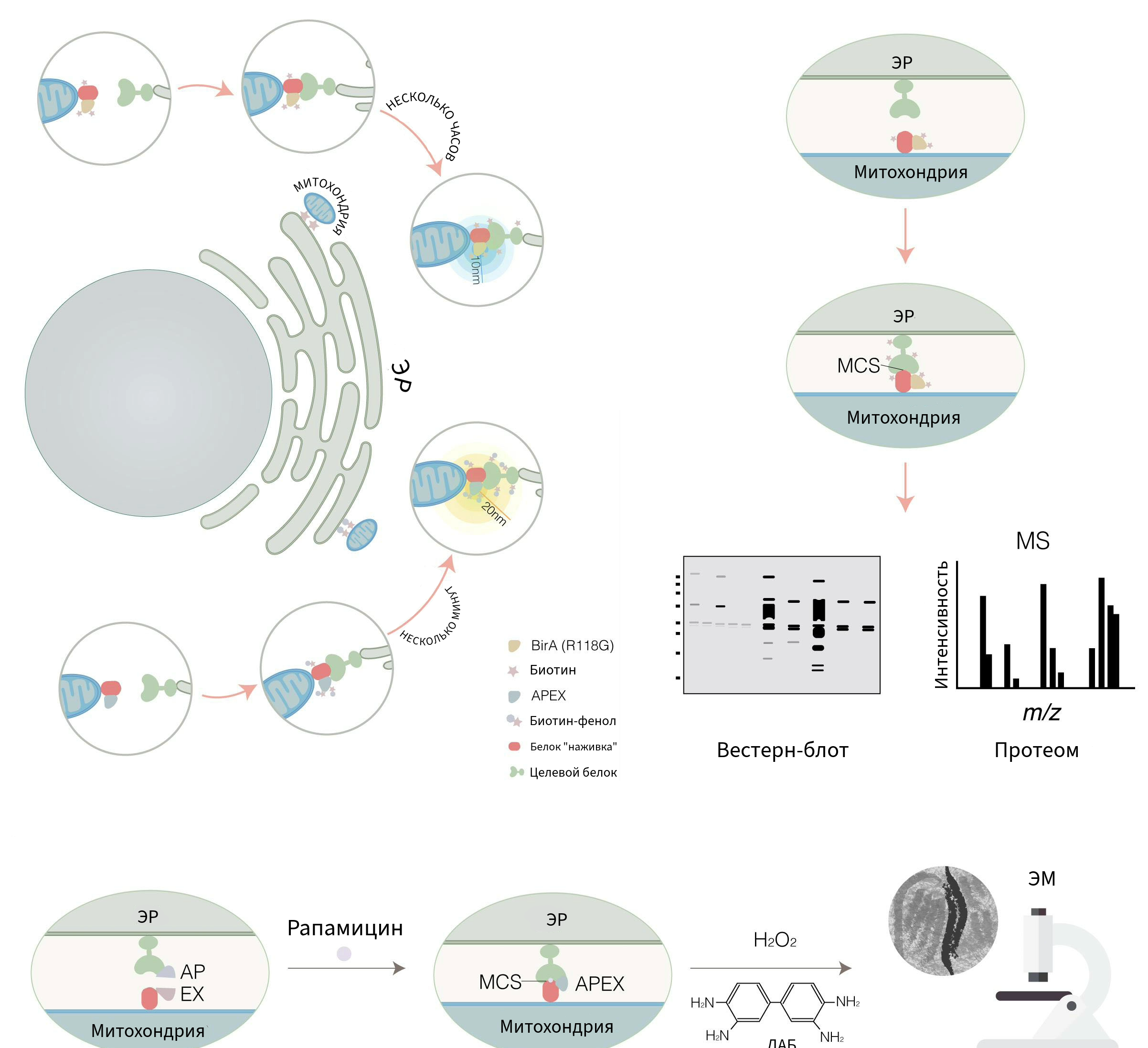
Рисунок 8. Методы, использующие биотинилирование как основной метод для изучения мембранных контактов.
адаптировано из [2]
А как же электронная микроскопия?
Как только электронная микроскопия получила широкое распространение, она стала одним из основных методов, применяемых для анализа клеточных структур. И при обсуждении любой клеточной структуры сразу же возникает вопрос: применяется ли данный метод при изучении интересующего нас объекта, и если да, то зачем же нам нужны все эти усложнения c применением множества косвенных исследований? Современные микроскопические подходы позволяют получить хорошие модели контактов, однако такие методы являются крайне трудоемкими. Кроме того, агрессивная химическая фиксация не позволяет нам изучать живые клетки и повышает риск появления артефактов.
А в жизни оно как?
Всякая живая система динамична: каждый ее элемент — это что-то большее, чем фиксированная клеточная структура. Чтобы по-настоящему изучить клетку, нужно рассматривать ее элементы в динамике.
Здесь нашли свое применение небезызвестные генетически кодируемые флуоресцентные белки. Измеряя степень перекрытия сигнала, можно определить его уровень. Однако даже конфокальная микроскопия не всесильна: ее дифракционный предел составляет 200–500 нм. Частично эта проблема решается при помощи TIRFM — «супер-микроскопа», сканирующего не весь образец, а только его самую верхнюю часть, подобно лучу прожектора, проходящему по поверхности земли. Для того, чтобы заглянуть за дифракционный предел, разработаны методы «суперразрешения» (SIM, STED, PALM/STORM). Основной их особенностью является то, что только небольшая группа флуорофоров активируется и регистрируется, а затем по полученным данным компьютер восстанавливает изображение. Обрабатывать такие данные дорого и сложно, поэтому данные методы зачастую применяются только высоко специализированных лабораториях.
Как упоминалось ранее, косвенные подходы являются не менее информативными и важными в случае работы с MCS. В частности, методы на основе взаимодействия меток, активирующихся при сближении, являются одними из наиболее интересных направлений на данный момент. Можно выделить несколько способов: применение «разделенных» флуоресцентных белков, где применяются две части белка, которые по отдельности молчат (данный метод неидеален, так как сами по себе белки при взаимодействии могут стабилизировать контакт, давая нам ложноположительный контакт), схожей техникой является применение димеризующихся флурофоров, где два белка светятся при образовании гетеродимера (рис. 9) [23]. В данной области FRET (безызлучательный перенос энергии возбуждения от одной флуоресцентной молекулы — донора — к другой — акцептору) стал одним из наиболее незаменимых и ценных методов. Основой данного подхода является применение донорной и акцепторной молекул, энергия флуоресценции между которыми может передаваться на расстоянии не более 10 нм. Этим он и идеален: при размещении на двух органеллах наличие мембранного контакта опосредуется флуоресцентным сигналом. Например, так были изучены контакты между митохондриями и лизосомами, где выяснилось, что 70% таких контактов существует менее минуты, что выступило в качестве доказательства их динамичной природы.
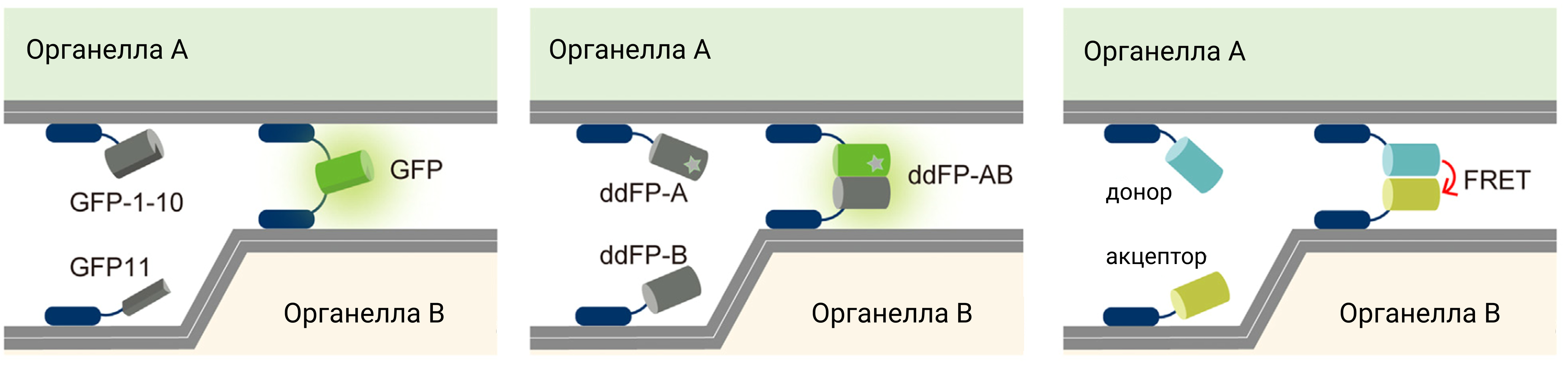
Рисунок 9. Применение репортёров, зависимых от расстояния, для визуализации мембранных контактов.
адаптировано из [23]
Если хочешь понять, как что-то работает — повтори
На протяжении всей истории ученые, чтобы что-то изучить, выбирали один из наиболее эффективных методов исследования — сломать нечто важное (или не очень важное) и посмотреть, как без этого будет существовать объект их исследования. Однако это не всегда представляется возможным. Еще один способ, позволяющий понять устройство — это что-то создать. «Создание искусственных контактов» — это метод, позволяющий устанавливать не только «визуальную составляющую», но и подтвердить функцию конкретного белка. Здесь как удобный метод изучения можно выделить химическую димеризацию. При помощи зависимого связывания FKBP и FRB (двух белков, применяемых в качестве модулей для индуцируемой димеризации, где FKBP является белком, связывающим иммунодепрессант FK 506, а FRB домен белка mTOR, связывающийся с FKPB в присутствии рапамицина) можно соединить две мембраны, заменив домены на димеризующие. Так было доказано, что ORP5 переносит PI4P и PS между ЭР и плазматической мембраной. Также находит свое применение оптогенетика, подразумевающая использование фоторецепторов для управления контактом (CRY2—CIBN) и свет-управляемые димеры. Фоторецепторы позволяют локально и точно индуцировать формирование мембранных контактов. С помощью Opto-VAP удалось показать способность эндогенного OSBP переносить PI4P в живой клетке. Однако не существует лекарства от всех болезней, так и тут, любое искусственной сближение мембран увеличивает количество контактов, иногда на 20–90%, что само по себе меняет физиологию клетки.
А для чего вообще надо изучать мембранные контакты?
Кроме научного интереса, несомненно важной и значимой части любого открытия, всегда стоит вопрос: а в общем-то зачем мы все это делаем? Каждый ученый находит свой ответ на этот вопрос; в нашем конкретном случае ответом служат болезни, вызванные нарушением функционирования данных контактов. Любое нарушение в структуре клетки в последующем приведет к нарушениям во всем организме; как говорил Теодор Шванн, «разнообразие организмов зависит от разнообразия строения, соединения и образования их клеток».
Как упоминалось ранее, контакты могут обусловливать специфичные функции тех или иных органелл/групп органелл или даже клеток. Например, многие белки, участвующие в формировании контактов, ассоциированы с развитием нейродегенеративных заболеваний: болезни Паркинсона, болезни Шарко-Мари-Тута (CMT) [24] и иных. Сама по себе болезнь Паркинсона является довольно многосторонним заболеванием, причины развития которого сокрыты как в генетических аспектах, так и в окружающей среде. Например, роль митохондрий и лизосом в развитии болезни Паркинсона обычно рассматривалась отдельно друг от друга, сейчас же активно изучается влияние контактов между ними на этиологию заболевания. (В нейронах, полученных от пациентов, контакт между митохондрией и лизосомой является более продолжительным, чем в контроле.) CMT же объединяет группу нарушений периферической нервной системы; часть этих нарушений связана с мутациями в генах, отвечающих за формирование контактов между митохондриями и лизосомами.
Не одними лизосомами едины. Нарушения контактов между эндоплазматическим ретикуломом и митохондриями также могут быть связаны с различными патологиями (болезнью Паркинсона, боковым амиотрофическим склерозом), наиболее же глубоко эта закономерность изучена на примере болезни Альцгеймера. Основной особенностью, характерной для этого заболевания, является формирование бляшек, состоящих из бета-амилоида. Повышение уровня тау-белка, расщепленного каспазой 3 в клетках HeLa, имеет связь с увеличением числа взаимодействий между ЭР и митохондриями, что может являться компенсаторной реакцией на нарушение гомеостаза ионов кальция при болезни Альцгеймера [25].
Большое внимание научным сообществом, что сейчас, что в прошлом, уделяется различным новообразованиям и процессам их формирования. Сейчас проводится множество исследований, рассматривающих возможность корреляции между нарушениями в регуляции мембранных контактов и раком. Это открывает новые возможности для развития противоопухолевой терапии.
Наиболее интригующим в этом всем является просматривание некоторой закономерности между применением химиотерапевтических препаратов и появлением новых контактов между эндоплазматическим ретикулумом и митохондриями. (Конечно, нет исследований, которые напрямую доказывают наличие такой закономерности, предполагается, что данные препараты могут влиять на белки, участвующие в формировании контактов) Например, экспрессия Mfn2, контролирующего стабильность контактов ЭР-митохондрия и транспорт кальция с липидами, снижается в неонатальных кардиомиоцитах, контактировавших с доксирубицином [26].
Наиболее же интересным в этом всем является то, как особенности мембранных контактов применяются различными патогенами для поддержания собственного существования. Бактерии, проникающие внутрь клетки, формируют компартмент, в котором возможно поддержание их жизнедеятельности. Сам по себе процесс перестраивания вакуолярного транспорта клетки хозяина процесс довольно изученный, но формирование мембранных контактов, в частности с эндоплазматическим ретикулумом, является одной из современных теорий того, как бактерии создают для себя такую нишу [27].
Изучение мембранных контактов является важным этапом развития биологии и медицины. Это не просто фундаментальные исследования устройства клетки, а новые возможности. Понимание того, как дисфункция этой сложной сети взаимодействий между органеллами влияет на развитие нейродегенеративных, онкологических и инфекционных заболеваний, открывает новые возможности в поиске уникальных мишеней для разработки лекарственных препаратов. Многие вопросы остаются открытыми, но ясно одно: рассматривание клетки как единой экосистемы — это будущее клеточной биологии.
Литература
- G.K. Voeltz, E.M. Sawyer, G. Hajnóczky, W.A. Prinz. (2024). Making the connection: How membrane contact sites have changed our view of organelle biology. Cell. 187, 257-270;
- Xue Huang, Chen Jiang, Lihua Yu, Aimin Yang. (2020). Current and Emerging Approaches for Studying Inter-Organelle Membrane Contact Sites. Front. Cell Dev. Biol.. 8;
- Yael Elbaz-Alon, Yuting Guo, Nadav Segev, Michal Harel, Daniel E. Quinnell, et. al.. (2020). PDZD8 interacts with Protrudin and Rab7 at ER-late endosome membrane contact sites associated with mitochondria. Nat Commun. 11;
- Maria Bohnert. (2020). Tether Me, Tether Me Not—Dynamic Organelle Contact Sites in Metabolic Rewiring. Developmental Cell. 54, 212-225;
- Ofer Moldavski, Triana Amen, Smadar Levin-Zaidman, Miriam Eisenstein, Ilana Rogachev, et. al.. (2015). Lipid Droplets Are Essential for Efficient Clearance of Cytosolic Inclusion Bodies. Developmental Cell. 33, 603-610;
- Luca Scorrano, Maria Antonietta De Matteis, Scott Emr, Francesca Giordano, György Hajnóczky, et. al.. (2019). Coming together to define membrane contact sites. Nat Commun. 10;
- Haoxi Wu, Pedro Carvalho, Gia K. Voeltz. (2018). Here, there, and everywhere: The importance of ER membrane contact sites. Science. 361;
- Michal Eisenberg-Bord, Nadav Shai, Maya Schuldiner, Maria Bohnert. (2016). A Tether Is a Tether Is a Tether: Tethering at Membrane Contact Sites. Developmental Cell. 39, 395-409;
- Constance J. Jeffery. (2018). Protein moonlighting: what is it, and why is it important?. Phil. Trans. R. Soc. B. 373, 20160523;
- Clare S. Harper, Antoineen J. White, Laura L. Lackner. (2020). The multifunctional nature of mitochondrial contact site proteins. Current Opinion in Cell Biology. 65, 58-65;
- William A. Prinz, Alexandre Toulmay, Tamas Balla. (2020). The functional universe of membrane contact sites. Nat Rev Mol Cell Biol. 21, 7-24;
- Stephanie Vrijsen, Céline Vrancx, Mara Del Vecchio, Johannes V. Swinnen, Patrizia Agostinis, et. al.. (2022). Inter-organellar Communication in Parkinson's and Alzheimer's Disease: Looking Beyond Endoplasmic Reticulum-Mitochondria Contact Sites. Front. Neurosci.. 16;
- Tito Calì, Emmanuelle M. Bayer, Emily R. Eden, György Hajnóczky, Benoit Kornmann, et. al.. (2025). Key challenges and recommendations for defining organelle membrane contact sites. Nat Rev Mol Cell Biol. 26, 776-796;
- Karin M. Reinisch, William A. Prinz. (2021). Mechanisms of nonvesicular lipid transport. Journal of Cell Biology. 220;
- Alberts B. Molecular biology of the cell. 7th edition. W. W. Norton & Company, 2022. — 1552 p.;
- David A Baum, Buzz Baum. (2014). An inside-out origin for the eukaryotic cell. BMC Biol. 12;
- Louise H. Wong, Alberto T. Gatta, Tim P. Levine. (2019). Lipid transfer proteins: the lipid commute via shuttles, bridges and tubes. Nat Rev Mol Cell Biol. 20, 85-101;
- Bruno Mesmin, Joëlle Bigay, Joachim Moser von Filseck, Sandra Lacas-Gervais, Guillaume Drin, Bruno Antonny. (2013). A Four-Step Cycle Driven by PI(4)P Hydrolysis Directs Sterol/PI(4)P Exchange by the ER-Golgi Tether OSBP. Cell. 155, 830-843;
- Michael R. Wozny, Andrea Di Luca, Dustin R. Morado, Andrea Picco, Rasha Khaddaj, et. al.. (2023). In situ architecture of the ER–mitochondria encounter structure. Nature. 618, 188-192;
- Загадочный кальциевый язык;
- Yihan Shen, Nagendra Babu Thillaiappan, Colin W. Taylor. (2021). The store-operated Ca 2+ entry complex comprises a small cluster of STIM1 associated with one Orai1 channel. Proc. Natl. Acad. Sci. U.S.A.. 118;
- Simona Boncompagni, Antonio Michelucci, Laura Pietrangelo, Robert T. Dirksen, Feliciano Protasi. (2017). Exercise-dependent formation of new junctions that promote STIM1-Orai1 assembly in skeletal muscle. Sci Rep. 7;
- Fubito Nakatsu, Shinya Tsukiji. (2023). Chemo- and opto-genetic tools for dissecting the role of membrane contact sites in living cells: Recent advances and limitations. Current Opinion in Chemical Biology. 73, 102262;
- Одна болезнь, сто генов, миллионы людей: как вылечить болезнь Шарко—Мари—Тута;
- Soojin Kim, Robert Coukos, Fanding Gao, Dimitri Krainc. (2022). Dysregulation of organelle membrane contact sites in neurological diseases. Neuron. 110, 2386-2408;
- Aurora Gil-Hernández, Miguel Arroyo-Campuzano, Arturo Simoni-Nieves, Cecilia Zazueta, Luis Enrique Gomez-Quiroz, Alejandro Silva-Palacios. (2021). Relevance of Membrane Contact Sites in Cancer Progression. Front. Cell Dev. Biol.. 8;
- Simone Vormittag, Rachel J Ende, Isabelle Derré, Hubert Hilbi. (2023). Pathogen vacuole membrane contact sites – close encounters of the fifth kind. microLife. 4.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚