
Железный аргумент старения
02 апреля 2025
Железный аргумент старения
- 718
- 0
- 2
Железный дровосек — жертва прогрессирующего патологического процесса, при котором железо распространяется по организму.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В любой версии списка микроэлементов обязательно есть железо Fe — переходный металл, который легко меняет степень окисления и очень широко распространен в неживой природе. А в живом организме этот металл буквально необходим как воздух — без него невозможно дыхание на клеточном уровне, связывание и транспорт кислорода по телу и многие другие процессы. Однако в последнее время мы узнаем все больше плохого о «старом друге». Избыток железа или его перераспределение вызывают старение и тяжелые заболевания, в том числе мозга. Коварный элемент все чаще фигурирует в патогенезе распространенных недугов — сердечно-сосудистых, онкологических, нейродегенераций (включая болезни Альцгеймера и Паркинсона) и прогрессивно накапливается с возрастом. Напрашивается очевидный вопрос: можно ли их лечить, избавив организм от железных «залежей»? Насколько это будет реалистично в будущем и какими первыми успехами ученые могут похвастаться уже сейчас?
Конкурс «Био/Мол/Текст»-2024/2025
 Эта работа заняла первое место в номинации «Старение и долголетие» конкурса «Био/Мол/Текст»-2024/2025.
Эта работа заняла первое место в номинации «Старение и долголетие» конкурса «Био/Мол/Текст»-2024/2025.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Хороший, плохой и гемовый
Железо — это химический элемент (в более-менее чистом виде металл), который буквально окружает нас со всех сторон. Из него сделаны арматура зданий, машины, рельсы, телефоны, бытовые приборы и даже вилки с ложками, которые мы используем каждый день. Неудивительно: земная кора на 5% состоит из железа, а планета в целом (со всеми ее внутренними оболочками) — на целую треть.
Возникшая на Земле жизнь просто не могла не включить в состав такой изобильный элемент. Тем более что железо — переходный металл, который охотно меняет свою степень окисления. И потому служит хорошим донором и/или акцептором электронов, участвуя в окислительно-восстановительных реакциях. Без них биохимические процессы и метаболизм любой клетки просто немыслимы.
Среди большого набора степеней окисления в соединениях железа преобладают две. Это 1) закисное (ferrous), или двухвалентное железо Fe(II) и 2) окисное (ferric), оно же трехвалентное железо Fe(III). Разумеется, одно легко переходит в другое, на чем и держится участие элемента в хитросплетении биохимических процессов.
Разные живые клетки нашли этому металлу непохожие биохимические применения. Например, железобактерии живут тем, что окисляют закисное железо в окисное, получая «энергетические дивиденды» для метаболизма. Обычно железо в клетке не «валяется» в чистом виде, в виде свободных ионов, — почему это важно, мы расскажем после. Элемент чаще связан с органическими молекулами или складируется внутри специальных белков-депо с полостями внутри.
Железо в составе белков с железо-серными кластерами (FeS) появилось на заре эволюции и было унаследовано разными доменами и царствами организмов от общего предка. Такие белки синтезируются в митохондриях и работают как ферменты для самых главных метаболических процессов.
В случае человека это знаменитый цикл Кребса — основа энергетического метаболизма. Электронтранспортная цепь митохондрий, обеспечивающая дыхание на молекулярном уровне. А также ряд других процессов, требующих FeS-белки в качестве вспомогательный веществ — кофакторов (рис. 1)
Отдельная история — и в биохимическом, и в эволюционном плане, — это гемовое железо. Тут металл уже не «пришит» непосредственно к белку (по остаткам цистеина), а удерживается в специальной выемке другого вещества — органической молекулы порфирина. Такая конструкция называется «гем», и в этом слове легко узнать древнегреческое название крови. Корень, который мы встречаем и в «гематоме» (то есть синяке), и в «гематологии».
Гемовое железо тоже работает как кофактор, однако на первом плане — его участие в транспорте кислорода. Гем в качестве «вставной» простетической группы входит в гемоглобин и миоглобин. Зачем нужны такие белки — всякий помнит еще со школьной скамьи. Не уступают им по значению гемсодержащие белки электрон-транспортной цепи, работающие в ней бок о бок с FeS-белками. А гемопротеин P450 нужен, в частности, чтобы избавлять нас от ксенобиотиков — чужеродных, зачастую опасных и при этом плохо растворимых в воде веществ.
Организм взрослого человека в норме содержит 3–4 грамма железа. Примерно столько же находится, скажем, в стандартном гвозде длиной восемь сантиметров. Металл входит прежде всего в состав гемоглобина, а также миоглобина и специальных белков — хранилищ и транспортеров железа (ферритин, трансферрин, церулоплазмин и другие).
Запасы железа необходимо постоянно пополнять, и потому взрослый человек должен ежедневно получать 10–20 миллиграмм этого микроэлемента с пищей. Его основные источники — пища животного происхождения, которая поставляет нам гемовое железо. Негемового сравнительно много в бобовых, однако усваивается оно довольно плохо.
«Железный» метаболизм человека довольно сложен и включает в себя абсорбцию этого элемента, его циркуляцию по организму, хранение в депо и оркестрирующую их все регуляцию. Ее задача — удержать концентрацию ионов железа на нужном уровне, не слишком высоком или низком.
Поступающее в организм с пищей железо имеет трехвалентную форму (Fe3+) (рис. 1) [1]. В просвете двенадцатиперстной кишки оно восстанавливается до Fe2+ ферментом-цитохромом Dcytb, который локализован на поверхности клеток эпидермальной выстилки кишечника.
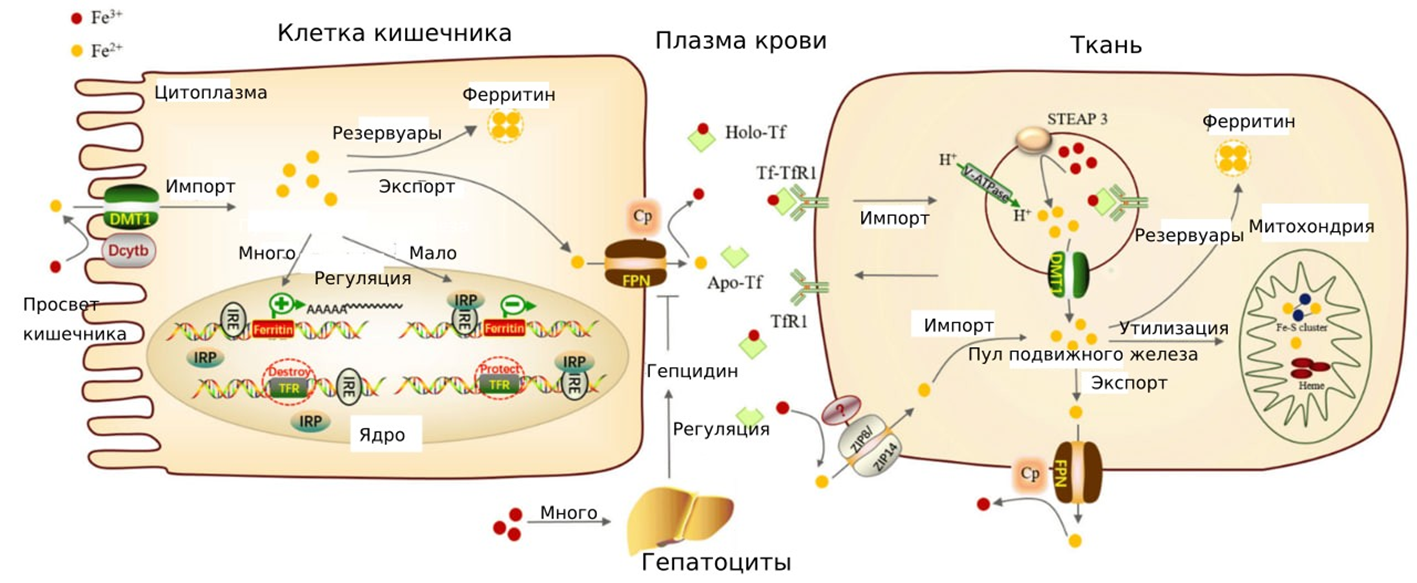
Рисунок 1. Роль железа в нормальном метаболизме человека.
Затем железо транспортируется в цитоплазму клеток белком DMT1 (транспортер бивалентных металлов). Часть его попадает в ферритин — крупный белковый комплекс, который работает как «склад» для железа и может накопить в себе более четырех тысяч ионов. При недостатке элемента ферритин начинает его выпускать наружу.
При избытке ионы железа экспортируется из клеток ферропортином FPN — единственным белком с такой функцией. Далее Fe2+ окисляются до Fe3+ церулоплазмином Cp (содержащий медь белок плазмы крови). Во внеклеточной среде железо подхватывает трансферрин Tf — он с током крови переносит микроэлемент по самым разным органам и тканям. Прибыв в нужное место, ферритин со своим «грузом» связывает специфический рецептор на поверхности клеток (TfR1). Комплекс лиганда с рецептором Tf-TfR1 подвергается эндоцитозу и оказывается в цитоплазме внутри везикул (эндосом), которые начинают закисляться благодаря АТФазе V-типа, закачивающей туда протоны. Кислая среда меняет форму белкового комплекса Tf-TfR1 и тот выпускает Fe3+.
Тут в дело вступает белок STEAP3, превращающих трехвалентное железо в двухвалентное. Внутрь клеток Fe2+ импортирует уже знакомый нам DMT1. Теперь ионы могут использоваться в цитоплазме, хранится внутри ферритина или импортироваться в митохондрии. «Энергостанции клеток» нуждаются в железе для синтеза FeS-кластеров и гема, необходимых для клеточного дыхания. Излишки ионов экспортируются во внеклеточную среду с помощью FPN.
При недостатке железа (который грозит таким сложным осложнением, как железодефицитная анемия) белки IRP (iron-responsive element-binding protein) начинают связывать свои мишени на мРНК — расположенные в 5′-нетранслируемой области железозависимые элементы IRE. Тем самым защищая мРНК от расщепления нуклеазами и, как следствие, подавляя экспрессию ферритина. Если железа вновь станет достаточно, IRP прекратит взаимодействовать с IRE, что приведет к разрушению мРНК рецепторов трансферрина TfR и возобновлению синтеза ферритина [1].
Как мы видим, железо необходимо человеку как воздух. Или как кислород. И так же, как кислород (который из жизненной необходимости легко становится причиной разрушений), железо способно создать большие проблемы для здоровья.
Fe значит «Фентон»
Столетие назад жизнь казалось чем-то более простым и легко познаваемым, и ученые были полны энтузиазма. Они верили, что «вся сила — в гемоглобине» и стоит как следует накормить голодное человечество мясом, одеть в одежду с пуговицами из крови коров, наделать побольше пенициллина, — как все станет очень хорошо. Тогда же популярными стали «кровавые ириски» для детей — гематоген, который встречается на постсоветском пространстве по сей день.
Однако устройство живого организма оказалось куда сложнее ожиданий столетней давности. И связанный с железом энтузиазм тоже сильно убавился. Все больше исследований показывают, что избыток железа и его нахождение не к месту, — это большая проблема. Причем негативные эффекты металла в целом определяют те же его свойства, что и положительные (целевые функции).
В свободной форме — то есть в виде ионов в растворе, — железо попросту токсично. Если его достаточно много, железо катализирует реакцию Фентона (рис. 2). То есть превращение перекиси водорода H2O2 в гидроксильный радикал OH• — самую агрессивную из всех активных форм кислорода (АФК или RAS).
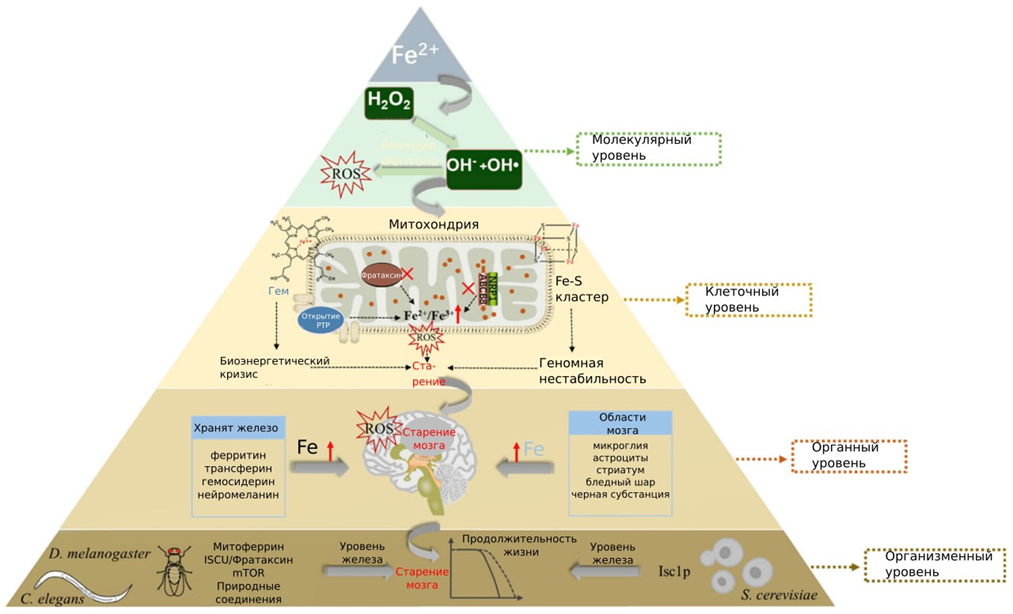
Рисунок 2. Различные уровни организации организма, затронутые нарушениями метаболизма железа, и их связь.
Злостный радикал портит все на своем пути без разбора — а в клетке на пути попадаются чувствительные к окислению липидные мембраны и хрупкая ДНК. Первые в результате ждет перекисное окисление липидов, вторую — разрывы (в том числе двухцепочечные) и мутации. Как итог, клетка может быть ввергнута в ферроптоз — выделенный недавно особый тип клеточный гибели, вызванный тем самым «полезным микроэлементом». Показано, что такая программируемая клеточная смерть играет важную роль при раке и нейродегенерациях [2].
Кроме того, с возрастом нарастают нарушения синтеза FeS-белков и гема в митохондриях. Они могут вызвать проблемы с энергетическим метаболизмов и запустить геномную нестабильность. В случае снижения экспрессии фратаксина (митохондриального белка, удаляющего железо и связанного с патогенезом атаксии Фридрейха), нейронального белка нейропилина Nrp1 (работате в связке с тирозинкиназными рецепторами) растет концентрация железа в митохондриях. Что вызывает окислительный стресс и опять-таки ускоряет молекулярные процессы старения.
Тот же эффект оказывает рост концентрации PTP (mPTP, mitochondrial permeability transition pore) — белка, который появляется на внутренней мембране митохондрий при некоторых патологиях. PTP пропускает молекулы меньше полутора килодальтонов, что может привести к разбуханию митохондрий и запуску клеточной смерти.
На тканевом и органном уровнях для возрастной аккумуляции железа характерна неоднородность — одни области организма страдают от нее в разной степени. Различаются также формы, в которых накапливается железо. В случае мозга это ферритин, трансферрин, гемосидерин (уже не белок, а темно-желтый пигмент, содержащий оксид железа) и нейромеланин (похожий на меланин, но накапливающийся в некоторых областях мозга).
Целые организмы — такие как лабораторные «супермодели», как пекарские дрожжи S. cerevisiae, нематода C. elegans и дрозофила D. melanogaster, — способны регулировать уровень железа в организме. Для этого служат путь mTOR, фратаксин, митоферрин и так далее. Однако с возрастом все эти организмы накапливают в себе все больше железо. Это связано с их старением и сокращением ожидаемой продолжительности жизни [1].
Железо против мозга
Однако вернемся к человеку — железо вовлечено в развитие многих его болезней, которые ассоциированы со старением. А поскольку само старение имеет похожие механизмы, то и в возрастных изменениях сейчас все чаще винят железо. Среди них выделяются повреждения мозга, которые сейчас обозначены как ferrosenescence (буквально «железостарение» или «железное старение»). Его все чаще упоминают как важный процесс патогенеза нейродегенераций.
Известно, что старение сопровождается нарушением абсорбции железа во всем организме, его транспорта и хранения в специальных белковых депо. Последствия проявляются буквально с ног до головы. Могут страдать функции половых органов, кишечник, кожа, печень, легкие, сердце, глаза и нервная система, включая мозг.
Мутации в генах «железного» метаболизма вызывают различные заболевания. Например, наследственный гемохроматоз, который может развиться при мутациях в генах HDE (Homeostatic Iron Regulator), гемоювелина, гепцидина, рецептора трансферрина 1 и так далее (рис. 3). Результат однообразен: железо, которое человек постоянно потребляет с пищей, не может покинуть организм. Оно все больше накапливается в различных органах, вызывая артрит, цирроз, гепатоцеллюлярную карциному, диабет, недостаток половых гормонов, кардиомиопатию и другие неприятные последствия…
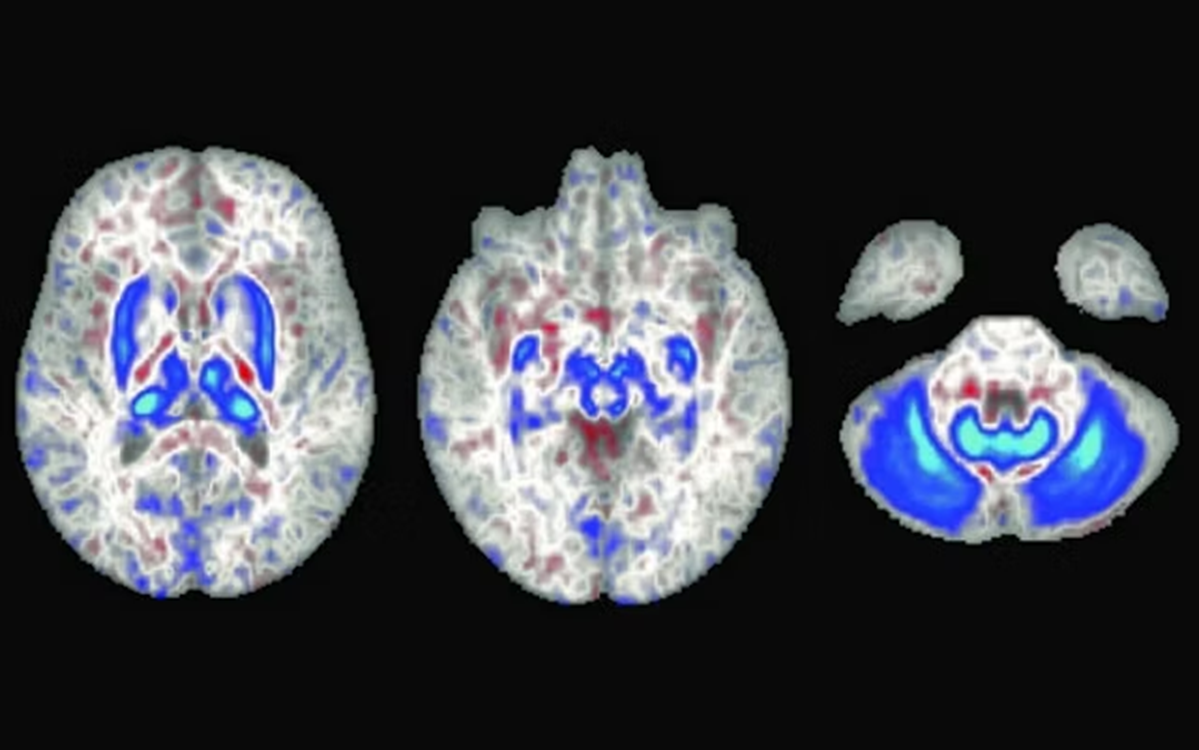
Рисунок 3. МРТ головного мозга пациента с гемохроматозом, синим показана высокая концентрация железа.
В частности, мутации в гене белка L-ферритина приводят к нейроферритинопатии. Болезнь проявляется быстрым старением и нарушением движений. Она относится к большой группе нейродегенераций с накоплением железа в мозге (ННЖМ, или NBIA, то есть Neurodegeneration with Brain Iron Accumulation). За прошедшее столетие таких описали более десятка — в основе каждой лежат вполне конкретные гены и мутации, многие из которых уже известны. Из названия очевидно, что в мозге пациентов образуются включения из соединений железа (их можно заметить, например, с помощью магнитно-резонансной томографии). Все ННЖМ при заметных различиях в симптоматике объединяет быстрое прогрессирование и отсутствие эффективного лечения.
Негативное влияние железа на мозг не ограничивается «малыми», то есть редкими или орфаннымм нейродегенерациями. Все больше данных показывают, что коварный металл — важный участник патогенеза болезней Альцгеймера, Паркинсона, хореи Гентингтона и бокового амиотрофического склероза (БАС). Это уже главные «тяжеловесы» среди нейродегенераций, которые изучают и не слишком успешно пытаются лечить десятилетиями. Первые две широко распространены и встречаются все чаще — это острая социальная проблема, значение которой быстро растет.
Вкратце связь железа с развитием нейродегенерации выглядит следующим образом (рис. 4). Ионы Fe3+ абсорбируются и используются различными клетками мозга — нейронами, астроцитами, олигодендроцитами и микроглией. Изменения концентрации белков, участвующих в метаболизме железа, могут привести к нарушению его обмена и как следствие — к массовой гибели нейронов.
Известно, что нарушение активности церулоплазмина и недостаток нейромеланина могут ускорить начало болезни Паркинсона. Рост внутриклеточной концентрации железа активирует специфические ферменты бета- и гамма-секретазу, ускоряя образования ими бета-амилоида — одной из ключевых молекул для патогенеза болезни Альцгеймера. Железо также стимулирует агрегацию бета-амилоида на вокруг клеток микроглии. Коварный металл также связывает тау-белок — вторую (а скорее даже первую) значимую для этой нейродегенерации молекулу. В результате тау активнее фосфорилируется и образует нейрофибриллярные клубки (NFT) внутри нейронов [1].
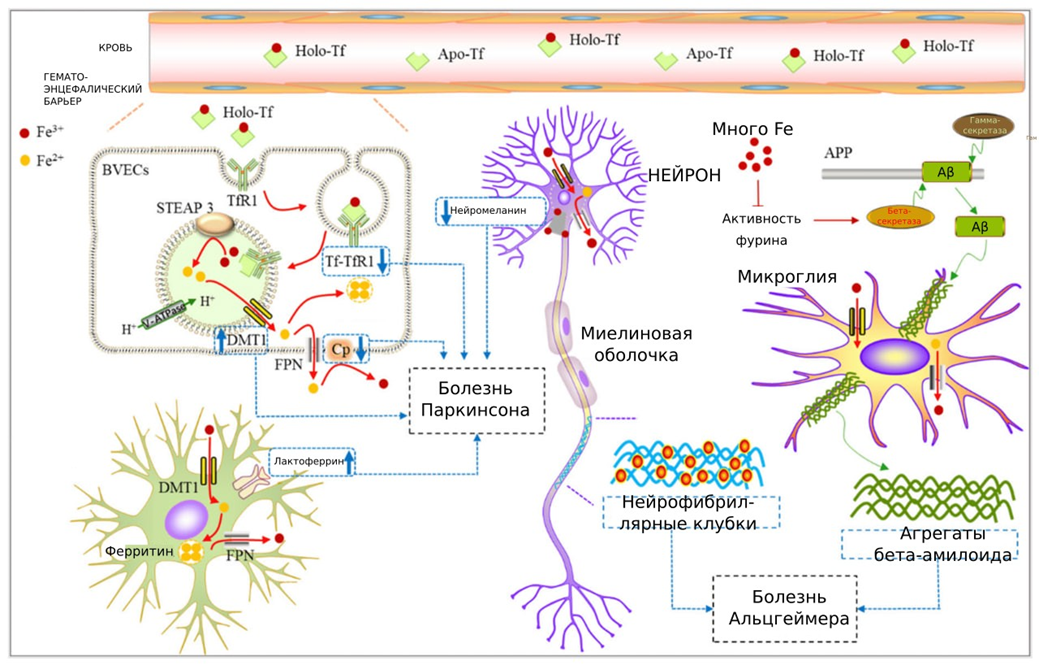
Рисунок 4. Роль железа в развитии нейродегенераций.
Естественно предположить, что «малые», «большие» нейродегенерации и старение объединяют общие патологические изменения метаболизма. В том числе обмена пресловутого железа. Потому изучение ННЖМ и им подобных болезней могут быть полезны не только для лечения самих редких заболеваний [1].
Действительно, ведь основа у большинства нейродегенераций общая — патологические изменения конформаций белков, то есть протеинопатии. В том числе «молекулярные эпидемии», распространяющиеся по прионоподобному механизму. В случае болезни Альцгеймера в них вовлечены бета-амилоид и тау-белок, при болезни Паркинсона — альфа-синуклеин. Уже известно, что образование всех трех белков ускоряется в присутствии железа, — либо за счет прямого связывания с металлом, либо опосредованно через генерацию АФК [3].
Подробнее о нейродегенерациях и тяжелой борьбе с ними читайте в статье [3].
Прочие «железные» болезни
Известно также, что высокий уровень в крови ферритина, — белкового комплекса, работающего как депо ионов железа, — связан с худшим исходом ишемического инсульта. Что подчеркивает его повреждающее действие на мозг. А еще железо участвует в развитии возрастной макулярной дегенерации. В сетчатке таких пациентов оказалось больше железа, чем у здоровых людей. Другие «железные» болезни — это патологии сердечно-сосудистой системы: гипертония, аритмии, кардиомиопатия, гипертрофии сердца и так далее. Их сопровождает повышенное содержание железа в сердце.
Диабет второго типа также не остался в стороне. Он зачастую развивается у пациентов с гемохроматозом. Более того, недостаток рецепторов ферритина повышает риск заболеть таким диабетом. Механизм, по-видимому, связан с образованием разрушительных гидроксильных радикалов. Железо также способствует развитию тяжелых диабетических осложнений со стороны сетчатки и почек.
Дальше — больше. Железо со своей «свитой» из АФК стимулирует развитие рака. Это согласуется с тем, что больные гемохроматозом зачастую также страдают от цирроза и гепатокарциномы. Избыток железа — известный фактор развития многих злокачественных опухолей, включая колоректальный рак, рак печени, молочной железы и легких. А также миелодисплазии и острого миелоидного лейкоза.
Считается, что онкологические болезни стимулирует железо, поступающее с пищей в гемовой форме. Это прежде всего красное мясо, «канцерогенности» которому прибавляет нитрозирование белков при термической обработке.
Курильщиков здесь ждет отдельная плохая новость. Сигаретный дым содержит много железа, которое дополнительно повреждает ткани легких. К тому же развитие ХОБЛ (хронической обструктивной болезни легких) активирует белок, участвующий в реакции на этот металл, — IRP2 (Iron-Responsive element-binding protein 2). Что делает его перспективной мишенью для таргетной терапии болезней легких.
Далее, гемохроматозу часто сопутствуют проблемы с суставами и костями. И тут не обошлось без железа: оно накапливается в синовиальной жидкости («смазка» внутри суставной сумки), заодно нарушая иммунный ответ при артрите (рис. 5).
В целом, избыток железа также сильно ударяет по иммунитету. Он стимулирует размножение микробов в теле при инфекциях, а также подавляет воспалительную реакцию на них. В частности, моноциты в крови выделяют меньше фактора некроза опухолей TNFα в ответ на бактериальные липополисахариды. Тем временем сама инфекция усугубляет проблемы с высокой концентрацией железа.
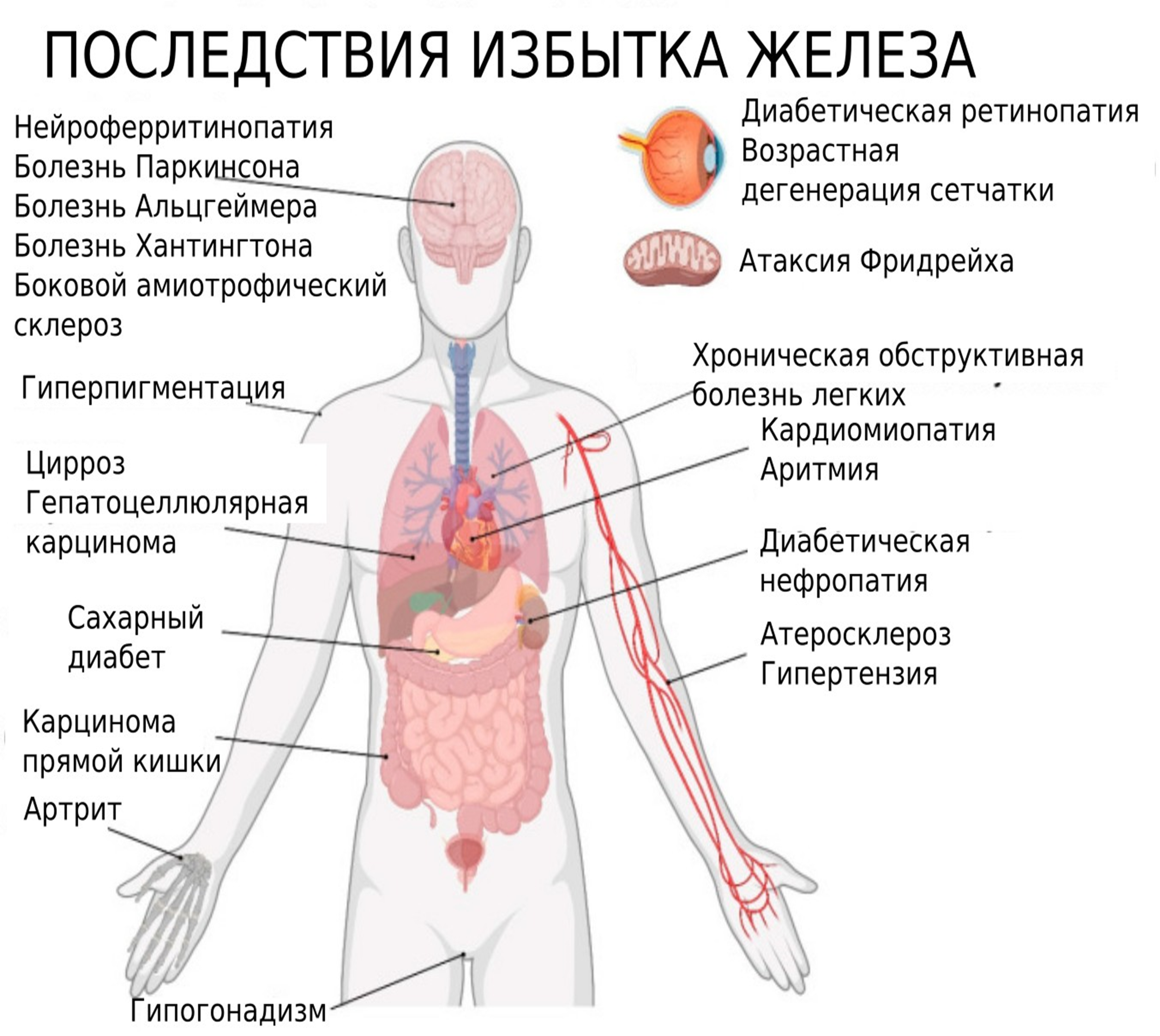
Рисунок 5. Многообразие повреждений тканей и органов при избытке железа.
Содержание этого металла неуклонно растет даже при нормальном старении. Причина — отсутствие у человека активных механизмов удаления этого металла. Лишь небольшая его часть покидает тело при слущивании клеток выстилки кишечника, с мочой и при кровепотерях. Такой небольшой отток не может компенсировать неуклонный рост концентрации металла, который становится разрушительным [4].
Уберем металлолом?..
Выходит, железо (а вернее сказать: его избыток там, где не следует) — источник многих проблем. Значит, имеет смысл его удалять из организма? Тем более, что это не кажется таким уж трудным с технической точки зрения…
Действительно, этот подход в лечении используют уже давно. Частично «обезжелезить» человека можно с помощью, например, регулярных кровопусканий. Одного из самых древних методов терапии в истории, который к тому же можно реализовать как гирудотерапию или регулярное донорство крови. Кровопускание эффективно снижает уровень железа и потому применяется у больных гемохроматозом. Оно продлевает пациентам жизнь и может предотвратить осложнения: цирроз и диабет. Кстати, обратный процесс (то есть переливание крови), как и следовало ожидать, напротив, создает проблемы с избытком железа [4].
Далее, гемохроматоз, разные ННЖМ и болезни сердца лечат с помощью хелаторов — молекул-«клешней», которые охватывают собой ионы металлов и тем обезвреживают их. Успехи хелирующей терапии пока довольно скромные. Остается ряд проблем, которые сейчас пытаются решить с помощью новых препаратов.
До сих пор широко применяется такой «старый» синтетический (то есть искусственно полученный) хелатор железа как десферриоксамин (дефероксамин). Его безопасность доказана, однако препарат не слишком удобен — требует внутривенного введения из-за низкой биодоступности.
Деферипрон — другой синтетический хелатирующий агент, по активности связывания железа сравнимый с дефероксамином. Его преимущества: пероральный прием и способность проникать через биологические мембраны и гематоэнцефалический барьер. Поэтому препарат лучше накапливается в нужных тканях.
Деферазирокс также назначают внутрь, он одобрен для лечения хронического избытка железа после многократных переливаний крови (рис. 6). Далее, салицилальдегид изоникотиноил гидразон (SIH) — малая липофильная молекула. Она прочно связывает ионы закисного железа, которые находятся в цитоплазме клетки. Отношение хелатирующей активности к токсическим эффектов выгодно отличает SIH от других препаратов группы.
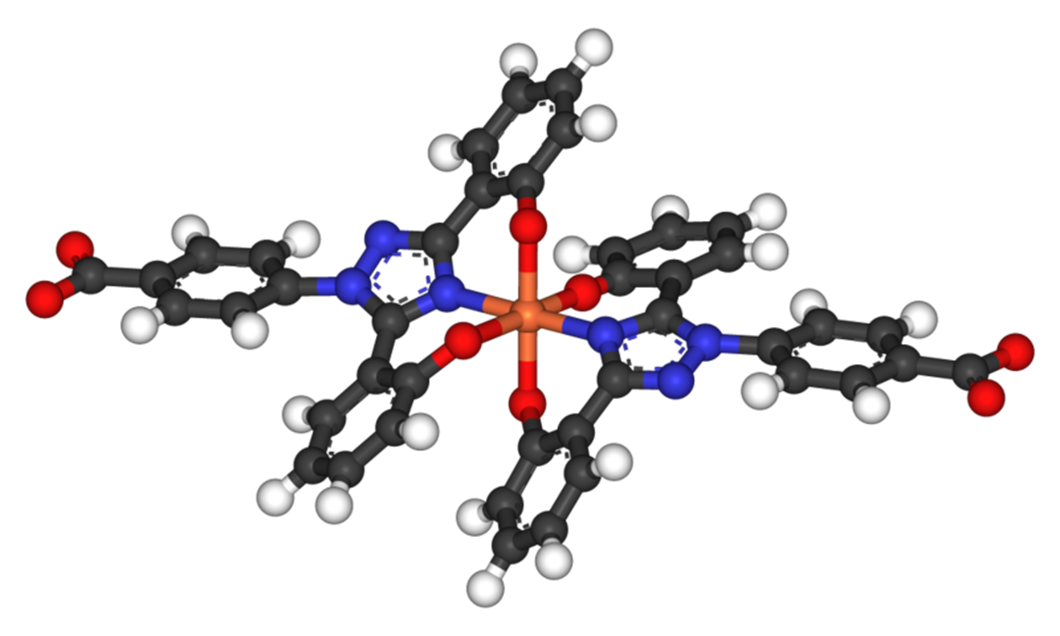
Рисунок 6. Две молекулы деферазирокса хелатировали железо III (оранжевый атом в центре).
Препараты-тиосемикарбазоны (триапин, Dp44mT, DpC) сочетают активность хелатора и ингибитора рибонуклеотидредуктазы (RR). Это зависимый от железа фермент, катализирующий медленный этап синтеза ДНК. Тиосемикарбазоны уже используют для лечения онкологических заболеваний.
Дексразоксан — это хелатор, одобренный к применению при токсическом повреждении сердца, вызванное доксорубицином. Клиохинол, — небольшая липофильная молекула, которая помимо железа также хелатирует ионы меди и цинка, — перспективен для лечения нейродегенераций. К тому же клиохинол подавляет активность связанного со старением митохондриального белка Clock-1.
Справляются с удалением излишков железа и «старые добрые» препараты, которые давно используют с другими целями. Так, длительный прием аспирина снижает концентрации ферритина в крови пациентов и к тому же увеличивает среднюю продолжительность жизни у нематоды C. elegans. Ибупрофен, доксициклин, эналаприл и широко известный как геропротектор метформин также способны хелатировать железо и продлевать жизнь, уменьшая повреждения от АФК [4].
Отдельная перспективная группа хелаторов железа — это уже не синтетические, а природные соединения. Многие мы потребляем с едой и напитками. Таков куркумин из популярной приправы и флоранол, компонент корня бразильского растения Dioclea grandiflora. Их способность связывать железо показано в экспериментах.
Кверцетин — алкалоид, который содержится в красном вине, зеленом чае, яблоках и ягодах, — превосходит по активности хелатирующий химический препарат ферроцин. Эпигаллокатехин-3-галлат (EGCG) из того же чая, байкалеин из шлемника байкальского Scutellaria baicalensis, апоцинин из растения Picrorhiza kurroa, дубильная кислота и другие соединения также могут быть полезны как хелаторы. Фитиновая кислота — ее содержит белок сои — способна уменьшить абсорбцию негемового железа. Поэтому добавление соевых бобов в диету может уменьшить избыточное содержание железа.
С растительным сырьем, однако, есть и проблемы. Неизвестны его точный состав и конкретное действующее вещество, что может приводить к побочным эффектам и затрудняет определение нужной дозы.
Снижение концентрации железа в организме можно добиться и без каких-либо препаратов. Например, ограничив потребление красного мяса, в котором особенно много этого металла в гемовой форме. Близкий результат дает и ограничение потребляемых калорий. Кстати, снизить поступление с пищей меди — другого переходного металла, — ранее рекомендовали для профилактики нейродегенерации.
Выходит, эти геропротекторы являются также «ферропротекторами», что вновь подчеркивает связь старения и возрастных изменений с накоплением железа [1], [4].
Итак, исследования связи коварного переходного металла — железа, — с изменениями при старении становятся трендом. Мы все больше узнаем о «железных механизмах» возрастных перестроек в организме. Есть основания надеяться, что идущие в этом направлении исследования будут плодотворны и в будущем помогут людям продлить здоровое долголетие. А может, заодно продвинуть давно буксующие поиски лекарств от нейродегенераций.
Литература
- Yao Tian, Yuanliangzi Tian, Zhixiao Yuan, Yutian Zeng, Shuai Wang, et. al.. (2022). Iron Metabolism in Aging and Age-Related Diseases. IJMS. 23, 3612;
- Заговор с целью нейродегенерации: бета-амилоид и тау-белок;
- Нейродегенерации, или Массовые вымирания нейронов;
- William J. Chen, George P. Kung, Jaya P. Gnana-Prakasam. (2022). Role of Iron in Aging Related Diseases. Antioxidants. 11, 865.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





