Бактерии тоже могут начинать синтез белка на IRES
03 марта 2015
Бактерии тоже могут начинать синтез белка на IRES
- 1912
- 0
- 0
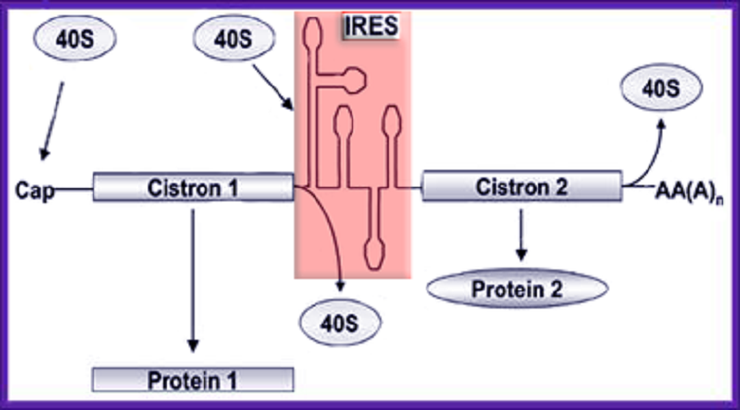
Структурированная РНК — ключ к сердцу трансляционной машины: перед IRES не могут устоять ни эукариотические, ни бактериальные рибосомы.
Рисунок в полном размере.
рисунок с сайта mol-biol4masters.masters.grkraj.org
-
Автор
-
Редактор
До сих пор считалось, что рибосомы бактерий и эукариот распознают совершенно разные сигналы инициации синтеза белка, однако недавно удалось найти пример сигнала, который может узнаваться и теми, и другими. Этот универсальный сигнал —- участок внутренней посадки рибосомы (IRES), структурированный регуляторный фрагмент 5’-нетранслируемой области мРНК вирусов и эукариот.
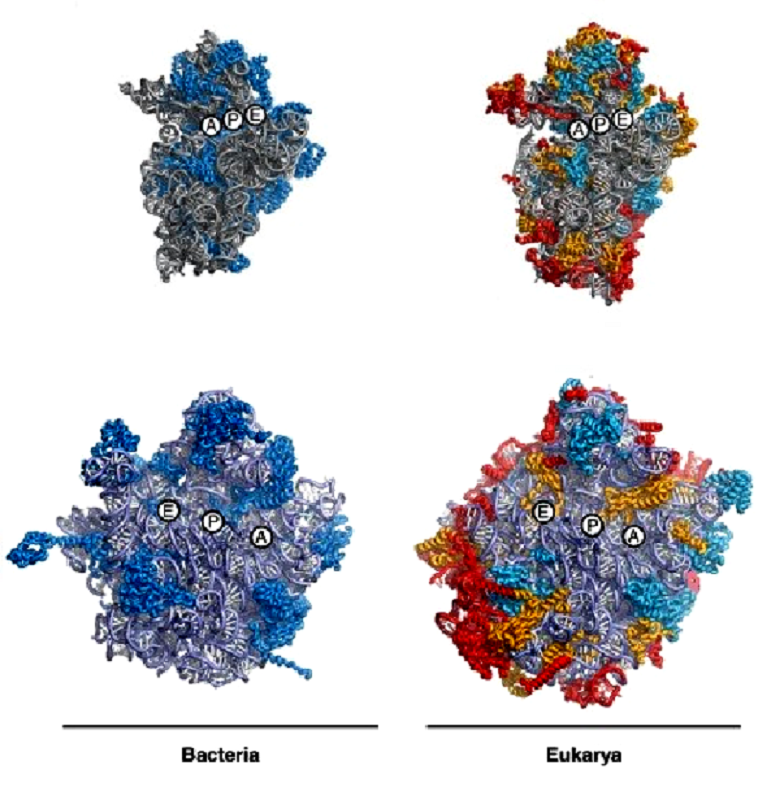
Рисунок 1. Сравнение структур бактериальной и эукариотической рибосом. Сверху показаны малые субъединицы рибосом, снизу — большие. Функциональные центры рибосомы: А — аминоацильный, Р — пептидилтрансферазный, Е — сайт выхода.
Индивидуальность каждой клетки обеспечивается ее набором белков, синтезом которых занимаются рибосомы — молекулярные машины, состоящие из РНК и белка. У представителей двух доменов живых организмов — бактерий и эукариот — рибосомы устроены на удивление сходным образом (рис. 1) и даже конформацию меняют в процессе трансляции одинаково. Однако они узнают совершенно разные сигналы на молекулах матричной РНК, «инструкцию» которых они считывают в ходе синтеза белка.
Рибосомы бактерий узнают определенную последовательность нуклеотидов РНК, называемую последовательностью Шайна-Дальгарно. Бактериальная рибосома связывается с ней, так как в составе 16S рибосомной РНК есть комплементарная последовательность «анти-Шайна-Дальгарно», и приступает к синтезу белка.
Рибосомы эукариот узнают совершенно другую структуру — кэп (англ. cap — шапка) — метилированный гуанозин, связанный через трифосфатную группу с 5’-концом РНК . Такие структуры есть только у эукариотических РНК, и рибосомы бактерий не умеют распознавать этот сигнал. Эукариотические рибосомы, в свою очередь, совершенно не привлекает бактериальная последовательность Шайна-Дальгарно. Такие различия вкусов кажутся немного неожиданными, учитывая, как похоже устроены рибосомы бактерий и эукариот. Однако ученым все-таки удалось найти пример стартового сигнала, который по вкусу и тем, и другим [1].
Регуляторную функцию при трансляции выполняет не только 5’-, но и 3’-конец мРНК — поли(А)-хвост, да еще и с поли(У)-«прихвостнем»: «мРНКаааауу» [2]. — Ред.
Вирусы, как правило, «путешествуют налегке», сохраняя лишь ограниченный набор самых необходимых генов. Собственный аппарат синтеза белка они не кодируют, поэтому почетную задачу производства своих белков вирусы делегируют клетке, которую заразили. Однако рибосомы эукариот возьмутся синтезировать белки на основе только тех РНК, которые имеют на своем конце кэп. Некоторые вирусы поэтому кодируют ферменты, которые кэпируют их РНК, чтобы клетка принимала их за свои. Другие вирусы доходят даже до воровства «шапочек», отрезая кэп у клеточных РНК и пришивая к своим. А некоторые придумали «отмычку» к рибосомам эукариот, которая даже не пытается маскироваться под кэп, зато мимикрирует под другого важного участника трансляции — молекулу тРНК. Каждая тРНК приносит с собой определенную аминокислоту, которую рибосома добавляет к растущей цепочке белка. Так вот, вирусная РНК может содержать фрагмент, очень похожий на такой переносчик аминокислоты. Этот компактно «уложенный» фрагмент, называемый IRES, входит в рибосому, после чего она может начать кэп-независимый синтез «по инструкции» РНК, к которой такой фрагмент «приделан» [3]. IRES, в отличие от кэпа, не обязан находиться на конце РНК, чтобы эукариотическая рибосома его опознала. Именно IRES, как выяснили ученые, способны узнавать и бактериальные рибосомы.
РНК с межгенным IRES кишечного вируса клопа Plautia stali (PSIV) и без всяких признаков последовательности Шайна-Дальгарно, как оказалось, может служить инструкцией для синтеза белка у бактерий (рис. 2). При этом рибосомы представителей разных доменов один и тот же IRES связывали немного по-разному. Это и не удивительно, поскольку с эукариотической рибосомой IRES связывается через белки, которых просто нет в рибосоме бактериальной. Структурная целостность IRES, однако, была необходима в обоих случаях, и нарушение структуры IRES делало невозможным его связывание с бактериальными рибосомами.
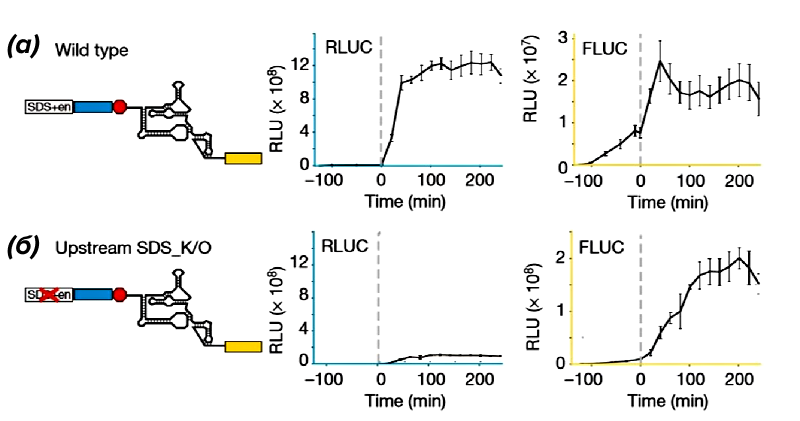
Рисунок 2. Активности двух люцифераз, ген одной из которых (синий цвет) встроен в вектор после «нормального» сайта связывания бактериальной рибосомы (последовательности Шайна-Дальгарно), а другой (желтый цвет) — после IRES эукариотического вируса. (а) — последовательность Шайна-Дальгарно интактна — синтезируются обе люциферазы; (б) — юактериальная последовательность «сломана» — синтез «желтой» люциферазы (от вирусного сигнала) идет в 10 раз активнее, т.к. снизилась конкуренция между сигналами за рибосомы.
Изучение комплексов IRES с рибосомами бактерий и эукариот показало: комплексы, которые формируются у бактерий, очень нестабильны, в отличие от комплексов с эукариотическими рибосомами. Учитывая, что IRES все-таки работает у бактерий, можно было предположить, что он просто делает это иначе, чем в клетках эукариот. При работе IRES с эукариотической рибосомой синтез белка начинается прямо с него — то есть сам IRES служит началом инструкции по синтезу белка. Старт-кодон (тройка нуклеотидов РНК, обычно AUG, с которой начинается трансляция) не необходим в этом случае ни в составе IRES, ни после него. У бактерий, как оказалось, тот же IRES действует по-другому. Он нужен, по-видимому, чтобы привлечь рибосому, но синтез белка начинается не с него, а со старт-кодона, который обязательно должен располагаться чуть дальше по ходу цепи РНК. Расстояние не очень важно, оно может варьировать между 13 и 15 нуклеотидами. Если перед старт-кодоном инструкции добавить еще один старт-кодон, сдвинутый относительно его рамки считывания, эффективность синтеза с рабочего старт-кодона упадет, но не слишком сильно. То есть бактериальная рибосома, связавшись с IRES, ищет старт-кодон где-то поблизости от него, но все-таки не любой.
Взаимодействие бактериальной рибосомы с вирусным IRES оказалось не таким слаженным, как эукариотической, к которой вирусы «притирались» долгое время. Тем не менее, оказалось, что и бактерии способны инициировать синтез белка на особым образом структурированной РНК. Можно предположить, что такой механизм инициации трансляции — самый древний, и его могут использовать представители самых разных групп живых организмов.
Видео 1. Моделирование кэп-зависимой и IRES-опосредованной инициации трансляции.
Литература
- Timothy M. Colussi, David A. Costantino, Jianyu Zhu, John Paul Donohue, Andrei A. Korostelev, et. al.. (2015). Initiation of translation in bacteria by a structured eukaryotic IRES RNA. Nature. 519, 110-113;
- мРНКаааауу;
- Трансляция Нох-генов: особая регуляция особых белков.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚