
Двухцепочечная РНК защищает трансгенные растения только от нежелательных насекомых
16 марта 2015
Двухцепочечная РНК защищает трансгенные растения только от нежелательных насекомых
- 1441
- 0
- 1
Транспластомный картофель — в массы!
Рисунок в полном размере.
-
Автор
-
Редакторы
Темы
Ученые получили трансгенные растения, в хлоропластах которых образуется двухцепочечная РНК, нарушающая работу жизненно важного гена колорадского жука — гена белка цитоскелета β-актина. Все личинки жуков, которые в эксперименте питались листьями таких растений, погибали в течение пяти дней. В то же время разработанный подход высокоселективен в отношении вредителя и безопасен для опылителей.
XXI век — это век биотехнологий: развиваются методы адресной доставки лекарств в определенные органы или клетки с минимальным количеством побочных эффектов [1], становится возможным контролировать активность отдельных генов в разных тканях организма. Но при этом в сельском хозяйстве по-прежнему используются на удивление грубые методы — к примеру, применение инсектицидов, действующих абсолютно не избирательно и причиняющих вред не только поедающим растения насекомым-вредителям.
Каким же образом возможно точечно воздействовать на одних лишь вредителей? Все виды живых существ отличаются друг от друга своей ДНК, поэтому делать ДНК-ориентированную систему защиты от с/х-вредителей — это первое, что приходит на ум. Механизм можно позаимствовать у природы — во всех клетках эукариот существует система уничтожения подозрительных нуклеиновых кислот, которая используется для защиты от вирусов.
Дело в том, что только у вирусов бывают нуклеиновые кислоты особой структуры — двухцепочечные РНК (дцРНК). У всех остальных организмов молекулы РНК представлены в виде одиночных цепочек нуклеотидов. Обнаружив двухцепочечную РНК, клетка активирует механизм защиты под названием РНК-интерференция [2]. Специальные белки (Dicer) режут подозрительную молекулу РНК на фрагменты. Антисмысловые цепи этих фрагментов раздаются другим белкам (RISK), как фотороботы сотрудникам правоохранительных органов. Когда эти белки находят РНК или ДНК с похожей последовательностью (неважно, одноцепочечные или двухцепочечные), они ее уничтожают. А поскольку РНК — это единственный способ для гена проявить свою активность, получается, что гены, которым соответствовала двухцепочечная РНК, перестают работать.
Такой системой можно манипулировать: например, заставить клетку отключать собственные гены, «скормив» ей искусственно синтезированную двухцепочечную РНК с соответствующей последовательностью. Организм будет считать, что защищается от вирусов, и сам же отключит собственные гены. Если эти гены будут жизненно важными — организм погибнет.
Именно такую систему защиты от вредителей пытались реализовать в последние годы биотехнологи, создавая трансгенные растения вопреки предубеждению части общества относительно ГМО [3]. Они получали растения, в тканях которых синтезировались дцРНК с фрагментами генов колорадского жука (Leptinotarsa decemlineata). Если насекомое ело трансгенное растение, двухцепочечная РНК с последовательностью одного из важных генов попадала в его клетки. Запускался механизм РНК-интерференции, и жук погибал.
К сожалению, эта система работала не так эффективно, и колорадские жуки после поедания трансгенных растений гибли не всегда. Проблема заключалась в том, что дцРНК синтезировалась в ядре растительной клетки, а затем попадала в цитоплазму, где встречалась с белком Dicer и разрезалась на фрагменты (рис. 1, справа). Когда насекомые ели растения с заранее нарезанной на короткие фрагменты РНК, ответ их клеток оказывался слабым [4]. Во-первых, короткие двухцепочечные РНК, как показано на примере некоторых насекомых, могут хуже поглощаться клетками. Во-вторых, существует вероятность, что нарезанные «чужими» для насекомых белками фрагменты РНК вызывают слабую реакцию клетки. Необходимо было найти способ сохранять длинную дцРНК в клетках растений до попадания в пищеварительную систему жуков. И такой способ был предложен: решили перенести синтез дцРНК из ядра клетки в хлоропласты, где нет белка Dicer [5].
Как известно, хлоропласты произошли от цианобактерий, которые поселились внутри клеток эукариот, дав им возможность фотосинтезировать. У бактерий нет системы классической РНК-интерференции, потому и у хлоропластов ее тоже нет. Поэтому двухцепочечную РНК решено было производить именно в хлоропластах, чтобы она дошла до насекомых-вредителей в неразрезанном виде (рис. 1, слева). Кроме того, локализация дцРНК в хлоропластах практически исключает возможность её появления в клетках цветов, а следовательно, и нанесения вреда насекомым-опылителям.
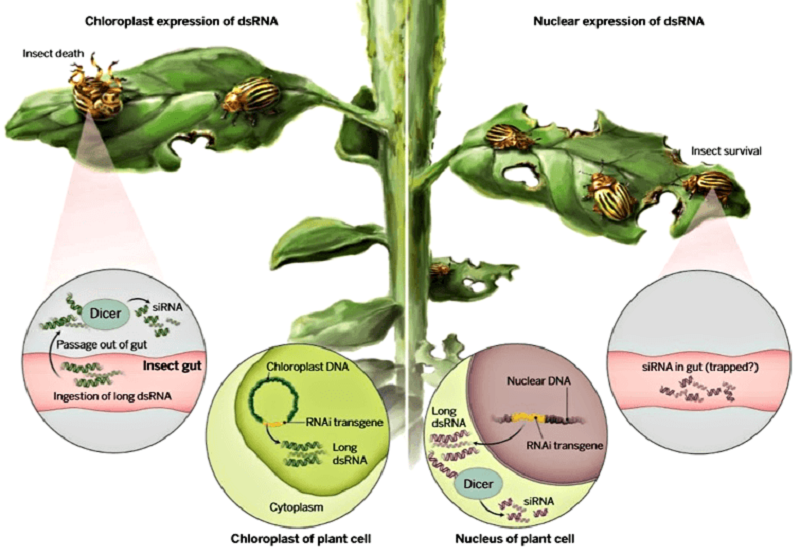
Рисунок 1. Схема защиты трансгенных растений от колорадского жука. Специфичность обеспечивается благодаря образованию в растении двухцепочечных РНК, соответствующих фрагменту жизненно важного гена определенного вредителя. Длинная дцРНК при попадании в клетку вызывает отключение соответствующего гена. Справа — двухцепочечная РНК синтезируется в ядре растительной клетки и режется на кусочки еще в самом растении. Такая короткая дцРНК не вызывает гибели существенного количества вредителей. Слева — ДНК, кодирующая двухцепочечную РНК, встроена в геном хлоропластов, и в этом случае РНК, оставшись невредимой, вызывает сильный ответ в клетках жуков, что приводит к их гибели.
Чтобы РНК образовывалась в клетках в двухцепочечном виде, синтезировали фрагменты ДНК, кодирующие обе цепи — смысловую и антисмысловую. Эти фрагменты встраивались в ДНК хлоропластов благодаря последовательностям нуклеотидов, гомологичным определённым последовательностям в хромосомах пластид. После синтеза двух молекул одноцепочечной РНК они налипали друг на друга и образовывали дцРНК.
ДНК-матрицу доставляли в хлоропласты, обстреливая листья растений крошечными золотыми «пулями», облепленными ее молекулами. После этого из листьев получали культуру клеток (каллус), из которой отбирали клетки, чьи хлоропласты содержали привнесенную ДНК. А из подходящих клеток выращивали целые растения (растение иногда удается восстановить из отдельных его фрагментов: возможно, вы пробовали проращивать, к примеру, стебли роз, из которых можно получить полноценное растение).

Рисунок 2. Листья «дикого» (слева) и трансгенного (справа) картофеля (в хлоропластах которого образуется двухцепочечная РНК для блокировки гена АСТ колорадского жука) каждый день давали личинкам. Фотография сделана на третий день эксперимента, и видно, что личинки колорадского жука почти не едят листья трансгенного картофеля.
В эксперименте с трансгенным картофелем использовали дцРНК для двух генов колорадского жука: ACT, кодирующего β-актин (белок цитоскелета), и SHR, кодирующего субъединицу белкового комплекса, вовлеченного в мембранную перестройку при транспорте везикул [5]. Двухцепочечная РНК, как и было задумано, синтезировалась в хлоропластах и сохраняла длину до попадания в организм колорадских жуков. Оказалось, что наиболее эффективна в деле борьбы с вредителями дцРНК для гена АСТ: когда листьями такого картофеля кормили личинок колорадского жука, все они погибали уже в течение трёх дней. Анализ подтвердил, что у личинок, которые питались листьями трансгенного картофеля, подавлялась экспрессия целевого гена. Листья трансгенного картофеля, в котором двухцепочечная РНК образовывалась в хлоропластах, были повреждены вредителями намного меньше, чем листья растений, у которых дцРНК синтезировалась в ядре, а также чем листья обычного картофеля (рис. 2).
Предложенный метод целенаправленной защиты растений от вредителей позволяет разработать различные варианты его применения. Например, последовательность нуклеотидов дцРНК можно подбирать таким образом, чтобы она действовала против нескольких видов насекомых, или производить в хлоропластах набор отдельных молекул двухцепочечной РНК для разных вредителей.
Литература
- Работа курьером, район — организм;
- Обо всех РНК на свете, больших и малых;
- Элементы: «ГМО — мифические опасности»;
- Steve Whyard. (2015). Insecticidal RNA, the long and short of it. Science. 347, 950-951;
- Jiang Zhang, Sher Afzal Khan, Claudia Hasse, Stephanie Ruf, David G. Heckel, Ralph Bock. (2015). Full crop protection from an insect pest by expression of long double-stranded RNAs in plastids. Science. 347, 991-994.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




