История автоматизации: от сифона к лаборатории роботов
02 ноября 2020
История автоматизации: от сифона к лаборатории роботов
- 2006
- 0
- 4
В роботизированное будущее: жми на газ!
иллюстрация Анастасии Волчок
-
Автор
-
Редакторы
-
Иллюстратор
Темы
Автоматизация — основа современной экспериментальной науки. В любой исследовательской лаборатории есть компьютеры и приборы, которые автоматизируют и существенно упрощают пробоподготовку, проведение экспериментов или анализ результатов. А уж в клинических и промышленных лабораториях или отделах разработки фармацевтических компаний можно найти полностью роботизированные модули или их комплексы, которые берут на себя заботы о приеме, анализе и хранении образцов. В этой статье, которая открывает спецпроект про автоматизацию в биологии, мы расскажем, как всё начиналось и как мы пришли к тому, что есть сейчас.
Автоматизация в биологии

Работа в современной биологической лаборатории кардинально отличается от той, что велась в ней каких-то 100–150 лет назад. Многие процедуры давно превратились в рутину, которую зачастую выполняет не сам экспериментатор, а автоматизированные приборы. Это позволяет не только упростить процесс, но и высвободить время для новых творческих задач. В спецпроекте «Автоматизация в биологии» мы проследим, какой путь прошли современные приборы, повсеместно использующиеся в экспериментах по геномике и протеомике, цитометрии, генной инженерии и драг-дизайну.
Куратором спецпроекта стал Денис Баев — глава центра коллективного пользования по проточной цитометрии и сортировке клеток Института канцерогенеза Кандиоло, Италия.
Партнер спецпроекта — компания Beckman Coulter Life Sciences, мировой лидер в разработке решений для автоматизации сложных биомедицинских лабораторных процессов.
Автоматизация необходима по нескольким причинам. Во-первых, машины меньше ошибаются. Уже сейчас специалисты говорят о кризисе воспроизводимости в современной науке [1–3]. Автоматизация же помогает избежать неточностей и ошибок, которые появляются из-за человеческого фактора. Во-вторых, для обслуживания автоматизированной лаборатории нужно меньше сотрудников, и это может существенно снизить стоимость проведения анализов или разработки лекарств [4], [5]. К тому же автоматизация позволяет оптимизировать процессы и работать 24 часа в сутки — всё делается быстрее. Наконец, для работы с автоматизированным оборудованием не нужно обладать глубинными познаниями в инженерии и электронике: достаточно выбрать нужные параметры процесса и нажать на кнопку. Всё это освобождает исследователей от рутины и позволяет им сконцентрироваться на творческих задачах.
Конечно, так было не всегда. Первое упоминание автоматизированного устройства для лаборатории появилось менее 150 лет назад — в 1875 году [6]. А еще до 50-х годов прошлого века не существовало готовых решений: исследователям приходилось быть по совместительству и инженерами и самим конструировать нужные для своих задач аппараты. В этом обзоре, который открывает цикл статей об автоматизации разных областей биологических исследований, мы попробуем разделить эволюцию автоматизации на этапы и понять, как меньше чем за 150 лет мы прошли путь от стеклянных трубок до полностью роботизированных лабораторий, почти не требующих участия человека.
В начале было стекло...
Отправной точкой в истории лабораторной автоматизации можно назвать изобретение, впервые упомянутое в 1875 году в журнале American Chemist [7]. Таддеус М. Стивенс, профессор аналитической химии из Индианы, описал механизм, который позволял оставлять без присмотра процесс промывки фильтрата. Это был стеклянный резервуар с двумя отверстиями: одно для выхода жидкости для промывки, второе — для поступления воздуха. Размер последнего можно было менять: чем оно больше, тем быстрее капала жидкость (рис. 1а).
Чтобы еще лучше контролировать процесс, исследователи начали использовать капилляры и сифоны. На рисунке 1б изображено одно из таких устройств: конец капилляра достигал воронки с фильтратом, и через него же поступал воздух в резервуар с промывочной жидкостью [8]. Когда воронка наполнялась, конец капилляра оказывался погружен. Воздух в емкость не поступал, и жидкость не капала. Когда воронка опустошалась, в капилляр начинал попадать воздух, и жидкость снова капала на воронку. Конкретно этот прибор был описан в 1917 году — стекло было основным материалом автоматизации еще долго, вплоть до 1950-х годов.
Сифоны — это изогнутые трубки, по которым жидкость может течь вверх без использования насоса, движимая дальнейшим током вниз. Их изобретение приписывается еще древним египтянам, а в 1892–1894 годах они легли в основу первых автоматической бюретки [9] и пипетки [10]. Принцип работы обеих схож: жидкость набирается в трубку резиновой грушей или ртом, а избыток жидкости, оказавшийся над нулевым уровнем, сливается обратно в сосуд через внутренний или внешний сифон (рис. 1В).
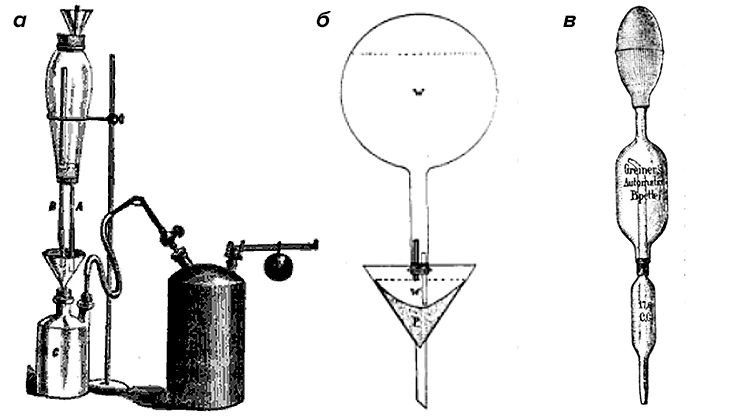
Рисунок 1. Первые опыты автоматизации лабораторных устройств. а — Первое автоматизированное устройство для автоматической промывки фильтрата, 1875 г. б — Прибор для промывки фильтрата с капилляром, который контролирует поступление жидкости для промывки, 1917 г. в — Первая автоматическая пипетка, 1894 г.
Итак, первые лабораторные автоматизированные приборы использовались в основном в аналитической химии для промывки фильтратов и проведения экстракций. Это были системы из стеклянных резервуаров, капилляров и сифонов; они имели сложную форму и в большинстве случаев выдувались конечными потребителями под конкретные задачи. Ни о каких коммерческих готовых решениях для лабораторий еще не было и речи. Однако они начали появляться и в других областях: потребителем первого автоматизированного устройства, которое можно было просто купить, ничего не изобретая и не конструируя, стала, пожалуй, важнейшая индустрия того времени — угольная. Для нее была создана дробилка для угля Sturtevant Automatic Coal Crusher, которая помогала получать однородные образцы для анализа качества сырья. Машина тщательно перемалывала кусочки угля и отбирала определенную часть полученной смеси.
Искра и электричество. Первая мировая и автоматизация промышленности
Стеклянные детали, несмотря на хрупкость и сложность в обращении, использовались в лабораториях еще долго — их закат стал очевиден только в 50-х годах XX века. Однако они плохо подходили для задач промышленности или военных нужд, и в первой четверти двадцатого века началась новая эра автоматизации — электрическая.
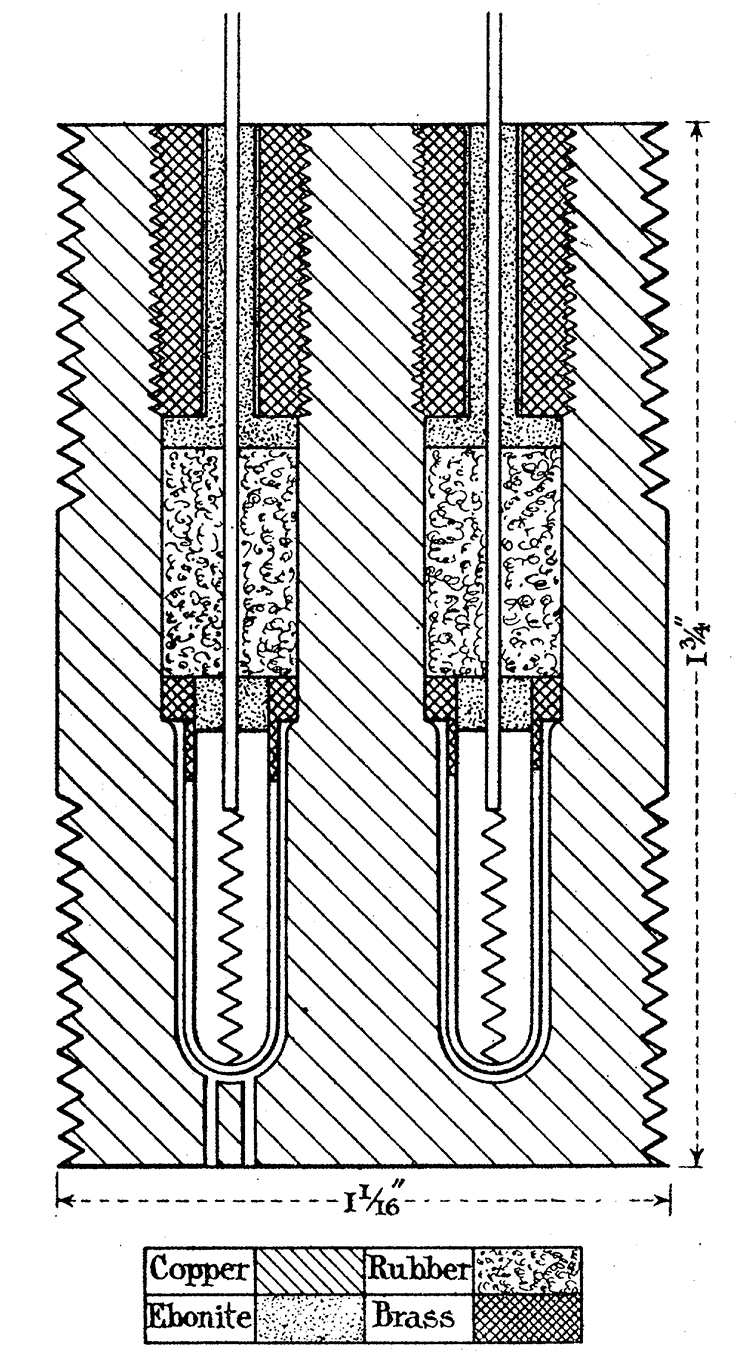
Во время Первой мировой войны стороны конфликта активно использовали воздушные шары, чтобы следить за движениями войск противника. Чтобы автоматически находить дефекты шаров, в 1915 году был придуман катарометр [11], или детектор газа по теплопроводности (рис. 2а), — сейчас такие используются в газовых хроматографах. Принцип работы прибора — измерение изменения проводимости нити накаливания под струей газа. Через нить накаливания пропускается постоянный ток, и при прохождении чистого газа температура нити остается постоянной. При добавлении другого газа, который обладает другой теплоемкостью, меняется общая теплоемкость смеси и, соответственно, проводимость нити.
Электричество проникло и в лаборатории. Титрование — способ определения количества вещества в растворе — играет огромную роль и в аналитической химии, и на производствах, и в клинических анализах. Принцип прямого титрования таков: к раствору с неизвестным количеством искомого вещества постепенно добавляют реагент, и по тому, сколько его пришлось израсходовать, определяют содержание вещества в исходном растворе. Ключевой момент метода — определение конечной точки титрования, то есть секунды, когда реакция завершена, и надо прекратить добавление реагента. Эту точку можно определять по изменению цвета, электродному потенциалу, pH, проводимости раствора и многими другими способами.
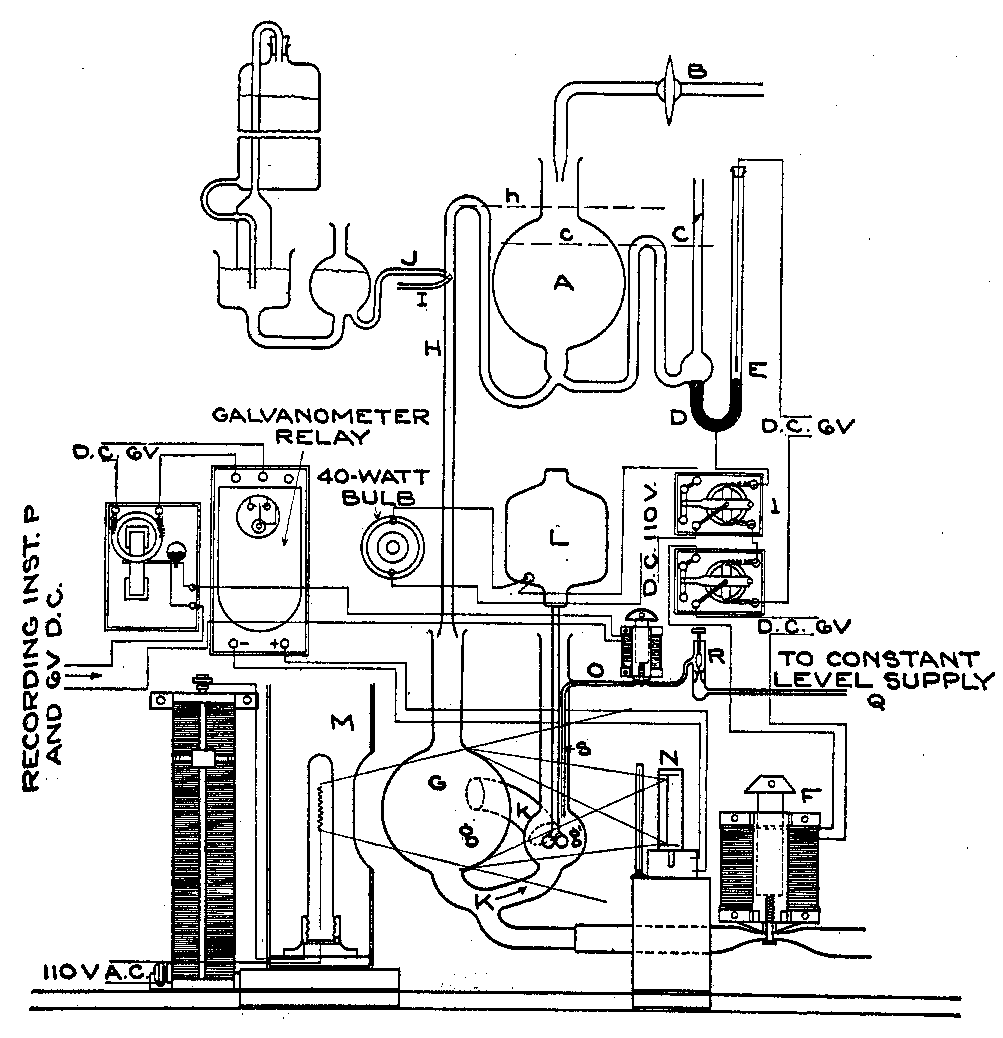
В 1959 году выпустили руководство по автоматическим титраторам [12]. К тому моменту их было множество — в обзоре есть сравнение десятка коммерческих приборов. Согласно нему, первый полуавтоматический титратор был создан в 1914 году — он автоматически определял конечную точку по изменению электродного потенциала. В 1928 году изобрели первый прибор, который использовал фотоэлемент, чтобы определять конечную точку по изменению цвета раствора, и радиолампу, чтобы дополнительно усиливать сигнал. По заявлению изобретателей, такой прибор был в 165 раз чувствительнее человеческого глаза. А в 1933 году на бумажном производстве появился первый полностью автоматизированный титратор, в котором было автоматизировано добавление и образца, и реагентов (рис. 2б) [13]. С одной стороны приемника образца находился сифон, ведущий в титровальную емкость, а с другой — столбик ртути. Когда приемник наполнялся, столбик ртути поднимался, замыкая два электрических контакта. В результате срабатывали клапаны, которые выливали предыдущий образец из емкости для титрования, и та постепенно наполнялась свежим раствором. По пути из приемника к образцу добавлялся индикатор. Фотоэлемент фиксировал результат титрования, который записывался самописцем.
Другим важным аналитическим изобретением стал pH-метр. От его отсутствия особенно страдала сахарная индустрия: рафинирование — это многоступенчатый процесс, и на многих этапах важно контролировать pH раствора. В 1928 году производители попытались использовать вольфрамово-каломельные электроды, но их было сложно калибровать и менять, они часто выходили из строя, и оказалось проще использовать обычные pH-индикаторы.
Использование pH-метров отложили, но ненадолго. В 1934 году Арнольд О. Бекман, профессор Калифорнийского технического университета, изобрел первый современный pH-метр (рис. 3а) [14]. Хотя изначальный «оптимистичный» расчет показывал, что он продаст порядка 600 экземпляров за 10 лет, в первый же, 1936, год у него купили 444 прибора. Новая модель G (рис. 3б) была представлена в 1937 году и продавалась до 50-х — к 1955 году продали более 126 тысяч приборов. Это изобретение стало первым успешным проектом компании National Technical Laboratories — будущей Beckman Instruments, а позднее — Beckman Coulter. Это изобретение было настолько значимым, что в 2004 году Американское химическое сообщество признало первый pH-метр Национальной исторической химической вехой (ACS National Historical Chemical Landmark).
Таким образом, к концу 30-х годов XX века стало понятно, что автоматизация необходима не только промышленности, но и лаборатории: она делает производство стабильнее, исследования проще, продукт — однороднее и дешевле, а его выход — больше.
Новая война — новый всплеск автоматизации
Участие во Второй мировой войне потребовало от всех стран, включая США, беспрецедентного роста промышленности [15]. Это наращивание мощностей осуществлялось силами большого количества быстро нанятых и не очень квалифицированных сотрудников. Чтобы делать сложную аналитическую работу и контролировать производство при ограниченных познаниях в физике и инженерии, им было необходимо полностью или полуавтоматическое оборудование. В дело пошли все прошлые наработки: например, стекло и электричество встретились в сифоне-таймере, который позволял включать и выключать прибор через регулярные промежутки времени. Устройство состояло из трубки, внутри которой находились электрические контакты и к которой присоединялся сифон. Когда трубка заполнялась водой, контакты замыкались, и прибор включался. Постепенно вода заполняла сифон и уходила по нему в другую емкость — контакты открывались, прибор выключался. Длительность циклов можно было регулировать глубиной расположения контактов: чем они выше, тем цикл короче.
Многие технологии были направлены на экономию и повторное использование реагентов и ценных металлов: так, самым сложным оборудованием того времени стал прибор для автоматического контроля тока при разделении меди и олова в растворе соляной кислоты.
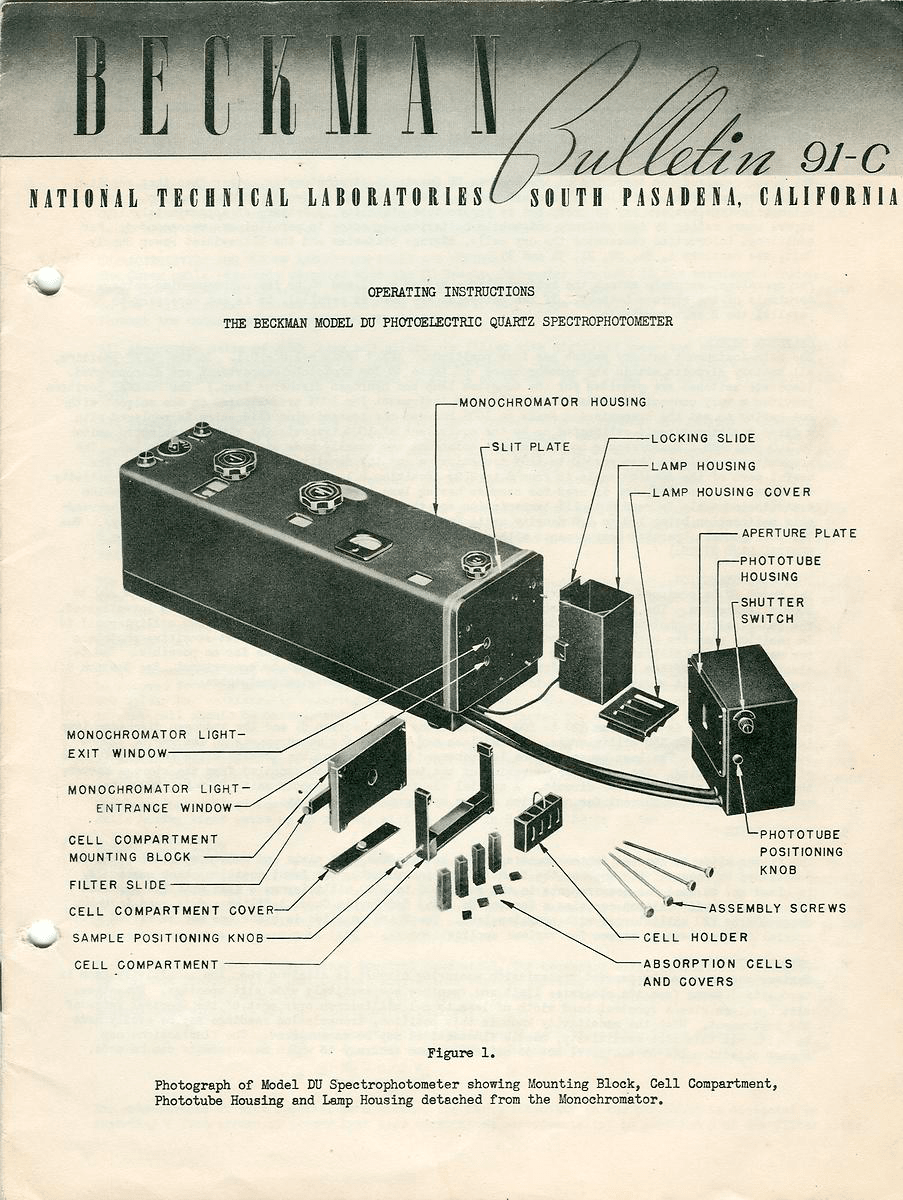
Возросла и потребность в фармацевтических исследованиях, например, изучении пенициллина и витаминов. В этих целях использовали первый коммерческий спектрофотометр DU, изобретенный тем же Арнольдом О. Бекманом [16], и работающий как в видимой, так и в УФ-части спектра (рис. 4а). До изобретения прибора в 1941 году набор оборудования для нахождения биомолекул и измерения их содержания обходился лабораториям в $3000 — по тем временам огромную сумму [17]. Нужно было проанализировать образец много раз при разных длинах волн, зафиксировать эти спектры на множестве фотопластинок и нанять специалиста, который сравнил бы эти спектры и составил один общий. Новый прибор сделал анализ сложных смесей точным и быстрым — то, что раньше требовало неделю, теперь занимало часы и минуты. Современные спектрофотометры (рис. 4б) построены по тем же принципам, что и их прародитель: в них есть такая же кварцевая призма и фотоэлемент, усиливающий сигнал.
Спектрофотометр стал одной из первых «черных коробочек» в лаборатории: исследователю не надо было разбираться в принципах механизма: он покупал прибор, ставил в него образцы, закрывал крышку, задавал нужные параметры и получал результат. По значимости для современного мира некоторые сравнивают этот прибор с первой машиной Форда — настолько же революционным и коммерческим было изобретение. Нобелевский лауреат Брюс Меррифилд назвал спектрофотометр, возможно, самым важным изобретением на пути развития биологической науки.
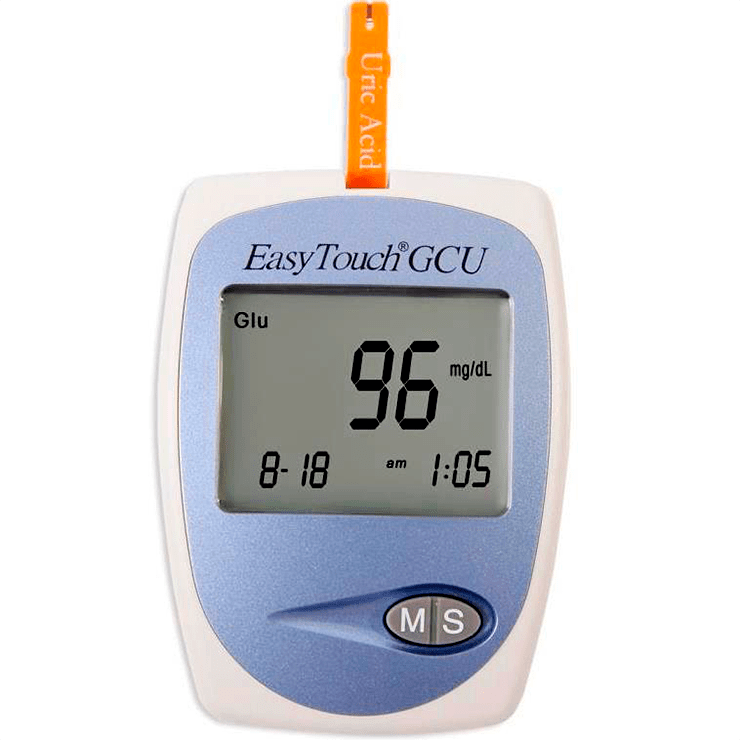
В 1956 году появился первый автоматический анализатор Technicon AutoAnalyzer (рис. 5а). Это был анализатор крови, который за две с половиной минуты измерял в ней уровень мочевины, сахара и кальция — основных веществ, по которым судят о наличии диабета, почечной недостаточности и других заболеваний. Компания Technicon позже стала частью Siemens, а сейчас пациенты могут делать простые анализы крови сами при помощью портативных анализаторов (рис. 5б) .
Наша статья посвящена, в основном, автоматизации лабораторных процессов, но о том, что происходит в клинике, можно прочитать, например, в статье «Что они делают с нашей кровью? Это уже клиника» [20]. — Ред.
Таким образом, всего за пару десятков лет фокус приложения автоматизации сместился со стекла на электричество, а итоговые приборы стали доступны для работы конечному потребителю практически с любой подготовкой: оказалось достаточно купить подходящую машину, вставить образцы и нажать на кнопку.
Компьютер и роботы
Все пути современной лаборатории (как и квартиры) ведут к компьютеру: он задает параметры, контролирует их соблюдение, получает и обрабатывает полученные данные. Первое упоминание компьютера в связи с автоматизацией пришлось на 1948 год. Компания Reeves Instrument Corporation начала рекламировать аналоговый компьютер, который моделировал дифференциальные уравнения (рис. 6а). Это было нужно химикам-исследователям и тем, кто придумывал автоматическое оборудование для контроля производственных процессов. А уже через четыре года в лабораторию пришел и цифровой компьютер: Atlantic Refining Company совместила его с масс-спектрометром (рис. 6б) [21]. Это устройство могло сделать полный анализ смеси из двадцати углеводородов за 10 минут и напечатать результат на бумажной ленте. Так появилось привычное современное сочетание прибора с ПК.
Следующим этапом на пути к полностью автоматизированной лаборатории стала роботизация. Первого промышленного робота запатентовали в 1961 году: это был простой манипулятор Unimate, который «служил» на сборочной линии General Motors (видео 1). В последующие 1960–70-е годы роботы играли важную роль в космической программе США, их управление развивалось, а размеры становились все меньше. И, конечно, скоро им нашлось место во вполне земных лабораториях.
Видео 1. Работа манипулятора Unimate
В 1981 году была основана компания Zymark Corporation [22], которая выпустила Zymate Laboratory Automation System (рис. 7а) — единственную на тот момент систему, специально разработанную для химических и биотехнологических лабораторий. Ее центральным звеном был Zymate Robot — манипулятор под контролем микропроцессора, который крутился, двигался по горизонтали и вертикали и мог поднимать и перемещать пробирки, мерные стаканы и колбы, переливать жидкости из одной емкости в другую и, главное, быстро передвигаться между несколькими лабораторными станциями, расставленными вокруг него. Он мог совершать лабораторные манипуляции, получать данные и проверять их по заданному критерию качества, при необходимости перепроверять образцы, ставить стандарты и контроли или менять процедуру, пока не будет получен достоверный результат. В 1982 году робот был представлен публике на Питтсбургской конференции по аналитической химии и прикладной спектроскопии PittCon. Там методом твердофазной экстракции он разделил популярный напиток — виноградный Kool-Aid — на три компонента: красный, синий и прозрачный (рис. 7б).
К 1986 году компания представила обновленную версию системы, в ней были новые лабораторные станции, сменные кисти и интерфейсы [23]. В нее можно было интегрировать разные аналитические инструменты и увеличивать производительность лабораторий с учетом их нужд и запросов. Так, подобные роботы стали использоваться в преаналитической подготовке образцов, а также в тестировании эффективности и стабильности препаратов в фармацевтической индустрии. Работники же клинических лабораторий начали использовать их для лабораторных анализов, которые было сложно выполнять вручную: например, для иммуногистохимического анализа рецепторов к эстрогенам [24].
Лабораторная автоматизация на полную катушку: 1980–90-е годы XX века
Следуя за успехом Zymate, многие другие компании представили свои решения для автоматизации лабораторных процессов. В первую очередь это было оборудование для точного и массового дозирования, которое снижало вероятность человеческой ошибки в этом простом, но монотонном процессе. Именно в то время обозначились основные игроки современного рынка автоматического лабораторного оборудования. Так, в 80-х появились платформы Hamilton Microlab. В начале 90-х годов устройство Microlab 2200 использовалось, например, для автоматизации измерения уровня гликогемоглобина методом аффинной хроматографии [25] или проведения экстракции веществ на твердой фазе [26]. Обновленные приборы серии выпускаются и сейчас.
В то же время была разработана платформа от компании Tecan, которая использовалась для синтеза на твердой фазе потенциальных новых лекарств [27]. Станция Biomek 1000 компании Beckman Coulter также изначально создавалась для решения задач фармацевтических компаний, но позже нашла применение и во многих молекулярно-генетических задачах, например, подготовке ДНК к ПЦР и секвенированию [28], выделении геномной ДНК из клеток [29] и других. Современные платформы Biomek конструируются и оптимизируются под выполнение самых разных задач: от манипуляций с генетическим материалом до работы с клеточными культурами.
Кроме того, в 1980-е годы появились попытки совместить несколько роботов и анализаторов, наладить между ними связь с помощью конвейеров или других роботов и получить полностью роботизированную лабораторию, которая может работать без участия человека. Такой подход особенно актуален при автоматизации клинических лабораторий: элементы соединяются в непрерывную производственную линию и последовательно выполняют простые манипуляции, позволяющие получить результат лабораторного анализа.
Наши дни
Современные эксперты предсказывают несколько трендов будущего развития автоматизации лабораторий.
Один из них — диджитализация и использование облачных хранилищ и систем. Например, облачная интеграция лабораторных устройств, чтобы ученые могли лучше планировать эксперименты и отказаться от устаревшей ручной обработки данных. Или организация доступа небольших лабораторий к крупным облачным хранилищам данных — например, к инфраструктуре ЦЕРН. И, конечно, будущее не обойдется без работы с большими данными (Big Data).
Другой тренд — «коботизация»: использование «коботов» — роботов, которые оснащены датчиками силы и препятствий, а потому могут работать не отдельно, а в коллаборации с учеными. Так роботы могут стать полноценными коллегами сотрудников лабораторий, а не просто слепо следовать программе.
Что касается полной автоматизации лабораторий, несмотря на изначальный оптимизм, она всё же пока оказывается слишком сложной и дорогой для большинства небольших научно-исследовательских лабораторий. К тому же, нередко разные производители приборов делают комплектующие по-разному, и их нельзя совместить с деталями других компаний. Конвейеры разной высоты, пробирки и штативы для них разной формы и размера, разный софт, интерфейсы — всё это затрудняет интеграцию и замену сломавшихся деталей. В середине 1990-х годов некоторые производители и пользователи автоматизированных систем объединились для решения этой проблемы. Например, в комитет вошли представители Coulter Corporation [34] (теперь в составе Beckman Coulter), Клиника Мэйо, Boehringer Mannheim Diagnostics (теперь в составе компании «Рош») и Becton Dickinson Container System (сейчас Becton Dickinson). В 1996 они, вместе с NCCLS (Национальным комитетом по клиническим и лабораторным стандартам), начали разрабатывать единые стандарты интерфейсов, контейнеров, штрихкодов и других деталей, необходимых для слаженной работы системы. Сейчас NCCLS переименован в CLSI (Институт клинических лабораторных стандартов), и в него входит более 1400 организаций. Сегодня полностью автоматизированные лаборатории применяются в основном в отделах R&D фармацевтических компаний [35]. Там их стоимость оправдана: они позволяют в несколько раз быстрее делать скрининг потенциальных лекарств и, соответственно, получать и производить новые препараты (видео 4).
Видео 4. Система полной автоматизации лаборатории Power Express от Beckman Coulter
Клиническим и исследовательским лабораториям больше подходят модульные автоматизированные решения (видео 5). Разные модули выполняют конкретные функции: центрифугирование и аликвотирование, анализ образцов, постаналитическое хранение или поиск. Так каждая лаборатория может выбирать, какую функцию ей выгоднее автоматизировать, а при необходимости собрать из модулей и полностью автоматизированную лабораторию.
Видео 5. Модуль для преаналитической обработки образцов (загрузки, сортировки, аликвотирования, маркировки) Automate 2550 от Beckman Coulter
Видео 6. Работа клинических лабораторий в 1966 г.
Видео 7. Работа клинических лабораторий в 2011 г.
Видео 8. Работа клинических лабораторий в 2019 г.
За почти 150 лет и один обзор мы прошли путь автоматизации от простой возможности контролировать скорость фильтрации до полностью автоматизированных лабораторий, которые сами тестируют (а некоторые — еще и придумывают) новые лекарства и делают анализы (рис. 9). Мы прошли этапы стекла, электричества, компьютеров и роботов, видели влияния требований промышленности и войн и наблюдали за тем, как передовые технологии прошедшего десятилетия становились рутиной следующего. Но на всем протяжении цель автоматизации оставалась неизменной: сделать науку точнее и доступнее.
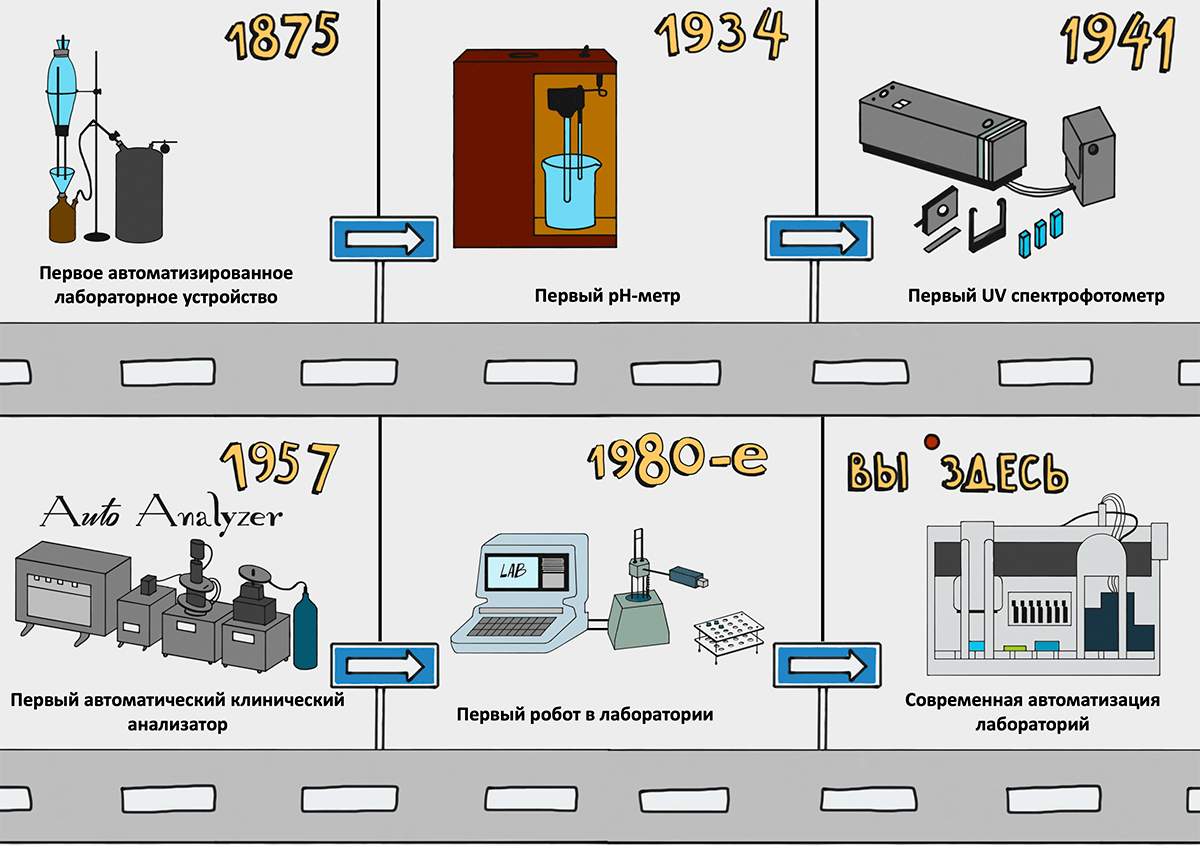
Рисунок 10. Краткая история автоматизации лабораторного оборудования
иллюстрация Анастасии Волчок
В следующих статьях цикла читайте о том, как появились роботы, которые могут сами поставить ПЦР и секвенсовую реакцию, вырастить и рассортировать клетки, придумать новые лекарства и выбрать из них лучшие и многое-многое другое.
Литература
- S. Buck. (2015). Solving reproducibility. Science. 348, 1403-1403;
- Мечты о воспроизводимости;
- Кризис в науке: проблема воспроизводимости. (2017). «Популярная механика»;
- Laszlo Sarkozi, Elkin Simson, Lakshmi Ramanathan. (2003). The effects of total laboratory automation on the management of a clinical chemistry laboratory. Retrospective analysis of 36 years. Clinica Chimica Acta. 329, 89-94;
- Claudia Archetti, Alessandro Montanelli, Dario Finazzi, Luigi Caimi, Emirena Garrafa. (2017). Clinical laboratory automation: a case study. J Public Health Res. 6;
- Kevin Olsen. (2012). The First 110 Years of Laboratory Automation. J Lab Autom.. 17, 469-480;
- Stevens T.M. (1875). Rapid and automatic filtration. Am. Chem. 6, 102;
- Elbert C. Lathrop. (1917). A Simple Device for the Automatic and Intermittent Washing of Precipitates.. J. Ind. Eng. Chem.. 9, 527-528;
- Edward R. Squibb. (1894). AUTOMATIC ZERO BURETTE.. J. Am. Chem. Soc.. 16, 145-148;
- Emil. Greiner. (1894). A NEW AUTOMATIC PIPETTE.. J. Am. Chem. Soc.. 16, 643-643;
- Daynes H.A. and Shakespear G.A. (1920). The theory of the katharometer. Proc. R. Soc. Lond. A. 97, 273-286;
- Philips J. Automatic titrators. Elsevier, 2012. — 234 p.;
- K. Hickman, C. R. Sanford. (1933). Automatic Titrating Devices. Ind. Eng. Chem. Anal. Ed.. 5, 65-68;
- Development of the Beckman pH Meter. (2004). National Historic Chemical Landmark;
- Kevin K. Olsen. (1997). Rosie the Robot, Laboratory Automation and the Second World War, 1941 to 1945. Laboratory Robotics and Automation. 9, 105-112;
- Simoni R.D., Hill R.L., Vaughan M., Tabor H. (2003). A classic instrument: the beckman DU spectrophotometer and its inventor, Arnold O. Beckman. J. Biol. Chem. 49: e1;
- Thackray A. and Myers M. Arnold O. Beckman: one hundred years of excellence. Chemical Heritage Foundation, 2000 — 379 p.;
- Эволюция наперегонки, или Почему антибиотики перестают работать;
- Антибиотики и антибиотикорезистентность: от древности до наших дней;
- Что они делают с нашей кровью? Это уже клиника!;
- C&EN REPORTS: Pittsburgh Conference on Analytical Chemistry and Applied Spectroscopy. (1952). Chem. Eng. News. 30, 1092-1094;
- Conal F. Timoney, Robin A. Felder. (1998). A Pioneering Company in Laboratory Automation. JALA: Journal of the Association for Laboratory Automation. 3, 12-16;
- James N. Little. (1986). The Zymate Laboratory Automation Systems. Journal of Liquid Chromatography. 9, 3197-3201;
- Robin A. Felder. (1992). Clinical laboratory robotics in the 1990s. Chemometrics and Intelligent Laboratory Systems. 17, 111-118;
- C D Herold, K Andree, D A Herold, R A Felder. (1993). Robotic chromatography: development and evaluation of automated instrumentation for assay of glycohemoglobin. Clinical Chemistry. 39, 143-147;
- Paul D. Whitter, Paul L. Cary, John I. Leaton, Jim E. Johnson. (1999). Automated Extraction for the Analysis of 11-nor-Δ9-Tetrahydrocannabinol-9-Carboxylic Acid (THCCOOH) in Urine Using a Six-Head Probe Hamilton Microlab 2200 System and Gas Chromatography-Mass Spectrometry. Journal of Analytical Toxicology. 23, 286-289;
- Thomas A.W. and Nettekoven M. (2002). Accelerating drug discovery by integrative implementation of laboratory automation in the work flow. Current Medicinal Chemistry. 9, 2179–2190;
- A. B. Civitello, S. Richards, R. A. Gibbs. (1992). A simple protocol for the automation of DNA cycle sequencing reactions and polymerase chain reactions. DNA Sequence. 3, 17-23;
- Mischiati C., Feriotto G., Gambari R. (1993). A new automated method for isolation of genomic DNA from eukaryotic cells. Boll. Soc. Ital. Biol. Sper. 69, 7–11;
- Masahide Sasaki, Takeshi Kageoka, Katsumi Ogura, Hiromi Kataoka, Tadashi Ueta, Shigeyoshi Sugihara. (1998). Total laboratory automation in Japan. Clinica Chimica Acta. 278, 217-227;
- Masahide Sasaki. (1993). A fully automated clinical laboratory. Chemometrics and Intelligent Laboratory Systems. 21, 159-168;
- Felder R.A., Savory J., Margrey K.S., Holman J.W., Boyd J.C. (1995). Development of a robotic near patient testing laboratory. Arch. Pathol. Lab. Med. 119, 948–951;
- 12 методов в картинках: иммунологические технологии;
- Charles D Hawker, Marc R Schlank. (2000). Development of Standards for Laboratory Automation. Clinical Chemistry. 46, 746-750;
- Hawker C.D., Genzen J.R., Wittwer C.T. Automation in the clinical laboratory. In: Rifai N. Tietz textbook of clinical chemistry and molecular diagnostics (6th Edition). Saunders, 2018. — 1888 p..
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚