Холестерин против COVID-19? Анализ новых исследований
22 марта 2021
Холестерин против COVID-19? Анализ новых исследований
- 6332
- 0
- 2
Модель молекулы холестерина. Возможно, развитие коронавирусной инфекции во многом связано с ним.
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В 2020 году в интернете появилось много противоречивых публикаций о связи уровня холестерина с тяжестью протекания коронавирусной инфекции COVID-19. Но как холестерин и коронавирус влияют друг на друга на самом деле? Не найдя убедительных ответов, мы попробовали разобраться в проблеме самостоятельно.
Конкурс «Био/Мол/Текст»-2020/2021
 Эта работа заняла второе место в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Эта работа заняла второе место в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
24 октября 2020 года журнал Cell предопубликовал исследование, в ходе которого ученые выявили гены человека, ассоциированные с заражением коронавирусом SARS-CoV-2 и заболеванием [1]. Публикации, рассматривавшие изменения в работе белков, выходили и раньше, однако исследователи Нью-Йоркского университета первыми изучили связь с развитием инфекции на уровне генома и проверили ее. Они обнаружили шесть генов (рис. 1), работа которых как бы помогала заражению посредством торможения биосинтеза холестерина. «Отключение» этих генов в клетках легких ускоряло его производство, препятствуя инфицированию.
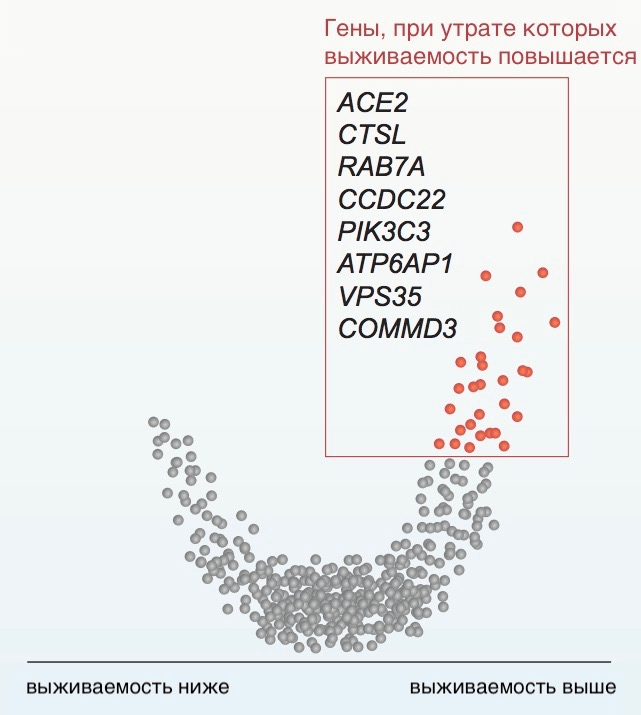
Рисунок 1. Выживаемость клеток при «отключении» различных генов (выживаемость для каждого гена показана своей точкой). Рамкой выделены гены человека, «отключение» которых увеличивало выживаемость. Среди них те самые шесть регуляторов, которые оказались важны для SARS-CoV-2 при инфицировании клетки. Выживаемость при «отключении» различных генов определена на основе экспериментов с CRISPR-Cas9 над клетками эпителия альвеол из карциномы легкого. Рисунок представляет собой так называемый volcano plot, на котором по оси абсцисс нанесена величина различий, а по оси ординат — их статистическая значимость.
Поскольку выявленные гены кодируют регуляторы синтеза не только холестерина, но и различных липидов, делать выводы о важности роли именно холестерина было бы нельзя, если бы не одно совпадение. В рамках того же исследования, но несколько позднее, ученые проверяли воздействие более 20 000 препаратов, которые могли бы подойти для лечения коронавирусной инфекции, и обнаружили, что оказавшиеся эффективными вещества активировали биосинтез холестерина. Кроме того, в дополнительных экспериментах амлодипин — препарат, повышающий количество холестерина внутри клеток [6], — способствовал тому, что клетки эпителия альвеол успешнее боролись с инфекцией [1].
Однако есть масса данных о том, что легче коронавирусную инфекцию переносят люди, которые принимают статины — препараты, понижающие уровень холестерина [7], [8]. Чтобы разобраться, на чьей стороне правда, давайте рассмотрим проблему внимательней.
Холестерин мешает коронавирусу?
Начнем с гипотезы «холестерин против ковида», ее подтверждает широкий ряд доводов. Ранее в рамках другого исследования та же исследовательская группа установила, что протекание коронавирусной инфекции подавляет синтез холестерина [9]. Это подтверждается и реальными данными. У ковидных пациентов больницы в Вэньчжоу во время болезни количество холестерина в плазме крови резко снижалось — почти вдвое [10], [11]. Тем интересней, что степень падения холестерина соответствовала тяжести заболевания, и самый низкий уровень зафиксировали у пациентов в критическом состоянии. То же следует из данных, опубликованных сотрудниками Уханьского университета, и данных корейских ученых [12], [13].
Верно и обратное: лекарства, стимулирующие работу тех же путей синтеза холестерина, которые ковид тормозил, препятствовали развитию инфекции, судя по результатам экспериментов над клеточными культурами [9]. Среди проверенных лекарств был и амлодипин, красной нитью ведущий нас к клиническим данным, скрытым чуть дальше. Этот эффект установлен также вне стен лабораторий: сразу два клинических исследования 2020 года обнаружили, что инфицированные коронавирусом пациенты, которые принимали амлодипин или препараты с аналогичным механизмом действия, умирали в несколько раз реже, чем не принимавшие. И ИВЛ им были нужны в разы реже. И в реанимации их удавалось спасти чаще в разы. Данные, собранные в больницах Тунцзи в Китае [14] и Бруклина в США [15], не противоречат друг другу, будучи полученными на разных континентах. Правда, это информация о небольшом количестве пациентов (в первом случае о десятках, во втором случае о сотнях), и необходимы дальнейшие, более обширные проверки. Но в совокупности с результатами лабораторных исследований эти клинические данные выглядят довольно надежно. Велика сила науки!
Конечно, здесь перед нами встает вопрос, не может ли такой «больничный» эффект амлодипина объясняться его основным, сосудорасширяющим, действием? Ведь принимая его, пациенты могли снизить вероятность смерти от закупорки артерий. Могли, однако лабораторные данные говорят о том, что амлодипин мешает коронавирусу буквально на клеточном уровне.
Взаимосвязь холестерина и коронавируса
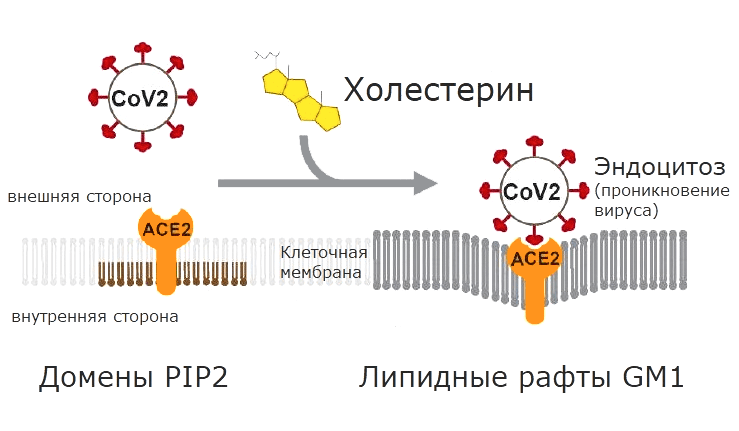
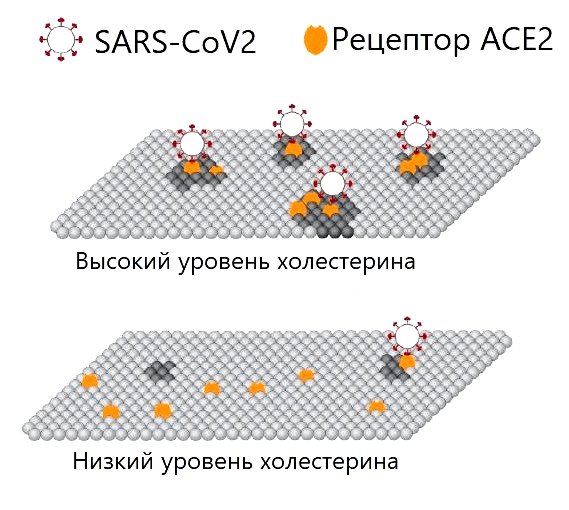
Так как холестерин может быть связан с коронавирусом? Войдя в контакт с поверхностными рецепторами ACE2, вирус должен проникнуть внутрь клетки, обернувшись участком наружной мембраны. Значительно успешнее проникновение через мембраны, в которых много холестерина (рис. 2, 3) [16].
Но как «потребность» в мембранном холестерине у коронавируса совмещается с тем, что активация биосинтеза холестерина мешает развитию инфекции? Ведь должно же быть наоборот! Реальные механизмы связи развития ковида с синтезом холестерина неизвестны. Ученым только предстоит обнаружить их. А пока они заняты, мы, не встретив ни одного объяснения, предложили свое.
Вот наша гипотеза
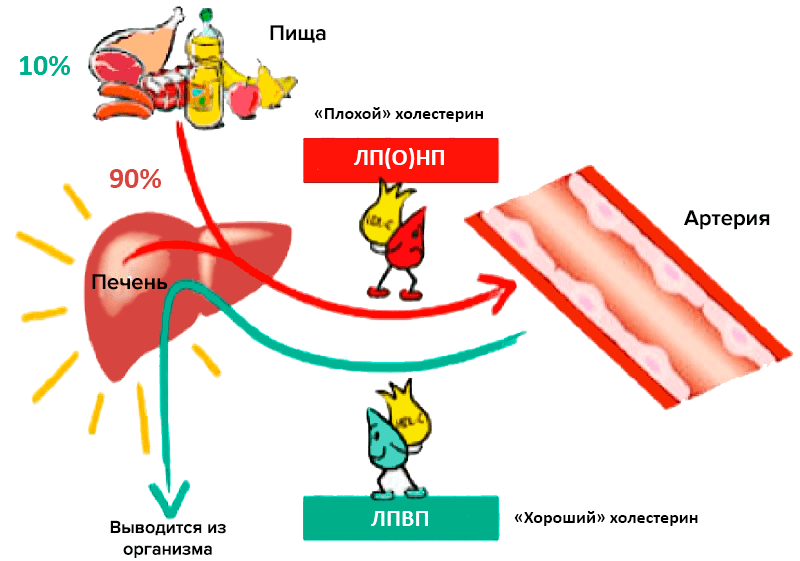
На самом деле, всё это не так странно, как кажется. В клетки печени холестерин собирается со всего организма специальными транспортными системами — это тот самый так называемый хороший холестерин. А дальше организм от него de facto избавляется, выделяя в кишечник в составе желчи (рис. 4). В кишечнике же происходит обратный захват, и обычно бо́льшая часть холестерина возвращается в организм. Но этот обратный захват регулируется, и его активность может изменяться . Помните упавший холестерин у тяжелобольных? У этих людей падал в крови уровень как «хорошего», так и «плохого» холестерина. Особенно заметно уменьшение количества «хорошего» холестерина, который мог «эвакуироваться» через печень, и уже не возвращался.
Подробнее про обмен холестерина читайте на «Биомолекуле» [2].
В то же время так называемый «плохой» холестерин, наоборот, разносится по всему организму. Со временем его остатки поглощаются макрофагами и выводятся из организма, также через печень. При избытке «плохого» холестерина они, перегруженные, оседают на стенках артерий. Так появляются те самые атеросклеротические бляшки, которые сужают просвет сосудов, мешая движению крови.
Так вот, еще в исследованиях амлодипина, проведенных в 1980-е годы, было установлено, что при воздействии этого препарата «плохой» холестерин начинал активно запасаться [6], [19]. Клетки забирали его из кровотока, пряча внутрь себя, это подтверждается и более свежими исследованиями [20], [21]. Так уровень холестерина в крови снижался, что могло привести к уменьшению его количества в мембранах клеток, в первую очередь клеток легких, куда он забирался из крови. А это уже преграда на пути вируса.
Вот пока единственное из пришедшего нам в голову, что объясняет происходящее. Приглашаем читателя поучаствовать в дискуссии.
Статины лечат коронавирусную инфекцию?
Как видите, система обмена холестерина в организме очень сложна, поэтому невозможно говорить о пользе использования статинов при COVID-19 однозначно. Давайте по порядку.
Прием статинов до заражения коронавирусом и госпитализации действительно повышал вероятность более легкого течения болезни и благополучного исхода [7], [8], [22]. Потому что со временем благодаря им в организме уменьшается количество «плохого» холестерина. То есть затем его становится меньше в мембранах различных тканей, и вирусу всё сложнее и сложнее заражать клетки. Кроме того, ниже вероятность осложнений при COVID-19, потому что статины стабилизируют атеросклеротические бляшки и тем самым как бы противостоят влиянию на них цитокинового шторма, который развивается при COVID-19 [22].
Однако этот эффект вообще не успевает развиться, если начать принимать статины уже после заражения коронавирусом. Потому что сперва количество холестерина в мембранах, наоборот, повышается, так как в качестве ответа на снижение синтеза захватывается больше «плохого» холестерина [23]. Как понимаете, это только помогает развитию инфекции. Такое быстрое действие статинов оказывается полезным в критических состояниях благодаря их иммуномодулирующему и антитромботическому эффектам [24], в остальных случаях совмещать статины с ковидом может быть опасно. Поэтому статины для лечения коронавирусной инфекции вряд ли годятся. Впрочем, только клинические исследования могут окончательно ответить на такие вопросы.
Итак, холестерин играет видную роль в развитии коронавирусной инфекции, и препараты, которые влияют на его обмен, облегчают протекание болезни на разных ее этапах. Поэтому в статье нам было интересно связать разрозненные данные о взаимном влиянии SARS-CoV-2 и холестерина в цельную картину. Это важно для понимания эффектов различных препаратов, неоднозначных из-за сложности обмена холестерина. Сейчас актуальна инфекция COVID-19, но даже когда эпидемия сойдет на нет, понимание взаимосвязи коронавирусных инфекций и холестерина будет полезным для быстрой разработки лечения инфекций новых коронавирусов: этот не первый и не последний (очень похоже влияние мембранного холестерина на первый SARS-CoV [25]). Кроме того, обсуждение этой темы обращает внимание на важность холестерина в развитии инфекций многих других вирусов. Например, публикуются исследования подобного рода, касающиеся вируса иммунодефицита человека [26], [27].
Литература
- Zharko Daniloski, Tristan X. Jordan, Hans-Hermann Wessels, Daisy A. Hoagland, Silva Kasela, et. al.. (2021). Identification of Required Host Factors for SARS-CoV-2 Infection in Human Cells. Cell. 184, 92-105.e16;
- Хороший, плохой, злой холестерин;
- Сколько можно съесть мышиного яду? Очерк о витамине D;
- Холестериновая страшилка, которая правит миром;
- Липидный фундамент жизни;
- SEIJIRO MORI, HIDEKI ITO, KIYOTAKA YAMAMOTO. (1988). Effects of calcium antagonists on low density lipoprotein metabolism in human arterial smooth muscle cells.. Tohoku J. Exp. Med.. 154, 329-333;
- Lori B. Daniels, Amy M. Sitapati, Jing Zhang, Jingjing Zou, Quan M. Bui, et. al.. (2020). Relation of Statin Use Prior to Admission to Severity and Recovery Among COVID-19 Inpatients. The American Journal of Cardiology. 136, 149-155;
- Vincenzo Castiglione, Martina Chiriacò, Michele Emdin, Stefano Taddei, Giuseppe Vergaro. (2020). Statin therapy in COVID-19 infection. European Heart Journal - Cardiovascular Pharmacotherapy. 6, 258-259;
- Hoagland D.A., Clarke D.J.B., Møller R., Han Y., Yang L., Wojciechowicz M.L. et al. (2020). Modulating the transcriptional landscape of SARS-CoV-2 as an effective method for developing antiviral compounds. bioRxiv;
- Xingzhong Hu, Dong Chen, Lianpeng Wu, Guiqing He, Wei Ye. (). Low Serum Cholesterol Level Among Patients with COVID-19 Infection in Wenzhou, China. SSRN Journal;
- Xingzhong Hu, Dong Chen, Lianpeng Wu, Guiqing He, Wei Ye. (2020). Declined serum high density lipoprotein cholesterol is associated with the severity of COVID-19 infection. Clinica Chimica Acta. 510, 105-110;
- Nie S., Zhao X., Zhao K., Zhang Z., Zhang Z., Zhang Z. (2020). Metabolic disturbances and inflammatory dysfunction predict severity of coronavirus disease 2019 (COVID-19): a retrospective study. medRxiv;
- Wonhwa Lee, June Hong Ahn, Hee Ho Park, Hong Nam Kim, Hyelim Kim, et. al.. (2020). COVID-19-activated SREBP2 disturbs cholesterol biosynthesis and leads to cytokine storm. Sig Transduct Target Ther. 5;
- Lei-Ke Zhang, Yuan Sun, Haolong Zeng, Qingxing Wang, Xiaming Jiang, et. al.. (2020). Calcium channel blocker amlodipine besylate therapy is associated with reduced case fatality rate of COVID-19 patients with hypertension. Cell Discov. 6;
- Isaac Solaimanzadeh. (2020). Nifedipine and Amlodipine Are Associated With Improved Mortality and Decreased Risk for Intubation and Mechanical Ventilation in Elderly Patients Hospitalized for COVID-19. Cureus;
- Wang H., Yuan Z., Pavel M.A., Hansen S.B. (2020). The role of high cholesterol in age-related COVID19 lethality. bioRxiv;
- Липидный фундамент жизни;
- Кавеолы: уникальные «порталы» клеточной мембраны;
- S. Ranganathan, J.A.K. Harmony, R.L. Jackson. (1982). Effect of Ca2+ blocking agents on the metabolism of low density lipoproteins in human skin fibroblasts. Biochemical and Biophysical Research Communications. 107, 217-224;
- I. Salehi, M. Mohammadi, F. Mirzaei, F.G. Soufi. (2012). Amlodipine attenuates oxidative stress in the heart and blood of high-cholesterol diet rabbits. Cardiovascular Journal of Africa. 23, 18-22;
- Zekeriya Arslan, Seyit Ahmet Ay, Murat Karaman, Mustafa Cakar, Turgay Celik, et. al.. (2013). An Additional LDL-Lowering Effect of Amlodipine; Not Only an Antihypertensive?. Clinical and Experimental Hypertension. 35, 449-453;
- Dina Radenkovic, Shreya Chawla, Matteo Pirro, Amirhossein Sahebkar, Maciej Banach. (2020). Cholesterol in Relation to COVID-19: Should We Care about It?. JCM. 9, 1909;
- Eva Kočar, Tadeja Režen, Damjana Rozman. (2021). Cholesterol, lipoproteins, and COVID-19: Basic concepts and clinical applications. Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids. 1866, 158849;
- Xiao-Jing Zhang, Juan-Juan Qin, Xu Cheng, Lijun Shen, Yan-Ci Zhao, et. al.. (2020). In-Hospital Use of Statins Is Associated with a Reduced Risk of Mortality among Individuals with COVID-19. Cell Metabolism. 32, 176-187.e4;
- Geetanjali Meher, Surajit Bhattacharjya, Hirak Chakraborty. (2019). Membrane Cholesterol Modulates Oligomeric Status and Peptide-Membrane Interaction of Severe Acute Respiratory Syndrome Coronavirus Fusion Peptide. J. Phys. Chem. B. 123, 10654-10662;
- Melaku Adal, Rawleigh Howe, Desta Kassa, Abraham Aseffa, Beyene Petros. (2018). Associations of gender and serum total cholesterol with CD4+ T cell count and HIV RNA load in antiretroviral-naïve individuals in Addis Ababa. BMC Public Health. 18;
- Sekai C. Mathabire Rücker, Alia Tayea, Joseph Bitilinyu-Bangoh, Elkin H. Bermúdez-Aza, Leon Salumu, et. al.. (2018). High rates of hypertension, diabetes, elevated low-density lipoprotein cholesterol, and cardiovascular disease risk factors in HIV-infected patients in Malawi. AIDS. 32, 253-260.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚