
Микро-/нанороботы — новые Друзья человечества
14 июля 2020
Микро-/нанороботы — новые Друзья человечества
- 2957
- 3
- 2
Подвижные объекты: микроробот, змея, подводная лодка и ракета
рисунок автора статьи
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Все удивительное начинается с природы. Первые «двигатели» микрометрового размера были созданы ею миллиарды лет назад. Ими были бактериальные жгутики, которые преобразовывали энергию химических связей АТФ в движение на микроуровне. В последние десятилетия ученые, вдохновленные этим изобретением, пытаются приручить молекулы для создания подобных микро- и наномашин. Недавние работы на стыке нанотехнологий, медицины и робототехники доказывают: микро-/нанороботы могли бы помочь нам изобрести эффективные подходы в доставке лекарств и создать сверхчувствительные методы диагностики заболеваний; они быстро и точно выполнят автономные хирургические операции на клеточном или молекулярном уровнях; обнаружат источник загрязнения воды и очистят ее от токсинов. Этот обзор — о самых перспективных инновациях в области бионаноробототехники и о возможностях ее применения.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2020/2021.

Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.

Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Часть 1. Вступление
Самые маленькие моторы
Рассмотрите заглавную иллюстрацию статьи. Там есть ракета, подводная лодка, змея и микроробот. Что-нибудь заметили схожее? Несмотря на множество отличий, включая размер, строение и происхождение, их всех объединяет способность к движению. Основа этого процесса — преобразование химических веществ или внешнего источника энергии в движение [1].
Для продолжения нашего путешествия важно понимать, что такое «микро», а что — «нано»? В микро-диапазон входят все объекты, имеющие размер от 100 мкм до 100 нм. Приставка «нано-» используется для объектов размером от 1 до 100 нм (рис. 1).
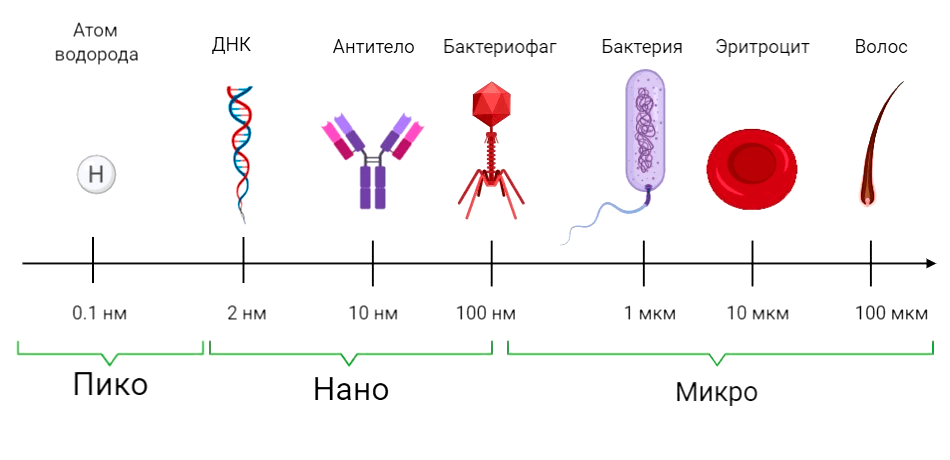
Рисунок 1. Шкала микро-, нано- и пикоразмерных объектов
рисунок автора статьи
В статье мы часто будем использовать слова «микромоторы» и «микро-/нанороботы». Они имеют похожий, но не одинаковый смысл, поэтому давайте познакомимся с ними поближе.
- Микромоторы (микроактуаторы)
- это автономные устройства или частицы, способные преобразовывать разные виды энергии в движение.
- Микро-/нанороботы (микро-/наноботы)
- это управляемые устройства, способные не только двигаться, но и выполнять определенные виды задач. Например, связывать токсические вещества или контролируемо доставлять лекарства или гены в определенную область тела.
В начале мы сказали, что главная особенность всех микромоторов — это превращение одного вида энергии в движение. Но до 2002 года никто не использовал этот подход, пока группа химика Джорджа Уайтсайдса не решила применить его для создания подвижного автономного микроактуатора [2]. Устройство имело полуцилиндрическую форму с маленькой платиновой областью (рис. 2а). Как только оно помещалось в воду, смешанную с перекисью водорода, последняя начинала разлагаться под действием платины. При этом выделялись пузырьки кислорода, которые толкали микромотор вперед. Стоит заметить, что ученых не сильно интересовали параметры движения моторов — их главной целью было наблюдение за поведением таких частиц.
Сегодня известно несколько способов движения микро-/наноботов в различных средах (рис. 2). Самый распространенный из них — химический двигатель, который описан в опытах Уайтсайдса. Он использует энергию химических реакций на поверхности устройства для создания пузырьков газа [3] или градиента концентраций, способствующего движению за счет направленной диффузии [4]. Другой любопытный и древний тип двигателей — биологический. Он работает за счет вращения жгутиков вокруг своей оси [5]. Еще один — физический, например, с применением магнитного поля (рис. 2) для перемещения микророботов, что очень напоминает движения бактерий с помощью жгутиков [6].
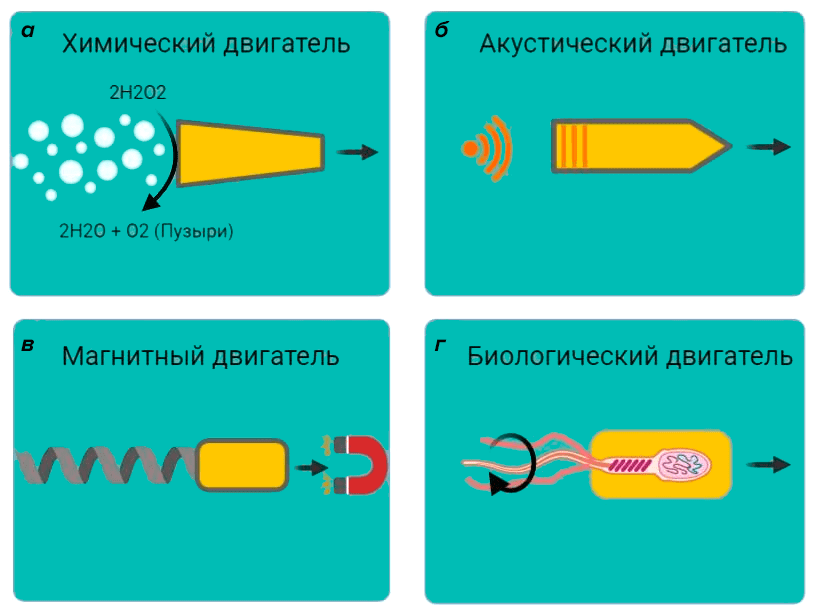
Рисунок 2. Механизмы работы разных микромоторов. а — Химический двигатель основан на каталитическом разложении перекиси водорода на платиновой поверхности. Это вызывает образование пузырей кислорода, двигающих микроробота (есть и другие виды реакций, о которых поговорим далее). б — Акустический мотор, работа которого вызывается ультразвуком, заставляющим микробота часто колебаться вокруг своей оси и тем самым продвигаться в определенном направлении [7]. в — Движение за счет магнитного поля и ферромагнетика (сильно намагничивающегося вещества: никеля, кобальта или железа). г — Биологический мотор основан на вращении (у бактерий) или биении жгутиков (у сперматозоидов) [8] за счет работы другого молекулярного двигателя — АТФ-синтазы [9].
рисунок автора статьи
Другая очень важная особенность всех микро-/наномоторов — способность к функционализации, то есть к изменению поверхности устройства с приобретением способности к выполнению каких-то задач. Например, на наноботе можно закрепить рецепторы или короткий ДНК фрагмент для обнаружения молекул, или связать нанобота с лекарством [10].
Сочетание маленького размера, управляемости, подвижности и возможности приобретения новых свойств делает их перспективным инструментом для решения многих задач. Поэтому ученые вооружаются этими технологиями для преодоления глобальных вызовов в медицине, фармакологии и экологии (рис. 3). На тему разнообразия нанороботов на «Биомолекуле» опубликован прекрасный обзор [11], а здесь мы поговорим исключительно об инновационных применениях этих созданий.
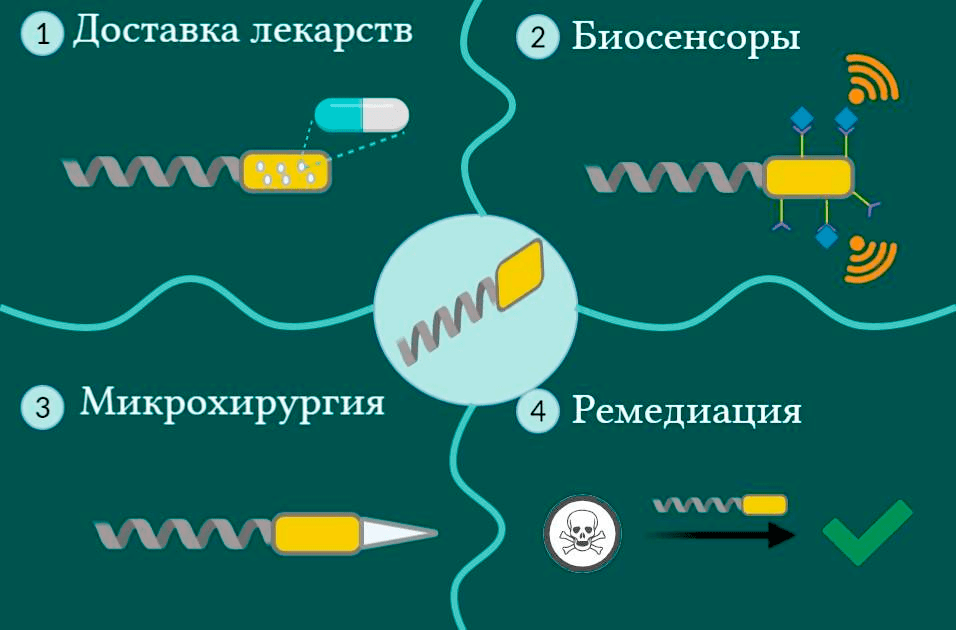
Рисунок 3. Области применения синтетических микро-/наномашин. Исследователи тестируют эти устройства в медицине для доставки лекарств (1) [12], генов, вакцин и в качестве биосенсоров (для диагностики заболеваний) (2). Также они применяются в микрохирургии (3) для удаления патологических тканей или взятия их образцов и для удаления токсических веществ из воды (ремедиации) (4).
рисунок автора статьи
Часть 2. Применение в медицине
Доставка лекарств
Вакцинация как способ стимулирования иммунной системы от опасных инфекций имеет большое значение в мире. По оценкам ВОЗ, иммунизация спасает до 2–3 миллионов жизней в год [13]. Обычно ее проводят внутримышечно. Недостаток этого способа в том, что остается много загрязненных шприцов и игл. Они представляют угрозу для пациентов, медицинских работников и окружающей среды, так как могут содержать ВИЧ, вирус гепатита В или другие источники инфекции. Для решения этой проблемы создали другие способы, например, оральную вакцину (вводимую через рот). Она безопасна в плане инфекции и ее использование не требует особых медицинских знаний и инъекций большими иглами, но эффективность низкая [14]. Чтобы исправить этот недостаток, ученые из Университета Сан-Диего разработали микроробота, который принимался оральным способом в виде раствора, достигал тонкого кишечника и доставлял антигены к слизистой оболочке [15]. Они показали принцип работы на примере вакцинации от бактерии Staphylococcus aureus.
Для реализации своей идеи исследователи использовали работу каталитически движимого мотора. Главный принцип всех химических двигателей — поверхностные реакции с образованием пузырьков газа или разности концентраций, необходимых для движения системы (рис. 2а). В нашем случае использовалась реакция магния с водой с образованием водорода (H2). В эксперименте после проглатывания воды с микроботами, происходило их пассивное (без движения) прохождение через желудок и активация в тонком кишечнике. Там они быстро начинали двигаться и встраиваться в слизистую оболочку.
Чтобы создать свой микромотор, ученые применили технику послойного нанесения покрытий. В начале они использовали микрочастицы магния, на которые накладывали слой диоксида титана. Он служил каркасом всей конструкции, поддерживая ее форму. Затем наносили слой оболочек эритроцитов со встроенными антигенами. Он играл роль контейнера, в котором происходила не только загрузка, но и нейтрализация антигена [16]. Ключевой частью конструкции была оболочка из хитозана, которая помогала роботу «прилипнуть» к стенкам кишечника и выгрузить антиген [17]. Такое встраивание в слизистую обеспечивало усиленную стимуляцию иммунной системы. Последним покрытием был слой pH-чувствительного полимера. Именно он защищал всю систему от кислотных условий желудка (рис. 4) [18].
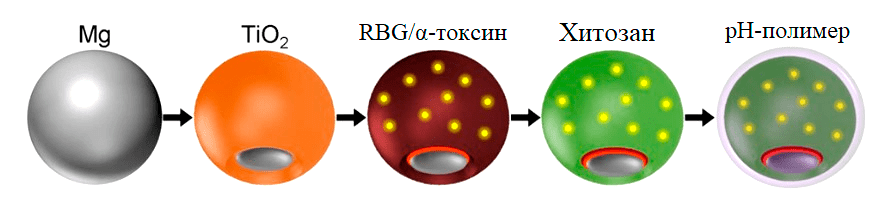
Рисунок 4. Принцип создания микромотора. Основа двигателя — это магниевые микрочастицы размером 20 мкм. На них ассиметрично наносится слой диоксида титана, оставляя маленькую открытую область магния, которая и будет мотором. Затем наносится мембрана эритроцитов (red blood cell membrane) со встроенным в неё α-токсином. Следующими слоями располагали хитозан для мукоадгезии и метакрилатный pH-полимер для защиты от низких pH. Заметьте, что только pH-оболочка покрывает сферу полностью.
Чтобы доказать возможность использования системы в клинических условиях, ученые испытали ее в желудочно-кишечном тракте мышей (рис. 5). Для этого им орально ввели микроробота с вакциной. Спустя 6 часов оценили эффективность. Результаты показали, что такая система эффективно накапливается в кишечнике и способствует усиленной выработке антител (рис. 6).
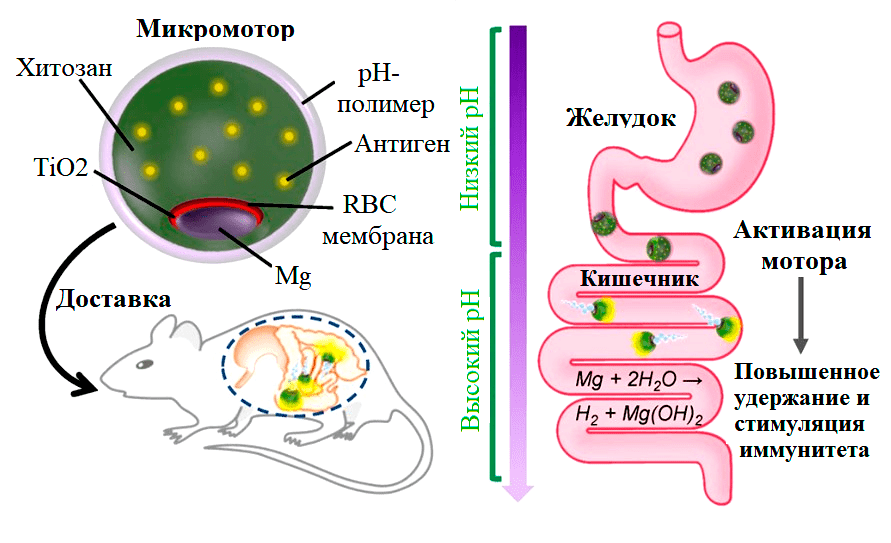
Рисунок 5. Схематический принцип работы микромотора, созданного в Университете Сан-Диего. После перорального введения микросфер, они проходят по пищеводу и достигают желудка. При этом в кислых условиях (pH 2–5) pH-полимер защищает содержимое капсул. При попадании же в кишечник оболочка депротонируется и растворяется в течение 20 минут, открывая магниевую область. Затем происходит реакция с образованием водорода, и робот с антигенами начинает автономно двигаться и плотно встраиваться в стенки кишечника (видео 1). Слизистая кишечника — самый большой лимфатический орган тела. Именно через нее происходит взаимодействие антигенов и иммунных клеток, вызывающее выработку антител (IgA) [19]. В результате стимулируется иммунитет.
[15], рисунок с модификациями
Видео 1. Сравнение движения микроактуатора в желудке и кишечнике

Рисунок 6. Результаты тестирования микромотора. Для облегчения наблюдения микросферы пометили флуоресцентным красителем. Контрольная группа имела неподвижный мотор, полностью покрытый диоксидом титана (TiO2). Устройства растворили в воде и ввели голодным крысам. По окончании эксперимента сигнал флуоресценции двигающихся частиц в кишечнике был в 4 раза выше контрольных, что показывает высокую эффективность встраивания подвижного микроробота в стенки кишечника.
[15], рисунок адаптирован
В будущем можно будет расширить применение микроботов, доставляющих различные грузы: генные конструкции, лекарства или факторы роста для восстановления тканей. Возможно, такие системы будут главными доставщиками всего, что только можно, в наш организм. Правда, сначала ученым придется повысить контролируемость конструкций и поработать над размером для их более эффективного использования.
Биосенсоры
Сейчас наиболее точным и распространенным типом биосенсоров становятся микроРНК — короткие (18–25 нуклеотидов) одноцепочечные некодирующие РНК. Экспрессия этих важных молекул обнаружена у животных, растений и некоторых вирусов. Они участвуют в делении и дифференцировке клеток [20]. Высокая активация определенных микроРНК может быть связана с заболеваниями, начиная от рака и заканчивая диабетом. Поэтому их можно использовать как маркер (признак) в диагностике болезней [21].
Разработано много методов детекции (обнаружения) микроРНК, включая нозерн-блоттинг [22], количественную ПЦР [23], микроматрицы [24] и другое. Но здесь есть проблема: только малая часть из них может анализировать образцы в реальном времени в плазме крови или в неповрежденных клетках [25]. Вдобавок они требуют долгого времени инкубации (около 14 часов при температуре 37 °C), высокую плотность клеток (в среднем 60 тыс.) и имеют высокий порог чувствительности. Интересно, но и здесь нанороботам есть что предложить. Они умеют не только находить следы болезней в популяции живых клеток, но и, как недавно впервые было показано, даже в одной единственной клетке!
Исследователи из Университета Алькалы-де-Энарес и Университета Сан-Диего создали подвижный биосенсор для обнаружения раковых клеток [26]. Для этого они использовали золотые нанопроволоки, покрытые оксидом графена. В качестве сенсора ученые взяли одноцепочечную ДНК (оцДНК) с флуоресцентной меткой, которая была комплементарна микроРНК-21 — некодирующей РНК, синтезируемой на высоком уровне в 80% типов опухолей и служащей отличным маркером онкологических заболеваний [27]. Эту оцДНК с флуорофором связали с наномотором. Для управления таким устройством группа воспользовалась ультразвуком с постоянной частотой (рис. 2б). Ученые показали, что подвижный биосенсор способен не только быстро определять наличие раковых клеток при комнатной температуре, но и делать это с очень высокой чувствительностью (рис. 7). К слову, он превосходит один из наиболее признанных методов для детекции микроРНК — ПЦР с обратной транскрипцией (ОТ-ПЦР).
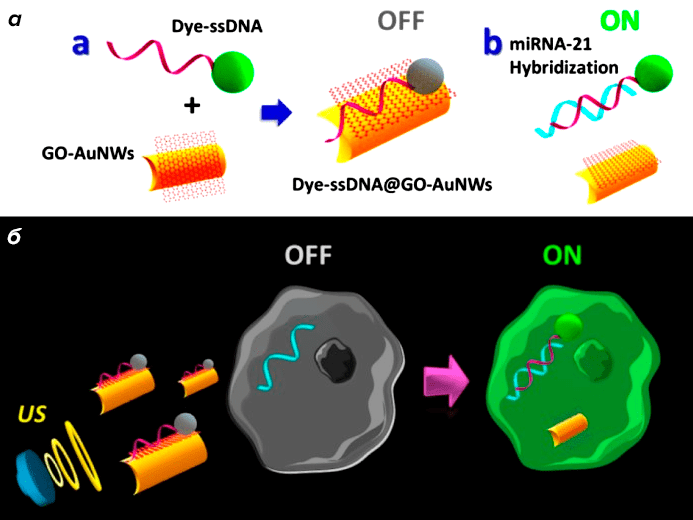
Рисунок 7. Механизм действия биосенсора для обнаружения некоторых типов рака. а — На золотые нанопроволоки, покрытые оксидом графена, иммобилизованы зонды (одноцепочечные ДНК с флуорофором). При этом флуоресценция метки гасится слоем графена. б — Сам наномотор быстро движется и проникает внутрь клетки под действием ультразвука (видео 2). Попадая в раковые клетки, зонды комплементарно связываются со специфическими мишенями микроРНК и освобождаются от графена. В результате этого клетки начинают светиться.
Видео 2. Этапы проникновения наномотора в раковые клетки молочной железы (MCF-7). Для движения нановолокон использовали ультразвук с частотой 2,66 МГц и напряжением 6 В для детекции флуоресцентного сигнала.
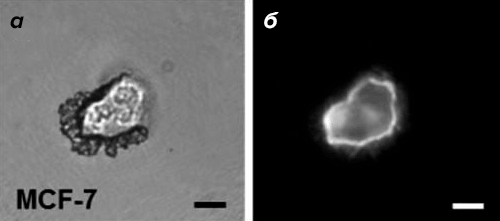
Рисунок 8. Определение микроРНК-21 в единичной клетке MCF-7. Фотографии с оптического (а) и электронного (б) микроскопов раковой клетки после 10 минут инкубации с нанороботом в ультразвуковом поле (частота 2,66 МГц и напряжение 6 В). Яркое свечение клетки показывает гиперпроизводство РНК-мишеней.
Благодаря такой технологии интенсивность флуоресценции увеличивается пропорционально концентрации микроРНК-21, что позволяет устройству определять опасные клетки. Однако появилась проблема: в раковых клетках шейки матки (HeLa) внутриклеточная концентрация РНК-мишени в 44 раза меньше, чем в клетках MCF-7 [28]. Ранее ни один из других методов не мог обнаружить такое низкое содержание микроРНК-21 в единичной клетке.
Но исследователи сумели справиться и с этой задачей, повысив интенсивность флуоресценции в несколько раз (рис. 8). Чтобы добиться такого результата, они увеличили скорость движения наномашины для большей вероятности связывания оцДНК и микроРНК.
Микророботы для персонализированной медицины
Микромоторы в организме человека работают как хорошо управляемые машины. Они контролируемо двигаются в желудке, кровотоке, проникают в труднодоступные ткани, например, в тромбы или опухолевое окружение. Способны ли они выполнять еще какие-либо действия?
Исследователи уже давно заинтересовались этим вопросом: они думают, что микро-/нанороботы помогут нам продлить жизнь с помощью эффективной и безопасной медицины. Поэтому одна из важнейших целей в области микроробототехники — создание интегрированных функциональных систем для выполнения безболезненных и точных операций на пациентах. Для этого биоинженерам потребуются не только автономные доставщики лекарств, но и имплантируемые управляемые роботы маленького размера.
Сейчас одной из самых проблемных и сложных областей медицины является офтальмология. C 1990 по 2020 годы число людей с полной слепотой увеличилось более чем на 30% и эта цифра продолжает расти [29], [30]. Патологии сетчатки — основная причина потери зрения у взрослых. В хирургии для борьбы с такими заболеваниями используют внутриглазные инъекции и лазеры, которые довольно болезненны, неэффективны и приводят ко множеству осложнений [31], [32]. Поэтому сейчас развиваются новые и более безопасные способы глазных операций с помощью управляемых микроботов.

Рисунок 9. Внешний вид трубчатого магнитного микроробота. Корпус с наконечником сделан из кобальт-никелевого сплава и нержавеющей стали. Размер устройства 350 мкм × 3,4 мм.
Биоинженеры из Технической школы Цюриха решили сконструировать магнитного имплантируемого микроробота для лечения сетчатки (рис. 9) [33]. Работы, опубликованные ранее, уже показывали эффективность подобных устройств, но они были высокоиммуногенные, и для их введения требовалась хирургия [34]. Поэтому ученые поменяли дизайн устройства: они нашли наиболее биосовместимый магнитный сплав с самой высокой намагниченностью — кобальт-никелевый (Co–Ni). Затем создали из него полые трубки с острым наконечником и загрузили его лекарством. То, как происходило введение микробота, хорошо показано на видео 3. Подробнее с экспериментом можно познакомиться на рисунке 10.
Видео 3. Введение лекарства в капилляр сетчатки микроботом, созданным в Технической школе Цюриха
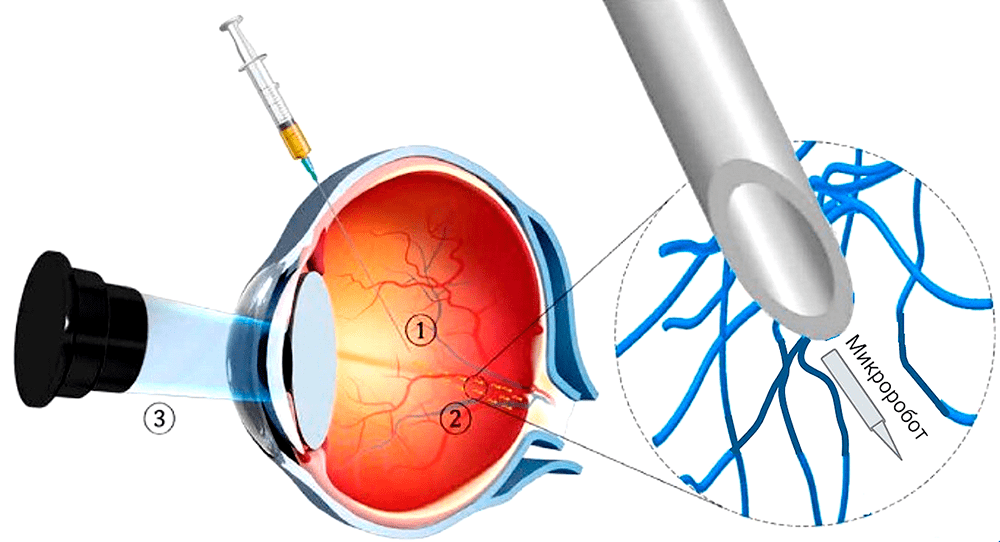
Рисунок 10. Схема эксперимента по адресной доставке лекарств с использованием магнитного микроробота. С помощью инъекции его ввели в центр стекловидного тела глаза иглой диаметром 0,6 мм (1). После этого навели магнитное поле, за счет которого микробот двигался к сетчатке (2). После доставки лекарств он извлекался с помощью этой же иглы и в определенной ориентации под действием магнитного поля [35]. Наблюдения проводили офтальмоскопом со встроенной камерой (3).
Для подтверждения эффективности и применимости устройства, исследователи протестировали его на кролике (рис. 11). Для этого животному сделали инъекцию микроробота в центр глаза. Сначала ученые проверили маневренность устройства в стекловидном теле. Затем они исследовали точность адресной доставки и высвобождения лекарства. Ученые продемонстрировали высокую управляемость устройства и постепенное высвобождение лекарства, что позволяет использовать их разработку в качестве прототипа настоящего устройства для лечения разных патологий глаза у человека.
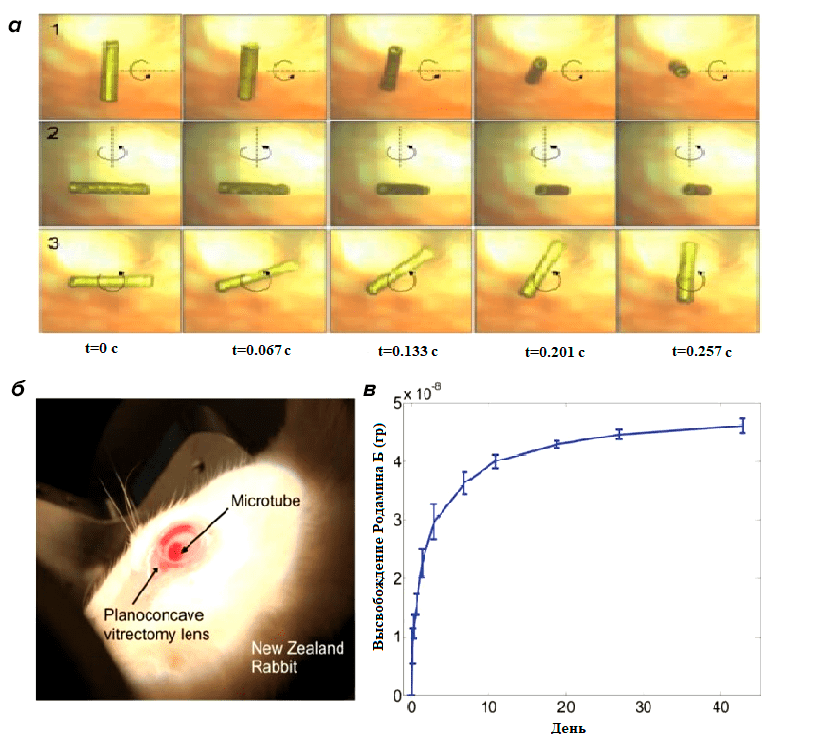
Рисунок 11. Тестирование устройства для доставки лекарств внутрь глаза. а — Микроробот очень точно и быстро выполняет движения вокруг трех осей, несмотря на высокую вязкость стекловидного тела глаза. б — Имплантация микробота внутрь глазного яблока анастезированного животного. в — Измерения скорости выхода лекарства. В качестве модельного препарата использовали краситель родамин B, который вводили в сетчатку. Вещество медленно высвобождается в течение 42 дней, что доказывает эффективность и высокую маневренность устройства.
Часть 3. Применение в экологии
Окружающая среда: сбор и транспортировка загрязнений
Сейчас одной из главных причин загрязнения океана и грунтовых вод является нефть. Она появляется там по нескольким причинам: это и утечка на шахтах, и проблемы во время транспортировки, и мытье нефтетанкеров. Например, в результате инцидентов с Exxon Valdez в 1989 году [37] и Deepwater Horizon в 2010 году [38] разлилось более двух миллионов тонн сырой нефти. Другая крупнейшая авария в России произошла 29 мая 2020 года в Норильске. Там разлилось более 20 тысяч тонн дизеля, которые до сих пор не могут ликвидировать [39]. Чтобы уменьшить разрушающее воздействие на природу, необходимо разрабатывать методы удаления нефти и нефтепродуктов из воды. Основной из них, механическая очистка, довольно дорогостоящий и малоселективный способ [40]. Но что здесь могут предложить микроботы?
Многие опасные вещества могут быть захвачены, перенесены и нейтрализованы с помощью микророботов. Они способны эффективно выполнять все эти функции за счет быстрой скорости и особых поверхностей для связывания токсинов. Для движения им обычно необходим источник топлива, который присутствует в небольших концентрациях в среде (например, перекись водорода) [41]. Используя эти знания, ученые нашли отличное применение микроботам.
В 2012 году группа биоинженеров из Каталонского института нанонауки и нанотехнологий (ICN2) создала устройство для быстрого сбора и утилизации нефти в водоемах [42]. Они задействовали самодвижущиеся свойства микромоторов: как уже говорилось, микророботы способны быстро перемещаться с помощью химического двигателя на основе платины. При взаимодействии c платиной перекись водорода разлагается с выделением пузырьков кислорода, толкающих устройство вперед. Ученые частично покрыли платиновый мотор слоем никеля для магнитного управления и нанесли на него частички золота, а затем — последний элемент — супергидрофобное покрытие, которое связывалось с золотом и способствовало прочному захвату капель нефти (рис. 12 и видео 4).
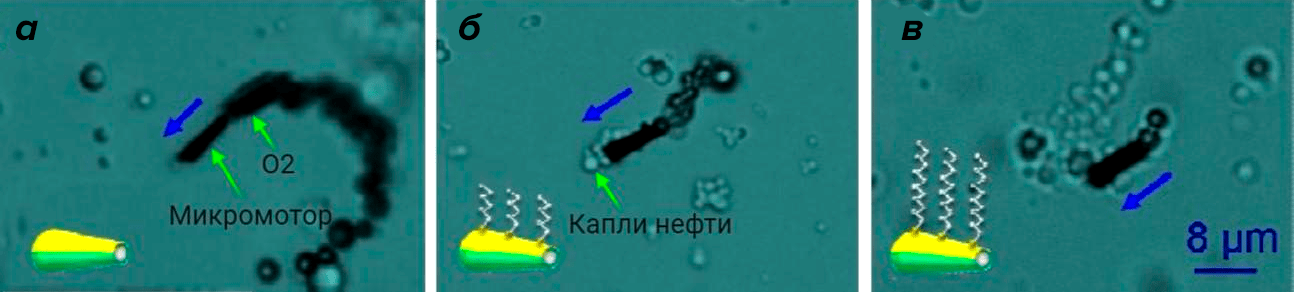
Рисунок 12. Тестирование поверхностных веществ для захвата капель масла. Немодифицированные микроботы (а), модифицированные «серными спиртами»: гексантиолом (б) (с шестью атомами углерода) и додекантиолом (в) (с двенадцатью атомами углерода). Последние показали наибольшую способность к связыванию, захватывая до сорока пяти мелких капель. Микромоторы имели мощную тягу, перемещая грузы, в десять раз превышающие их собственный объем.
Видео 4. По строению микроробот имеет трубчатую форму размером 8×1 мкм. Он способен двигаться со скоростью до 100 мкм/с даже в среде с очень низким уровнем топлива (0,2% H2O2). Но при увеличении количества захваченных капель скорость сильно снижается, так как платиновый двигатель перекрывается каплями масла и блокируется [43].
Ученым оставалось определить, какое из высокогидрофобных веществ будет наиболее эффективным. Они протестировали три главных кандидата и определили, что додекантиолы («серные спирты» с двенадцатью атомами углерода) наиболее сильно связывали и удерживали капли масла (рис. 12). В будущем инженеры собираются испытывать эти устройства для очистки водоемов от производственных отходов лекарств [44] и моторных масел. Также они хотят улучшать микроробота, чтобы не только собирать, но и разрушать вредные вещества прямо на месте.
Ремедиация водоемов от тяжелых металлов
Помимо загрязнения окружающей среды нефтепродуктами, есть более глобальная проблема. Она связана с увеличением объемов производства и попаданием тяжелых металлов в почву и, особенно, водоемы. Даже несмотря на введение ограничительных мер по выбросу таких веществ, концентрация большинства из них увеличивается. Так, содержание кадмия, никеля и хрома в атмосфере в 2012 году по сравнению с 1941 годом выросло в 10, 13 и 16 раз соответственно [45].
Опасность же тяжелых металлов для человека и животных заключается в том, что при попадании в организм они стимулируют производство активных форм кислорода в клетках и вызывают окислительный стресс. Последний приводит к повреждению структуры белков и ДНК, нарушая их работу и вызывая гибель клеток [46]. Поэтому очень важно иметь дешевые и простые способы утилизации этих загрязнителей.
Сейчас существует много технологий для удаления и переработки тяжелых металлов из жидкости: мембранная фильтрация, адсорбция, ионообменное выделение и другие. Однако все они дорогостоящие и малоэффективные [47]. Чтобы предложить метод, лишенный этих недостатков, ученые обращаются за помощью к новым наноматериалам и нашим мини-двигателям.
Так, исследователи из Института интеллектуальных систем Макса Планка в своей статье предложили использовать графенового микроробота для сбора и удаления тяжелых металлов из водоемов [48]. Чтобы быстро и качественно захватывать химические вещества, нужна как скорость, так и высокая степень связывания. В этом и была основная идея ученых: они совместили подвижность микробота и высокую связывающую способность оксида графена (видео 5) [49]. В качестве целевого тяжелого металла выбрали Pb2+ (ионы свинца), так как они являются весьма распространенным отходом. Особенностью этого устройства стало не только умение собирать и утилизировать опасные вещества, но и возможность его повторного использования (рис. 13).
Видео 5. Магнитное управление микророботом для сбора Pb2+. Тесты проводили в микрофлюидных каналах с водой, загрязненной тяжелым металлом. Устройство сохраняло подвижность более часа. Скорость менялась от 500 мкм/с до 50 мкм/с в зависимости от концентрации топлива в среде (изначально 1,5% перекиси водорода).
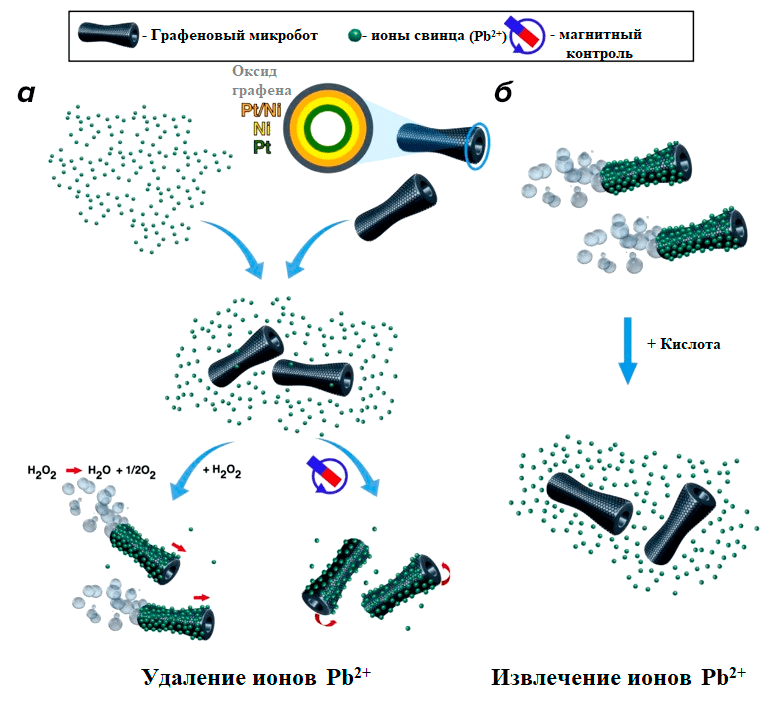
Рисунок 13. Использование графенового микробота для сбора и извлечения ионов свинца. а — Строение и принцип действия микроробота. Внутренний слой платины (Pt) использовался для движения, средней пласт никеля (Ni) для магнитного управления, а внешняя многослойная поверхность оксида графена — для адсорбции Pb2+. После попадания в загрязненную среду микробот активно удерживал на себе тяжелый металл и доставлял его в нужное место. б — Устройство очищается от ионов свинца с помощью азотной кислоты (HNO3) со стопроцентным выходом. Микробот же остается полностью рабочим, поэтому способен к многоразовому использованию.
Чтобы доказать эффективность своего устройства, ученые сравнили два типа микроботов по способности удалять ионы свинца: подвижный и неподвижный. Результаты показали, что те, которые активно перемещались, были в 10 раз эффективней пассивных микророботов. Еще исследователи измерили точную концентрацию тяжелых металлов, удаленных подвижными микроботами. Оказалось, что за час они уменьшили количество токсинов в 20 раз и собрали до 95% всех ионов свинца.
Эксперименты ученых доказали, что микромоторы способны эффективно удалять токсичные ионы свинца из водоемов, а также повторно использоваться после очистки от них. Еще одна хорошая новость по этому исследованию, что такая система с графеновыми слоями — универсальна. Кроме связывания Pb2+ оксид графена может удалять и другие металлы, например, кадмий, ртуть, арсенит [50], и пестициды [51]. Не исключено, что такие устройства смогут в будущем очищать наше тело от разных токсинов или применяться для добычи драгоценных металлов, таких как золото, платина или палладий [52]. В дальнейшем ученые хотят придумать автономную программу для управления микроботами прямо в водоеме за счет магнитного поля. Но пока у разработки есть большое ограничение: низкая скорость из-за малой концентрации топлива в среде (примерно 0,008% H2O2 на поверхности морей) [53]. Для решения этой проблемы авторы хотят использовать бестопливные моторы (акустические, световые), способные двигаться под действием внешних стимулов.
Выводы, проблемы и перспективы
Пока мы только начинаем знакомиться с удивительными жителями наномира и их возможностями. Достижения последних десятилетий — это только первые шаги в нашем длинном нанопутешествии. Постепенно ученые пытаются создавать и «одомашнивать» микро-/наноботов, чтобы использовать их во благо человечества. Шаг за шагом эти устройства делают революцию в медицине: они выполняют микрохирургические операции с высокой точностью, проводят быструю и дешевую диагностику заболеваний на клеточном и молекулярном уровнях и эффективно доставляют лекарства в труднодоступные области организма (например, в опухоли или печень [54]). Также они помогают решать глобальные экологические проблемы: от мониторинга и обнаружения загрязнений до транспорта и ликвидации загрязнителей.
В будущем микро-/наномоторы будут совершенствоваться по природным принципам. Биологические наномашины, такие как рибосома или кинезины (белки, «шагающие» по микротрубочкам), имеют все характеристики идеального робота: высокая скорость, биосовместимость и способность к биоразложению после выполнения своих функций. Но, чтобы достигнуть Святого Грааля природы, нужно преодолеть трудности сегодняшнего дня. Очень малое до сих пор было придумано относительно возможностей бестопливных способов движения, а также новых видов моторов, таких как ферментативный или биогибридный. Нам также нужно больше исследований и разработок для отслеживания микро-/наноботов и повышения их управляемости внутри организма. Победа над этими проблемами откроет нам новые горизонты не только в наномедицине и экологии, но и в понимании всего нашего мира.
Благодарности
В редактировании и улучшении статьи мне сильно помогли мои друзья и знакомые. Я хочу сказать большое спасибо этим людям:
Вдобавок выражаю большую благодарность главному и выпускающему редакторам этой работы: Надежде Потаповой и Андрею Панову!
Без всех вас эта небольшая история о микро- и наногероях не была бы такой, какая она есть. В написании работы мне также очень пригодились советы от Nature и Кормака Маккарти [55], [56]
Я буду очень рад, если у меня будет возможность поблагодарить их!
Литература
- Wei Gao, Xiaomiao Feng, Allen Pei, Christopher R. Kane, Ryan Tam, et. al.. (2014). Bioinspired Helical Microswimmers Based on Vascular Plants. Nano Lett.. 14, 305-310;
- Rustem F. Ismagilov, Alexander Schwartz, Ned Bowden, George M. Whitesides. (2002). Autonomous Movement and Self-Assembly. Angew. Chem. Int. Ed.. 41, 652-654;
- Jinxing Li, Isaac Rozen, Joseph Wang. (2016). Rocket Science at the Nanoscale. ACS Nano. 10, 5619-5634;
- Wei Wang, Wentao Duan, Suzanne Ahmed, Thomas E. Mallouk, Ayusman Sen. (2013). Small power: Autonomous nano- and micromotors propelled by self-generated gradients. Nano Today. 8, 531-554;
- Veronika Magdanz, Mariana Medina-Sánchez, Yan Chen, Maria Guix, Oliver G. Schmidt. (2015). How to Improve Spermbot Performance. Adv. Funct. Mater.. 25, 2763-2770;
- Bradley J. Nelson, Ioannis K. Kaliakatsos, Jake J. Abbott. (2010). Microrobots for Minimally Invasive Medicine. Annu. Rev. Biomed. Eng.. 12, 55-85;
- Loai K. E. A. Abdelmohsen, Fei Peng, Yingfeng Tu, Daniela A. Wilson. (2014). Micro- and nano-motors for biomedical applications. J. Mater. Chem. B. 2, 2395-2408;
- S. A. Rudneva, V. B. Сhernykh. (2018). A mechanism of sperm cilia beating. Androl. genit. hir.. 19, 15-26;
- Фотосинтез в образах;
- Maria Guix, Carmen C. Mayorga-Martinez, Arben Merkoçi. (2014). Nano/Micromotors in (Bio)chemical Science Applications. Chem. Rev.. 114, 6285-6322;
- «Врачи-нанороботы» — миф или реальность?;
- Наночастицы — инструмент адресной доставки лекарств;
- Immunization. WHO;
- Myron M Levine. (2010). Immunogenicity and efficacy of oral vaccines in developing countries: lessons from a live cholera vaccine. BMC Biol. 8;
- Xiaoli Wei, Mara Beltrán-Gastélum, Emil Karshalev, Berta Esteban-Fernández de Ávila, Jiarong Zhou, et. al.. (2019). Biomimetic Micromotor Enables Active Delivery of Antigens for Oral Vaccination. Nano Lett.. 19, 1914-1921;
- Ronnie H. Fang, Brian T. Luk, Che-Ming J. Hu, Liangfang Zhang. (2015). Engineered nanoparticles mimicking cell membranes for toxin neutralization. Advanced Drug Delivery Reviews. 90, 69-80;
- Shu-jun Cao, Shuo Xu, Hui-ming Wang, Yong Ling, Jiahua Dong, et. al.. (2019). Nanoparticles: Oral Delivery for Protein and Peptide Drugs. AAPS PharmSciTech. 20;
- Wei Gao, Renfeng Dong, Soracha Thamphiwatana, Jinxing Li, Weiwei Gao, et. al.. (2015). Artificial Micromotors in the Mouse’s Stomach: A Step toward in Vivo Use of Synthetic Motors. ACS Nano. 9, 117-123;
- Aayam Lamichhane, Tatsuhiko Azegami, Hiroshi Kiyono. (2014). The mucosal immune system for vaccine development. Vaccine. 32, 6711-6723;
- Haifeng Dong, Jianping Lei, Lin Ding, Yongqiang Wen, Huangxian Ju, Xueji Zhang. (2013). MicroRNA: Function, Detection, and Bioanalysis. Chem. Rev.. 113, 6207-6233;
- Soo-Ryoon Ryoo, Jieon Lee, Jinah Yeo, Hee-Kyung Na, Young-Kwan Kim, et. al.. (2013). Quantitative and Multiplexed MicroRNA Sensing in Living Cells Based on Peptide Nucleic Acid and Nano Graphene Oxide (PANGO). ACS Nano. 7, 5882-5891;
- G. S. Pall, C. Codony-Servat, J. Byrne, L. Ritchie, A. Hamilton. (2007). Carbodiimide-mediated cross-linking of RNA to nylon membranes improves the detection of siRNA, miRNA and piRNA by northern blot. Nucleic Acids Research. 35, e60-e60;
- Juan Li, Bo Yao, Huang Huang, Zhao Wang, Changhong Sun, et. al.. (2009). Real-Time Polymerase Chain Reaction MicroRNA Detection Based on Enzymatic Stem-Loop Probes Ligation. Anal. Chem.. 81, 5446-5451;
- Peter T Nelson, Don A Baldwin, L Marie Scearce, J Carl Oberholtzer, John W Tobias, Zissimos Mourelatos. (2004). Microarray-based, high-throughput gene expression profiling of microRNAs. Nat Methods. 1, 155-161;
- Yafeng Wu, Jianyu Han, Peng Xue, Rong Xu, Yuejun Kang. (2015). Nano metal–organic framework (NMOF)-based strategies for multiplexed microRNA detection in solution and living cancer cells. Nanoscale. 7, 1753-1759;
- Berta Esteban-Fernández de Ávila, Aída Martín, Fernando Soto, Miguel Angel Lopez-Ramirez, Susana Campuzano, et. al.. (2015). Single Cell Real-Time miRNAs Sensing Based on Nanomotors. ACS Nano. 9, 6756-6764;
- Cuiyun Yang, Baoting Dou, Kai Shi, Yaqin Chai, Yun Xiang, Ruo Yuan. (2014). Multiplexed and Amplified Electronic Sensor for the Detection of MicroRNAs from Cancer Cells. Anal. Chem.. 86, 11913-11918;
- Shozo Honda, Yohei Kirino. (2015). Dumbbell-PCR: a method to quantify specific small RNA variants with a single nucleotide resolution at terminal sequences. Nucleic Acids Res. 43, e77-e77;
- Global trends in the magnitude of blindness and visual impairment. WHO;
- Global vision impairment facts. (2020). The International Agency for the Prevention of Blindness;
- Schmidt-Erfurth U.M., Richard G., Augustin A., Aylward W.G., Bandello F., Corcòstegui B. et al. (2007). Guidance for the treatment of neovascular age-related macular degeneration. Acta ophthalmologica Scandinavica. 85, 486–494;
- Alfred Sommer, Hugh R. Taylor, Thulasiraj D. Ravilla, Sheila West, Thomas M. Lietman, et. al.. (2014). Challenges of Ophthalmic Care in the Developing World. JAMA Ophthalmol. 132, 640;
- Vikram S. Brar, Mariam Nasir, Dev R. Sahni, Jessica Randolph, Natario L. Couser. (2019). Genetic Abnormalities of the Retina and Choroid. Ophthalmic Genetic Diseases. 137-162;
- E Lavik, M H Kuehn, Y H Kwon. (2011). Novel drug delivery systems for glaucoma. Eye. 25, 578-586;
- Franziska Ullrich, Christos Bergeles, Juho Pokki, Olgac Ergeneman, Sandro Erni, et. al.. (2013). Mobility Experiments With Microrobots for Minimally Invasive Intraocular Surgery. Invest. Ophthalmol. Vis. Sci.. 54, 2853;
- Zhiguang Wu, Jonas Troll, Hyeon-Ho Jeong, Qiang Wei, Marius Stang, et. al.. (2018). A swarm of slippery micropropellers penetrates the vitreous body of the eye. Sci. Adv.. 4, eaat4388;
- Subhasis Biswas, Sanjeev K Chaudhari, Suparna Mukherji. (2005). Microbial uptake of diesel oil sorbed on soil and oil spill clean-up sorbents. J. Chem. Technol. Biotechnol.. 80, 587-593;
- G. E. Machlis, M. K. McNutt. (2010). Scenario-Building for the Deepwater Horizon Oil Spill. Science. 329, 1018-1019;
- Слащева М. (2020). «Черный яд». Как разливы нефти убивают окружающую среду. «Нож»;
- Qing Zhu, Qinmin Pan, Fatang Liu. (2011). Facile Removal and Collection of Oils from Water Surfaces through Superhydrophobic and Superoleophilic Sponges. J. Phys. Chem. C. 115, 17464-17470;
- Wei Gao, Sirilak Sattayasamitsathit, Aysegul Uygun, Allen Pei, Adam Ponedal, Joseph Wang. (2012). Polymer-based tubular microbots: role of composition and preparation. Nanoscale. 4, 2447;
- Maria Guix, Jahir Orozco, Miguel García, Wei Gao, Sirilak Sattayasamitsathit, et. al.. (2012). Superhydrophobic Alkanethiol-Coated Microsubmarines for Effective Removal of Oil. ACS Nano. 6, 4445-4451;
- C. Vericat, M. E. Vela, G. Corthey, E. Pensa, E. Cortés, et. al.. (2014). Self-assembled monolayers of thiolates on metals: a review article on sulfur-metal chemistry and surface structures. RSC Adv.. 4, 27730-27754;
- Jerker Fick, Hanna Söderström, Richard H. Lindberg, Chau Phan, Mats Tysklind, D.G. Joakim Larsson. (2009). CONTAMINATION OF SURFACE, GROUND, AND DRINKING WATER FROM PHARMACEUTICAL PRODUCTION. Environ Toxicol Chem. 28, 2522;
- J.A. Rodríguez Martín, C. De Arana, J.J. Ramos-Miras, C. Gil, R. Boluda. (2015). Impact of 70 years urban growth associated with heavy metal pollution. Environmental Pollution. 196, 156-163;
- Neeti Sharma. (2014). Free Radicals, Antioxidants and Disease. Biol Med (Aligarh). 06;
- Fenglian Fu, Qi Wang. (2011). Removal of heavy metal ions from wastewaters: A review. Journal of Environmental Management. 92, 407-418;
- Diana Vilela, Jemish Parmar, Yongfei Zeng, Yanli Zhao, Samuel Sánchez. (2016). Graphene-Based Microbots for Toxic Heavy Metal Removal and Recovery from Water. Nano Lett.. 16, 2860-2866;
- Huai-Ping Cong, Xiao-Chen Ren, Ping Wang, Shu-Hong Yu. (2012). Macroscopic Multifunctional Graphene-Based Hydrogels and Aerogels by a Metal Ion Induced Self-Assembly Process. ACS Nano. 6, 2693-2703;
- Weijun Peng, Hongqiang Li, Yanyan Liu, Shaoxian Song. (2017). A review on heavy metal ions adsorption from water by graphene oxide and its composites. Journal of Molecular Liquids. 230, 496-504;
- Sarita Yadav, Neetu Goel, Vinod Kumar, Sonal Singhal. (2019). Graphene Oxide as Proficient Adsorbent for the Removal of Harmful Pesticides: Comprehensive Experimental Cum DFT Investigations. Analytical Chemistry Letters. 9, 291-310;
- Roto Roto. (2018). Surface Modification of Fe3O4 as Magnetic Adsorbents for Recovery of Precious Metals. Advanced Surface Engineering Research;
- Mark J. Hopwood, Insa Rapp, Christian Schlosser, Eric P. Achterberg. (2017). Hydrogen peroxide in deep waters from the Mediterranean Sea, South Atlantic and South Pacific Oceans. Sci Rep. 7;
- Dandan Li, Moonkwang Jeong, Eran Oren, Tingting Yu, Tian Qiu. (2019). A Helical Microrobot with an Optimized Propeller-Shape for Propulsion in Viscoelastic Biological Media. Robotics. 8, 87;
- 11 простых правил написания научных обзоров;
- Как написать хорошую научную статью?.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





