
Миссия выполнима: как белки бактериофагов становятся лекарствами будущего
07 апреля 2026
Миссия выполнима: как белки бактериофагов становятся лекарствами будущего
- 327
- 0
- 3
Бактериофаг-шпион в поиске бактерий.
Рисунок в полном размере.
сгенерировано с помощью Perplexity
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Глобальный кризис антибиотикорезистентности заставляет науку искать новые пути борьбы с бактериальными инфекциями. Оказалось, что самое совершенное оружие против бактерий создала сама природа — это бактериофаги. Но сегодня ученые берут на вооружение не целые вирусы, а их высокоспециализированные белки. В этой статье мы рассмотрим, как эти молекулярные «инструменты» — от «отмычек», вскрывающих бактериальную защиту, до «подрывных зарядов», разрушающих клетку изнутри, — становятся основой для лекарств нового поколения, систем целевой доставки и биотехнологических платформ, открывая новую эру в борьбе с инфекциями.
Конкурс «Био/Мол/Текст»-2025/2026
 Эта работа заняла первое место в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.
Эта работа заняла первое место в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Когда в 1928 году Александр Флеминг открыл пенициллин, человечеству могло показаться, что война с бактериями выиграна. Однако мы явно недооценивали противника. Сегодня антибиотики стремительно теряют силу, и на смену триумфу пришла глобальная угроза — антибиотикорезистентность, которая уже к 2050 году может уносить до 10 миллионов жизней в год [1].
В поисках решения ученые обратились к древним и идеальным убийцам бактерий, миллионы лет оттачивавшим свое оружие — бактериофагам. Попытки использовать целых фагов для лечения инфекций предпринимаются уже почти столетие, однако широкого распространения в мировой медицине этот подход не получил. С открытием антибиотиков фаготерапия отошла на второй план, но главная причина крылась в сложной природе самих фагов. Как отмечается в статье «Бактериофаги в медицине» [2], их действие в реальных условиях кардинально отличается от «упрощенных» лабораторных моделей. В пробирке фаги эффективно уничтожают быстрорастущие бактерии, но в организме патогены часто находятся в «стационарной фазе», включая защитные механизмы. В таких условиях многие фаги впадают в «режим гибернации», и их терапевтический эффект становится слабым или непредсказуемым. Поэтому сегодня ученые берут на вооружение уже не целые вирусы с их сложной «биологией», а их секретное оружие — белки, действие которых можно стандартизировать и контролировать.
Эти молекулярные «инструменты» способны с хирургической точностью уничтожать патогены, не затрагивая полезную микрофлору. Они — основа нового поколения препаратов, «энзибиотиков», и наша главная надежда.
В этой статье мы отправимся на сверхсекретную миссию вместе с бактериофагами. Мы заглянем в их арсенал шпионских гаджетов и понаблюдаем за работой каждого инструмента в деле. Вы увидите, как «отмычки» вскрывают бактериальные замки, «буры» проделывают точечные проходы, а «подрывные заряды» обеспечивают эффектный финал. Наша задача — не просто подсмотреть, а перенять их лучшие технологии, чтобы превратить вирусное оружие в инновационные инструменты для медицины — от лабораторий до больничных палат.
Не все фаги одинаковы
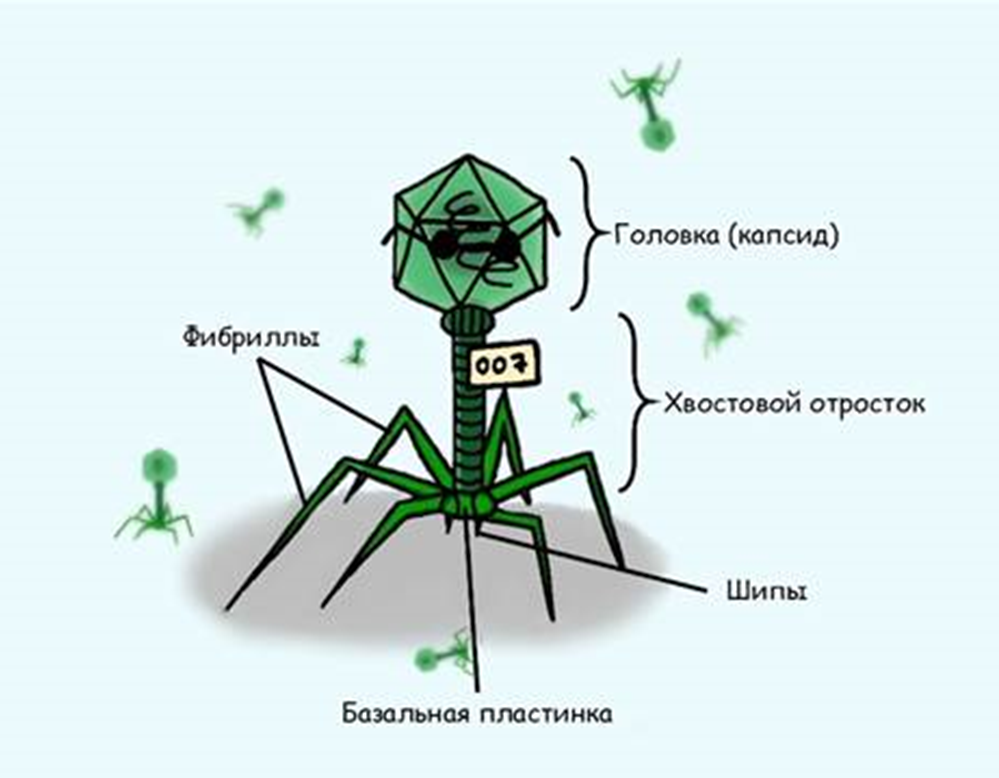
Рисунок 1. Общее строение бактериофага: схематическое изображение «хвостатого» фага порядка Caudovirales с подписями основных структурных компонентов.
рисунок автора
Для того, чтобы лучше понимать механизмы действия энзибиотиков, необходимо поближе познакомиться с нашими союзниками. Бактериофаги различаются по морфологии, типу нуклеиновой кислоты и характеру взаимодействия с бактериями. О бактериофагах на «Биомолекуле» выходил целый спецпроект.
Хотя разнообразие фагов огромно, наиболее изученные из них, и особенно те, что используются в терапии и как источник полезных ферментов, часто относятся к порядку Caudovirales («хвостатые вирусы»). Их строение напоминает космический аппарат или шприц и включает несколько ключевых компонентов (рис. 1):
- Головка (капсид) — это белковая «капсула», главная функция которой — надежно упаковать и защитить генетический материал фага, его «инструкцию по захвату» — ДНК или РНК. Капсид построен из множества копий одного или нескольких структурных белков, образующих прочную оболочку.
- Хвостовой отросток — это «шприц» или «инъектор» фага, сложная белковая структура, ответственная за прикрепление к поверхности бактерии и доставку генетического материала внутрь клетки.
- Базальная пластинка, от которой могут отходить белковые шипы или фибриллы. Они обеспечивают первый контакт с поверхностью бактерии (первичное узнавание).
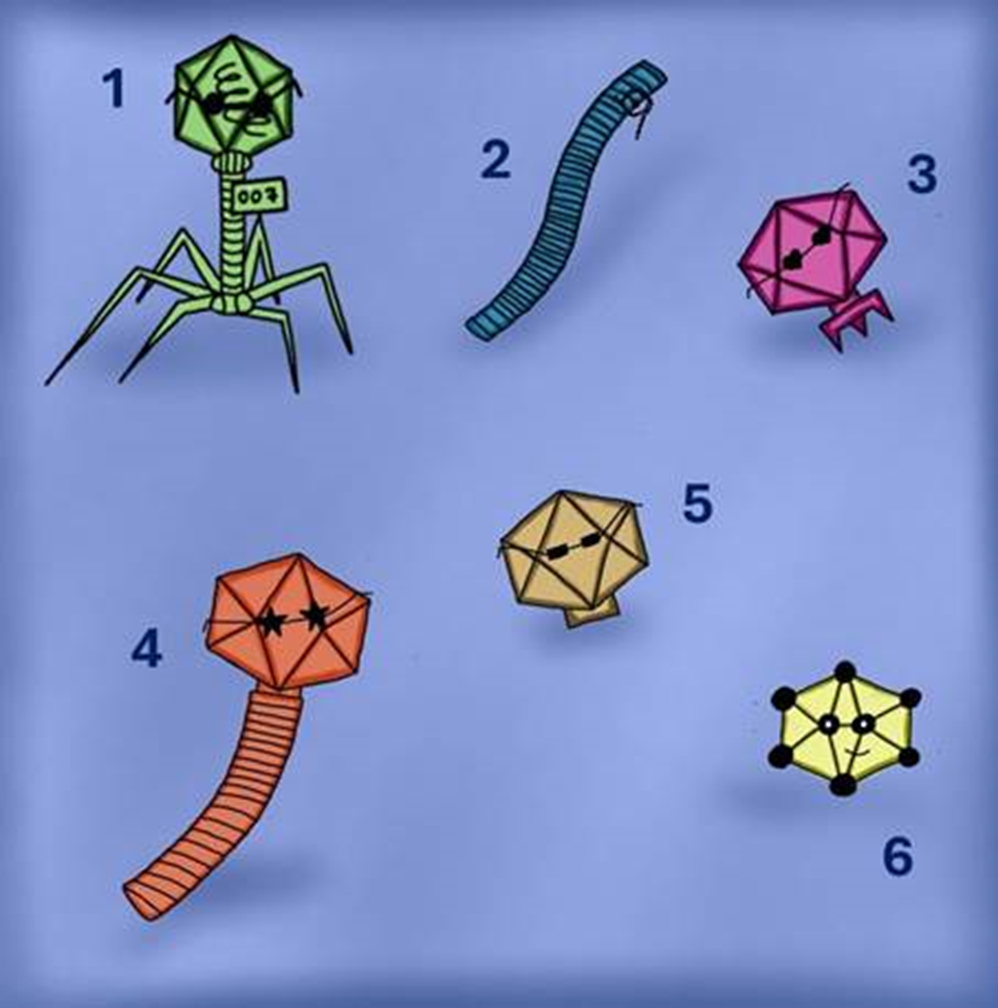
Рисунок 2. Разнообразие капсидов: 1 — с сокращающимся отростком, 2 — нитевидные, 3 — с коротким несокращающимся отростком, 4 — с длинным несокращающимся отростком, 5 — без отростка и капсомеров, 6 — без отростка, с капсомерами.
рисунок автора
Существуют и другие, не менее интересные бактериофаги (рис. 2):
- Бесхвостые фаги (например, Microviridae), чья капсидная оболочка имеет форму икосаэдра.
- Нитевидные фаги (например, Inoviridae), которые действительно похожи на тонкие гибкие нити. Они не убивают клетку, а постоянно «отпочковываются» от ее поверхности, что делает их интересными инструментами для нанотехнологий.
Белковый арсенал бактериофагов
Теперь, когда мы знаем союзника в лицо, пришло время вскрыть тот самый чемоданчик со шпионскими гаджетами — ключевыми белковыми инструментами, которые фаги используют на разных этапах своей миссии. Как и любой уважающий себя спецагент, фаг действует по четкому плану: сначала — идентификация цели и взлом. Только потом — проникновение в самое сердце вражеской крепости.
Рецептор-связывающие белки — «молекулярные отмычки»
Первым делом наш агент должен опознать цель и проверить замок. Хвостатые фаги используют широкий спектр рецептор-связывающих белков, таких как хвостовые фибриллы (tail fibers), хвостовые шипы (tail spikes) и центральный хвостовой шип (central tail spikes), для проникновения в бактериальные клетки через соответствующие рецепторы на их поверхности. Этими рецепторами могут быть белки (например, порины), углеводы (входящие в состав липополисахаридов или капсул) или тейхоевые кислоты.
Представьте себе, что у каждой бактериальной двери (то есть у каждого штамма) есть свой уникальный замок. Шипы и фибриллы — это наборы отмычек, настроенные только на конкретный тип замка. Такая избирательность гарантирует, что фаг атакует только свою цель, не трогая полезных бактерий или клетки человека.
Рассмотрим механизм узнавания на примере фага Т4 — одного из самых изученных бактериофагов. Раньше ученые думали, что он, как посадочный модуль, опускается на бактерию, предварительно закрепив все свои длинные хвостовые фибриллы. Однако новейшие исследования показали, что его тактика гораздо хитрее [3].
Оказалось, что его шесть длинных фибрилл работают не синхронно, а поочередно (рис. 3). Одна фибрилла вытягивается, находит «замок» (например, липополисахарид или белок на поверхности бактерии) и ненадолго «прилипает» к нему. Пока первая держится, вытягивается вторая — и так далее.
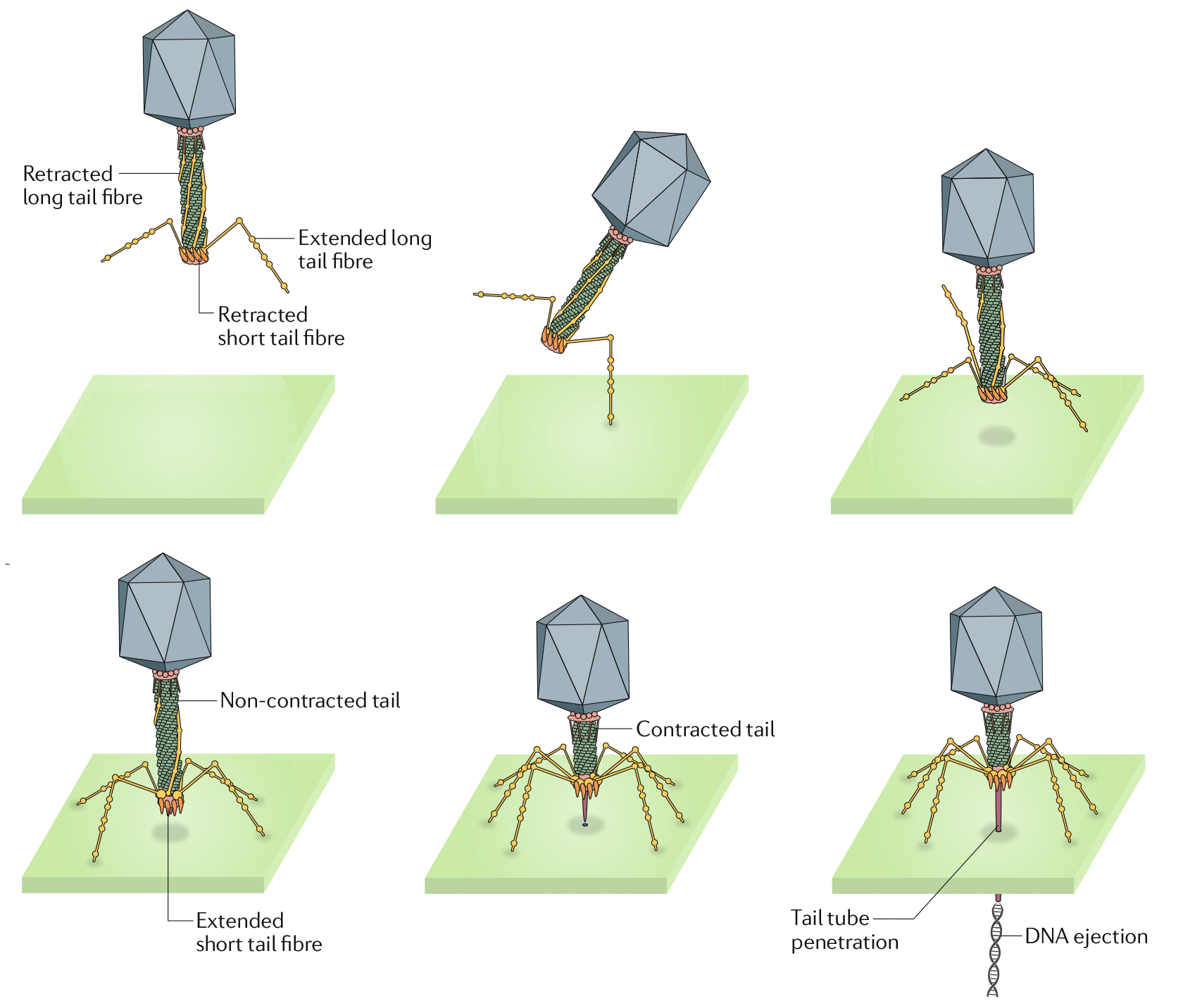
Рисунок 3. Модель адсорбции фага Т4 на поверхности хозяина.
Этот процесс «походки» позволяет фагу не просто прикрепиться, а буквально пройти по бактерии в поиске идеальной точки для необратимой адсорбции и впрыскивания своей ДНК. Такая обратимая стадия поиска — ключевой фактор, определяющий, на каких именно хозяев может напасть этот вирус.
Деполимеразы — «универсальные растворители»
Но что, если дверь не просто заперта, а еще и забаррикадирована? Многие бактерии носят плотную капсулу из полисахаридов или живут в крепости из слизи, называемой биопленкой. Этот щит делает их практически неуязвимыми для антибиотиков и иммунной системы. Здесь фаги используют деполимеразы.
Деполимеразы действуют точечно и стратегически — они лишают врага его главной защиты. Если фибриллы — это отмычки, то деполимеразы — это универсальные растворители, которые буквально разъедают эти сахарные баррикады, очищая путь к следующему рубежу обороны.
Деполимеразы расщепляют О-гликозидные связи бактериальных полисахаридов с получением олигосахаридных продуктов путем гидролитического или негидролитического разрыва связи. Такие типы действия, соответственно, разделяют деполимеразы на два основных класса: гидролазы и лиазы (рис. 4) [4].
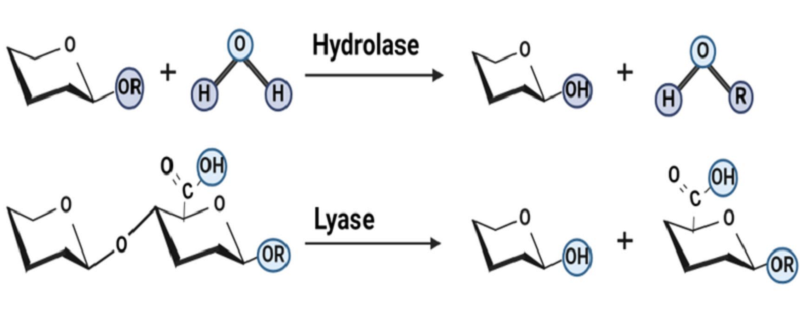
Рисунок 4. Механизмы действия деполимеразы.
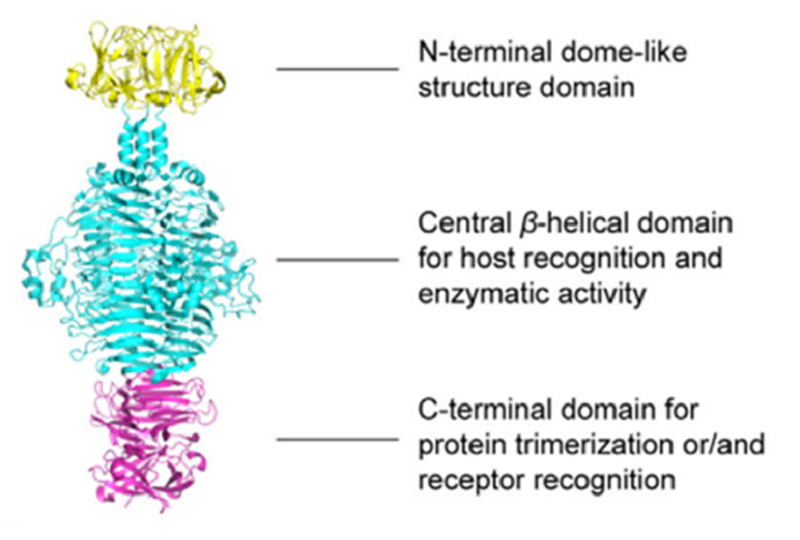
Рисунок 5. Доменная организация деполимеразы.
На структурном уровне деполимеразы обычно имеют модульную архитектуру, состоящую из трех доменов: консервативного N-концевого домена, вариабельного центрального домена и C-концевого домена (рис. 5):
N-концевой домен образует структуру, отвечающую за прикрепление деполимеразы к базальной пластинке фаговой частицы. Центральный домен образует вытянутую параллельную β-спиральную структуру с каталитическим карманом, способствующим распознаванию хозяина и ферментативной активности. С-концевой домен обычно участвует в связывании с рецептором и может содержать шаперон, способствующий правильному сворачиванию белка [4].
Такая модульная архитектура превращает деполимеразу в идеальный шпионский гаджет с функцией быстрой смены специфичности. Когда противник меняет замки, наш агент не теряется и использует две разные стратегии:
- «Захват чужого протокола». Фаг может экстренно заменить центральный домен своего фермента на чужой, «позаимствовав» его у другого вируса (горизонтальный перенос генов).
- «Апгрейд прошивки». Фаг постепенно, из поколения в поколение, совершенствует свой существующий инструмент, накапливая точечные улучшения (вертикальный перенос генов). Представьте, будто фаги постоянно вносят мелкие правки в конструкцию отмычки, чтобы она работала эффективнее и точнее.
И вот, когда полисахаридные баррикады наконец растворены, перед агентом возникает новая преграда — многослойная стена. У грамотрицательных бактерий это наружная мембрана, а за ней — прочный пептидогликановый каркас. У грамположительных — толстый слой пептидогликана, укрепленный тейхоевыми кислотами. Преодолеть эту защиту — задача не из легких.
Вирион-ассоциированные пептидогликан-гидролазы (VAPGH) — «молекулярные буры»
Многие фаги (особенно фаги с сокращающимся хвостом — Myoviridae) несут на кончике хвоста VAPGH (вирион-ассоциированные пептидогликан-гидролазы) — ферменты, которые работают как молекулярные буры. Их цель — прочная сеть пептидогликана, главный структурный каркас бактериальной клеточной стенки. Они не разрушают всю стену, а лишь просверливают в ней микроскопическое отверстие, достаточное для того, чтобы протолкнуть внутрь свой генетический материал.
Они используют разную тактику в зависимости от типа противника:
- Против грамположительных бактерий: VAPGH — это первый и главный таран, бьющий прямо в толстую пептидогликановую стенку.
- Против грамотрицательных бактерий: задача сложнее — им нужно работать через небольшое отверстие в наружной мембране, которое создают другие белки, и атаковать тонкий, но прочный слой пептидогликана под ней.
Некоторые VAPGH, такие как белок gp5 фага T4, представляют собой целый «многофункциональный инструмент». Помимо лизоцимного домена (gp5), который необходим для расщепления клеточного межмембранного слоя пептидогликанов, он имеет еще и β-спиральный домен, образующий острую «иглу», которая физически прокалывает мембрану после ослабления пептидогликана [5]. Настоящий шпионский девайс «два в одном»!
Агент успешно проник в штаб-квартиру врага, доставил секретные инструкции (вирусную ДНК), и теперь начинается самая важная часть — обеспечить себе эффектный выход и выполнить главную задачу: размножиться и высвободить фаговые частицы наружу.
Пока враг отвлечен репликацией вирусных инструкций, внутри его базы тихо и незаметно производятся эндолизины — мощные подрывные заряды, также нацеленные на главные несущие конструкции бактерии — пептидогликановый слой. Если VAPGH работают на входе, то эндолизины — это оружие, активируемое на выходе, которое приводит к разрыву клетки (лизису) и освобождению сотен новых фаговых частиц.
Как типичный шпионский гаджет, эндолизин имеет модульное устройство:
- Каталитический домен (EAD, enzymatically active domains) — это сам заряд, фермент, который молниеносно разрезает ключевые связи в пептидогликане.
- Домен связывания (CBD, cell wall-binding domains) — это якорь, который фиксирует эндолизин на специфических структурах бактериальной клеточной стенки, позволяя каталитическому домену эффективно разрушать пептидогликан.
Заряды установлены, но они находятся в цитоплазме, отделенные от пептидогликана внутренней мембраной. Кто даст команду «огонь»?
Холины — «перфораторы внутренней мембраны»
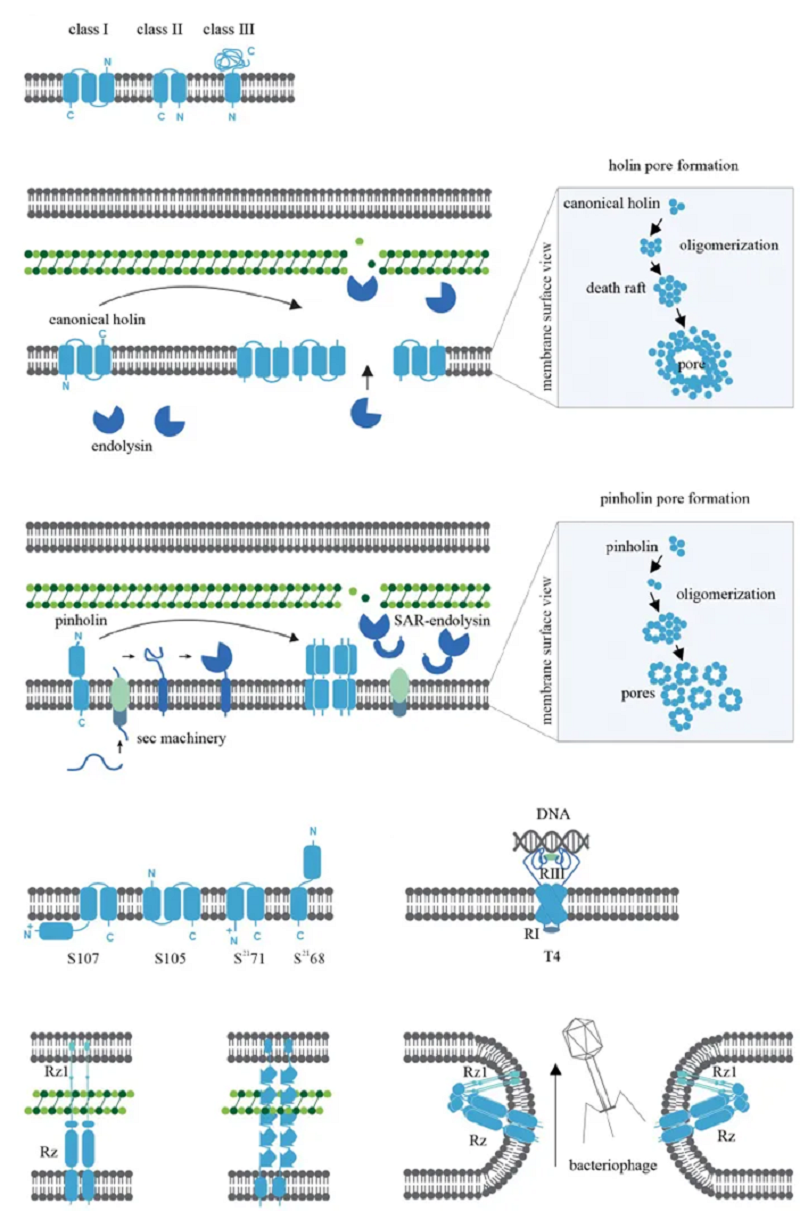
Рисунок 6. Классификация и механизм действия холинов.
Холины (holin — от англ. hole — «дыра») — это белки-детонаторы, которые подают сигнал для начала разрушения клеточной стенки. Не стоит путать холины бактериофагов с предшественником нейромедиатора ацетилхолина — холином (choline). В строго заданный момент холины встраиваются во внутреннюю мембрану и создают в ней поры, способствуя тем самым началу лизиса пептидогликанов с помощью эндолизинов.
Эволюция разработала несколько типов «детонаторов» для разных тактических задач и условий (рис. 6) [6]. Их основное различие — в «форме» и способе «заякоривания» в мембране:
- Холины класса I: универсальные. Имеют три трансмембранные спирали в конфигурации N-out/C-in (N-конец белка снаружи, а С-конец внутри клетки). Наиболее распространенная и изученная группа.
- Холины класса II: обходятся двумя трансмембранными спиралями (N-in/C-in). Не менее эффективны, но, возможно, более специализированы.
- Холины класса III: сложные детонаторы. Имеют всего одну трансмембранную спираль, но зато обладают крупным периплазматическим доменом (N-in/C-out). Этот дополнительный домен, свисающий в периплазму, может играть роль в регуляции времени лизиса или взаимодействии с другими компонентами [6].
Спанины — «перфораторы внешней мембраны»
Миссия на финише. Внутренние опоры (пептидогликан) рухнули под натиском эндолизинов, прошедших через поры холинов. Но для грамотрицательных бактерий это еще не конец. У них есть вторая линия обороны — внешняя мембрана, окружающая клетку. Если ее не разрушить, новое поколение агентов-фагов окажется в ловушке, запертое в клетке (сферопласте), неспособное отправиться на новые задания. Именно здесь на сцену выходят спанины — специалисты по внешним укреплениям, чья задача — финальный, сокрушительный подрыв внешней стены.
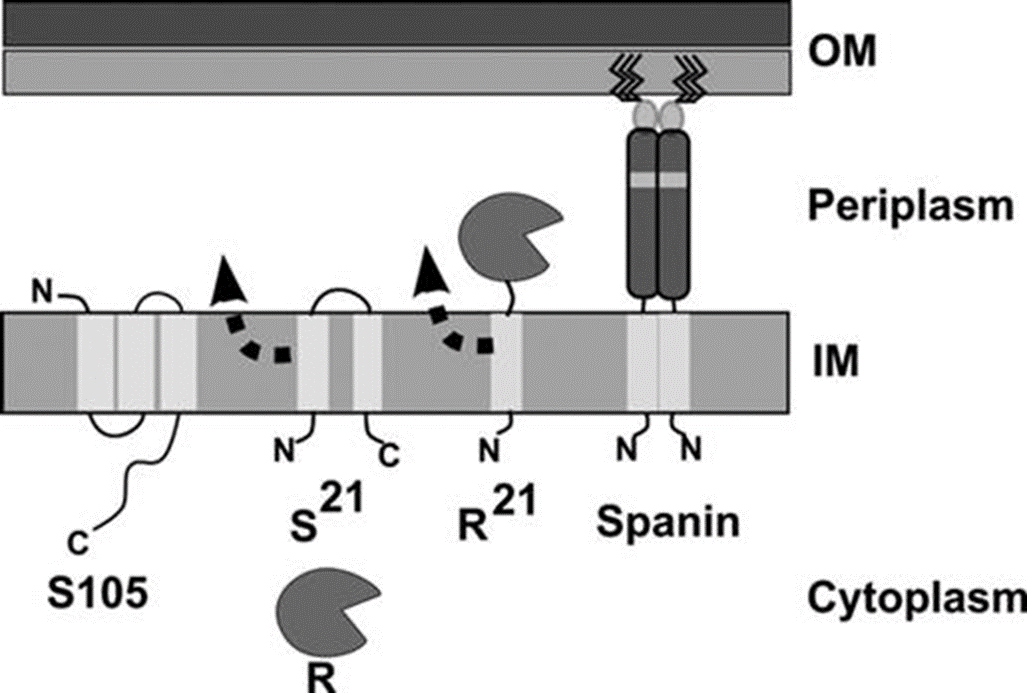
Рисунок 7. Топология и локализация спанинов (OM — внешняя мембрана, IM — внутренняя мембрана, periplasm — периплазматическое пространство, R — эндолизин, spanin — спанин).
Спанины накапливаются в виде комплексов, соединенных через пептидогликановый слой. После разрушения пептидогликана спанины получают свободу движения. Спанины меняют конформацию, сближая наружную и внутреннюю мембраны, что приводит к их слиянию и образованию «поры», через которую сотни новобранцев-фагов вырываются на свободу (рис. 7) [7].
Эволюция создала две основные тактики для выполнения этой миссии [6]:
- Двухкомпонентные спанины (2CS) — «напарники». Это классическая диверсионная группа из двух специалистов: i-спанин внедряется во внутреннюю мембрану (IM), а o-спанин закрепляется на внешней мембране (OM). Вместе они образуют гетерокомплекс, который и стягивает мембраны, приводя к их слиянию.
- Унимолекулярные спанины (u-spanin) — «мастер-одиночка». Более элегантное и компактное решение. Это одиночный белок-гибрид, который сам выполняет работу двух: его N-конец заякоривается во внешней мембране, а C-конец с трансмембранным доменом пронзает внутреннюю мембрану.
Итак, миссия по захвату и уничтожению вражеской базы близится к логическому завершению. Изучив весь этот сложноустроенный арсенал бактериофагов, понимаешь, что имеешь дело не с примитивными вирусами, а с высокоэффективными агентами, оснащенными уникальным набором специализированных инструментов. Каждый из них отточен эволюцией для ювелирного выполнения своей задачи.
Их невероятная специфичность и мощь могут быть «перепрофилированы» и поставлены на службу человеку для борьбы с инфекциями, создания новых технологий и многого другого. В следующих главах мы подробно рассмотрим, как именно эти молекулярные «шпионские гаджеты» меняют современную медицину и технологии.
Применение в медицине и технологиях
Рецептор-связывающие белки
Изучив, как рецептор-связывающие белки с ювелирной точностью находят свою цель в природе, ученые задались вопросом: а можно ли этот уникальный механизм «перенастроить» на службу человеку? Ответом стало создание одной из самых мощных биотехнологических платформ — фагового дисплея.
В основе метода — все те же белки, но теперь их способность избирательно связываться с мишенью используется для поиска и отбора ценных молекул. Например, у фага Т4 для дисплея часто используется белок gp10 малого шипа базальной пластинки. На его кончик можно «подвесить» довольно крупные белки. Особенно впечатляющих результатов удалось достичь в создании антител.
Представьте себе миллионы разных фагов, каждый из которых на своем «кончике» демонстрирует уникальный вариант антитела. Эту коллекцию пропускают через поверхность с нанесенными целевыми молекулами (антигенами). Большинство фагов просто смываются, но те немногие, чьи антитела идеально подошли к мишени, прочно «приклеиваются» к ней. Эти фаги отбираются, а по их ДНК определяют точную структуру успешного антитела. Затем нужный ген встраивают в штаммы-продуценты, которые начинают массово производить именно это, уже проверенное и эффективное антитело.
Подробнее про метод фагового дисплея рассказывается в статье «12 методов в картинках: иммунологические технологии» [8].
Помимо фагового дисплея, с помощью рецептор-связывающих белков создаются платформы для точечной доставки антибиотиков. Чтобы достичь терапевтической концентрации в очаге инфекции, мы вынуждены создавать высокую концентрацию повсюду, что приводит к побочным эффектам и ускоряет селекцию устойчивых штаммов. Решением становится целевая доставка, при которой антибиотик направляется прямиком к патогенам.
Ученые создали наноразмерные контейнеры на основе мезопористых кремниевых частиц (UPSNs), которые, подобно губкам, способны вмещать огромное количество антибиотика (до 60% от собственной массы). Однако главная инновация заключается не в самом контейнере, а в его «системе самонаведения». Для этого используются два типа высокоспецифичных фаговых белков: рецептор-связывающие белки (RBP), которые фаг использует как «ключ», и клеточно-связывающие домены (CBD) — часть ферментов эндолизинов, с высоким сродством связывающиеся с пептидогликаном клеточной стенки [9].
Исследователи разработали модульные платформы для разных типов бактерий. Например, для борьбы с грамотрицательной Klebsiella pneumoniae антибиотик рифампицин загружали в UPSNs, покрывали липидным бислоем для стабильности и конъюгировали с рецептор-связывающими белками фага P545 [9].
Эффективность такого подхода уже подтверждена в исследованиях in vivo на мышиных моделях пневмонии. Оказалось, что рифампицин, доставленный с помощью фаговых белков, подавлял инфекцию так же эффективно, как и свободный антибиотик, но в дозе, меньшей в 16–27 раз. Но самое главное — эта технология позволила вновь сделать патогены уязвимыми к антибиотикам, от которых у них уже была выработана устойчивость.
Меняя RBP или CBD на белки от других фагов, можно перенацелить систему практически на любую бактериальную мишень. Доказанная биосовместимость наночастиц и сохранение их эффективности даже после нескольких введений, несмотря на иммунный ответ, открывают реальный путь для клинического применения.
Деполимеразы
Особую медицинскую значимость деполимеразы имеют в борьбе с бактериальными биопленками. Биопленка — это сообщество бактерий, погруженных в вырабатываемый ими внеклеточный матрикс, состоящий из полисахаридов, ДНК и белков. Эта структура действует как «крепость», защищая бактерии от антибиотиков и иммунной системы организма, что приводит к хроническим и рецидивирующим инфекциям, особенно связанным с медицинскими имплантатами, такими как катетеры.
Фаговые деполимеразы целенаправленно атакуют полисахаридный каркас этой биопленки, буквально растворяя его. Например, деполимераза фага vB_PmiS_PM-CJR эффективно разрушала биопленки уропатогена Proteus mirabilis, значительно снижая бактериальную биомассу [10]. Такие открытия создают перспективы для лечения катетер-ассоциированных инфекций мочеполовых путей, где биопленки Proteus mirabilis вызывают до 20–40% случаев. Например, покрытие катетеров деполимеразами позволит предотвращать адгезию и образование биопленок, снижая риск хронических инфекций.
Интересным является и синергизм деполимераз с антибиотиками: так, деполимераза Dpo71 усиливала действие колистина (антибиотика) против биопленок Acinetobacter baumannii, поскольку разрушение матрикса делало бактерии вновь уязвимыми для лекарств [4]. В итоге эффективное разрушение полисахаридных матриц биопленок облегчает проникновение антибиотиков в бактериальные сообщества, приводя к лизису бактерий при дозах ниже стандартных, что снижает токсичность и вероятность аллергических реакций.
Несмотря на доказанную антибактериальную активность фаговых деполимераз in vitro, клинических испытаний этого подхода до сих пор не проводилось [11]. Таким образом, существует необходимость в детальном изучении применения фаговых деполимераз в качестве потенциальных терапевтических препаратов.
Эндолизины
Эндолизины, разрушающие пептидогликан бактериальной клеточной стенки, представляют собой новый класс антимикробных средств для борьбы с устойчивыми инфекциями. В отличие от традиционных антибиотиков, они обладают высокой специфичностью к целевым бактериям и крайне низким риском развития устойчивости, поскольку атакуют высококонсервативные бактериальные структуры.
Особый интерес представляет их применение против грамотрицательных бактерий, таких как Acinetobacter baumannii — одного из самых проблемных внутрибольничных патогенов. Например, эндолизин LysAB54 продемонстрировал активность в отношении метициллин-резистентного A. baumannii без использования пермеабилизаторов внешней мембраны (веществ, которые нарушают проницаемость внешней мембраны грамотрицательных бактерий), вызывая снижение количества бактерий на 4 порядка. Другой эндолизин, PlyF307, не только эффективно уничтожал планктонные клетки, но и разрушал биопленки A. baumannii на катетерах [12]. Здесь так же, как и в случае с деполимеразами, имеет место синергетическая терапия: комбинация эндолизина LysABP-01 с колистином позволяла снизить минимальную ингибирующую концентрацию (МИК) последнего в 32 раза, что открывает путь к использованию меньших и менее токсичных доз антибиотиков [12].
Несколько препаратов на основе эндолизинов уже проходят клинические испытания, в том числе Exebacase (CF-301) против стафилококков и SAL200, что подтверждает их переход из области исследований в практическую медицину [12].
Вирион-ассоциированные пептидогликан-гидролазы (VAPGH)
Идея точечного разрушения клеточной стенки здесь схожа с использованием эндолизинов. Если «одолжить» у фага этот «бур» (VAPGH) и научиться доставлять его к бактериям, можно создавать высокоспецифичные антимикробные средства. Более того, поскольку VAPGH атакуют структуру, критически важную для выживания бактерии, у последних гораздо меньше шансов развить устойчивость, чем к традиционным антибиотикам.
Искусственно синтезированные пептиды, имитирующие активный центр VAPGH, уже показывают эффективность in vitro против таких патогенов, как Staphylococcus aureus. Они не убивают бактерию полностью, но создают в ее оболочке «прорехи», делая ее уязвимой для действия иммунной системы или других препаратов [13].
Холины
Холины демонстрируют мощную антибактериальную активность, поскольку представляют собой белки, которые создают отверстия в бактериальной мембране.
Например, холин HolGH15, выделенный из бактериофага стафилококка, показал высокую эффективность против опасного пищевого патогена Listeria monocytogenes, которая вызывает листериоз [14].
Listeria встречается повсеместно и в основном передается через рот при употреблении зараженных пищевых продуктов, после чего бактерии проникают в кишечник и вызывают системные инфекции. Лечение включает длительный прием антибиотиков, в первую очередь, ампициллина и гентамицина, к которым возбудитель обычно чувствителен.
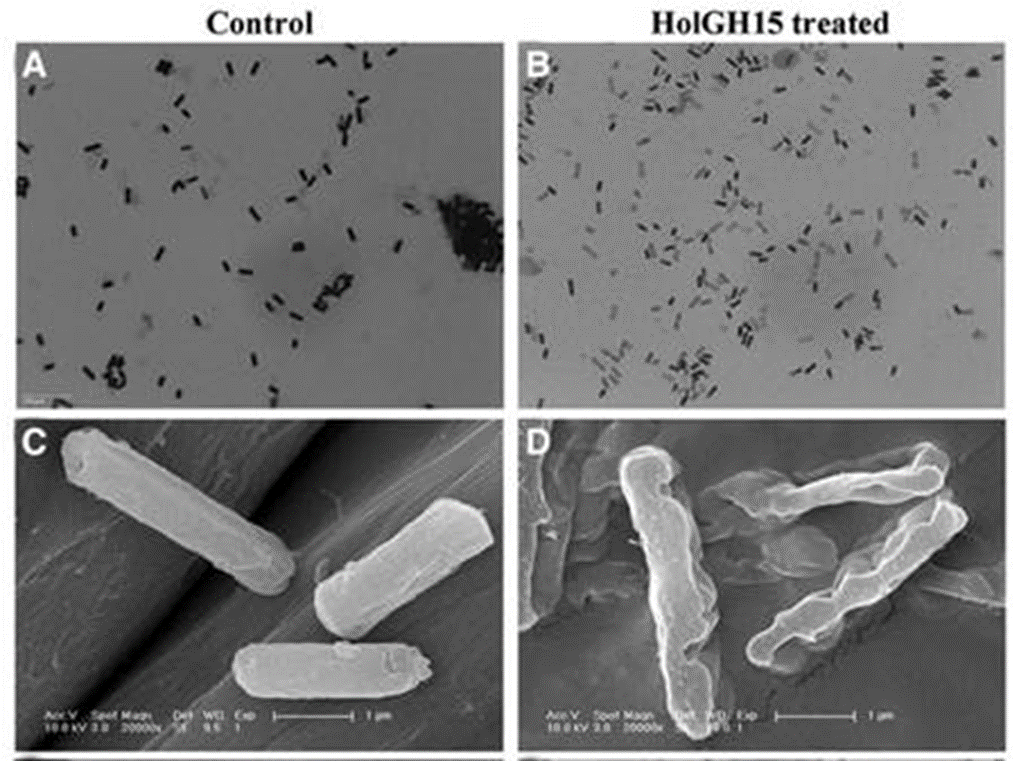
Рисунок 8. Изменение морфологии клеток Listeria monocytogenes после обработки холинами.
Было показано, что холин HolGH15 полностью уничтожает бактерии даже в условиях холодильника (+4 oC), что открывает путь к его использованию в качестве природного консерванта для опрыскивания мяса, фруктов и овощей. Главное преимущество холинов — крайне низкий риск развития у бактерий устойчивости, так как мишенью является сама структура мембраны, а не конкретный метаболический путь.
На рисунке 8 изображены интактные клетки патогена Listeria monocytogenes (А, С) и обработанные HolGH15 в концентрации 120 lg/мл (В, D). Клетки бактерий, подвергшиеся воздействию HolGH15, демонстрировали значительные повреждения, которые приводили к разрыву клеток [14].
Это делает холины перспективными агентами как в пищевой промышленности, так и в терапии инфекций, особенно в комбинации с другими антимикробными средствами для усиления эффекта. Однако, как и в случае с деполимеразами, клинических испытаний этих подходов до сих пор не проводилось.
Спанины
Практическое применение спанинов, в отличие от эндолизинов и VAPGH, имеет ключевое ограничение: они эффективны только против грамотрицательных бактерий. Это связано с их уникальным механизмом действия: как мы уже знаем, спанины физически соединяют внутреннюю и внешнюю мембраны бактерии, чтобы ее разрушить. Поскольку у грамположительных бактерий отсутствует внешняя мембрана, для спанинов в их клетках просто нет мишени.
При этом, в отличие от многих других ферментов, спанины демонстрируют исключительно широкий спектр действия на грамотрицательных бактериях. Например, белок T1-спанин показал высокую эффективность против всех протестированных клинических изолятов E. coli, Klebsiella spp., Pseudomonas aeruginosa и Acinetobacter spp., включая штаммы, устойчивые к карбапенемам. При этом его эффективность превзошла даже потенциал эндолизинов того же фага, которые оказались неспособны справиться с некоторыми из этих патогенов [15]. Наиболее перспективной технологией является упаковка гена, кодирующего T1-спанин, в синтетические неразмножающиеся фаговые капсиды.
кодирующего T1-спанин, в синтетические неразмножающиеся фаговые капсиды. Механизм работы синтетических неразмножающихся фаговых капсидов напоминает запрограммированного шпионского робота. По своей сути, это белковая оболочка обычного бактериофага, лишенная его главного компонента — вирусного генома. Вместо него внутрь капсида упаковывается плазмида — кольцевая молекула ДНК, несущая единственный ген, например, ген белка-спанина [15].
Процесс можно разбить на ключевые этапы:
- Доставка. Синтетический капсид сохраняет способность природного фага узнавать специфические рецепторы на поверхности бактерии-мишени и прочно прикрепляться к ним. После связывания он «впрыскивает» содержимое — плазмиду с геном спанина — в цитоплазму бактерии.
- Активация «смертельного» гена. Попав в клетку, плазмида начинает работать как автономная инструкция. Бактериальные механизмы считывают ген T1-спанина и синтезируют большое количество этого белка.
- Исполнение программы. Синтезированный T1-спанин встраивается в клеточные мембраны. Как было описано ранее, он формирует мосты между внутренней и внешней мембраной, что приводит к их слиянию, нарушению целостности клетки и мгновенному лизису.
- Самоуничтожение. Это критически важное отличие от живой фаговой терапии. Поскольку внутрь капсида был упакован только ген спанина, а не полный фаговый геном, инфицированная бактерия не производит новые вирусные частицы. Высвободившиеся после лизиса бактерии капсиды являются «пустыми» и не способны к новому заражению. Это делает технологию локальной, контролируемой и экологически безопасной.
Таким образом, эта платформа сочетает в себе высочайшую специфичность фагов (за счет нацеливания капсида) с мощью белка, разрушающего бактериальные клетки. К тому же такой способ обладает предсказуемой безопасностью нереплицирующейся системы, что открывает путь к созданию принципиально нового класса антимикробных препаратов точечного действия.
Этот подход, как и другие рассмотренные нами примеры, демонстрирует общую стратегию: ученые не копируют фаги целиком, а берут на вооружение их лучшие «разработки» — высокоспециализированные белки. Каждый из этих молекулярных инструментов находит свое уникальное применение в медицине и биотехнологиях, открывая новые возможности в борьбе с инфекциями.
Чтобы наглядно обобщить огромный потенциал белкового арсенала бактериофагов, обратимся к сводной таблице:
| Белок | Функция у фага | Применение | Стадия разработки |
|---|---|---|---|
| Рецептор-связывающие белки | Узнавание и прикрепление к бактериальной клетке | Фаговый дисплей для открытия новых лекарств (антител); целевая доставка антибиотиков | Фаговый дисплей активно используется в биотехнологиях; целевая доставка — эксперименты in vivo на мышиных моделях |
| Деполимеразы | Разрушение полисахаридной капсулы и матрикса биопленки | Борьба с хроническими инфекциями, связанными с биопленками (на катетерах, имплантатах); синергия с антибиотиками | Эксперименты in vivo на модельных животных |
| Эндолизины | Разрушение клеточной стенки для выхода потомства | Высокоспецифичные антимикробные препараты против резистентных патогенов (в т. ч. грамотрицательных) | Несколько препаратов проходят клинические испытания (фаза II) |
| VAPGH | Локальное разрушение пептидогликана для впрыскивания ДНК | Создание пептидных антимикробных средств, ослабляющих клеточную стенку | Эксперименты in vitro |
| Холины | Создание пор во внутренней мембране для выхода эндолизинов | Самостоятельные антимикробные средства, особенно в пищевой промышленности | Доклинические исследования (in vitro и на животных моделях) |
| Спанины | Разрушение внешней мембраны грамотрицательных бактерий | Узконаправленные препараты против устойчивых грамотрицательных патогенов; платформа на основе синтетических капсидов | Перспективная технология на стадии доказательства концепции |
Заключение
Наше путешествие в мир молекулярных охотников подошло к концу. Мы увидели, что уже сегодня эти молекулярные инструменты вышли за пределы фундаментальной науки. Они помогают создавать новые антитела, доставлять лекарства точно в цель, бороться с биопленками и защищать наши продукты. И хотя многие разработки еще находятся на доклинической стадии, первые препараты на основе эндолизинов уже проходят клинические испытания. Война с бактериями далека от завершения, но теперь у человечества есть новые, куда более совершенные союзники!
Литература
- O'Neill J. (2014). Review on Antimicrobial Resistance Antimicrobial Resistance: Tackling a crisis for the health and wealth of nations. The Review on Antimicrobial Resistance. 20, 1–16;
- Бактериофаги в медицине;
- Franklin L. Nobrega, Marnix Vlot, Patrick A. de Jonge, Lisa L. Dreesens, Hubertus J. E. Beaumont, et. al.. (2018). Targeting mechanisms of tailed bacteriophages. Nat Rev Microbiol. 16, 760-773;
- Honglan Wang, Yannan Liu, Changqing Bai, Sharon Shui Yee Leung. (2024). Translating bacteriophage-derived depolymerases into antibacterial therapeutics: Challenges and prospects. Acta Pharmaceutica Sinica B. 14, 155-169;
- Shuji Kanamaru, Petr G. Leiman, Victor A. Kostyuchenko, Paul R. Chipman, Vadim V. Mesyanzhinov, et. al.. (2002). Structure of the cell-puncturing device of bacteriophage T4. Nature. 415, 553-557;
- Gayan S. Abeysekera, Michael J. Love, Sarah H. Manners, Craig Billington, Renwick C. J. Dobson. (2022). Bacteriophage-encoded lethal membrane disruptors: Advances in understanding and potential applications. Front. Microbiol.. 13;
- Joel Berry, Manoj Rajaure, Ting Pang, Ry Young. (2012). The Spanin Complex Is Essential for Lambda Lysis. J Bacteriol. 194, 5667-5674;
- 12 методов в картинках: иммунологические технологии;
- Xinghong Zhao, Xinyi Zhong, Shinong Yang, Jiarong Deng, Kai Deng, et. al.. (2024). Guiding antibiotics towards their target using bacteriophage proteins. Nat Commun. 15;
- Cormac J. Rice, Stephen A. Kelly, Seamus C. O’Brien, Erinn M. Melaugh, Jan C. B. Ganacias, et. al.. (2021). Novel Phage-Derived Depolymerase with Activity against Proteus mirabilis Biofilms. Microorganisms. 9, 2172;
- Zhimin Guo, Mengmeng Liu, Dan Zhang. (2023). Potential of phage depolymerase for the treatment of bacterial biofilms. Virulence. 14;
- Fazal Mehmood Khan, Fazal Rasheed, Yunlan Yang, Bin Liu, Rui Zhang. (2024). Endolysins: a new antimicrobial agent against antimicrobial resistance. Strategies and opportunities in overcoming the challenges of endolysins against Gram-negative bacteria. Front. Pharmacol.. 15;
- Lorena Rodríguez, Beatriz Martínez, Yuan Zhou, Ana Rodríguez, David M Donovan, Pilar García. (2011). Lytic activity of the virion-associated peptidoglycan hydrolase HydH5 of Staphylococcus aureusbacteriophage vB_SauS-phiIPLA88. BMC Microbiol. 11;
- Jun Song, Wenchao Niu, Rui Wu, Jianfa Wang, Liancheng Lei, et. al.. (2021). The Phage Holin HolGH15 Exhibits Potential As an Antibacterial Agent to Control Listeria monocytogenes. Foodborne Pathogens and Disease. 18, 574-581;
- Wakana Yamashita, Shinjiro Ojima, Azumi Tamura, Aa Haeruman Azam, Kohei Kondo, et. al.. (2024). Harnessing a T1 Phage-Derived Spanin for Developing Phage-Based Antimicrobial Development. BioDesign Research. 6, 0028.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





