Наночастицы для окраски биомолекул и QLED-дисплеев — за что вручили Нобелевскую премию по химии (2023)
05 октября 2023
Наночастицы для окраски биомолекул и QLED-дисплеев — за что вручили Нобелевскую премию по химии (2023)
- 686
- 0
- 2
Мунджи Бауэнди (слева), Луис Брюс и Алексей Екимов (справа) — лауреаты Нобелевской премии по химии 2023 года. Их открытие помогает окрашивать биологические клетки и производить яркие диспеи.
Рисунок в полном размере.
иллюстрация Анастасии Самоукиной
-
Автор
-
Редакторы
-
Рецензент
-
Иллюстратор
Нобелевский комитет вручил премию по химии за создание уникальных наночастиц — квантовых точек. В отличие от других материалов, их электрические, оптические и иные физические свойства меняются при увеличении размеров частиц. Для сравнения, вода в кристаллике льда любого размера не меняет цвет и температуру плавления. Это открытие важно с разных сторон. Оно фундаментально изменило химию, потому что ввело в использование новый класс материалов. Эти частицы расширили возможности для развития технологий, к примеру, цветных экранов QLED. Наконец, квантовые точки помогают биологам окрашивать нужные молекулы в живых клетках, а хирургам — находить опухоль во время операций.
В статье мы сначала разберем особенности квантовых точек, а затем обсудим их применение в биологии и медицине.
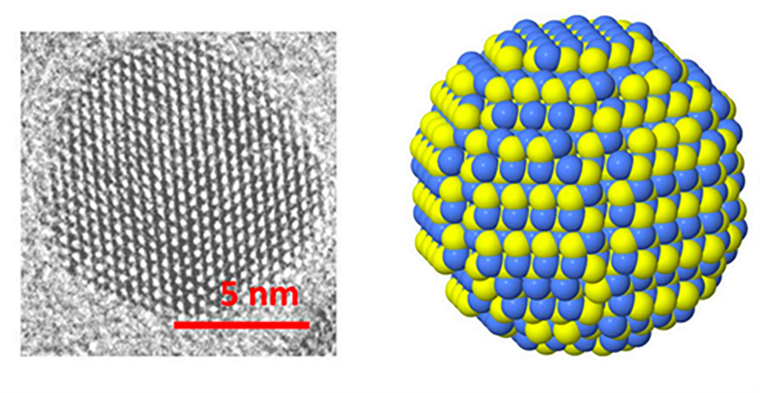
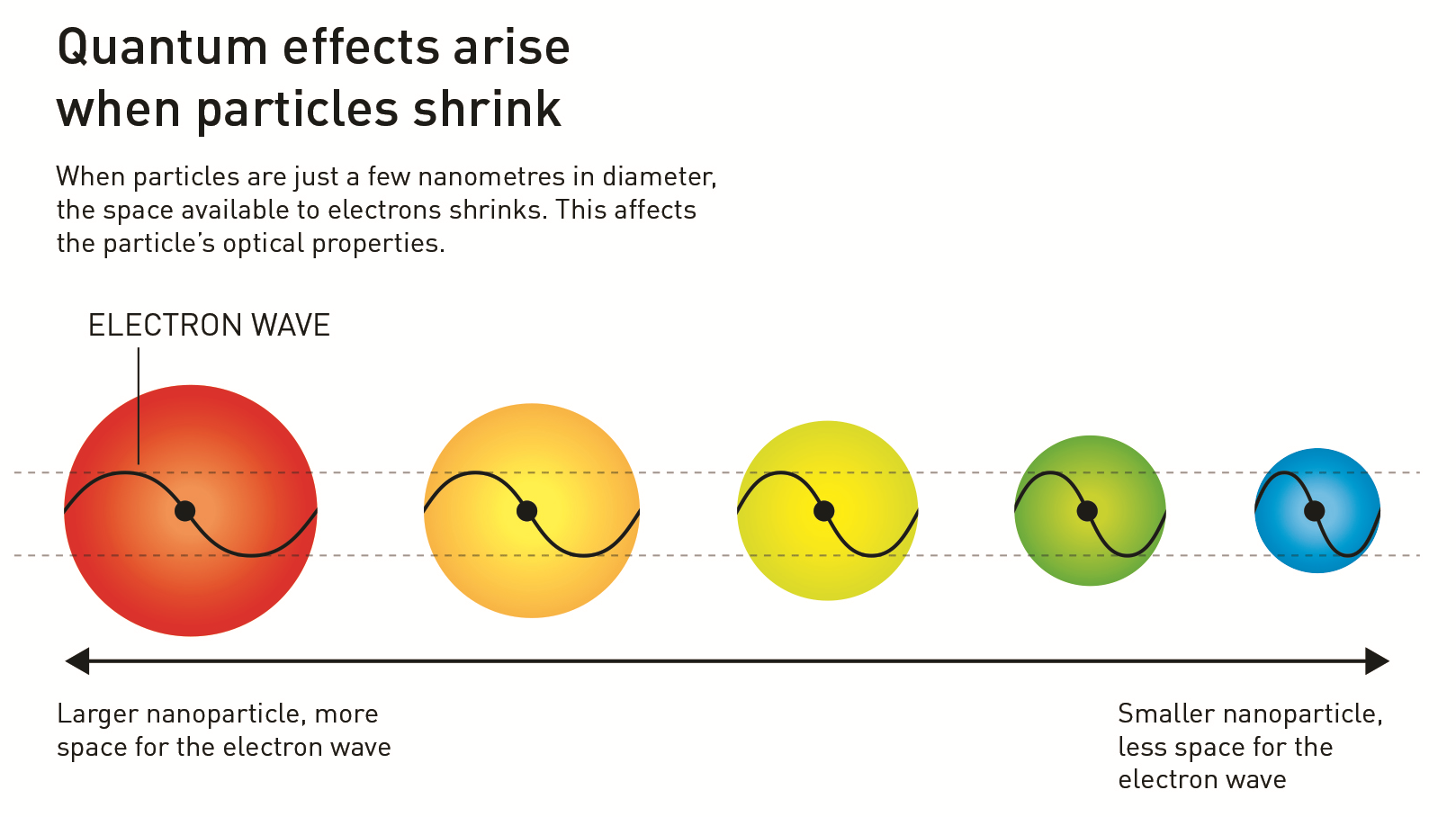
Квантовые точки (КТ) — это нанокристаллы, внутри которых в строгом порядке уложены всего от ~100 до ~10 тыс. атомов (рис. 1А) [1]. Размеры КТ в несколько нанометров соизмеримы с шириной волн элементарных частиц, например, электронов и фотонов (рис. 1Б). Из-за этого КТ меняют свойства частиц (например, длину волны) на квантовом уровне иначе, чем другие материалы. Разберем это на примере флуоресценции.
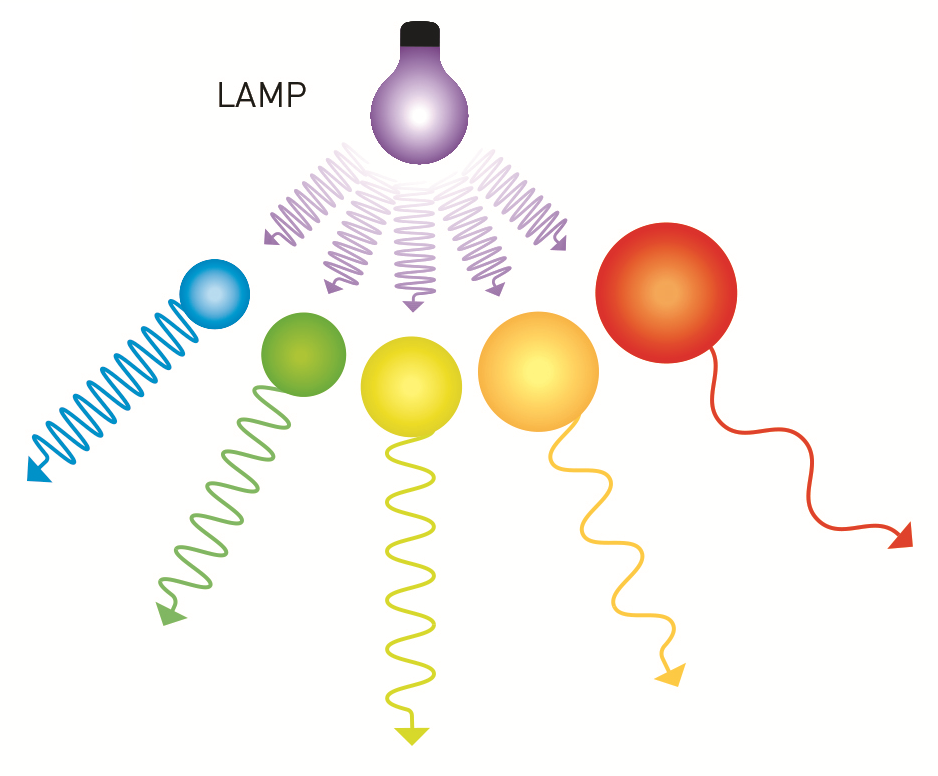
Для начала, КТ — это флуорофоры, то есть они способны поглощать энергию фотонов света и излучать их с потерей в энергии. Это свойство не уникально и используется в биологии. Например, белок GFP поглощает ультрафиолетовое излучение и испускает свет зеленого спектра. Квантовая точка из 300 атомов кадмия и селена может так же. Однако этот же материал при увеличении размера частицы работает иначе. Несколько дополнительных слоев, и КТ из 6000 атомов CdSe уже излучает красный свет в ответ на этот же ультрафиолет (рис. 1Б, 1В). Поигравшись с размером КТ, можно подтвердить прямую зависимость цвета флуоресценции от размера нанокристалла. Ясно, что белок GFP не изменит цвета флуоресценции, если взять его в 20 раз больше.
Объясняется это тем, что молекулы белка от количества не изменяются. И чтобы получить флуоресценцию нового цвета, мы будем использовать другую молекулу. В случае с КТ сам материал менять не обязательно, нужно просто увеличивать или уменьшать размер нанокристалла (рис. 1В). В этом особенность КТ: точки с разными свойствами синтезируются из одного и того же материала. А чем больше нанокристалл, тем больше энергии света он поглощает, и, соответственно, тем более красный (длинноволновый) свет испускает.
Размер КТ определяет не только оптические, но и другие физические свойства. Так, меняется их электрическая проводимость и магнитные свойства, точка плавления материала — и даже воздействие на химические реакции. Влияние размера КТ на элементарные частицы объясняется эффектом квантового ограничения, подробнее об этом — во врезке.
Написать «увеличить размер» просто, но на разработку идеи квантовых точек ушли десятки лет. Размышления о теоретической возможности создать материал с такими свойствами появились еще в 1920-ых. Но в жизнь их воплотили нынешние нобелевские лауреаты, вступившие в игру спустя полвека.
Достижения лауреатов
Алексей Екимов в 1980-х годах работал в Ленинграде над окраской стекла. В ходе работы ученый соединил медь и хлор в нанокристаллы и внедрил их в стекло. Тогда он скромно назвал их «микрокристаллами», чтобы статья прошла цензоров, не веривших в реальность такого материала; название «квантовые точки» будет присвоено позже.
Ученый точно контролировал условия синтеза и благодаря этому получил КТ разного размера. Сравнив образцы стекла, содержащие кристаллы разных размеров, он выяснил, что их цвет также различался. Тогда Алексей вместе с соавтором Александром Эфросом сделал верное предположение — связал это с квантовыми эффектами КТ, внедренных в состав стекла [3].
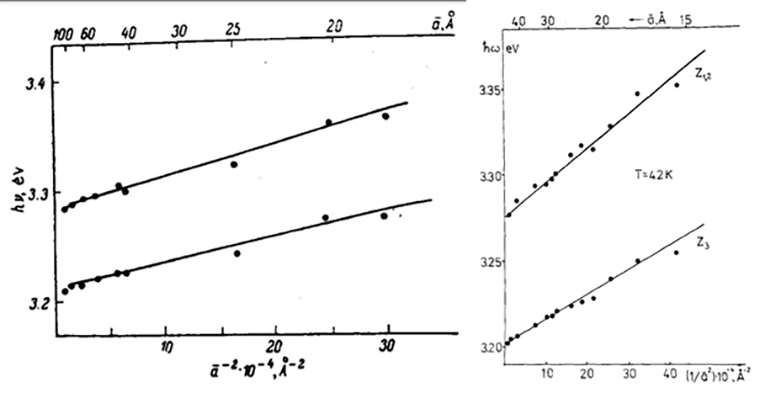
Рисунок 2. Спектр поглощенного света снижается при увеличении среднего размера нанокристаллов CuCl: графики из статей А. Екимова 1981 и 1985 гг.
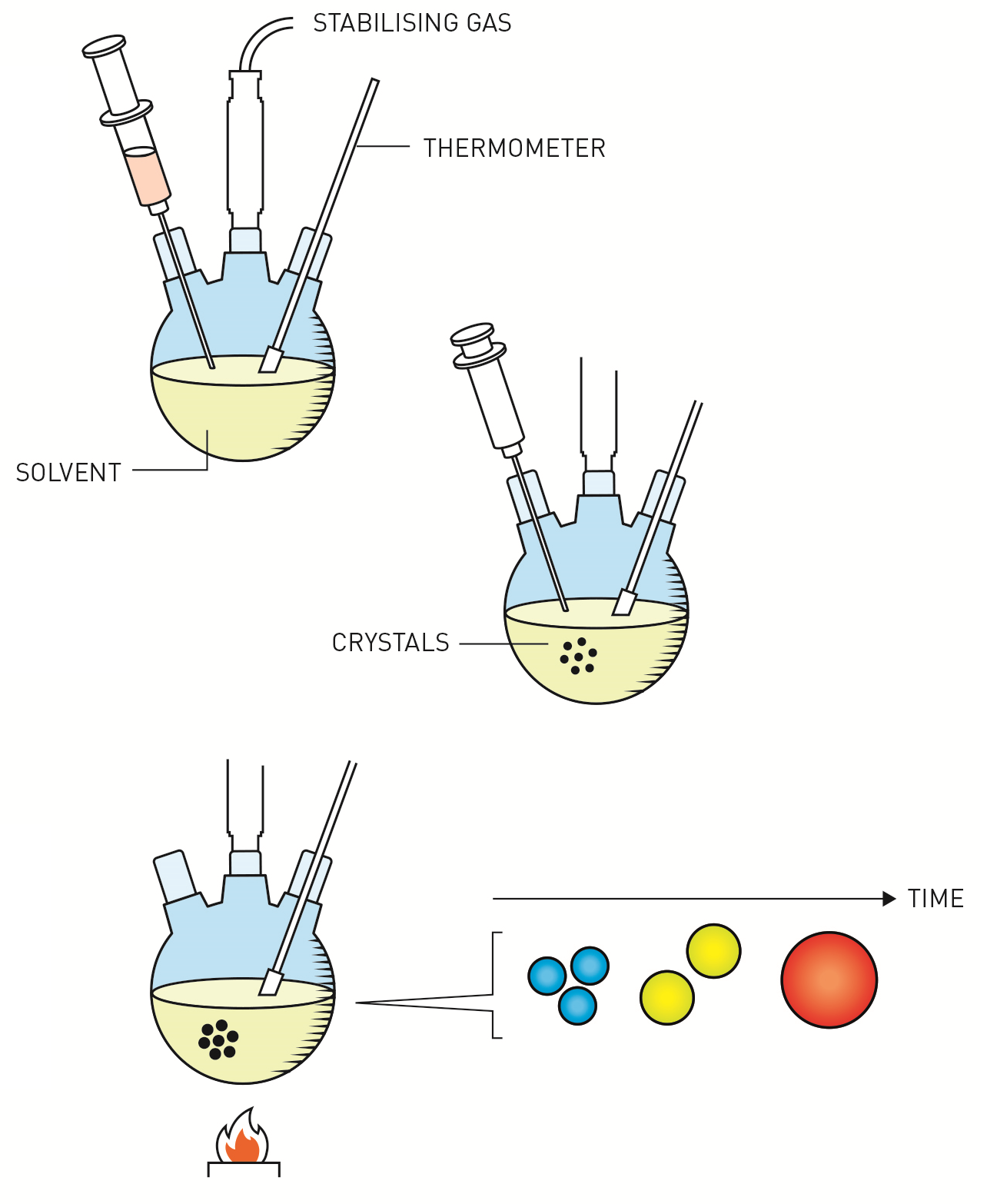
Рисунок 3. Как Монджи Бауэнди синтезировал частицы по этапам. Он запускал рост кристаллов, добавляя в подготовленный и разогретый раствор (сверху) субстрат, благодаря чему рост КТ запускался единовременно (посередине). Процесс роста нанокристаллов контролировался температурой: при ее понижении рост останавливался (внизу). Это, вкупе с раствором, который защищал поверхность частицы, помогло отладить качество синтеза.
Луис Брюс в это же время столкнулся с КТ в поисках катализаторов химических реакций, которые запускаются солнечным светом. Он вместе с коллегами синтезировал нанокристаллы сульфида кадмия (CdS), чтобы с его помощью управлять расщеплением воды на водород и кислород — и получить потенциальное топливо. Сравнив кристаллы размером 4,5 нм с кристаллами в 12,5 нм, они обнаружили, что мелкие кристаллы поглощают свет, смещенный в синюю часть спектра относительно крупных КТ. Объяснили это также квантовыми эффектами.
Монджи Бауэнди спустя десятилетие разработал метод синтеза квантовых точек, который оказался достаточно качественным и дешевым для промышленного производства. Он контролировал количество слоев атомов в частице с помощью температуры и растворителя; его подход описан на рис. 3.
Как используют квантовые точки
Квантовые точки применяют в различных сферах:
- Биологические исследования. КТ помогают точно визуализировать внутренние структуры клеток и живых организмов и процессы, протекающие внутри них. Этому мы посвятили следующую часть статьи.
- Производство дисплеев для телевизоров по технологии QLED. Они отличаются тонкостью, яркостью и точностью цветопередачи. К примеру, эту технологию активно использует компания Samsung. В последнее время КТ используют для изготовления гибких дисплеев.
- Производство солнечных батарей. КТ могут переводить энергию солнечного света в химические реакции. Среди прочего, КТ способны помочь с разработкой т.н. солнечного топлива.
- Усовершенствование LED-ламп. КТ в их составе преобразуют синий LED-свет в спектр цветов, приятных человеческому глазу.
Самые мощные фонарики: использование частиц в биологии и медицине
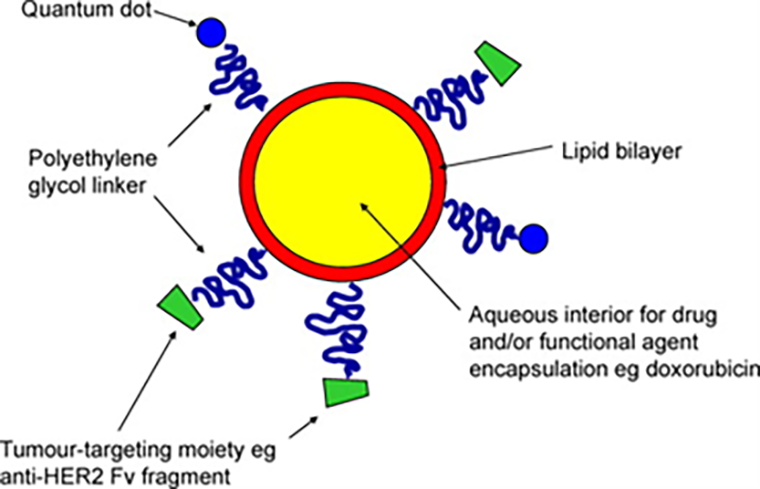
Квантовые точки нашли яркое применение в окраске живых клеток и тканей. Точнее, для окраски их элементов, интересных исследователю. Для этого КТ модифицируют, сначала покрывая защитной и гидрофильной оболочками для естественного перемещения внутри крови. Затем к КТ пришивают биологические молекулы, которые наделяют их определенными свойствами внутри организма (рис. 4). Так, можно соединить КТ с белком, который активно усваивается раковой опухолью. Тогда с помощью флуоресцентной микроскопии мы сможем наблюдать свечение заданного цвета в области опухоли. Это помогает исследователям уточнять границы образования и его размеры.
О работе разных видов микроскопии рассказано в статье «12 методов в картинках: микроскопия» [4].
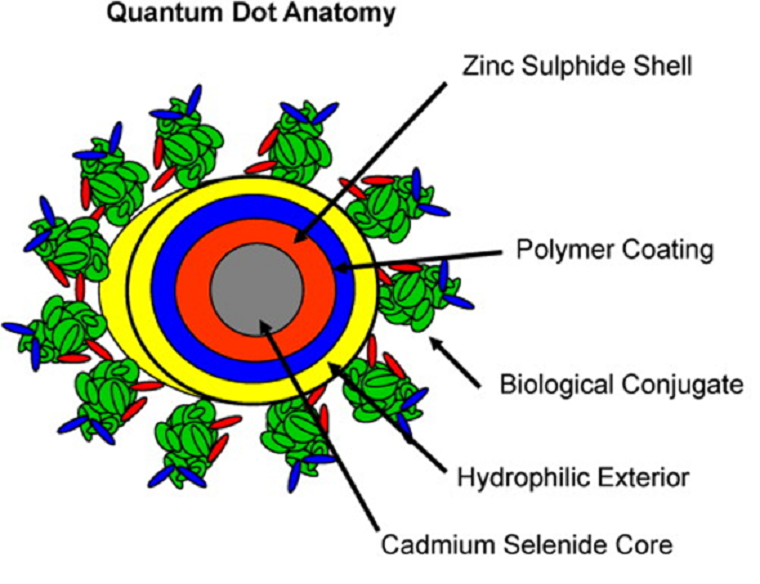
Рисунок 4. Состав КТ для биологических исследований. Ядро (серое) — КТ из атомов кадмия и селена, работает флуоресцентом. Слой снаружи от ядра (красный) — решетка из сульфида цинка, которая делает флуоресценцию ярче. Внутренний слой оболочки (фиолетовый) — сеть из полимеров, которая стабилизирует структуру. Наружный слой (желтый) — гидрофильные соединения, которые прячут гидрофобную природу КТ и позволяют перемещаться в крови. Снаружи пришиты биомолекулы (зеленые); они распознаются специфичными рецепторами внутри организма и, к примеру, остаются на поверхности целевых клеток или поглощаются ими. Все части структуры работают так, чтобы КТ воспринималась организмом естественно, «маскировала» свою природу, а в итоге — достигла биологической мишени и подсветила ее.
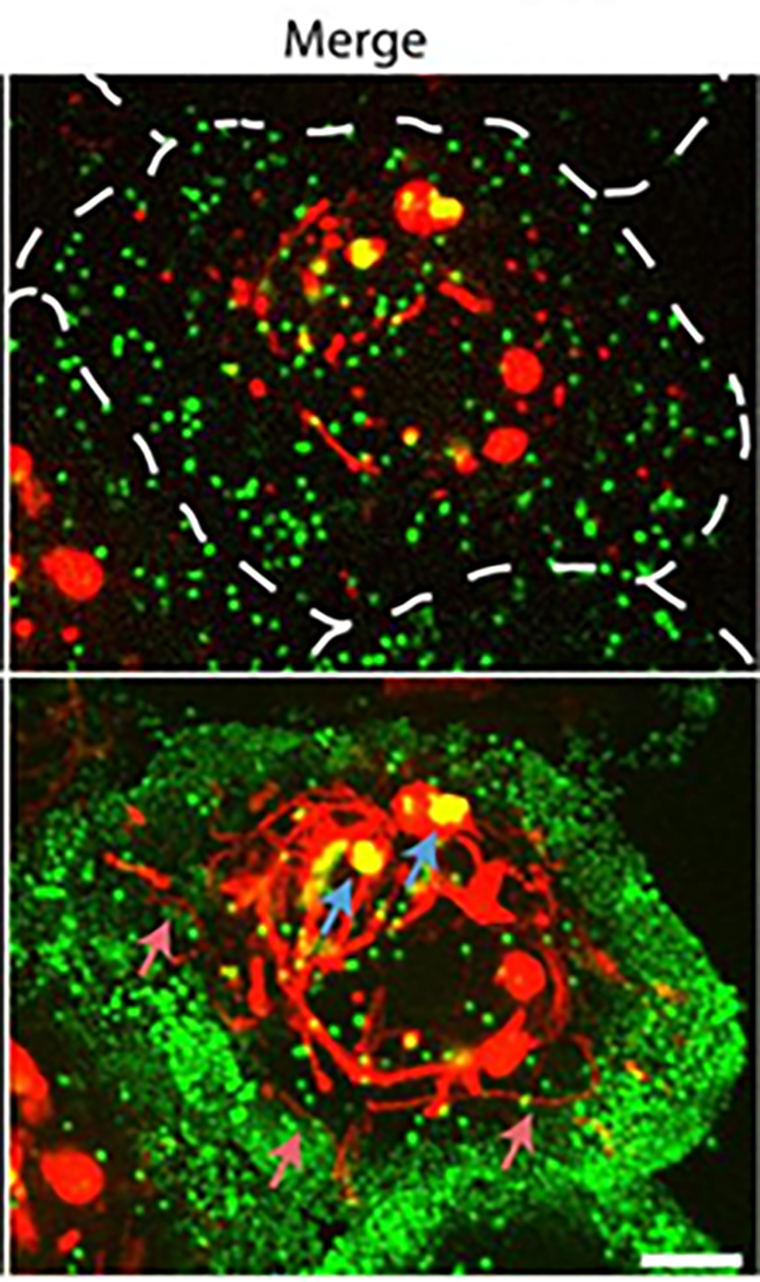
Пока что применение КТ для визуализации биологических объектов и процессов распространено только в экспериментальных условиях. Так, пришивая частицы к белкам, доставляющим лекарство к опухоли, удобно следить за их перемещениями (рис. 5А) [5]. Или можно получить четкое изображение разных частей цитоскелета или транспортных белков разными цветами внутри клетки и наблюдать, как они перестраиваются при изменении условий (рис. 5Б) [6]. Для этого достаточно «нацелить» КТ разных размеров на различные белки.
Несмотря на потенциал КТ для визуализации биологических процессов, медики опасаются применять их на пациентах. Дело в том, что токсичность КТ считается недостаточно изученной. Так что синтез КТ без тяжелых металлов в составе — важный тренд в этом направлении [7], [8]. Перспективы использования квантовых точек мы обсуждаем во следующей врезке.
Итак, Нобелевскую премию по химии вручили за претворение в реальность идеи квантовых точек. Это напоминает о том, что в науке ценно создавать то, что работает. Так, Монджи Бауэнди получил награду за обновление синтеза КТ, которое не изменило науку фундаментально, но сделало ее достижения доступными для производства.
На основе пресс-релиза Нобелевского комитета.
Литература
- Alexander L. Efros, Louis E. Brus. (2021). Nanocrystal Quantum Dots: From Discovery to Modern Development. ACS Nano. 15, 6192-6210;
- Квантовые точки — наноразмерные сенсоры для медицины и биологии;
- A.I. Ekimov, Al.L. Efros, A.A. Onushchenko. (1985). Quantum size effect in semiconductor microcrystals. Solid State Communications. 56, 921-924;
- 12 методов в картинках: микроскопия;
- Richard J. Byers, Elizabeth R. Hitchman. (2011). Quantum Dots Brighten Biological Imaging. Progress in Histochemistry and Cytochemistry. 45, 201-237;
- Emmanuel Derivery, Eline Bartolami, Stefan Matile, Marcos Gonzalez-Gaitan. (2017). Efficient Delivery of Quantum Dots into the Cytosol of Cells Using Cell-Penetrating Poly(disulfide)s. J. Am. Chem. Soc.. 139, 10172-10175;
- Na Liu, Meng Tang. (2020). Toxicity of different types of quantum dots to mammalian cells in vitro: An update review. Journal of Hazardous Materials. 399, 122606;
- Bina Gidwani, Varsha Sahu, Shiv Shankar Shukla, Ravindra Pandey, Veenu Joshi, et. al.. (2021). Quantum dots: Prospectives, toxicity, advances and applications. Journal of Drug Delivery Science and Technology. 61, 102308;
- A. Paul Alivisatos, Weiwei Gu, Carolyn Larabell. (2005). Quantum Dots as Cellular Probes. Annu. Rev. Biomed. Eng.. 7, 55-76;
- Shuming Nie, Steven R. Emory. (1997). Probing Single Molecules and Single Nanoparticles by Surface-Enhanced Raman Scattering. Science. 275, 1102-1106.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚