
«Огуречная» мечта
25 октября 2013
«Огуречная» мечта
- 2883
- 6
- 2
В чем связь между зараженным вирусом огурцом и противоопухолевым препаратом доксорубицином? Как они вместе могут стать «волшебной пулей» против онкологических заболеваний?
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Нанотехнологии постепенно проникают во все сферы человеческой жизни. Синтез нанотехнологических принципов и запросов медицины привел в конце прошлого столетия к оформлению новой науки — наномедицины. Одновременно с появлением термина «нанотехнология» медики задумались о возможности создать такой тип лекарственных препаратов, которые бы словно точечный бомбовый удар проникали в очаг заболевания и устраняли его причину. Так возникла концепция адресной доставки медицинских препаратов — поистине проблема третьего тысячелетия, — и с самого момента появления она стала ежегодно претерпевать новый виток развития. Один из таких витков произошел в начале 2013 года. И связан он, как это ни удивительно, с вирусом... мозаики огурца. Славное прошлое, интригующее настоящее, многообещающее будущее — все есть у этого вируса. О медицинской судьбе «грозы огурцов» читайте в этой статье.
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучшее новостное сообщение».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Таблетки, капсулы, инъекции — эти медицинские термины знакомы каждому из нас с детства. Однако в последнее время ситуация кардинально изменилась. Липосомы, мицеллы, дендримеры, квантовые точки, фуллерены, полимерные наноносители, нанокапсулы, нанотрубки и прочие термины с модной приставкой «нано» — вот новые инструменты врачей и фармацевтов в борьбе с опаснейшими заболеваниями (рис. 1).
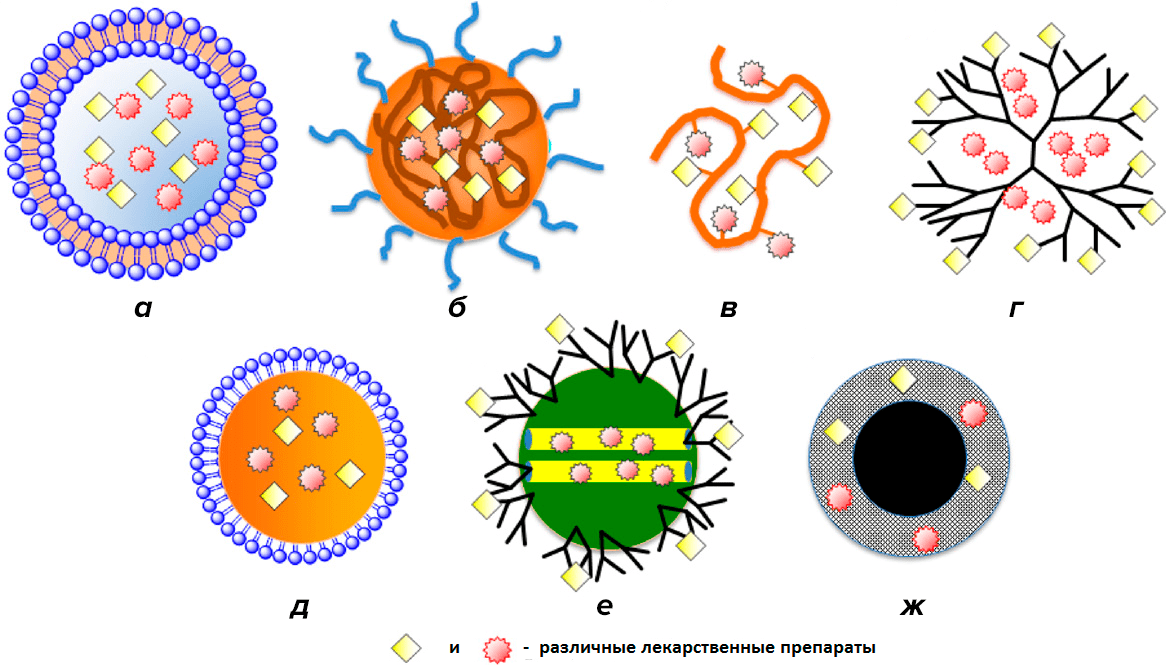
Рисунок 1. «Наноконтейнеры» — наноструктуры для доставки лекарственных препаратов. а — Липосома. б — Полимерная мицелла. в — Полимер—лекарственный конъюгат. г — Дендример. д — Масляная наноэмуслия. е — Мезопористая (поры 2–50 нм диаметром) наночастица окиси кремния. ж — Наночастица оксида железа.
Начиная со второй половины прошлого столетия фарминдустрия стала меняться на глазах: появляются новые термины и приобретают новые значения старые, расширилось понятие «лекарственная форма», нанотехнологии стали играть все бóльшую роль в производстве лекарств, изобретены «умные» лекарства. Фармацевтическая НАНОБИОМЕДтехнология — этот шедевр словотворчества является ни чем иным, как новым учебным курсом для студентов-фармацевтов в ММА им. И. М. Сеченова. После такого пропадают все сомнения о том, что новая медицина в России прижилась. Хотя сейчас речь пойдет не совсем об этом.
Пролог
«Волшебная пуля» нашего времени
Догадывался ли Пауль Эрлих, что его «волшебная пуля», словно семя, прорастет в древо под названием «направленный транспорт лекарственных препаратов»? Великий немецкий бактериолог уже в конце XIX века задумался о возможности создания препарата, который бы ликвидировал патогенные микроорганизмы и опухолевые клетки без повреждения здоровых тканей. (А задумался он об этом, вероятно, слушая оперу «Волшебный стрелок» своего великого соотечественника Карла Марии фон Вебера; рис. 2.)
Рисунок 2. Пауль Эрлих и Карл Мария фон Вебер. Говорят, что Пауль Эрлих (слева) создал концепцию «волшебной пули», слушая оперу Карла Марии фон Вебера (справа). Вот повод нам поразмыслить о волшебной силе музыки!
Мечта Эрлиха дала ростки того, что называют сейчас controlled drug delivery (контролируемая доставка лекарств), в середине 60-х годов XX века. Однажды американский онколог Джуда Фолкман (рис. 3) пропускал кроличью кровь через артериовенозный шунт марки Silastic® (особый вид силиконовой резины) и обнаружил, что если трубки шунта снаружи подвергать воздействию анестезирующих газов, то кролики засыпают. Это натолкнуло Фолкмана на идею создания герметичных капсул из материала Silastic, заполненных лекарством, которое бы с постоянной скоростью выходило из капсул в месте их имплантации [3].
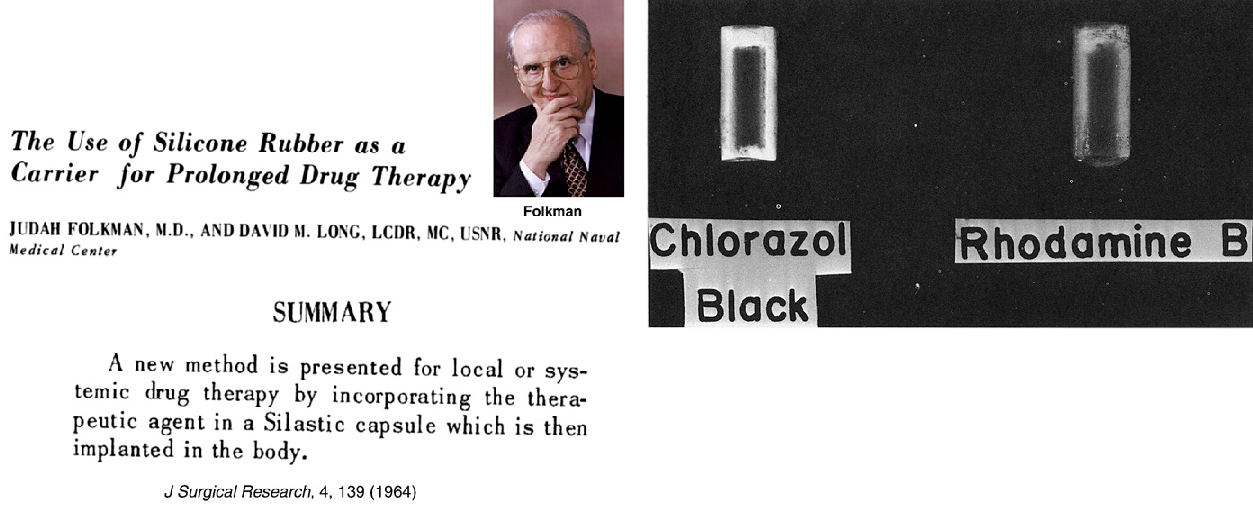
Рисунок 3. С чего все начиналось... Статья Джуды Фокмана о первой имплантируемой системе для контролируемой доставки лекарств (слева) и примеры капсул (справа), содержащих различные красители. Видно, что более высокомолекулярный краситель хлоразол черный проходит через стенки капсулы медленнее, чем родамин B, молекулярная масса которого почти вдвое меньше.
Итак, начало положено. В последующие десятилетия новая область науки буквально проскочила сразу несколько этапов в своем развитии. Дабы избежать многословности, достаточно сказать, что появление этой сферы очень удачно совпало со всемирным развитием нанотехнологий. Системы доставки лекарств, стремительно пройдя через макро и микро этапы развития, стали действительно нано уже в 1970—1980-х годах. Контейнеры для лекарств стали «наноконтейнерами» — наноразмерными переносчиками, содержащими инкапсулированное, диспергированное, адсорбированное или конъюгированное лекарственное вещество. Сформировавшаяся к тому времени концепция нанотерапии включает три пункта [3]:
- ПЭГилирование. Полиэтиленгликоль (ПЭГ) — вещество, часто используемое в качестве носителя для биоорганических молекул. Это, в частности, позволяет создавать ПЭГ-конъюгированные лекарства, формирующие в организме депо с высокой концентрацией нужного лекарства. Высокое сродство ПЭГа к воде повышает время циркуляции в организме, стабильность, растворимость и биодоступность препарата.
- «Активное нацеливание» предполагает присоединение к наноносителям «молекулярного адреса» (вектора), в качестве которого могут выступать самые разные молекулы — антитела, рецепторы, пептиды и небольшие молекулы и т.д. Причем часто упор делается на то, что здоровые и больные клетки несут на поверхности одинаковый набор молекул, но в разном количестве (разный уровень экспрессии).
- EPR-эффект (enhanced permeation and retention effect — эффект расширенной проницаемости и задержания) или «пассивное нацеливание». Дело в том, что наночастицы, многие лекарства и т.д. имеют склонность накапливаться в опухолях сильнее, чем в нормальных тканях (ученые связывают этот факт с особенностями кровоснабжения опухолей). Пассивный захват наночастиц также производится ретикуло-эндотелиальной системой (РЭС) организма, т.е. тканевыми макрофагами — клетками, осуществляющими барьерные и иммунные функции.
Эврика! Ключ к борьбе с опухолями найден! Но (всегда есть «но») не стоит забывать: противоопухолевые препараты стремятся инкапсулировать не случайно. Зачастую они в свободной форме могут нести вред здоровым клеткам организма вследствие своей высокой цитотоксичности. Следовательно, наноконтейнер с лекарством является своеобразной бомбой замедленного действия, т.к. «взрыв» должен произойти не где-нибудь по дороге, а внутри опухолевой клетки. Разумеется, эта проблема решаема. Однако если бы имеющиеся способы ее решения не имели явных изъянов, то все бы уже давно перестали волноваться. Судите сами [4]:
- При выборе в качестве нацеливающих молекул моноклональных антител [5] эффективность часто выше, чем при использовании более естественных векторов, но опухоли имеют на этот случай свой туз в рукаве. Вернее не в рукаве, а на цитоплазматической мембране — набор рецепторов на поверхности каждой опухолевой клетки уникален, и далеко не факт, что антитело найдет себе рецептор «по вкусу». В результате — промах.
- Липосома — казалось бы, проверенная временем система, — и та имеет проблемы (хотя решаемые): быстрая деградация, малый объем; липосомы могут блокировать легочные капилляры, повышать уровень глюкозы в крови, нарушать свертываемость крови и обмен холестерина.
- Относительно недавно стали применять в качестве контейнеров классические наноразмерные объекты: фуллерены и углеродные нанотрубки. С одной стороны, они высоко реакционноспособны, но с другой — без модификации они нерастворимы в воде. К тому же есть вероятность токсичности углеродных наночастиц.
- Наконец, еще одно нововведение — квантовые точки [6] — заряженные наночастицы проводника/полупроводника, флуоресцирующие в определенном спектральном диапазоне. Их также в последнее время «облепляют» лекарствами. Но, увы, металлы, входящие в состав квантовых точек, токсичны.
Все это заставляет ученых искать все более хитрые способы доставки лекарств прямо по адресу, в целости и сохранности. В частности, делается упор не столько на синтетические контейнеры, столько на природные. Вот и в нынешнем году ученые в очередной раз пошли по этому пути.
Часть первая
В игру вступают...
Вирусы!.. У автора этих строк в последнее время возникает ощущение, что скоро без этих — не побоюсь сказать — наносуществ не будет обходиться ни одна область современной науки.
По многочисленным статьям и обзорам на тему вирусных нанотехнологий становится ясна вся важность вирусов как технологических инструментов нового поколения [7]. Преимущества вирусной системы скоро будут понятны читателям при рассмотрении конкретного примера (о котором, собственно, эта статья).
Восточная медицина
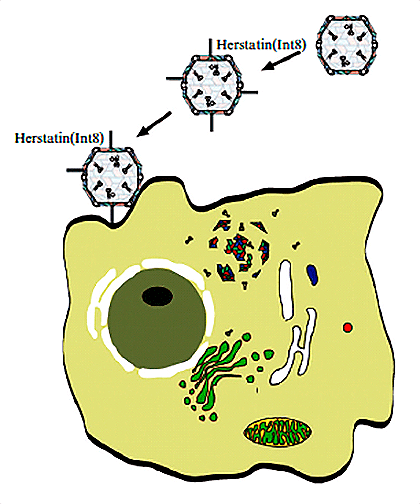
Рисунок 4. CPMV в терапии. Лекарство помещается внутрь капсида, к поверхности которого пришивается лиганд — молекула, взаимодействующая с рецептором (в данном случае это белок Herstatin или рецептор-связывающий домен, кодируемый интроном 8). При взаимодействии лиганд–рецептор происходит эндоцитоз вируса и последующее высвобождение лекарства при деградации вируса в цитоплазме.
Вообще, вирусы в фарминдустрии сравнительно недавно. Их капсиды достаточно удобно использовать в качестве наноконтейнеров, однако прежде чем загружать лекарство внутрь, капсид нужно специальным образом подготовить. Сначала нужно получить пустые капсиды нужного размера, а потом модифицировать их лигандами к необходимым клеточным рецепторам. Вот пример: вирус мозаики вигны (Cowpea mosaic virus, CPMV). Лишь в начале XXI века результаты исследований по направленной доставке этого вируса к клеткам позволили говорить о чем-то фармацевтическом. Например, в 2004 году было достигнуто взаимодействие CPMV с рецепторами клеток млекопитающих in vitro («в пробирке»), а в 2006 году доказана возможность образования пустых вирионов CPMV как в природе, так и в пробирке. Эти достижения проложили путь к новой таргетной терапии (рис. 4) [8].
А недавно, весной 2013 года, китайские ученые из Южного Медицинского Университета открыли новую страницу романа под названием «Drug Delivery» [9]. Китайский рецепт прост: взяли вирус мозаики огурца, противоопухолевый препарат доксорубицин, смешали и — voilà... на следующий день получили готовую систему вирус—лекарство. Восток — дело тонкое!
Пару слов о главных героях. Вирус мозаики огурца (Cucumber mosaic virus, CMV) — 29-нанометровый икосаэдрический вирус семейства Bromoviridae, геном которого представлен тремя одноцепочечными РНК с положительной полярностью (обладает свойствами информационной РНК), каждая из которых окружена своей белковой оболочкой (рис. 5). CMV — классический пример вируса с икосаэдрической симметрией, состоящий из пентонов и гексонов [7]. Пентамерные и гексамерные капсомеры формируют отверстия (поры), и в итоге белковая оболочка вируса пронизана сквозными каналами. Это не мешает вирусу нормально существовать, а исследователям эта пористость только на руку!
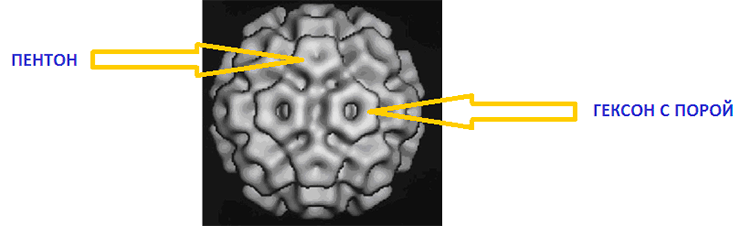
Рисунок 5. Электронная микрофотография вируса мозаики огурца. Стрелками отмечены пентоны и гексоны.
Доксорубицин (Dox) представляет собой широко применяемый антибиотик антрациклиновой группы (структурно близкие антибиотики, преимущественно блокирующие синтез ДНК; рис. 6). Dox известен с конца 60-х годов прошлого века и применяется при лечении самых разных опухолей. Как и у прочих антрациклиновых антибиотиков, основной механизм его действия сводится к интеркаляции (встраиванию) молекул между цепями ДНК.
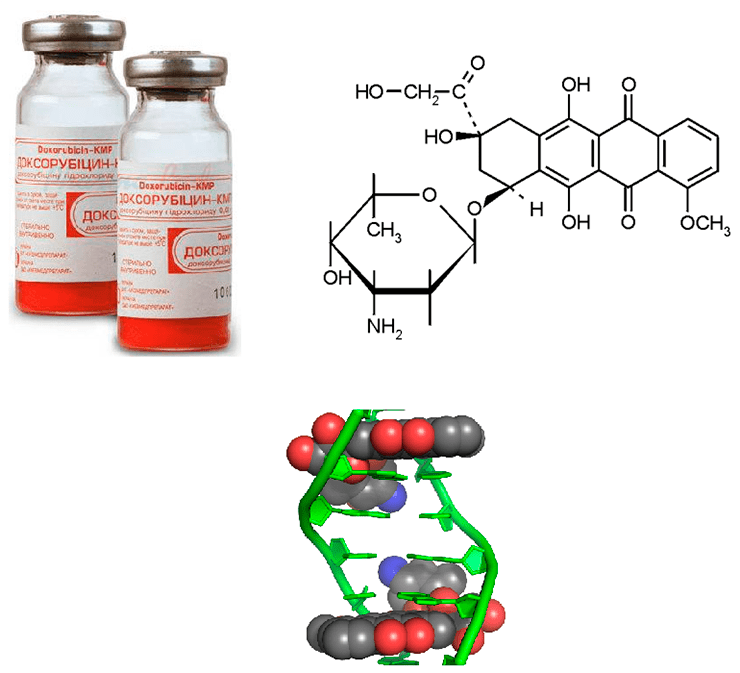
Рисунок 6. Доксорубицин. Слева — Раствор для инъекций. Справа — химическая формула препарата. Внизу — принцип его действия.
Какое лекарство не имеет побочного эффекта! Вот и у нашего героя он имеется. И какой! Высокая кардиотоксичность. Дилатационная кардиомиопатия, застойная сердечная недостаточность, аритмия, общее нарушение самочувствия, аллергические реакции — и это неполный список возможных последствий с неприятными названиями. Теперь понятна важность введения инкапсулированного доксорубицина.
Прежде, чем перейти непосредственно к тому, что сделали ученые, необходимо оговориться, что вирус мозаики огурца — новичок в деле доставки лекарств. Чего не скажешь о доксорубицине. Он уже «засветился» в статье сингапурских ученых (которая имеет ряд сходств с работой китайцев), засунувших его в пустой вирус хлоротической кольцевой пятнистости гибискуса (как поэтично!) [11]. Умно, но придумка из КНР не хуже!
«Троянский конь» для опухоли
Вирус ведет себя как слепой в организме человека (благо хоть не разрушается при физиологическом pH)! В принципе, возможна доставка вируса благодаря EPR-эффекту: для этого есть все предпосылки — большой биоконъюгат и опухолевая ткань. Но стóит помнить про макрофаги, которые не прочь полакомиться наночастицами во благо организма. Поэтому для увеличения вероятности попадания препарата в опухоль ученые применили принцип «активного нацеливания», а в качестве «прицела» выбрали классическую в онкологии молекулу фолиевой кислоты (folic acid, FA; рис. 7). Причина — повышенный уровень экспрессии рецептора фолиевой кислоты (folic acid receptor, FR) на опухолевых клетках в сравнении со здоровыми клетками. Таким образом, фолиевая кислота взаимодействует со своим рецептором, вызывая так называемый «рецептор-опосредованный эндоцитоз» [12] вируса (проще говоря, его поглощение клеткой). Примечательно, что клетки, на которые ученые нацелили свое новое оружие, отличаются еще и тем, что на них рецептора FR очень много — это культура опухолевых клеток OVCAR-3 (клетки рака яичника человека).
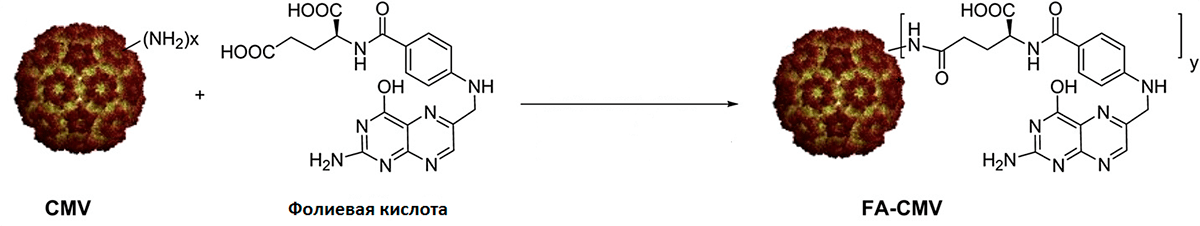
Рисунок 7. Конъюгация CMV и фолиевой кислоты посредством образования классической амидной связи.
О возможности доксорубицина связываться с ДНК уже было упомянуто. Но и с РНК вируса он тоже взаимодействует: как посредством электростатического притяжения (положительно заряженного доксорубицина и отрицательно заряженной РНК), так и за счет интеркаляции в двуцепочечные участки РНК вируса мозаики огурца (рис. 8). «Загрузка» доксорубицина в капсид осуществляется через те самые поры, которые так хорошо видны на электронных микрофотографиях на рисунке 5.
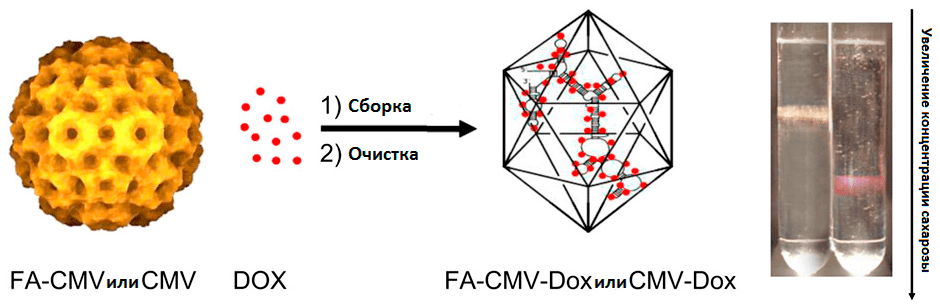
Рисунок 8. «Загрузка» вирусных частиц доксорубицином. Успешность загрузки можно подтвердить центрифугированием в градиенте сахарозы (справа). При этом в центрифужную пробирку сначала наливают раствор с градиентом концентрации сахарозы (5–35%), а затем добавляют объект, плотность которого надо прикинуть. В итоге более плотные частицы будут находиться в зоне с большей концентрацией сахарозы: профили распределения CMV (левая пробирка) и комплекса FA—CMV—Dox (правая пробирка) подтверждают успешную загрузку.
Часть вторая
И волки сыты, и овцы целы
Опухолевым клеткам явно не по себе от доксорубицина. К клеткам OVCAR-3 добавили просто доксорубицин, CMV—Dox, FA—CMV—Dox или FA—CMV—Dox + f (f означает добавку свободной фолиевой кислоты). Как и следовало ожидать, поглощение клетками лекарства максимально в случае FA—CMV—Dox. И это естественно: без фолиевого «навигатора» вирусу так же сложно проникнуть в клетку, как если к комплексу FA—CMV—Dox добавить фолиевую кислоту, которая свяжется с рецептором и инактивирует препарат. Случай со свободной FA в науке называется контролем и подтверждает возможность рецептор-опосредованного эндоцитоза.
Ну а дальше дело техники: достаточно посмотреть в микроскоп на окрашенные специальным образом клетки и убедиться, что наиболее интенсивное свечение ядра и цитоплазмы наблюдается в клетках с конструкцией FA—CMV—Dox (рис. 9а). Выраженность действия доксорубицина можно оценить по количеству апоптотических опухолевых клеток (апоптоз — вариант запрограммированной клеточной гибели). В результате, под световым микроскопом видно, что происходит после обработки клеток доксорубицином в составе вируса, еще и с фолиевой кислотой на поверхности (рис. 9).
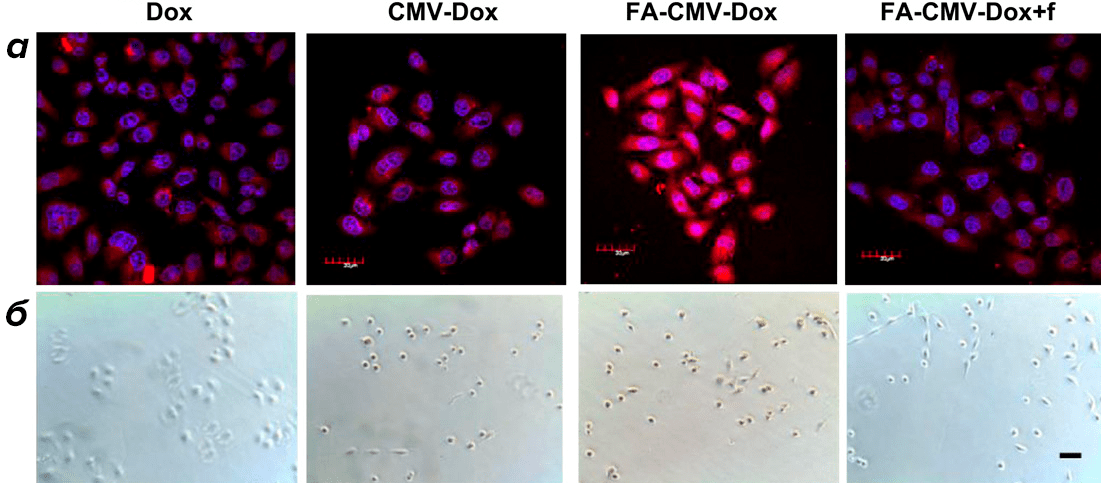
Рисунок 9. Визуализация действия разных форм доксорубицина на клетки OVCAR-3. а — Клетки OVCAR-3, инкубированные с различными лекарственными формами доксорубицина (ядра клеток окрашены синим красителем DAPI, который вместе с красной флуоресценцией доксорубицина дает фиолетовый цвет). б — результаты, полученные методом TUNEL (данные световой микроскопии) с использованием биотинилированных дУТФ (биотин — витамин, который используется во флуоресцентных методах).
А что видно на гистологическом уровне? Для ответа на этот вопрос на помощь пришли лабораторные мыши. Но не обычные, а голые бестимусные, у которых в результате мутации отсутствует или поврежден тимус, а вместе с ним и иммунная система (рис. 10). Для иммунологии такие мыши являются очень важным модельным объектом (в частности, для изучения онкологических заболеваний). Затем китайские исследователи применили методику ксенотрансплантации.

Рисунок 10. Бестимусная голая мышь линии BALB/c (одна из старейших инбредных линий белых лабораторных мышей). (Инбредный — происходящий от скрещивания родственных особей).
Свободный доксорубицин вызывает расширение всех камер сердца, появление пристеночных тромбов, разрозненность кардиомиоцитов и т.п. При использовании достижений направленной доставки лекарств опухоли теряли характерный дольчатый вид и приобретали EPR-повреждения (рис. 11). И опухоль побеждена!
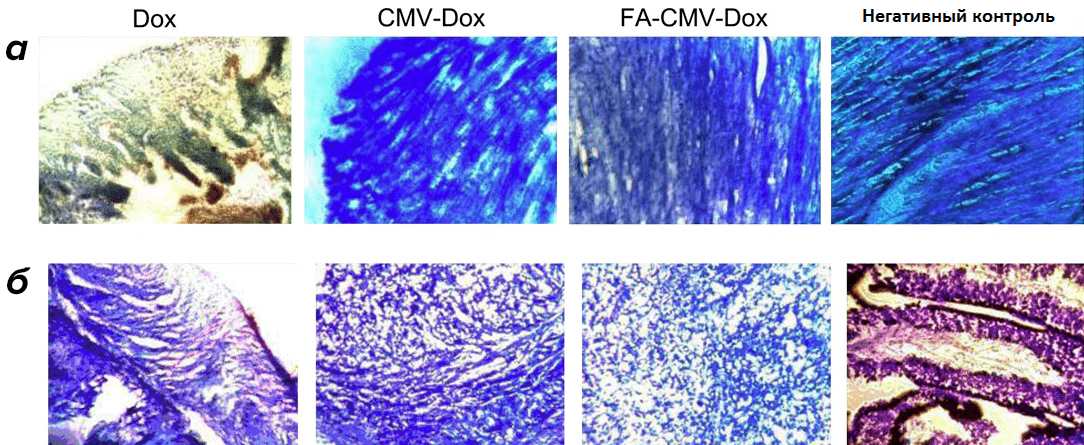
Рисунок 11. Срезы сердечной (а) и опухолевой (б) тканей. Видно, что в случае терапии комплексом FA—CMV—Dox опухоль теряет свой исходный вид, а ткань сердца при этом сохраняет здоровый облик (она компактнее, чем при обработке свободным доксорубицином, и кардиомиоциты не разрушены).
На десерт...
А как же доксорубицин попадает в клетки опухоли, спросите вы? Помощь в освобождении доксорубицина от цепей РНК оказывает сама опухоль! Все благодаря высокой активности в ней ферментов, расщепляющих РНК, — РНКаз. Есть данные о том, что это связано с повышением содержания эозинофилов (вид лейкоцитов) в крови — эозинофилии — при различных видах онкологических заболеваний. В этом случае эозинофилы активно продуцируют эозинофильный нейротоксин, по своей природе являющийся РНКазой, с активностью в 1000 раз больше, чем у ее родственниц. К слову, рак яичников, фигурирующий в этой работе, сопровождается эозинофилией. Прибавьте к этому высокую чувствительность CMV к РНКазам и пористость его капсида. И представьте, насколько это мощная штука!
Часть третья
Автор данной статьи надеется, что убедил читателей в том, что у вирусных капсидов есть явные преимущества перед синтетическими средствами доставки лекарств и других терапевтических агентов. Легкость в приготовлении, узкий диапазон размеров и форм частиц, способность к пассивному и активному нацеливанию, высокая стабильность и точность высвобождения активного агента — вот основные преимущества оболочек вирусов. Следует добавить, что инертность капсидов в физиологических условиях организма позволяет лекарственному средству выходить из капсида без внешнего контроля. Хотя регулирование физических параметров (таких как pH, ионный состав среды, температура и т.п.) позволяет осуществить более точную доставку лекарства, чаще к этому прибегают в случае синтетических наноконтейнеров, нежели биогенных.
Ретроспектива
Успехи настоящего заставляют задуматься о прошлом. В 2007 году группа японских биологов показала возможность использования CMV для наработки в растении большого количества терапевтического белка — кислого фактора роста фибробластов (aFGF) (участвует в делении и дифференцировке различных клеток, формировании кровеносных сосудов и эмбриональном развитии) [13]. Для этой цели был создан вирусный вектор — генетическая конструкция на основе вирусного генома для переноса в растительную клетку чужеродной генетической информации с последующим синтезом соответствующего белка, — в который вставили ген aFGF. После ряда манипуляций выбранное растение становится фабрикой по производству терапевтически важного белка.
Вспоминая работу сингапурских ученых, следует отметить, что она действительно во многом схожа с китайской работой: то же лекарство (доксорубицин), та же «инкрустация» капсида (фолиевой кислотой), те же раковые клетки (OVCAR-3). Но их китайские коллеги явно улучшили данную методику. Во-первых, вирус хлоротической кольцевой пятнистости гибискуса не такой пористый, что уменьшает его «грузоемкость». А во-вторых, РНК вируса не участвует, и доксорубицин помещается в пустой капсид. Но это никого не смущало, поскольку лекарство связали с полистиролсульфоновой кислотой, которая придает доксорубицину и больший размер, и суммарный отрицательный заряд. Вариант отличный, хотя эта кислота не очень безопасна. Китайский препарат более биологичен.
В статье американских ученых из Корнелльского университета 2012 года рассказывается о различных манипуляциях с вирусподобными частицами (ВПЧ) CMV, собранными из белка оболочки и нуклеиновой кислоты в комплексе с другими молекулами [14]. В том числе доказана возможность упаковки в капсид флуоресцирующего красителя. Внутри ВПЧ была проведена целая реакция: ДНК конъюгировали с белком биотином, а с флуорохромом — стрептавидин. Приготовленный комплекс ДНК —биотин—стрептавидин —флуорохром добавили к белку оболочки вируса и изучили свойства полученных ВПЧ. Работает! За этим открытием явно большое будущее, но об этом ниже. Вирус огуречной мозаики явно начинает все сильнее интересовать ученых разных специальностей, хотя работ до сих пор немного. И дает повод помечтать...
Эпилог, или взгляд в будущее
Методические наработки китайских ученых можно использовать при лечении других заболеваний. Ну, для начала, конечно, других видов онкозаболеваний. Для этого у вирусного наноконтейнера есть достаточно приспособлений — фолиевая кислота, доксорубицин, опухолевые РНКазы. Говоря об РНКазах, стоит заметить, что в таких органах, как поджелудочная железа, селезенка, легкие и печень, концентрациях этих ферментов сравнительно высока. И это можно использовать для лечения заболеваний этих органов, прикрепив соответствующие «молекулярные адреса» и присоединив к РНК нужный лекарственный агент (при опухолях в этих органах содержание РНКаз увеличивается, и тогда можно легко применять антрациклиновые антибиотики). Фолиевая кислота, разумеется, направляет в опухоль капсулу, однако наведение можно также обеспечить, обработав ее полиэтиленгликолем, маскирующим «волшебную пулю» от макрофагов («стэлс-вирус»). Касательно пор — через них можно закачать в полость капсида довольно большой спектр соединений, в т.ч. и наночастиц. Эксперимент по упаковке флуоресцентного красителя в CMV подтверждает возможность использовать этот вирус для дешевой визуализации физиологических процессов, органов и тканей in vivo. Остается убедить медиков...
Нанолекарства — это будущее фармацевтической отрасли, но в нашей стране они пока не очень активно выходят из лабораторий в клиники. Но разработок много, и это не может не радовать! Остается надеяться, что, глядя на успехи западных лабораторий, отечественные любители всего «экологически чистого» захотят лечиться не химиотерапией, а более биологичными способами, — в частности препаратами на основе фитовирусов, которыми российские биологи успешно занимаются в связи с потребностями сельского хозяйства. И пусть жители всего мира перестанут падать в обморок при любом упоминании слова «вирусы», ибо с ними давно пора подружиться!
Литература
- Che-Ming Jack Hu, Liangfang Zhang. (2012). Nanoparticle-based combination therapy toward overcoming drug resistance in cancer. Biochemical Pharmacology. 83, 1104-1111;
- Allan S. Hoffman. (2008). The origins and evolution of “controlled” drug delivery systems. Journal of Controlled Release. 132, 153-163;
- Judah Folkman, David M. Long. (1964). The use of silicone rubber as a carrier for prolonged drug therapy. Journal of Surgical Research. 4, 139-142;
- Ивонин А. Г., Пименов Е. В., Оборин В. А., Девришов Д. А., Копылов С. Н. (2012). Направленный транспорт лекарственных препаратов: современное состояние вопроса и перспективы. «Известия Коми НЦ УрО РАН». 9, 46–55;
- Моноклональные антитела;
- Квантовые точки — наноразмерные сенсоры для медицины и биологии;
- Вирусы-платформы: яд во благо;
- N. F. Steinmetz, T. Lin, G. P. Lomonossoff, J. E. Johnson. (2009). Structure-Based Engineering of an Icosahedral Virus for Nanomedicine and Nanotechnology. Viruses and Nanotechnology. 23-58;
- Qingbing Zeng, Hanbin Wen, Qing Wen, Xiaohui Chen, Yuegang Wang, et. al.. (2013). Cucumber mosaic virus as drug delivery vehicle for doxorubicin. Biomaterials. 34, 4632-4642;
- William R. Wikoff, Chao Jo Tsai, Guoji Wang, Timothy S. Baker, John E. Johnson. (1997). The Structure of Cucumber Mosaic Virus: Cryoelectron Microscopy, X-Ray Crystallography, and Sequence Analysis. Virology. 232, 91-97;
- Yupeng Ren, Sek Man Wong, Lee-Yong Lim. (2007). Folic Acid-Conjugated Protein Cages of a Plant Virus: A Novel Delivery Platform for Doxorubicin. Bioconjugate Chem.. 18, 836-843;
- Доставка лекарственных препаратов на основе рецептор-опосредованного эндоцитоза;
- Kouki Matsuo, Jin- Sung Hong, Noriko Tabayashi, Akira Ito, Chikara Masuta, Takeshi Matsumura. (2006). Development of Cucumber mosaic virus as a vector modifiable for different host species to produce therapeutic proteins. Planta. 225, 277-286;
- X. Lu, J. R. Thompson, K. L. Perry. (2012). Encapsidation of DNA, a protein and a fluorophore into virus-like particles by the capsid protein of cucumber mosaic virus. Journal of General Virology. 93, 1120-1126.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





