Опухоли мозга как болезни нейронных сетей
23 марта 2026
Опухоли мозга как болезни нейронных сетей
- 177
- 0
- 1
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Опухоль мозга — это не просто некое чужеродное для организма анатомическое образование. Такие опухоли тесно связаны с процессами с процессами, протекающими в нервной ткани. В этом тексте я предлагаю посмотреть на мозговые опухоли в трех приближениях. Сначала — на уровне одной спирали ДНК, где может происходить мутация в гистоне H3 или серотонилирование гистона. Потом — на уровне взаимодействия нейронов и опухоли: как сами нейроны могут ускорять или замедлять рост опухолевых клеток, а белок тромбоспондин-1 интегрирует глиобластомы в нейронную сеть. И наконец — на уровне ткани: как миелин, обеспечивающий быструю работу мозга, используется опухолью в качестве источника энергии и средства защиты.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Мутантный гистон как причина
Диффузная внутримостовая глиома у детей — агрессивная опухоль ствола мозга, которую нельзя радикально удалить из-за ее расположения, а химио- и лучевая терапия недостаточно эффективны.
В клетках глиомы есть генетическая особенность, являющаяся причиной возникновения опухоли — мутация гена одного из белков-гистонов [1]. Роль гистонов в клетках объясняется следующим. Если бы мы вытянули молекулу ДНК, которая содержится в любой нашей клетке, в виде прямой линии — получившаяся нить была бы длиной в человеческий рост. Сложить, упаковать эту нить ДНК в компактном виде в клетке довольно сложно. На одном из уровней компактизации (упаковки) природа использует нуклеосомы — структурные единицы, в которые упакована нить ДНК. На нуклеосому «наматывается» ДНК, как нитка на катушку. Каждая нуклеосома состоит из нескольких белков-гистонов — H2А, H2B, H3 и H4.
Нуклеосомы во внутримостовой глиоме несут одну очень специфическую поломку — мутацию с заменой лизина-27 (K27) на метионин (M) в гистоне H3 (H3K27M). Информация о правильном строении гистона содержится в ДНК, и, если эта информация изменена (а именно это и происходит в случае мутации при глиоме), клетка не может создавать правильный белок, и каждый гистон образуется с поломкой. Таких гистонов для намотки ДНК нужно очень много, поэтому в клетках ломается вся система компактизации. Формально это поломка всего одного гена, но из-за того, что кодируемый им гистон содержится в миллионах нуклеосом по всему геному, сразу нарушается вся система упаковки ДНК.
В нормальном гистоне H3 на аминокислотный остаток лизина специальный фермент вешает метку — метильную группу. Она обозначает, что участок ДНК, намотанный на этот гистон, надо пропускать, он не несет важной для клетки информации. Так клетка выключает целые блоки генов (например, эмбриональные программы, которые взрослой клетке не нужны). В случае мутации H3K27M лизин меняется на метионин. Казалось бы, всего один аминокислотный остаток. Но теперь на гистон нельзя повесить ту же метку — она может присоединяться только к остатку лизина-27. В итоге на многих участках генома исчезает метка, информация начинает читаться со всей «нечитаемой» раньше ДНК. ДНК все еще намотана на нуклеосомы, но ярлыки «выключено» исчезли. В такой ситуации клетка может создавать белки, характерные для эмбриональных клеток, и которые не должны работать во взрослой клетке, т.к. они необходимы для активного деления. Размывается информация про дифференцировку клеток (рис. 1).
Клетка оказывается в странном состоянии: это уже не нормальная взрослая клетка, но и не нормальный эмбриональный предшественник. Получается, что процессы деления оказываются нарушенными, и клетка легко может превратиться в раковую. Мутация увеличивает вероятность превращения клетки в раковую во много раз, а в клетках опухоли поддерживает аномальное функционирование клетки.
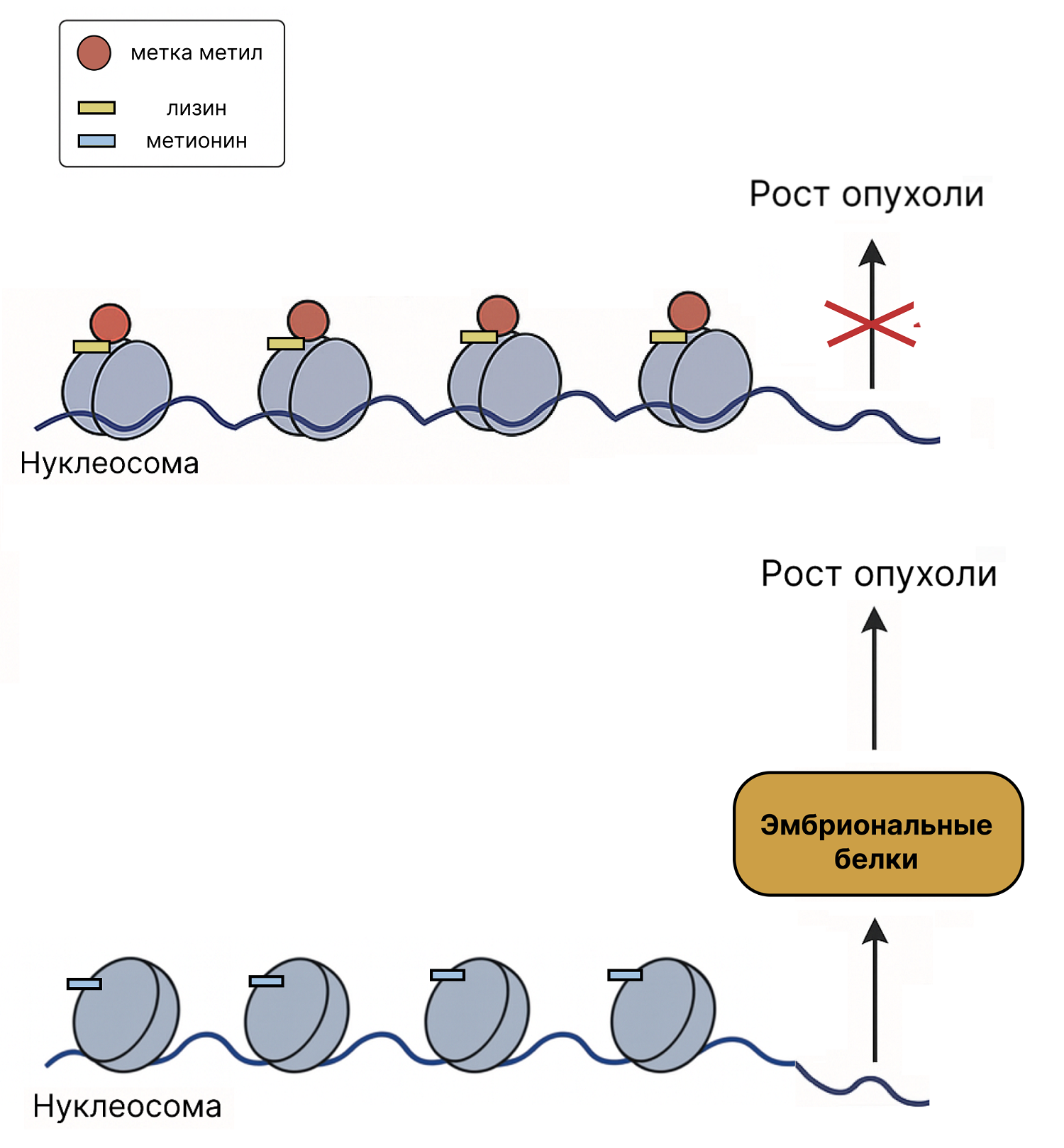
Рисунок 1. В норме к лизину в гистоне H3 присоединяется метильная метка — этот сигнал «выключает» целые блоки генов. При мутации H3K27M лизин заменен на метионин, метка больше не ставится, и многие участки генома перестают быть «выключенными». Клетка начинает активировать эмбриональные и пролиферативные программы, теряет признаки дифференцировки и переходит в состояние, способствующее опухолевому росту.
рисунок автора, выполнен с использованием ChatGPT
Серотонин как «мейкап» на гистонах: эпендимома, ETV5 и NPY
Эпендимома — преимущественно детская опухоль мозга. В ткани мозга она существует не сама по себе, а в плотном нейронно-глиальном окружении.
Ключевую роль в ее развитии на молекулярном уровне, как и в случае с диффузной внутримозговой глиомой, играют гистоны. В эпендимоме вместо мутации решающим событием становится серотонилирование гистонов [2]: молекула серотонина ковалентно присоединяется к гистону, меняя то, какие гены и с какой интенсивностью считываются.
Серотонин вырабатывается серотонинергическими нейронами. Высвободившийся из нейронов серотонин воздействует на опухолевые клетки эпендимомы. Обычно серотонин работает как нейромедиатор, то есть вещество, обеспечивающее передачу сигнала между нейронами. В эпендимоме же серотонин важен не только как нейромедиатор, но и как внутриклеточная молекула. Опухолевые клетки активно захватывают серотонин из микроокружения с помощью белка-переносчика SLC6A4. Этот переносчик есть и в неопухолевых клетках, однако в клетках опухоли его экспрессия значительно возрастет. Из-за этого внутриклеточный пул серотонина становится выше. После проникновения серотонина в клетеку происходит присоединение его к гистону H3 (серотонилирование) при участии фермента TGM2. Серотониновая метка в разы увеличивает работу активных генов и помогает поддерживать опухолевую программу роста. В нормальных клетках подобная модификация тоже может возникать, но она гораздо слабее и не становится критически необходимой для выживания. Так, серотонилирование оказывается принципиально необходимым для опухолевого роста: когда при фармакологической блокаде серотонин не присоединяется к гистону, рост эпендимомы резко тормозится, фактически блокируется [2]. Одновременно меняется экспрессия транскрипционных факторов развития — белков, которые определяют «программу» клетки: насколько она незрелая, способна делиться, склонна к агрессивному росту. Без этой модификации гистонов опухолевые клетки не могут поддерживать нужный им режим развития, и опухоль не формируется. Это объясняет, почему серотонилирование важно для функционирования самой опухолевой клетки.
Но в мозге опухоль живет внутри активной нервной ткани, поэтому тот же серотонин влияет и на работу окружающих нейронных сетей — и через них тоже может менять рост опухоли. Точный механизм процесса многослойный: это и перестройка активности коры, и влияние на экспрессию генов белков, таких как нейропептид Y, он усиливает тормозные процессы в локальных сетях и тем самым снижает темпы роста опухоли.
Поскольку механизм включает и регуляцию генов, и эффекты на уровне нейронных цепей, логично исследовать, какие звенья этой оси можно использовать как терапевтические мишени. Исследователи взяли набор транскрипционных факторов, чья экспрессия изменяется при блокаде серотонилирования, и провели высокопроизводительный скрининг in vivo: фактически, по одному блокировали в живых клетках и наблюдали, без работы каких факторов рост эпендимомы затормозится [2].
Из этого набора неожиданно выявился ETV5: оказалось, что этот фактор усиливает прогрессию опухоли и делает это через усиление именно репрессивных состояний хроматина. ETV5 блокирует считывание с определенных участков ДНК. Среди генов, которые ETV5 подавляет, выделяется нейропептид Y — нейропептид, участвующий в регуляции нейронной активности, пищевого поведения, тревожности и целого ряда других процессов [3] (рис. 2).
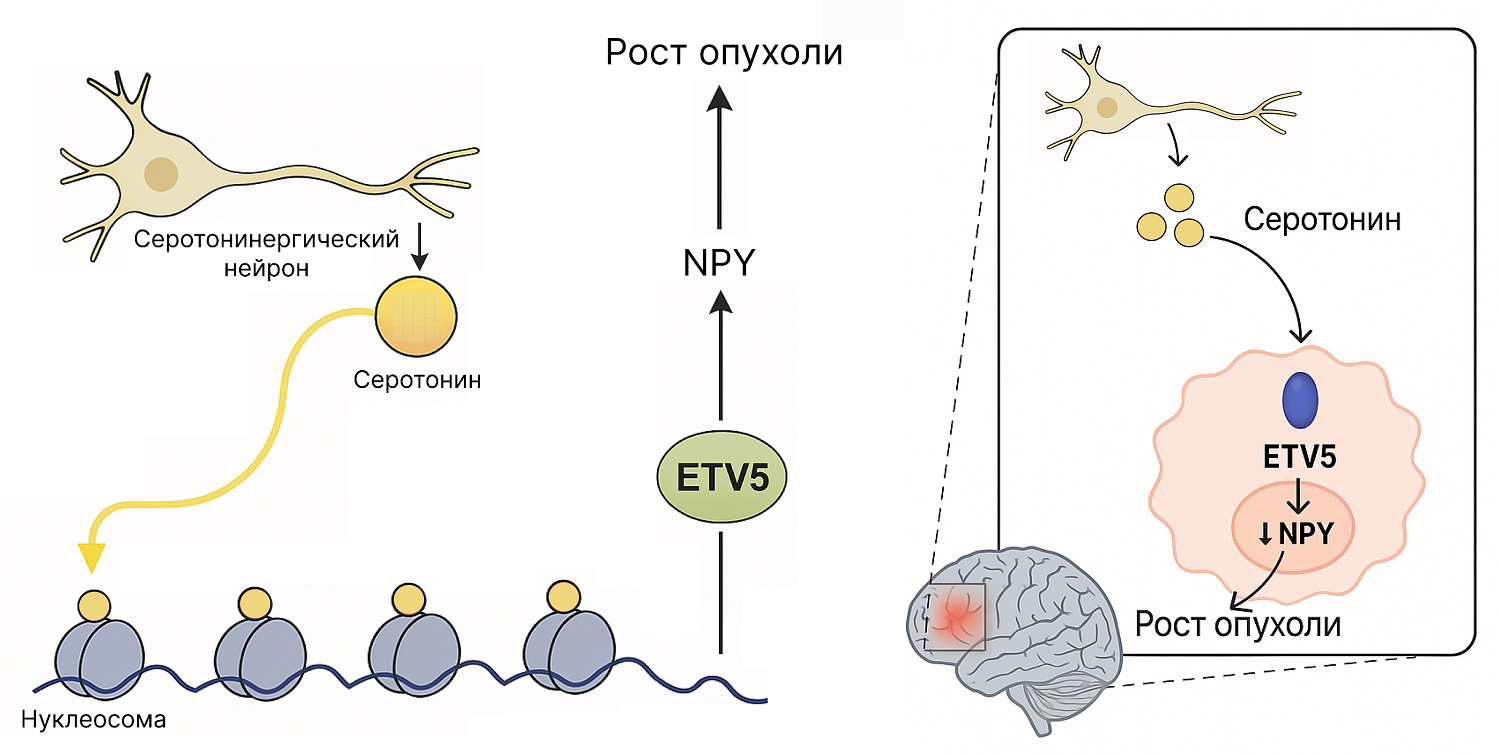
Рисунок 2. Серотонинергические нейроны посылают сигналы в область опухоли; серотонин попадает в опухолевые клетки и, помимо медиаторной роли, может химически «вшиваться» в гистоны. Гистоновое серотонилирование меняет экспрессию набора транскрипционных факторов развития, среди которых ключевую роль играет ETV5. Активный ETV5 усиливает репрессивные хроматиновые состояния и подавляет гены, ограничивающие рост опухоли, включая NPY. Когда ETV5 активен и уровень NPY низкий, эпендимома растет лучше и поддерживает сетевую гиперактивность мозга вокруг себя. Если вмешаться в эту ось — заблокировать серотонилирование или вернуть NPY, — опухоль и ее влияние на нейронные сети заметно ослабевают.
рисунок автора, выполнен с использованием ChatGPT
Глиома и гипервозбудимость
Исследования серотонинергических нейронов показывают, что определенные нейронные цепи и их режим работы могут заметно сдерживать рост опухоли. Но для других типов мозговых опухолей, прежде всего высокозлокачественных глиом, ситуация оказывается иной: здесь уже сама корковая активность и вызванная опухолью гипервозбудимость нейронов начинают поддерживать и усиливать ее рост.
Работа Venkatesh et al. [4] показывает, что рост глиомы зависит от активности окружающих нейронов. При повышении активности коры объем опухоли и число делящихся клеток растут быстрее. Ключевым звеном оказывается растворимая форма белка нейролигина-3 (NLGN3). Белок NLGN3, добавленный к глиомным клеткам, активирует сигнальные пути, ускоряет клеточный цикл и одновременно повышает экспрессию NLGN3 уже в самой опухоли, формируя своеобразную петлю: активность нейронов вызывает усиленную продукцию NLGN3, а это, в свою очередь, усиливает рост глиомы. В результате жизнеспособность и агрессивность опухоли напрямую зависят от активности нейронной сети и от NLGN3 как посредника этого влияния. При отсутствии этого белка рост высокозлокачественных глиом почти останавливается, даже если сама нейронная активность все еще остается высокой [4].
На этот процесс можно взглянуть и с другой точки зрения. В работе Buckingham et al. [5] фокус смещен на обратное направление влияния — от глиомы к нейронной сети. Клетки опухоли активно используют белок-транспортер cystine/glutamate antiporter (SLC7A11). Этот белок закачивает внутрь клеток цистин и одновременно выбрасывает во внеклеточное пространство глутамат. Концентрация глутамата снаружи клеток существенно повышается, и это приводит к перегрузке рецепторов на нейронах. На уровне мозга животных это проявляется в виде устойчивой гипервозбудимости коры и спонтанных эпилептиформных разрядов, а у части даже приводит к клиническим судорожным эпизодам. Блокада транспортера cystine/glutamate antiporter снижает уровень внеклеточного глутамата и заметно нормализует электрическую активность.
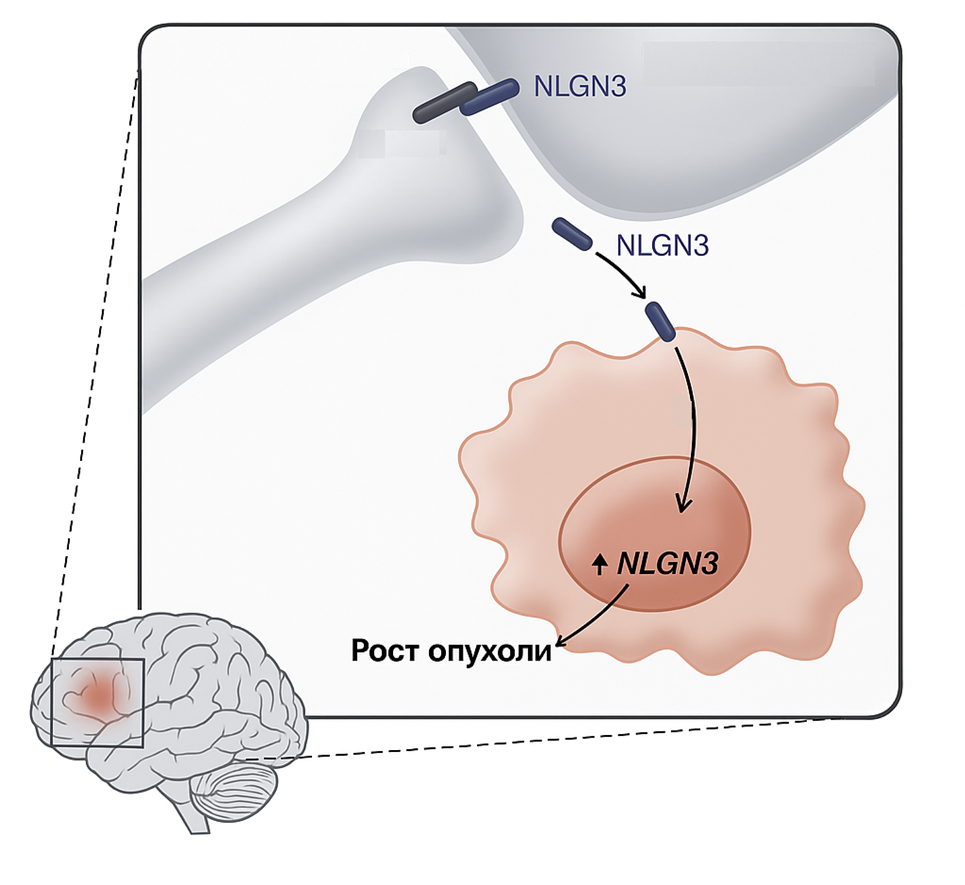
Рисунок 3. Рост глиомы зависит от активности окружающих нейронов: при ее усилении опухоль растет быстрее и больше делится. Ключевым медиатором служит растворимый neuroligin-3 (NLGN3): добавленный к глиомным клеткам, он активирует сигнальные пути, ускоряет цикл деления и повышает экспрессию NLGN3 уже в самой опухоли, формируя петлю положительной обратной связи. Без NLGN3 рост высокозлокачественных глиом почти останавливается, даже при сохраненной высокой активности коры.
рисунок автора, выполнен с использованием ChatGPT
Вместе эти данные формируют представление о положительной обратной связи взаимодействия глиомы и коры головного мозга. Опухоль повышает уровень внеклеточного глутамата и тем самым сдвигает окружающие нейронные цепи в состояние хронической гипервозбудимости. Усиленная активность нейронов в ответ увеличивает высвобождение NLGN3 и других активность-зависимых факторов, которые поддерживают рост и выживание глиомных клеток. Таким образом, рост гиомы подпитывается нейронной активностью, в том числе через NLGN3, как митогенный сигнал [4], а сама опухоль усиливает возбудимость прилежащей коры за счет выброса глутамата [5] (рис. 3).
Тромбоспондин-1 (TSP-1) — это белок, который помогает нейронам образовывать синапсы. В глиобластоме его особенно много в тех ее частях, которые сильнее всего взаимодействуют с остальным, здоровым мозгом [6]. Сами опухолевые клетки начинают активно выделять TSP-1. Из-за этого между нейронами и опухолью образуется больше возбуждающих синапсов, и глиобластома буквально врастает в нейронные сети и использует их активность себе на пользу. Если заблокировать выделение TSP-1, то количество таких синапсов и скорость роста опухоли в моделях уменьшается. Поэтому этот белок считают одним из ключевых факторов, который определяет, насколько глиобластома связана с мозгом и насколько агрессивно она себя ведет.
Опухоль мозга устроена неоднородно с точки зрения связи с мозгом. Одни ее участки (HFC, high functional connectivity, высокая функциональная связность) сильно «подключены» к остальной коре, другие (LFC, low functional connectivity, низкая функциональная связность) — почти не вовлечены в общую сетевую активность. Клетки из HFC-зон образуют больше синапсов с нейронами, ведут себя агрессивнее, а их количество связано с более плохим прогнозом по выживаемости, чем количество клеток из LFC-областей. То есть разные части одной и той же опухоли по-разному встроены в мозговые сети и по-разному опасны.
Внутри глиобластомы есть особый подтип клеток, который предназначен для взаимодействия с нейронами. В участках опухоли с высокой функциональной связанностью с мозгом (HFC-зоны) часть злокачественных клеток сама начинает активно вырабатывать тромбоспондин. В зонах с низкой связанностью TSP-1 в основном производят астроциты, а сами опухолевые клетки почти не вовлечены.
Иммуногистохимическое окрашивание, определяющее количество тромбоспондина, хорошо показывают последствия этого: в HFC-зонах плотность синапсов выше, чем в LFC, причем увеличены и пресинаптические, и постсинаптические структуры. Опухолевые клетки в этих участках буквально встраиваются в области с повышенной синаптической плотностью — они не просто соседствуют с нейронами, а живут внутри синаптических узлов.
Исследователи пересаживали клетки глиобластомы с высокой функциональной связанностью с мозгом и с низкой функциональной связанностью с мозгом в гиппокамп мышей. HFC-клоны образовывали больше синапсов (и между нейронами, и между нейронами и опухолью), давали более крупные опухоли и снижали выживаемость животных по сравнению с LFC-клетками.
Отдельно авторы разбирают роль TSP-1 в росте и структурной организации опухолевых клеток [6]. При прямом контакте с нейронами, экспрессирующими TSP-1, опухолевые клетки начинают делиться в несколько раз активнее, чем без нейронов, формируют больше длинных цитоплазматических отростков — опухолевых микротрубок (tumour microtubes), которые связывают клетки друг с другом. При подавлении TSP-1 число таких микротрубок снижается, вместе с этим падают инвазия и способность опухоли к интеграции в нейронное микроокружение
Миелин меняет профессию
Для быстрой передачи сигналов мозгу позвоночных нужны не только синапсы, а еще и миелин, липидная оболочка вокруг аксонов, которая увеличивает скорость передачи сигнала в нервной системе [7]. В опухолевых клетках мозга миелин приобретает другую, неожиданную роль — он из защитной оболочки аксонов, способствующей передаче импульсов без проблем, становится питанием для опухолевых клеток.
При глиобластоме миелиновая оболочка в белом веществе теряет целостность: миелиновые слои вокруг аксонов дезорганизуются и фрагментируются, образуя богатые липидами обломки, которые затем фагоцитируются микроглией и макрофагами — иммунными клетками, которые должны очищать ткань и помогать в защите от чужеродных воздействий. Однако в опухолевых тканях микроглия и макрофаги поглощают обломки миелина, заполняют свои клетки холестерином и липидами и превращаются в липид-нагруженные макрофаги. В ответ на перегрузку липидами начинается их экспорт наружу. Клетки глиобластомы захватывают миелиновые липиды, получая готовые «строительные блоки» и топливо. Параллельно липид-нагруженные макрофаги становятся иммуносупрессивными — хуже запускают воспалительный ответ против опухоли [8]. Когда исследователи в экспериментах блокировали рецептор CD36, необходимый для захвата липидов, количество липид-нагруженных макрофагов падало, рост опухоли замедлялся, а ответ на терапию улучшался. В итоге миелин при глиобластоме — не фон, а реальное топливо и щит для рака.
Заключение
Таким образом, опухоли мозга сегодня рассматриваются как болезни нейронных сетей: опухоль не просто растет внутри ткани, а вступает в плотный диалог с нейронами, глией, микроглией и сосудами.
Многие опухоли стимулируют рост нервных волокон, используют симпатическую и парасимпатическую иннервацию, чтобы улучшать собственный метаболизм, подавлять иммунитет и повышать устойчивость к терапии. На этом фоне новые терапевтические идеи выглядят уже не как очередная химиотерапия, а как попытка вмешаться в это взаимодействие: ингибировать суперэнхансеры (BRD4, CDK7), изменить гистоновый код, например, серотонилирование гистонов, вмешаться в переработку миелина макрофагами или блокировать синапсы «нейрон—опухоль» с помощью уже знакомых неврологических препаратов.
В соответствии с этим, одна из задач онкологии мозга — научиться лишать опухоль доступа к ресурсам мозговой сети, блокировать интеграцию с ней, оставляя как можно больше пространства для нормальной нейропластичности. Те же механизмы, которые позволили мозгу стать таким гибким, в искаженном виде «подкармливают» опухоль. Вопрос в том, сможем ли мы научиться выключать эту «темную сторону» пластичности, не нарушая саму способность мозга меняться.
Литература
- Surya Nagaraja, Nicholas A. Vitanza, Pamelyn J. Woo, Kathryn R. Taylor, Fang Liu, et. al.. (2017). Transcriptional Dependencies in Diffuse Intrinsic Pontine Glioma. Cancer Cell. 31, 635-652.e6;
- Hsiao-Chi Chen, Peihao He, Malcolm McDonald, Michael R. Williamson, Srinidhi Varadharajan, et. al.. (2024). Histone serotonylation regulates ependymoma tumorigenesis. Nature. 632, 903-910;
- Rajeshwari Bale, Gaurav Doshi. (2023). Cross talk about the role of Neuropeptide Y in CNS disorders and diseases. Neuropeptides. 102, 102388;
- Humsa S. Venkatesh, Tessa B. Johung, Viola Caretti, Alyssa Noll, Yujie Tang, et. al.. (2015). Neuronal Activity Promotes Glioma Growth through Neuroligin-3 Secretion. Cell. 161, 803-816;
- Susan C Buckingham, Susan L Campbell, Brian R Haas, Vedrana Montana, Stefanie Robel, et. al.. (2011). Glutamate release by primary brain tumors induces epileptic activity. Nat Med. 17, 1269-1274;
- Saritha Krishna, Abrar Choudhury, Michael B. Keough, Kyounghee Seo, Lijun Ni, et. al.. (2023). Glioblastoma remodelling of human neural circuits decreases survival. Nature. 617, 599-607;
- Обёртка для аксона;
- Daan J. Kloosterman, Johanna Erbani, Menno Boon, Martina Farber, Shanna M. Handgraaf, et. al.. (2024). Macrophage-mediated myelin recycling fuels brain cancer malignancy. Cell. 187, 5336-5356.e30.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚