Пластисфера: невидимый мир
14 декабря 2021
Пластисфера: невидимый мир
- 1149
- 1
- 0
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В наше время образуется огромное количество пластиковых отходов, в связи с чем в природе оказывается множество маленьких пластиковых частиц, называемых микропластиком. Эти частицы наносят вред некоторым животным и несут потенциальную угрозу для человека. Однако для микроорганизмов они предоставляют массу ценных ресурсов и новых возможностей. На частицах пластика образуются сложные и богатые сообщества микроорганизмов, в совокупности называемые пластисферой. Эти сообщества могут оказывать значительное влияние не только на сами микроорганизмы, но и на окружающие их экосистемы, а также на жизнь людей. В будущем пластисфера может послужить как спасением от пластикового кризиса, так и источником новых глобальных проблем.
Конкурс «Био/Мол/Текст»-2021/2022
 Эта работа заняла первое место в номинации «Школьная» конкурса «Био/Мол/Текст»-2021/2022.
Эта работа заняла первое место в номинации «Школьная» конкурса «Био/Мол/Текст»-2021/2022.

Партнер номинации — некоммерческая школа-пансион «Летово».

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Введение. Осторожно, микропластик!
Пластиковое загрязнение несомненно является одной из наиболее серьезных экологических проблем. В природе накапливается огромное количество незнакомых ей синтетических полимеров, и это, конечно, оказывает на нее серьезное влияние. Природные сообщества уже начинают меняться под воздействием пластика. Эти изменения пока еще не очень заметны человеческому глазу, однако учитывая скорость, с которой они происходят, недооценивать их не стоит, так как это может отразиться и на жизни людей.
Так как системы утилизации отходов почти во всем мире работают крайне плохо, огромное количество пластика попадает в экосистемы. Там он, хотя и очень медленно, распадается на мелкие фрагменты под действием тепла и солнечного излучения. Такие фрагменты называют микропластиком. По примерным оценкам в мировом океане их должно быть более 350 млн тонн [1].
Существуют опасения, что микропластик или продукты его деградации могут представлять опасность для здоровья людей, так как он может поедаться животными и, встраиваясь в пищевые цепи, попадать в организм человека вместе с едой. Однако пока не получено данных, однозначно подтверждающих угрозу для здоровья. Хотя вопрос этот еще недостаточно изучен, так что не стоит оставлять его без внимания, тем более что уровень загрязнения постоянно растет [2].
Пластисфера и ее обитатели
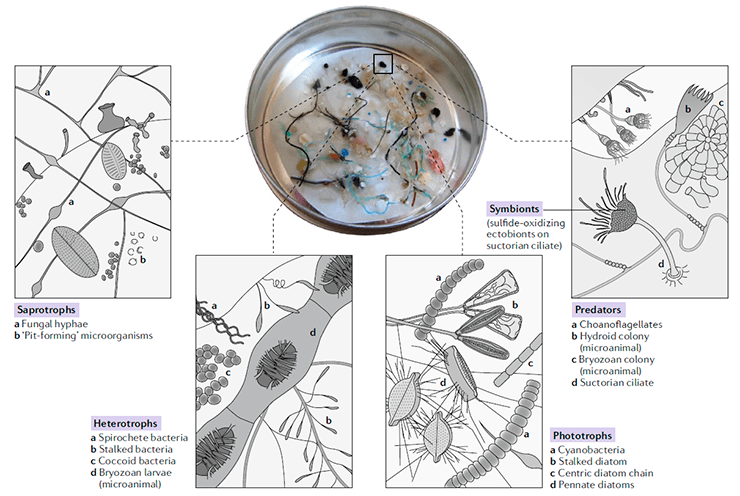
Многим живым организмам микропластик несомненно вредит, однако есть и такие, кому он идет на пользу. Представители самых разных систематических и экологических групп способны колонизовать частицы пластика, образуя на них комплексные сообщества с собственным круговоротом веществ и множеством внутривидовых и межвидовых взаимодействий. На частицах пластика создаются уникальные условия обитания, в связи с чем сообщества на них сильно отличаются от сообществ окружающей среды и часто являются более сложными и богатыми. Такие сообщества в совокупности называют пластисферой.
Колонизируя фрагменты пластика, микроорганизмы образуют на их поверхности биопленки — агрегаты клеток, окруженные полимерным внеклеточным матриксом, или попросту слизью, который они сами синтезируют. Образование биопленок сопровождается значительными изменениями в образе жизни микроорганизмов, их переходом от планктонной или свободноплавающей стадии к сидячей. Повышается экспрессия генов, ответственных за прикрепление, хемотаксис, коммуникацию. Биопленки — это не случайные сборища микроорганизмов, а высокоорганизованные сообщества, сравнимые с тканями многоклеточных организмов. В них устанавливается определенная плотность популяции, при достижении которой скорость размножения снижается, а также происходит равномерное распределение ресурсов между членами сообщества.
Частицы пластика являются точками большого скопления природных ресурсов. Это связано с тем, что на поверхности раздела фаз за счет адгезии возрастает концентрация различных веществ. Это является одной из причин образования биопленок. Скопление микроорганизмов приводит к еще большему накоплению ресурсов, что привлекает новых колонизаторов.
В состав пластисферы входят организмы, занимающие различные экологические ниши. В освещенных экосистемах преобладают фотоавтотрофы, такие как цианобактерии, диатомовые, зеленые, хлорарахниофитовые водоросли и другие. Они являются основой многих пищевых цепей и, как правило, первыми колонизуют частицы пластика. Кроме того, микропластик населяют азотфиксирующие бактерии, способные поглощать недоступный для других организмов атмосферный азот и переводить его в более удобные формы.
Также в пластисферные сообщества входят различные гетеротрофы: множество видов бактерий, археи и разнообразных одноклеточных и многоклеточных эукариот, включая инфузории, грибы, мшанки и гидроидные полипы. Они могут питаться другими живыми организмами, выделяемыми ими веществами, например, слизью, останками мертвых, а также самим пластиком. Полимеры под действием тепла и солнечного излучения постепенно распадаются на мономеры, которые могут поглощать микроорганизмы. Обрастание частиц пластика микроорганизмами ускоряет процесс их деградации, так как они размножаются в трещинах на поверхности полимера, способствуя их расширению. Кроме того, некоторые микроорганизмы способны синтезировать ферменты, расщепляющие синтетические полимеры [1].
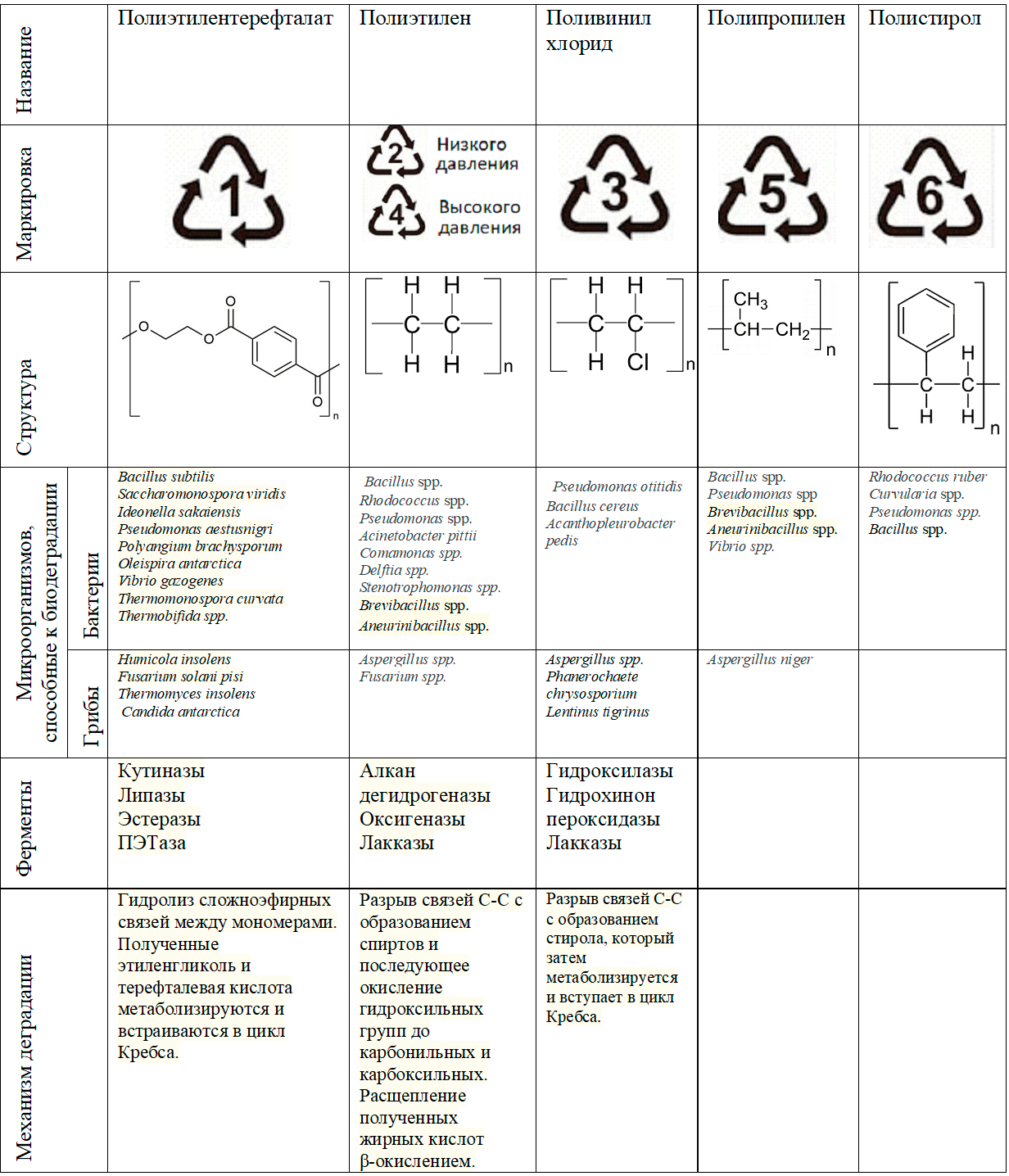
Появление в природе синтетических полимеров открывает микроорганизмам новые свободные экологические ниши, осваивание которых позволяет им избежать конкуренции за пищевые ресурсы. Хотя по меркам эволюции пластик появился в природе совсем недавно, у многих бактерий и грибов в ходе естественного отбора уже выработалась способность расщеплять связи между звеньями полимеров и использовать их в качестве источников углерода и энергии. Лучше всего они справляются с гидролизуемыми полимерами, такими, как полиэтилентерефталат (ПЭТ), однако есть микроорганизмы, способные разрушать даже полимеры с наиболее прочными связями между мономерами, например, полиэтилен. В целом, для всех наиболее распространенных видов пластика были найдены грибы и бактерии, способные их разлагать. Хотя процесс биодеградации пока еще происходит крайне медленно [3], [4].
Таблица 1. Основные синтетические полимеры и их биодеградация. На основе источников [3], [4], [8].
Полиэтилентерефталат — самый вкусный пластик
Лучше всего из основных синтетических полимеров разлагается полиэтилентерефталат, и процесс его биодеградации наиболее хорошо изучен . ПЭТ — один из наиболее часто используемых видов пластика. Из него изготавливают одноразовые бутылки для напитков, контейнеры для еды и другие одноразовые изделия, а также пленки и синтетические волокна. ПЭТ получают поликонденсацией этиленгликоля и терефталевой кислоты. Мономером ПЭТ является моно-2-гидроксиэтилтерефталевая кислота (МГЭТ) — сложный эфир этиленгликоля и терефталевой кислоты.
О биодеградации ПЭТ и даже получении при этом ванилина (!) вы узнаете, прочитав статью «Ванильные мечты о пластике» [14]. — Ред.
У различных бактерий и грибов найдено большое число гидролаз, включая кутиназы (ферменты, катализирующие расщепление растительного полимера кутина), липазы, эстеразы, способных катализировать расщепление ПЭТ помимо своего основного субстрата. Способность расщеплять ПЭТ показана, например, для кутиназ TfH и TfH BTA-2 из актинобактерии Thermobifida fusca, липазы В из гриба Candida antarctica и многих других гидролаз. Помимо этого, у бактерии Ideonella sakaiensis 201-F6 обнаружен фермент ПЭТаза , обладающий гораздо большей активностью и специфичностью к ПЭТ. Полиэтилентерефталат является основным субстратом ПЭТазы.
Подробно об открытии этого фермента рассказывает статья «“Пластик, сэр!”, или Бактериальная диета в стиле хай-тек» [15]. — Ред.
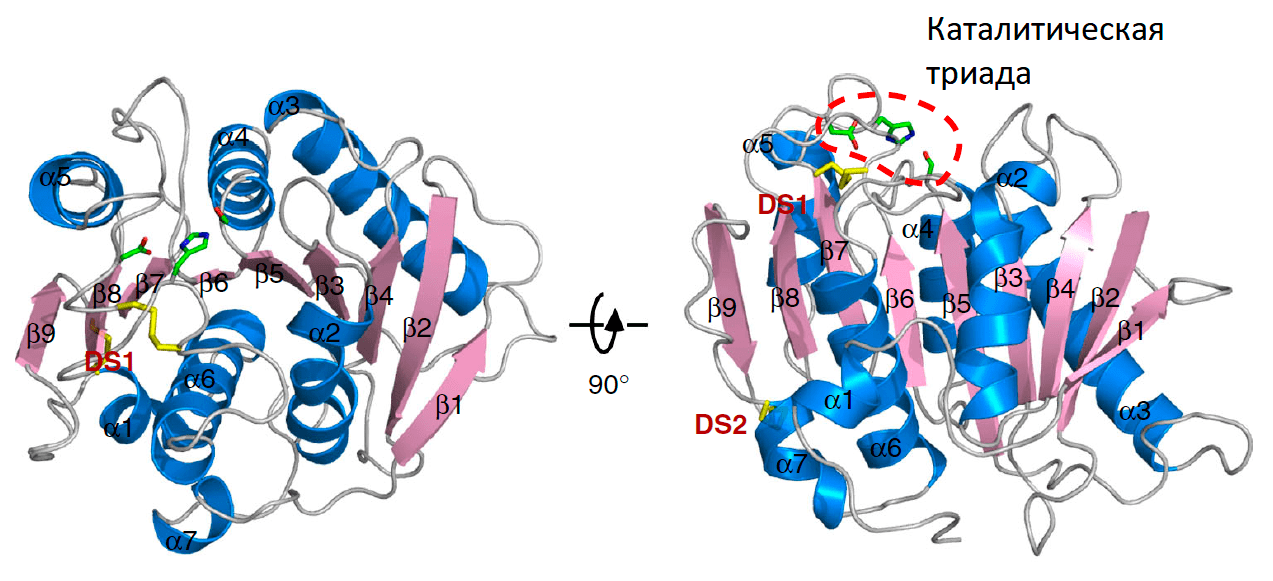
ПЭТаза высоко гомологична некоторым кутиназам и обладает структурой, каноничной для суперсемейства альфа\бета-гидролаз. Структура фермента показана на рисунке 1а. Кроме того, активный центр фермента состоит из каталитической триады: серина, гистидина и аспаргиновой кислоты (S131-H208-D177) — консервативной для гидролаз. Также фермент обладает оксианионной дырой, образованной метионином и тирозином (M132, Y58). Оксианионная дыра, необходимая для стабилизации карбонильного радикала расщепляемого субстрата, присутствует и у других гидролаз. Это говорит о том, что ПЭТаза расщепляет свой субстрат по тому же общему механизму, что и многие другие гидролазы, включая наши собственные пищеварительные ферменты, например, химотрипсин, гидролизующий пептидную связь в белках. Механизм каталитического расщепления ПЭТ показан на рисунке 1б.
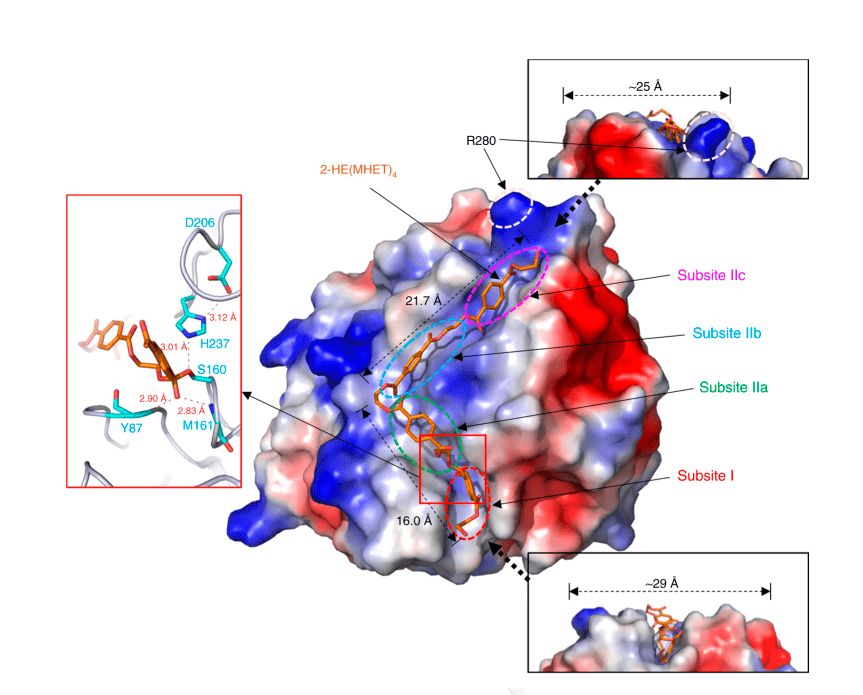
Однако у ПЭТазы имеется ряд отличительных особенностей. Во-первых, субстрат-связывающая щель длиннее и шире, по сравнению со щелями других гидролаз, способных расщеплять ПЭТ. Это связано с различиями в аминокислотной последовательности. Благодаря этому ПЭТ идеально подходит по форме к ферменту.
Во-вторых, у ПЭТазы имеются две дисульфидные связи, в то время как у других гидролаз только одна. Это придает ферменту более гибкую и прочную структуру, облегчающую связывание с субстратом.
В-третьих, триптофан, находящийся рядом с активным центром ПЭТазы, может принимать три различные конформации, в то время как в других гидролазах он жестко зафиксирован. Это связано с тем, что рядом с триптофаном в ПЭТазе находится серин, а у других гидролаз на этом месте расположен более громоздкий гистидин, препятствующий изменению конформации. Ароматическая система триптофана взаимодействует с ароматической системой терефталевой кислоты за счет стекинг-взаимодействий, повышая сродство фермента к субстрату, а изменение конформации триптофана способствует отсоединению продукта реакции [5–7].
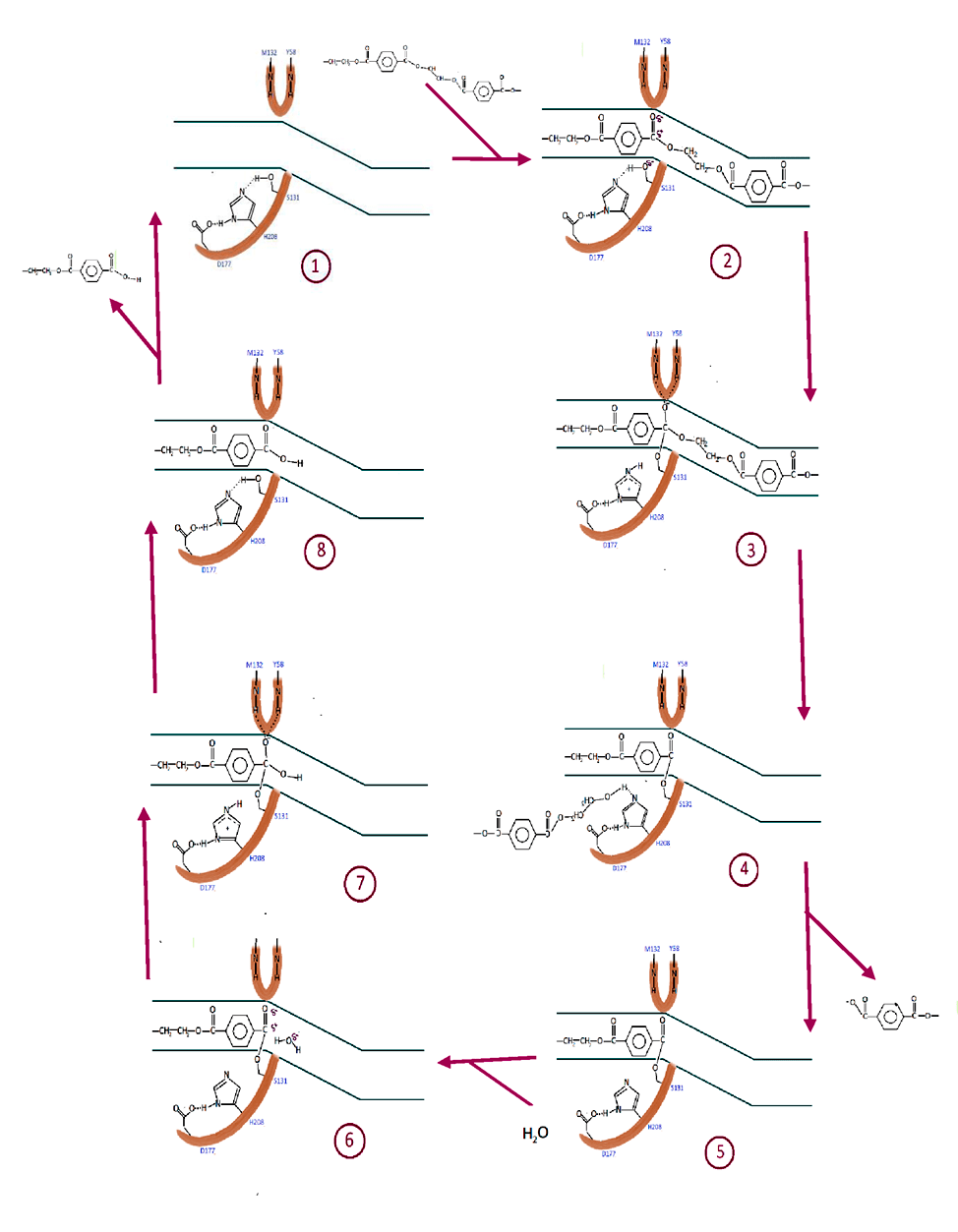
Рисунок 2. Гидролиз полиэтилентерефталата. 1. Свободный фермент. 2. Фрагмент ПЭТ фиксируется в субстрат-связывающей щели. 3. Нуклеофильная атака карбонильного углерода ПЭТ остатком серина. Образуется промежуточное соединение ПЭТ с сериновым остатком фермента. Кислород карбонильной группы фиксируется в оксианионной дыре. Водород серина переходит на гистидин. 4. Разрыв связи. Одна часть субстрата ковалентно связана с серином, другая — водородной связью с гистидином. 5. Одна из частей расщепленного ПЭТ покидает фермент. 6–7. Нуклеофильная атака карбонильного углерода водой. Гидроксильная группа воды соединяется с карбонильным углеродом, протон переходит на гистидин. Кислород карбонильной группы фиксируется оксианионной дырой. 8. Возвращение фермента в исходное состояние и отсоединение оставшегося продукта.
на основе [5–7]
Основным продуктом гидролиза ПЭТ является МГЭТ. Реакция происходит во внешней среде, после чего МГЭТ транспортируется через внешнюю мембрану бактерий в периплазму, где МГЭтаза, закрепленная на внутренней стороне внешней мембраны, расщепляет ее до этиленгликоля и терефталевой кислоты, которые затем проникают в цитоплазму и встраиваются в метаболические пути. МГЭТаза — еще один фермент, уникальный для I. sakaiensis [7], [8].
Терефталевая кислота превращается в протокатеховую, которая вступает в бета-кетоадипатный путь и расщепляется до сукцинил-КоА и ацетил-КоА, которые затем встраиваются в цикл трикарбоновых кислот или другие метаболические пути. Бета-кетоадипатный путь имеется у многих грибов и бактерий, способных утилизировать ароматические соединения, например, производные лигнина [7–9].
Этиленгликоль окисляется до глиоксалевой кислоты, которая встраивается в глиоксилатный цикл — видоизмененный цикл трикарбоновых кислот, присущий микроорганизмам и растениям [7], [10]. Схема метаболизма ПЭТ показана на рисунке.
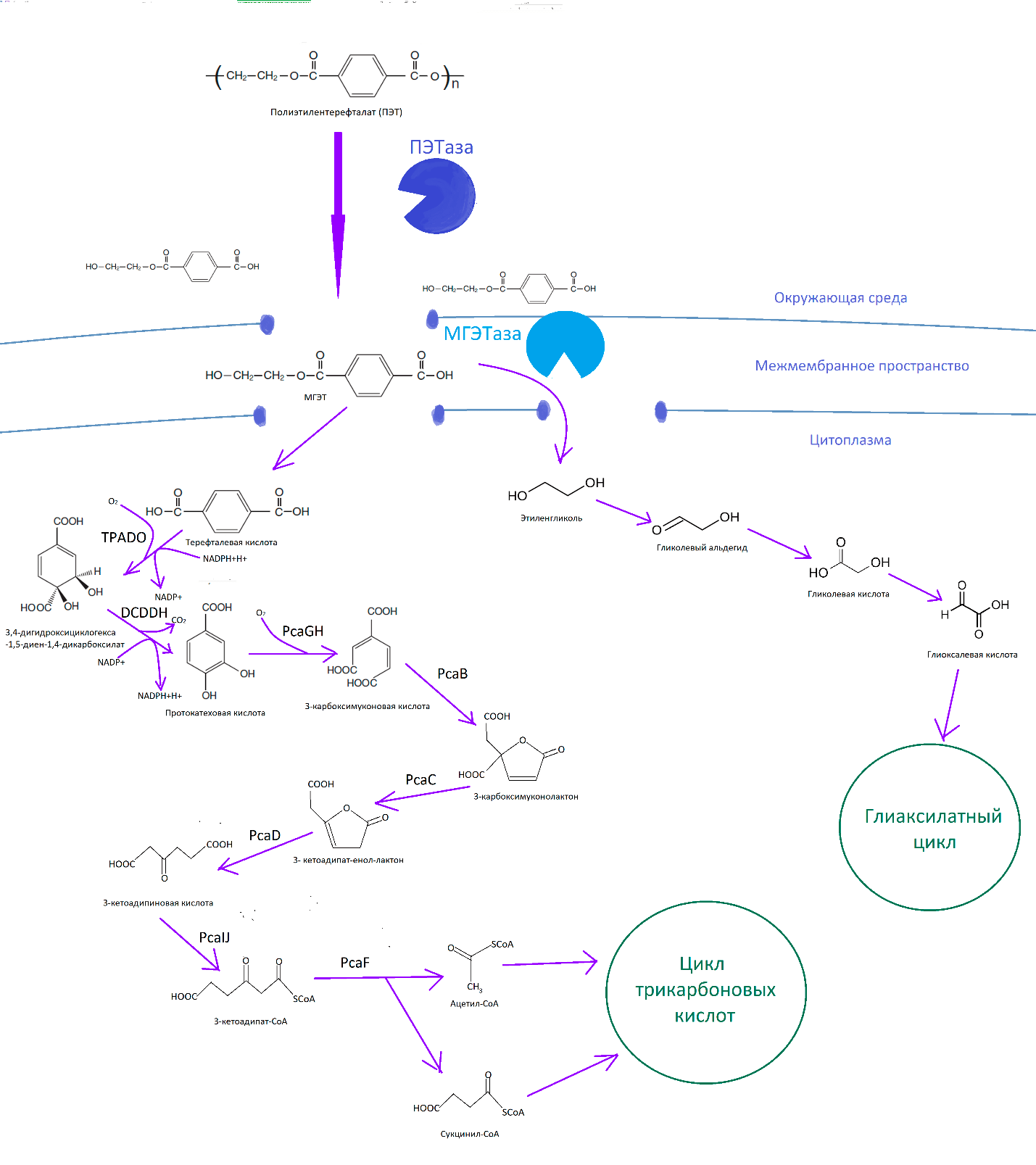
Рисунок 3. Метаболизм полиэтилентерефталата
на основе [7–10]
Сейчас проводится много исследований, направленных на поиск новых ферментов, способных катализировать расщепление синтетических полимеров, а также на модификацию уже известных с целью улучшения их свойств. В будущем, вероятно, станет возможным использование микроорганизмов для утилизации пластиковых отходов, но на данном этапе это нерентабельно, так как процесс протекает слишком медленно [7].
Выгоды жизни в пластисфере
Микропластик является источником не только углерода и энергии, но и других ценных ресурсов. Некоторые полимеры, такие, как нейлон, содержат азот, отсутствие которого является одним из главных ограничивающих факторов для многих организмов. Кроме того, в состав многих видов пластика входят различные металлы, которые используются для придания материалу необходимых свойств, таких как гибкость, цвет, устойчивость к ультрафиолету и др. Некоторые металлы выполняют важные биологические функции, поэтому в следовых количествах необходимы микроорганизмам. Также некоторые микроорганизмы, например, железобактерии, способны получать энергию при окислении металлов.
Колонизуя частицы пластика, микроорганизмы не только получают доступ к ценным ресурсам, но и ряд других возможностей. В биопленках между микроорганизмами образуются тесные контакты, в связи с чем возрастает частота горизонтального переноса генов. Этот способствует распространению полезных для микроорганизмов генов, например, тех, которые позволяют расщеплять синтетические полимеры. Это свойство пластисферы несет потенциальную угрозу для человека, так как повышает вероятность передачи опасных генов, например, генов устойчивости к антибиотикам или генов, отвечающих за патогенность.
Помимо этого, микропластик может способствовать распространению населяющих его микроорганизмов, так как частицы пластика перемещаются при помощи течения, ветра, животных на большие расстояния. Малоподвижные организмы могут осваивать новые местообитания, используя пластик в качестве транспортного средства. Однако такие путешествия могут приводить к негативным последствиям для экосистем и человека. Таким образом могут перемещаться водоросли, вызывающие опасное цветение воды, или возбудители каких-либо заболеваний. Инвазивные виды могут не встретить в новых местообитаниях конкурентов или естественных врагов, что приведет к их массовому размножению и вытеснению аборигенных видов. Местные виды, никогда ранее не сталкивавшиеся с новыми патогенами, не могут в достаточной мере оказать им сопротивление, что приводит к массовым вспышкам заболеваний. Среди микроорганизмов, населяющих микропластик, найдены некоторые потенциально опасные для человека, например, бактерии из рода Vibrio.
Таким образом, кусочек пластика для микроба — квартира со всеми удобствами. А так как таких квартир становится все больше, те, у кого есть возможность их заселить, получают конкурентное преимущество [1].
Заключение. Пластисфера распространяется повсюду
Микропластик сейчас распространен по всей планете. Частицы пластика плавают на поверхности воды, в ее толще, оседают на дно. Микропластик в больших количествах обнаружен не только в антропогенно-нагруженных водоемах, но даже в наименее тронутых человеком экосистемах, таких как озеро Байкал [11]. Пластисфера распространяется во всех природных условиях, в том числе самых суровых. Микропластик вместе с организмами, способными его колонизовать и разлагать, есть даже за полярным кругом, хотя, конечно, биодеградация там происходит еще медленнее, чем в более благоприятных условиях [12].
Хотя больше всего пластисферу изучают в мировом океане, в наземных экосистемах микропластик и его обитатели также присутствуют. Частицы пластика в значительных количествах накапливаются в почве, где на них образуются сообщества микроорганизмов [13]. Более того, микропластик встречается не только в почве, но и в самых неожиданных местах, таких как пищеварительные тракты некоторых животных. Обнаружено два вида бабочек — Galleria mellonella и Plodia interpunctella, — личинки которых могут поедать и переваривать полиэтиленовые пакеты. В основном эти черви питаются пчелиным воском, который тоже является довольно трудноперевариваемым субстратом. Поэтому, неудивительно, что они научились есть пакеты. В кишечнике P. interpunctella нашли бактерий Enterobacter asburiae YP1 и Bacillus sp. YP1, благодаря которым черви и обладают своей способностью.
Помимо этого, показано, что личинки мучных хрущаков могут переваривать полистирол. В эксперименте личинок Tenebrio molitor в течение месяца кормили только вспененным полистиролом. Жуки чувствовали себя прекрасно, и потом окуклились и превратились во взрослых особей. Способность переваривать полистирол у этих животных тоже связана с симбиотическим бактериями в кишечнике [3], [4].
Таким образом, хотя микропластик для нас невидим и пока еще не оказывает на нашу жизнь ощутимого влияния, он постепенно проникает всюду и оказывает несомненное влияние на эволюцию микроорганизмов. В будущем пластисфера может послужить как спасением от пластикового кризиса, так и источником новых глобальных проблем.
Литература
- Linda A. Amaral-Zettler, Erik R. Zettler, Tracy J. Mincer. (2020). Ecology of the plastisphere. Nat Rev Microbiol. 18, 139-151;
- Madeleine Smith, David C. Love, Chelsea M. Rochman, Roni A. Neff. (2018). Microplastics in Seafood and the Implications for Human Health. Curr Envir Health Rpt. 5, 375-386;
- Ambika Arkatkar, Asha A. Juwarkar, Sumit Bhaduri, Parasu Veera Uppara, Mukesh Doble. (2010). Growth of Pseudomonas and Bacillus biofilms on pretreated polypropylene surface. International Biodeterioration & Biodegradation. 64, 530-536;
- John A. Glaser. (2019). Biological Degradation of Polymers in the Environment. Plastics in the Environment;
- Seongjoon Joo, In Jin Cho, Hogyun Seo, Hyeoncheol Francis Son, Hye-Young Sagong, et. al.. (2018). Structural insight into molecular mechanism of poly(ethylene terephthalate) degradation. Nat Commun. 9;
- Xu Han, Weidong Liu, Jian-Wen Huang, Jiantao Ma, Yingying Zheng, et. al.. (2017). Structural insight into catalytic mechanism of PET hydrolase. Nat Commun. 8;
- Clodagh M. Carr, David J. Clarke, Alan D. W. Dobson. (2020). Microbial Polyethylene Terephthalate Hydrolases: Current and Future Perspectives. Front. Microbiol.. 11;
- Shosuke Yoshida, Kazumi Hiraga, Toshihiko Takehana, Ikuo Taniguchi, Hironao Yamaji, et. al.. (2016). A bacterium that degrades and assimilates poly(ethylene terephthalate). Science. 351, 1196-1199;
- Jennifer R. Davis, Jason K. Sello. (2010). Regulation of genes in Streptomyces bacteria required for catabolism of lignin-derived aromatic compounds. Appl Microbiol Biotechnol. 86, 921-929;
- Björn Mückschel, Oliver Simon, Janosch Klebensberger, Nadja Graf, Bettina Rosche, et. al.. (2012). Ethylene Glycol Metabolism by Pseudomonas putida. Appl Environ Microbiol. 78, 8531-8539;
- О. В. Ильина, М. Ю. Колобов, В. В. Ильинский. (2021). Пластиковое загрязнение прибрежных поверхностных вод среднего и южного Байкала. Вод. ресурсы. 48, 42-51;
- Aneta K. Urbanek, Waldemar Rymowicz, Aleksandra M. Mirończuk. (2018). Degradation of plastics and plastic-degrading bacteria in cold marine habitats. Appl Microbiol Biotechnol. 102, 7669-7678;
- Ruimin Qi, Davey L. Jones, Zhen Li, Qin Liu, Changrong Yan. (2020). Behavior of microplastics and plastic film residues in the soil environment: A critical review. Science of The Total Environment. 703, 134722;
- Ванильные мечты о пластике;
- «Пластик, сэр!», или Бактериальная диета в стиле хай-тек.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚