
Разноцветные «чудеса» науки
01 ноября 2012
Разноцветные «чудеса» науки
- 9897
- 3
- 0
Это буйство красок вызвано антоцианами — пигментами растений
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Несколько столетий назад началась одна из самых интересных и красивых историй — история изучения цвета у растений. В ходе изучения растительных пигментов были сделаны важнейшие открытия современной биологии (законы Менделя, мобильные генетически элементы, явление РНК-интерференции). На сегодняшний день вопросы о биохимической природе пигментов растений, их биосинтезе и его регуляции достаточно подробно исследованы. А полученные данные активно применяются учёными для манипуляций с цветом у растений.
Конкурс «био/мол/текст»-2012
 Эта работа заняла первое место в номинации «Приз зрительских симпатий» конкурса «био/мол/текст»-2012.
Эта работа заняла первое место в номинации «Приз зрительских симпатий» конкурса «био/мол/текст»-2012.
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific.
В последнее время как в российских, так и в зарубежных СМИ появляются сообщения о «чудо-фруктах», «чудо-овощах» и «чудо-цветах» с необычной окраской, которая либо не встречается у данных видов растений, либо встречается, но очень редко. Так, например, немалый фурор среди российской общественности произвела новость о создании уральскими селекционерами сорта картофеля «Чудесник» с фиолетовой окраской мякоти (рис. 1, слева).
И хотя на российском рынке фиолетовая морковь и перец являются чем-то необычным и очень редким, за рубежом овощами с фиолетовой окраской уже никого не удивить (рис. 1, в центре). Среди «чудес» науки, которые поражают воображение многих людей, можно упомянуть голубые розы (рис. 1, справа), впервые созданные в 2004 году австралийской компанией «Флориген» (Florigene) при поддержке японского холдинга «Сантори».

Рисунок 1. Растения экзотических цветов. Слева: Клубень картофеля сорта «Чудесник», выведенного сотрудниками Уральского научно-исследовательского института сельского хозяйства. В центре: Морковь с пурпурной окраской корнеплода на рынке в Турции. Справа: Первая в мире «синяя» роза, созданная австралийскими учеными из компании «Флориген» (Florigene) при поддержке японского холдинга «Сантори».
Приведенные примеры растений с необычной для нас окраской различных органов объединяет то, что все они были искусственно созданы человеком с помощью манипуляций с окраской, которая обусловлена растительными пигментами — антоцианами. Однако без всестороннего исследования природы антоциановой окраски и генетической составляющей биосинтеза антоциановых соединений манипуляция с окраской у различных видов растений была бы невозможна.
Что такое антоцианы? Несколько слов о химии
На сегодняшний день достаточно хорошо исследованы такие растительные пигменты, как флавоноиды, каротиноиды и беталаины; они имеют различную химическую структуру и придают растениям различную окраску. И хотя каротиноиды и беталаины тоже очень интересные пигменты, в данной статье мне бы хотелось остановиться на пигментах флавоноидной природы, поскольку именно они обусловливают огромное разнообразие оттенков цветов у растений. К данной группе относятся повсеместно распространенные среди цветковых растений антоцианы, которые не только окрашивают растения в розовые, красные, оранжевые, алые, пурпурные, голубые, темно-синие цвета, но и являются очень полезными для человека биологически активными молекулами [1]. И хотя другие флавоноидные соединения также могут участвовать в образовании цвета у растений (например, ауроны обеспечивают желтую окраску, а бесцветные флавонолы стабилизируют антоциановые пигменты), основное внимание в статье будет уделено именно антоцианам.
Итак, антоцианы — это растительные пигменты, которые могут присутствовать у растений в генеративных (цветках, пыльце) и вегетативных (стеблях, листьях, корнях) органах, а также в плодах и семенах [2]. При этом данные соединения могут либо постоянно присутствовать в клетке, либо появляться на некоторое время на определенной стадии развития растений или при действии стресса. Последнее обстоятельство навело ученых на мысль, что данные соединения нужны не только для окраски цветов и плодов для привлечения насекомых-опылителей и распространителей семян, но и для борьбы с различными типами стрессов [3].
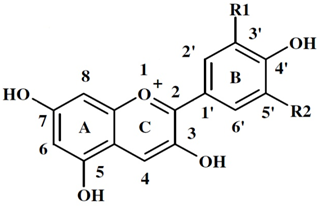
Рисунок 2. Базовая структура антоцианидинов и антоцианов. Представлена нумерация атомов углерода.
Первые опыты по изучению антоциановых соединений и их химической природы были проведены известным английским химиком Робертом Бойлем еще в 1664 г., когда он впервые обнаружил, что под действием кислот синий цвет лепестков василька изменялся на красный, под действием же щелочи лепестки зеленели [4]. В 1913–1915 гг. немецкие биохимики Р. Вильштеттер и А. Штоль опубликовали серию работ, проливших свет на вопрос о сущности природной окраски антоцианов. Из цветков различных растений они выделили индивидуальные пигменты и описали их химическое строение. Оказалось, что антоцианы в клетках находятся преимущественно в виде гликозидов. Их агликоны (базовые молекулы-предшественники), получившие название антоцианидинов, связаны преимущественно с сахарами глюкозой, галактозой, рамнозой [4].
Все антоцианы (которых известно более 500, и число это растет [5]) имеют общий С15-углеродный скелет, образованный двумя бензольными кольцами А и В, соединенными С3-фрагментом. При этом от других флавоноидных соединений антоцианы отличаются наличием положительного заряда и двойной связи в С-кольце (рис. 2). Несмотря на огромное разнообразие антоциановых соединений, все они представляют собой производные шести основных антоцианидинов: пеларгонидина, цианидина, пеонидина, дельфинидина, петунидина и мальвидина, которые отличаются боковыми радикалами R1 и R2 (рис. 2, табл. 1). Поскольку при биосинтезе (о нем речь пойдет чуть ниже) пеонидин образуется из цианидина, а петунидин и мальвидин — из дельфинидина, можно выделить три основных антоцианидина: пеларгонидин, цианидин и дельфинидин, которые, таким образом, являются предшественниками всех антоциановых соединений.
| Антоцианидин | R1 | R2 | Цвет |
|---|---|---|---|
| цианидин (Cy) | ОН | Н | пурпурный |
| пеонидин(Pn) | ОСН3 | Н | пурпурно-синий |
| пеларгонидин (Pg) | Н | Н | красно-оранжевый |
| мальвидин (Mv) | ОСН3 | ОСН3 | пурпурный |
| дельфинидин (Dp) | ОН | ОН | синий |
| петунидин (Pt) | ОСН3 | ОН | пурпурный |
Имея общее строение С15-углеродного скелета, индивидуальные соединения в классе антоцианов выделяют на основе наличия, положения и характера модификаций основного С15-углеродного скелета. В качестве примера строения индивидуального соединения антоциана с модификациями А-, В- и С-колец на рисунке 3 приведена структура так называемого «небесно-синего антоциана», который придает растениям ипомеи голубую окраску.
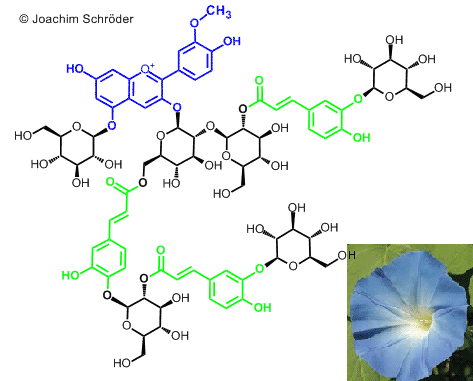
Рисунок 3. Структура «небесно-синего антоциана» (C08642). Соединение выделено из Ipomoea tricolor. На рисунке отмечены: синим — пеонидин (метилированное производное цианидина); зеленым — остатки кофейной кислоты; черным — остатки глюкозы.
Какую именно окраску будет иметь растение, зависит от многих факторов:
- структуры и концентрации антоцианов (которая, кстати, зависит и от наличия стресса — засухи, интенсивного освещения, холода);
- pH в вакуолях, где они накапливаются (см. выше описание опытов Роберта Бойля);
- наличия ко-пигментов, стабилизирующих антоциановую окраску;
- ионов металлов (алюминия, железа, магния, молибдена, вольфрама), с которыми антоцианы могут образовывать комплексы, меняя свой цвет на голубой. В этом случае очень показательным является пример образования комплекса антоцианов корня горчицы с ионами молибдена (рис. 4);
- локализации этих соединений в тканях растений.
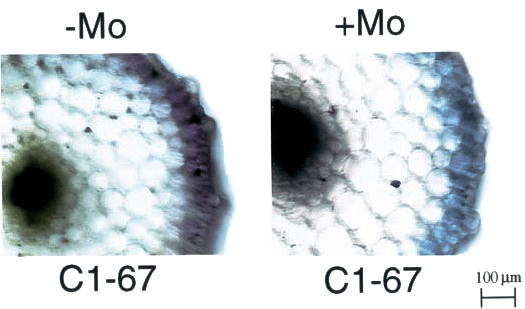
Рисунок 4. Поперечный срез корней горчицы, росших в среде с молибденом (+Мо) и без него (−Мо). Данный вид растения накапливает антоцианы в эпидермисе корня, которые с ионами молибдена образуют комплексы, меняя при этом цвет с пурпурного на синий.
Существует такая закономерность: голубой (синий) цвет имеет дельфинидин и его производные, красно-оранжевую окраску имеют производные пеларгонидина, а пурпурно-красную — цианидина. При этом голубой цвет обусловливают гидроксильные группы (табл. 1, рис. 3), метилирование которых (присоединение группы —CH3) приводит к «покраснению» [7]. Однако следует учитывать, что одно и то же антоциановое соединение в зависимости от сдвига в величине кислотности клеточного сока может приобретать различные оттенки. Так, раствор антоцианов в кислой среде имеет красный, в нейтральной — пурпурный, а в щелочной — желто-зелёный цвет (рис. 5).

Рисунок 5. Изменение окраски раствора антоцианов, выделенных из краснокочанной капусты, при изменении рН раствора от 1 до 10 (слева направо).
Итак, чем обусловлены оттенки антоциановой пигментации, почему они разные у разных видов растений, или даже у одних и тех же растений в разных условиях произрастания, становится ясно. Вооружившись уже изложенными данными, каждый читатель может сам поэкспериментировать со своими домашними растениями, понаблюдав за изменением их окраски. Однако, если в ходе этих экспериментов вы добьетесь желаемого оттенка цвета и ваше растение выживет, то уже точно оно не передаст данный оттенок своим потомкам. Чтобы эффект был стойким, необходимо разобраться еще в одном аспекте формирования цвета, а именно в генетической составляющей биосинтеза антоцианов в клетках растений.
Молекулярно-генетические основы биосинтеза антоцианов
Данный вопрос исследован на сегодняшний день достаточно полно, чему немало поспособствовали мутанты различных видов растений с нарушенным биосинтезом антоцианов. Было установлено, что на биосинтез антоцианов (а, следовательно, и на формируемый оттенок у растения) влияют мутации в трех типах генов [8]:
- Кодирующих ферменты, участвующие в цепи биохимических превращений (структурные гены).
- Определяющих транскрипцию структурных генов в нужное время в нужном месте (регуляторные гены).
- Кодирующих транспортеры антоцианов в вакуоли (известно, что антоцианы, находящиеся в цитоплазме, окисляются и формируют агрегаты бронзового цвета, которые являются очень токсичными для клеток растений [9]).
Благодаря методам биохимии и молекулярной генетики все стадии биосинтеза антоцианов и осуществляющие их ферменты на сегодняшний день известны и достаточно полно исследованы (рис. 6), в том числе из многих видов растений выделены структурные и регуляторные гены биосинтеза антоцианов [8]. Знание особенностей биосинтеза антоциановых пигментов у конкретного вида растения позволяет проводить манипуляции с его окраской на генетическом уровне, создавая растения с необычной пигментацией, которые будут передавать новые признаки окраски из поколения в поколение.
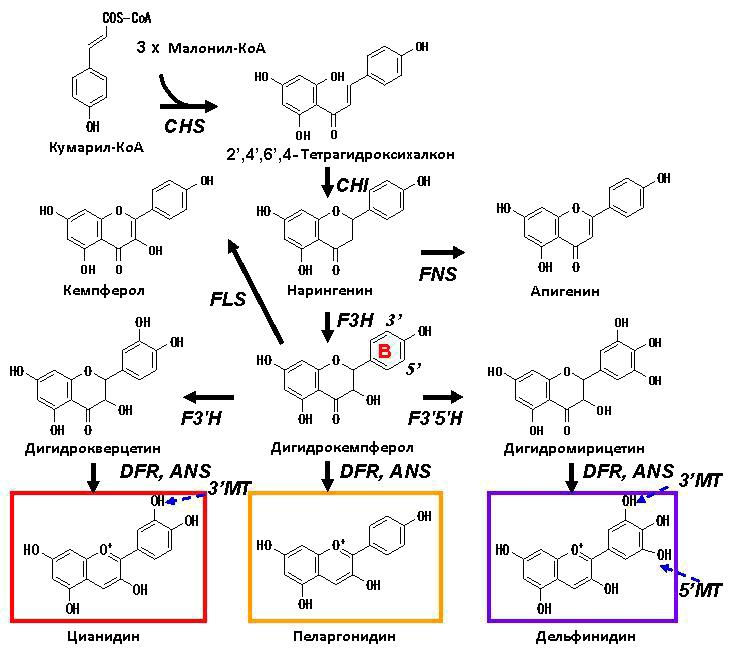
Рисунок 6. Биосинтез антоцианидинов: цианидина, пеларгонидина, дельфинидина. Антоцианидины далее подвергаются реакциям модификации (гликозилированию, ацилированию, метилированию), которые осуществляются гликозилтрансферазами (GT), ацилтрансферазами (AT) и метилтрансферазами (MT). Типичная окраска, которую имеют антоцианы, образующиеся из приведенных антоцианидинов, представлена на рисунке, но она зависит от многих факторов: pH, ко-пигментации с бесцветными флавоноидами, комплексами с ионами тяжелых металлов. Заметьте, что метилированию В-кольца (синие прерывистые стрелки) подвергаются антоцианы, а не антоцианидины. Аббревиатуры: халконсинтаза (CHS); халконфлаванонизомераза (CHI); дигидрофлавонол 4-редуктаза (DFR); флаванон-3-гидроксилаза (F3H); флавоноид-3′-гидроксилаза (F3′H); флавоноид-3′,5′-гидроксилаза (F3′5′H); антоцианидинсинтаза (ANS); флавон синтаза (FNS); флавонол синтаза (FLS).
[7], рисунок с модификациями
Подходы и «горячие точки» для модификации цвета у растений
В связи с вышеизложенным «горячими точками» для модификации цвета у растений в основном являются структурные и регуляторные гены. Гены, кодирующие транспортеры, также используются для изменения цвета, но не так часто, как две другие группы генов.
Подходы, с помощью которых можно модифицировать окраску растений, делятся на два типа. К первому типу относятся подходы на основе методов селекции, позволяющие ввести гены от доноров — растений близкородственного вида, имеющих нужный признак. По славам авторов «Чудесника», именно методом селекции был создан этот сорт (рис. 1, слева). Ещё один яркий пример — это пшеница с пурпурным и голубым цветом зерна, обусловленным антоцианами (рис. 7).

Рисунок 7. Пурпурное (слева), голубое (справа) и неокрашенное (в центре) зерно пшеницы.
В дикой природе пшеница с пурпурным зерном впервые была обнаружена в Эфиопии (где, по всей видимости, и появился данный признак), а потом гены, которые обусловливают этот признак, были введены методами селекции в возделываемые сорта мягкой пшеницы [10]. Пшеница с голубым зерном в природе не встречается, но зато голубое зерно имеет родственник пшеницы — пырей. Скрещивая пырей и пшеницу и ведя отбор по данному признаку, селекционеры получили пшеницу с голубым зерном, как у пырея [10]. В вышеназванных примерах в геном пшеницы были введены регуляторные гены. То есть, пшеница и так имеет функциональный аппарат биосинтеза антоцианов (все ферменты необходимые для биосинтеза в порядке), а, вводя методами селекции регуляторные гены от родственных видов, у пшеницы запускают машину биосинтеза антоцианов именно в зерне.
Схожий пример, но уже с использованием второй группы методов манипуляции с окраской — методов генетической инженерии: были получены томаты с повышенным содержанием антоцианов [11]. В норме спелые томаты содержат каротиноиды, в том числе жирорастворимый антиоксидант ликопин; из флавоноидов в них есть небольшое количество нарингенина халкона (2′,4′,6′,4-тетрагидроксихалкон, см. рис. 6) и рутина (гликозированный 5,7,3′,4′-тетрагидрооксифлавонол). Вводя в растения томата генетическую конструкцию, содержащую регуляторные гены биосинтеза антоцианов львиного зева Ros1 и Del под управлением промотора E8, активного в плодах томата, авторам удалось получить томаты с высоким содержанием антоцианов (рис. 8). Таким образом, запустить «машину» биосинтеза антоцианов в определенной ткани можно посредством манипуляции с регуляторными генами, которую проводят либо методами селекции, либо методами генетической инженерии.

Рисунок 8. Томаты с повышенным содержанием антоцианов в плодах, полученные методом генетической инженерии
Пример использование генетической инженерии, для манипуляций с окраской за счет структурных генов биосинтеза антоцианов — пионерская работа, проведенная на петунии [12]. В этой работе впервые в истории были применены методы генетической инженерии с целью изменения окраски растений. В норме растения петунии вовсе не содержат пигментов, производных от пеларгонидина (рис. 6). Это связано с тем, что для фермента DFR (дигидрофлавонол 4-редуктазы) петунии самым предпочтительным субстратом является дигидромирицетин, менее предпочтительным — дигидрокверцетин, а дигидрокемпферол вовсе не используется в качестве субстрата (рис. 6).
Совершенно другая картина субстратной специфичности фермента DFR наблюдается у кукурузы, DFR которой предпочтительнее использует дигидрокемпферол в качестве субстрата [13]. Вооружившись этими знаниями, Мейер с коллегами использовали мутантную линию петунии, у которой отсутствовали функциональные ферменты F3′Н и F3′5′H. Глядя на рисунок 6, нетрудно заметить, что данная мутантная линия накапливала дигидрокемпферол, который не является субстратом для DFR петунии, но зато является субстратом для DFR кукурузы. Введя в мутантную линию генетическую конструкцию, содержащую ген Dfr кукурузы, Мейер получил петунию с несвойственной для неё кирпично-красной окраской цветков (рис. 9).

Рисунок 9. Петунии. а — Мутантная линия петунии с бледно-розовой окраской венчика из-за присутствия следовых количеств антоцианов — производных цианидина и дельфинидина. б — Генетически модифицированная петуния, накапливающая антоцианы — производные пеларгонидина.
Однако не всегда у исследователей под руками есть такие удобные мутанты с отсутствием какой-либо ферментативной активности, поэтому наиболее часто при модификации окраски растений приходится её «выключать» и «включать» другую, требуемую активность. Именно такой подход был реализован при создании первой в мире розы с синей окраской бутонов (рис. 1, справа), схема создания которой приведена на рисунке 10.
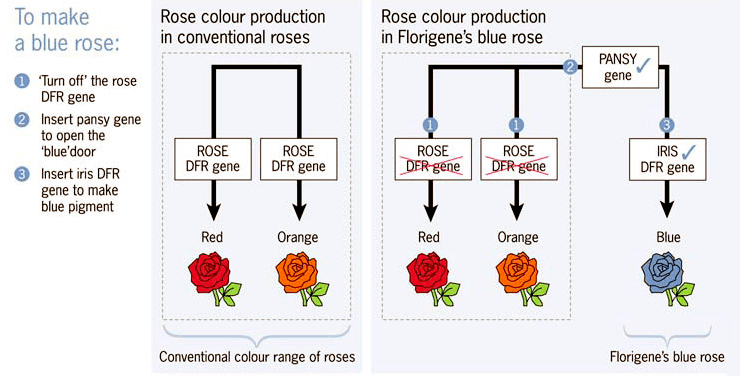
Рисунок 10. Схема создания синей розы.
У роз, созданных усилиями селекционеров, окраска лепестков варьирует от ярко-красных и нежно-розовых до жёлтых и белоснежных. Интенсивное изучение биосинтеза антоцианов у роз позволило установить, что они не имеют F3′5′H-активности, а фермент DFR розы использует в качестве субстратов дигидрокверцетин и дигидрокемпферол, но не дигидромирицетин (рис. 6). Поэтому при создании синей розы учёные выбрали следующую стратегию.
- Сначала «отключали» собственный фермент DFR (для этого применялся подход, основанный на РНК-интерференции).
- Затем в геном розы был введен ген, кодирующий функциональный F3′5′H анютиных глазок.
- После этого в геном был введен ген Dfr ириса, который кодирует фермент с дигидромирицетин-субстратной специфичностью, производящий дельфинидин — предшественник антоцианов с синей окраской.
При этом, чтобы F3′5′H анютиных глазок и F3′H розы не конкурировали друг с другом за субстрат (оба фермента используют в качестве субстрата дигидрокемпферол, рис. 6), для создания синей розы был выбран доступный генотип с отсутствием F3′H активности.
Еще одни яркий пример использования накопленных данных о биосинтезе флавоноидных пигментов с целью создания растений с несвойственной для них окраской — это получение методами генетической инженерии растений торении с жёлтой окраской цветков (рис. 11).
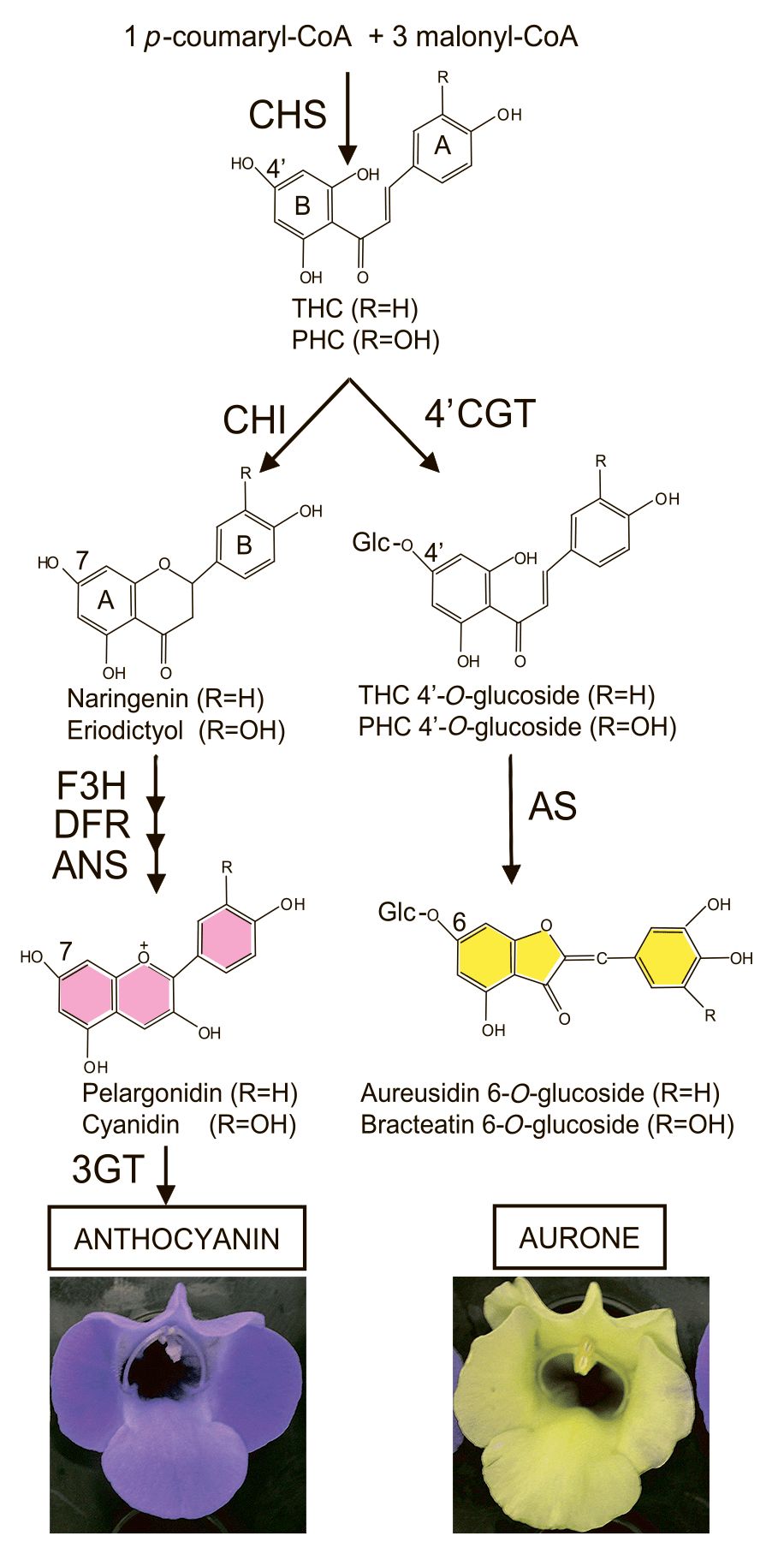
Рисунок 11. Схема биосинтеза антоцианов и ауронов. Снизу приведены цветки обычной, накаливающие антоцианы (слева), и трансгенной торении, накапливающие ауроны (справа). THC — тетрагидроксихалкон, PHC — пентагидроксихалкон.
[14], рисунок с модификациями
Известно, что жёлтую окраску имеют два типа пигментов: ауроны (класс пигментов флавоноидной природы, которые обусловливают яркую жёлтую окраску цветков львиного зева и георгин), и каротиноиды (пигменты цветков томатов и тюльпанов). В ходе анализа биосинтеза ауронов у львиного зева было установлено, что данные пигменты синтезируются из халконов посредством двух ферментов — 4′CGT (4′-халконгликозилтрансферазы) и AS (ауреузидинсинтазы) (рис. 11). Введение генетических конструкций с генами 4′Cgt и As львиного зева в растения торении, в норме имеющие синюю окраску цветков, совместно с ингибированием биосинтеза антоциановых пигментов привело к накоплению ауровнов и, следовательно, к яркой жёлтой окраске цветков (рис. 11). (Читатель самостоятельно может предположить, на уровне работы каких ферментов может быть заблокирован биосинтез антоцианов в этом случае.) Разработанная специалистами стратегия может быть использована для получения желтой окраски цветков не только у торении, но и у герани и фиалки [14].
Приведенные примеры — это лишь малая доля того, какие манипуляции ученые проводят с тем, что им очень хорошо известно — с биосинтезом антоцианов.
Заключение
Как видно, огромному успеху в манипуляции с окраской у растений способствует интенсивное исследование биохимической природы пигментов, а также особенностей их биосинтеза у различных видов растений — как на уровне ферментов, так и на молекулярно-генетическом уровне. Накопленный к настоящему времени багаж знаний об антоциановых соединениях открыл неисчерпаемые возможности для создания декоративных растений с необычной окраской, а также культурных видов растений с повышенным содержанием антоциановых пигментов. И хотя достижения селекции — необычно окрашенные овощи и фрукты — уже сейчас доступны покупателям в ряде стран, декоративные растения, созданные методами генетической инженерии, в большинстве своем на рынке являются ещё достаточно редкими. Дело в том, что из-за ряда нерешенных трудностей — таких, например, как стабильность наследования модифицированной окраски, — они ещё не коммерциализированы (за исключением некоторых сортов петунии, синей розы, лиловой гвоздики). Однако работа в этом направлении продолжается. Будем надеяться, что в скором времени появятся радующие глаз «чудеса» науки, которые будут доступны всем любителям прекрасного.
Литература
- Mary Ann Lila. (2004). Anthocyanins and Human Health: An In Vitro Investigative Approach. Journal of Biomedicine and Biotechnology. 2004, 306-313;
- Wheldale M. The anthocyanin pigments of plants. Cambridge University Press, 1916. — 320 p.;
- Meng Zhao, Hong Ding, Jian-Kang Zhu, Fusuo Zhang, Wen-Xue Li. (2011). Involvement of miR169 in the nitrogen-starvation responses in Arabidopsis. New Phytologist. 190, 906-915;
- Карабанов И.А. Флавоноиды в мире растений. Минск: «Ураджай», 1981. — 80 с.;
- Andersen O.M. and Jordheim M. The anthocyanins. In: Flavonoids: chemistry, biochemistry and applications / ed. by Andersen O.M. and Markham K.R. Boca Raton, FL: CRC Press, 2006. P. 452–471;
- K. L. Hale. (2001). Molybdenum Sequestration in Brassica Species. A Role for Anthocyanins?. PLANT PHYSIOLOGY. 126, 1391-1402;
- Yoshikazu Tanaka, Filippa Brugliera, Steve Chandler. (2009). Recent Progress of Flower Colour Modification by Biotechnology. IJMS. 10, 5350-5369;
- Joseph Mol, Erich Grotewold, Ronald Koes. (1998). How genes paint flowers and seeds. Trends in Plant Science. 3, 212-217;
- Kathleen A. Marrs, Mark R. Alfenito, Alan M. Lloyd, Virginia Walbot. (1995). A glutathione S-transferase involved in vacuolar transfer encoded by the maize gene Bronze-2. Nature. 375, 397-400;
- A. C. Zeven. (1991). Wheats with purple and blue grains: a review. Euphytica. 56, 243-258;
- Eugenio Butelli, Lucilla Titta, Marco Giorgio, Hans-Peter Mock, Andrea Matros, et. al.. (2008). Enrichment of tomato fruit with health-promoting anthocyanins by expression of select transcription factors. Nat Biotechnol. 26, 1301-1308;
- Peter Meyer, Iris Heidmann, Gert Forkmann, Heinz Saedler. (1987). A new petunia flower colour generated by transformation of a mutant with a maize gene. Nature. 330, 677-678;
- G. Forkmann, B. Ruhnau. (1987). Distinct Substrate Specificity of Dihydroflavonol 4-Reductase from Flowers of Petunia hybrida. Zeitschrift für Naturforschung C. 42, 1146-1148;
- E. Ono, M. Fukuchi-Mizutani, N. Nakamura, Y. Fukui, K. Yonekura-Sakakibara, et. al.. (2006). Yellow flowers generated by expression of the aurone biosynthetic pathway. Proceedings of the National Academy of Sciences. 103, 11075-11080.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





