
SciNat за апрель 2026 #4: оцифровка древнего кракена, молекулярный атлас кровеносных сосудов и искусственный лед в Арктике
26 апреля 2026
SciNat за апрель 2026 #4: оцифровка древнего кракена, молекулярный атлас кровеносных сосудов и искусственный лед в Арктике
- 367
- 0
- 0
На обложке последнего выпуска Science Translational Medicine показан кобиметиниб, низкомолекулярный ингибитор ERK-киназы. Ученые обнаружили, что этот препарат обладает еще одним, ранее неизвестным механизмом воздействия на опухоли. Как этот механизм лишает рак шансов на выживание, читайте в нашем новом материале. — Phase separation–based HTS identifies cobimetinib as a YAP-TEAD inhibitor that suppresses hyperactivated YAP-induced cancer progression
.-
Автор
-
Редактор
Из нового выпуска дайджеста «Биомолекулы» вы узнаете о последних достижениях в лечении онкологических заболеваний и муковисцидоза. Теперь мы лучше знаем, как работают клетки: как остеокласты понимают, какие клетки кости нужно уничтожить, а кардиомиоциты — в какую сторону расти? Японские ученые придумали технологию для создания 3D-моделей ископаемых останков вымерших моллюсков. Амбициозный стартап из Нидерландов работает над восстановлением ледового покрова в Арктике. Ждет ли их успех, или они буквально сольют деньги в океан — читайте в нашем дайджесте!
Онкология
Как для известного лекарства нашли новую мишень в раковых клетках
В наших клетках работает сложная система безопасности — сигнальный путь Hippo. Свое название (от англ. hippopotamus — «бегемот») он получил из-за того, что его поломка заставляет клетки и ткани разрастаться до гигантских размеров. В нормальном состоянии Hippo контролирует баланс пролиферации и апоптоза, т.е. деления и гибели клеток. Но если в этой системе происходит сбой, включается режим бесконтрольного роста и деления клеток. Главные виновники этого процесса — белковый комплекс YAP-TEAD. Именно из-за него при поломке системы Hippo клетки начинают «сходить с ума», заставляя опухоль расти бесконтрольно.
Ученые решили найти способ «выключить» этот опасный механизм. Используя современные методы высокопроизводительного скрининга, они обнаружили нечто любопытное: против рака легких и печени может быть эффективен препарат кобиметиниб, который уже одобрен FDA и давно используется в медицине как ингибитор протеинкиназы ERK. Оказалось, что кобиметиниб также обладает второй активностью: он может ингибировать работу белка TEAD и блокирует его работу. Без этого белка комплекс YAP-TEAD распадается, и раковая клетка теряет способность бесконтрольно делиться.
Исследование показало впечатляющие результаты. Препарат смог подавить опухоли, которые уже выработали устойчивость к стандартной терапии (например, к сорафенибу). В сочетании с другими лекарствами кобиметиниб значительно усиливал их эффект, буквально «добивая» раковые клетки в легких и печени. Поскольку кобиметиниб уже одобрен для клинического применения, путь от лаборатории до реальной помощи пациентам может быть гораздо короче. Это открытие дает врачам новый мощный инструмент. Вместо поиска принципиально новых молекул, ученые нашли способ использовать уже известное лекарство, чтобы нанести удар по одной из самых коварных мишеней в онкологии. — Phase separation–based HTS identifies cobimetinib as a YAP-TEAD inhibitor that suppresses hyperactivated YAP-induced cancer progression.
Генная терапия
Как «починить» редкую мутацию, вызывающую муковисцидоз
Муковисцидоз — тяжелое наследственное заболевание, при котором из-за мутаций в гене CFTR нарушается работа некоторых желез, что сильнее всего бьет по дыхательной и пищеварительной системам. Для многих видов мутаций уже есть лекарства, но обладателям редкой «ошибки» 1717-1G>A повезло меньше: для них до сих пор нет одобренной терапии.
Команда исследователей разработала метод редактирования этой мутации. Для этого ученые использовали редактор адениновых оснований (ABE). Если обычные «генетические ножницы» CRISPR/Cas9 разрезают ДНК (что может быть рискованно), то редакторы оснований действуют более аккуратно: они превращают одну букву генетического кода в другую, не разрывая саму спираль. Сначала технологию проверили на культуре клеток человека (HEK293), добившись исправления 30% мутаций. Затем метод испытали на клетках дыхательных путей и «мини-кишечниках» (органоидах), выращенных из биоматериала реальных пациентов с этой мутацией. «Генетический ремонт» прошел успешно. Проверки показали, что после редактирования клетки начали производить рабочий белок, и каналы CFTR снова стали пропускать ионы, как у здорового человека. Это открытие дает надежду на то, что в будущем вместо пожизненного приема таблеток пациенты смогут пройти процедуру редактирования генома, которая один раз и навсегда устранит причину болезни на уровне ДНК. — Functional correction of the untreatable CFTR 1717-1G>A mutation through mRNA- and sgRNA-optimized base editing, «Биомолекула»: «Муковисцидоз — первые надежды», «Трансгенные животные и современная медицина: сломать, чтобы починить».
Эндокринология
Как атлас кровеносных сосудов помог найти рецептор, вовлеченный в развитие диабетической васкулопатии
Сахарный диабет второго типа (СД2) известен большим количеством осложнений. Заболевания периферических сосудов — ангиопатии — ведут к поражению сосудов нижних конечностей, сетчатки и почек. Нарушение функций клеток эндотелия сосудов и макрофагов считаются главными причинами развития ангиопатий. Авторы статьи изучили мезентериальные (брыжеечные) артерии здоровых людей и пациентов с диабетом 2 типа, используя секвенирование одиночных клеток и пространственные методы. В итоге они создали подробный атлас того, как диабет меняет работу генов и связи между клетками в сосудах. Они обнаружили ген TREM2 (triggering receptor expressed on myeloid cells), который приводил к перепрофилированию клеток-макрофагов, заставляя их активно секретировать провоспалительные вещества, способствовавшие быстрому прогрессированию поражения сосудов. Ингибирование TREM2 с помощью антител улучшало состояние сосудов, тогда как активация, наоборот, усугубляла ишемическое повреждение. — Diabetes-induced TREM2–endothelial cell signaling impairs ischemic vascular repair.
Цитология
Как наш организм защищает кости от саморазрушения при воспалении
В нашем теле идет постоянная стройка: одни клетки создают костную ткань, а другие — остеокласты — ее разрушают (это нормальный процесс обновления). Однако при воспалении остеокласты начинают уничтожать ткани слишком быстро, и возникает резорбция кости. Ученые выяснили, какой механизм за этим стоит и кто в организме работает «усмирителем» этого процесса.
Важную роль в этом играет инфламмасома NLRP3 — особый белковый комплекс внутри клетки, который запускает мощную воспалительную реакцию. Если инфламмасома активна, кость разрушается агрессивнее. Существует белок Tmem178, который выступает в роли «предохранителя», сдерживая активацию инфламмасомы.
Авторы исследования выяснили, что самый важный сигнал для «включения» инфламмасомы — это ионы кальция. Если его уровень внутри клетки резко растет, то воспалительный процесс усиливается. Также ученые обнаружили, что Tmem178 ограничивает приток кальция в клетку, и благодаря этому инфламмасома остается «выключенной», а кость не разрушается сверх меры. Для того, чтобы доказать это, авторы вывели мышей, у которых отсутствовал Tmem178. У таких животных кальций беспрепятственно проникал в остеокласты, воспалительный комплекс работал на полную мощность, и кости быстро становились хрупкими. Как только у мышей «выключили» NLRP3, разрушение костей прекращалось. Это открытие объясняет, почему при хронических воспалительных заболеваниях (например, при артрите) часто страдают кости. Понимание роли белка Tmem178 может помочь в создании новых лекарств от остеопороза и других болезней, при которых организм ошибочно разрушает собственный скелет. Полный вариант статьи читайте на страницах Science Signaling. — Activation of the NLRP3 inflammasome in osteoclasts is suppressed by a Tmem178-dependent mechanism that restricts Ca2+ influx.
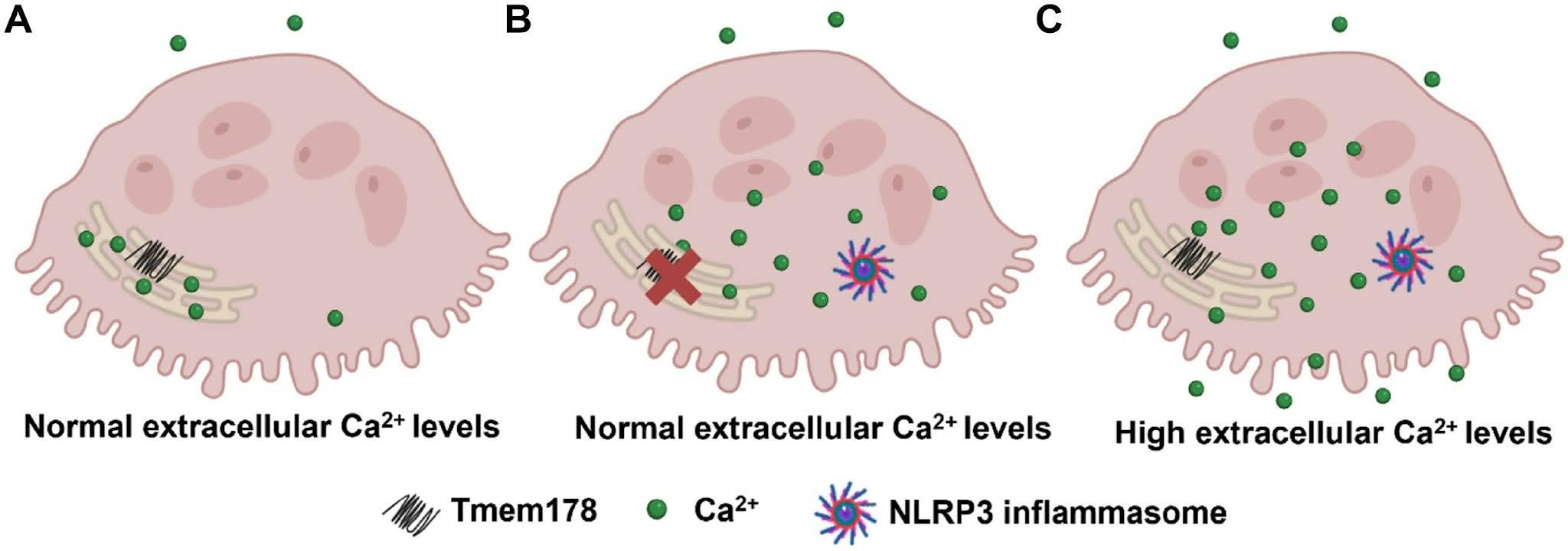
Рисунок 1. Белок Tmem178 предотвращает «включение» инфламмасомы NLRP3 в остеокластах, ингибируя приток кальция.
Как кардиомиоциты «выбирают», в какую сторону им расти
Сердце — это удивительный орган, который умеет подстраиваться практически под любые нагрузки. Чтобы справляться с давлением, его главные клетки — кардиомиоциты — могут расти либо в длину, либо в ширину. Рост «в ширину» называется концентрической гипертрофией: стенки сердца утолщаются, чтобы выдерживать напор крови.
Ученые давно знали, что для такого роста клетке нужно производить много нового белка. Но оставалось загадкой: как клетка понимает, что новые миофибриллы нужно откладывать именно в толщину, а не в длину? Исследователи обнаружили, что ключевую роль в этом процессе играет белок 4EBP1. Оказалось, что при утолщении сердца этот белок получает особый сигнал сразу от двух важных белков клетки: фермента mTORC1 и ядерной протеинкиназы ERK. Самое интересное выяснилось при изучении «географии» клетки. Когда фермент ERK активируется в ядре клетки, он заставляет белок 4EBP1 «перетянуть» производство белков ближе к центру клетки. Вместо того, чтобы равномерно распределять новые белки по всей клетке, рибосомы начинают работать в основном во внутренних слоях. В результате новые структуры мышечных волокон (саркомеры) откладываются в глубине кардиомиоцита, из-за чего он неизбежно раздается вширь.
Это исследование показало, что клетка обладает ювелирной точностью: она может направлять синтез белка в конкретные части клетки. Понимание этого механизма дает медикам новую цель. Если мы научимся управлять этими процессами, то сможем контролировать опасное утолщение стенок сердца при гипертонии и других заболеваниях. — mTORC1 and nuclear ERK spatially control translation in cardiomyocytes through 4EBP1 phosphorylation, «Биомолекула»: «Как вылечить сердце? Достижения современной науки».
Палеонтология
Как японские ученые оцифровали кракена
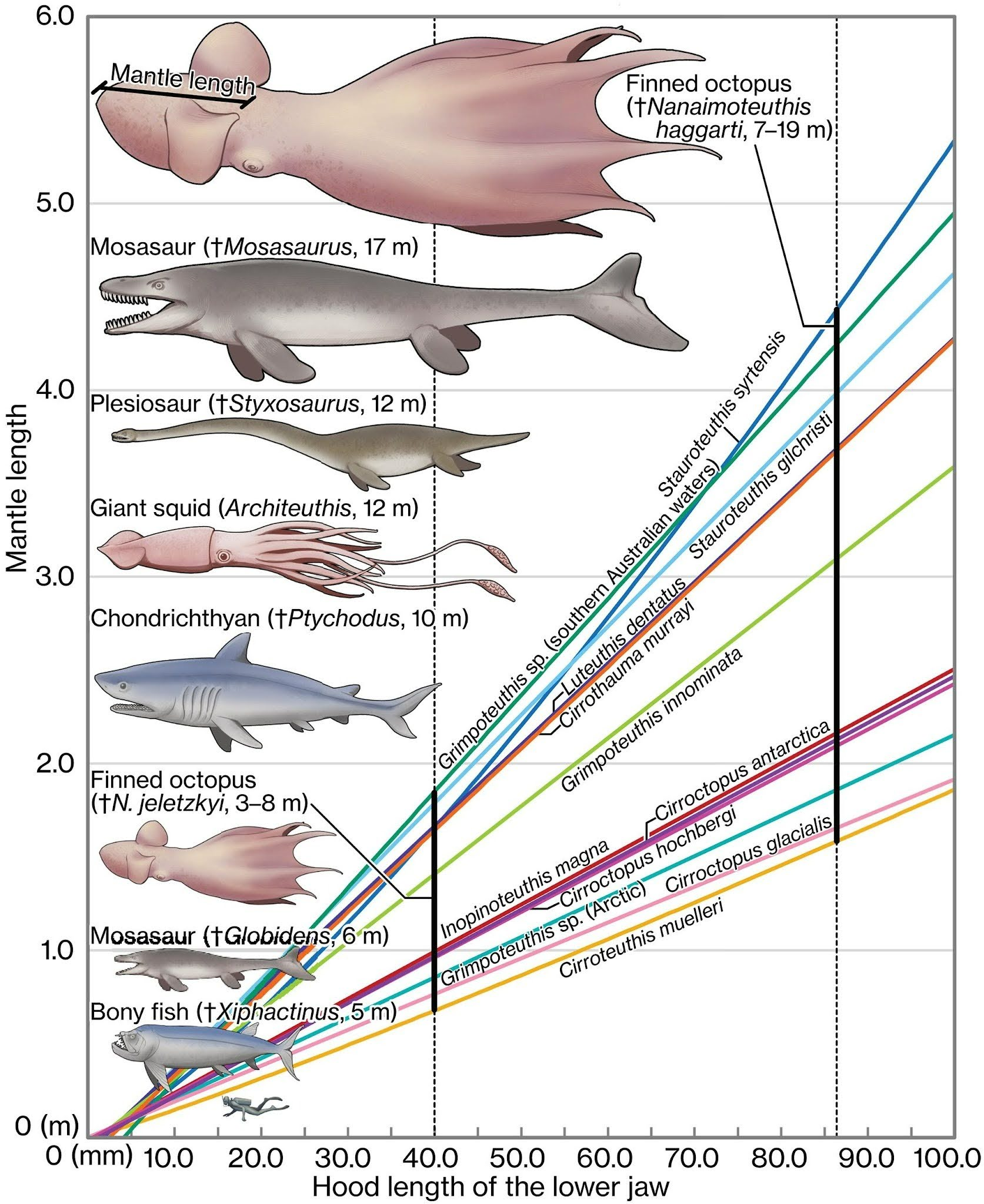
Рисунок 2. Сравнение размеров животных позднего мелового периода.
Истории о гигантских чудовищах-кракенах — популярный миф, пугавший моряков и вдохновлявший писателей и режиссеров. Но что, если это не совсем миф?
Мы знаем сравнительно немного об ископаемых головоногих моллюсках, вымерших многие миллионы лет назад. Отчасти это связано с тем, что мягкие тела беспозвоночных редко сохраняются, из-за чего до нас доходит слишком мало ископаемых останков для изучения. Во многих случаях от осьминогов остаются только хитиновые клювы. Однако они настолько хрупкие, что извлечь их из окружающей породы очень сложно.
В прошлом году ученые из Университета Хоккайдо в Японии представили метод «цифровой добычи ископаемых». Они делают тысячи послойных снимков породы, содержащей окаменелые останки, срезают тончайшие пласты и собирают из них детальную 3D-модель. С помощью этой технологии уже удалось найти множество скрытых остатков и доказать, что некоторые виды моллюсков появились на миллионы лет раньше, чем считалось ранее. В статье, опубликованной в Science на этой неделе, ученые представили описание 15 останков клювов животных, которые датируются ранним меловым периодом (100–72 млн лет назад). В этот период в море господствовали рептилии (плезиозавры, плиозавры и другие). Все найденные ископаемые, как сообщают исследователи, принадлежат двум видам вымерших осьминогов: Nanaimoteuthis jeletzkyi и N. haggarti. Основываясь на размере их клюва, авторы предполагают, что длина N. haggarti, в частности, могла составлять от 7 до 19 метров. На данный момент это может самое крупное из когда-либо описанных беспозвоночных. На основе только размера клюва сложно сделать вывод об их реальном размере, но эти животные вполне могли соперничать по размерам с самыми крупными морскими обитателями того времени. Изучив степень износа клюва осьминогов, ученые сделали вывод о том, что эти животные также могли быть высшими хищниками, как и рептилии того периода, что ставит под сомнение теорию о доминировании позвоночных животных в меловом периоде. — Earliest octopuses were giant top predators in Cretaceous oceans.
Экология
Как искусственный лед поможет «заморозить» глобальное потепление
На этой неделе СМИ облетела новость: окончательно растаял крупнейший в мире айсберг А23а, чья площадь в полтора раза превышала территорию Москвы. Ученые наблюдали за гигантом 40 лет, и, хотя исчезновение льдов — процесс естественный, океанологи уверены: без глобального потепления А23а просуществовал бы значительно дольше.
На фоне этой новости журнал Science рассказал об амбициозном проекте по восстановлению арктических льдов. Полярные шапки работают как природный экран, отражая солнечные лучи и сдерживая нагрев планеты. Их разрушение грозит экологической катастрофой: от затопления побережий до гибели северных экосистем. Исследователи из голландского стартапа Arctic Reflections предложили простое решение: выкачивать воду из-подо льда на поверхность, чтобы она быстрее застывала на морозе.

Рисунок 3. Пейзаж с четырьмя насосами. В ходе эксперимента в канадской Арктике свежеобразовавшийся морской лед оказался ярче окружающих участков, что потенциально позволяет отражать больше солнечных лучей и сохранять более низкую температуру льда.
Первые опыты были неудачными, но недавние тесты у Шпицбергена дали результат. Ученым удалось создать прочный лед, который не только пережил зиму, но и отражал свет на 40% эффективнее природного. Впрочем, авторы признают: «замораживание» Арктики — лишь попытка выиграть время. Главным же способом борьбы с кризисом остается радикальное сокращение выбросов от сжигания топлива. — Artificially engineered sea ice grows—but tests are too small to combat melting.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚




