Время не ждет: как убить дракона под названием «старение»
07 апреля 2025
Время не ждет: как убить дракона под названием «старение»
- 1149
- 0
- 5
Кадр из анимационной адаптации «Басни о Драконе-Тиране» философа Ника Бострома. Дракон-тиран — аллегорическое изображение старения. Объединившись, люди победили дракона с помощью науки и технологий.
Рисунок в полном размере.
-
Автор
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: В современном мире здоровый образ жизни стал модной тенденцией. Но каждый знает: как бы ты ни следил за своим здоровьем, всё равно природа возьмет свое, и наступит старость. В незапамятные времена искать источник вечной молодости было заботой правителей и высшей знати. С ростом уровня качества жизни всё больше людей хотят пожить подольше. Особо храбрые из них не готовы сидеть сложа руки. Они ступили на тропу войны со старостью. Какие подходы самые перспективные? Какие препараты уже протестированы на людях? Чем геронтологии поможет ИИ? Как заработать стартапу в области долголетия? И самое главное: когда, наконец, можно будет купить лекарство от старения в ближайшей аптеке? Обсудим эти вопросы и разберемся, кто взялся за непростую задачу поиска вечной юности и что из этого вышло.
Конкурс «Био/Мол/Текст»-2024/2025
Эта работа опубликована в номинации «Академия & Бизнес» конкурса «Био/Мол/Текст»-2024/2025.

Генеральный партнер конкурса и партнер номинации — международная инновационная биотехнологическая компания BIOCAD.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»

Рисунок 1. Аврора и Тифон, картина Себастьяна Риччи, 1705 год.
Про экономическую и социальную выгоду продления ожидаемой продолжительности жизни человека и активного периода его жизни хотя бы на 10 лет не сказал и не написал только ленивый [1]. Темпы технического прогресса в XXI веке нарастают, а разработка терапии старения по-прежнему ушла недалеко. Аппаратное медицинское обеспечение становится всё лучше и лучше, номинально продлевая человеческую жизнь, но слабо влияя на период активного долголетия. Хотим ли превратиться в Тифона, получившего бессмертие без вечной молодости? Биологию старения можно с увлечением изучать не одно десятилетие, но находятся энтузиасты, утверждающие, что уже сегодня в наших руках есть достаточно инструментов и информации, чтобы радикально отсрочить старость.
Неутешительное предсказание
Достижения в области здравоохранения больше не вносят такой существенный вклад в увеличение продолжительности жизни, как это было в XX веке. В прошлом столетии революция в области долголетия была связана со снижением смертности сначала в молодом возрасте, а затем в среднем и пожилом. С 1990 по 2019 год темпы роста продолжительности жизни в развитых странах замедлились [2].
Авторы статьи ограничились данными до 2019 года, чтобы исключить влияние пандемии COVID-19 на результаты исследования.
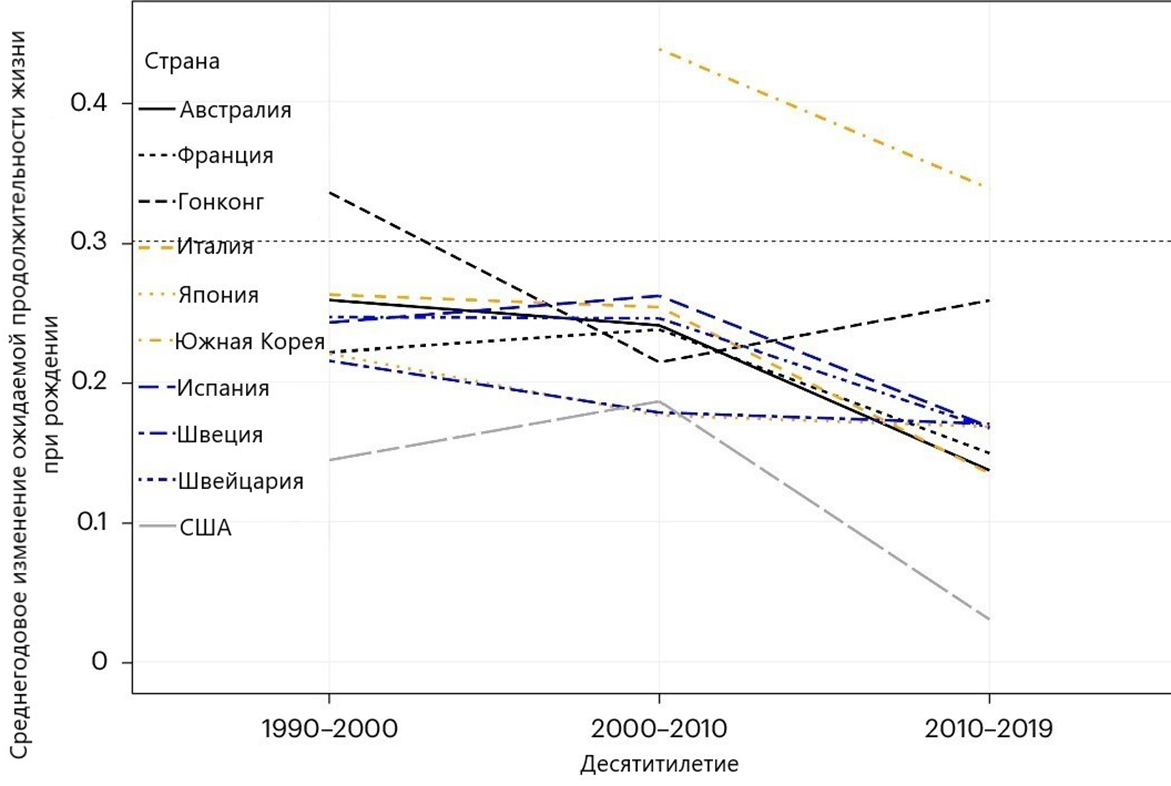
Рисунок 2. Среднегодовое увеличение ожидаемой продолжительности жизни при рождении (в годах) каждые десять лет в 9 группах населения с самой высокой ожидаемой продолжительностью жизни и в США: 1990-е, 2000-е, 2010-е гг. Темпы увеличения ожидаемой продолжительности жизни замедлились во всех популяциях, кроме Гонконга. Пунктирная линия указывает на среднегодовое изменение ожидаемой продолжительности жизни при рождении, ассоциированное с радикальным продлением жизни.
адаптировано из [2]
Ученые посчитали, что наиболее репрезентативной выборкой для прогнозирования распределения выживаемости при радикальном продлении жизни являются японские женщины. Чтобы ожидаемая продолжительность жизни при рождении возросла до 110 лет, нужно, чтобы около 70% доживали до 100 лет и около 6% — до 150 с лишним лет. Эта цифра на 28 лет превышает возраст самого долгоживущего человека в истории — Жанны Кальман.
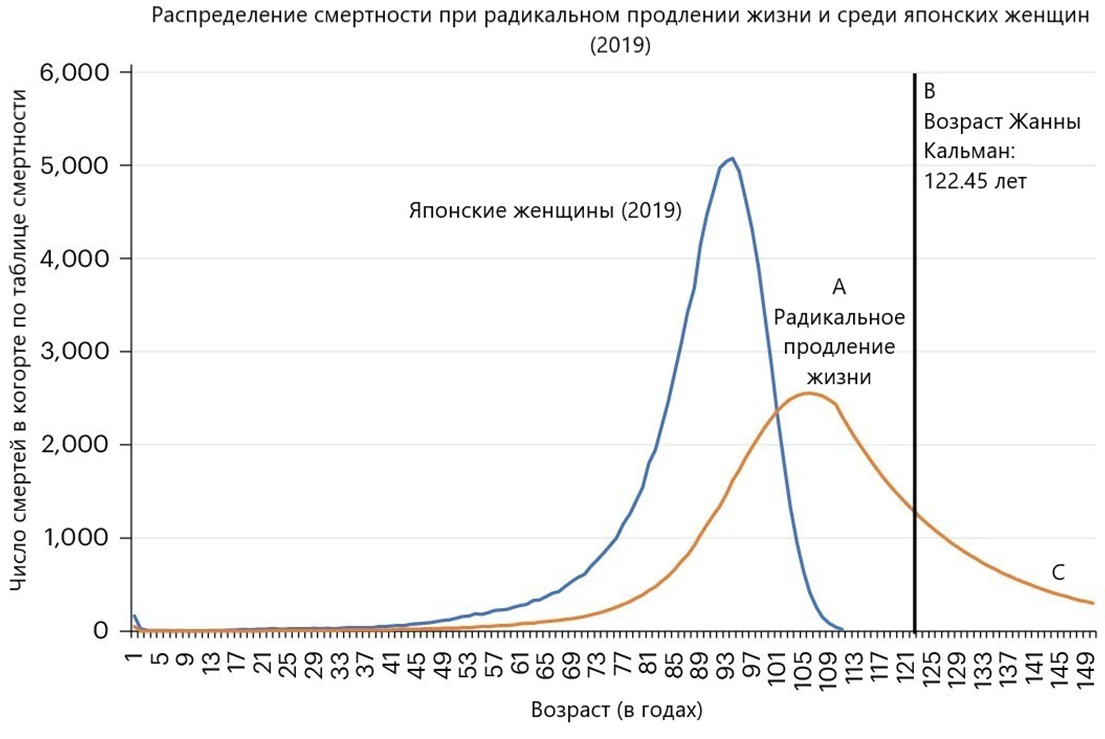
Рисунок 3. Необходимая динамика выживания для японских женщин в возрасте 100, 122 и 150 лет. Доказательства радикального продления жизни требуют распределения смертности, которое резко отличается от наблюдаемого среди населения с самой высокой средней продолжительностью жизни.
адаптировано из [2]
Смертность от старости с 1990 года не снижалась даже близко с темпами, необходимыми для радикального увеличения продолжительности жизни в этом столетии. Естественная продолжительность жизни человеческой популяции при отсутствии какого-либо медицинского вмешательства на протяжении всей жизни неизвестна, но можно предположить, что она будет намного ниже продолжительности жизни, наблюдаемой сегодня в странах с высоким уровнем дохода. Недавнее ее увеличение, вероятно, является результатом добавления так называемого «искусственного времени» — времени выживания, обусловленного медицинскими и общественными мерами.
Таким образом, на сегодняшний день для увеличения ожидаемой продолжительности жизни при рождении необходимо ускорение снижения уровня смертности в пожилом возрасте. Именно «таблетка от старости» позволит человечеству преодолеть «стеклянный потолок» ограничения долголетия к концу ХХI века.
Голубые зоны
Первое, что приходит на ум, когда человек задается вопросом «Как жить дольше?», — это подсмотреть секрет долголетия у тех, кто уже прожил очень долгую жизнь. Так появилась концепция «голубых зон» [3],[4]. Согласно ей, на Земле существуют места, где доля долгожителей существенно больше, чем в популяции в целом. К ним относятся остров Икария (Греция), Окинавские острова (Япония), провинция Нуаро (Италия), Лома-Линда (США), полуостров Никоя (Коста-Рика). Однако лауреат Шнобелевской премии по демографии 2024 года доктор Сол Джастин Ньюман получил интересные результаты [5]: регионы с наибольшим числом долгожителей характеризуются высоким уровнем бедности, недостаточным финансированием системы здравоохранения, низкой средней продолжительностью жизни, большим количеством пожилых внутренних иммигрантов, а также частыми случаями подделки документов и ошибок в свидетельствах о рождении и смерти. Все эти факторы в совокупности способны сильно влиять на демографические показатели и подталкивают людей искать чудо долголетия там, где его, возможно, и нет.
Новое применение старым препаратам
Поскольку старение является причиной и основным фактором риска развития болезней пожилого возраста [6], стоит проверить, нет ли среди существующих препаратов для лечения данных состояний тех, которые будут влиять на старение организма в целом. Например, сахароснижающий препарат метформин уже давно рассматривается в контексте профилактики и замедления старения [7]. Он показал свою эффективность в отношении сердечно-сосудистых заболеваний, рака, нейродегенеративных заболеваний, хронической болезни почек, синдрома поликистозных яичников, заболеваний опорно-двигательного аппарата [7]. Однако получены данные, что метформин уменьшает положительные эффекты физической активности [8].
10 лет назад было получено разрешение на проведение исследования The Targeting Aging with Metformin Trial (TAME), в котором как раз планировалось комплексно оценить его влияние на продолжительность жизни и развитие заболеваний, ассоциированных со старением [9]. Каждый год выходили статьи о том, что TAME будет запущено в скором времени. В одном из последних интервью организатор и идейный вдохновитель Нир Барзилай заявил, что задержка была связана в первую очередь с пандемией COVID-19 и недостаточным финансированием на проведение клинических испытаний в заявленном объеме. На данный момент предполагается задействовать хотя бы 4 научных центра из запланированных 14.
Вероятно, одна из причин нежелания государства и частных инвесторов финансировать данное исследование кроется в том, что метформин не защищен патентом и не слишком коммерчески выгоден. Как отмечает сам Нир Барзилай, цель проведения данного исследования — доказать FDA, что можно контролировать старение, а вместе с ним и целый пул возрастных заболеваний. Пока что единственная страна, которая разрешает проводить клинические испытания препаратов непосредственно против старения без фокуса на конкретных заболеваниях — Сингапур.
Не в бровь, а в глаз
На сегодняшний день опубликовано достаточное количество обзорных статей, в которых выделены основные признаки старения. В 2013 году Карлос Лопес-Отин с соавторами описал 9 ключевых признаков старения, распределив их на 3 группы (первичные, антагонистические, интегративные) [10]: нестабильность генома, укорочение теломер, эпигенетические альтерации, нарушение протеостаза, нарушение распознавания питательных веществ, митохондриальная дисфункция, клеточное старение, истощение пула стволовых клеток, изменение межклеточного взаимодействия. Через 10 лет ученые добавили еще 3 признаков [11]: нарушение макроаутофагии, хроническое воспаление и дисбиоз.
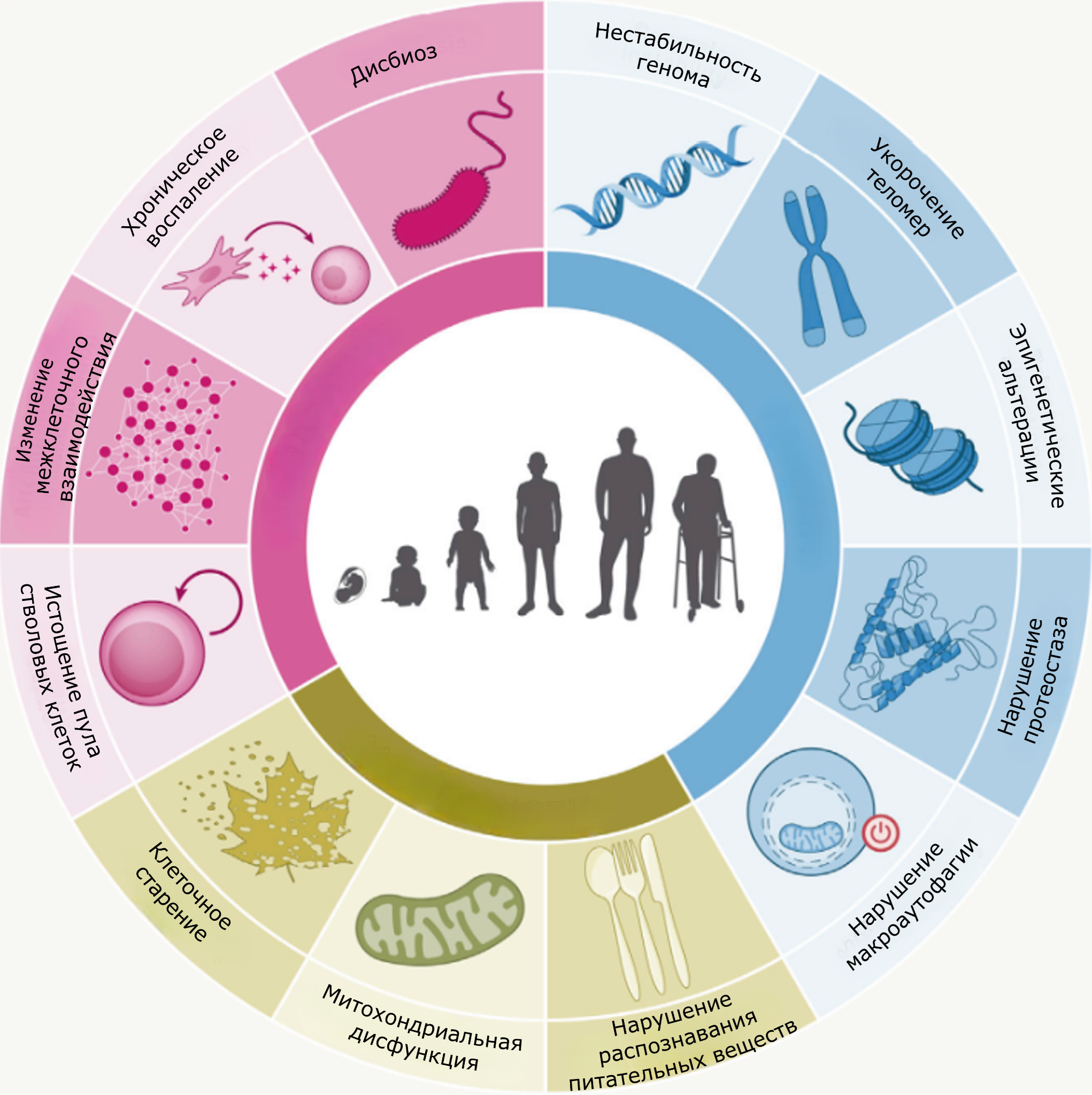
Рисунок 4. Ключевые признаки старения.
На основе существующих данных Александр Панчин с соавторами предлагает сводную схему, где также отражены достижения в разработке терапии против каждого из признаков старения [12].

Рисунок 5. Список ключевых признаков старения, описанных на сегодняшний день. Те признаки, для которых известна таргетированная терапия, продлевающая жизнь млекопитающих, обозначены «+», остальные «—».
С точки зрения науки, создание панацеи от старости — утопия, а вот выбрать конкретный механизм старения и попытаться воздействовать на него — другое дело. Первопроходцы терапии старения — компании Geron, Elixir Pharmaceuticals, Sirtus — решили пойти по этому пути и потерпели неудачи в клинических испытаниях. После провала Sirtus, в который вложили 700 миллионов долларов еще на доклинической стадии, инвесторы несколько лет обходили стороной стартапы в области терапии старения.
Несмотря на кажущуюся простоту такого подхода, пока что все клинические исследования таких препаратов провалились или показали неоднозначные результаты. Неудача постигла ResTORBio в 2019 году с ингибитором TORC1 RTB101 и Unity Biotechnology в 2020 году с сенолитиком UBX0101 [9]. Unity Biotechnology сосредоточился на разработке антиVEGF-терапии для лечения диабетического макулярного отека (ДМО) и возрастной макулярной дегенерации (ВМД). UBX1325 — ингибитор BCL-xL (регулятор апоптоза, его экспрессия повышена в патологических сосудах сетчатки) — проходит II фазу клинических испытаний в терапии ДМО. ResTORbio слилась с Adicet Bio, разработчиком гамма-дельта-CAR—T—терапии против аутоиммунных заболеваний и рака. Таким образом, обе компании отказались от терапии непосредственно старения в пользу разработок, обещающих более ранний коммерческий успех.
Другой способ поиска лекарства от старости кроется в изучении гетерохронного парабиоза [13]. Эксперименты на мышах демонстрировали многообещающие результаты еще с 2005 года. Что касается людей, идея спровоцировала появление компаний, предлагающих услуги по переливанию «молодой» крови, и так называемых blood boys — молодых персональных доноров, — а также привлекла внимание миллиардеров и технологических предпринимателей, в частности Брайана Джонсона и Питера Тиля. Переливание крови от blood boy даже обыгрывалось в сериале HBO «Кремниевая долина». Стартап Ambrosia продавал данную услугу за $8000, зарегистрировав свою деятельность как проведение клинического испытания [14]. При этом не было ослепления и плацебо-контроля. Было заявлено, что 600 человек в возрасте 35 лет и старше получат плазму от донора моложе 25 лет, а кровь участников будет протестирована перед инфузиями и через месяц после на более чем 100 биомаркеров. В 2019 году FDA выпустило предупреждение, согласно которому переливание крови от молодых доноров для профилактики старения и возраст- ассоциированных заболеваний не имеет доказанной эффективности и безопасности. После этого заявления Ambrosia прекратила свою деятельность.
К настоящему времени испытания переливания «молодой» крови пожилым и/или больным показали неоднозначные результаты. В исследовании 2020 года был сделан вывод, что парабиоз восстанавливает экспрессию генов в отдельных типах клеток [15]. Несмотря противоречивые данные, ученые задались вопросом: «Что такое есть в „молодой“ крови, что улучшает некоторые показатели старого организма?». Компания Alkahest концентрируется на изучении протеома плазмы. Мишени их терапии — хронокины — белки, концентрация которых в плазме с возрастом изменяется. Регулируя их уровень в крови, можно способствовать регенераторным и противодействовать дегенеративным процессам. Один из кандидатов Alkahest — AKCT4290 — ингибитор CCR3, рецептора эотаксина. Эотаксин — хемокин, хемоаттрактант преимущественно для эозинофилов. Его уровень повышен при нормальном старении и болезнях пожилого возраста (болезни Альцгеймера, болезни Паркинсона, возрастной макулярной дегенерации и др.). Компания не афишировала результаты II фазы клинических исследований, завершившихся в 2018 и 2021 годах. Успехи Alkahest не остались незамеченными: в 2020 году Griffols приобрел Alkahest за 146 миллионов долларов.

Рисунок 6. Прогресс Alkahest в разработке лекарственных препаратов, действующих на хронокины.
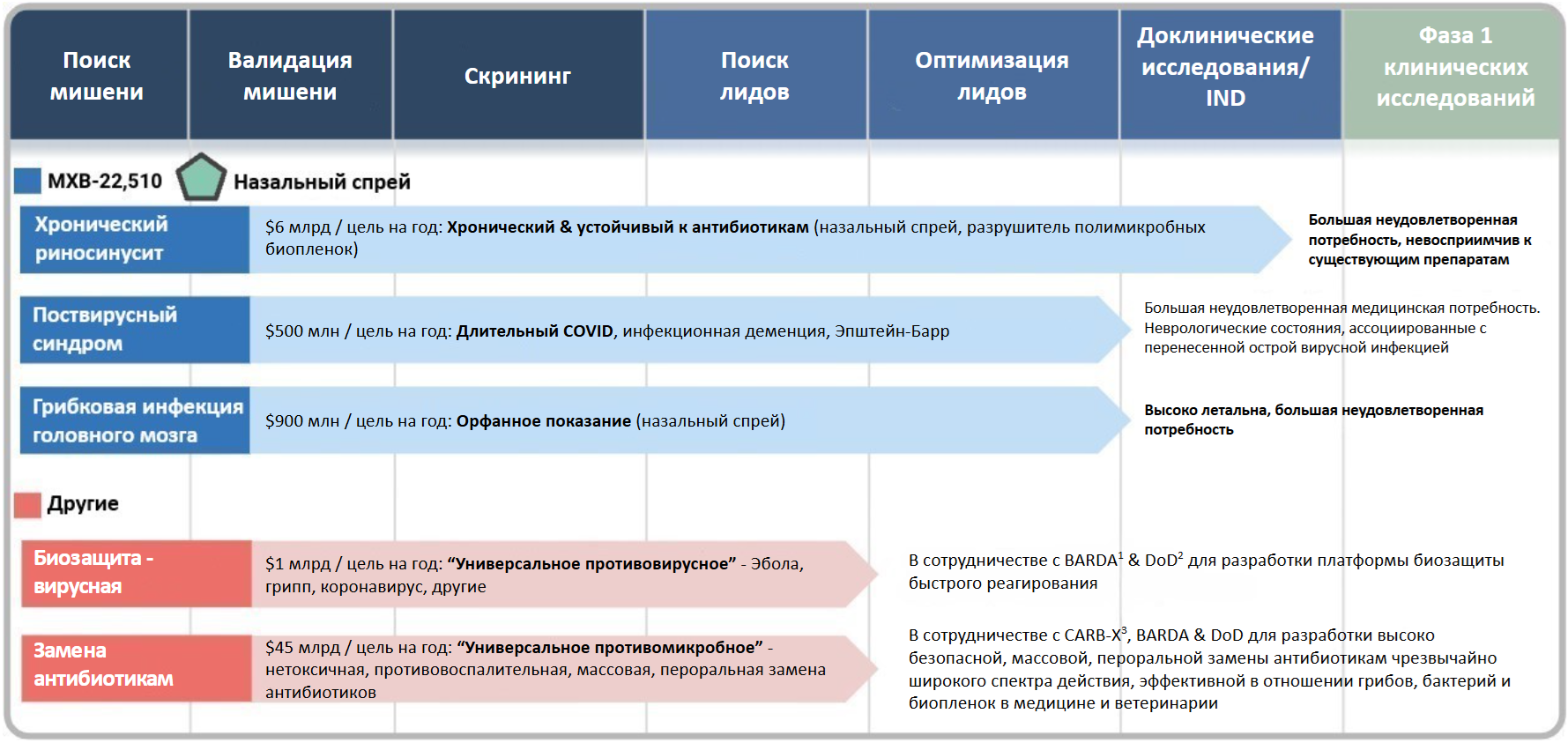
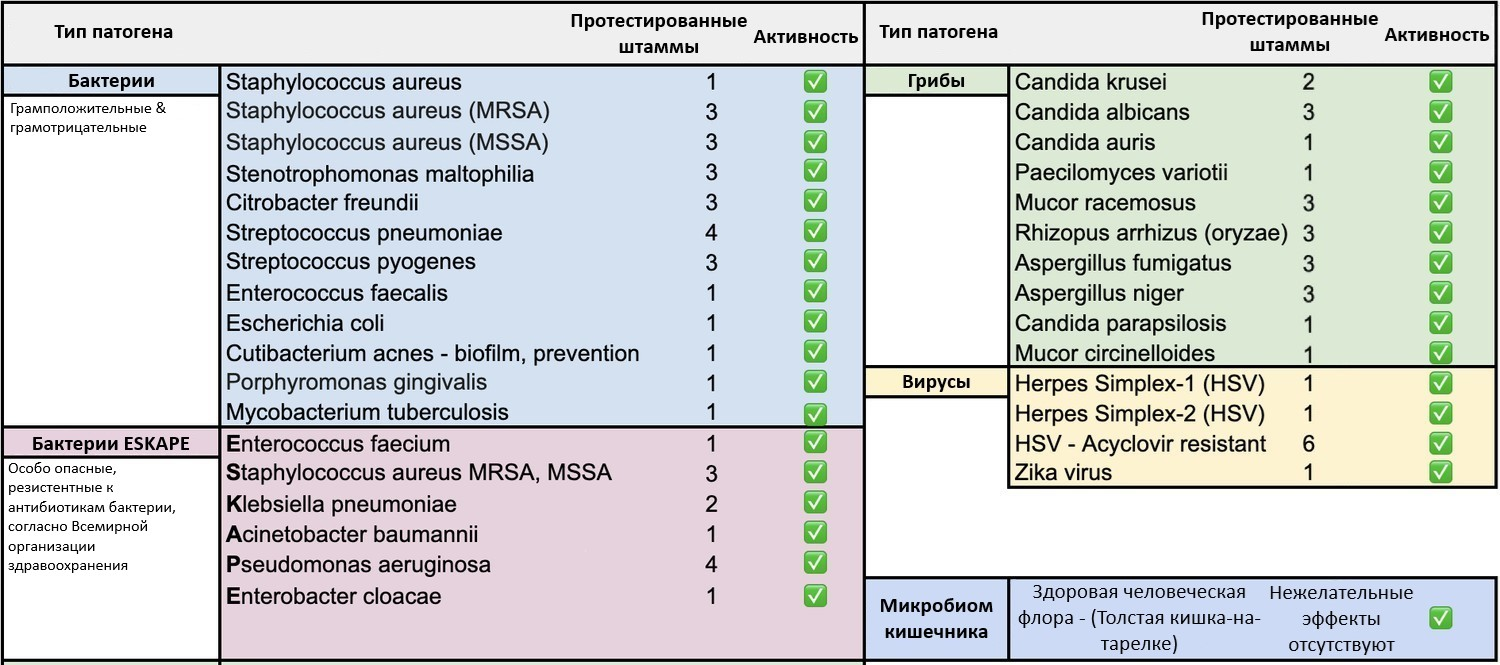
Компания Maxwell Biosciences стремится опровергнуть утверждение One drug, one bug. Она разрабатывает практически универсальное противоинфекционное лекарственное средство, эффективное в том числе в отношении биопленок, и не действующее на нормальную микрофлору человека. Его же они предлагают в качестве лекарства от старения. 2 года ученые с помощью ИИ сравнивали данные крови молодых и старых организмов (мышей, человека). Кандидатом был выбран пептид LL-37. Он участвует в процессах роста, регулирует воспаление, укрепляет ключевые ткани, экспрессируется повсеместно, возможно, является самым важным антимикробным пептидом, и его экспрессия уменьшается с возрастом. Экспрессия LL-37 повышается при соблюдении общепринятых принципов ЗОЖ. Данный пептид быстро разрушается протеазами и элиминируется из кровотока. Была разработана его более стабильная форма — кларомер MXB-22,510 — лидирующий актив Maxwell Biosciences. Клинические испытания запланированы на 2025 год.
В 2021 [16] и 2022 [17] году вышли статьи, демонстрирующие, что «омоложение» старых мышей происходит и при замене половины крови «возраст-нейтральным» 5% раствором альбумина. Инфузионная терапия уже давно стала неотъемлемой частью клинической практики и, возможно, получит новое применение в геронтологии.
Комбинированная терапия
Неудачи в испытаниях препаратов, направленных на одну из причин старения, возможно, обусловлены тем, что старение — сложный мультифакторный процесс. Один механизм развития подавляется, тогда как остальные остаются нетронутыми. Действительно, сейчас стандарт лечения многих заболеваний — это комбинированная терапия несколькими препаратами разных групп. На мышиных моделях был показан синергический эффект некоторых потенциальных препаратов от старения [12].
На сегодняшний день есть предположение, что одной комбинацией можно поразить сразу 13 ключевых признаков старения, а без использования генетических модификаций — 9 [12]. Как выбрать препараты и комбинации, которые следует тестировать в первую очередь? Ключевую роль играют такие показатели, как стоимость, эффективность в отношении уже состарившегося организма, возможность поддержания вмешательства в течение длительного времени, проверенная безопасность, разнообразие мишеней в комбинации, взаимодействие препаратов.
Критики этого подхода заявляют, что вероятность суммации — и тем более синергии — нескольких препаратов комбинации мала, и в большинстве случаев увеличение продолжительности жизни либо будет обусловлено препаратом с самым длительным эффектом, либо и вовсе не произойдет.
В 2023 году LEV Foundation совместно с Ichor Life Sciences инициировал цикл масштабных исследований комбинированной терапии старения на мышах RMR (Robust Mouse Rejuvenation). Кейтлин Льюис и Обри ди Грей предлагают применение не менее 4 вмешательств, каждое из которых показало свою эффективность в увеличении средней и максимальной продолжительности жизни мышей. Терапия направлена на конкретные признаки старения и тестируется на животных, преодолевших рубеж половины жизни. Комбинированная терапия в RMR1 включает в себя рапамицин, навитоклакс (противоопухолевый препарат, сенолитик), трансплантацию гемопоэтических стволовых клеток и экспрессию теломераз. По предварительным данным, RMR1 продемонстировало увеличение продолжительности жизни на 10–15%, однако были выявлены различия влияния одинаковых интервенций на мужских и женских особей. Причины слабого результата авторы видят, в частности, в способе доставки препаратов и частоте их введения. В RMR2 LEVF намерен протестировать рапамицин, дейтерированные жирные кислоты, сывороточный альбумин, частичное клеточное перепрограммирование и мезенхимальные стволовые клетки. Ученые оценивают не только показатели продолжительности жизни, но и взаимодействия между различными вмешательствами. Помимо научной цели, данное исследование призвано показать, что старение — это поддающаяся решению медицинская проблема, а не закономерный факт жизни.
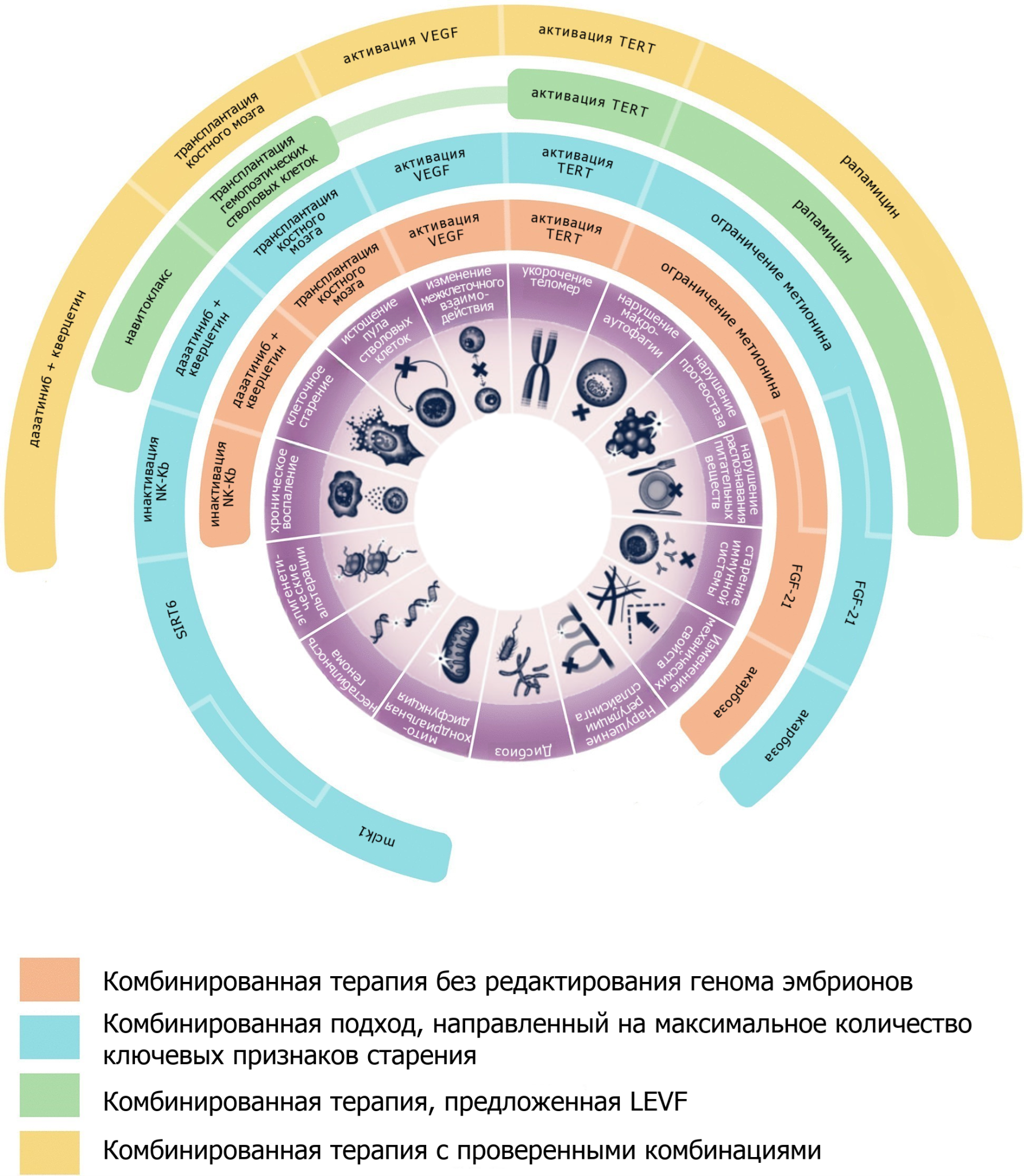
Рисунок 8. Возможные стратегии комбинированной терапии старения.
В 2015–2017 годах с Стэнфорде было проведено клиническое исследование TRIIM [18]. Его целью было изучение возможности использования рекомбинантного человеческого гормона роста для предотвращения или устранения иммунологического старения среди 9 относительно здоровых мужчин в возрасте от 51 до 65 лет. Для регенерации тимуса использовали соматотропин, а чтобы ограничить диабетогенный эффект гормона роста в «коктейль молодости» добавили метформин и дигидроэпиандростерон (ДГЭА). При этом и метформин, и ДГЭА не обладают тимотропным действием, однако улучшают некоторые показатели старения. Все перечисленные препараты уже одобрены FDA для лечения различных заболеваний. За 2 года плотность тимуса у участников увеличилась. 4 вида эпигенетических часов показали снижение эпигенетического возраста на 2,5 года по сравнению с хронологическим, которое сохранялось в течение 6 месяцев. Несмотря на активацию иммунной системы, хроническое воспаление не усилилось, а уровень СРБ статистически значимо снизился через 9-12 месяцев. Увеличился лимфоцитарно-моноцитарный индекс (ЛМИ), высокие показатели которого связаны с лучшими прогнозами в отношении 8 типов рака, сердечно-сосудистых заболеваний, инсульта, генерализованного воспаления. Увеличилась популяция наивных Т-лимфоцитов. Были отмечены и неожиданные результаты: потемнение волос, увеличение СКФ, снижение количества моноцитов, снижение уровня ПСА и PD-1. Ученые предположили, что эпигенетическое омоложение могло быть связано с повышением уровня HAD+ в тканях. Ранее уже было показано, что трансплантация тимуса может влиять на неиммунологические аспекты старения. Однако предполагается, что омолаживающие эффекты вмешательства связаны не только с влиянием регенерированного тимуса, но и с непосредственным действием каждого вещества на процессы старения вместе и по отдельности.
Главный исследователь TRIIM и соучредитель Intervene Immune Грег Фейхи предполагает, что ГР и ДГЭА могут быть теми самыми факторами молодости при гетерохронном парабиозе. В 2020 году было запущено расширенное исследование TRIIM-X. Его цель — доказать, что результаты TRIIM не были случайностью. В нем участвовали 28 мужчин и женщин в возрасте от 40 до 80 лет. Недавно завершилась часть TRIIM-XA. Результаты пока не опубликованы, но Грег Фейхи говорит о следующих выводах: увеличилось количество наивных Т-клеток, подрос тимус, потемнели и стали лучше расти волосы на голове и теле, улучшилась физическая форма (увеличилась мышечная сила и VO2max), увеличилась мышечная масса и уменьшился процент жира, купировалась анемия, снизились уровни ПСА и PD-1. Таким образом, похоже, что результаты TRIIM подтвердились. Ученые планируют продолжать исследования в данном направлении, расширяя возрастной диапазон и оптимизируя терапию. TRIIM получил небольшое финансирование, и участники платят за себя сами. Компания Intervene Immune создана для коммерциализации разработки.
Эпигенетический откат
Клеточное перепрограммирование — одно из самых «модных» направлений среди стартапов в области долголетия. Помимо получения индуцированных плюрипотентных стволовых клеток, эпигенетическое перепрограммирование позволяет омолаживать сенесцентные клетки. Пока ни одна компания не перешла к клиническим испытаниям. В этом направлении работает и компания Altos — на данный момент самый финансируемый биотех-стартап с инвестициями в 3 миллиарда долларов.
ИИ и Большие данные
С появлением искусственного интеллекта подходы к поиску терапии старения расширились. Мишень для нового лекарственного препарата можно выбрать на основе больших данных, таких как транскриптомика. Кроме того, ИИ позволяет отделить причину старения от его следствия. Такой подход позволит сэкономить время и деньги на доклинических и клинических испытаниях, значительно сокращая список потенциальных препаратов. В то же время исчезает необходимость строить полноценную биотехнологическую компанию с полным циклом разработки лекарственного препарата. Стартапы могут продавать свои наработки большой фарме. Так, с 2023 года стартап Gero сотрудничает с Pfizer. Коллаборация направлена на выявление потенциальных терапевтических мишеней для лечения фиброзирующих заболеваний.
Гонконгская компания Insilico Medicine, в свою очередь, разработала платформу поиска биологических мишеней с поддержкой ИИ PandaOmics [19]. Они предлагают искать цели двойного назначения — одновременно для терапии болезней и старения. С января 2022 Incilico Medicine сотрудничает с китайским фармацевтическим гигантов Fosun Pharma. Это облегчает выход на китайский рынок и позволяет извлечь выгоду из «инфраструктуры стоимостью полмиллиона долларов и сотен тысяч ученых».
Помимо омиксных данных, ИИ оценивает текстовую информацию, финансы, точку зрения ключевых лидеров мнений. Предусмотрена приоритизация потенциальных мишеней по важнейшим параметрам. В частности, преимущество получили мишени, дисрегуляция которых имеет место в развитии 2 и более классов заболеваний (воспалительных, неврологических, метаболических, фиброзирующих).
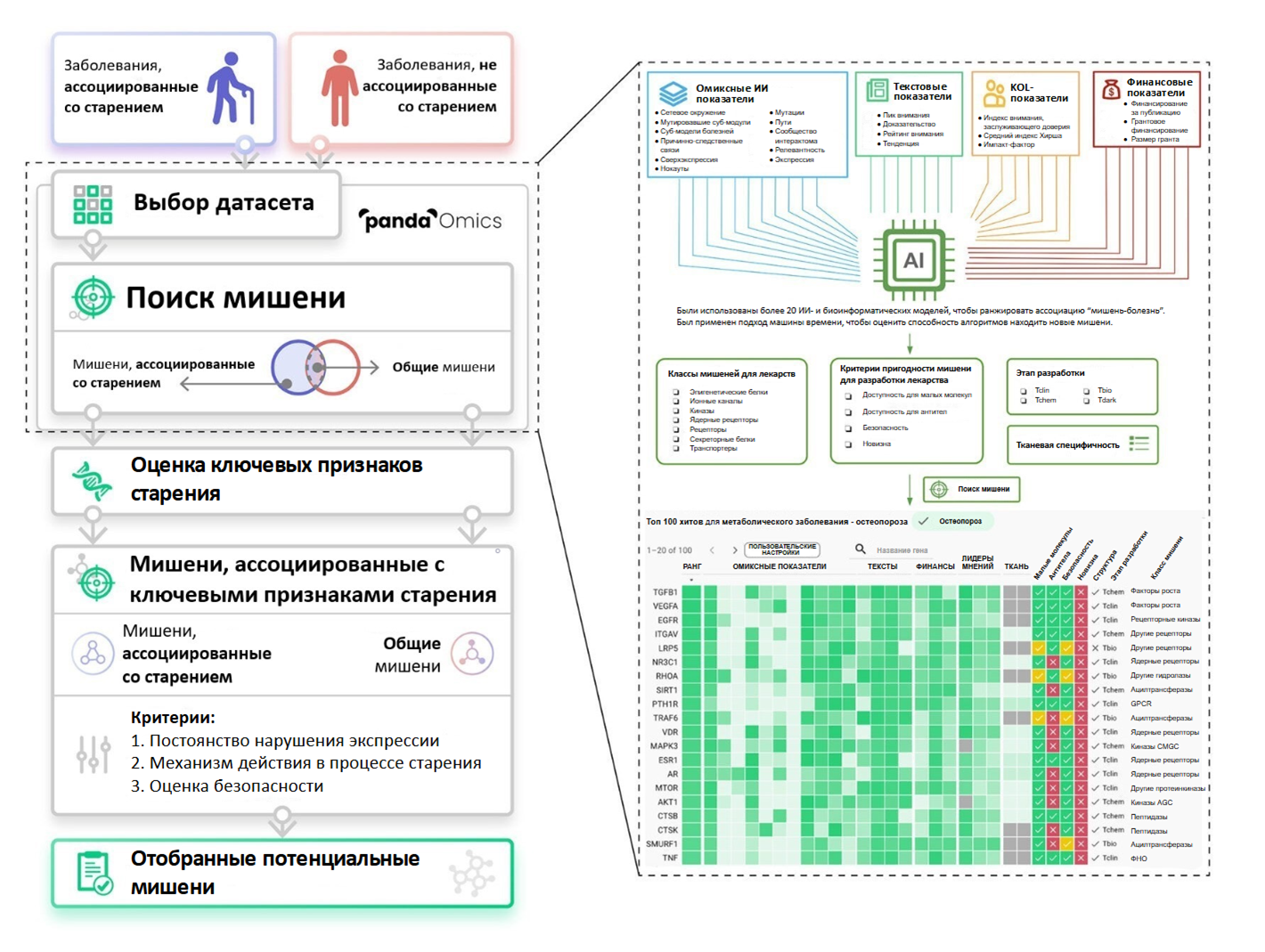
Рисунок 9. Алгоритм работы PandaOmics. Транскриптомные наборы данных о возрастных заболеваниях и болезнях, не ассоциированных со старением, обработаны PandaOmics. Ранжирование генов в каждом заболевании проводилось с помощью более 20 моделей ИИ. Список потенциальных мишеней с двойным назначением предложен путем оценки их связи с признаками старения, профилями экспрессии, механизмом действия и безопасностью.
Если сопоставить полученные результаты со схемой ключевых признаков старения, получится следующая картина:
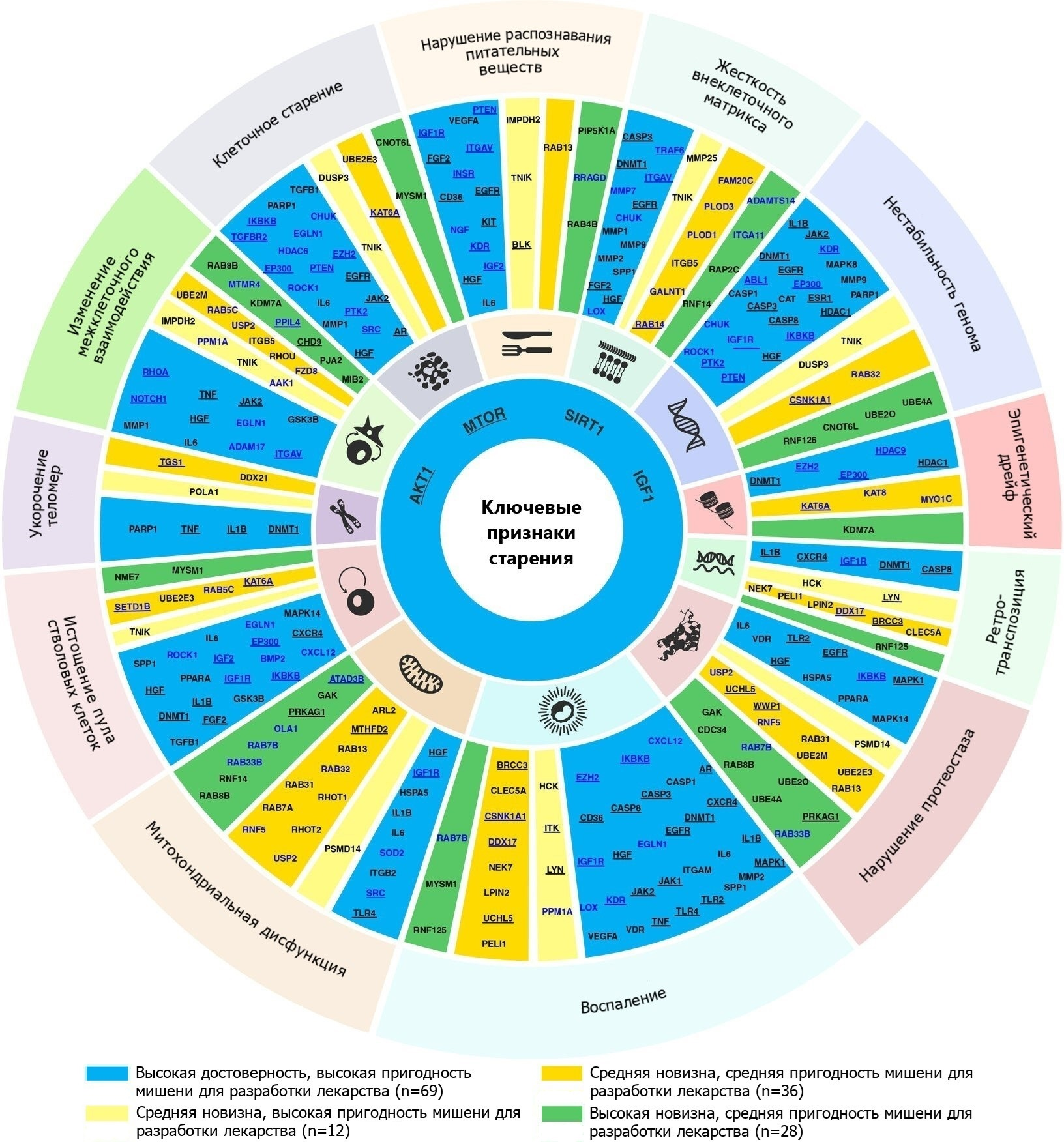
Рисунок 10. Связь мишеней, полученных с помощью ИИ, с ключевыми признаками старения. Потенциальные мишени (145 генов) ранжированы по степени новизны и потенциалу стать лекарственным средством (определяется доступностью мишени малым молекулам). Синим написаны названия генов возрастных заболеваний, черным — заболеваний, не связанных со старением. Гены-драйверы онкологических заболеваний подчеркнуты.
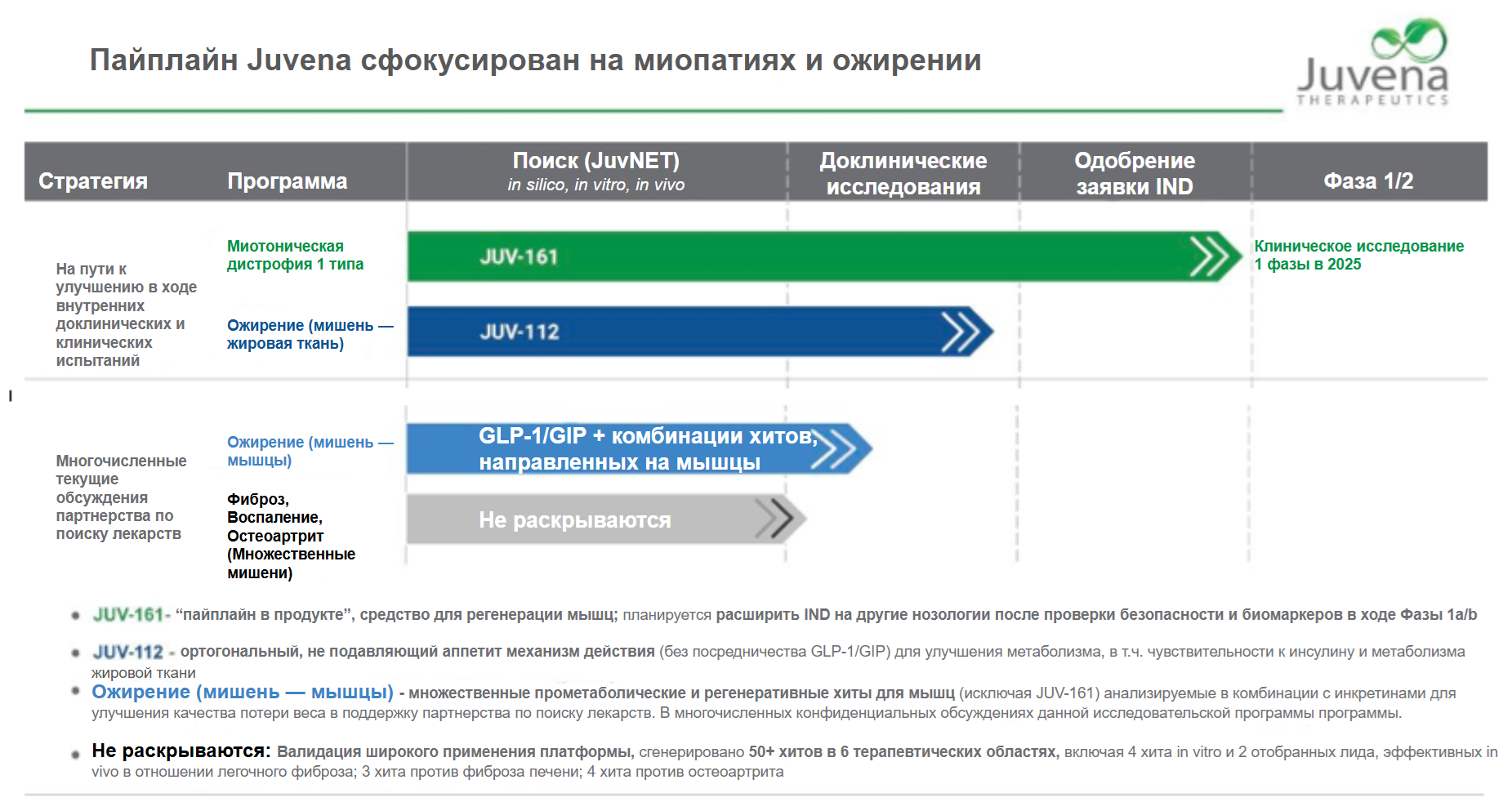
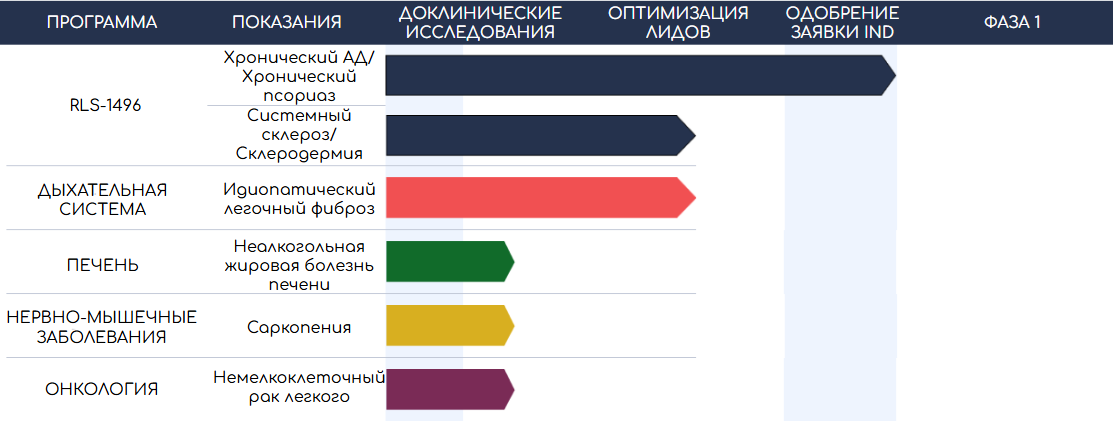
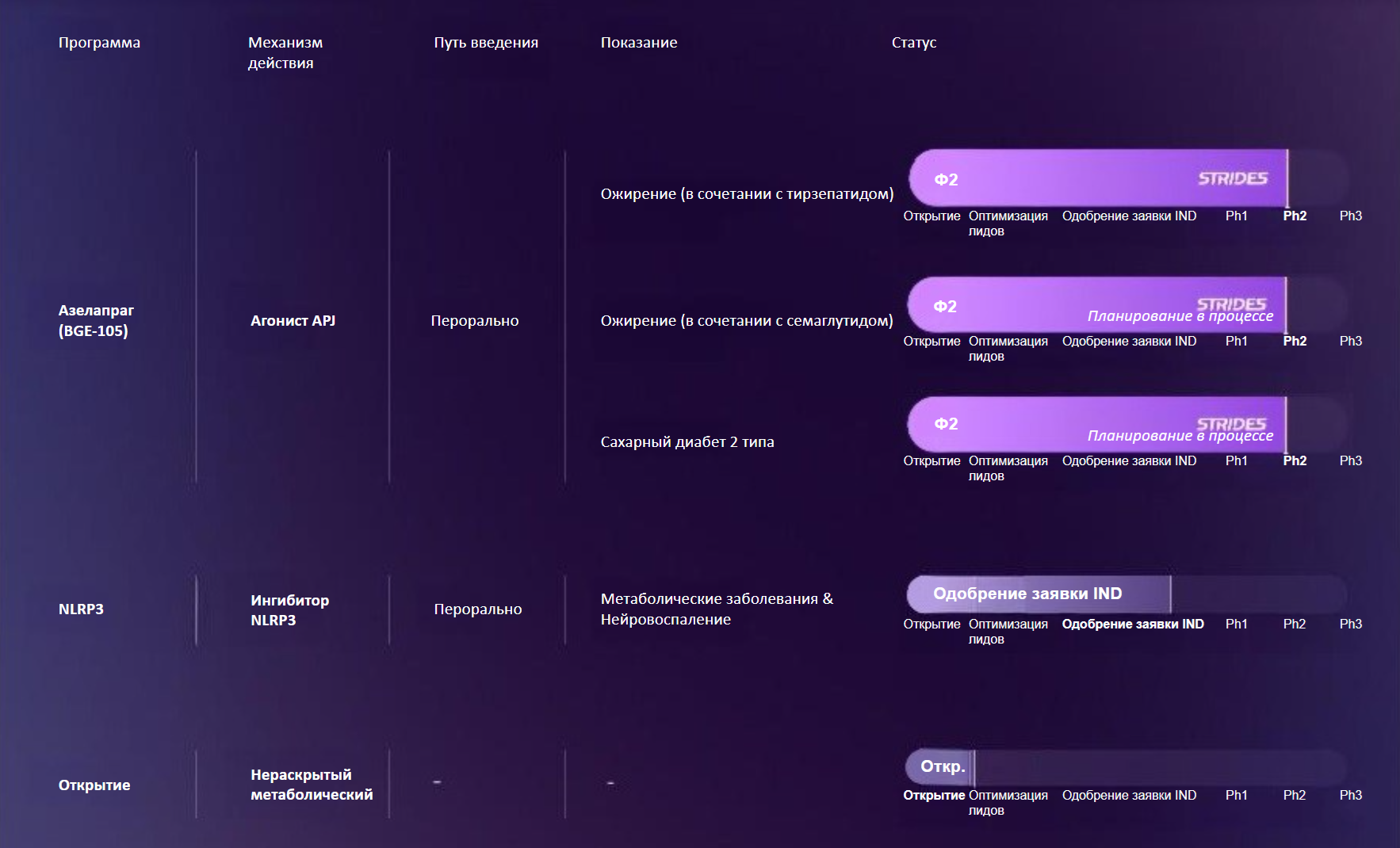
Другие компании также разрабатывают свои ИИ-платформы для поиска мишеней и лекарств: Alembic (Rubedo Life Sciences, воздействие на сенесцентные клетки), JuvNET (Juvena Therapeutics, терапия миопатий и метаболических заболеваний путем изменения белковой сигнализации), платформа от BioAge (оценка компонентов метаболического старения для терапии ожирения и нейровоспаления). Одни только собираются начать клинические исследования (Juvena Therapeutics, Rubedo Life Sciences), другие вовсю тестируют найденные молекулы (BioAge). В начале декабря 2024 года после 5 месяцев работы компания BioAge сообщила о прекращении STRIDES — двойного слепого плацебо-контролируемого клинического исследования II фазы азелапрага в виде монотерапии и в комбинации с тирзепатидом. Азелапраг — агонист апелиновых рецепторов, тирзепатид — агонист глюканогоподобного пептида-1 — препарат для лечения сахарного диабета 2 типа и ожирения. Цель комбинации — снизить потери мышечной массы при похудении. У 11 из 204 участников отмечалось повышение печеночных трансаминаз без клинических симптомов. Препараты для терапии ожирения должны иметь крайне высокий профиль безопасности, поэтому исследование было прекращено. Компания планирует продолжить наблюдение за набранными участниками и проанализировать полученные данные. Другой актив BioAge — ингибитор NLP3, гена, кодирующего белок-компонент инфласоммы. Он направлен на предотвращение хронического воспаления, ассоциированного со старением, в частности нейровоспаления. Ожидается, что препарат будет одобрен для клинических испытаний во второй половине 2025 года. 18 декабря 2024 BioAge анонсировала начало многолетнего партнерства с Novartis. Фармацевтический гигант предлагает 20 млн долларов в виде авансовых платежей и финансирования исследований и до 530 млн долларов на последующие долгосрочные разработки.
Однако «цифровая» геронтология столкнулась с проблемой качества первичных данных. В данной области воспроизводимость исследований крайне низкая — всего 20–40%. Выводы, полученные на основе некорректной информации, не будут соответствовать действительности. Поэтому стартапы, работающие методами ИИ и машинного обучения, предлагают активно вводить в практику публикацию первичных данных, как например в робототехнике.
Особняком стоит Calico с финансированием 2,5 миллиарда долларов. Компания была основана Google Inc. и Артуром Д. Левинсоном в 2013 году, но за более чем десятилетие не смогла добиться прорыва в терапии старения и сделала выбор в пользу препаратов для лечения бокового амиотрофического склероза, лейкоэнцефалопатии с исчезающим белым веществом и злокачественных новообразований. Сейчас проходят их клинические испытания I–II фазы.
Кто платит?
Кто готов вкладывать деньги в разработку терапии старения? За последние 10 лет появились венчурные фонды, финансирующие непосредственно сферу старения и долголетия, а не биотех в целом: Longevity Vision Fund, Heathspan Capital, Methuselah Fund, The Longevity Fund, Juvenescene, LongeVC, Kizoo, Miximon, Longevitytech.fund, Think capital, Hevolution. Hevolution — крупнейшая НКО с фокусом на терапии старения [45], [46]. Она финансируется Саудовской Аравией и имеет годовой бюджет в 1 миллиард долларов. Hevolution спонсирует как отдельные проекты, так и целые научные учреждения, а также организует крупнейшие конференции в области геронтологии и организует программы подготовки профильных кадров. Уже инвестировано более 400 миллионов долларов, выдано более 160 грантов.
| Инвестиции | Сумма (в млн USD) |
|---|---|
| Импакт-инвестиции | |
| Aeovian Pharmaceuticals; Продвигает селективные ингибиторы mTOR1, направленные на проверенный путь старения. |
$20,0 |
| Альянс прорывных инноваций; Объединяет лидеров индустрии для наставничества и финансирования компаний, работающих над увеличением продолжительности здоровой жизни. |
$10,0 |
| Vandria SA; Продвигает платформу митофагии c потенциалом для лечения заболеваний ЦНС. |
$7,9 |
| Rubedo Life; Направлен на клеточное старение, один из ключевых признаков старения. |
$2,0 |
| Научные гранты | |
| Программа возможностей фонда Hevolution для исследований в области геронауки; Финансирует доклинические проекты в биологии старения & трансляционной геронауки. |
$230,0 |
| Программа содействия развитию геронауки фонда Hevolution; Финансирует исследования, которые заслуживают внимания по мнению Национального института США по проблемам старения, но не получили финансирование. |
$27,0 |
| Программа награждения новых исследователей; Поддерживает начинающих исследователей через Американскую ассоциацию исследований старения (AFAR). |
$20,2 |
| Impetus Grants; Поддерживает 14 инновационных академических исследовательских проектов в науке о здоровой продолжительности жизни. |
$7,0 |
| Колл фонд Hevolution для приема заявок на гранты в Саудовской Аравии; Имеет целью создать первые группы ученых в области старения в Саудовской Аравии. |
$5,2 |
| Обучение геронауке фонда Hevolution для постдоков; Отбирает опытных PhD или MD/PhD кандидатов, специализирующихся на биологии старения и/или геронауки. |
$5,0 |
| Программа развития геронауки фонда Hevolution в Латинской Америке; Способствует развитию лучших исследований в области биологии старения и геронауки в Латинской Америке. |
$5,0 |
| Программа стипендий для постдоков фонда Hevolution Саудовской Аравии 2024; Обучает саудовских ученых и знакомит их с областью исследований старения. |
$1,9 |
| Международное сотрудничество | |
| XPrize Healthspan; Финансирует приз XPrize Healthspan за разработку доступной терапии восстановления функции мышц, когнитивных функций и иммунитета. |
$40,0 |
| Северо-Западный университет; Спонсирует исследования, сосредоточенные на определении и поддержании здорового, быстро восстанавливающегося протеостаза. |
$32,4 |
| Институт Бака; Ускоряет открытия терапевтических вмешательств, направленных конкретно против старения. |
$21,0 |
| Медицинский колледж Альберта Эйнштейна; Финансирует исследования, сосредоточенные на старении. |
$20,0 |
| Школа общественного здоровья Университета Индианы в Блумингтоне; Именная кафедра для продвижения исследований здорового старения на глобальном уровне. |
$2,0 |
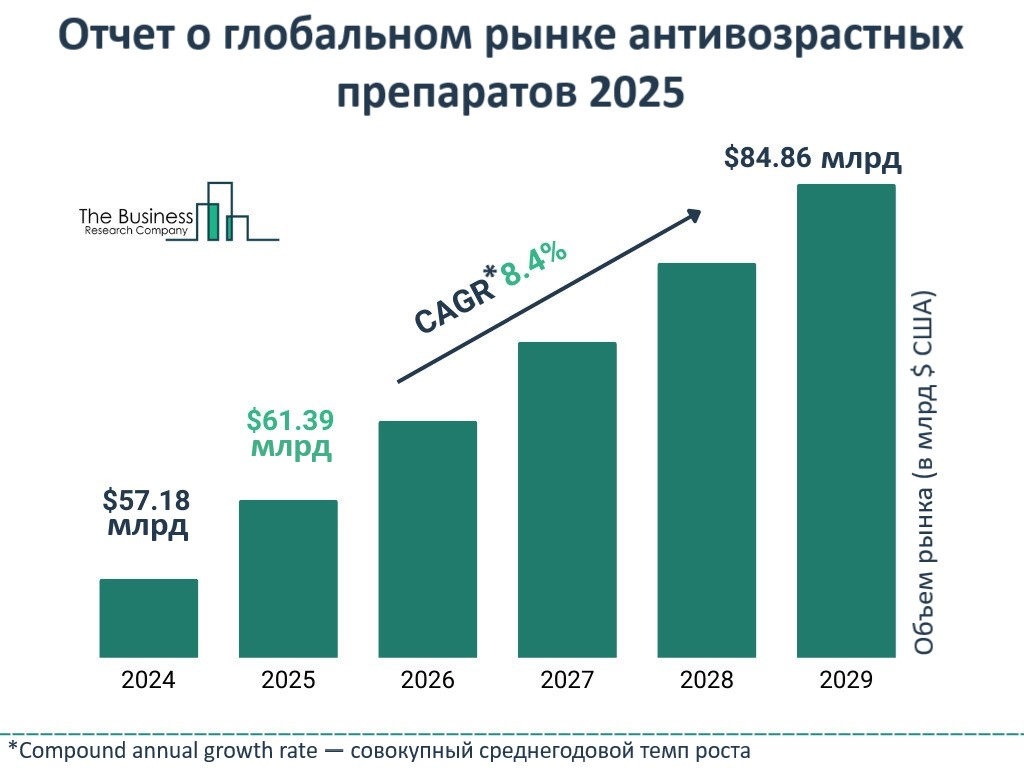
Рисунок 12. Прогнозируемый рост рынка терапии старения. Совокупный годовой темп роста рынка — 7,3%.
Где деньги, Лебовски?
Как стартапы зарабатывают деньги, пока препарат против старения не выпущен на рынок? Есть несколько вариантов:
- Разработка терапии старения собак (например, стартап Loyal). Клинические испытания и регистрацию препаратов в ветеринарии проводить проще и быстрее.
- Разработка часов старения. Приложения для определение биологического возраста от Gero и Insilico Medicine подробно обсуждаются в статье «Как и почему искусственный интеллект биологический возраст определял» [20].
- Разработка лекарственных препаратов в области косметологии и реконструктивной медицины (например, компания Retro Biosciences).
- Разработка терапии заболеваний, ассоциированных со старением (например, компания Cyclarity Therapeutics (бывш. Underdog Pharmaceuticals).
С одной стороны, перечисленные подходы позволяют стартапам заработать. С другой стороны, есть риск, что компания уйдет в шоттермизм и откажется от долгосрочной разработки терапии старения. В свою очередь, фонды и большая фарма могут расценивать уход в около-longevity сферу как признак того, что в серьезной разработке компания не может предложить ничего достойного.
Резюме и перспективы
Подавляющее большинство компаний декларируют своей миссией в первую очередь лечение хронических заболеваний, ассоциированных со старением. Победа над самим старением же откладывается до лучших времен. Клинические исследования нечасто радуют положительными результатами. Внимание широкой публики редко приковано к новостям геронтологии. В 2024 году на экраны вышел фильм «Субстанция», вольно и антинаучно представляя терапию старения и выставляя в дурном свете неприятие старости.
В то же время, область поиска терапии старения находит всё большее признание как в научных кругах, так и за их пределами. Longevity-сообщества и НКО (Open Longevity, SENS Longevity Foundation, Longevity Science Foundation, Longevity Escape Velocity Foundation, Lifespan.io и др.) растут и активно пропагандируют идеи продления жизни. Появились политические партии, выступающие за борьбу против старения (Партия за биомедицинские исследования в области омоложения (Германия), Траснгуманистическая партия США). Существуют отдельные институты, занимающиеся изучением старения: Институт биологии старения Общества Макса Планка, Институт Бака по исследованию старения и др. Инвестиции в область долголетия в биотехе ежегодно растут, и перспективные проекты могут получить достаточное финансирование и поддержку. Nature и Lancet запустили отдельные журналы по старению и долголетию Nature Aging (2020) и Lancet Healthy Longevity (2021). ООН объявила 2021-2030 годы Декадой здорового долголетия. Проводится порядка 366 клинических исследований antiage-терапии, 138 из которых направлены непосредственно на изучение и лечение процесса старения. 25 препаратов проходят III фазу клинических испытаний, но все они направлены исключительно против конкретных возраст-ассоциированных заболеваний. Насчитывается более 200 стартапов в области борьбы со старением.
Не стоит забывать, что даже самые очевидные открытия, значительно улучшившие качество жизни человечества, будь то базовые правила асептики и антисептики или вакцинопрофилактика, десятилетиями воспринимались в штыки перед тем, как стать рутинной практикой. Энтузиасты продления жизни берут лучшее от современных технологий и опыта предшественников и не собираются останавливаться в достижении своей конечной цели — победе над старением.
Литература
- Andrew J. Scott, Martin Ellison, David A. Sinclair. (2021). The economic value of targeting aging. Nat Aging. 1, 616-623;
- S. Jay Olshansky, Bradley J. Willcox, Lloyd Demetrius, Hiram Beltrán-Sánchez. (2024). Implausibility of radical life extension in humans in the twenty-first century. Nat Aging. 4, 1635-1642;
- Michel Poulain, Giovanni Mario Pes, Claude Grasland, Ciriaco Carru, Luigi Ferrucci, et. al.. (2004). Identification of a geographic area characterized by extreme longevity in the Sardinia island: the AKEA study. Experimental Gerontology. 39, 1423-1429;
- Michel Poulain. (2011). Exceptional Longevity in Okinawa:. DemRes. 25, 245-284;
- Saul Justin Newman The global pattern of centenarians highlights deep problems in demography — Cold Spring Harbor Laboratory;
- Claudio Franceschi, Paolo Garagnani, Cristina Morsiani, Maria Conte, Aurelia Santoro, et. al.. (2018). The Continuum of Aging and Age-Related Diseases: Common Mechanisms but Different Rates. Front. Med.. 5;
- Sheng Chen, Donghao Gan, Sixiong Lin, Yiming Zhong, Mingjue Chen, et. al.. (2022). Metformin in aging and aging-related diseases: clinical applications and relevant mechanisms. Theranostics. 12, 2722-2740;
- Adam R. Konopka, Jaime L. Laurin, Hayden M. Schoenberg, Justin J. Reid, William M. Castor, et. al.. (2019). Metformin inhibits mitochondrial adaptations to aerobic exercise training in older adults. Aging Cell. 18;
- Что общего у противозачаточных средств и терапии старения?;
- Carlos López-Otín, Maria A. Blasco, Linda Partridge, Manuel Serrano, Guido Kroemer. (2013). The Hallmarks of Aging. Cell. 153, 1194-1217;
- Carlos López-Otín, Maria A. Blasco, Linda Partridge, Manuel Serrano, Guido Kroemer. (2023). Hallmarks of aging: An expanding universe. Cell. 186, 243-278;
- Alexander Y. Panchin, Anna Ogmen, Artem S. Blagodatski, Anastasia Egorova, Mikhail Batin, Timofey Glinin. (2024). Targeting multiple hallmarks of mammalian aging with combinations of interventions. Aging. 16, 12073-12100;
- Часы старения: обнулить, замедлить, обратить вспять?;
- Jocelyn Kaiser. (2016). Antiaging trial using young blood stirs concerns. Science. 353, 527-528;
- Melod Mehdipour, Colin Skinner, Nathan Wong, Michael Lieb, Chao Liu, et. al.. (2020). Rejuvenation of three germ layers tissues by exchanging old blood plasma with saline-albumin. Aging. 12, 8790-8819;
- Melod Mehdipour, Taha Mehdipour, Colin M. Skinner, Nathan Wong, Chao Liu, et. al.. (2021). Plasma dilution improves cognition and attenuates neuroinflammation in old mice. GeroScience. 43, 1-18;
- Róbert Pálovics, Andreas Keller, Nicholas Schaum, Weilun Tan, Tobias Fehlmann, et. al.. (2022). Molecular hallmarks of heterochronic parabiosis at single-cell resolution. Nature. 603, 309-314;
- Gregory M. Fahy, Robert T. Brooke, James P. Watson, Zinaida Good, Shreyas S. Vasanawala, et. al.. (2019). Reversal of epigenetic aging and immunosenescent trends in humans. Aging Cell. 18;
- Frank W. Pun, Geoffrey Ho Duen Leung, Hoi Wing Leung, Bonnie Hei Man Liu, Xi Long, et. al.. (2022). Hallmarks of aging-based dual-purpose disease and age-associated targets predicted using PandaOmics AI-powered discovery engine. Aging. 14, 2475-2506;
- Как и почему искусственный интеллект биологический возраст определял.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚