
Биодеградация белого фосфора: как яд стал удобрением
08 апреля 2016
Биодеградация белого фосфора: как яд стал удобрением
- 3419
- 4
- 4
Бактерии лучше всех умеют превращать токсичное в практичное — это хоть как-то реабилитирует их, виновников смертоносных эпидемий, в глазах человека.
коллаж автора статьи
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Одним из самых опасных загрязнителей окружающей среды является белый фосфор — вещество чрезвычайно токсичное и огнеопасное. Несмотря на риски обращения с ним, белый фосфор (как и его разновидность технической чистоты, желтый фосфор) — краеугольный камень химии фосфора, сырьё для производства самых разных продуктов — от спичек до удобрений и пестицидов. А еще, несмотря на официальный запрет, наложенный Международной конвенцией, белый фосфор применяется в военных целях. В этой статье повествуется о становлении уникального научного исследования, в котором белый фосфор впервые был обезврежен и превращен в полезный для окружающей среды фосфат при помощи микроорганизмов.
«Био/мол/текст»-2016
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2016.

Спонсор номинации — Future Biotech, проект, объединяющий профессионалов и энтузиастов в области биологии и биотехнологий.
Генеральным спонсором конкурса, согласно нашему краудфандингу, стал предприниматель Константин Синюшин, за что ему огромный человеческий респект!
Спонсором приза зрительских симпатий выступила фирма «Атлас».
Что такое биодеградация?
Совершённый в двадцатом столетии научно-технический прорыв оставил человечеству в наследство не только блага цивилизации, поднимающие уровень жизни, но и множество проблем, остающихся нерешенными. И сейчас, в первые десятилетия века двадцать первого, разразился кризис. Одна из проблем — пагубное воздействие отходов цивилизации на окружающую среду.
Что делать с отходами? Вопрос, на который нелегко ответить. Речь в первую очередь идет об отходах химической промышленности. Поскольку «кровь цивилизации» на сегодняшний день — нефть и природный газ, значит отходы — это преимущественно продукты их переработки [1–4]. Зачастую токсичные, с трудом разлагающиеся в природе. Не менее опасны отходы металлургии — тяжелые металлы и их соединения. Значительную угрозу экологическому балансу создают и удобрения — азотные, калийные и фосфорные. Запасы химического оружия — это вообще отдельная тема, и их утилизация — проблема чрезвычайной остроты. Достаточно сказать, что для производителей химических арсеналов их творения представляют не меньшую угрозу, чем для противника.
И всё-таки, вернемся к «крови цивилизации» — нефти. Будучи продуктом переработки живых организмов, она представляет собой органическое вещество и состоит практически целиком из биогенных элементов (углерода, водорода, серы, азота и других). Значит, теоретически любой нефтепродукт можно вернуть в природный круговорот. На практике это сделать непросто — не любое углеродистое соединение полезно для жизнедеятельности. Необходима трансформация отходов в безвредные вещества.
Она производится разными способами. Органическое вещество можно сжечь, подвергнуть пиролизу (фактически снова превратить в нефть и уголь) или воздействию агрессивных химических реагентов (кислоты, щелочи, перекиси водорода, гипохлоритов), иногда с использованием высоких температур и давлений. Все эти способы широко применяют на практике и постоянно совершенствуют. Без них существование городов и промышленных предприятий стало бы невозможным.
Тем не менее в последние десятилетия одним из наиболее часто применяемых методов обезвреживания промышленных, бытовых и сельскохозяйственных стоков, химического оружия и взрывчатых веществ становится биодеградация [5–7]. В ряде случаев она приходит на смену более ранним методам химической деструкции. Главная причина — сравнительная экологическая безвредность этого метода. Биодеградация — это, как ясно из названия, обезвреживание токсичных веществ организмами—деструкторами, в большинстве случаев микроскопическими [8]. Под воздействием ферментных систем адаптированных микроорганизмов токсичные отходы разлагаются в мягких условиях, без применения жестких химических и физических воздействий.
Привнесенные микроорганизмы-деструкторы не выдерживают конкуренции с исконной микрофлорой водоемов и почв и вытесняются ею после ликвидации загрязнения и восстановления экологического баланса. В некотором смысле биодеградация — это самый естественный способ разложения отходов. Все миллиарды лет существования биосферы микроорганизмы «съедали» отходы ее жизнедеятельности, осуществляли минерализацию органики. Точно так же они поступают и с отходами производства.
Почему же популярность биодеградации начала расти только в последнее время? Отчасти это можно объяснить господствовавшим предубеждением: до недавнего времени было принято думать, что большинство продуктов химической промышленности — вещества, чуждые природе и в ней не встречающиеся. А раз в природе их нет, значит, природа и не способна самостоятельно их уничтожать. В популярных памфлетах экологов до сих пор приходится слышать фразы вроде «диоксины губительны для всего живого» или «полиэтилен не разлагается столетиями». Из специальной литературы уже известно, что полибромдиоксины выделяются морскими губками [9] и уже выведены культуры микроорганизмов, разлагающие полиэтилен (наблюдать за которым веками ни у кого возможности не было) [10].
Или другой пример — постулат «зеленой химии» о прекращении использования в промышленности галогенов (фтора, хлора, брома и йода) как чуждых окружающей среде элементов, игнорирующий присутствие в природе 2 500 галогенорганических веществ как биологического, так и абиотического происхождения — и это порядком устаревшие данные за 1996 год, с тех пор их количество должно было возрасти еще [11]. Конечно, играет роль и лобби: политические круги, заинтересованные в сокращении промышленных мощностей, склонны преувеличивать экологическую угрозу. А самое главное — совершенствование методов химического анализа позволило существенно расширить спектр известных природных веществ. Оказалось, что большинство химических продуктов, пусть в следовых количествах, но постоянно выделяется живыми организмами и циркулирует в биосфере [12].
Бурно развивающаяся наука метаболомика резко расширяет спектр соединений, которые с полным основанием можно называть природными. Например, окись этилена никогда не рассматривалась в качестве такового. Наоборот, это широко известный дезинфицирующий агент, канцероген, мутаген и нервно-паралитический яд, токсичный для всех форм жизни. К тому же этиленоксид пожаро- и взрывоопасен. Однако известно, что этиленоксид образуется эндогенно в результате окисления этилена оксидазами [13]. Сам этилен, в свою очередь, выделяется растениями и микроорганизмами, выполняя функции фитогормона [14]. Присутствуя в атмосфере, этилен проникает в организм животных и аэробных микробов, в которых окисляется до этиленоксида. Таким образом, некоторое количество (пул) этого токсиканта постоянно находится в биосфере. По-видимому, еще никто не подсчитывал общее количество эндогенной окиси этилена в биосфере или ее биопродукцию за год. Вполне возможно, что она сравнима с годовым промышленным производством этого соединения. В любом случае есть основания называть этиленоксид природным веществом! И это далеко не единственный пример. Соответственно, микроорганизмы-деструкторы с подобными веществами постоянно сталкиваются и способны их разлагать.
Конечно, это не единственная причина длительной непопулярности биодеградации. Как и любой метод, она имеет ограничения. В природе ни одно токсичное вещество не накапливается в чистом виде. Например, фенол в следовых концентрациях всегда присутствует в биосфере — как продукт распада ароматических аминокислот [15]. Однако только с возникновением химической промышленности стало возможным наполнять этим веществом цистерны. Поэтому для ликвидации цистерны концентрированного фенола биодеградация не подходит. Как известно, даже концентрированный раствор глюкозы может служить консервантом. Зато биодеградация очень эффективна при случайных разливах токсичных веществ в воде или почве. Не случайно в патентной базе ФИПС при наборе ключевого слова «биодеградация» открывается солидное количество патентов по устранению нефтяных пленок.
Другое ограничение биодеградации — недостаточная скорость эволюции. Микроорганизмы «не поспевают» за промышленностью. Для ускорения эволюции подходят разнообразные приемы: создание накопительных культур, генная инженерия, направленная селекция и так далее, но они требуют глубоких знаний и высокого технологического уровня, а также значительных вложений. Позволить это могут немногие государства и корпорации.
В интереснейшей статье [16] сообщается о том, что бактерия-мутант «научилась» производить нужный ей белок (точнее, подладила под новые потребности уже имеющийся), и потребовалось ей на это всего четверо суток! По всей видимости, общее разнообразие ферментов, участвующих в биодеградации ксенобиотиков (веществ, «чуждых жизни»), бесконечно велико и основано на спонтанном либо направленном мутагенезе. Это позволяет биосфере быть готовой к усвоению даже тех веществ, которые еще не синтезированы.
Сейчас известно, что гены, кодирующие ферменты биодеградации, часто собраны на мобильных молекулах ДНК — плазмидах. Например, на плазмиде pADP1 локализованы гены atz, позволяющие бактерии-хозяину утилизировать пестицид атразин, а мегаплазмида pNL1 содержит bph-гены, ответственные за катаболизм бифенила, и множество других генетических кластеров для деградации ароматики [17], [18]. Плазмиды с «экзотическими» генами быстро распространяются в популяции микробов в присутствии токсичного вещества и так же быстро элиминируются после его уничтожения: живой клетке становится невыгодно содержать бесполезные гены. Природа, как известно, скупа на нововведения — точно так же, при помощи плазмидных генов, у микроорганизмов распространяется и устойчивость к антибиотикам. По этой же причине созданные в лабораториях узкоспециализированные микроорганизмы-деструкторы в большинстве своем не способны жить в нормальных природных условиях — их вытесняют более приспособленные «дикие» штаммы. То есть для них наличие в среде ксенобиотика — необходимое условие существования. Соответственно, они обречены на поддержание в коллекциях культур или загрязненных почвах вокруг предприятий, риск бесконтрольного распространения таких микроорганизмов минимален.
Еще одна проблема, связанная с биодеградацией — уязвимость деструкторов. Как и любые организмы, они чувствительны к факторам среды. Например, микроорганизм может эффективно разлагать иприт, но при этом быть чувствительным к ионизирующему излучению. А микроорганизмы, устойчивые к радиации, имеют низкий темп размножения и медленный метаболизм, то есть мало подходят на роль деструкторов [19], [20]. Поэтому биодеградация никогда не вытеснит другие методы ликвидации отходов. Но эффективная ликвидация возможна только комплексом методов, обязательно включающим биодеградацию.
Как уже упоминалось чуть выше, организмы-деструкторы существуют в коллекциях. В России крупнейшая из них — Всероссийская коллекция промышленных микроорганизмов (ВКПМ), созданная в 1969 году и насчитывающая около двух десятков тысяч культур. ВКПМ не только поддерживает культуры, следит за сохранением их свойств, но и ведет каталог, устанавливает таксономическую принадлежность поступающих микроорганизмов, предоставляет культуры заинтересованным лицам (и принимает свод правил предоставления).
Естественная среда обитания деструкторов — активные илы и осадки сточных вод (ОСВ), скапливающиеся в отстойниках очистных сооружений (рис. 1). Здесь они постоянно участвуют в процессе водоочистки. Почва вокруг предприятий тоже служит источником ценных культур, поскольку незначительные утечки реагентов происходят, несмотря на все меры предотвращения.
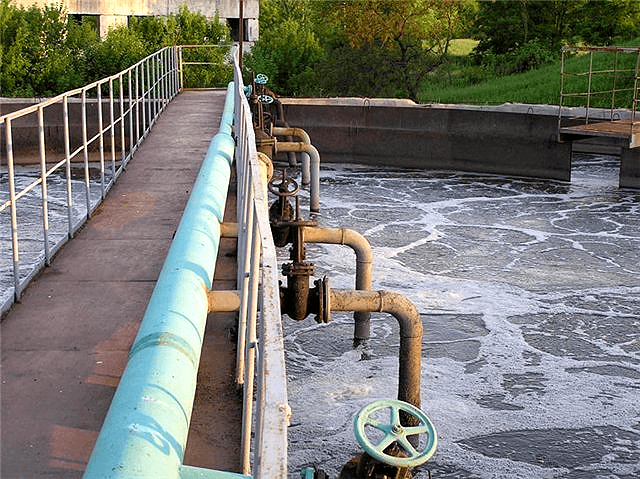
Рисунок 1. Отстойники очистных сооружений химических предприятий — естественная среда обитания микроорганизмов-деструкторов.
Для устранения случайных разливов токсичных веществ используют микроорганизмы в составе наполняющих материалов — как правило, пористых сорбентов (торфа, компоста, соломы, золы от сгоревшего угля и так далее). Такой сорбент впитывает ксенобиотик, удаляет его из воды или почвы, а содержащиеся в нём микробы приступают к деструкции. Описания подобных материалов и методов их применения даны в соответствующих патентах.
Причиной написания этой статьи стало то, что с недавнего времени наш авторский коллектив (о котором расскажу чуть позже) сам начал заниматься биодеградацией. Причем объект исследования мы выбрали очень необычный — белый фосфор [7], [12], [21–31]. В доступной литературе не удалось найти сведений о деградации элементного, в том числе белого, фосфора активным илом без искусственного внесения химических реагентов. Не найдена информация и о путях метаболизма белого фосфора в присутствии микробиоты или в тканях высших организмов. В изданной литературе речь идет исключительно об абиогенных путях деградации и детоксикации белого фосфора. О токсичности белого фосфора для прокариот тоже ничего не известно. Потому количественные данные о снижении выделения газообразных продуктов жизнедеятельности микроорганизмов ОСВ в присутствии различных концентраций белого фосфора без преувеличения уникальны. Получая их, мы опирались исключительно на результаты собственных исследований.
Наибольшую трудность для метаболизма белого фосфора представляет отсутствие углеродного скелета. Большинство ксенобиотиков, как уже говорилось, производится из нефти и относится к органическим соединениям, сравнительно легко преобразуемым в биологические молекулы. Ферментные системы клетки адаптированы к метаболизму органических веществ. Белый фосфор — это простое вещество, не только чрезвычайно токсичное, но и не встречающееся в природе.
Как известно, разработка подходов к биодеградации нового объекта начинается с поиска микроорганизмов, разлагающих родственные соединения. Например, штаммы, разлагающие хлорбензоаты, выведены путем направленной селекции из культур, разлагающих незамещенный бензоат [32]. В случае с белым фосфором такой отбор невозможен: микробный метаболизм, скажем, серы или селена имеет очень отдаленное сходство, слишком велика разница в свойствах веществ.
Таким образом, попытка осуществить его биодеградацию — довольно смелый научный вызов. Однако высокая реакционная способность белого фосфора и возможность преобразовать его в биологически совместимый фосфат позволяют рассчитывать на решение этой проблемы.
Итак, что же такое белый фосфор?
Белый фосфор (Р4) — один из самых опасных загрязнителей окружающей среды. Это вещество обладает высокой химической активностью и летучестью, легко воспламеняется (вплоть до самовоспламенения) на воздухе, при соприкосновении с кожей вызывает тяжелые ожоги, поражает все системы внутренних органов человека и животных. Хроническое отравление приводит к глубокой инвалидности, затрагивая кальциевый обмен и разрушая кости, вызывая малокровие, поражая печень, сердечно-сосудистую и репродуктивную системы [33], [34]. Гидрофобность белого фосфора сочетается с высокой липофильностью. Это свойство делает его еще более опасным, поскольку белый фосфор легко накапливается в жировой ткани. Особенно страдают от загрязнения этим веществом водоплавающие птицы — утки и лебеди, — поскольку белый фосфор проникает в их организм из водной среды во время кормежки, а также питающиеся ими хищные птицы [35]. Показано, что из организма кур-несушек белый фосфор может переходить в яйца. Обнаружен он и в рыбах — пресноводных и морских.
Тем не менее белый фосфор широко применяется в промышленности: в производстве красного фосфора, треххлористого фосфора, фосфорных кислот и фосфатов для технического использования и пищевой промышленности, дымообразующих и зажигательных составов, в металлургии [21]. Значит, не исключается попадание белого фосфора в окружающую среду.
По химической природе белый фосфор представляет собой простое вещество, аллотропную модификацию элементного фосфора. Белый фосфор высокой чистоты — это бесцветные кристаллы с сильным коэффициентом преломления света, внешне похожие на алмазы. Плавится он при 44,1 °С, кипит при 280,5 °С. Из всех аллотропных модификаций фосфора имеет наименьшую плотность (1,8 г/см3 при 20 °С). Кроме того, белый фосфор — самая химически активная и термодинамически нестабильная модификация фосфора. При хранении, особенно на свету, он постепенно полимеризуется в красный фосфор и темнеет. Технический белый фосфор (желтый фосфор) — аморфная, похожая на пчелиный воск масса желтоватого или светло-коричневого цвета, с характерным запахом чеснока (рис. 2). Содержит примеси красного фосфора и других веществ. В присутствии кислорода воздуха белый фосфор медленно окисляется до оксида Р2О3 практически без выделения тепла. Окисление сопровождается слабым зеленоватым свечением (явление хемилюминесценции).
Белый фосфор чрезвычайно огнеопасен, горит ослепительно белым пламенем. Теплота сгорания белого фосфора составляет очень большую величину — 24 000 Дж/г. Легко самовоспламеняется, особенно при механическом воздействии, например, трении. Температура самовоспламенения — всего 30 °С. Горение белого фосфора сопровождается выделением густого белого дыма, состоящего из частичек оксида фосфора Р2О5. Пятиокись фосфора, в свою очередь, является одним из самых гигроскопичных веществ, впитывая атмосферную влагу и образуя туман из капелек ортофосфорной кислоты, Н3РО4. Формирование кислотного тумана делает случаи возгорания фосфора еще более опасными. Чтобы предотвратить окисление и возгорание, белый фосфор хранят под водой, с которой он практически не реагирует.

Рисунок 2. Белый фосфор (Р4): внешний вид (слева) и структура (справа).

Рисунок 3. Портрет рабочего спичечной фабрики с симптомами «фосфорной челюсти». Начало ХХ века.
Высочайшая химическая активность белого фосфора определяет его токсичность. Летальная доза белого фосфора для взрослого мужчины составляет всего 0,05-0,1 г. Предельно допустимая концентрация паров фосфора в воздухе производственных помещений — 0,03 мг/м3, что соответствует первому классу опасности по ГОСТ; временно допустимая концентрация в атмосферном воздухе — 0,0005 мг/м3, ПДК в питьевой воде — 0,0001 мг/л [36].
Наиболее известный симптом хронического отравления белым фосфором — остеопороз, возникающий в результате нарушения кальций-фосфорного обмена [34]. При этом существенно снижаются прочность и эластичность костной ткани, возникают боли в спине. Симптомы сопровождаются гиперфосфатемией — возрастанием уровня фосфата и ионов кальция в моче, то есть необходимые организму элементы выделяются с мочой. В тяжелых случаях остеопороз переходит в остеонекроз — отмирание костной ткани и образование свищей. В медицине существует термин «фосфорная челюсть» (phossy jaw), означающий разрушение нижней челюсти у человека при длительном контакте с фосфором (рис. 3). В XIX и начале XX века «фосфорная челюсть» нередко встречалась у рабочих спичечных фабрик, вдыхавших пары белого фосфора [37].
Другой симптом отравления белым фосфором — малокровие, наблюдаемое как у людей, так и у животных. Ну и, пожалуй, одним из наиболее выраженных последствий отравления белым фосфором является поражение печени.
Несмотря на официальный запрет, белый фосфор используется в военных целях — для приготовления зажигательных смесей. Им начиняют гранаты, авиабомбы, артиллерийские снаряды. В последнее время доносятся печальные сведения о применении фосфорных боеприпасов правительством Украины на Юго-Востоке страны. Обстрелы боеприпасами с белым фосфором вызывают сильнейшие пожары. Это, безусловно, оружие массового уничтожения, вполне сравнимое с ядерным. Ожоги, вызванные горящим фосфором, особенно тяжелы, поскольку термический ожог дополняется кислотным (фосфорная кислота — основной продукт горения фосфора). Они с большим трудом поддаются лечению. Горящий фосфор испаряется, и его пары выжигают легкие.
В производстве спичек белый фосфор использовали вплоть до 1906 года, когда была принята Бернская конвенция, запрещающая применение белого фосфора: после ее подписания спичечные головки стали изготовлять на основе красного фосфора, значительно менее токсичного и огнеопасного. Таким образом, опасность белого фосфора в быту почти полностью устранена. Однако риск аварий на промышленных предприятиях и транспортных путях сохраняется.
16 июля 2007 года на 12-м километре перегона Ожидов-Красное Львовской железной дороги произошла крупная авария товарного поезда. Состав из 58 вагонов следовал из Казахстана в Польшу транзитом через Россию и Украину. 15 цистерн товарного эшелона содержали желтый фосфор. С рельсов сошли только цистерны с фосфором. В момент аварии была нарушена герметизация шести цистерн, из которых полился горящий жидкий фосфор (рис. 4). Организаторы транспортировки понадеялись только на защитное действие герметизации и не оборудовали в цистернах систему охлаждения [38].

Рисунок 4. Ликвидация возгорания желтого фосфора на Львовской железной дороге.
блог «Сегодня»
По мнению В. Станкевича, доктора медицинских наук, заведующего лабораторией гигиены почвы и отходов Института гигиены и медицинской экологии Украины, фосфор нужно перевозить с такими же мерами предосторожности, как и ядерные отходы. Из этого, безусловно, следует необходимость поиска новых, более эффективных способов обезвреживания такого опасного технологического продукта, как белый фосфор.
Единственное предприятие по производству технического белого (желтого) фосфора в РФ — ОАО «Фосфор» (г. Тольятти) — обанкротилось в 2002 году. Теперь территория предприятия, где на 180 га хранятся 6 000 тонн фосфорного шлама, является причиной частых возгораний, неблагоприятной экологической обстановки в городе и его окрестностях [13]. По информации с сайта «Безформата.ру», в 2012 году на территории бывшего ОАО «Фосфор» зафиксировано 36 (!) случаев возгорания фосфошлама. А с января по август 2014 года — 16 случаев самовозгорания (TLT.ru).
Казалось бы, такой набор свойств свидетельствует о полной невозможности биологической деструкции подобного вещества. И впрямь, белый фосфор считается «биоцидом», то есть веществом, губительным для любых форм жизни. Между тем, у элемента фосфора есть уникальное качество: будучи сильнейшим ядом в виде простого вещества, в окисленном состоянии он абсолютно необходим для всех форм жизни. Таким образом, возможна его полная детоксикация. Проблема обезвреживания белого фосфора (на 100% состоящего из биогенного элемента фосфора!) в окружающей среде состоит в отсутствии эффективных и безвредных способов превращения его в безопасную форму, представляющую собой остаток фосфорной кислоты. Только на первый взгляд это превращение кажется легким.
А мы-то что сделали?
Наши исследования по биодеградации белого фосфора начались, когда судьба свела меня с замечательным человеком и ученым Дмитрием Григорьевичем Яхваровым. Была весна 2009 года, и я находился в труднейшем положении, оставшись без темы научной работы и руководства. Тогда я мог вообще не остаться в науке. Яхваров — химик, а не биолог, но это человек широчайшего кругозора и глубокого взгляда в перспективу, а также неиссякаемого научного любопытства. К тому же — талантливый руководитель, который не запугивает подчиненных и не контролирует их, а мотивирует. Таких ученых и людей очень мало. Неудивительно, что он автор нескольких крупных открытий. В то время Яхваров тесно сотрудничал с голландской корпорацией Thermphos International, производившей белый фосфор и жестоко страдавшей от штрафов за загрязнение окружающей среды. Для руководства фирмы поиск способа обезвреживания стоков с предприятий был ох как актуален. И именно Дмитрий Григорьевич стал автором идеи. Мы поговорили с ним пару минут в коридоре, и у меня в голове буквально «загорелась лампочка»: я понял, что это предложение — то самое научное открытие, которым я грезил всю жизнь. Я, к тому моменту порядком уставший от мытарств с венчурным фондом и выбиванием средств на реализацию чего-то, что никто заведомо не собирался реализовывать, согласился, не колеблясь ни секунды. Но «открытие» на тот момент было только в грезах. Его еще следовало осуществить.
До начала работы с Яхваровым я занимался изучением биогаза — возобновляемого топлива, выделяющегося из осадков сточных вод на очистных сооружениях водоканала. К тому моменту меня хорошо знали на этом режимном объекте и предоставляли возможность отбора проб осадков. Вместе с моим лучшим учеником и помощником Димой Белостоцким мы привозили канистры и ведра с осадком в наш институт, и именно с осадков началась работа по биодеградации белого фосфора.
С чего начинается любая научная работа? Конечно же, с поиска литературных источников. Начинающему первопроходцу нужно знать, что в мире сделано по данному направлению до него. Статей и патентов по биодеградации нашлось немерено (ссылки на некоторые из них привожу здесь, еще больше ссылок можно найти в других моих статьях). А по биодеградации белого фосфора — ничего. Вообще никаких источников, ни на русском, ни на английском языках! Нашлась, правда, работа, в которой вскользь упоминалось, что в начале восьмидесятых годов в Америке исследовали рост микробов в присутствии белого фосфора и пришли к выводу, что они не растут. То есть деструкция этого вещества в окружающей среде носит исключительно абиотический характер [39]. Причем очень медленный: те же американцы подсчитали, что скорость распада частиц белого фосфора, оказавшихся на дне водоема, может превышать 10 000 лет! Более того, я не нашел никакой информации по путям метаболизма белого фосфора. Про симптоматику отравлений высших животных и человека информации даже с избытком, а вот биохимическую основу этих процессов, похоже, никто не выяснял. Либо эта информация засекречена и доступна лишь избранным: всё-таки белый фосфор интересует военных.
Начало, конечно, малообнадеживающее. Но, с другой стороны, оно внушало оптимизм: любые полученные нами результаты становились первыми в мире! Самый первый наш эксперимент был чистейшей авантюрой: я внес в осадок сточных вод белый фосфор в соотношении 1:1000 и принялся наблюдать, что получится. Никто не мог даже предположить заранее, какие будут результаты. Работа ведется уже почти семь лет, а завершиться она могла через три недели. Осадок в герметично закрытой склянке с трубкой, погруженной в воду температурой 37 °С, вначале бодро выделял газ (который собирался в перевернутый вверх дном мерный цилиндр, заполненный солевым раствором), но через пару недель его активность упала до нуля. Сомнений не было — всё живое в нём умерло. Вся литература пестрит информацией, что белый фосфор — биоцид! Ладно, думаю, эксперимент есть не просит, пусть простоит до отпуска. И упорство было вознаграждено. Еще через пару недель мертво застывший уровень жидкости в цилиндре опустился на один миллилитр. Это легко списать на случайность — изменение температуры и прочее. Но с каждым днем уровень падал всё быстрее, то есть газ накапливался! А газ — смесь углекислого газа и метана — продуцируется микроорганизмами, населяющими осадок, то есть скорость его выделения отражает активность микробного метаболизма. Значит, после длительного периода угнетения они адаптировались к неблагоприятным условиям. Мы решили продолжать работу.
Вначале исследования продвигались очень медленно. Анаэробные бактерии размножаются небыстро, наблюдения за кинетикой выделяющегося газа длились по 150–200 суток. Измерять объем выделяющегося газа нужно было каждый день. И каждый день нужно было доливать воду в термостатируемую баню. Поэтому в тот период я ходил на работу и по выходным, вызывая всеобщее недоумение.
Разумеется, протоколы экспериментов были усовершенствованы. Каждый опыт мы теперь ставили в трех повторах для учета статистики, белый фосфор вносили не кусками, а в виде однородной водной эмульсии, полученной диспергированием ультразвуком, варьировали концентрацию фосфора от 0,001 до 0,1%. Естественно, что с ростом концентрации яда активность микрофлоры снижалась. Это ярко иллюстрирует приведенная диаграмма (рис. 5).

Рисунок 5. Кинетика выделения газа в зависимости от концентрации белого фосфора. Удельные выходы газа обратно пропорциональны концентрации токсичного вещества.
Но кинетика всегда носила один и тот же характер. В первые дни активность микрофлоры в опыте и контроле (осадке без белого фосфора) была совершенно одинаковой, затем в опытных вариантах она снизилась вплоть до полного угнетения, но потом микрофлора адаптировалась (хотя уровень ее метаболизма был существенно ниже, чем в контроле, удельное выделение газа падало по мере роста концентрации белого фосфора). При помощи спектроскопии ЯМР мы установили, что активация микрофлоры после периода угнетения совпадает с исчезновением сигнала белого фосфора, то есть эти явления взаимосвязаны. Более того, скорость деградации белого фосфора оказалась прямо пропорциональной активности микрофлоры. В образцах осадка с низкой активностью микрофлоры (например, отобранного в морозные зимние месяцы) сигнал белого фосфора в спектре наблюдался и через год после внесения, а в других случаях исчезал через два месяца. То есть микробный метаболизм активно влияет на деградацию белого фосфора!
Один эксперимент, в котором биодеградация сравнивалась в трех образцах осадка одной партии, но отобранного с разной глубины (соответственно, с разным видовым составом микрофлоры), продемонстрировал взаимосвязь между микробным метаболизмом и скоростью разложения белого фосфора особенно ярко. Чем глубже залегал слой ила, тем меньше было удельное выделение газа из него. Анализ показал, что концентрация метаболитов в субстратах трех проб заметно различается. Интенсивность сигнала белого фосфора была обратно пропорциональна активности микробного метаболизма в них. Концентрация Р4 в растворе в первом образце была в 7,8 раз ниже, чем во втором, и в 13,3 раза ниже, чем в третьем. Это означает четкую зависимость между скоростью исчезновения белого фосфора в субстрате и интенсивностью микробного метаболизма в нём. Если бы Р4 подвергался абиогенной деструкции, скорость его разложения и интенсивность сигнала ГХ/МС во всех трех пробах были бы одинаковыми!
Результаты этих ранних исследований более подробно и менее популярно изложены в публикациях [22], [23], [25], [29]. Очень большую поддержку на этом этапе (и на последующих тоже) мне оказала моя Alma Mater, кафедра биохимии Казанского университета, и ее замечательная заведующая — профессор Фарида Кашифовна Алимова. Вообще, в университете в успех работы верили куда больше, чем в стенах Института Арбузова (ИОФХ), без их поддержки работа не сдвинулась бы с места. Со мной работали замечательные иностранные студенты (особо хочу упомянуть Йав Акосах, очень одаренного студента из Ганы) и аспирант Яхварова — Рустем Кагиров, теперь эксперт в Сколково. Посильную помощь оказывали и сотрудники ИОФХ, особенно Салима Тахиятулловна Минзанова, которой я во многом обязан своей кандидатской диссертацией, и Владимир Савич Резник, мудрый старик, на тот момент замдиректора ИОФХ, одним из первых разглядевший в работе немалый потенциал.
Но, пожалуй, наиболее значимым результатом, полученным в то время, стало наблюдение, что поверхность осадков с белым фосфором со временем покрывается колониями микробов. Это само по себе удивительно: устойчивые к этому токсиканту микроорганизмы не описаны нигде! Но еще более удивительно то, что контрольные осадки без белого фосфора «не зарастали». Не увидел бы это своими глазами — не поверил бы. Выходило, что в отравленной среде микробы росли лучше, чем в чистой! Чтобы не быть голословным, приведу таблицу с количествами колоний, выросших в посевах из контрольного и опытного осадков (табл. 1).
| Субстрат | Разведение | |||||
|---|---|---|---|---|---|---|
| 107 | 108 | |||||
| Опыт | 56 | 76 | 70 | 21 | 26 | 21 |
| Контроль | 5 | 0 | 1 | 0 | 1 | 0 |
Получается, в контроле вырастало от нуля до пяти колоний, а в опыте при том же разведении — не один десяток! По всей видимости, этому парадоксу есть только одно объяснение. Микроорганизмы, растущие на поверхности отравленного осадка, лучше адаптируются к присутствию белого фосфора. В контрольных субстратах они угнетены другими группами микроорганизмов, а в опытных не имеют конкурентов. Разумеется, этих необыкновенных микробов требовалось изучить подробнее. Замечательные микробиологи, работающие в виварии ИОФХ, Александра Дмитриевна Волошина (рис. 6) и Наталья Владимировна Кулик, произвели посевы бактерий на чашки Петри. Так мы впервые получили культуры микробов, устойчивые к белому фосфору. Они были идентифицированы как представители родов Bacillus, Pseudomonas и Streptomyces [22], [23], [28], [29].

Рисунок 6. Основные участники работ по биодеградации белого фосфора. а — Антон Зуфарович Миндубаев; б — Дмитрий Григорьевич Яхваров; в — Александра Дмитриевна Волошина; г — Елена Валерьевна Горбачук; д — Шамиль Завдатович Валидов; е — Фарида Кашифовна Алимова; ж — Любовь Геннадьевна Миронова (слева) и Салима Тахиятулловна Минзанова (справа).
Осенью 2011 года появился повод для большой гордости: по теме вышла первая статья, в ВАКовском журнале «Ученые записки Казанского университета» [22]. Хоть рейтинг журнала невысок, опубликоваться в нём непросто. Редколлегия состоит из авторитетных профессоров, иногда статьи лежат в редакции годами и бесконечное число раз дорабатываются. Я всегда привожу этот журнал как пример того, что импакт-фактор никак не влияет на уровень рецензирования статей.
А полгода спустя, в марте 2012-го, случилось непредвиденное. Компания Thermphos International, которая выступала в роли заказчика работы, разорилась. Если до этого момента администрация института проявляла к работе какое-то призрачное подобие интереса, то после вообще перестала видеть в ней смысл. Меня перевели в другую лабораторию, чтобы снова заниматься биогазом, к которому, признаюсь, душа у меня на тот момент уже не лежала. Мы с Яхваровым посовещались и пришли к твердому убеждению продолжать работу. В отличие от администрации мы прекрасно понимали, что наше исследование — нечто большее, чем заказ фирмы: мы заполняли белое пятно в науке! Исследование это носит больше фундаментальный характер, чем прикладной. Пришлось у нового завлаба с боями выбивать возможность продолжать работу. А в конце того года я познакомился с большим энтузиастом своего дела, редактором журнала «Бутлеровские сообщения», Александром Ивановичем Курдюковым. После этого у меня начался вал публикаций, и вся работа была представлена на страницах этого журнала. Я очень благодарен Александру Ивановичу, хотя порой докучаю ему невероятными объемами своих статей.
В 2014–2015 годах нас очень выручил Российский фонд фундаментальных исследований (РФФИ). Сбылась сокровеннейшая мечта — у работы появилось финансирование. Это стало настоящим подарком к Новому году: ранее приходилось всё делать за счет своей зарплаты, даже в командировки ездить. И результаты не замедлили появиться. С финансированием у нас произошел настоящий прорыв в исследованиях.
Наконец-то появилась возможность реализовать давнюю идею — отойти от работ с осадками и приступить к выращиванию чистых культур в искусственных культуральных средах. Осадки сточных вод (ОСВ) имеют важное преимущество — богатое видовое разнообразие микробного сообщества, позволяющее добиться биодеградации даже такого «трудного» загрязнителя, как белый фосфор. Однако есть у ОСВ и ряд недостатков: сложнейший химический состав, но главное — непостоянство этого состава, а значит, и свойств субстрата. ОСВ практически не поддается стандартизации, поэтому наблюдения за ним затруднительны. Следовательно, дальнейшую работу необходимо было вести в искусственных культуральных средах, имеющих стандартный, постоянный состав. Только в таких средах можно выращивать чистые культуры устойчивых микроорганизмов, устанавливать их таксономическую принадлежность, получать новые штаммы, наконец (и это важнейшая задача), вести селекцию микроорганизмов на способность обезвреживать всё возрастающие концентрации белого фосфора. Известно, что самый эффективный способ выращивать чистую культуру микроорганизма-деструктора с сохранением его свойств — регулярно пересевать ее в культуральную среду, содержащую в качестве единственного источника биогенных элементов тот ксенобиотик, который эта культура должна расщеплять. Например, микроорганизмы, обезвреживающие нефть, выращивают в средах, содержащих нефть в качестве единственного источника углерода.
А.Д. Волошина, которую я уже упоминал выше, — очень опытный и талантливый микробиолог, специально для наших исследований разработала культуральную среду, содержащую белый фосфор в качестве единственного источника фосфора. Особо подчеркну: сделано это было впервые в истории! А основная нагрузка по приготовлению этих сред возлагается на аспирантку Яхварова, Лену Горбачук. Меня всегда восхищало, как эта хрупкая девушка совершенно не боится работать с белым фосфором — при помощи ультразвука готовит из навески белую, как молоко, эмульсию в шленке. Разумеется, в атмосфере инертного газа аргона — иначе белый фосфор моментально воспламенится! А потом пипеткой нужный объем эмульсии вносится в среду — так в ней создается нужная концентрация белого фосфора.
На деньги гранта было закуплено необходимое оборудование. Например, ультразвуковая ванна «Сапфир» объемом 1,3 литра, с помощью которой диспергируем белый фосфор. Этот приборчик для нас жизненно необходим, а до получения финансирования мы были вынуждены обращаться к тем, у кого такая ванночка была. Или фотоэлектроколориметр АР-101 (Apel, Япония), с помощью которого позже провели интереснейшее исследование роста псевдомонад в присутствии белого фосфора.
Очень важная (хотя и неочевидная на первый взгляд) задача для нас — транспортировка между ИОФХ и университетом. Перевозить приходится и культуры микробов, и ростовые среды, и чрезвычайно зловонные осадки сточных вод, и, наконец, сам белый фосфор в инертной атмосфере в шленке. То есть весьма опасные (либо для нас очень ценные) предметы. Причем всё это в подавляющем числе случаев заключено в стеклянную посуду, которая легко бьется. В этом нам неоценимую помощь оказывает замечательная женщина, коллега Салимы Тахиятулловны, инженер-исследователь Любовь Геннадьевна Миронова. Она умеет так аккуратно сложить все банки и колбы, что риск повредить их сводится к минимуму, даже при поездке общественным транспортом и при ходьбе по обледенелым зимним дорогам. Конечно, обращаемся мы к Любови Геннадьевне не только с этим вопросом: будучи отличным хозяйственником, она всегда помнит, что у нас есть и где что лежит.
Мы начали работу всё с теми же штаммами бактерий, которые ранее выделили из осадков. Неожиданно мы стали обладателями сюрприза: сам химический реактив белый фосфор оказался обсеменен спорами черного аспергилла, который начал беззастенчиво расти в средах и подавлять бактерий. Вот вам и биоцид! Конечно, такой грибок нельзя было оставить без внимания. Возможно, устойчивость к белому фосфору возникла у него давно, раз его споры контактировали с этим веществом долгое время. И ведь как растет этот аспергилл! Мы специально посеяли его на агаризованные среды трех видов: с фосфатом, вообще без источника фосфора и с белым фосфором. На фотографии (рис. 7) наглядно виден результат через шесть суток после посева. На среде с фосфатом выросло значительное число сравнительно мелких колоний, то есть большинство спор проросло, что естественно в благоприятных условиях. На среде без источников фосфора колонии выросли немногочисленные, занимающие сравнительно большую площадь, но очень слабые (практически прозрачные, с неразвитым мицелием и отдельными конидиеносцами, выглядящими как россыпь черных точек, а не сплошное черное поле). По всей видимости, сказалась нехватка фосфора: агар, используемый для приготовления среды, содержит примесь фосфата, но недостаточную для полноценного роста грибов. Самое интригующее, что на среде с 0,05% белого фосфора колоний выросло меньше, чем в контроле с фосфатом, однако они производят впечатление совершенно нормальных, не испытывающих дефицита питательных веществ. Отсюда следует вывод, что на среде с белым фосфором выживают не все споры гриба, но выжившие способны использовать в качестве источника фосфора либо сам белый фосфор, либо продукты его химических превращений. Значительный размер колоний, выросших в присутствии Р4, объясняется менее жесткой конкуренцией между немногими адаптировавшимися культурами.
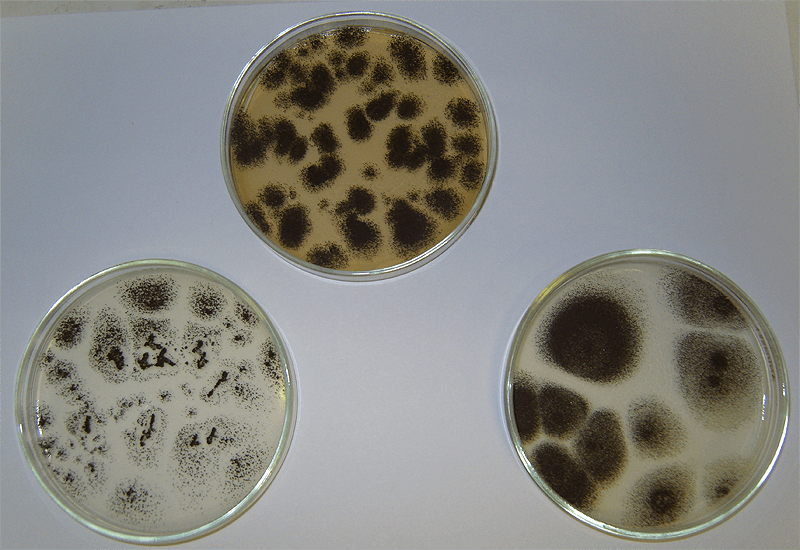
Рисунок 7. Первый пересев устойчивых аспергиллов. Слева внизу — среда без источника фосфора: на ней растут 33 ослабленные колонии аспергилла. Вверху — среда с фосфатом: на ней — 49 спорообразующих колоний Aspergillus niger. Справа внизу — среда с 0,05% белого фосфора: выросли 11 крупных спорообразующих колоний A. niger. Чашки сфотографированы через шесть суток после пересева.
Но этот Aspergillus niger, как выяснилось, не единственный микроб, растущий на белом фосфоре. Неплохо растут и стрептомицеты, хотя их устойчивость пониже. С культурой стрептомицетов, выделенной из ОСВ с белым фосфором, много работает наш коллега из Туркменистана, аспирант кафедры биохимии Керемли Сапармырадов (которого на кафедре все зовут Кешей). В частности, сравнивая линию стрептомицетов, пересеваемых на белый фосфор, и линию их близких родственников, которых Кеша пересевал в стандартную среду, мы показали, что в отсутствие белого фосфора устойчивость к нему исчезает, и микроб становится самым обыкновенным. Поэтому расхожие страхи о том, что микробы-мутанты заполонят весь земной шар, совершенно необоснованны.
Прознав о том, что микробы «кушают» белый фосфор, сотрудники кафедры буквально всучили нам свой объект исследования — грибок триходерму. С ней они работают много лет, и что только не делают: триходермой и огурцы в совхозе защищают от вредителей, и ферменты для стирального порошка из нее выделяют, и идентичный натуральному ароматизатор с запахом кокоса. А тут еще намереваются с ее помощью обезвреживать белый фосфор! Начали мы работать с триходермой без особого энтузиазма, но очень быстро поняли, какой подарок нам преподнесла кафедра. Триходерма в первом же посеве продемонстрировала устойчивость к белому фосфору бóльшую, чем у других исследуемых нами микроорганизмов! «Триходерма, она такая!» — прокомментировали на кафедре. Более подробные сведения об этой работе можно почерпнуть из нашей статьи [30].
Разумеется, очень важной задачей был поиск метаболитов белого фосфора. Метод ЯМР еще в начале исследований показал, что белый фосфор в средах с микробами исчезает. Но из закона сохранения массы следует, что исчезновение вещества должно сопровождаться накоплением продуктов его превращений. По спектру этих продуктов можно судить о путях метаболизма белого фосфора (практически не выявленных до сих пор), а также о перспективах и целесообразности практического внедрения его биодеградации. Зачастую продукты метаболизма какого-либо вещества оказываются более опасными, чем исходный субстрат (так называемые летальные метаболиты), что накладывает ограничения на применение метода.
Вот эту-то очень простую, казалось бы, задачу мы не могли решить несколько лет. Дело в том, что потенциальные метаболиты должны присутствовать в среде в следовых концентрациях, а сотрудники нашей лаборатории радиоспектроскопии упорно не желали снимать для нас спектры с большим накоплением. Пятьсот-тысячу сканов, не больше. А нам-то надо тысяч тридцать! Но что поделать, у них съемка поставлена на поток, они привыкли к высоким концентрациям веществ, которые им приносят химики. При этом они никогда не уставали ворчать, что для работы им требуется высочайшее повеление «сверху». «У вас опять ничего нет», — заявляли они с сердитыми лицами, показывая нам очередной спектр, в котором действительно ничего не было.
На помощь нам опять пришел университет. На химфаке я познакомился с опытным (а главное, добросовестным, не ищущим повода для отказа) спектроскопистом Хасаном Хаяровым. Надо снять спектр с числом сканов восемьдесят тысяч? Для Хасана это не вопрос, даже если на съемку уйдет трое суток. И проблема решилась как по волшебству! Хасан снял нам изумительные спектры ЯМР, в которых как на ладони видны сигналы метаболитов. Гипофосфит, фосфит... фосфат! Фосфат, основа обмена веществ в любой клетке. И в культуральной среде фосфату неоткуда было взяться — только из белого фосфора, внесенного изначально. Мы стали свидетелями потрясающей вещи: страшнейший яд белый фосфор превратился в фосфорное удобрение! Стадии этого процесса представлены в изображенной мною схеме предполагаемого метаболического пути белого фосфора (рис. 8) [26].

Рисунок 8. Предполагаемый метаболический путь белого фосфора. Знаком вопроса обозначены еще не обнаруженные превращения.
Правда, мы до сих пор не знаем, как это происходит. Возможно, он окисляется чисто химическим путем, и живые клетки включают в свой метаболизм продукты его окисления. Удаляя их из окружающей среды, микроорганизмы смещают химическое равновесие в сторону дальнейшего окисления Р4 — согласно известному принципу Ле Шателье для динамических равновесных систем — и таким образом ускоряют деградацию белого фосфора. Вероятно, этот механизм биодеградации имеет место, но возможен и дополнительный путь, намного более интересный для биологов, — синтез ферментов с неизвестным видом активности, для которых белый фосфор является субстратом. Их обнаружение (или обнаружение новой активности у уже известных ферментов) стало бы значительным фундаментальным достижением, причем вполне реалистичным, учитывая разнообразие специфических ферментов с уже установленными экзотическими активностями. Причем оба представленных пути биодеградации не исключают друг друга, а, напротив, отлично сочетаются.
Бактерии Pseudomonas alcaliphila, выделенные из ОСВ с белым фосфором, высевали на среды идентичного состава, содержащие 0,01 и 0,05% белого фосфора. Оптическая плотность культуры измерялась на купленном на грант фотоэлектроколориметре. Измерения показали, что псевдомонады, в отличие от грибов и стрептомицетов, не растут в средах, содержащих белый фосфор в качестве единственного источника фосфора. То есть организмы из разных таксономических групп имеют различную устойчивость к белому фосфору! В работе [27] мы уже сообщали о том, что бактерии из рода Bacillus выживают при концентрации белого фосфора в ОСВ 0,1%, но только за счет сильного замедления метаболизма и темпа размножения, а не за счет эффективной деструкции этого вещества. Это справедливо и для P. alcaliphila. Различие в устойчивости к белому фосфору — серьезный аргумент в пользу того, что он разлагается под воздействием ферментных систем (которые различаются у разных культур микробов), а не только за счет абиотического окисления.
Особо хочу подчеркнуть: биодеградация белого фосфора — задача не только прикладная, но и фундаментальная. Будучи биогенным элементом, фосфор в биосфере Земли включен в биогеохимический круговорот, именуемый в англоязычной литературе phosphorus recycling. Исследования последних лет значительно расширили наши представления о круговороте фосфора. Выяснилось, что в него вступают не только фосфаты, но и фосфин, гипофосфиты, фосфиты, природные и антропогенные тиофосфаты, фторфосфаты, фосфорамиды, фосфорорганические соединения [40]. За исключением элементного фосфора, о метаболизме которого почти ничего не известно. Элементный фосфор в некотором смысле остается «слабым звеном» круговорота. Поэтому осуществление биологической деградации элементного фосфора — с перспективой ее применения на практике — задача, без сомнения, важная.
Но это еще не конец истории. Делая пересевы микроорганизмов с интервалом в среднем 60 суток, мы добились роста устойчивости. Наилучшую приспособляемость к белому фосфору проявили именно стрептомицеты. Через пять последовательных посевов их устойчивость возросла пятикратно. Грибы растут и адаптируются медленнее: у аспергилла после восьми пересевов устойчивость повысилась вдвое. Однако их устойчивость (особенно в случае триходермы) изначально была выше, чем у актиномицетов [31]. Нам удалось вырастить микроорганизмы в среде, концентрация белого фосфора в которой достигла 1%. Согласно патенту [41], концентрация белого фосфора в сточных водах предприятий не должна превышать двух частей на миллион, то есть 0,0002%. Стало быть, концентрация белого фосфора 1% — это превышение ПДК в сточных водах в 5000 раз! А ПДК элементного фосфора в водных объектах хозяйственно-питьевого и культурно-бытового водопользования, согласно данным из монографии [42], составляет всего 0,0001 мг/л, то есть концентрация 1% превышает ее уже в сто миллионов (1×108) раз! Сам факт устойчивости микроорганизмов к такой концентрации токсиканта удивителен и служит примером приспособительных возможностей живых организмов. А ведь грибы в этих условиях даже размножались, хотя споры созревали заметно медленнее и в меньшем количестве.
Вполне возможно, что концентрация 1% — не предельная, и после продолжительной селекции возможен рост и в средах с более высокими концентрациями фосфора. Работы в этом направлении сдерживаются исключительно соображениями техники безопасности: с ростом концентрации горячие эмульсии белого фосфора становятся всё более опасными в обращении. Следовательно, для приготовления культуральных сред с содержанием P4 более 1% по массе требуется разработка новых методов его внесения в среды.
Осенью 2014 года нас ждал еще один приятный сюрприз. Написанная мною заявка «Биологическая деградация — новый подход к обезвреживанию белого фосфора» завоевала третье место на Конкурсе инновационных работ молодых ученых в области зеленой химии с международным участием, проводимом в рамках выставки «Международная химическая ассамблея ICA-2014. Зеленая химия» (21–24 октября 2014 года, ЦВК ЭКСПОЦЕНТР, Москва). По мнению экспертов — организаторов конкурса (в их числе декан химического факультета МГУ, академик РАН В.В. Лунин и президент РХО В.П. Иванов), исследование уже на тот момент находилось на пороге научного открытия мирового уровня и имеет перспективы для демилитаризации и защиты окружающей среды от отходов химической промышленности.
В настоящее время у нас началось плодотворное сотрудничество с настоящим профессионалом, генетиком микроорганизмов Шамилем Валидовым. Этот человек, прежде чем придти работать в университет, долгое время трудился в Пущино и Нидерландах. Начнем с того, что именно Шамиль подсказал нам, как стерилизовать белый фосфор. Проблема непростая. Нагревать его в автоклаве до 120 °С нельзя — слишком химически активен. По этой же причине не подходит облучение ультрафиолетом. Нам предлагали всякие устрашающие способы стерилизации, вроде использования радиоактивного кобальта-60. Я к подобным предложениям относился с изрядной долей здорового скепсиса. А Шамиль надоумил: надо просто повстряхивать навеску белого фосфора пятнадцать минут в ацетоне — и все споры погибнут. «Все так делают», — добавил он.
Шамиль, сравнивая культуру нашего гриба с данными из базы GenBank, показал, что она действительно является новым штаммом черного аспергилла — его мы назвали A. niger АМ1 [31]. С Шамилем я получил бесценный опыт выделения ДНК из мицелия гриба. Сейчас приоритетная задача у нас — сравнение экспрессии генов грибов, выросших на белом фосфоре и фосфате. Методом обратной транскрипции Шамиль получил на основе матричных РНК грибов комплементарные ДНК. Сейчас они хранятся в состоянии глубокой заморозки. Планируем провести их секвенирование, которое может приоткрыть завесу над механизмами биодеградации белого фосфора, над тем, какие гены задействованы в этом процессе. Но сейчас у нас опять нет средств — инициативный проект в РФФИ поддержку не получил. А без генетики журналы из Scopus и Web of Science не желают принимать наши статьи. Получается забавная ситуация — ведь РФФИ отказал именно по причине отсутствия рейтинговых публикаций! Хотя с деньгами опубликоваться было бы легче. Но одно знаю твердо: раз столько, казалось бы, неразрешимых проблем удалось решить, значит, найдется выход и из этого непростого положения.
Что можно сказать в заключение? Признаюсь, когда без малого семь лет назад я впервые смешал осадок сточных вод с белым фосфором, я даже не представлял себе, что работа выйдет на такой уровень. И достигнуто это было исключительно благодаря упорству, готовности преодолевать передряги финансового, правового и административного характера. А какое счастье я испытал, когда осознал: мы смогли это! Смогли сделать то, чего не делал никто в мире. Раньше я много комплексовал и нередко бывал неуверен в себе. Теперь знаю: научное открытие (пускай даже еще незавершенное и не всеми признанное) — это отличный способ поднять самооценку. Теперь я уверен, что могу справиться с любыми трудностями. Ощущаю себя реализовавшимся как ученый и как человек. И обращаюсь к молодым, талантливым ребятам: дерзайте! Если у вас есть интересные идеи, и вы чувствуете в себе потенциал их реализовать, не бойтесь. Хотя трудностей на вашем пути будет немало, но и награда будет очень велика!
Литература
- Пластик на завтрак;
- А ты такой холодный, как... пластик в океане;
- Бактерии-нефтедеструкторы для биоремедиации супесчаных почв Воронежской области;
- Пределы биодоступности углеводородов в грунтах;
- Neilson A.H. and Allard A.S. Environmental degradation and transformation of organic chemicals. NY: CRC Press, 2007. — 710 p.;
- Khomenkov V.G., Shevelev A.B., Zhukov V.G., Zagustina N.A., Bezborodov A.M., Popov V.O. (2008). Organization of metabolic pathways and molecular-genetic mechanisms of xenobiotic biodegradation in microorganisms: a review. Prikl. Biokhim. Mikrobiol. 44, 117–135;
- Миндубаев А.З. и Яхваров Д.Г. (2013). Биодеградация как метод переработки отходов. Часть 1. Биодеградация ксенобиотиков. Бутлеровские сообщения. 33, 1–37;
- «Зеленые» революционеры;
- Utkina N.K., Denisenko V.A., Scholokova O.V., Virovaya M.V., Gerasimenko A.V., Popov D.Y. et al. (2001). Spongiadioxins A and B, two new polybrominated dibenzo-p-dioxins from an Australian marine sponge Dysidea dendyi. J. Nat. Prod. 64, 151–153;
- Reddy M.M., Deighton M., Gupta R.K., Bhattacharya S.N., Parthasarathy R. (2008). Biodegradation of oxo-biodegradable polyethylene. J. Appl. Polym. Sci. 111, 1426–1432;
- Gribble G.W. Naturally occurring organohalogen compounds — a comprehensive update. Wien: Springer Verlag GmbH, 2010. — 613 p.;
- Миндубаев А.З. и Яхваров Д.Г. (2013). Биодеградация как метод переработки отходов. Часть 2. Взгляд на проблему. Являются ли ксенобиотики ксенобиотиками? Бутлеровские сообщения. 34, 1–20;
- Swenberg J.A., Lu K., Moeller B.C., Gao L., Upton P.B., Nakamura J., Starr T.B. (2011). Endogenous versus exogenous DNA adducts: their role in carcinogenesis, epidemiology, and risk assessment. Toxicol. Sci. 120, 130–145;
- Eckert C., Xu W., Xiong W., Lynch S., Ungerer J., Tao L. et al. (2014). Ethylene-forming enzyme and bioethylene production. Biotechnol. Biofuels. 7, 1–11;
- Smith E.A. and Macfarlane G.T. (1997). Formation of phenolic and indolic compounds by anaerobic bacteria in the human large intestine. Microb. Ecol. 33, 180–188;
- Бактерии способны заменить утраченный белок всего за 96 часов;
- Shapir N., Mongodin E.F., Sadowsky M.J., Daugherty S.C., Nelson K.E., Wackett L.P. (2007). Evolution of catabolic pathways: Genomic insights into microbial s-triazine metabolism. J. Bacteriol. 189, 674–682;
- Seeger M., Hernández M., Méndez V., Ponce B., Córdova M., González M. (2010). Bacterial degradation and bioremediation of chlorinated herbicides and biphenyls. J. Soil Sci. Plant Nutr. 10, 320–332;
- Флагеллин защитит от поражения радиацией;
- Радиофобия. Сон разума рождает чудовищ;
- Миндубаев А.З. и Яхваров Д.Г. (2014). Фосфор: свойства и применение. Бутлеровские сообщения. 39, 1–24;
- Миндубаев А.З., Акосах Й.А., Алимова Ф.К., Афордоаньи Д.М., Болормаа Ч., Кагиров Р.М. и др. (2011). О разложении белого фосфора осадком сточных вод. Учен. зап. Казан. ун-та. Сер. Естеств. науки. 153, 110–119;
- Миндубаев А.З., Алимова Ф.К., Ахоссийенагбе С.К., Болормаа Ч., Волошина А.Д., Кулик Н.В. и др. (2013). Возможность анаэробной детоксикации белого фосфора. Бутлеровские сообщения. 33, 22–34;
- Миндубаев А.З., Волошина А.Д., Яхваров Д.Г. (2013). Биологическая деградация белого фосфора: осуществимость и перспективы. Бутлеровские сообщения. 33, 1–17;
- Миндубаев А.З., Алимова Ф.К., Ахоссийенагбе С.К., Минзанова С.Т., Миронова Л.Г., Яхваров Д.Г. (2013). Новое подтверждение биодеградации белого фосфора. Бутлеровские сообщения. 36, 1–12;
- Миндубаев А.З., Алимова Ф.К., Ахоссийенагбе С.К., Болормаа Ч., Волошина А.Д., Кулик Н.В. и др. (2013). Микробный метаболизм белого фосфора. Бутлеровские сообщения. 36, 34–52;
- Миндубаев А.З., Алимова Ф.К., Ахоссийенагбе С.К., Волошина А.Д., Горбачук Е.В., Кулик Н.В. и др. (2014). Метаболиты и устойчивая микрофлора в субстратах с содержанием белого фосфора 0,1%. Бутлеровские сообщения. 37, 67–78;
- Болормаа Ч., Сапармырадов К.А., Алимова Ф.К., Миндубаев А.З. (2014). Сравнение показателей фитотоксичности, фунгицидной и бактерицидной активности стрептомицетов из различных местообитаний. Бутлеровские сообщения. 38, 147–152;
- Миндубаев А.З., Волошина А.Д., Горбачук Е.В., Кулик Н.В., Ахоссийенагбе С.К., Алимова Ф.К. и др. (2014). Белый фосфор как новый объект биологической деструкции. Бутлеровские сообщения. 40, 1–26;
- Миндубаев А.З., Волошина А.Д., Горбачук Е.В., Кулик Н.В., Алимова Ф.К., Минзанова С.Т. и др. (2015). Включение белого фосфора в природный круговорот веществ. Культивирование устойчивой микрофлоры. Бутлеровские сообщения. 41, 54–81;
- Миндубаев А.З., Волошина А.Д., Горбачук Е.В., Валидов Ш.З., Кулик Н.В., Алимова Ф.К. и др. (2015). Адаптация микроорганизмов к белому фосфору, как результат направленной селекции. Генетическая идентификация устойчивого аспергилла и метаболическое профилирование стрептомицета А8. Бутлеровские сообщения. 44, 1–28;
- Наумова Р.П. Микробный метаболизм неприродных соединений. Казань: Изд-во Казанского университета, 1985. — 239 с.;
- Toxicological profile for white phosphorus. Atlanta: Agency for Toxic Substances and Disease Registry (ATSDR), 1997. — 248 p.;
- Вербовой А.Ф. (2002). Состояние костной ткани и кальций-фосфорного обмена у рабочих фосфорного производства. Казанский медицинский журнал. 83, 147–150;
- Roebuck B.D., Nam S.I., Macmillan D.L., Baumgartner K.J., Walsh M.E. (1998). Toxicology of white phosphorus (P4) to ducks and risk for their predators: effects of particle size. Environ. Toxicol. Chem. 17, 511–518;
- Амиров Д.Л. Комплексное лечение гнойно-воспалительных заболеваний мягких тканей у рабочих фосфорного производства: автореф. дис....канд. мед. наук. — Бишкек, 1993;
- Медведев Ю. и Басин Е. (2012). Фосфорные некрозы челюстей. Врач. 1, 21–25;
- Бадюгин И.С. (2009). Зажигательные и токсические свойства фосфора. Уроки Львовской аварии. Военно-медицинский журнал. 330, 20–26;
- Spanggord R.J., Renwick R., Chou T.W., Wilson R., Podoll R.T., Mill T. et al. Environmental fate of white phosphorus/felt and red phosphorus/butyl rubber military screening smokes. Menlo Park: SRI International, 1985. — 48 p.;
- Singh B.K. and Walker A. (2006). Microbial degradation of organophosphorus compounds. FEMS Microbiol. Rev. 30, 428–471;
- Barber J.C. (1996). Processes for the disposal and recovery of phossy water. US Patent US5549878;
- Алексеенко В.А., Бузмаков С.А., Панин М.С. Геохимия окружающей среды. Пермь: Изд-во Пермского университета, 2013. — 358 с.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





