Биодеградация ксенобиотиков как самозащита природы
29 августа 2017
Биодеградация ксенобиотиков как самозащита природы
- 4886
- 0
- 4
Полигон твердых бытовых отходов — нерешенная проблема современности.
сайт www.nsktv.ru
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Загрязнение окружающей среды и переработка отходов — серьезные проблемы современности. Одним из лучших путей их решения является биодеградация — наиболее естественный и экологически безопасный способ уничтожения отходов цивилизации. Представленная статья ставит задачу показать, что наша биосфера всю историю своего существования находится под надежной и неусыпной охраной микробов-деструкторов, для которых самые ядовитые отходы являются лакомством. А заодно осветить возможности биодеградации.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Свободная тема» конкурса «био/мол/текст»-2017.

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.

Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Как грибы спасли мир
Наверное, каждый читатель знаком с понятием о круговоротах биогенных элементов — углерода, азота, фосфора, серы, железа. Слово «круговорот» указывает на замкнутость — в течение длительного времени атомы элемента в него вовлечены, и надолго из цикла не изымаются. Именно замкнутость круговоротов элементов определяет устойчивость биосферы, существующей уже несколько миллиардов лет.
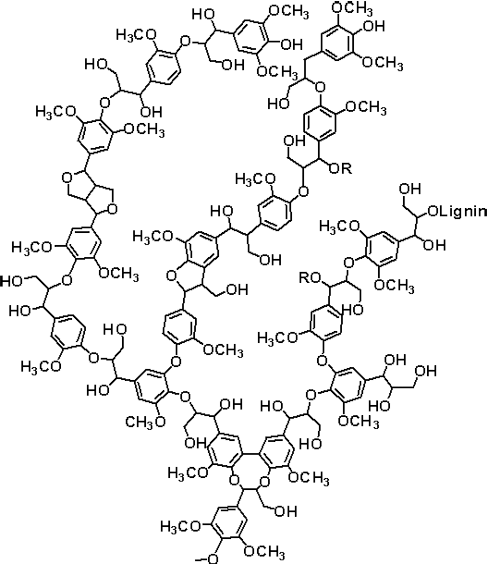
Но однажды в истории нашей планеты произошел разрыв круговорота, пожалуй, самого важного для жизни элемента — углерода. Было это около 300 миллионов лет назад, в каменноугольном периоде. Тогда облик планеты стремительно менялся, и появилась новая экосистема, доселе не встречавшаяся — лес (рис. 1б). Лес состоит из деревьев, а деревья производят древесину. Значительная составная часть древесины — лигнин — является гидрофобным и нерастворимым сшитым полимером оксикоричных спиртов; фактически, он представляет собой природную пластмассу (рис. 1а). Даже в наши дни он подвергается биодеградации с трудом, при помощи ферментов лакказ, продуцируемых некоторыми грибами-ксилотрофами. А в описываемое время грибы-деструкторы древесины еще не существовали. Мертвая древесина тогда не гнила, а обугливалась (подвергалась абиотической деструкции). Или все-таки гнила, но частично: тогдашние редуценты выедали целлюлозу, а лигнин в виде «бурой гнили» оставался и со временем все равно превращался в уголь. Так на месте первых лесов формировались залежи каменного угля. Процесс карбонификации древесины шел, вероятно, по той же схеме, что и на современных торфяниках: лигнин → торф → бурый уголь → каменный уголь. На каждой стадии схемы росло относительное содержание углерода в ископаемых остатках.
То есть, как раненое существо теряет кровь, так и биосфера того времени стала терять углерод. В теории, это могло привести к катастрофе. Через несколько миллионов лет значительная часть углерода из живого вещества должна была превратиться в мертвый уголь, и жизнь на Земле или полностью погибла бы, или была бы отброшена в своем развитии обратно в ранний палеозой.
Но этот страшный сценарий не сбылся. Появление нового пищевого ресурса открыло новую экологическую нишу, которая должна была заполниться. И со временем развились нужные грибы, необходимые ферменты и хитроумные приемы, используемые грибами для разложения лигнина без вреда для собственных тканей [1]. Конечно, формирование углей продолжается и сейчас — на сфагновых болотах и торфяниках, где создаются уникальные условия с подавлением процесса гниения. Но масштабы этого процесса уже не те, заходит он не столь далеко, останавливаясь, как правило, на стадии бурого угля. В целом круговорот углерода в биосфере снова стал замкнутым, что, в конечном итоге, привело к появлению нас с вами. Этот пример очень эффектно демонстрирует возможности биодеградации — деструкции токсичных или трудноусваиваемых веществ специализированными формами жизни.
Живой и мертвый... кислород
И, надо заметить, пример этот далеко не первый. Задолго до появления деревьев атмосфера Земли стала насыщаться продуктом жизнедеятельности цианобактерий, агрессивным и токсичным окислителем — молекулярным кислородом О2. Для первых живых организмов и современных анаэробных бактерий кислород так же ядовит, как газообразный хлор для человека! Случилось событие, именуемое не иначе как кислородной катастрофой.
Но жизнь и тогда сумела приспособиться. Сначала появились аэротолерантные микробы, умеющие обезвреживать кислород (опять биодеградация!) [2]. Позже жизнь «догадалась», что кислород — чрезвычайно сильный акцептор электронов, и окисляя им органические молекулы, можно получить баснословное количество необходимой для жизнедеятельности энергии. И сейчас большинство форм жизни без кислорода существовать не способно (рис. 2) [3].
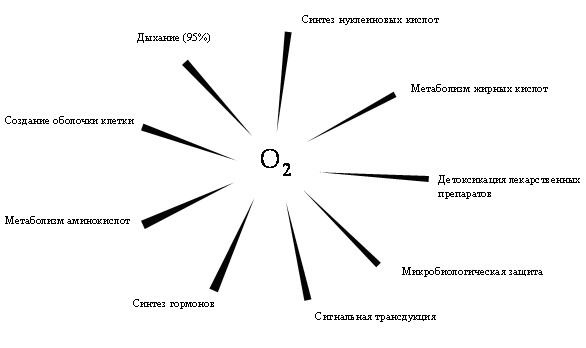
Рисунок 2. Наиболее важные биологические процессы, связанные с окислением молекулярным кислородом. Самым значимым из них является, конечно же, аэробное дыхание. В наши дни нелегко себе представить, что пару миллиардов лет назад кислород был вредным для всего живого ксенобиотиком!
[3], рисунок с изменениями
Короче говоря, экологический кризис, охвативший Землю в наше время и связанный с загрязнением окружающей среды человеком, не первый и наверняка не последний. С уверенностью можно сказать, что он будет преодолен. Это, конечно, не значит, что на кризис следует закрывать глаза. Ведь предыдущие кризисы длились миллионы лет, а хочется завершить его побыстрее! Но, с другой стороны, демонизировать человеческий род и представлять его «раковой опухолью на теле земли» тоже не стоит. В конце концов, появление новых видов, умеющих производить новые вещества, происходит постоянно. И в процессе эволюции постоянно появляются новые виды, приспособленные эти вещества кушать, то есть возвращать обратно в круговорот элементов.
В свете вышесказанного, ажиотаж вокруг сжигания ископаемого топлива не вполне обоснован. Ведь сейчас в биосферу возвращается тот углерод, который был из нее когда-то изъят.
Terra incognita
Человек приспособил биодеградацию для своих нужд. Это явление используется для очистки сточных вод уже сотню лет. Английский химик Диброн в 1887 году смог очистить сточную жидкость, выдерживая в ней культуру микроорганизмов. А в 1916 году в той же Англии, в промышленном Манчестере, построили первый аэротенк, и ввели понятие «активный ил» [4]. Не единожды биодеградация освещалась и на страницах «Биомолекулы» в увлекательных и интересных статьях [5–11]. Как известно, изложение явления в популярной форме свидетельствует о большом к нему интересе.
Тем не менее еще лет двадцать—двадцать пять назад считалось, что способность к метаболизму ксенобиотиков (в переводе с древнегреческого этот термин означает «чуждый жизни»: ξενος — чуждый и βιος — жизнь) у микроорганизмов очень ограничена, и большинство из них не используется. Но в настоящее время убедительно показана способность как аэробных, так и анаэробных микроорганизмов к деградации ксенобиотиков. Когда процесс осуществляется не индивидуальным микроорганизмом, а структурированной микробной ассоциацией (сложность которой вполне сопоставима с многоклеточным организмом), эффективность и глубина деградации органических соединений заметно увеличивается. Микроорганизмы, способные к переработке ксенобиотиков, довольно разнообразны, и зачастую высоко специализированы.
Биодеградация имеет глубокую фундаментальную основу, заключающуюся в громадном разнообразии видов и форм микроорганизмов, встречающихся в природе, и скорости их непрерывной эволюции. Микробиологи сходятся во мнении, что описанные в настоящее время микробы составляют от 0,1% до нескольких процентов их подлинного разнообразия. Свыше 90% из них не растут в искусственных средах и именуются общим термином «некультивируемые» [12], [13]. Это громадный пробел в таксономии! Нам практически ничего неизвестно об их метаболических путях и возможностях метаболизма. Здесь спрятано много удивительных тайн и будущих переворотов в науке. Когда эти тайны будут разгаданы, наши представления о жизни на Земле существенно изменятся, а классический учебник биохимии разрастется до объемов энциклопедии «Терра». Следовательно, нет ничего удивительного в том, что постоянно пополняется список веществ, подверженных биодеградации [14].
Правильный путь
Эффективность метода биодеградации основана на поразительных гибкости и совершенстве метаболических путей микроорганизмов. Вот один пример. Ацетонитрил, сильнополярный органический растворитель и комплексообразователь, сравнительно легко подвергается биодеградации культурами микроорганизмов, продуцирующих ферменты нитрилазы и амидазы, например, Nocardia rhodochrous LL100-211. Нокардии гидролизуют ацетонитрил сначала до ацетамида, а затем до практически безвредного ацетата аммония, легко утилизируемого микроорганизмами в качестве источника углерода и азота [15]. А в организме млекопитающих тот же ацетонитрил при помощи цитохрома Р450 окисляется до формальдегидциангидрина, далее распадающегося на чрезвычайно токсичные летальные метаболиты формальдегид и синильную кислоту (рис. 3) [16]. Вот насколько биохимия микроорганизмов совершеннее таковой у высших животных!
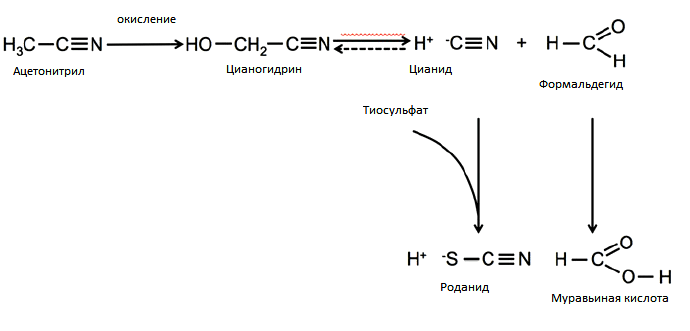
Рисунок 3. Метаболизм ацетонитрила у млекопитающих заканчивается летальными метаболитами — цианидом и формальдегидом. Этим определяется и токсичность самого ацетонитрила. А микробы при помощи ферментов нитрилаз превращают ацетонитрил в уксусную кислоту и аммиак — источники углерода и азота.
[16], рисунок с изменениями.
Примеров биодеградации много, и перегружать ими статью не стоит. Хотя для меня, как человека увлеченного, соблазн велик. Но выберем наиболее показательные.
Защитники генофонда
Высшие ароматические соединения (бензпирен, дибензофуран, дибенздиоксины и прочие), или арены, печально известны как сильнейшие канцерогены и мутагены. Самое страшное, что эти вещества легко образуются, например, при неполном сгорании органики и в небольшой концентрации всегда содержатся в дыме. То есть при вдыхании отравленного смогом городского воздуха всегда попадают в наши легкие. К тому же ароматические молекулы обладают высокой устойчивостью — это каждый изучал еще в школьном курсе химии.
А благодаря выраженной липофильности полиароматика еще и склонна аккумулироваться в живых организмах. Самое главное, полиароматические молекулы плоские и легко укладываются в стопку нуклеотидов ДНК, то есть обладают сродством к «молекуле жизни». Причем не просто укладываются, а в результате окисления цитохромами активируются и образуют с нуклеотидами ковалентные связи — так называемые аддукты. Это неизбежно приводит к повреждению хрупкой двойной спирали, на чем, собственно, и основан механизм токсического действия бензпирена, хризена и подобных молекул.
Кажется, что есть повод для паники — от таких зловредных соединений нет спасения! Тем не менее, с появлением в атмосфере Земли кислорода на ней постоянно что-то горело, полиароматические молекулы образовывались, а их уровень оставался низким. В роли спасителей выступили, как не трудно догадаться, микробы.
Поскольку высшие арены представляют собой большие молекулы достаточно сложного строения, для них характерны длинные, многообразные и сложные пути катаболизма с множеством промежуточных продуктов [17]. Эта сложность замечательно отображена на схеме (рис. 4). Циклы в молекуле раскрываются и деградируют последовательно, и при этом образуется арен более простого строения. Таким образом, к микробным метаболитам можно отнести большинство высших ароматических систем. А конечными продуктами деградации становятся, как видно из той же самой схемы, совершенно безвредные (и даже полезные для здоровья) уксусная и янтарная кислоты, вступающие далее в цикл Кребса.
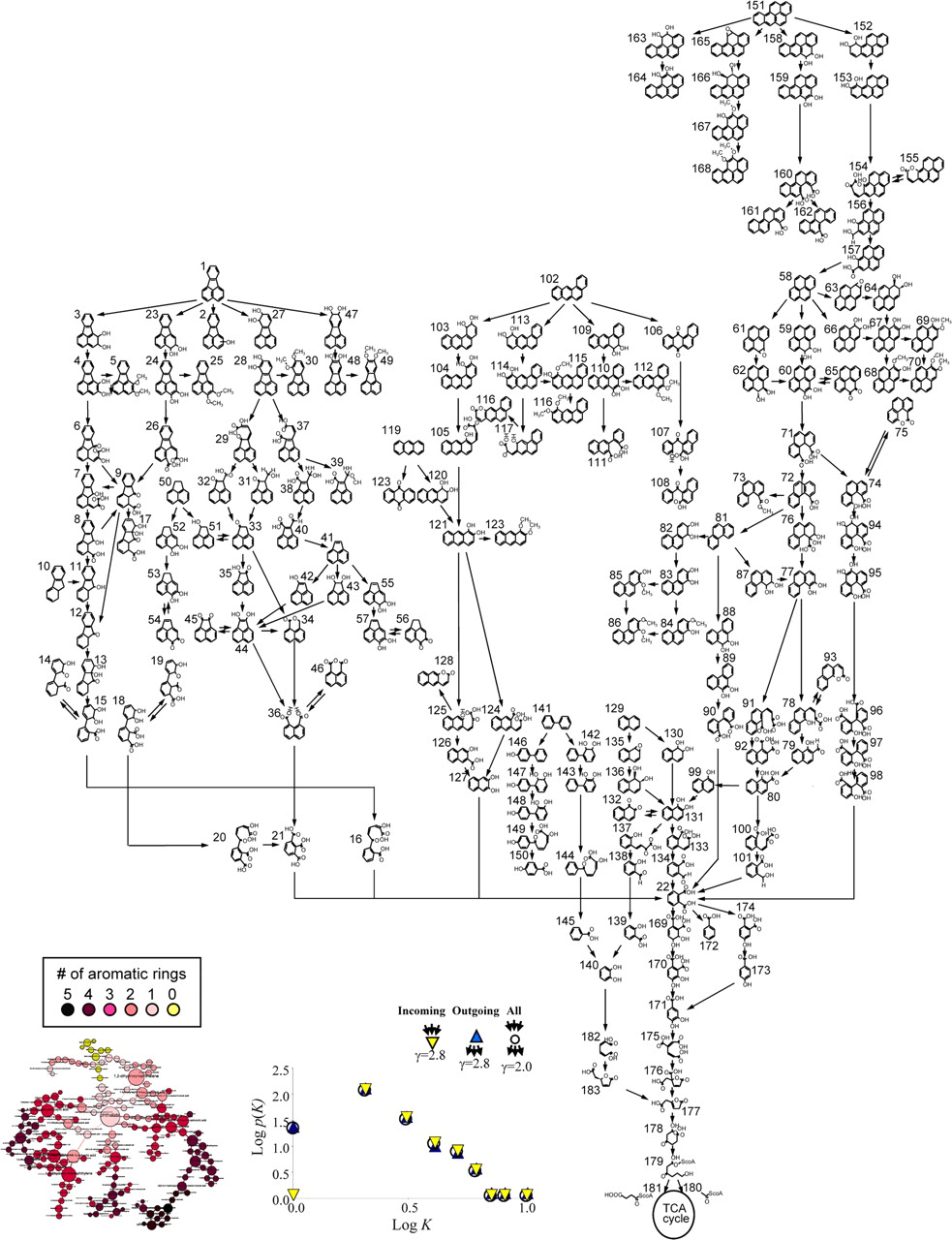
Рисунок 4. Биодеградация ароматических соединений. Читателя никто, конечно же, не заставляет учить эту схему наизусть, но она наглядно демонстрирует сложность метаболических путей биодеградации.
Чтобы увидеть рисунок в полном размере, нажмите на него.
Как результат, микробы способны кушать даже асфальт и каменный уголь [6], [8], [18], [19], состоящие из высших аренов очень сложного строения, по молекулярной массе сравнимых с белками, химически и физиологически крайне инертных. А высшие формы жизни не вымирают от рака и мутаций.
Трудное вещество
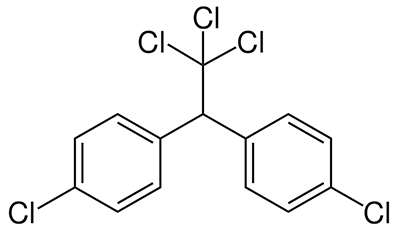
Знаменитейшим из пестицидов, безусловно, является вещество с мудреным названием 1,1,1-трихлор-2,2-ди(п-хлорфенил)этан. Широкой общественности запомнилось его сокращенное название ДДТ. Слава этого соединения не ослабевает даже сейчас, хотя официально ДДТ много лет как запрещен и не производится. Причина кроется в свойствах этого вещества (рис. 5а).
Будучи ароматическим соединением, ДДТ очень устойчив и может сохраняться в окружающей среде десятками лет. Он сильно гидрофобен, почти нерастворим в воде, но хорошо — в жирах. Поэтому ДДТ склонен накапливаться в тканях живых организмов, всегда содержащих липиды, и неприметно «портить» обменные процессы. Сочетание жирорастворимости и устойчивости привело к тому, что следовые концентрации ДДТ обнаруживались даже в жировой ткани пингвинов, живущих в Антарктиде и питающихся рыбой из океана (рис. 5б). То есть в местах, где ДДТ никогда не применялся. Как ни парадоксально, но еще одна опасность ДДТ связана с его... низкой токсичностью для теплокровных (ДДТ — инсектицид и изначально разрабатывался для борьбы с беспозвоночными). Поэтому негативное влияние пестицида на окружающую среду проявляется не сразу, только когда ДДТ уже накопился до высоких концентраций и проник в живые организмы.
Долгое время именно ДДТ преподносился как пример вещества, не подверженного биодеградации. Теперь же известно, что этот непростой ксенобиотик в ряд стадий окисляется культурами специализированных микробов до п-хлорбензойной кислоты [20]. Далее уже другими микробами п-хлорбензойная кислота подвергается катаболизму по пути, общему для всех ароматических веществ [21]. То есть для полного обезвреживания ДДТ требуется не один, а несколько видов микробов, так называемая консорция видов. Причем пути деградации отличаются у разных культур микроорганизмов. Впрочем, факт биодеградации ДДТ не должен вселять излишнее благодушие. Да, она происходит, но очень медленно, и большинство промежуточных продуктов разложения не менее опасны.
Быстрота эволюции
Ниже показана схема биодеградации другого очень известного пестицида — атразина. Это вещество является гербицидом и подавляет рост сорняков. Но, к сожалению, его биологическая активность распространяется на животных и человека.
Атразин относится к группе так называемых «эндокринных дизрупторов» и влияет на баланс половых стероидных гормонов у позвоночных. В результате действия атразина самцы лягушек становятся гермафродитами, а у человека развивается рак молочной железы.
Схема, представленная на рисунке 6, довольно эффектно демонстрирует, как токсичный ксенобиотик атразин в не очень длинный ряд стадий превращается в дружественные биосфере вещества — аммиак, углекислый газ и хлорид-ион. Разложение атразина осуществляет штамм бактерий Pseudomonas sp. ADP [22]. Все стадии, кроме распада промежуточного продукта биодеградации — циануровой кислоты, — осуществляются специфическими ферментами, кодируемыми плазмидными генами atzA, atzB и atzC. Атразин применяется на полях с 1958 года, и за этот срок у почвенной микрофлоры появилась плазмида с новыми генами, кодирующими ферменты, ранее не встречавшиеся в природе! Это замечательный пример эволюции в действии.
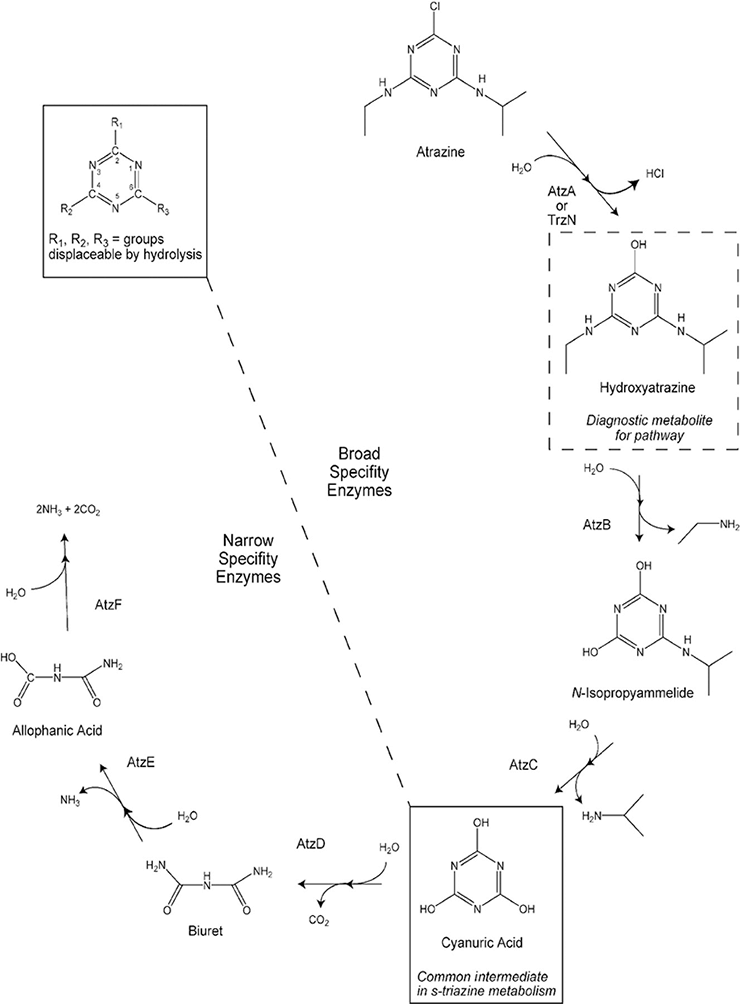
Рисунок 6. Биодеградация атразина. Эта схема нравится мне своей завершенностью: типичный ксенобиотик в небольшое число стадий превращается в природные вещества.
Поразительный пример
Иприт (ди-β-хлорэтилсульфид) (рис. 7, вверху) был одним из самых ранних боевых отравляющих веществ, применявшихся еще в Первую мировую войну, и остается одним из самых известных. И хотя из химических арсеналов его давно вытеснили более изощренные яды, утилизация начиненных ипритом боеприпасов до сих пор остается актуальной проблемой.

Рисунок 7. Яд и «противоядие». Вверху: структурная формула иприта. Внизу: гриб трутовик разноцветный Coriolus versicolor не только имеет живописную окраску, но и разлагает иприт.
«Википедия» и сайт www.boletosdeorum.pt
Иприт по своим химическим свойствам является сильным алкилирующим агентом, образует сшивки между молекулами биополимеров, этим необратимо их повреждая. Поэтому в месте попадания капель иприта на живую ткань появляются практически не заживающие нарывы и язвы. Конечно, крайне трудно представить, что какой-то живой организм способен усваивать иприт.
Поэтому деградация иприта [23] начинается с химического гидролиза щелочами до спирта тиодигликоля. Тиодигликоль — иприт, в котором концевые атомы хлора замещены на гидроксильные группы. Конечно, токсичность этого вещества неизмеримо ниже, и микроорганизмы-деструкторы с ним уже справляются сами, но все равно он подвергается биодеструкции чрезвычайно тяжело. Целая консорция микроорганизмов (как и в случае ДДТ) гидролизует тиодигликоль до смеси меркаптоэтанола и этиленгликоля. Оба соединения, в свою очередь, усваиваются микроорганизмами намного легче.
Таким образом, обезвреживание иприта является ярким примером комплексного подхода: биодеградация дополняется химической деструкцией. Впрочем, коллектив авторов из Японии в своей статье сообщает, что при помощи грибов Coriolus versicolor (рис. 7, внизу) и Tyromyces palustris им удалось обезвредить иприт напрямую, без применения химической стадии [24]. Этот пример биодеградации является, пожалуй, самым выдающимся!
Общие правила
Несмотря на бесконечное разнообразие метаболических путей, биодеградация подчиняется определенным общим закономерностям. Например, в аэробных условиях ксенобиотики окисляются, а в анаэробных, как правило, восстанавливаются. Негорючий растворитель тетрахлорэтилен [25] подвергается метаногенными архебактериями восстановительному дехлорированию с замещением хлора на водород. Конечным продуктом дехлорирования является этилен, а промежуточными — трихлорэтилен, изомерные дихлорэтилены и винилхлорид (рис. 8). Винилхлорид, кстати, является веществом более токсичным, чем исходный тетрахлорэтилен. То есть, биодеградация отнюдь не является панацеей и иногда усиливает токсические свойства веществ.
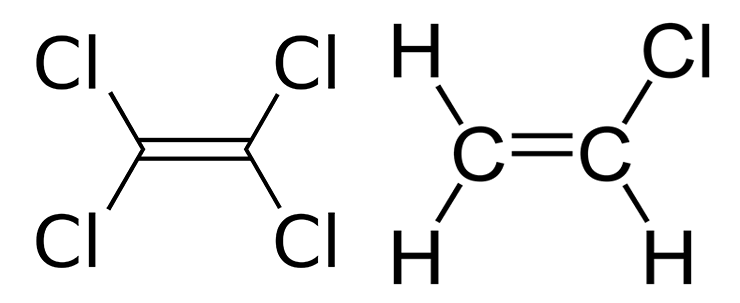
Рисунок 8. Структурные формулы тетрахлорэтилена (слева) и винилхлорида (справа).
«Википедия»
Детективная история
Цианиды (рис. 9) — излюбленное средство убийства в детективных романах. А еще они широко применяются в золотодобыче, производстве красителей и химии комплексных соединений. Все это многообразие сфер применения основано на одном ярко выраженном свойстве цианидов — они спонтанно образуют прочные комплексы с ионами переходных металлов. Причем неважно где — в пробирке, на золотом прииске или в эритроцитах человека.
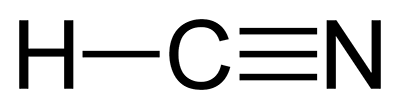
Рисунок 9. Структурная формула синильной кислоты.
Известно немалое разнообразие метаболических путей, которыми обезвреживаются цианиды [26]. Анаэробные бактерии восстанавливают синильную кислоту до метана и аммиака, аэробные микроорганизмы гидролизуют ее до формамида и далее до муравьиной кислоты и аммиака. В организме млекопитающих при помощи фермента роданазы цианид превращается в менее токсичный роданид, либо включается в состав непротеиногенной аминокислоты β-цианоаланина.
Дело в том, что цианиды, вопреки своей устрашающей репутации, не являются ксенобиотиками и широко распространены в природе. Косточки многих растений из семейства розоцветных содержат цианогенные гликозиды, выделяющие синильную кислоту при попытке эти косточки скушать. Поэтому красочно описанный в детективах запах синильной кислоты можно ощутить, просто разжевав во рту семечки из яблока. (А съев стакан ядрышек абрикосовых косточек, можно, между прочим, получить смертельную дозу цианида). Как следствие, многие живые организмы постоянно готовы к встрече с цианидами и научились их обезвреживать. Предупреждаю сразу: в очень низких концентрациях, конечно же! LD50 (полулетальная доза) синильной кислоты для мышей составляет 3,7 мг/кг, то есть она чрезвычайно токсична.
Похищение интеллектуальной собственности
Другой замечательный комплексообразователь и яд, угарный газ (монооксид углерода) (рис. 10), образуется в результате неполного сгорания органики и ряда биохимических процессов. Не имея ни вкуса, ни запаха, он может убить человека незаметно. Гемоглобин перестает связывать кислород, потому что угарный газ связывается с ним гораздо прочнее. То есть механизм токсического действия угарного газа тот же, что и у цианида. Наступает сонливость, потеря сознания, постепенно переходящая в смерть от удушья. Отравление угарным газом, к сожалению, нередкий гость в частных домах с печным отоплением.

Рисунок 10. Структурная формула монооксида углерода.
С точки зрения химика угарный газ интересен в первую очередь тем, что углерод в его составе не четырехвалентный (как в абсолютном большинстве своих соединений), а двухвалентный. Степень окисления +2 для углерода довольно экзотична.
Впрочем, все это нисколько не смущает [27] специализированных карбоксидобактерий, например Oligotropha carboxidovorans, которые в аэробных условиях окисляют СО в безобидный углекислый газ при помощи фермента дегидрогеназы монооксида углерода. В анаэробных условиях архебактерии восстанавливают его до метана. Надо отдать должное карбоксидобактериям, они большие труженики, занятые очисткой воздуха. Каждый год в результате бактериального окисления из нижних слоев атмосферы Земли удаляется сто миллионов тонн (!) угарного газа.
А наиболее «продвинутые» представители карбоксидобактерий могут не только получать энергию за счет окисления угарного газа в углекислый, но и использовать СО в качестве источника углерода. Для этого у них есть специальный метаболический путь, в котором СО-дегидрогеназа работает в сопряжении с ацетил-КоА-синтазой. Из угарного газа, коэнзима А и метильной группы, поставляемой аминокислотой метионином, образуется ацетил-КоА.
Здесь нельзя не вспомнить о том, что в шестидесятые годы корпорация «Монсанто» запатентовала метод производства уксусной кислоты из метанола и угарного газа при помощи родиевого катализатора по реакции:
СН3ОН + СО → СН3СООН
Эта простенькая (на первый взгляд!) и приносящая немалую прибыль реакция получила несколько помпезное название «процесс „Монсанто“».
Так вот, путь биологического усвоения СО является фактически тем же самым процессом, который бактерии осуществляют в окружающей среде, ничего не зная о патенте корпорации, и, естественно, его полностью игнорируя.
Изящный ход
Метиловый спирт не только очень сильный, но и коварный яд. Смертельная доза составляет всего тридцать миллилитров, а от пяти человек слепнет навсегда. А запах метанола практически не отличим от запаха винного, этилового спирта, и отравиться им очень легко. Поэтому, несмотря на то, что по меркам химических реактивов метанол очень дешев, достать его в лаборатории или на производстве особенно трудно. Для этого необходимо оформлять множество бумаг.
Причем сам по себе метанол практически не токсичен. Отравление вызывает формальдегид — чрезвычайно ядовитый и исстари применяемый биоцид, образующийся в результате окисления метилового спирта ферментом алкогольдегидрогеназой. Формальдегид — вещество реакционноспособное и склонное вступать в многообразные химические реакции. Поэтому он реагирует буквально со всем, что есть в организме, и является ядом широкого спектра действия.
Метилотрофные микроорганизмы, так же как люди, окисляют метанол алкогольдегидрогеназой до формальдегида. Но, в отличие от людей, формальдегид не убивает метилотрофов, а далее утилизируется в качестве источника углерода тремя известными путями, каждый из которых представляет собой реакцию присоединения с образованием гидроксиметильной группы [28].
В одном из путей формальдегид соединяется с глицином с образованием аминокислоты L-серина. Данную реакцию катализирует фермент серингидроксиметилаза, причем она обратима — СН2ОН группа серина является источником одноуглеродных молекул в живых системах.
В двух других путях формальдегид при помощи соответствующих ферментов присоединяется к пятиуглеродному сахару пентозе с образованием шестиуглеродного сахара гексозы (рис. 11). Фактически задолго до гениального русского химика-органика микробы «открыли» знаменитую реакцию Бутлерова — олигомеризацию формальдегида в сахар! То есть, в любом из трех случаев, известнейшие яды метанол и формальдегид в одну—две стадии превращаются в полезные вещества, аминокислоты и сахара! Эти превращения — яркая иллюстрация удивительного совершенства микробных метаболических путей.

Рисунок 11. Один из путей утилизации формальдегида метилотрофными бактериями. Фактически это та самая реакция Бутлерова, которая, согласно современным представлениям, привела к появлению сахаров в Первичном океане древней Земли, а впоследствии — и жизни на ней.
[28], рисунок с изменениями
Крайне любопытно, что при помощи фермента тирозинфеноллиазы из Escherichia intermedia образовавшийся L-серин может с отщеплением молекулы воды конденсироваться с фенолом с образованием незаменимой аминокислоты L-тирозина [25]! Фенол — известный антисептик, эффективно денатурирующий белки. На этом основана его высокая токсичность. Фенол входит в состав гуаши, и каждому, кто рисовал этой краской, знаком его специфический запах. Реакция конденсации фенола с серином также является обратимой, поэтому фенол в следовых концентрациях образуется как естественный метаболит ароматических аминокислот. Включение двух токсичных ксенобиотиков в состав аминокислоты, входящей в состав белков (рис. 12), является, пожалуй, наиболее изящным примером биодеградации.
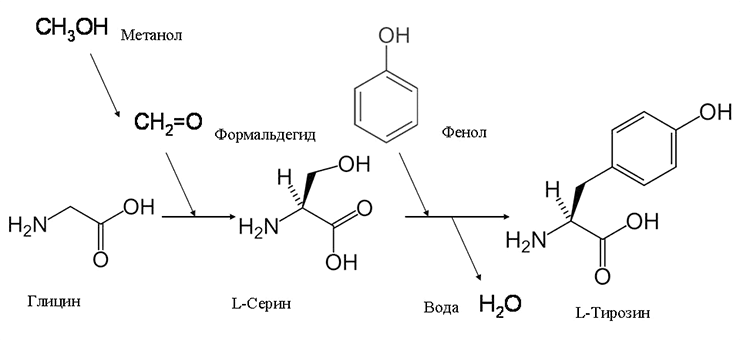
Рисунок 12. Вот так два ядовитых вещества превращаются в одно полезное. Включение формальдегида и фенола в состав аминокислот — блестящий пример биодеградации. Синтез серина из метанола осуществляется некоторыми метилотрофными бактериями, тирозина из фенола — Escherichia intermedia.
рисунок автора статьи
Сочетание свойств
Одним из наиопаснейших загрязнителей окружающей среды является тетраэтилсвинец, который длительное время использовался как антидетонационная присадка к моторным топливам (рис. 13). Китай производит его до сих пор для стран Третьего мира. Кроме того, тетраэтилсвинец во всем мире продолжает добавляться в авиационный бензин и специальные марки бензина для спортивных автомобилей.
Для него вообще не существует предельно допустимой концентрации — присутствие тетраэтилсвинца в воде даже на пороге обнаружения самым чувствительным прибором делает ее непригодной для использования!
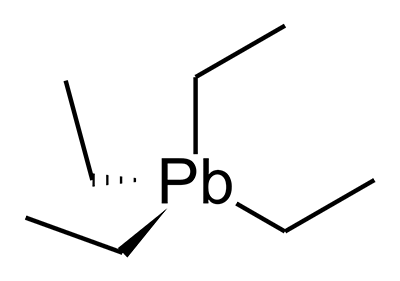
Рисунок 13. Структурная формула тетраэтилсвинца.
Тетраэтилсвинец Pb(C2H5)4 относится к так называемым элементоорганическим веществам. То есть это типичное органическое вещество — летучая жидкость, несмешивающаяся с водой, но отлично растворимая в жирах. И в то же время оно содержит свинец — элемент, совсем не характерный для органической химии.
Собственно, свинец и придает веществу токсичность. А боковые этильные группы придают ему липофильность и способность беспрепятственно проникать через клеточные мембраны. От этого токсичность тетраэтилсвинца становится экстремально высокой.
Казалось бы, такое вещество никто не способен скушать. И тем не менее, тетраэтилсвинец гидролизуют почвенные микроорганизмы до этилового спирта и ионов двухвалентного свинца [29]. Разумеется, свинец никуда не девается и остается опасным для окружающей среды. Но неорганические соли свинца менее токсичны, поскольку не проникают через липидные мембраны клеток.
Ферментативная металлургия
Для переходных (еще часто называемых «тяжелыми», хотя это не вполне корректно) металлов характерны несколько степеней окисления. Соответственно, биодеградация в их случае может сводиться к окислению или, наоборот, восстановлению. Хроматы CrO42- и дихроматы Cr2O72- (производные типичного переходного металла — хрома) — очень сильные окислители и канцерогены [30] — восстанавливаются Bacillus sphaericus до ионов трехвалентного хрома Cr3+, значительно менее токсичного и на три порядка менее сильного мутагена.
Соли двухвалентной ртути даже более токсичны, чем соли свинца. И тот, и другой элементы имеют сродство к доменам [31] «цинковых пальцев» в белках, намного большее, чем сам цинк, и легко вытесняют из активных центров этот полезный металл. При этом структура домена нарушается, и белок моментально утрачивает активность, причем необратимо.

Рисунок 14. «Жидкое серебро» — металлическая ртуть — может быть получена, в том числе, при помощи фермента.
сайт interesno.cc
Поскольку в следовых концентрациях ртуть присутствует в земной коре, ряд бактерий «научился» ее обезвреживать весьма своеобразным образом. Эти микроорганизмы содержат плазмидные гены mer, кодирующие фермент НАДФ(Н)-зависимую редуктазу, восстанавливающую ионы Hg2+ до металлической ртути (рис. 14), значительно менее ядовитой [32]. Мы знаем множество ферментов с самыми разнообразными активностями, зачастую весьма необычными. Но фермент, осуществляющий металлургический процесс, бесспорно, даже на их фоне является уникальным!
Рациональный подход
Разумеется, было бы нерационально формировать метаболические пути биодеградации «с нуля». Гораздо проще приспосабливать под новые нужды те пути, которые уже существуют в природе. Следует иметь в виду, что все органические вещества, состоящие из углерода, имеют общие свойства.
Полиэтилен (рис. 15) является самым массовым и широко известным искусственным полимером. Он дешев в производстве, получается из доступного сырья, сравнительно стоек, обладает хорошими прочностными характеристиками, неядовит. Поэтому из полиэтилена делают все — от водопроводных труб до пищевой пленки.
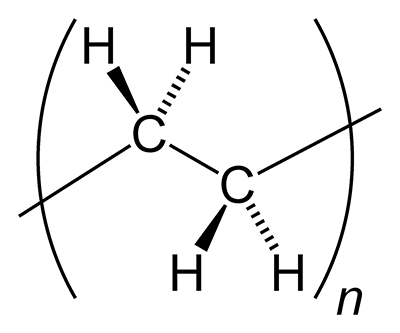
Рисунок 15. Фрагмент структуры полиэтилена.
Для нас же главным является то, что по своей химической природе полиэтилен является высшим алканом, состоящим из повторяющихся метиленовых звеньев —(СН2)n —. То есть, строение его очень похоже на строение пчелиного воска и жиров, которые микробы давно научились усваивать. Правда, есть отличие — цепочки полиэтилена значительно длиннее. Соответственно, его молекулы менее подвижны и в реакции вступают хуже. Следовательно, усвоить полиэтилен микробу все-таки труднее, чем воск или триглицерид. Поэтому полиэтиленовые пакеты даже в почве сохраняются годами [7], [9], [10].
Тем не менее, полиэтилен медленно разлагается почвенными бактериями Pseudomonas aeruginosa аналогично всем парафинам: сначала окисляется по схеме алкан → спирт → альдегид → жирная кислота → ацил-КоА, затем подвергается классическому β-окислению до уксусной кислоты [33]. Поскольку макромолекула полиэтилена подвергается ферментативной деструкции только с конца, разветвленный полиэтилен разлагается микроорганизмами быстрее, чем линейный [7]. Биодеградацию полиэтилена можно еще ускорить, если заранее внести в него так называемые «прооксиданты» — вещества, которые при попадании того же пакета в окружающую среду приобретают свойства окислителей и дополнительно рвут макромолекулы на куски.
Фенолформальдегидная смола (рис. 16) является, пожалуй, самой «классической» пластмассой, из которой делают выключатели и шары для бильярда. Так же как полиэтилен, фенолформальдегидные смолы до недавнего времени считались неприступными для ферментативного расщепления: сшитый в трехмерную сеть ни в чем не растворимый полимер слишком устойчив!
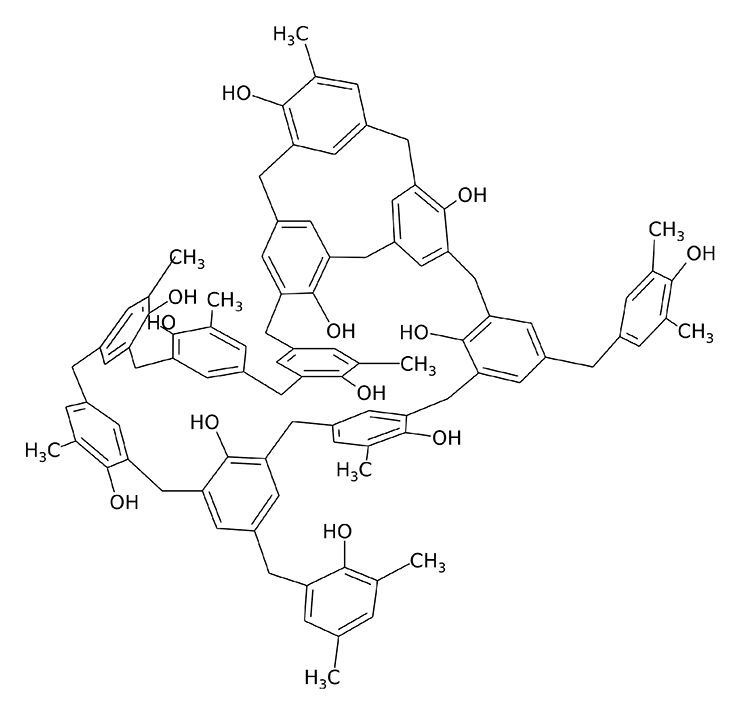
Рисунок 16. Фрагмент структуры фенолформальдегидной пластмассы.
Однако гриб Phanerochaete chrysosporium начинает растворять частицы пластика спустя всего трое суток после посева. При этом отмечается накопление в среде фенола — одного из продуктов биодеградации [34]. Как уже говорилось в начале, в природе грибы-трутовики разлагают лигнин древесины при помощи ферментов лакказ; те же самые лакказы принимают участие в деградации фенолформальдегидных пластмасс, по свойствам сходных с лигнином.
Из огня да в полымя
Зачастую биодеградация какого-либо не встречающегося в природе вещества сопровождается образованием других веществ, тоже неприродных. Например, взрывчатое вещество гексоген в анаэробных условиях (в активном иле) восстанавливается до смеси нитрозопроизводных. Один из них — диметилнитрозамин — особенно интересен тем, что в результате дальнейшего метаболического восстановления димеризуется, превращаясь в два изомерных диметилгидразина: симметричный и несимметричный (рис. 17).
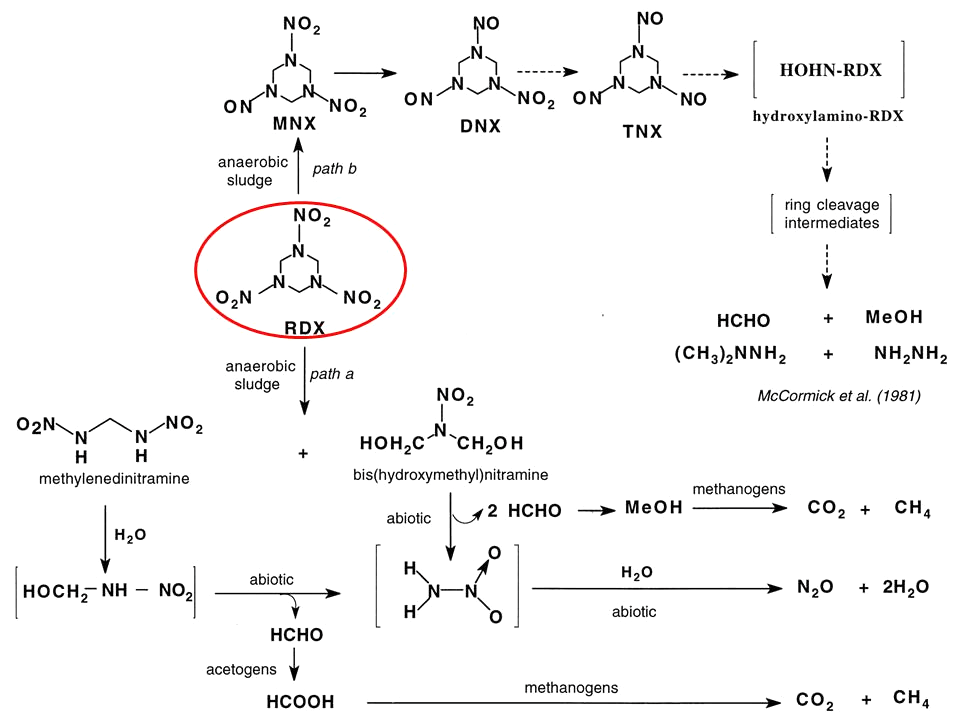
Рисунок 17. Анаэробная биодеградация гексогена (обведен красным) сопровождается образованием другого крайне вредного для окружающей среды вещества — гептила (CH3)2NNH2.
Чтобы увидеть рисунок в полном размере, нажмите на него.
Несимметричный диметилгидразин чрезвычайно токсичен и реакционноспособен, а известен как гептил — компонент ракетного топлива (рис. 18) [35].

Рисунок 18. Эта рухнувшая в алтайский лес отработанная ступень космической ракеты наверняка содержит гептил — несимметричный диметилгидразин.
Но это не фатально. Сам гептил, по методу отечественных разработчиков [36], утилизируется культурами бактерий Acinetobacter sp. H-1, Rhodococcus sp. H-2 и Arthrobacter sp. H-3 и вот теперь уже полностью обезвреживается.
О пользе безмозглости
Все производные фосфоновых кислот и некоторые замещенные фосфаты очень токсичны. Причем токсичность их имеет различные «оттенки» в зависимости от природы заместителей, поэтому среди фосфорорганических веществ есть пестициды, боевые отравляющие вещества и сильнодействующие лекарственные препараты.
Но, несмотря на внешнее разнообразие, все вещества этой группы имеют строго одно и то же биологическое свойство — они избирательно и необратимо ингибируют ферменты сериновые гидролазы. Например, ацетилхолинэстеразу, гидролизующую нейромедиатор ацетилхолин, передающий сигналы из нервной системы в мышцы. То есть все фосфорорганические соединения вызывают мышечные спазмы и паралич, в конце концов приводящий к остановке дыхания.
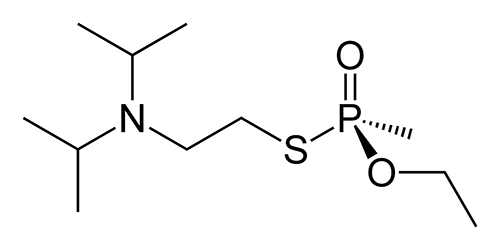
Ярким примером этой группы веществ является боевое отравляющее вещество американского производства VX (рис. 19), ставшее известным широкой публике благодаря кинобоевику «Скала». Для известности есть повод, правда, печальный. VX является одним из самых ядовитых веществ, созданных человеком. Следует вспомнить о том, что LD50 VX перорально для человека составляет всего 70 мкг/кг! То есть в 53 раза ниже, чем у синильной кислоты, о которой говорилось выше!
Впрочем, у нас с вами в результате эволюции развилась самая сложная в природе нервная система. А у представителей царства грибов ее нет вообще, и в данном случае это дает им неоспоримое преимущество. Замечательный по полноте собранного материала обзор [37] дает представление о микробной и грибной деградации фосфорорганических пестицидов и боевых отравляющих веществ, ее путях, ферментах и генетической основе. В указанном обзоре приведена схема биодеградации VX до фосфата и сульфата, аммиака, воды и углекислого газа при помощи широко известного съедобного гриба вёшенки Pleurotus ostreatus. В биодеградации фосфорорганических веществ участвуют экзотические ферменты, например С-Р-лиазы, способные разрывать связь углерод—фосфор, в природе встречающуюся очень редко.
Химия или биотехнология?
Известны и такие случаи биодеградации, в которых каждое промежуточное соединение является промышленно важным. Фактически это уже не биодеградация, а биотехнологическая трансформация вещества. Следует помнить о том, что живая клетка — это самая совершенная химическая фабрика. Вот почему биотехнологические процессы в наше время все настойчивее вторгаются в химическое производство. Например, известен следующий путь биодеградации антрацена грибком Aspergillus fumigatus, включающий в себя антрон, антрахинон, фталевый ангидрид и фталевую кислоту — все ценные крупнотоннажные продукты химической промышленности (рис. 20) [38]. Впрочем, это уже отдельная большая и интересная тема.
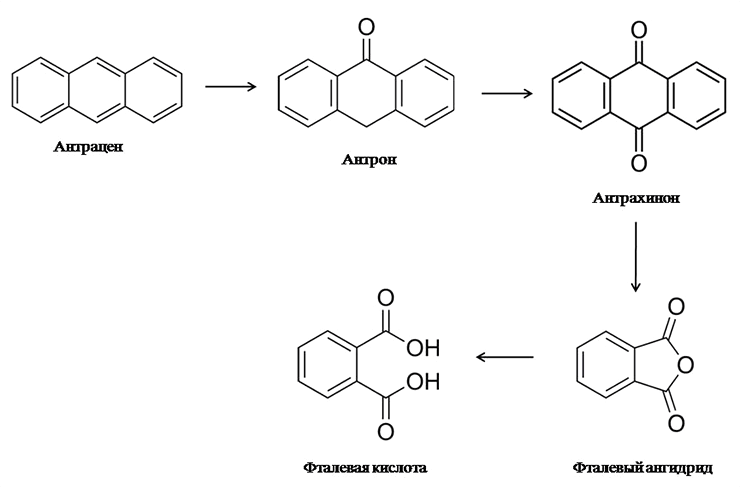
Рисунок 20. Биодеградация антрацена грибком Aspergillus fumigatus включает целый ряд практически важных веществ.
[38], рисунок с изменениями
Поймать двух зайцев
Если ксенобиотики способны обезвреживаться биосферой и включаться в ее состав в виде биогенных элементов, то можно пофантазировать и развить идею дальше. А что, если неприродные вещества превращать непосредственно в пищу?! То есть вместо одной проблемы решить сразу две — защитить окружающую среду и спасти население планеты от голода. Ведь ряд ксенобиотиков содержит в себе немало ценных атомов, например связанный азот, в котором нуждается все живое и мы с вами. Впрочем, зачем фантазировать? Такой пример уже есть. Предложено культивирование съедобных грибов на богатых азотом пластиках полиуретанах (рис. 21) с целью дальнейшего их употребления в пищу [39]! И даже создание на этой основе мини-ферм.
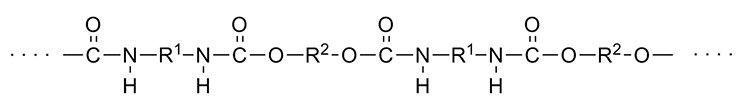
Рисунок 21. Полиуретаны содержат значительное количество азота — ценного биогенного элемента.
Ксенобиотик или пища?
Но микроорганизмы не только обезвреживают неприродные вещества. В ряду поколений они вырабатывают к ним все большую устойчивость, превращаясь в специализированные штаммы-деструкторы конкретных соединений. Римма Павловна Наумова (впоследствии профессор Казанского университета) в своей диссертационной работе [40] продемонстрировала пример адаптации накопительной культуры бактерий к ε-капролактаму (рис. 22) — мономеру капрона, широко известного синтетического волокна.

Рисунок 22. Капролактам и капрон. Слева: структурная формула капролактама — мономера капроновых волокон. А справа капрон, который делают из капролактама. Его, кстати, тоже едят микробы.
«Википедия» и сайт images.md.prom.st
Первый посев показал признаки роста только через 4 недели при концентрации капролактама всего полграмма в литре культуральной среды. Четвертый пересев продемонстрировал биодеградацию капролактама в концентрации уже 2 грамма в литре в течение 1–2 дней! Но это еще не все! Автору удалось получить штамм, разлагающий капролактам в концентрации 5 г/л и даже полимерный капрон (полиамид 6-аминокапроновой кислоты). К капролактаму в концентрации 15 граммов на литр (а это тридцатикратное увеличение концентрации по сравнению с исходной) вырабатывалась частичная адаптация. Фактически, капролактам для этих микробов уже не ксенобиотик, а пища .
Генетические основы биодеградации ε-капролактама до сих пор не известны. В последние годы в подмосковном Пущино занялись изучением плазмид биодеградации ε-капролактама и уже добились некоторых успехов: исследован оперон окисления и транспорта адипината — промежуточного продукта деградации капролактама [48]. — Ред.
Эпохальное событие
Но, специализируясь на одном источнике питания, микробы утрачивают способность усваивать другие. А реальные техногенные катастрофы (например, разливы нефти) сопровождаются попаданием в окружающую среду целой смеси токсичных веществ. В начале 1970-х гг. американский генетик бенгальского происхождения Ананда Мохан Чакрабарти, в то время работавший в кампании «Дженерал электрик», попытался решить эту проблему «в лоб». Для этого он взял бактерию Pseudomonas putida, одного из самых популярных промышленных биодеструкторов, и внес в нее ни много ни мало четыре плазмиды, кодирующие способность усваивать компоненты нефти.

Рисунок 23. Разнообразие структур соединений, разлагаемых «супербациллой» — настоящим универсалом биодеградации. а — Октан. б — Нафталин. в — Камфора. г — Салициловая кислота.
«Википедия»
Искусственно выведенный путем переноса плазмид штамм, прозванный «супербациллой», разлагает целый ряд продуктов химической промышленности, имеющих значительные структурные различия — камфору, октан, салициловую кислоту и нафталин (рис. 23) [41]. Благодаря этой способности, «супербацилла» на неочищенной нефти растет лучше природных культур.
Надо сказать, что на практике «супербацилла» никогда не использовалась для ликвидации нефтяных загрязнений. То есть она стала своего рода биотехнологической Царь-пушкой, никогда не стрелявшей. Причина в том, что культура, содержащая столько плазмид, неустойчива и склонна терять «лишние» гены, то есть вырождаться.
И тем не менее, она открыла новую эпоху в биотехнологии, став первым в истории запатентованным генномодифицированным организмом. Впоследствии были созданы другие штаммы, менее известные общественности и без приставки «супер-», но принесшие реальную пользу. Для нас же важно, что эпоха патентования генномодифицированных организмов началась именно с биодеградации. Это — показатель ее практической востребованности. А является генная инженерия благом или злом — уже отдельная тема.
Согласно работе, посвященной патентованию в области биоремедиации, за период с 1990 по 2013 годы в мире вышло 443 патента по этому направлению (имеются в виду только международные патенты) [42]. Из них более 60%, как нетрудно докадаться, приходится на США, 23% — на Азию, и только 10% — на старушку Европу. Российские патенты собраны в базе ФИПС. И здесь биодеградация представлена довольно весомо. Большинство патентов посвящены биодеградации нефти и нефтепродуктов, меньше — биодеградации пестицидов. Ряд патентов отражает биодеградацию других продуктов химической промышленности, присутствующих в сточных водах, и боевых отравляющих веществ. В замечательном учебнике «Прикладная экобиотехнология» довольно подробно описаны коммерческие биопрепараты на основе штаммов биодеструкторов [43]. В России их разработкой занимаются в Москве, Пущино, Санкт-Петербурге, Уфе, Казани, Перми, Сыктывкаре, Екатеринбурге и Новосибирске.
Кстати говоря, именно исследование окисления камфоры культурой Pseudomonas putida позволило изучить механизм каталитического действия цитохрома Р450. То есть биодеградация принесла не только практическую пользу, но и внесла свой вклад в фундаментальное научное знание.
А был ли ксенобиотик?
Способность биосферы к утилизации и обезвреживанию ксенобиотиков основана на том, что большинство из них ксенобиотиками не является. То есть в следовых количествах образуются в биосфере и постоянно в ней присутствует.
Например, четыреххлористый углерод (тетрахлорметан) разлагается культурой Pseudomonas sp. KC с образованием чрезвычайно токсичных промежуточных метаболитов — фосгена (дихлорангидрид угольной кислоты) и тиофосгена (рис. 24). Конечно, существуют эти опасные молекулы очень недолго — доли секунды — и моментально гидролизуются [44] (рис. 25).
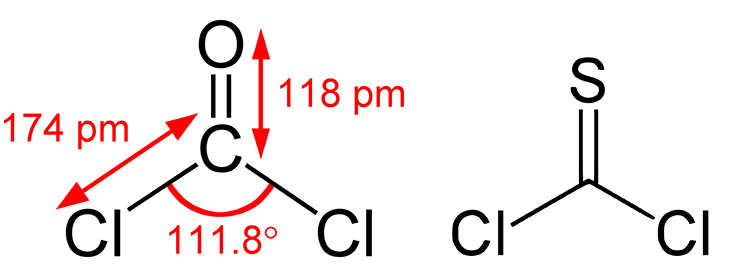
Рисунок 24. Структурные формулы фосгена (слева) и тиофосгена (справа).
«Википедия»
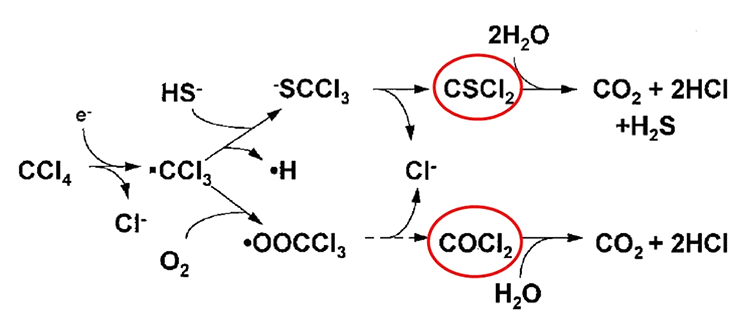
Рисунок 25. Аэробная биодеградация четыреххлористого углерода с образованием в качестве промежуточных метаболитов тиофосгена (вверху) и фосгена (внизу). На схеме эти страшные для всего живого вещества обведены красным цветом.
Фосген обладает запахом подгнивших фруктов и перепрелой листвы, но этот безобидный аромат не должен вводить в заблуждение. Он, так же как упоминавшийся выше иприт, склонен присоединяться к биополимерам, образуя с ними аддукты.
Будучи газообразным веществом при комнатной температуре, фосген поражает в первую очередь легкие, вызывая их отек и смерть от удушья. В Первую мировую войну фосген применяли как боевое отравляющее вещество, да и сегодня он не утратил значение в производстве поликарбонатов и мочевины.
Тиофосген (дихлорангидрид теперь уже тиоугольной кислоты) по свойствам схож с фосгеном, но тяжелее и при комнатной температуре представляет собой жидкость красного цвета. Он тоже очень ядовит, применяется в производстве тиомочевины и тиокарбаматов. Представить такие вещества, символизирующие саму смерть, в качестве природных крайне сложно!
Конечно, в этом месте последует справедливое возражение. Мол, фосген образуется в живых клетках, но четыреххлористый углерод, метаболитом которого он является, в природе не присутствует. Применяется четыреххлористый углерод в качестве промышленного растворителя, отличается негорючестью — им даже тушат возгорания. Но при этом весьма ядовитый, поражает печень и используется фармакологами в тестах на гепатопротективные свойства лекарств.
Четыреххлористый углерод, что удивительно, тоже является природным веществом — он среди прочих галогеналканов выделяется морскими красными водорослями Asparagopsis armata (рис. 26) [45]. То есть в биосфере существуют метаболические пути, ведущие и к четыреххлористому углероду, и к фосгену! А сам фосген с изрядной долей условности все-таки можно считать природным соединением.

Рисунок 26. Красная водоросль Asparagopsis armata — природный продуцент четыреххлористого углерода.
сайт www.marlin.ac.uk
Пара слов о своем
Микроорганизмы выживают при контакте даже с таким губительным для всех форм жизни веществом, как белый фосфор, способны адаптироваться к его присутствию в окружающей среде и перерабатывать его в менее опасные соединения. Впрочем, об этом довольно подробно (и, надеюсь, увлекательно) рассказано в статьях [46], [47].
Заключение
Перечисляя примеры биодеградации, многие из которых уже прочно вошли в практику, невольно испытываешь восхищение гибкостью метаболических путей. Биосфера способна перерабатывать практически любое химическое вещество. Микробные популяции создают новые, не существовавшие ранее ферменты (а заодно и кодирующие их плазмидные гены), в эксклюзивном порядке к любому продукту химической промышленности. Понимание этого вселяет надежду на то, что современный экологический кризис когда-нибудь будет преодолен. Ну а мы, люди науки, должны всеми мерами этому способствовать.
Литература
- D. Floudas, M. Binder, R. Riley, K. Barry, R. A. Blanchette, et. al.. (2012). The Paleozoic Origin of Enzymatic Lignin Decomposition Reconstructed from 31 Fungal Genomes. Science. 336, 1715-1719;
- Archibald F.S. and Fridovich I. (1983). Oxygen radicals, oxygen toxicity and the life of microorganisms. Acta Medica Portuguesa. 4, 101–112;
- Бертини И., Грей Г., Стифель Э., Валентине Дж. Биологическая неорганическая химия: структура и реакционная способность (Т. 1). М.: БИНОМ, 2013. — 456 с.;
- Трифонов О.В. Оценка эффективности работы очистных сооружений по гидробиологическим показателям. Руководство по контролю за работой очистных сооружений биологической очистки сточных вод в аэротенках. «Издательские решения», 2016. — 30 с.;
- «Зеленые» революционеры;
- Бактерии-нефтедеструкторы для биоремедиации супесчаных почв Воронежской области;
- А ты такой холодный, как... пластик в океане;
- Пределы биодоступности углеводородов в грунтах;
- «Дизайнерские» ферменты защищают от нервно-паралитических ядов;
- «Пластик, сэр!», или Бактериальная диета в стиле хай-тек;
- Пластик на завтрак;
- Иммуностимулирующие филаментные бактерии: наконец-то они приручены!;
- Zeyaullah M., Kamli M.R., Islam B., Atif M., Benkhayal F.A., Nehal M. et al. (2009). Metagenomics — an advanced approach for noncultivable micro-organisms. Biotechnology and Molecular Biology Reviews. 4, 49–54;
- Wackett L.P. The Metabolic pathways of biodegradation. In: The Prokaryotes: Applied Bacteriology and Biotechnology. Springer-Verlag Berlin Heidelberg, 2013. P. 383–393;
- DiGeronimo M.J. and Antoine A.D. (1976). Metabolism of Acetonitrile and Propionitrile by Nocardia rhodochrous LL100-211. Appl. Environ. Microbiol. 31, 900–906;
- Mateus F.H., Lepera J.S., Lanchote V.L. (2005). Determination of acetonitrile and cyanide in rat blood: application to an experimental study. J. Anal. Toxicol. 29, 105–109;
- O. Kweon, S.-J. Kim, R. D. Holland, H. Chen, D.-W. Kim, et. al.. (2011). Polycyclic Aromatic Hydrocarbon Metabolic Network in Mycobacterium vanbaaleniiPYR-1. Journal of Bacteriology. 193, 4326-4337;
- Eric E. Igbinigie, Simon Aktins, Yvonne van Breugel, Susan van Dyke, Michael T. Davies-Coleman, Peter D. Rose. (2008). Fungal biodegradation of hard coal by a newly reported isolate,Neosartorya fischeri. Biotechnol. J.. 3, 1407-1416;
- J.-S. Kim, D. E. Crowley. (2007). Microbial Diversity in Natural Asphalts of the Rancho La Brea Tar Pits. Applied and Environmental Microbiology. 73, 4579-4591;
- J. M. Aislabie, N. K. Richards, H. L. Boul. (1997). Microbial degradation of DDT and its residues—A review. New Zealand Journal of Agricultural Research. 40, 269-282;
- Francisco P.B., Ogawa N., Suzuki K., Miyashita K. (2001). The chlorobenzoate dioxygenase genes of Burkholderia sp. strain NK8 involved in the catabolism of chlorobenzoates. Microbiology. 147, 121–133;
- N. Shapir, E. F. Mongodin, M. J. Sadowsky, S. C. Daugherty, K. E. Nelson, L. P. Wackett. (2007). Evolution of Catabolic Pathways: Genomic Insights into Microbial s-Triazine Metabolism. Journal of Bacteriology. 189, 674-682;
- Варфоломеев С.Д. Химическая энзимология. М.: «Академия», 2005. — 473 c.;
- Wariishi H., Itoh N., Yoshida M., Tanaka H. (2002). Complete degradation of Yperite, a chemical warfare agent, by basidiomycetes. Biotechnology Letters. 24, 501–505;
- Fathepure B.Z. and Boyd S.A. (1988). Dependence of Tetrachloroethylene Dechlorination on Methanogenic Substrate Consumption by Methanosarcina sp. Strain DCM. Appl. Environ. Microbiol. 54, 2976–2980;
- Stephen Ebbs. (2004). Biological degradation of cyanide compounds. Current Opinion in Biotechnology. 15, 231-236;
- Stephen W. Ragsdale. (2004). Life with Carbon Monoxide. Critical Reviews in Biochemistry and Molecular Biology. 39, 165-195;
- Hiroya Yurimoto, Nobuo Kato, Yasuyoshi Sakai. (2005). Assimilation, dissimilation, and detoxification of formaldehyde, a central metabolic intermediate of methylotrophic metabolism. Chem. Record. 5, 367-375;
- H. Teeling, H. Cypionka. (1997). Microbial degradation of tetraethyl lead in soil monitored by microcalorimetry. Applied Microbiology and Biotechnology. 48, 275-279;
- Arundhati Pal, A.K. Paul. (2004). Aerobic chromate reduction by chromium-resistant bacteria isolated from serpentine soil. Microbiological Research. 159, 347-354;
- Роль слабых взаимодействий в биополимерах;
- Tamar Barkay, Susan M. Miller, Anne O. Summers. (2003). Bacterial mercury resistance from atoms to ecosystems. FEMS Microbiol Rev. 27, 355-384;
- M. M. Reddy, M. Deighton, Rahul K. Gupta, S. N. Bhattacharya, R. Parthasarathy. (2009). Biodegradation of oxo-biodegradable polyethylene. J. Appl. Polym. Sci.. 111, 1426-1432;
- Adam C. Gusse, Paul D. Miller, Thomas J. Volk. (2006). White-Rot Fungi Demonstrate First Biodegradation of Phenolic Resin. Environ. Sci. Technol.. 40, 4196-4199;
- J. Hawari, A. Halasz, T. Sheremata, S. Beaudet, C. Groom, et. al.. (2000). Characterization of Metabolites during Biodegradation of Hexahydro-1,3,5-Trinitro-1,3,5-Triazine (RDX) with Municipal Anaerobic Sludge. Applied and Environmental Microbiology. 66, 2652-2657;
- Мурзаков Б.Г. (2001). Способ биодеструкции гептила — несимметричного диметилгидразина. Патент 2174553;
- Brajesh K. Singh, Allan Walker. (2006). Microbial degradation of organophosphorus compounds. FEMS Microbiol Rev. 30, 428-471;
- Jin-Shao Ye, Hua Yin, Jing Qiang, Hui Peng, Hua-Ming Qin, et. al.. (2011). Biodegradation of anthracene by Aspergillus fumigatus. Journal of Hazardous Materials. 185, 174-181;
- J. R. Russell, J. Huang, P. Anand, K. Kucera, A. G. Sandoval, et. al.. (2011). Biodegradation of Polyester Polyurethane by Endophytic Fungi. Applied and Environmental Microbiology. 77, 6076-6084;
- Наумова Р.П. Микробный метаболизм 6-капролактама: дис.....канд. биол. наук. — Казань, 1966. — 183 с.;
- Cases I. and de Lorenzo V. (2005). Genetically modified organisms for the environment: stories of success and failure and what we have learned from them. Int. Microbiol. 8, 213–222;
- Saraswat S. (2014). Patent analysis on bioremediation of environmental pollutants. J. Bioremed. Biodeg. 5, 251;
- Кузнецов, А.Е., Градова Н.Б., Лушников С.В., Энгельхарт М., Вайссер Т., Чеботарева М.В. Прикладная экобиотехнология. Учебник для высшей школы. (Т.1., 2-е изд.). М.: БИНОМ, 2015. — 629 с.;
- T A Lewis, R L Crawford. (1995). Transformation of carbon tetrachloride via sulfur and oxygen substitution by Pseudomonas sp. strain KC.. J. Bacteriol.. 177, 2204-2208;
- Maria Kladi, Constantinos Vagias, Vassilios Roussis. (2004). Volatile halogenated metabolites from marine red algae. Phytochem Rev. 3, 337-366;
- Миндубаев А.З., Волошина А.Д., Валидов Ш.З., Яхваров Д.Г. (2017). Биодеградация белого фосфора. Природа. 5, 29-43;
- Биодеградация белого фосфора: как яд стал удобрением;
- T. Z. Esikova, O. V. Volkova, S. A. Taran, A. M. Boronin. (2015). Key role of the dca genes in ε-caprolactam catabolism in Pseudomonas strains. Microbiology. 84, 726-729.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚