
Биофотовольтаика. По-настоящему зелёная энергия
30 октября 2013
Биофотовольтаика. По-настоящему зелёная энергия
- 2267
- 3
- 2
Михаэль Гретцель держит в руках рекордную солнечную панель, изготовленную с применением технологии DSSC
-
Автор
-
Редакторы
Статья на конкурс «био/мол/текст»: Любое растение, способное к фотосинтезу, — природная станция по преобразованию солнечной энергии в энергию химической связи. Современная биология располагает знаниями, позволяющими скопировать и использовать этот механизм жизни для получения электричества. Насколько же эффективно подобное «подглядывание» за природой?
Конкурс «био/мол/текст»-2013
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2013 в номинации «Лучшее новостное сообщение».
Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Деньги правят миром
Сегодня всё прогрессивное человечество понимает, что нельзя продолжать эксплуатировать традиционные источники энергии бесконечно: сжигание ископаемого топлива небезопасно для окружающей среды, и его запасы не вечны; мирный атом не такой уж мирный и может привести к природной и гуманитарной катастрофе; а ради постройки ГЭС необходимо затапливать огромные площади обжитых и зачастую плодородных земель. Но все также понимают, что полноценной замены им в настоящее время нет. Методы получения «зеленой» энергии слишком дорогие и имеют массу ограничений, которые лучшие умы планеты стараются снять как можно скорее, пока ещё не стало слишком поздно.
Одним из стремительно развивающихся направлений альтернативной энергетики является фотовольтаика. В 2012 изготовители солнечных батарей выпустили продукции на 68 потенциальных гигаватт [1]; в то же время спрос на солнечные панели отстаёт от предложения рынка прежде всего по причине высокой стоимости оборудования [2]. Сегодня массово используются разве что твердотельные кремниевые солнечные панели. Они просты в изготовлении, долговечны, безопасны и, что самое главное, — имеют КПД до 20% [3], что выше, чем у других типов панелей. Несмотря на дороговизну подобных систем, современный потребитель выбирает именно их, предпочитая бóльшую эффективность за бóльшую цену. В результате исторически сложившейся монополии на рынке фотоэлементов, интерес к альтернативным технологиям пока невелик.
Как же будет выглядеть будущее солнечной энергетики? Какой может быть та революционная технология, что даст толчок к повсеместному применению солнечных батарей? Возможно, такой технологией являются биофотоэлементы.
Фотосинтез вдохновляет
Но, прежде чем рассказывать о биофотоэлементах, автор статьи считает необходимым просветить читателя относительно принципов работы одного из видов солнечных батарей. Создатели батарей на основе красителей (Dye Synthesized Solar Cells, DSSC) черпали вдохновение в явлении фотосинтеза [4], при котором пигмент хлорофилл в растениях улавливает и передаёт электронам энергию света.
На рисунке 1 приведена схема работы ячейки DSSC. Свет улавливается красителем на основе рутения, который передаёт его энергию электрону полупроводника, в данном случае — TiO2. Получив энергию, электрон выталкивается из полупроводника, словно после мощного пинка. Пройдя по цепи, электрон совершает работу и попадает в катализаторный слой, который обеспечивает его переход в электролит. Электролит содержит трииодид-анионы. При поступлении электрона трииодид превращаются в иодид. Иодид передаёт электрон TiO2 и возвращается в исходную форму. Цикл замкнулся.
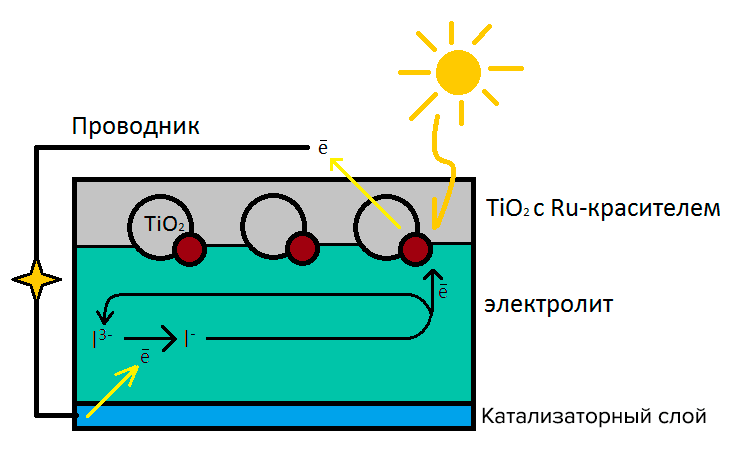
Рисунок 1. Схема ячейки DSSC (солнечной панели на основе красителя)
Ещё в 1970-х с пониманием процессов фотосинтеза стало понятно, что органические красители (в частности, природные) могут служить основой для нового источника электроэнергии [5]. Но вплоть до 1990-х годов никак не удавалось собрать более-менее эффективные системы типа DSSC. Сейчас часто наряду с термином DSSC применяется словосочетание «ячейка Гретцеля» по фамилии Швейцарского учёного Михаэля Гретцеля (1944 г.р.; на заглавной картинке), который смог довести до ума старую идею и получить жизнеспособную технологию. Сейчас он один из самых цитируемых химиков в мире, обладатель целого ряда естественнонаучных наград высокого уровня и автор настоящего рекорда по КПД DSSC-ячейки — 15% [6].
У данной технологии есть важные преимущества: лёгкость конструкции, способность работать при низком освещении, малый перегрев при работе (за счёт малой массы), достаточно высокий КПД. Что же мешает DSSC занять место кремниевых батарей? Во-первых, токсичность электролита. Во-вторых, дороговизна красителей и слоя катализатора, в состав которого входит платина. В-третьих, присутствие жидкого электролита накладывает ограничение на применение вне помещений. В-четвёртых, со временем краситель разлагается, и КПД падает, что плохо сказывается на сроке окупаемости установки.
Подводя итог, основная проблема DSSC — дороговизна и ненадёжность компонентов. Но не всё так мрачно: на сегодняшний день уже найдено множество решений, способных увеличить производительность DSSC. Например, в июле 2013 года в журнале Nature была опубликована статья, в которой предлагается относительно дешёвый свинцовый краситель [7].
Большие надежды
Фотосинтез в растениях и большинстве бактерий имеет много общего с технологией DSSC: пигмент улавливает энергию света и передаёт её электронам, которые при прохождении длинной цепочки окислений и восстановлений ряда веществ совершает работу по образованию энергоёмких химических связей.
Конечно, фотосинтез нельзя воспроизвести целиком: живые системы слишком сложны. К тому же при фотосинтезе происходит обмен не только энергией, но и веществом, что неуместно, если цель — просто получить электричество. Тем не менее, ничто не мешает позаимствовать лишь необходимые для решения поставленной задачи элементы фотосинтеза.
Фотосистема I (ФС-I) — комплекс мембранных белков и пигментов, лежащий в основе фотосинтеза. Хлорофилл здесь выступает аналогом рутениевого красителя из DSSC. По расчетам, КПД ФС-I в живых организмах составляет около 23% [8]. Весьма многообещающе. Но, помимо высокой эффективности, у ФС-I есть ряд не менее значимых преимуществ. Например, её легко добывать: в лабораторных условиях ФС-I получают центрифугированием лизата бактерий Thermosynechoccus elongates в градиентном сахарозном растворе. По заявлениям учёных, при массовом производстве фотосистему можно будет получать из высших растений при помощи ультрафильтрации через мембрану — недорогой процедуры. Широкая доступность сырья (листовой опад, отходы земледелия или даже выполотые на грядке сорняки) в комбинации с простотой выделения обеспечивают сверхнизкую стоимость конечного продукта.
Что также немаловажно, все материалы в биофотобатареях абсолютно безопасны. Это требование технологии: для нормальной работы ФС-I условия в батарее должны быть максимально приближены к тем, что наблюдаются в живых организмах. Таким образом, биофотобатереи биологически дружественны по определению. Помимо прочего, можно отметить лёгкость сборки, которая позволяет перенести этот этап производства прямо на место эксплуатации. То есть, имеется возможность транспортировать вместо собранных батарей их компоненты, что упрощает транспортировку.
От фотофизики к биоинженерии
Потенциал у биофотоэлементной технологии действительно велик, но раскрыть его совсем не просто. Несмотря на то, что фотосинтез активно изучается с середины прошлого века, до сих пор не было создано прототипа фотобатареи на основе природных пигментов, представляющего практический интерес . Есть несколько основных препятствий на пути биофотоэлементов, которые ещё предстоит преодолеть.
Впрочем, биотехнологии открывают перспективы не сколько для получения электроэнергии, сколько для других целей: например, для синтеза водорода, являющегося экологически чистым топливом: «Бактерии для водородной энергетики» [11]. — Ред.
Одно из них — иммобилизация ФС-I. В живом листе фотосистема I расположена в липидной мембране, которая одновременно фиксируют ФС-I и выступает в качестве «изоляции» во избежание коротких замыканий. В искусственных системах мембрану удаётся имитировать при помощи матрицы на основе пептида А6К (шесть аланинов, один лизин) или схожих веществ, с которыми ФС-I соединяется за счёт гидрофобного взаимодействия (гидрофобные части белкового комплекса буквально слипаются с гидорофобными аланинами) . Испытания показали, что применение этого соединения увеличивает напряжение холостого хода в три раза [9].
О физической природе гидрофобного эффекта мы рассказывали в статье «Физическая водобоязнь» [12]. — Ред.
Ещё один способ улучшить характеристики батареи — увеличение поглощающей поверхности, и тут на помощь приходят наноматериалы. Например, нанесение иммобилизованной ФС-I на наностержни из ZnO увеличивают поверхность батареи в 30 раз, а на губчатый TiO2 — в 300 раз (рис. 2) [10]! Чтобы разместить ФС-I на TiO2-подложке, не нужно никаких дополнительных манипуляций: достаточно подобрать достаточно большой размер пор, чтобы в них могла помещаться ФС-I, окружённая стабилизирующими пептидами, и дело будет сделано.

Рисунок 2. Поверхность губчатого TiO2 и наностерженей из ZnO, соответственно
При размещении фотосистемы на ZnO-стержнях один из белков ФС-I необходимо модифицировать для более плотного прилегания к субстрату (рис. 3). В ген, кодирующий белок PsaE, вводят мутацию, обеспечивающую повышенное сродство к ZnO. Потом этот ген «подселяют» в бактерии, которые в процессе жизнедеятельности вырабатывают мутантный белок PsaE—ZnO. После разрушения бактерий остаётся только отфильтровать нужный белок и слить его избыток с ещё не иммобилизованной ФС-I для обеспечения обмена PsaE на PsaE—ZnO.
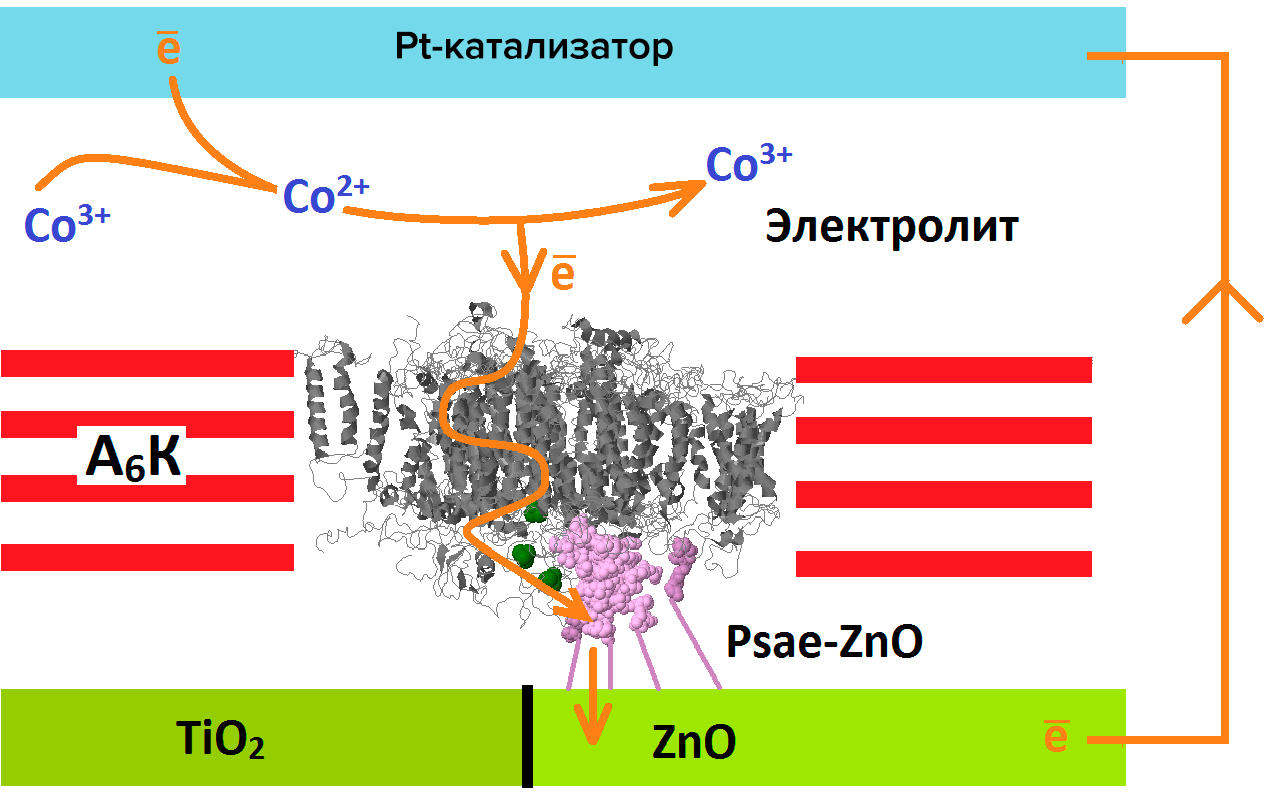
Рисунок 3. Элементарная ячейка биофотобатареи: одна молекула ФС-I иммобилизована на полупроводниковой подложке — либо ZnO, либо TiO2. В первом случае необходимо внесение модификации в ФС-I (см. текст). Как видно, общая схема очень похожа на DSSC.
Зелёный век совсем (не)далеко
Какой же эффект дают все эти манипуляции? К сожалению, довольно скромный: КПД лучшего лабораторного образца составляет пока лишь 0,08%, и с 2012 года рекорд не был побит. До теоретического максимума технологии ещё очень и очень далеко. Зато этот образец был испытан в условиях, максимально приближённых к реальности, а не под лучом мощного монохроматического лазера, как в прочих исследованиях на данную тему.
Есть ли у этой технологии какие-либо перспективы, сказать сложно. С одной стороны, гораздо проще совершенствовать хорошо зарекомендовавшие себя технологии, чем повысить КПД биофотоэлементов хотя бы в пять раз (по словам Андреаса Мершина, одного из ведущих специалистов в области биофотовольтаики, при достижении производительности в 1% целесообразно массовое производство таких батарей [13]).
К тому же проведённые исследования оставляют простор для оптимизации: можно ещё увеличить поглощающую поверхность, улучшить стабилизирующие агенты, подобрать оптимальные электролит и электроды. Нельзя забывать, что в клетках фотосинтезирующие единицы располагаются не в один слой, и их расположение может меняться в зависимости от угла и интенсивности освещения. То есть, мощным скачком может стать переход к многослойному нанесению ФС-I с элементами ориентации. Никто также не исключает, что в будущем более глубокое понимание процессов фотосинтеза позволит легко провести необходимые модификации.
В любом случае, остаётся только надеяться, что в скором времени мы услышим новости о прорыве в сфере зелёных технологий. Возможно, появление биофотобатерей ознаменует новую эру для человечества: не возврат к истокам, но воссоединение с природой на новом уровне.
Литература
- Shahan Z. (2013). Solar module manufacturing trends in 2012. CleanTechnica;
- Wang U. (2012). Report: solar panel supply will far exceed demand beyond 2012. Forbes;
- Sunpower E19/240 SOLAR PANEL;
- Волонтер фотосинтеза;
- HELMUT TRIBUTSCH. (2008). REACTION OF EXCITED CHLOROPHYLL MOLECULES AT ELECTRODES AND IN PHOTOSYNTHESIS*. Photochemistry and Photobiology. 16, 261-269;
- Papageorgiou N. (2013). Dye-sensitized solar cells rival conventional cell efficiency. EPFL;
- Julian Burschka, Norman Pellet, Soo-Jin Moon, Robin Humphry-Baker, Peng Gao, et. al.. (2013). Sequential deposition as a route to high-performance perovskite-sensitized solar cells. Nature. 499, 316-319;
- Itai Carmeli, Ludmila Frolov, Chanoch Carmeli, Shachar Richter. (2007). Photovoltaic Activity of Photosystem I-Based Self-Assembled Monolayer. J. Am. Chem. Soc.. 129, 12352-12353;
- Rupa Das, Patrick J. Kiley, Michael Segal, Julie Norville, A. Amy Yu, et. al.. (2004). Integration of Photosynthetic Protein Molecular Complexes in Solid-State Electronic Devices. Nano Lett.. 4, 1079-1083;
- Andreas Mershin, Kazuya Matsumoto, Liselotte Kaiser, Daoyong Yu, Michael Vaughn, et. al.. (2012). Self-assembled photosystem-I biophotovoltaics on nanostructured TiO2 and ZnO. Sci Rep. 2;
- Бактерии для водородной энергетики;
- Физическая водобоязнь;
- Fellet M. (2012). Plant proteins power solar panel. KQED Science.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





