
Экзосомы — маленькие машины времени внутри нас
26 марта 2026
Экзосомы — маленькие машины времени внутри нас
- 249
- 0
- 2
Стволовая клетка производит экзосомы, омолаживающие старую клетку.
Рисунок в полном размере.
сгенерировано с помощью нейросети Sora
-
Авторы
-
Редакторы
Статья на конкурс «Био/Мол/Текст»: Издавна люди стремились к сохранению здоровья, красоты и молодости, задумывались о поиске чудодейственных средств — волшебных пилюль и эликсиров молодости. До недавнего времени все это казалось лишь сказкой. Но наука не стоит на месте. Развивая представления о природе, окружающей и нашей собственной, маленьких помощниках, скрытых в нас самих, мы сделали выдающийся шаг — по-новому открыли внеклеточные везикулы, повысив их «из грязи», ненужных клеточных отходов, — «в князи», наиважнейшие регуляторы в нашем организме. Все многообразие предназначений и важность везикул ученым еще предстоит понять, а мы в данной статье расскажем об их влиянии на биологические процессы в нашем организме и применении в омоложении и регенеративной медицине.
Конкурс «Био/Мол/Текст»-2025/2026
Эта работа опубликована в номинации «Свободная тема» конкурса «Био/Мол/Текст»-2025/2026.

Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.

Партнер номинации — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.

«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Универсальный механизм коммуникации между клетками
Продукция внеклеточных везикул (ВВ) и, в частности, экзосом, является фундаментальной способностью живых клеток различных царств жизни: животных, растений, грибов и даже бактерий [1–3]. При этом интересно, что молекулярные механизмы, лежащие в основе формирования экзосом, эволюционно консервативны, похожи и восходят истоками к самому зарождению жизни. Согласно одной из гипотез, в древнейшие времена «мира РНК» в первичном бульоне из различных биомолекул спонтанно (подобно пузырям в ванной) образовывались пузырьки с билипидной мембраной, протоклетки, похожие на их потомков — современные ВВ. В дальнейшем, подвергаясь суровым условиям ранней Земли, эти пузырьки эволюционировали и стали настоящими клетками, которые сохранили суперспособность производить ВВ [1].
ВВ обнаруживаются во многих биологических жидкостях животных: крови, лимфе, молоке и так далее. Клетки растений также производят экзосомы, которые могут быть обнаружены и выделены из сока, мякоти и корней растений [4].
Структурно растительные и животные везикулы во многом похожи — они представляют собой шарообразные структуры из двух липидных оболочек с различными биологическими молекулами внутри. Содержимое ВВ внутри одного организма может отличаться и зачастую отражает свойства и состояние родительских клеток, которые их произвели, но среди основных компонентов можно выделить сигнальные белки, липиды, ДНК и различные виды РНК [5].
Механизмы образования и функции растительных и животных ВВ отличаются. У растений ВВ формируются тремя основными путями: (1) через мультивезикулярные тельца (МВТ), внутри которых будущие везикулы образуются и затем выбрасываются наружу при слиянии МВТ с клеточной оболочкой, (2) напрямую захватывая и выделяя клеточное содержимое во внеклеточное пространство (механизм EXPO — через экзоцист-положительные органеллы, уникальные для растений) и (3) в стрессовых ситуациях к процессу может подключиться вакуоль, сливаясь либо с МВТ, либо напрямую с плазматической мембраной (рис. 1) [6]. Для непосредственного отпочковывания ВВ растения используют похожую машинерию, как у животных [4].
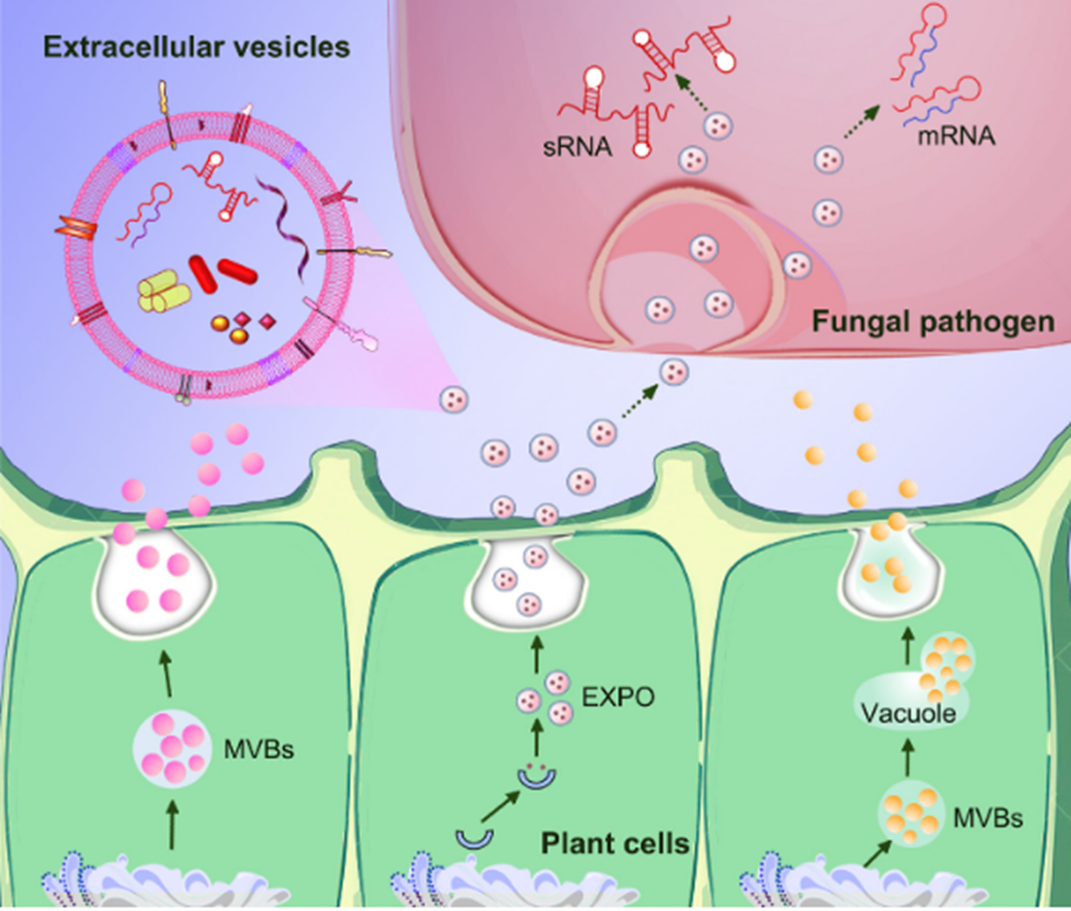
Рисунок 1. Механизмы образования внеклеточных везикул у растений: через мультивезикулярные тельца (MVB), механизм EXPO и задействуя вакуоли. Выделяемые везикулы содержат различные молекулы и могут быть доставлены в клетки патогенов.
адаптировано из [6]
Для животных характерно образование ВВ прямым отпочковыванием от мембраны (так образуются микровезикулы) или через МВТ. Вторым способом образуются экзосомы, разновидность внеклеточных везикул, и именно о них мы поговорим в данной статье. Подробнее о механизмах формирования везикул можно прочитать в статье «Экзосома — механизм координации и взаимопомощи клеток организма» [7].
Для многоклеточных организмов ВВ выступают в качестве маленьких «почтальонов» для обмена «сообщениями» между клетками. В зависимости от «текста сообщения» ответ может быть совершенно разным. Кроме того, некоторые сообщения могут доставляться другим организмам — например, для защиты растений от грибов и бактерий или для симбиотических (дружественных) отношений с некоторыми из них [7–9]. А как много везикул производится в нашем организме? На какие биологические процессы они могут влиять?
Роль экзосом: от эволюционной «оптимизации» до управления процессами в организме
Экзосомы — это не клеточные «отходы» или пассивно выделяемые пузырьки. Их стоит представлять себе как точные коммуникационные снаряды, для производства которых клетка тратит значительные ресурсы. В обычных условиях, когда нет необходимости в массовом обмене сигналами, такая расточительность биологически невыгодна. Более того, неконтролируемая и массовая секреция экзосом нарушила бы тонкий баланс межклеточных взаимодействий, создав информационный «шум» и потенциально спровоцировав нежелательные реакции (например, аутоиммунный ответ). Поэтому в норме базальный уровень их секреции достаточно низок [10], [11].
Однако в определенных ситуациях это правило перестает действовать. Клетки резко увеличивают производство экзосом, чтобы активно влиять на свое окружение. Раковые клетки — настоящие чемпионы по производству экзосом. Они «перепрограммируют» этот механизм в своих интересах, создавая «фабрики экзосом» для дальнейшего развития опухоли. Экзосомы могут подавлять иммунный ответ, стимулировать рост сосудов и готовить «почву» для метастазов [12], [13]. Но не только опухоли заставляют клетки активно общаться. Такие состояния, как гипоксия (нехватка кислорода), окислительный стресс или повреждение ДНК, заставляют клетку рассылать «сигналы тревоги», призывая соседей к помощи или адаптации. Иммунные клетки, в свою очередь, используют экзосомы для координации атаки и регуляции воспаления [10].
Таким образом, низкая базальная продукция экзосом — это не недостаток, а проявление эволюционной оптимизации, обеспечивающее точную и экономную коммуникацию без перегрузки системы [11]. Тем не менее, для терапевтических целей это ограничение можно обойти: культивирование клеток-продуцентов в биореакторах в условиях контролируемого стресса (например, гипоксии) вынуждает их активно производить нужные везикулы [14].
Биологические эффекты экзосом охватывают регуляцию множества процессов в нашем организме. Во-первых, экзосомы способны модулировать синтез компонентов внеклеточного матрикса. Они осуществляют прямое воздействие на миофибробласты — основные клетки, ответственные за фиброз, — доставляя в эти клетки микроРНК. Это приводит к «выключению» генов, ответственных за избыточный синтез коллагена, эластина и фибронектина, что одновременно подавляет пролиферацию и стимулирует запрограммированную гибель этих активированных миофибробластов [15]. В то же время, экзосомы способны повышать синтез компонентов внеклеточного матрикса, стимулируя его физиологическое обновление и «омолаживая» [16].
Во-вторых, экзосомы модулируют иммунный ответ и воспаление. Экзосомы действуют как дипломаты иммунной системы: они могут способствовать переходу макрофагов из провоспалительного (M1) в противовоспалительный и репаративный (M2) фенотип, подавляя выброс провоспалительных сигналов (цитокинов TNF-α, IL-1β и других) [17], [18].
В-третьих, экзосомы стимулируют здоровую регенерацию, активируя резидентные стволовые клетки и подавляя апоптоз функциональных паренхиматозных клеток (гепатоцитов в печени, кардиомиоцитов в сердце, эпителиальных клеток в почках), тем самым сохраняя функциональную ткань. Это ключевой момент: восстановление идет не через заполнение «пустоты» рубцом, а через сохранение и активацию собственных клеток органа. Таким образом, экзосомы не просто блокируют синтез коллагена, а перепрограммируют всю клеточную среду поврежденной ткани, переводя ее из состояния деструктивного фиброзирования в состояние конструктивного восстановления [19].
В-четвертых, экзосомы способны стимулировать образование новых кровеносных сосудов за счет доставки факторов роста (например, фактора роста сосудистого эндотелия, или VEGF) и специфических сигнальных молекул, таких как микроРНК. Эта способность играет двоякую роль: она критически важна для восстановления тканей, но также используется опухолями для своего роста [17].
Все эти функции делают экзосомы центральным элементом клеточного диалога, где экзосомы играют роль и слов, и самих гонцов. От точности этого диалога напрямую зависит здоровье тканей. Но что, если с возрастом гонцы начинают доставлять искаженные послания или их попросту становится слишком мало? Ответ на этот вопрос приближает нас к пониманию глубинных механизмов старения, когда нарушение экзосомальной коммуникации ведет к накоплению ошибок, хроническому воспалению и уменьшению способности к восстановлению.
Молекулярные механизмы старения
Когда мы стареем, это легко заметить внешне. Ученые не один десяток лет бьются над решением проблемы замедления старения, увеличения длительности жизни и поддержания «презентабельного вида» человека как можно дольше. А как происходит старение на молекулярном уровне?
Клеточное старение влияет на многие жизненные процессы (рис. 2). Подробно это обсуждается в статье «Зачем клетки стареют» [20]. Во-первых, клетка теряет способность правильно делиться. На концах хромосом находятся теломеры — защитные «колпачки», которые укорачиваются с каждым делением. Достигнув критической длины, они больше не могут защищать ДНК, что ведет к нестабильности генома и делает новые клетки дефектными. Это состояние называется сенесценцией. Такие «состарившиеся» клетки не погибают, а остаются метаболически активными и начинают пагубно влиять на окружение, выделяя особый комплекс сигнальных молекул [20–22].
Параллельно в клетке накапливаются повреждения: нарушается работа митохондрий, что усиливает окислительный стресс, повреждается ДНК, а механизмы ее починки работают все хуже. Нарушается и контроль качества белков, что приводит к накоплению вредных агрегатов. Эпигенетические «настройки» клетки, такие как метилирование ДНК и модификации гистонов, также сбиваются, что «включает» гены старения и «выключает» гены, необходимые для нормальной жизни и регенерации. В совокупности это приводит к прогрессирующей утрате функций тканей и органов и старению [20], [22].
Старение меняет и «клеточную почту» — экзосомы. Сигнальный профиль, который клетки рассылают непосредственно и через везикулы, радикально меняется, приобретая так называемый секреторный фенотип, ассоциированный со старением (SASP). В нем резко возрастает доля провоспалительных молекул (интерлейкинов, хемокинов), которые распространяют «сигналы старения» по организму [21], [23].
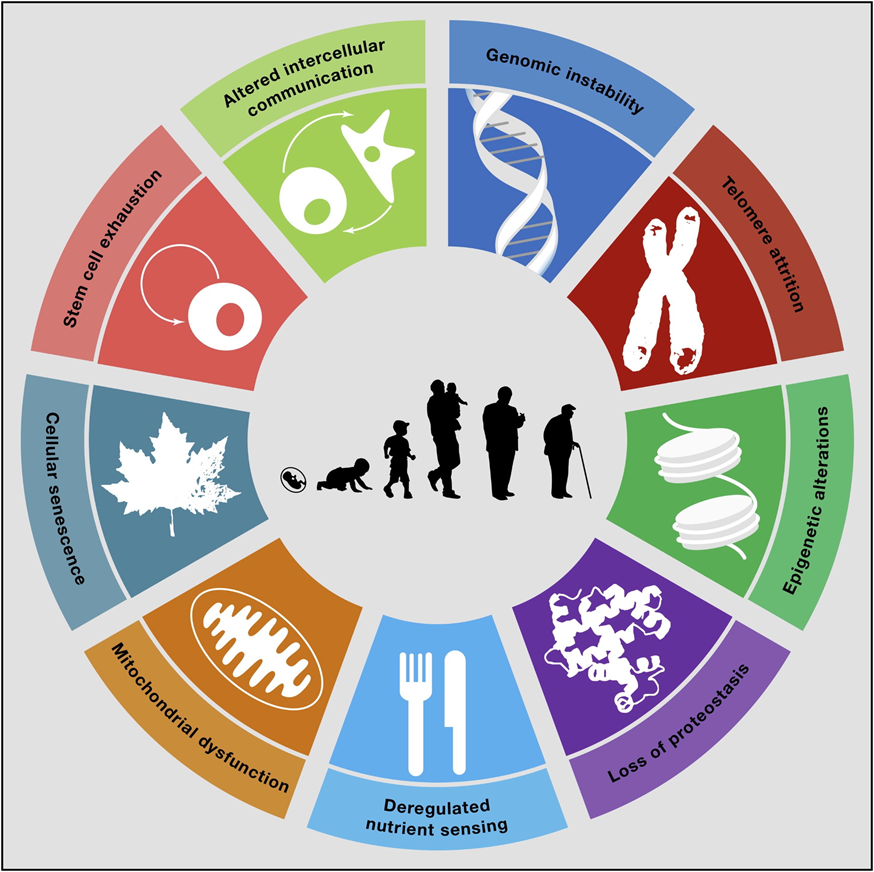
Рисунок 2. Ключевые признаки старения организма: нестабильность генома, укорочение теломер, эпигенетические изменения, потеря стабильности белков, нарушение чувствительности к нутриентам, дисфункция митохондрий, клеточное старение, старение стволовых клеток и нарушение межклеточной коммуникации.
Меняется и содержание ключевых регуляторов — микроРНК в экзосомах. Например, в экзосомах плазмы крови с возрастом снижается уровень регенеративных miRNA и повышается уровень провоспалительных [24].
Итак, старение «портит» клетки и «почту» нашего организма: производится меньше экзосом, а жизненно важные экзосомальные послания искажаются и начинают вредить. Но как обратить этот процесс и омолодить организм?
Молекулярные механизмы омоложения
На сегодняшний день не существует «магической таблетки» для полного обращения старения вспять. Однако стволовые клетки и, что еще важнее, их экзосомы представляют собой мощный инструмент для воздействия на отдельные биомаркеры этого процесса. Речь идет о достижении состояния, которое по ряду ключевых параметров может соответствовать организму на несколько лет моложе хронологического возраста.
Исторически фокус регенеративной медицины был направлен на МСК (мезенхимальные стволовые клетки). Многие исследования подтверждают, что пересадка стволовых клеток приводит к регенерации тканей. Однако клиническое применение живых стволовых клеток сопряжено с ограничениями: возможность неправильной дифференцировки, низкая выживаемость после трансплантации и, в редких случаях, образование опухолей [25].
Экзосомы предлагают принципиально иной подход — «одноразовый сигнал». Они доставляют свой молекулярный груз в клетку-мишень, меняя ее поведение на несколько часов или дней, после чего разрушаются. Так как экзосома — это не живая клетка, а лишь посылка с инструкциями, риски, присущие клеточной терапии, сведены к минимуму. Многочисленные исследования на животных подтверждают потенциал этого подхода: введение экзосом от молодых особей приводило к улучшению функций органов, метаболизма и даже увеличению продолжительности жизни старых животных [26–28].
Источник экзосом имеет значение. Наибольший регенеративный потенциал, судя по всему, несут экзосомы, полученные из самых молодых клеток организма — эмбриональных, или фетальных. МСК пупочного канатика и плаценты считаются чрезвычайно перспективным источником, так как это биологически молодые, активные клетки. С возрастом клетки-продуценты и их экзосомы теряют регенеративную активность и начинают, напротив, распространять провоспалительные сигналы. МСК костного мозга считаются классическим источником, но забор материала инвазивен, а потенциал клеток к пролиферации и дифференцировке ниже, чем из пупочного канатика. МСК жировой ткани легкодоступны, но их потенциал, так же как и у клеток костного мозга, может зависеть от возраста и состояния донора [29], [30].
В этом контексте привлекательной идеей представляется омоложение самих клеток-продуцентов экзосом. Эпигенетическое репрограммирование, например, с помощью временной активации факторов Яманаки (Oct4, Sox2, Klf4, c-Myc), позволяет «стереть» возрастные метки с ДНК клетки. Это «перезагружает» эпигенетические часы: у клеток восстанавливается длина теломер, улучшается функция митохондрий, репарируются повреждения ДНК, снижается уровень воспалительной секреции (рис. 3а). Таким образом, взрослые дифференцированные клетки возвращаются в эмбрионально-подобное состояние. Современные подходы частичного репрограммирования с помощью факторов Яманаки и культивирования их в условиях, имитирующих молодую среду (гипоксия, специфические факторы роста), позволяют добиться этого омоложения, сохраняя клеточную идентичность и избегая риска онкогенеза — улучшить состояние органов и вернуть регенеративный потенциал тканей, например, для старых мышей и с синдромом преждевременного старения (рис. 3б—в) [31], [32].
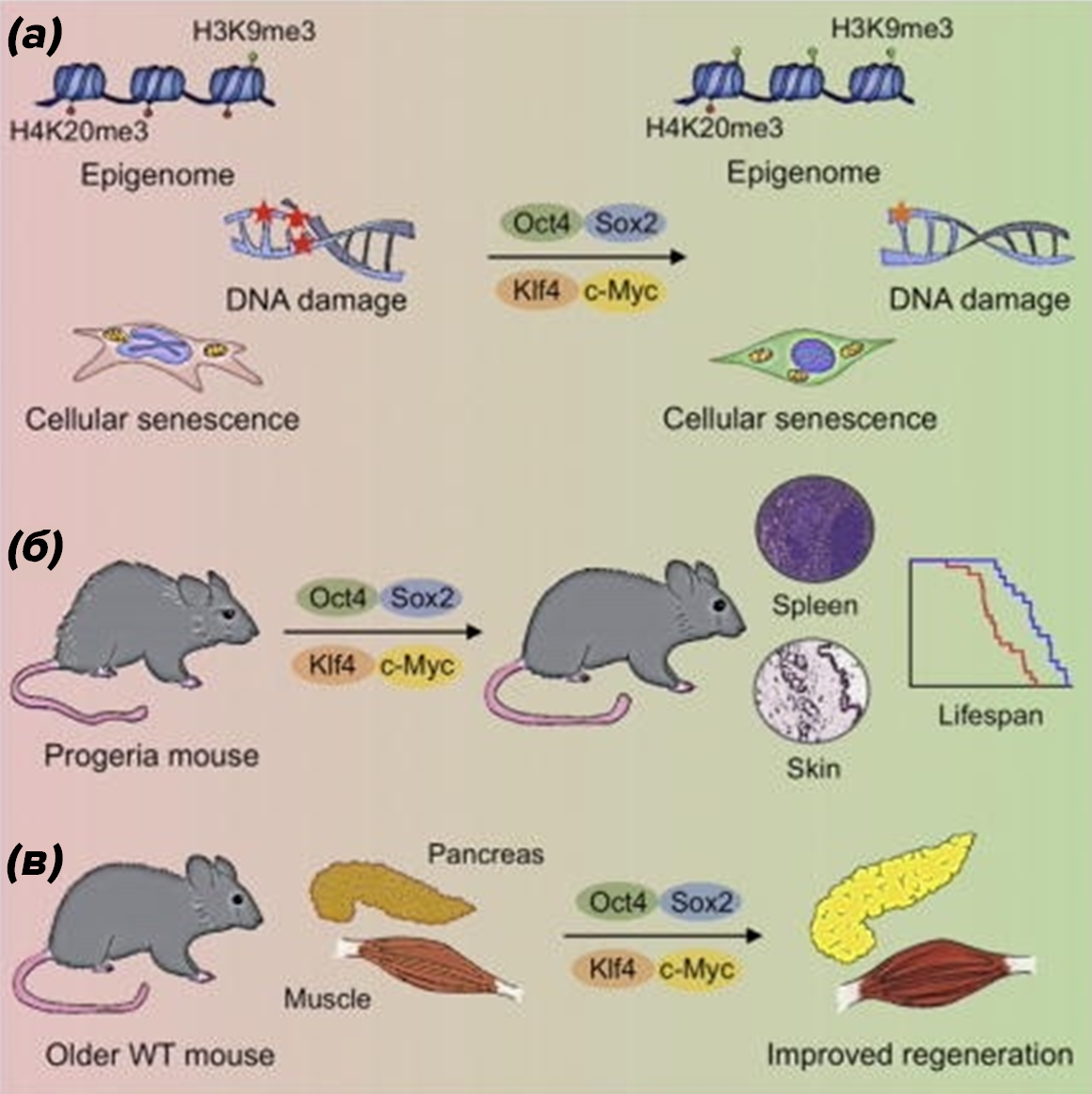
Рисунок 3. Факторы Яманаки и их омолаживающие эффекты: (а) — модификация эпигенома посредством изменения эпигенетических меток, в частности, метилирования гистонов; репарация повреждений ДНК, клеток из состояния сенесценции; (б) — улучшение состояния здоровья и омоложение мыши с синдромом преждевременного старения; (в) — улучшение регенерации тканей старой мыши дикого типа.
Экзосомы, полученные от эпигенетически перепрограммированных, молодых клеток будут нести в себе более мощный регенеративный сигнал, которые можно использовать как точный инструмент для локальной «перезагрузки» клеток. Но их природная форма — лишь первое поколение этого инструмента. Что, если мы сможем не просто использовать готовые экзосомы, а конструировать их с нуля и нагружать необходимым грузом, усиливая мощность и продлевая действие? Это уже не фантастика, а реальность инжиниринга, который превращает экзосомы в совершенное оружие против старения.
Инжиниринг экзосом
На данный момент существуют два подхода к загрузке экзосом терапевтическими молекулами (белками, нуклеиновыми кислотами, лекарствами): натуральный и искусственный. Проще говоря, можно либо запрограммировать клетку-производитель на создание «посылки» с нужным содержимым, либо вручную загрузить терапевтический груз в уже готовые, очищенные экзосомы [33].
Естественная загрузка использует встроенные клеточные механизмы. Клетки обладают сложной системой упаковки молекул в экзосомы, которая регулируется модификациями мембранных белков и перестройки липидного слоя клетки. Ученые могут «вмешаться» в этот процесс: например, генетически запрограммировать клетку на синтез нужной матричной РНК (мРНК) или микроРНК, которая затем автоматически упакуется в формирующиеся везикулы. Другой вариант — культивировать клетки в среде, насыщенной определенным лекарственным препаратом, который они поглотят и включат в состав экзосом [33].
Искусственная загрузка работает с уже готовыми, выделенными экзосомами. Этот подход проще контролировать и масштабировать для производства, что является его ключевым практическим преимуществом. Для загрузки используются различные физико-химические методы [31],[34].
- Одним из наиболее распространенных и эффективных методов является электропорация, при которой экзосомы подвергаются кратковременным импульсам электрического поля, что приводит к временному образованию пор в их мембране. Через них под действием диффузии внутрь проникают лекарства и нуклеиновые кислоты (ДНК и различные виды РНК). После этого мембрана быстро восстанавливает свою целостность, задерживая терапевтические молекулы внутри [35].
- При соникации смесь из подготовленных экзосом и лекарств обрабатывается ультразвуком. В результате создаются кавитационные пузырьки, которые нарушают целостность мембраны, что также позволяет лекарствам попасть внутрь. После этого смесь инкубируется для «заживления» мембраны экзосом. Но этот метод требует жесткого контроля во избежание необратимого повреждения экзосом [36].
- Другой достаточно простой в реализации метод — многократные циклы заморозки и оттаивания экзосом. Этот процесс вызывает повторяющееся временное разрушение и восстановление мембраны, что позволяет молекулам из окружающей среды проникать внутрь [37].
- Физическое продавливание (экструзия) смеси экзосом и лекарства через мембрану с порами нанометрового размера приводит к разрушению мембраны и повторному образованию везикул, иногда меньше изначальных, с терапевтическими молекулами внутри [36].
- Одним из наиболее эффективных методов является трансфекция с использованием различных агентов. В этом процессе амфифильные молекулы трансфецирующих агентов окружают нуклеиновые кислоты или лекарство, образуя сферические частицы (липосомы). Такие частицы эффективно сливаются с мембраной экзосом, доставляя нужное вещество внутрь [37].
- Перспективным направлением является создание химерных экзосом — гибридов с липосомами, которые похожи на везикулы, но создаются искусственно и могут содержать более одного липидного бислоя. Теоретически, такой подход может повысить емкость и стабильность носителей, однако он требует тщательного изучения на предмет потенциального повышения токсичности и иммуногенности [37].
На самом деле, методов загрузки экзосом намного больше, у каждого есть свои преимущества и недостатки, мы рассмотрели лишь некоторые наиболее распространенные (рис. 4). Выбор метода зависит от свойств загружаемого вещества (размера, заряда и гидрофобности). Критически важно сохранение целостности экзосом и биологической активности вводимого терапевтического агента. Многообразие методов оставляет большое поле для творчества исследователей и изобретателей.
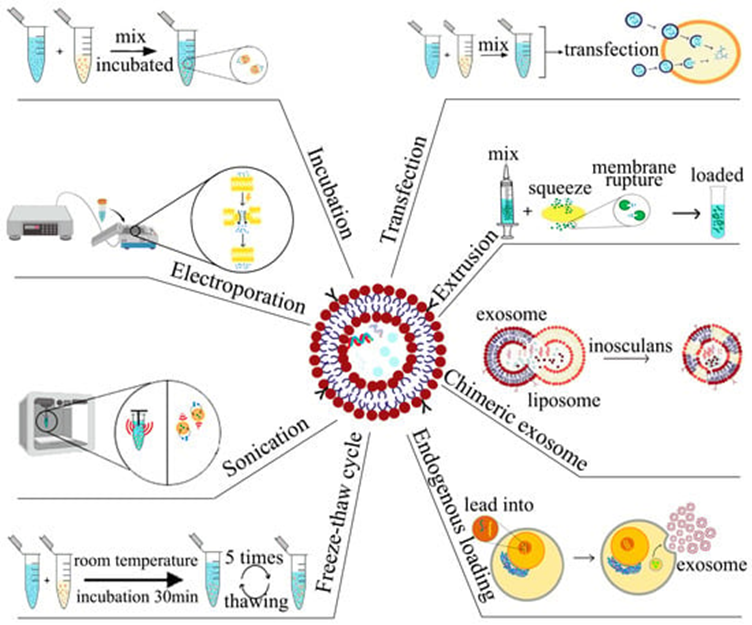
Рисунок 4. Стратегии для загрузки экзосом лекарствами: инкубация, электропорация, соникация, заморозка-разморозка, трансфекция, экструзия, химерный метод и эндогенная загрузка.
адаптировано из [37]
Итак, инжиниринг и использование методов загрузки терапевтических молекул позволяет превратить их в универсальную платформу для доставки лекарств и омоложения организма. Но стоит ли отказываться от использования стволовых клеток? И все ли так гладко в использовании экзосом?
Ограничения использования в терапии
МСК способны стабильно выделять в окружающую среду факторы «омоложения», в том время как однократное введение экзосом зачастую подразумевает временный эффект. Клеточная терапия теоретически может дать более долгий эффект, если клетки приживутся и будут работать, в том числе, производя экзосомы. Однако у клеточной терапии есть свои риски: имплантируемые клетки преимущественно погибают и, что более опасно, могут вызвать нежелательный иммунный ответ, неправильную дифференцировку и образование опухоли [25].
Схожие риски, хоть и в меньшей степени, присущи и экзосомам. Поскольку содержимое везикул соотносится с составом клеток-производителей, экзосомы, полученные от МСК пациентов с недиагностированными микроопухолями, могут за счет факторов роста вынудить клетки неправильно дифференцироваться и потенциально привести к появлению опухолей у пациента, который хотел омолодиться… Поэтому крайне важен тщательный отбор доноров и скрининг пациентов. В дополнение, многократное системное введение экзосом может, так же как и МСК, вызывать иммунные реакции и потенциально развитие аутоиммунного процесса [38], [39].
Помимо вопросов безопасности, от исходного биологического материала зависит и эффективность готового препарата, что создает три ключевые проблемы на этапе производства.
Во-первых, критическую роль играет возраст донора. Клетки-продуценты, полученные от пожилого донора, сами обладают сниженным регенеративным потенциалом и демонстрируют так называемый сенесцентный фенотип, который мы обсудили ранее, не способствующий омоложению [40].
Во-вторых, даже при отборе молодых доноров мы сталкиваемся с проблемой индивидуальных вариаций. Регенеративные способности и состав экзосом стволовых клеток отличаются для различных типов тканей и уникальны для каждого человека. Это означает, что клетки одного здорового донора могут продуцировать исключительно мощные экзосомы, в то время как клетки другого — давать значительно более слабый эффект, что приводит к непредсказуемому и нестабильному качеству конечного продукта [41].
В-третьих, фундаментальным биологическим ограничением является низкая естественная секреторная активность клеток. Подавляющее большинство здоровых несекреторных клеток в принципе не приспособлено для массового производства экзосом. Они выделяют их в очень небольших количествах, которых недостаточно для создания стандартизированного и эффективного терапевтического препарата в промышленных масштабах. Это приводит к необходимости «вынуждать» клетки продуцировать экзосомы в условиях контролируемого стресса [10], [14].
Таким образом, эти три фактора — возраст донора, индивидуальные особенности и низкий базовый уровень продукции — формируют серьезный вызов для создания высокоэффективных и стандартизированных экзосомных продуктов. Поэтому предполагается, что для большинства применений, не требующих замены крупных дефектов и участков утраченных тканей, экзосомы смогут эффективно заменить терапию стволовыми клетками, в то время как стволовые клетки будут незаменимы для процессов создания новой ткани (например, в тканевой инженерии) [25].
Проблема футбольных мяча и ворот
Однако даже идеально произведенный препарат сталкивается с другой фундаментальной проблемой — доставкой. Можно представить механизм действия экзосом как игру в футбол: чтобы запустить изменения в клетке-мишени, экзосома, словно мяч, должна точно попасть в «ворота» — специальные рецепторы на ее поверхности и внутриклеточные биохимические пути, за счет узнавания белка-лиганда в мембране экзосом [36].
Однако даже идеально произведенный препарат сталкивается с другой фундаментальной проблемой — доставкой. Можно представить механизм действия экзосом как игру в футбол: чтобы запустить изменения в клетке-мишени, экзосома, словно мяч, должна точно попасть в «ворота» — специальные рецепторы на ее поверхности и внутриклеточные биохимические пути, за счет узнавания белка-лиганда в мембране экзосом [42].
Старение можно сравнить с тем, что наш собственный «мяч» изнашивается и теряет эффективность за счет изменения состава экзосом — приобретения сенесцентного фенотипа (SASP) и обогащения провоспалительными молекулами. Эту проблему мы решаем, вводя молодые и активные экзосомы в организм. Однако ключевое ограничение заключается в другом: если у пациента попросту нет «ворот» (то есть необходимых рецепторов), то даже самый совершенный «мяч» не сможет выполнить свою задачу, и повлиять на процесс становится практически невозможно [43].
Проблема таргетирования (нацеливания) на нужные клетки, эффективности поглощения и избегания «переваривания» экзосом в лизосомах клеток-реципиентов являются существенными препятствиями в разработке экзосомальной терапии. К счастью, на данный момент активно ведутся исследования, посвященные инжинирингу поверхности экзосом для решения этих проблем посредством модификаций поверхностных и рецепторных белков и физико-химических методов (рис. 5) [42].
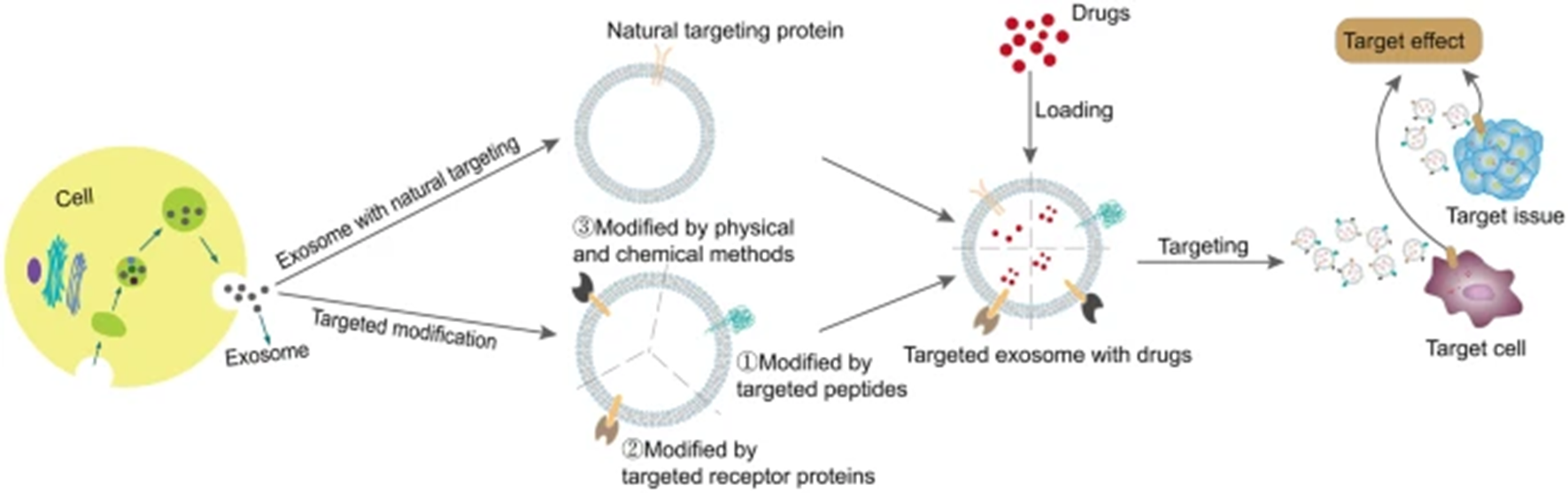
Рисунок 5. Стратегии таргетирования терапевтических экзосом: с помощью собственных таргетных белков на поверхности экзосом и посредством модификации поверхности 1) таргетными пептидами, 2) рецепторными белками и 3) физико-химическими методами. Далее в модифицированные экзосомы загружается лекарство и доставляется в целевые клетки и ткани.
Почему экзосомы пока не прошли IV фазу клинических исследований?
Ключевые ограничения экзосомальной терапии, от безопасности и стандартизации производства до эффективности доставки, становятся препятствиями для внедрения в клиническую практику. Экзосомы представляют собой новый класс терапевтических агентов, и регуляторным органам, таким как FDA (Управление по контролю качества пищевых продуктов и лекарственных средств) и EMA (Европейское агентство лекарственных средств) вместе с научным сообществом ISEV (Международное сообщество внеклеточных везикул) еще только предстоит определить их окончательную классификацию как биологических препаратов. Ключевой проблемой является отсутствие общепринятых стандартов для критически важных этапов: выбора клеток-источников, условий культивирования, методов выделения и контроля качества. Это приводит к высокой вариабельности состава и биологической активности экзосом между разными лабораториями и производственными партиями. Без единых стандартизированных протоколов и четких регуляторных требований процесс перевода терапий в клинику существенно замедляется [18].
С точки зрения клинического развития, экзосомы находятся в самом начале пути. Подавляющее большинство зарегистрированных исследований сосредоточено на фазе I (оценка безопасности) и фазе II (подтверждение первичной эффективности и дозировок). До фазы IV (пострегистрационное наблюдение за безопасностью в большой популяции) — еще несколько лет интенсивной работы. Тем не менее, обнадеживающие результаты доклинических исследований и растущее число биотехнологических компаний, инвестирующих в эту область, явно указывают на значительный потенциал и динамичное развитие экзосомальной терапии [18], [44]. Подробнее о клинических испытаниях читайте в статье «Клинические исследования: рыночный вопрос» [45].
Перспективы использования
Перспективы разработки препаратов на основе экзосом выглядят чрезвычайно многообещающе, особенно в таких динамичных областях, как ветеринария и косметология.
Исследования и препараты для применения в ветеринарной медицине отличаются менее строгим регулированием, что позволяет быстрее выводить продукты на рынок и открывает большие возможности. Многие доклинические исследования на различных животных моделях показали впечатляющие результаты. Основные усилия здесь сосредоточены на лечении остеоартрита, ускорении заживления ран и борьбе с дерматитами у собак и лошадей [46].
Клиническая космецевтика — один из самых быстрорастущих сегментов применения экзосом. На данный момент активно исследуются сыворотки и микроинъекции для осветления кожи, удаления морщин, заживления ран, лечения рубцов и ожогов [18]. В этой сфере экзосомы часто позиционируются как «биоактивные коктейли», что является стратегией для обхода строгих регуляторных требований — такие продукты могут свободно продаваться, если соответствуют общим требованиям безопасности для косметики и не имеют заявленной физиологической и фармакологической эффективности. В будущем развитие этого направления приведет к созданию персонализированных сывороток и гелей на основе инженерных экзосом, что откроет новые горизонты для эстетической медицины.
Заключение
Экзосомы — это не волшебный эликсир, а тонкий инструмент, позволяющий «перенастроить» язык межклеточного общения. Они учат старые клетки снова говорить на языке молодости, стимулируя регенерацию и подавляя воспаление. Несмотря на все трудности, от проблем таргетирования до регуляторных барьеров, этот подход открывает новую, более безопасную и точную главу в борьбе со старением. Возможно, биологическая «машина времени» — это не скачок в прошлое, а сигнал «перезагрузки», доставленный в крошечном пузырьке.
Литература
- Phillip W. Askenase. (2021). Ancient Evolutionary Origin and Properties of Universally Produced Natural Exosomes Contribute to Their Therapeutic Superiority Compared to Artificial Nanoparticles. IJMS. 22, 1429;
- Carmen Schwechheimer, Meta J. Kuehn. (2015). Outer-membrane vesicles from Gram-negative bacteria: biogenesis and functions. Nat Rev Microbiol. 13, 605-619;
- Marc Liebana-Jordan, Bruno Brotons, Juan Manuel Falcon-Perez, Esperanza Gonzalez. (2021). Extracellular Vesicles in the Fungi Kingdom. IJMS. 22, 7221;
- Yuan Zuo, Jinying Zhang, Bo Sun, Xinxing Wang, Ruiying Wang, et. al.. (2025). A New Perspective on Regenerative Medicine: Plant-Derived Extracellular Vesicles. Biomolecules. 15, 1095;
- Shynggys Sergazy, Sergazy Adekenov, Ilya Khabarov, Kymbat Adekenova, Assiya Maikenova, Mohamad Aljofan. (2025). Harnessing Mammalian- and Plant-Derived Exosomes for Drug Delivery: A Comparative Review. IJMS. 26, 4857;
- Minghui Cong, Shenyu Tan, Simin Li, Lina Gao, Luqi Huang, et. al.. (2022). Technology insight: Plant-derived vesicles—How far from the clinical biotherapeutics and therapeutic drug carriers?. Advanced Drug Delivery Reviews. 182, 114108;
- Экзосома — механизм координации и взаимопомощи клеток организма;
- Claire C. Chen, Linan Liu, Fengxia Ma, Chi W. Wong, Xuning E. Guo, et. al.. (2016). Elucidation of Exosome Migration Across the Blood–Brain Barrier Model In Vitro. Cel. Mol. Bioeng.. 9, 509-529;
- Qiang Cai, Baoye He, Shumei Wang, Stephen Fletcher, Dongdong Niu, et. al.. (2021). Message in a Bubble: Shuttling Small RNAs and Proteins Between Cells and Interacting Organisms Using Extracellular Vesicles. Annu. Rev. Plant Biol.. 72, 497-524;
- Simona Bernardi, Mirko Farina. (2021). Exosomes and Extracellular Vesicles in Myeloid Neoplasia: The Multiple and Complex Roles Played by These “Magic Bullets”. Biology. 10, 105;
- Rongxin Zhang, Te Bu, Ruidan Cao, Zhelong Li, Chen Wang, et. al.. (2022). An optimized exosome production strategy for enhanced yield while without sacrificing cargo loading efficiency. J Nanobiotechnol. 20;
- Héctor Peinado, Maša Alečković, Simon Lavotshkin, Irina Matei, Bruno Costa-Silva, et. al.. (2012). Melanoma exosomes educate bone marrow progenitor cells toward a pro-metastatic phenotype through MET. Nat Med. 18, 883-891;
- Yang Liu, Ke Shi, Yong Chen, Xianrui Wu, Zheng Chen, et. al.. (2021). Exosomes and Their Role in Cancer Progression. Front. Oncol.. 11;
- Hamish W King, Michael Z Michael, Jonathan M Gleadle. (2012). Hypoxic enhancement of exosome release by breast cancer cells. BMC Cancer. 12;
- Li Chen, David A. Brenner, Tatiana Kisseleva. (2019). Combatting Fibrosis: Exosome‐Based Therapies in the Regression of Liver Fibrosis. Hepatol Commun. 3, 180-192;
- Neil J. Patel, Anisa Ashraf, Eun Ji Chung. (2023). Extracellular Vesicles as Regulators of the Extracellular Matrix. Bioengineering. 10, 136;
- Fatemeh Soltanmohammadi, Maryam Maghsoodi, Effat Alizadeh, Khosro Adibkia, Yadollah Azarmi, et. al.. (2025). Bio fluid exosomes: promises, challenges, and future directions in translational medicine. J Transl Med. 23;
- Dolores R. Serrano, Francisco Juste, Brayan J. Anaya, Bianca I. Ramirez, Sergio A. Sánchez-Guirales, et. al.. (2025). Exosome-Based Drug Delivery: A Next-Generation Platform for Cancer, Infection, Neurological and Immunological Diseases, Gene Therapy and Regenerative Medicine. Pharmaceutics. 17, 1336;
- Экзосомы: научная альтернатива сказочным молодильным яблокам;
- Зачем клетки стареют;
- Клеточный SASPенс: как стареющие клетки общаются через SMS с молодыми и к чему это может привести?;
- Jun Guo, Xiuqing Huang, Lin Dou, Mingjing Yan, Tao Shen, et. al.. (2022). Aging and aging-related diseases: from molecular mechanisms to interventions and treatments. Sig Transduct Target Ther. 7;
- Carlos López-Otín, Maria A. Blasco, Linda Partridge, Manuel Serrano, Guido Kroemer. (2013). The Hallmarks of Aging. Cell. 153, 1194-1217;
- Mahdi Ahmadi, Jafar Rezaie. (2021). Ageing and mesenchymal stem cells derived exosomes: Molecular insight and challenges. Cell Biochemistry & Function. 39, 60-66;
- Chao Han, Xuan Sun, Ling Liu, Haiyang Jiang, Yan Shen, et. al.. (2016). Exosomes and Their Therapeutic Potentials of Stem Cells. Stem Cells International. 2016;
- Xingyu Li, Heng Zhang, Xuemeng Wang, Meng Lu, Qianqian Ding, et. al.. (2023). iPSC-derived exosomes promote angiogenesis in naturally aged mice. Aging;
- Xiaorui Chen, Yang Luo, Qing Zhu, Jingzi Zhang, Huan Huang, et. al.. (2024). Small extracellular vesicles from young plasma reverse age-related functional declines by improving mitochondrial energy metabolism. Nat Aging. 4, 814-838;
- Mijung Lee, Wooseok Im, Manho Kim. (2021). Exosomes as a potential messenger unit during heterochronic parabiosis for amelioration of Huntington's disease. Neurobiology of Disease. 155, 105374;
- Huimin Deng, Lina Zhu, Yiguo Zhang, Li Zheng, Song Hu, et. al.. (2022). Differential Lung Protective Capacity of Exosomes Derived from Human Adipose Tissue, Bone Marrow, and Umbilical Cord Mesenchymal Stem Cells in Sepsis‐Induced Acute Lung Injury. Oxidative Medicine and Cellular Longevity. 2022;
- Yang Zhang, Yanqi Zhong, Li Zou, Xiaoxia Liu. (2022). Significance of Placental Mesenchymal Stem Cell in Placenta Development and Implications for Preeclampsia. Front. Pharmacol.. 13;
- Alejandro Ocampo, Pradeep Reddy, Paloma Martinez-Redondo, Aida Platero-Luengo, Fumiyuki Hatanaka, et. al.. (2016). In Vivo Amelioration of Age-Associated Hallmarks by Partial Reprogramming. Cell. 167, 1719-1733.e12;
- Kristen C. Browder, Pradeep Reddy, Mako Yamamoto, Amin Haghani, Isabel Guillen Guillen, et. al.. (2022). In vivo partial reprogramming alters age-associated molecular changes during physiological aging in mice. Nat Aging. 2, 243-253;
- Yi-Fan Chen, Frank Luh, Yuan-Soon Ho, Yun Yen. (2024). Exosomes: a review of biologic function, diagnostic and targeted therapy applications, and clinical trials. J Biomed Sci. 31;
- Tatsuya Fukuta, Mayumi Ikeda-Imafuku, Satoshi Kodama, Junko Kuse, Ko Matsui, Yasunori Iwao. (2023). One-Step Pharmaceutical Preparation of PEG-Modified Exosomes Encapsulating Anti-Cancer Drugs by a High-Pressure Homogenization Technique. Pharmaceuticals. 16, 108;
- Margherita Alba Carlotta Pomatto, Benedetta Bussolati, Sergio D’Antico, Sara Ghiotto, Ciro Tetta, et. al.. (2019). Improved Loading of Plasma-Derived Extracellular Vesicles to Encapsulate Antitumor miRNAs. Molecular Therapy - Methods & Clinical Development. 13, 133-144;
- Xi X., Xia S., Lu R. (2021). Drug loading techniques for exosome-based drug delivery systems. Pharmazie. 76, 61–67;
- Haifeng Zeng, Shaoshen Guo, Xuancheng Ren, Zhenkun Wu, Shuwen Liu, Xingang Yao. (2023). Current Strategies for Exosome Cargo Loading and Targeting Delivery. Cells. 12, 1416;
- Johan Skog, Tom Würdinger, Sjoerd van Rijn, Dimphna H. Meijer, Laura Gainche, et. al.. (2008). Glioblastoma microvesicles transport RNA and proteins that promote tumour growth and provide diagnostic biomarkers. Nat Cell Biol. 10, 1470-1476;
- Rabab N. Hamzah, Karrer M. Alghazali, Alexandru S. Biris, Robert J. Griffin. (2021). Exosome Traceability and Cell Source Dependence on Composition and Cell-Cell Cross Talk. IJMS. 22, 5346;
- A. Stolzing, E. Jones, D. McGonagle, A. Scutt. (2008). Age-related changes in human bone marrow-derived mesenchymal stem cells: Consequences for cell therapies. Mechanisms of Ageing and Development. 129, 163-173;
- Xumeng Zhao, Xi Ming, Jiaying Wu, Xiaojian Zhu, Yi Xiao. (2026). Mesenchymal Stromal Cells: Bridging the Gaps in Hematologic Disease Therapy. Stem Cell Rev and Rep. 22, 434-488;
- Jiao He, Weihong Ren, Wei Wang, Wenyan Han, Lu Jiang, et. al.. (2022). Exosomal targeting and its potential clinical application. Drug Deliv. and Transl. Res.. 12, 2385-2402;
- Héctor Peinado, Haiying Zhang, Irina R. Matei, Bruno Costa-Silva, Ayuko Hoshino, et. al.. (2017). Pre-metastatic niches: organ-specific homes for metastases. Nat Rev Cancer. 17, 302-317;
- Caining Wen, Hui Ma, Limei Xu, Zhaodi Gu, Hao Li, et. al.. (2025). Recent advances in the clinical application of exosomes for disease diagnosis and therapeutic strategies. International Journal of Surgery. 111, 4609-4628;
- Клинические исследования: рыночный вопрос;
- Aliai Lanci, Eleonora Iacono, Barbara Merlo. (2024). Therapeutic Application of Extracellular Vesicles Derived from Mesenchymal Stem Cells in Domestic Animals. Animals. 14, 2147.
Комментарии
Раньше здесь был блок с комментариями. Но потом сервис Disqus, на котором они работали и за который мы платили, перестал открываться из РФ.
Когда появится возможность, мы вернём комментарии уже на внутреннем движке, а чтобы это произошло быстрее —
Оставьте донат 💚





